Синтез in situ твердотельных фотокатализаторов Z-схемы BiOBr0.3I0.7 / Ag / AgI с повышенной фотокаталитической активностью при облучении видимым светом
Аннотация
Серия новой полупроводниковой Z-схемы BiOBr 0.3 , управляемой видимым светом. Я 0,7 / Ag / Фотокатализаторы AgI были синтезированы с помощью простых методов осаждения на месте и фото восстановления. При облучении видимым светом BiOBr 0,3 Я 0,7 Образцы / Ag / AgI проявили повышенную фотокаталитическую активность по сравнению с BiOBr 0,3 Я 0,7 и AgI в деградации метилового оранжевого (МО). Оптимальное соотношение добавленного элементарного Ag составляло 15%, при этом 89% MO разлагались за 20 мин. Повышенная фотокаталитическая активность BiOBr 0,3 Я 0,7 / Ag / AgI можно приписать эффективному разделению фотогенерируемых электронно-дырочных пар посредством Z-схемы пути миграции носителей заряда, в котором наночастицы Ag действуют как электронные медиаторы. Исследование механизма показало, что · O 2 - и h + являются активными радикалами фотокаталитического разложения, и небольшое количество · ОН также участвует в процессе фотокаталитического разложения.
Фон
Чтобы противостоять критическим энергетическим и экологическим кризисам, фотокатализ обеспечивает потенциальную стратегию решения этих проблем, поскольку он не только напрямую преобразует солнечную энергию в химическую энергию [1,2,3,4,5,6], но также разлагает органические загрязнители под действием солнечного света. [7,8,9,10,11,12]. БиОБР x Я 1− x твердый раствор, новый фотокатализатор на основе BiOX, вызывает все больший интерес из-за его уникальной слоистой структуры с особыми электрическими и каталитическими свойствами, а также настраиваемой полосовой структуры. Однако BiOBr x Я 1− x имеет положительный потенциал зоны проводимости, что делает его слабым окислительно-восстановительным потенциалом и ограничивает его дальнейшее применение [13, 14].
Недавно было доказано, что фотокаталитические системы Z-схемы способны эффективно усиливать фотокаталитическую активность полупроводников благодаря их особому пути миграции носителей заряда [15,16,17]. В типичной фотокаталитической системе Z-схемы фотогенерируемые дырка и электрон с приблизительным потенциалом в разных полупроводниках объединяются через посредник электронов. Таким образом, фотогенерируемая дырка с более положительным потенциалом и фотогенерируемый электрон с более отрицательным потенциалом могут сохраняться, что обеспечивает лучшую окислительно-восстановительную способность. Вначале электронным посредником в системах Z-схемы был челночный окислительно-восстановительный посредник, такой как I - / IO 3– и Fe 2+ / Fe 3+ [15]; такая система называется системой PS-A / D-PS. Однако этот вид электронного посредника нестабилен для длительного использования и имеет низкую эффективность переноса электронов. Чтобы преодолеть этот недостаток, была разработана полностью твердотельная система Z-схемы с благородным металлом в качестве электронного посредника [18,19,20,21,22,23,24]. При использовании благородного металла в качестве электронного посредника перенос заряда и разделение фотогенерируемых электронно-дырочных пар более эффективны, что демонстрирует более высокий потенциал в практических приложениях. В последнее время йодид серебра широко применялся при создании фотокаталитических систем Z-схемы в качестве восстановителя из-за его особых характеристик фотолиза и отрицательного потенциала зоны проводимости. Метод осаждения in situ обеспечивает простой способ синтеза йодида серебра на элементе I, содержащемся в субстрате. Кроме того, наночастицы Ag могут быть фото восстановлены in situ с помощью AgI для создания фотокаталитической системы Z-схемы, такой как Ag 3 ЗП 4 / AgI [21], AgI / Ag / AgBr [22], AgI / Ag / Bi 2 МоО 6 [23] или AgI / Ag / I- (BiO) 2 CO 3 [24]. Таким образом, используя метод осаждения на месте и фото восстановления для создания нового фотокатализатора Z-схемы между BiOBr x Я 1− x и AgI могли бы стать возможной стратегией для повышения фотокаталитической активности и окислительно-восстановительной способности BiOBr x Я 1− x .
В этом исследовании полностью твердотельная Z-схема BiOBr 0,3 Я 0,7 / Ag / Фотокатализаторы AgI с различными мольными отношениями элементарного Ag синтезируются методами осаждения in situ и фото восстановления. БиОБР 0.3 Я 0,7 / Ag / Фотокатализаторы AgI характеризуются различными технологиями. Фотокаталитическая активность оценивается по разложению метилового оранжевого (МО) при облучении видимым светом и определяется оптимальная молярная доля элементарного серебра в фотокатализаторе. Кроме того, исследуется фотокаталитический механизм.
Методы / экспериментальные
Материалы
Пентагидрат нитрата висмута (Bi (NO 3 ) 3 · 5H 2 O), третичный бутанол (t-BuOH) и нитрат серебра (AgNO 3 ) были приобретены у Aladdin Industrial Corporation. Бромид калия (KBr), иодид калия (KI) и метиловый оранжевый (MO) были приобретены у Tianjin Zhiyuan Chemical Co., Ltd. Все реагенты использовались без дополнительной очистки.
Синтез BiOBr 0,3 Я 0,7 , БиОБР 0,3 Я 0,7 / AgI и BiOBr 0,3 Я 0,7 / Ag / AgI
БиОБР 0,3 Я 0,7 твердый раствор готовили методом гидролиза с помощью ультразвука согласно предыдущей работе [13]. БиОБР 0,3 Я 0,7 / Фотокатализатор AgI синтезирован методом осаждения in situ. Всего 0,5 г BiOBr 0,3 Я 0,7 был добавлен к 50 мл соответствующей концентрации AgNO 3 раствор, в котором молярное отношение Ag к I составляло 15%. Затем суспензию перемешивали при комнатной температуре в течение 1 часа для осаждения AgI, и полученный образец центрифугировали, трижды промывали деионизированной водой и сушили при 60 ° C в течение 12 часов.
Серия БиОБР 0.3 Я 0,7 Фотокатализаторы / Ag / AgI были получены методами осаждения на месте и фото восстановления. В типичном эксперименте 0,5 г BiOBr 0,3 Я 0,7 был добавлен к 50 мл различных концентраций AgNO 3 растворов, и суспензии перемешивали при комнатной температуре в течение 1 ч для осаждения AgI. Затем полученные суспензии облучали лампой Xe мощностью 300 Вт (200 мВт / см 2 ) в течение 10 мин при непрерывном перемешивании для фото-восстановления наночастиц Ag. Наконец, полученные образцы центрифугировали, трижды промывали деионизированной водой и сушили при 60 ° C в течение 12 часов. Изменяя AgNO 3 концентрация, BiOBr 0,3 Я 0,7 / Ag / AgI с различными молярными отношениями Ag / I. Когда молярные отношения Ag / I составляли 5%, 10%, 15% и 20%, образцы после приготовления были названы BAA-1, BAA-2, BAA-3 и BAA-4 соответственно.
Характеристика материала
Кристаллические структуры приготовленных фотокатализаторов охарактеризованы на приборе Bruker D8 ADVANCE для рентгеновской дифракции (XRD). Изображения с помощью сканирующей электронной микроскопии (SEM) и данные энергодисперсионной спектроскопии (EDS) были записаны на тепловизионной системе Zeiss Ultra 55 FESEM. Изображения просвечивающей электронной микроскопии (ПЭМ) и ПЭМ высокого разрешения (ПЭМВР) регистрировали на приборе JEM-2100. Рентгеновская фотоэлектронная спектроскопия (XPS) проводилась на приборе Thermo ESCALAB 250Xi с монохроматизированным источником линии Al Ka (150 Вт). Измерения электронного парамагнитного резонанса (ЭПР) проводили на спектрометре Bruker ER 200-SRC. УФ – видимая спектроскопия диффузного отражения (UV – Vis DRS) проводились на спектрофотометре U-41000 HITACHI (Токио, Япония) с использованием BaSO 4 в качестве справки.
Тесты фотокаталитической активности
Фотокаталитическую активность приготовленного фотокатализатора определяли по разложению МО под облучением видимым светом. В типичном эксперименте лампа Xe мощностью 300 Вт (AM 1,5, выходной световой ток 15 А, 200 мВт / см 2 ) с отсекающим фильтром 400 нм использовался в качестве источника видимого света, а вся система охлаждалась циркулирующей водой. Всего 100 мг приготовленного фотокатализатора добавляли к 150 мл водного раствора, содержащего 10 мг / л MO. Затем суспензию перемешивали в течение 30 мин в темноте до достижения адсорбционно-десорбционного равновесия. После этого суспензию облучали с помощью Xe-лампы, отбирали 7 мл раствора и центрифугировали для удаления катализаторов с 5-минутными интервалами времени. Концентрация МО в разложившемся растворе была определена с помощью УФ-видимой спектроскопии при 465 нм.
Результаты и обсуждение
Анализ структуры и морфологии
Диаграммы XRD BiOBr 0,3 Я 0,7 , BAA- x и BiOBr 0,3 Я 0,7 / AgI показаны на рис. 1а. Все дифракционные пики BiOBr 0,3 Я 0,7 можно найти в BAA- x и BiOBr 0,3 Я 0,7 / AgI, что указывает на то, что конструкция фотокаталитической системы Z-схемы не изменила кристаллическую фазу BiOBr 0,3 Я 0,7 . Пик дифракции около 23,7 градуса принадлежит AgI (JCPDS № 09-0399), что соответствует дифракции (111). При увеличении отношения элементарного Ag интенсивность дифракционного пика BAA- x при 23,7 градусах увеличивается, указывая на то, что AgI откладывается на BBA- x поверхность. Кроме того, отсутствуют дифракционные пики для Ag 0 . были обнаружены из-за его низкого содержания.
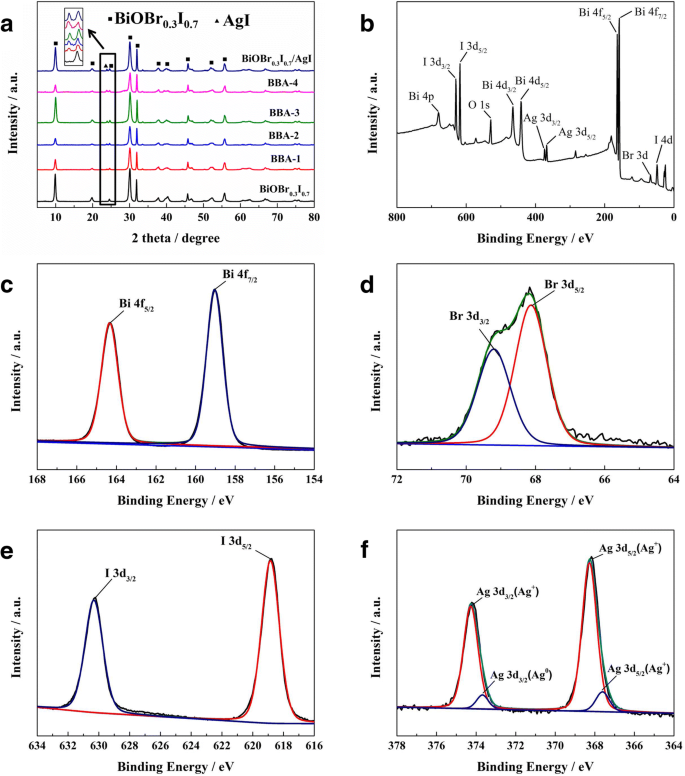
Рентгенограммы BiOBr 0,3 Я 0,7, БАД-х и БиОБР 0,3 Я 0,7 / AgI ( a ), XPS-обзорные спектры БАД-15 ( б ), РФЭС-спектры БАД-15 Bi 4f ( c ), Br 3d ( d ), Я 3d ( e ) и Ag 3d ( f )
Морфология и микроструктура образцов были исследованы с помощью SEM и TEM. Структура нанопластинок размером от 200 до 600 нм относится к BiOBr 0,3 Я 0,7 [13]. Можно заметить, что небольшая частица размером примерно 10 нм и пластинчатая структура были сформированы in situ на поверхности BiOBr 0,3 Я 0,7 , которые могут быть отнесены к Ag и AgI (рис. 2а). Для дальнейшего изучения морфологии БАД- x Были записаны изображения ПЭМ и ВРТЭМ, а также изображения в инфракрасном диапазоне с преобразованием Фурье (БПФ). Понятно, что наночастицы AgI и Ag образовывались in situ на поверхности BiOBr 0,3 Я 0,7, что согласуется с результатом СЭМ (рис. 2б). Решетка Ag (0,233 нм), AgI (примерно 0,350 нм) и BiOBr 0,3 Я 0,7 (приблизительно 0,285 нм) (рис. 2c), что указывает на то, что наночастицы Ag были сформированы in situ на поверхности BiOBr 0,3 Я 0,7 , установив контакт с БиОБР 0.3 Я 0,7 и AgI. На рисунке 2d показана структура BiOBr 0,3 . Я 0,7 / AgI и соединение между BiOBr 0,3 Я 0,7 и AgI; частицы Ag не наблюдались. Согласно результатам SEM и TEM, BAA- x Фотокатализатор Z-схемы был успешно синтезирован методами осаждения на месте и фото восстановления.

СЭМ-изображения BBA-3 ( a ), ПЭМ-изображения BBA-3 ( b ), HRTEM и FFT изображения BAA-3 ( c ) и BiOBr 0,3 Я 0,7 / AgI ( d )
Анализ состава и оптические свойства
Химический состав и химическое состояние BAA-x были проанализированы с помощью XPS-спектроскопии. Из обзорного спектра XPS (рис. 1b), Bi, Br, I, O и Ag наблюдались для BAA- x образец. Наиболее сильные пики при 164 эВ и 159 эВ соответствуют Bi 4f 5/2 и Би 4ф 7/2 (Рис. 1в). Пик Br можно разделить на две составляющие:пик при 69 эВ принадлежит Br 3d 3/2, а пик при 68 эВ принадлежит Br 3d 5/2 (Рис. 1d) . Пики I при 630 эВ и 619 эВ можно отнести к I 3d 3/2 и я 3d 5/2, соответственно (рис. 1д). Пики Ag 3d могут быть разделены как Ag + пики и Ag 0 пики. Сильные пики при 374,2 эВ и 368,2 эВ можно отнести к Ag + в BBA- x . Слабые пики при 373,6 и 367,6 эВ можно отнести к Ag 0 . в BBA- x , что свидетельствует о существовании металлических наночастиц Ag на поверхности БАД- x образец (рис. 1е).
Фактический состав свежеприготовленных образцов был определен анализом SEM-EDS. Как показано в Таблице 1, BiOBr 0,3 Я 0,7 / Образец AgI содержит примерно 2,79% AgI, а отношение остального элементарного I к элементарному Br составляет примерно 7/3, что означает, что нанесенный AgI не изменяет элементный состав BiOBr 0,3 Я 0,7 . После светового облучения содержание элементов Ag в БАД-3 выше, чем в BiOBr 0,3 Я 0,7 / AgI, что указывает на то, что металлический Ag образуется в результате фото-восстановления in situ. Фактическое содержание AgI и Ag в БАД- x образцы были рассчитаны по данным SEM-EDS (Таблица 1). Содержание AgI в BAA- x Образец был рассчитан на основе содержания элемента Bi на основе отношения Bi / I в BiOBr 0,3 Я 0,7 . Общее содержание элементов Ag можно разделить на две части:AgI и металлический Ag; таким образом, содержание металлического Ag можно рассчитать по общему содержанию элементов Ag и содержанию AgI. Металлический Ag можно найти во всех BAA- x образцы, что указывает на то, что наночастицы Ag могут быть уменьшены с помощью фотооблучения.
На рис. 3 показаны результаты спектроскопии диффузного отражения (DRS) в УФ-видимой области для полученных фотокатализаторов и AgI. AgI имеет край поглощения примерно при 450 нм, а BiOBr 0,3 Я 0,7 имеет более широкое поглощение в видимой области от 400 до 650 нм. Все БАД- x образцы имеют такие же области поглощения, как и BiOBr 0,3 Я 0,7, а БАД- x демонстрирует более сильное поглощение видимого света от 400 до 575 нм. По мере увеличения содержания элемента Ag в БАД- x , способность поглощения видимого света немного снижается. Согласно предыдущим сообщениям, образцы с эффектом поверхностного плазмонного резонанса (ППР) Ag демонстрируют заметное увеличение полосы поглощения в диапазоне видимого света [25,26,27]. Однако с увеличением содержания элементов Ag БАД- x образцы не показывают полосу поглощения, которая могла бы быть отнесена к эффекту ППР Ag, что указывает на то, что эффект ППР Ag несущественен в BAA- x образцы [28].
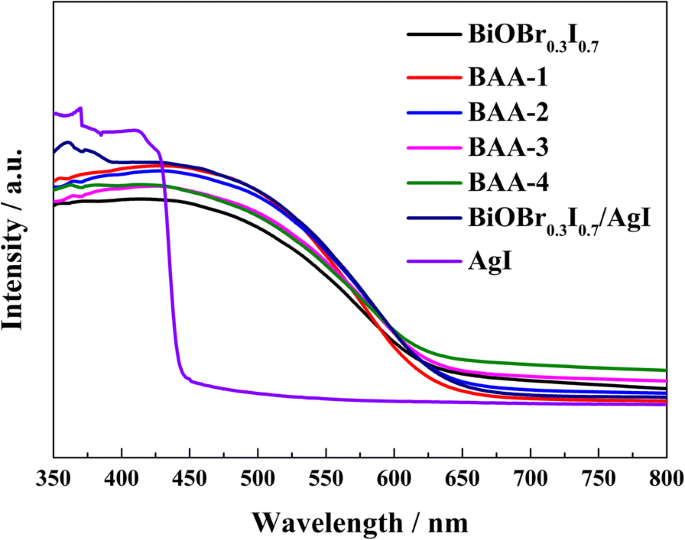
УФ – видимые спектры DRS BiOBr 0,3 Я 0,7 , BAA- x , и BiOBr 0,3 Я 0,7 / AgI
Потенциал запрещенной зоны BiOBr 0,3 Я 0,7 и AgI был рассчитан методом Кубелки – Мунка на основе спектров DRS в УФ-видимой области, которые составляют 1,61 эВ и 2,83 эВ для BiOBr 0,3 Я 0,7 и AgI соответственно. Ленточные структуры BiOBr 0.3 Я 0,7 и AgI рассчитывались по следующим эмпирическим формулам.
$$ {E} _ {\ mathrm {VB}} =\ chi - {E} _ {\ mathrm {e}} + 0.5 {E} _ {\ mathrm {g}} $$ (1) $$ {E } _ {\ mathrm {CB}} ={E} _ {\ mathrm {v}} - {E} _ {\ mathrm {g}} $$ (2)где E g потенциал запрещенной зоны, E VB - потенциал валентной зоны, E CB - потенциал зоны проводимости, E e - энергия свободных электронов в водородном масштабе, составляющая примерно 4,5 эВ, а χ представляет собой абсолютную электроотрицательность полупроводника, выраженную как среднее геометрическое значение абсолютной электроотрицательности составляющих атомов. Таким образом, E VB БиОБР 0,3 Я 0,7 и AgI были рассчитаны как 2,71 эВ и 2,52 эВ относительно нормального водородного электрода (NHE) и их соответствующего E CB равны 1,10 эВ и -0,31 эВ относительно NHE, соответственно, что согласуется с предыдущими отчетами [13, 21].
Эксперименты с фотокаталитической активностью и механизмами
Фотокаталитическую активность приготовленных образцов оценивали по разложению МО под действием видимого света. Исходя из холостого (в отсутствие катализатора) эксперимента, самофотолиз МО при облучении видимым светом можно не учитывать. Как показано на рис. 4, BAA- x проявил превосходную фотокаталитическую активность по сравнению с BiOBr 0,3 Я 0,7 и чистый AgI. С увеличением содержания элементов Ag фотокаталитическая активность БАД- x сначала увеличился, а затем уменьшился. Эта тенденция совпадает с предыдущими сообщениями о полупроводниках, украшенных благородными металлами [28,29,30,31]. Согласно результатам EDS и экспериментам по фотокаталитической активности, при низком содержании добавленных элементов Ag (5%) небольшое количество AgI не может создать эффективную систему Z-схемы для облегчения разделения фотогенерированного носителя. Когда доля добавленных элементов Ag была увеличена до 15%, БАД-3 показал самую высокую фотокаталитическую активность среди БАД- x фотокатализаторы, которые разрушили примерно 89% МО в течение 20 минут при облучении видимым светом. Этот результат показал, что разделение зарядов более эффективно для увеличенных количеств наночастиц Ag. После увеличения доли добавленных элементов Ag до 20% фотокаталитическая активность BAA-4 снизилась. Причина может заключаться в том, что низкое содержание AgI привело к избытку наночастиц Ag на поверхности. Тогда избыточные наночастицы Ag могли накапливать электроны, которые притягивали фотогенерированные дырки, что приводило к межфазной электронно-дырочной рекомбинации. БАД-3 проявляет более высокую фотокаталитическую активность, чем BiOBr 0,3 Я 0,7 / AgI с таким же содержанием элементарного Ag, демонстрируя, что образование наночастиц Ag может улучшить фотокаталитическую активность БАД- x . На основании вышеизложенного можно сделать вывод, что БАД- x имеет более высокую окислительно-восстановительную способность, чем BiOBr 0,3 Я 0,7 , демонстрируя, что изготовление фотокаталитической системы Z-схемы между BiOBr 0,3 Я 0,7 и AgI - эффективная стратегия улучшения фотокаталитической активности и окислительно-восстановительной способности BiOBr 0,3 Я 0,7 .
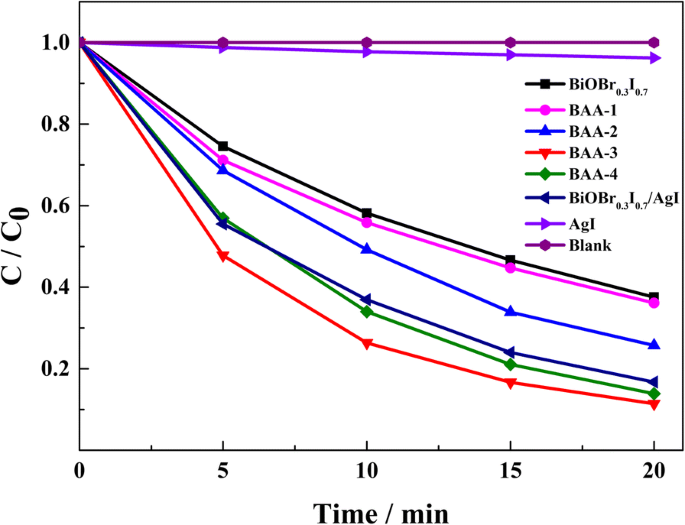
Фотокаталитическая активность деградации МО на разных образцах
Чтобы определить, какие радикальные частицы являются основными активными частицами в фотокаталитическом процессе, были проведены эксперименты по улавливанию радикалов и измерения ЭПР для изучения фотокаталитического механизма BAA- x . В экспериментах по улавливанию радикалов третичный бутанол (t-BuOH), N 2 , и йодид калия (KI) были добавлены в качестве поглотителей гидроксильных радикалов (· OH), супероксидных радикалов (· O 2 - ) и дырки (h + ), соответственно. KI и N 2 имеют очевидный ингибирующий эффект на фотокаталитическую активность БАД-3 (рис. 5а), указывая на то, что h + и · O 2 - являются доминирующими активными видами, а h + является основным активным веществом в фотокаталитической деградации. Фотокаталитическая активность BAA-3 немного подавляется добавлением t-BuOH, что указывает на то, что во время фотокаталитического процесса образовалось небольшое количество · OH. Между тем, из экспериментов ЭПР (рис. 5b – d), когда БАД-3 находится под облучением видимым светом, · OH и · O 2 - сигналы могут быть обнаружены и h + сигнал поглотителя 2,2,6,6-тетраметилпиперидина (TEMP) снижен, что согласуется с экспериментом по захвату радикалов. Согласно исследованию механизма и зонной структуры, возможный фотокаталитический механизм Z-схемы БАД- x показана на рис. 6. При облучении видимым светом электроны в валентной зоне (VB) BiOBr 0,3 Я 0,7 и AgI оба возбуждаются до своей зоны проводимости (CB); после этого фотогенерированные электроны в нижней части CB BiOBr 0,3 Я 0,7 переходят к наночастицам Ag, а затем продолжают перемещаться к вершине VB AgI, рекомбинируя с тамошними фотогенерированными дырками. Оставшиеся фотогенерированные электроны в CB AgI (-0,31 эВ) с более отрицательным потенциалом проявляют сильную восстановительную способность и реагируют с O 2 (O 2 / · O 2 - =- 0,046 эВ, по сравнению с NHE) [21], что позволяет · O 2 - деградировать МО. Между тем, фотогенерированные дырки (2,71 эВ) в VB BiOBr 0,3 Я 0,7 проявляют сильную окислительную способность с прямым разложением МО, и, согласно экспериментам по улавливанию радикалов, небольшое количество фотогенерируемых дырок реагирует с H 2 O для образования · OH (· OH / OH - =1,99 эВ по сравнению с NHE) [32], что может еще больше ухудшить MO.
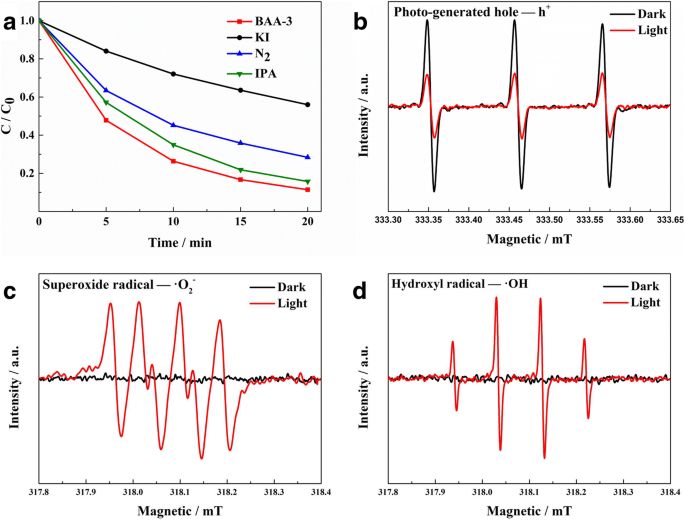
Результаты эксперимента по улавливанию радикалов в присутствии БАД-15 ( a ) и спектры ЭПР фотогенерированной дыры ( b ), · O 2 - радикальный ( c ) и · радикал OH ( d )
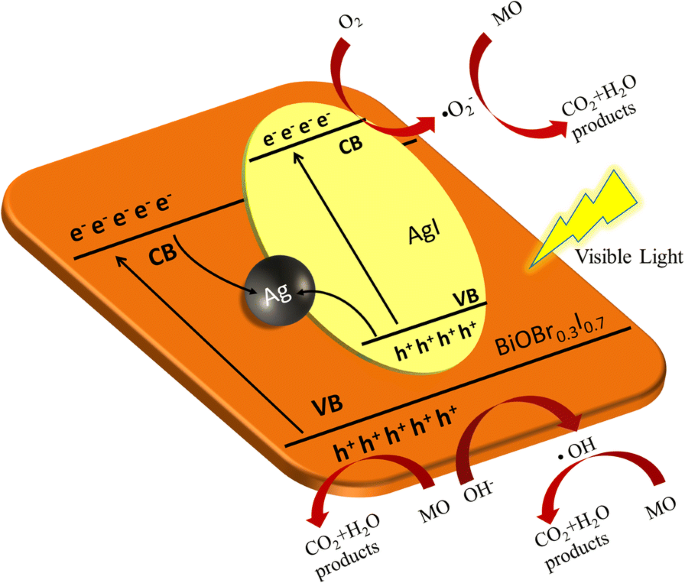
Схема механизма фотодеградации МО БАД- x
Заключение
Новая твердотельная Z-схема БАД- x фотокатализаторы были приготовлены с помощью простых методов осаждения на месте и фото восстановления. БАД- x проявил превосходную фотокаталитическую активность в отношении разложения МО по сравнению с BiOBr 0,3 Я 0,7 при облучении видимым светом. Повышение фотокаталитической активности, вероятно, связано со специальной Z-схемой пути миграции носителей заряда, ведущей к эффективному разделению фотогенерируемых электронно-дырочных пар и поддержанию высокой окислительно-восстановительной способности. Оптимальное молярное соотношение добавленных элементов Ag в БАД- x составляет 15%. Механистические эксперименты показали, что · O 2 - и h + являются активными радикалами, и что при фотокаталитическом разложении образуется небольшое количество · OH. На основании вышеуказанного исследования БАД- x показывает потенциал для практического применения в очистке окружающей среды от органических загрязнителей.
Сокращения
- AM 1.5:
-
Масса воздуха 1,5
- CB:
-
Полоса проводимости
- EDS:
-
Энергодисперсионная спектроскопия
- EPR:
-
Электронный парамагнитный резонанс
- БПФ:
-
Инфракрасное преобразование Фурье
- HRTEM:
-
Просвечивающая электронная микроскопия высокого разрешения
- MO:
-
Метиловый апельсин
- NHE:
-
Нормальный водородный электрод
- SEM:
-
Сканирующая электронная микроскопия
- SPR:
-
Поверхностный плазмонный резонанс
- t-BuOH:
-
Третичный бутанол
- ТЕМ:
-
Просвечивающая электронная микроскопия
- UV – Vis DRS:
-
Спектроскопия диффузного отражения в ультрафиолетовой и видимой областях
- VB:
-
Группа валентности
- XPS:
-
Рентгеновская фотоэлектронная спектроскопия
- XRD:
-
Рентгеновская дифракция
Наноматериалы
- Гидротермальный синтез наночастиц In2O3, гибридные двойники, гексагональные дисковые гетероструктуры ZnO для по…
- Фотокаталитическая активность, усиленная Au-плазмонными наночастицами на фотоэлектроде нанотрубки TiO2, покры…
- Новый фотокатализатор на гетеропереходе Bi4Ti3O12 / Ag3PO4 с улучшенными фотокаталитическими характеристиками
- Синергетические эффекты наночастиц Ag / BiV1-xMoxO4 с повышенной фотокаталитической активностью
- Синтез нанопластин Cu2ZnSnSe4 в одном резервуаре и их фотокаталитическая активность, управляемая видимым светом
- Фотокаталитическая активность тройного нанокомпозита аттапульгит – TiO2 – Ag3PO4 для разложения родамина B при мод…
- Легкий синтез и повышенная фотокаталитическая активность в видимом свете новых композитов с гетеропереходо…
- Эффективные фотокатализаторы, полученные путем равномерного декорирования наночастиц Cu2O на массивах Si нано…
- Улучшенные чувствительные к видимому свету фотокаталитические свойства нанолистовых композитов Ag / BiPbO2Cl
- Изготовление полых микросфер TiO2, промотированных CdTe / BiOI, с превосходными фотокаталитическими характеристик…



