Гидротермальный синтез наночастиц In2O3, гибридные двойники, гексагональные дисковые гетероструктуры ZnO для повышения фотокаталитической активности и стабильности
Аннотация
В 2 О 3 Наночастицы гибридных двойников гексагонального диска (THD) ZnO с различным соотношением были изготовлены гидротермальным методом. Полученный ZnO / In 2 О 3 композиты состоят из шестиугольных дисков ZnO диаметром около 1 мкм и In 2 О 3 наночастицы размером около 20–50 нм. С увеличением In 2 О 3 содержание в ZnO / In 2 О 3 В композитах края полос поглощения образцов сместились из УФ в видимую область света. По сравнению с чистым ZnO, ZnO / In 2 О 3 композиты демонстрируют повышенную фотокаталитическую активность в отношении разложения метилового оранжевого (МО) и 4-нитрофенола (4-НП) под воздействием солнечного света. Благодаря подходящему выравниванию их запрещенной структуры In 2 О 3 и ZnO, формирование гетероструктуры типа п может улучшить эффективное разделение фотогенерируемых пар электрических дырок и обеспечить удобные пути переноса носителей.
Фон
В последние годы загрязнение окружающей среды и нехватка энергии создали серьезные социальные и экономические проблемы для человеческого общества. Фотокатализ на основе полупроводников широко используется как высокоэффективный метод решения этих проблем [1,2,3]. Среди этих полупроводниковых оксидов металлов оксид цинка (ZnO) был признан многообещающим фотокатализатором благодаря своим выдающимся электрическим и оптическим свойствам, низкой стоимости, высокой биологической безопасности, универсальным формам и структурам, безвредности для окружающей среды и высокой способности органических загрязнителей к фотокаталитическому разложению. УФ-свет. Однако ZnO с широкой запрещенной зоной (Eg =3,3 эВ) может быть активирован только ультрафиолетовым (УФ) светом, что ограничивает его практическое применение для солнечной энергии [4,5,6,7,8]. Другой главный недостаток ZnO - быстрая рекомбинация фотоиндуцированных электронно-дырочных пар, что приводит к низкому квантовому выходу любых фотокаталитических реакций [9,10,11,12]. Следовательно, как расширить край поглощения ZnO до области видимого света для использования около 43% солнечного спектра, одновременно подавляя фото-генерируемую рекомбинацию электронно-дырочных пар, все еще остается большой проблемой для ученых. В последние несколько лет использовались различные стратегии модификации для активации фотокатализа ZnO в видимом свете, включая сенсибилизацию, соединение полупроводников и легирование. Эффективная стратегия - соединение ZnO с другим узкозонным полупроводником (например, CdS [13], CdSe [14], Cu 2 O [15], C 3 N 4 [16], ZnFe 2 О 4 [17], Ag 3 ЗП 4 [18], CuInS 2 [19], AgBr [20] и BiVO 4 [21]) для формирования гетероструктур типа ZnO / узкозонный проводник. Формирование гетероструктур типа II было признано привлекательным путем для преодоления ограничений ZnO, поскольку оно способствует эффективному разделению зарядов, увеличивает эффективные границы раздела контактов и улучшает оптическое поглощение [22, 23].
В 2 О 3 с шириной запрещенной зоны 2,56 эВ зарекомендовал себя как эффективный сенсибилизатор для расширения спектров поглощения света за счет связывания других полупроводников. Кроме того, его валентность и зона проводимости разнесены по сравнению с ZnO [24, 25]. Много исследований по In 2 О 3 Сообщалось, что композит -ZnO может разрушать органические соединения и производить водород путем фотокатализа [26,27,28]. Эти результаты показывают, что включение In 2 О 3 в наноструктуре ZnO может заметно ингибировать рекомбинацию фотогенерируемых электронно-дырочных пар и, таким образом, улучшать фотокаталитическую активность. Насколько нам известно, редко сообщалось о производстве и улучшении фотокаталитической активности и стабильности ZnO с помощью In 2 О 3 гибрид наночастиц.
В этой статье В 2 О 3 Наночастицы гибридного THD ZnO с различным соотношением были получены гидротермальным методом. Микроструктура и оптические свойства ZnO / In 2 О 3 исследованы гетероструктуры. Фотокаталитическая активность и фотостабильность ZnO / In 2 О 3 композиты оценивали по МО и 4-НП при световом облучении. Наконец, были обсуждены и предложены перенос заряда и вероятный фотокаталитический механизм на основе оптических характеристик, структуры запрещенной зоны и реакции активных частиц.
Экспериментальный
Формирование ZnO / In 2 О 3 гетероструктура
Во-первых, 0,1 моль ZnAc и определенный молярный состав In (NO 3 ) 2 с расчетным атомным процентом от In до Zn (примерно 2,0, 5,0, 8,0, 12,0 и 15,0 атомных%) растворяли в 50 мл деионизированной воды с образованием прозрачного раствора. Затем 15 мл триэтаноламина (ТЭА) по каплям добавляли в указанный выше раствор при перемешивании магнитной мешалкой. После этого смешанный раствор нагревали при 90 ° C в течение 4 ч, полученные осадки центрифугировали, несколько раз промывали деионизированной водой и этанолом и сушили в сушильном шкафу при 60 ° C. Окончательный ZnO / In 2 О 3 Таким образом, композиты получали отжигом при 200 ° C в течение 1 ч. Согласно молярным отношениям In / Zn 0, 2, 5, 8, 12 и 15%, композиты были обозначены как Zn-In-0, Zn-In-1, Zn-In-2, Zn-In-3. , Zn-In-4 и Zn-In-5 соответственно. Для сравнения чистый In 2 О 3 также были изготовлены в тех же условиях.
Характеристика
Кристаллические структуры изучали методом порошковой рентгеновской дифракции (XRD) с излучением Cu-Kα 0,154178 нм. Морфология и размер ZnO / In 2 О 3 композиты измеряли методом автоэмиссионной сканирующей электронной микроскопии (FESEM; JSM-6700F, Япония). Химический состав анализировали с помощью рентгеновской энергодисперсионной спектроскопии (EDS), установленной на SEM. Детальные микроструктуры образцов были охарактеризованы с помощью просвечивающей электронной микроскопии высокого разрешения (FE-SEM SUPRA ™ 40). Химическое состояние образцов анализировали с помощью рентгеновской фотоэлектронной спектроскопии (XPS; PHI-5300, ESCA, USA). Спектры рассеянного отражения в УФ-видимой области (УФ-видимый DRS) образцов измеряли на спектрофотометре UV-3600. Спектры фотолюминесценции (PL; Renishaw1000, UK) измеряли при комнатной температуре с использованием He-Cd-лазера в качестве источника возбуждающего света на длине волны 325 нм. • Спектры ФЛ с захватом ОН были получены в 5 * 10 −3 Растворы M терефталевой кислоты, содержащие 0,01 М раствор NaOH, с разным временем облучения; длина волны возбуждения - 325 нм.
Фотокаталитический тест
Фотокаталитическую активность приготовленных образцов оценивали по фотокаталитическому разложению MO и 4-NP. Распределение длин волн ксеноновой лампы было аналогично солнечному свету; таким образом, в качестве источника света использовалась ксеноновая лампа мощностью 500 Вт. Для каждого измерения фотокаталитической активности обычно 10 мг фотокатализатора диспергировали в 50 мл водного раствора MO (5 мг / л) или 4-NP (1 мг / л), а затем перемешивали в темноте в течение 30 минут для достижения адсорбционно-десорбционное равновесие. Фотокаталитическая реакция проводилась с использованием ксеноновой лампы в качестве источника солнечного света при непрерывном перемешивании. Через указанные интервалы отбирали пробы из аликвот объемом 3 мл и анализировали путем регистрации изменений полосы поглощения (464 и 317 нм) в УФ-видимых спектрах MO или 4-NP, соответственно. Чтобы исследовать фотостабильность катализатора Zn-In-4, была проведена циклическая деградация. В этом случае повторно использовался Zn-In-4, который отделяли и собирали центрифугированием. После промывки водой и этанолом несколько раз и сушки при 60 ° C в течение ночи катализатор Zn-In-4 повторно использовали со свежим водным раствором MO (5 мг / л) для последующих реакций в идентичных условиях.>
Эксперименты по улавливанию были выполнены для исследования основных активных частиц в фотокаталитическом процессе. Экспериментальное оборудование и процедуры были идентичны тестам на фотокаталитическую активность, за исключением того, что в раствор MO были добавлены различные типы поглотителей (1 мМ). В данном случае метод флуоресценции использовался для обнаружения образования свободных гидроксильных радикалов (• OH), а терефталевая кислота (TPA) использовалась в качестве молекулы зонда. Более подробно, синтезированный Zn-In-4 (0,025 г) диспергировали в 50 мл смешанного раствора 0,25 ммоль ТФК и 1 ммоль NaOH при перемешивании магнитной мешалкой. После облучения ксеноновой лампой (500 Вт) в течение 90 минут супернатант реакционного раствора собирали и исследовали с помощью флуоресцентного спектрофотометра FP-6500 с длиной волны возбуждения 315 нм.
Результаты и обсуждение
Анализ морфологии и фазовой структуры
На рис. 1 представлены СЭМ-изображения изготовленного ZnO / In 2 . О 3 композиты с разной загрузкой In 2 О 3 . Из рис. 1а хорошо видно, что чистый ZnO имеет форму двойника гексагонального диска. Гексагональный диск-двойник имеет среднюю длину стороны около 700–1000 нм, а высота каждого диска составляет около 300–400 нм. На рис. 1 четко показано, что все образцы сохраняют морфологию THD, а размер образцов не изменяется с In 2 О 3 увеличение содержания. Единственная разница в том, что количество In 2 О 3 наночастицы на поверхности ZnO / In 2 О 3 композиты увеличиваются с увеличением In (NO 3 ) 3 содержание. Следует отметить, что в 2 О 3 наночастицы равномерно распределены на поверхности каждого THD ZnO. Есть редкие агрегации даже для более высоких In 2 О 3 образец содержимого. Спектры ЭДС ZnO / In 2 О 3 Образцы (вставленные в соответствующее изображение на сканирующем электронном микроскопе) детектировались диспергированными образцами на проводящей углеродной ленте. Обнаруживаются элементарный цинк, кислород и индий, и соответствующие весовые и атомные проценты для всех образцов указаны в таблице 1.

СЭМ изображения ZnO / In 2 О 3 композиты с разными In 2 О 3 сумма ( a - е ). вставки - спектры EDS соответствующих образцов
На рисунке 2 представлены дифрактограммы ZnO / In 2 . О 3 композиты. Для образца Zn-In-0 все дифракционные пики хорошо совпадают со структурой ZnO вюрцита (JCPDS 36–1451). Для ZnO / In 2 О 3 В композитах с гетероструктурой три новых характеристических пика появляются при значениях 2θ 30,6, 51,1 и 60,7, которые могут быть отнесены к кристаллическим плоскостям (222), (440) и (622) объемно-центрированной кубической структуры In 2 О 3 (JCPDS, № 71–2194) соответственно. Однако с увеличением молярного отношения In:Zn в ZnO / In 2 О 3 композитов, интенсивности типичных характеристических пиков, индексированных как In 2 О 3 увеличивать. Никаких характерных пиков для других примесей не наблюдается, что подтверждает, что успешно изготовленный ZnO / In 2 О 3 композиты обладают высокой чистотой.
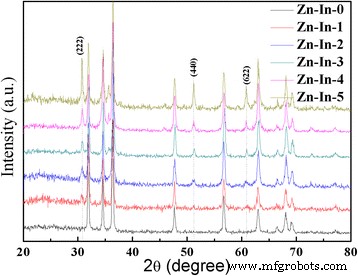
Картины XRD ZnO / In 2 О 3 композиты с разными In 2 О 3 сумма
Для дальнейшего получения информации о морфологии и структуре на рис. 3 представлены изображения образца Zn-In-4, полученные с помощью ПЭМ-ВР. Можно обнаружить, что шестиугольные дисковые структуры имеют диаметр около 800 нм, а поверхности покрыты In 2 О 3 наночастицы . Очевидно, что ZnO / In 2 О 3 Гетероструктура состоит из двойниковых гексагональных дисков ZnO и In 2 О 3 наночастицы. На рис. 3 (б) показаны края сдвоенных гексагональных дисков, покрытые наночастицами диаметром 20–50 нм. Изображение ВР-ПЭМ области белого квадрата на фиг. 3b показано на фиг. 3c, на фиг. 3c можно наблюдать четко различимую границу раздела. Расстояние 0,248 нм согласуется с межплоскостным расстоянием между плоскостями (002) гексагональной фазы ZnO [12]. В левой части четко виден In 2 О 3 (222) грани с шагом 0,285 нм, что согласуется с сообщенным значением [24]. Хорошее кристаллическое качество и четкая граница раздела между ZnO и In 2 О 3 было бы полезно для разделения фотогенерируемых носителей заряда. На рис. 3d представлена диаграмма электронной дифракции (SAED) на границе раздела, которая состоит из двух наборов зонных дифракционных пятен. Эти смешанные дифракционные картины дополнительно указывают на присутствие In 2 О 3 кристаллическое ядро на границе раздела гексагонального диска ZnO.

Изображение TEM ( a ) и изображения HR-TEM ( b , c ) образца Zn-In-4
Анализ XPS
Измерение XPS проводилось для дальнейшей идентификации элементарного и химического состояний поверхности ZnO / In 2 О 3 композиты. Обзорные спектры (рис. 4а) показывают наличие энергетических областей Zn2p, In3d, O1s и C1s. Спектр Zn2p высокого разрешения на рис. 4b показал два основных подгоночных пика с центрами при 1044,21 и 1021,36 эВ, которые относятся к Zn2p1 / 2 и Zn2p3 / 2, соответственно, что указывает на степень окисления Zn (II) в ZnO [20]. Что касается спектра In 3d (рис. 4c), есть два характерных пика с центрами при 444,16 и 451,73 эВ, которые можно отнести к In 3d 5/2 и в 3D 3/2 , которые указывают на наличие In 3+ в ZnO / In 2 О 3 композиты [27, 29]. В XPS-спектре O 1 s (рис. 4d асимметричный профиль можно разделить на два симметричных пика с центрами 530,06 и 531,74 эВ соответственно. Пик, расположенный при 530,06 эВ, соответствует связыванию решеточного кислорода с In и Zn (обозначен как In-O и Zn-O). Кроме того, пик с центром при 531,74 эВ связан с поверхностно поглощенными формами кислорода [26, 30]. Во многих документах зафиксировано, что поверхностные формы кислорода могут продуцировать первичные активные супероксидные радикалы и гидроксил радикалы, которые способны улавливать фотоиндуцированные электроны и дырки для повышения фотокаталитической активности [8, 31].
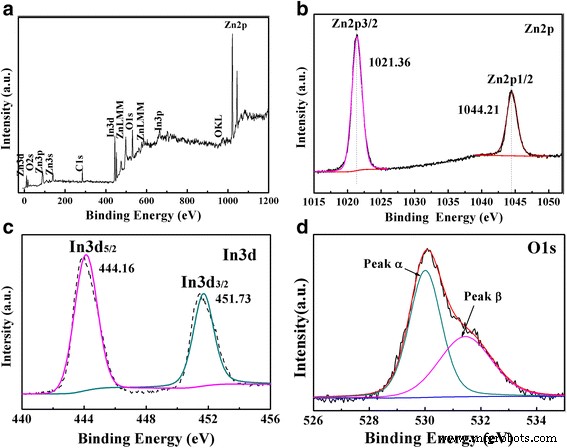
Обзорный спектр XPS Zn-In-4 и соответствующие XPS-спектры высокого разрешения:( b ) Zn2p, ( c ) In3d и ( d ) O1s. Блоки на фиг. 4 ( a ), ( b ), ( d ) должно быть «Энергия связывания», а не «Энергия связывания». Сменный Рис. 4 ( a ), ( b ), ( d ) показано в приложении
Оптические характеристики
На рис. 5а показаны спектры диффузного отражения в УФ-видимой области (УФ-видимый DRS) полученного ZnO / In 2 . О 3 композиты. ZnO без покрытия демонстрирует широкое поглощение с краем поглощения при 385 нм из-за собственной широкой запрещенной зоны, тогда как длина волны отсечки чистого In 2 О 3 наночастицы, расположенные на длине волны 450 нм. С увеличением In 2 О 3 при содержании от 2 до 15 ат.% края полос поглощения образцов смещаются от 380 до 420 нм, а цвет приготовленных образцов также от беловато-желтого до ярко-желтого. Этот результат означает, что в 2 О 3 наночастицы успешно встраиваются в ZnO. На вставке - увеличенное изображение DRS в УФ-видимой области с длиной волны от 350 до 420 нм. Согласно методу Кубелки-Мунка [32], значения энергии запрещенной зоны для ZnO и In 2 О 3 оценивается в 3,18 и 2,75 эВ соответственно [25, 33]. Графики (F (R) hν) 1/2 в зависимости от hν фотокатализаторов представлены на рис. 5b.
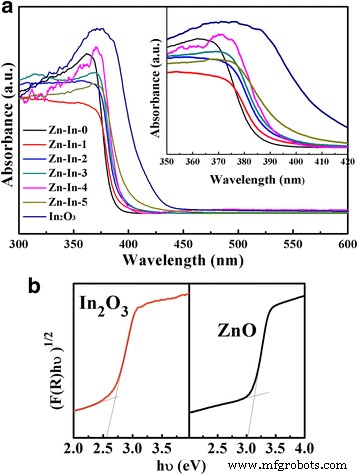
а УФ-видимые спектры диффузного отражения полученных композитов и b запрещенная зона чистого ZnO и In 2 О 3 образцы
Техника фотолюминесценции (ФЛ) широко используется для исследования эффективности миграции, переноса и разделения фотоиндуцированных электронно-дырочных пар в фотокатализаторе. Более высокая интенсивность ФЛ указывает на более высокую скорость рекомбинации фотогенерированных носителей заряда; меньшее количество фотогенерированных электронов и дырок, участвующих в фотокаталитических окислительно-восстановительных реакциях, приводит к более низкой фотокаталитической активности [15, 34, 35]. Следовательно, чтобы исследовать эффект In 2 О 3 наночастиц к ZnO, спектры излучения ФЛ ZnO / In 2 О 3 композиты с разным содержанием In 2 О 3 были измерены при комнатной температуре при длине волны возбуждения 325 нм, как показано на фиг. 6. В этом исследовании Zn-In-0 показывает сильный пик излучения УФ-люминесценции с центром около 380,0 нм. УФ-излучение приписывается ближнему краю полосы излучения ZnO. После модификации In 2 О 3 , интенсивность излучения ZnO / In 2 О 3 образцы значительно упали. Этот результат указывает на то, что эффективность рекомбинации фотоиндуцированных электронно-дырочных пар может быть эффективно подавлена за счет образования структуры гетероперехода. Однако образцы Zn-In-4 показали самую низкую интенсивность пика излучения ФЛ, что означает, что Zn-In-4 имеет самую высокую фотокаталитическую активность для всех ZnO / In 2 О 3 образцы.
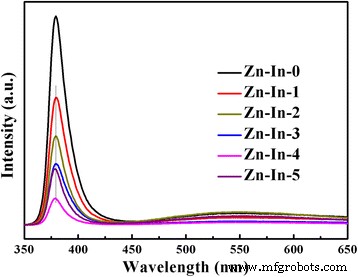
Спектры ФЛ ZnO / In 2 О 3 композиты с разными In 2 О 3 сумма
Фотокаталитическая активность
Фотокаталитическая активность ZnO / In 2 О 3 образцы были оценены по деградации МО и 4-НП при моделированном солнечном облучении. Как показано на рис. 7, саморазложение MO и 4-NP незначительно без добавления фотокатализаторов, что указывает на фотохимическую стабильность этих двух типов органических красителей. На рисунке 7а показаны кривые деградации МО на ZnO / In 2 . О 3 образцы. Под воздействием солнечного излучения только 35% МО разлагается за 90 минут для фотокатализаторов Zn-In-0, что объясняется его более высокой шириной запрещенной зоны. Для сравнения, скорость разложения MO составляет примерно 64 и 82% для Zn-In-1 и Zn-In-2 после 90 минут обработки, соответственно. МО может быть практически полностью разрушен после 90 минут обработки Zn-In-3, 70 минут Zn-In-5 и всего 60 минут композитного фотокатализатора Zn-In-4. Временная эволюция спектральных изменений, сопровождающих фоторазложение МО по исходному Zn-In-4, показана в Дополнительном файле 1:Рисунок S1. Интенсивность характерного пика поглощения МО при 664 нм постепенно уменьшалась с увеличением времени облучения, и цвет раствора, содержащего МО, также изменился с первоначального лимонно-желтого до почти прозрачного цвета после 60-минутной реакции, что указывает на то, что МО полностью разложились. во время фотокаталитического процесса. Согласно очевидному уравнению кинетики псевдопервого порядка, относительные константы скорости k app для различных катализаторов рассчитаны и суммированы на рис. 7b. Соответствующие им константы скорости ( k ) определены как 0,0058, 0,010, 0,0193, 0,0450, 0,0687 и 0,0584 мин −1 для Zn-In-0, Zn-In-1, Zn-In-2, Zn-In-3, Zn-In-4, Zn-In-5 соответственно. Можно обнаружить, что константы скорости k сначала увеличиваются, а затем уменьшаются с увеличением In 2 О 3 содержание в ZnO / In 2 О 3 композиты. Zn-In-4 проявляет самую высокую фотокаталитическую активность. 4-NP был выбран в качестве еще одного типичного целевого соединения для оценки фотокаталитической активности ZnO / In 2 О 3 композитов, а также кривые фотокаталитического разложения 4-НП под действием ZnO / In 2 О 3 композиты показаны на рис. 7в, г. С In 2 О 3 с увеличением содержания скорость разложения 4-NP сначала увеличивается, а затем уменьшается. Кроме того, самая высокая скорость разложения достигается для образца Zn-In-4 с удалением почти 100% 4-NP после 80-минутного облучения солнечным светом. Константы скорости k Zn-In-4 примерно в 12 раз выше, чем Zn-In-0. Основываясь на приведенном выше анализе, мы можем сделать вывод, что фотокаталитическая активность ZnO значительно усиливается In 2 О 3 гибрид наночастиц. При увеличении молярного отношения In 2 О 3 до ZnO, эффективность разложения сначала увеличивается, а затем уменьшается, что означает, что оптимальная загрузка In 2 О 3 важен для повышения фотокаталитической активности ZnO / In 2 О 3 композиты.
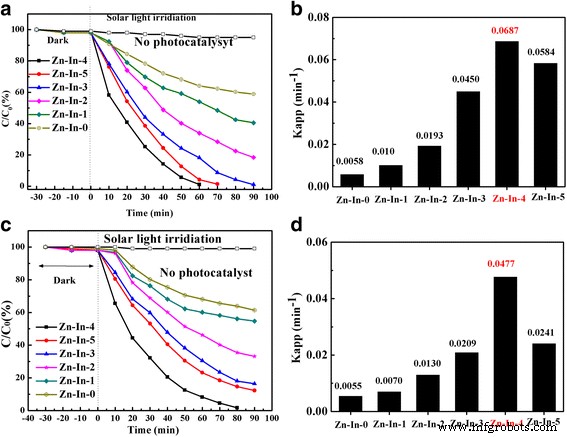
Кривые фотокаталитического разложения и константы скорости линейного кинетического моделирования МО ( a , b ) и 4-НП ( c , d ) с помощью Zn-In-0, Zn-In-1, Zn-In-2, Zn-In-3, Zn-In-4, Zn-In-5
Как мы все знаем, массовое соотношение компонентов имеет большое влияние на фотокаталитические характеристики в гетероструктурной фотокаталитической системе [27, 36]. При увеличении массового отношения In 2 О 3 в ZnO / In 2 О 3 композитов, не было значительной разницы в склонности к деградации МО и 4-НП, и появляется максимальная эффективность разложения для образца Zn-In-4. Однако интенсивности ФЛ образцов демонстрируют противоположную тенденцию к изменению. Этот результат показывает, что соответствующее количество In 2 О 3 в композитах способствует быстрому разделению фотогенерируемых носителей заряда и, таким образом, повышает фотокаталитическую активность [5, 37].
Хорошо известно, что ZnO имеет плохую стабильность при разложении органических загрязнителей. Таким образом, исследование фотостабильности и воспроизводимости фотокатализатора на основе ZnO очень важно для фотокаталитических характеристик. Эксперименты по рециркуляции проводились по разложению растворов МО (рис. 8а) и 4-НП (рис. 8б) над Zn-In-4 под воздействием солнечного света. Эффективность разложения MO снижается с 99,7 до 82,6% и 4-NP с 99,5 до 85,4% после пяти циклов. Существует небольшая разница в эффективности разложения Zn-In-4 для различных красителей после пяти испытаний на переработку под солнечным светом. Кроме того, кристаллическая структура, а также морфология Zn-In-4 не претерпели заметных изменений до и после пяти испытаний на переработку под воздействием солнечного света. Итак, Zn-In-4c устойчив к фоторазложению органических загрязнителей.
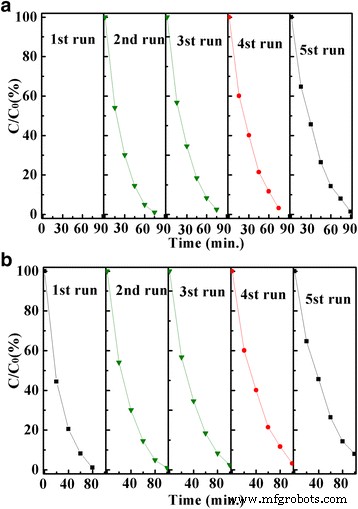
Эксперименты по переработке фотокаталитической деградации МО солнечным светом ( a ) и 4-НП ( b ) над Zn-In-4
Предлагаемый фотокаталитический механизм
Как хорошо известно, важно исследовать активные частицы в фотокаталитическом процессе, чтобы лучше понять механизм фотокатализа. Фотокаталитическая деградация красителей в основном затрагивает несколько активных радикалов, таких как дырка (h + ), супероксид-анион-радикал (• O 2 - ) и гидроксильные радикалы (• OH) [19, 38]. Чтобы оценить роль этих активных частиц, во время процессов фотодеградации использовали серию тушителей. Бензохинон (BQ), динатриевая соль этилендиаминтетрауксусной кислоты (EDTA-2Na), изопропанол (IPA) использовались в качестве поглотителей • O 2 - , фотогенерированные дырки и • OH при деградации МО соответственно. Как показано на рис. 9, при облучении солнечным светом фотокаталитическая активность композита Zn-In-4 значительно подавляется добавлением BQ или EDTA-2Na, что позволяет предположить, что оба фотогенерируемых • O 2 - а дырки являются основными окислительными формами и играют решающую роль в процессе разложения МО. Однако при добавлении IPA в фотокаталитическую систему наблюдается небольшое изменение характеристик фотодеградации, что позволяет предположить, что • OH оказывает очень небольшое влияние на фотокаталитическую реакционную систему. Чтобы исследовать фотоактивные гидроксильные радикалы (• ОН), были собраны спектры фотолюминесценции (ФЛ) с улавливанием ОН (как показано на рис. 9b) над суспензией Zn-In-4, в которой терефталевая кислота использовалась в качестве реагентов для улавливания:ОЙ. Было ясно, что пик излучения на длине волны 426 нм появляется при освещении, а его интенсивность немного меняется в зависимости от времени освещения [39, 40]. Следовательно, можно дополнительно подтвердить, что фотокаталитическая деградация МО по исходному ZnO / In 2 О 3 композит в основном регулировался • O 2 - и h + а не • OH под воздействием солнечного света.
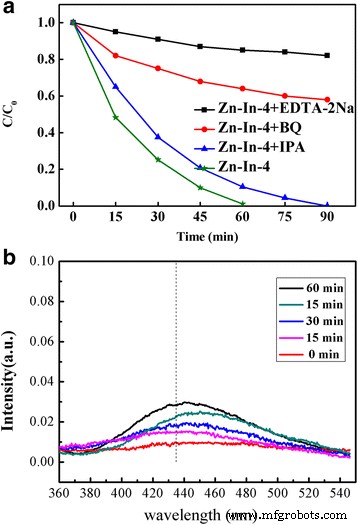
Эксперимент по улавливанию активных частиц во время фотокаталитической деградации МО над Zn-In-4 под воздействием солнечного света ( a ) и спектры ФЛ с захватом OH над образцом Zn-In-4 ( b )
Следовательно, чтобы полностью понять механизм фотокаталитической реакции, происходящей во время фотодеградации исходного ZnO / In 2 О 3 композиты, положения краев зоны валентной зоны (VB) и зоны проводимости (CB) обоих In 2 О 3 и ZnO необходимо определить. Для полупроводника VB и CB можно рассчитать в соответствии с эмпирическим уравнением [41]:
$$ {E} _ {CB} =X- {E} _C- \ raisebox {1ex} {$ 1 $} \! \ Left / \! \ Raisebox {-1ex} {$ 2 $} \ right. {E} _ {\ mathrm {g}} $$ (1) $$ {E} _ {VB} ={E} _ {CB} + {E} _g $$ (2)Где E VB это валентная зона, E CB зона проводимости, E C - энергия свободных электронов относительно нормального водородного электрода (около 4,5 эВ по отношению к NHE) и Eg - ширина запрещенной зоны полупроводника. X - абсолютная электроотрицательность полупроводника, согласно предыдущей литературе, значения X для In 2 О 3 и ZnO составили 5,24 и 5,94 эВ [27, 42] соответственно. Основываясь на результате на рис. 5 (b), ширина запрещенной зоны In 2 О 3 и ZnO оцениваются как 2,75 и 3,18 эВ соответственно. Учитывая приведенные выше уравнения, E CB из В 2 О 3 и ZnO оцениваются как -0,635 и -0,15 эВ соответственно; а E VB из В 2 О 3 и ZnO оцениваются в 2,12 и 3,03 эВ соответственно. На рисунке 10а показана структура энергетических зон ZnO / In 2 . О 3 гетероструктура. Уровень энергии Феми (E f ) из In 2 О 3 более отрицательный, чем у ZnO [33, 43]. Итак, чтобы добиться уравновешивания уровня энергии Ферми в In 2 О 3 / ZnO фотокатализатор типа гетероперехода, уровень Ферми ZnO сохраняет свое положение за счет эффекта пиннинга широкозонного полупроводника, в то время как уровень Ферми In 2 О 3 может сдвигаться вверх до достижения равновесия. Под воздействием солнечного излучения оба In 2 О 3 и ZnO поглощают свет, электроны будут возбуждены и мигрировать к CB, а дырки останутся на VB обоих In 2 О 3 и ZnO. Электроны на CB In 2 О 3 легко могли передать в КБ ЗнО. Одновременно дыры в VB ZnO мигрируют в VB In 2 . О 3 . Электроны, оставшиеся на CB ZnO, восстанавливают O 2 чтобы дать • O 2 - , являющийся мощным окислителем деструкции органических красителей [15, 44]. Отверстия, хранящиеся в VB In 2 О 3 может непосредственно окислять загрязнители до безвредных продуктов, как показано на рис. 10b. Основываясь на приведенном выше анализе, мы можем сделать вывод, что фото-сгенерированный h + и • O 2 - являются основными активными частицами для определения фотокаталитических характеристик, в то время как повышенная фотокаталитическая активность объясняется эффективным разделением и переносом фотогенерируемых носителей на границах гетероперехода, управляемым хорошо подобранными зонными структурами ZnO и In 2. О 3 .
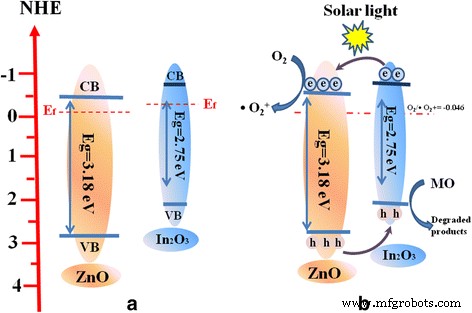
Принципиальная схема выравнивания энергии ( a ) и перенос заряда в ZnO / In 2 О 3 композиты под воздействием солнечного света ( b )
Выводы
Таким образом, в 2 О 3 Гибридные наночастицы THD ZnO с различными соотношениями были получены гидротермальным способом. Примечательно, что по сравнению с чистым ZnO полученный ZnO / In 2 О 3 проявляет гораздо лучшую фотокаталитическую активность по разложению МО и 4-НП при моделированном солнечном облучении, что можно приписать синергетическому эффекту между ZnO и In 2 О 3 , включая максимальную границу раздела гетероструктур с плотным контактом и отличную реакцию на солнечный свет в композите, что может повысить эффективность разделения фотогенерируемых зарядов. Эта работа может дать представление о важности рационального проектирования систем гетероструктур и предоставить потенциальный метод создания эффективных фотокатализаторов на гетероструктурах с контролируемыми размерами и пространственным распределением.
Наноматериалы
- Нановолокна и нити для улучшенной доставки лекарств
- Наночастицы для терапии рака:текущий прогресс и проблемы
- Фотокаталитическая активность, усиленная Au-плазмонными наночастицами на фотоэлектроде нанотрубки TiO2, покры…
- Синтез и эффективность in vitro покрытых полипирролом железо-платиновых наночастиц для фототермической терапии…
- Зеленая способность к синтезу и стабилизации наночастиц меди:каталитическая, антибактериальная, цитотоксич…
- Сапонины Platycodon из Platycodi Radix (Platycodon grandiflorum) для зеленого синтеза наночастиц золота и серебра
- Гидротермальный синтез гибридных наночастиц Fe3O4 @ C и эффективность магнитной адсорбции для удаления ионов тя…
- Изготовление иерархических гетероструктур ZnO @ NiO Core – оболочка для улучшения фотокаталитических характерист…
- Легкий синтез и повышенная фотокаталитическая активность в видимом свете новых композитов с гетеропереходо…
- Влияние легирования магнием на наночастицы ZnO для расширенной фотокаталитической оценки и антибактериально…



