Изготовление иерархических гетероструктур ZnO @ NiO Core – оболочка для улучшения фотокаталитических характеристик
Аннотация
Гетероструктуры ZnO @ NiO ядро – оболочка с высокой фотокаталитической эффективностью и возможностью повторного использования были получены электрохимическим осаждением на тканевые подложки из углеродного волокна. Их фотокаталитические свойства были исследованы путем измерения разложения родамина В и метилового оранжевого (МО) под воздействием ультрафиолетового излучения. Эффективность фотодеградации гетероструктур ZnO @ NiO по отношению к обоим красителям была лучше, чем у чистых наностержней ZnO и нанолистов NiO. Более высокие характеристики можно объяснить образованием p − n-гетероперехода между ZnO и NiO. В частности, гетероструктура ZnO @ NiO, образованная при осаждении NiO в течение 10 мин, разрушила 95% МО под воздействием ультрафиолетового излучения в течение 180 мин. Высокая эффективность фотодеградации гетероструктур ZnO @ NiO также объясняется высокой эффективностью разделения фотогенерированных носителей, что подтверждается более высоким фототоком гетероструктур ZnO @ NiO (в восемь раз) по сравнению с фототоком чистых наностержней ZnO. Более того, высокая эффективность фотодеградации гетероструктур ZnO @ NiO сохранялась в течение трех последовательных экспериментов по деградации и снизилась до 90% после третьего цикла.
Фон
За последние несколько десятилетий фотокатализ полупроводников как вид «зеленой технологии» привлек большое внимание из-за его потенциальных применений в защите окружающей среды и производстве энергии [1,2,3]. Типичные полупроводники, которые были исследованы, - это TiO 2 [4], ZnO [5,6,7], Cu 2 O [8, 9], CdS [10, 11] и C 3 N 4 [12]. Среди них ZnO был наиболее систематически исследован из-за его высокой подвижности электронов, разнообразной морфологии, простоты получения, низкой стоимости и нетоксичности [13, 14]. ZnO с прямой широкой запрещенной зоной (3,37 эВ) обычно демонстрирует проводимость n-типа из-за собственных дефектов, включая межузельные частицы цинка и кислородные вакансии. Однако ZnO как фотокатализатор имеет несколько ограничений:(1) его большая запрещенная зона способствует использованию ультрафиолетового света в основном для фотодеградации; 2) быстрая внутренняя рекомбинация фотогенерированных электронно-дырочных пар приводит к низкой эффективности фотодеградации [15,16]; (3) возникновение сильной фотокоррозии во время фотокаталитического процесса препятствует эффективному разложению органических загрязнителей. Поэтому разработка высокопроизводительного фотокатализа на основе ZnO остается сложной задачей.
Многие исследовательские группы занимались повышением эффективности разделения фотогенерированных носителей и расширением спектрального диапазона отклика с помощью, например, легирования [17], загрузки благородных металлов [5, 18, 19, 20] и комбинирования с другими полупроводниками [21, 22,23,24,25,26,27,28,29,30,31]. В качестве потенциального кандидата оксид никеля, полупроводниковый материал p-типа (Eg =3,5 эВ) с каменной солью или кубической структурой, вызвал большой интерес из-за его электронной структуры, высокой подвижности дырок и низкого рассогласования кристаллической решетки с ZnO. Таким образом, его можно использовать для создания p − n-гетероперехода с ZnO. Кроме того, гетеропереход ZnO @ NiO может образовывать зонную структуру II типа. Зона проводимости (CB) ZnO расположена между валентной зоной (VB) и CB-полосой NiO; такая конфигурация может препятствовать рекомбинации фотогенерированных электронно-дырочных пар, потенциально приводя к улучшенной фотокаталитической эффективности. Zhang et al. [32] сообщили о синтезе нановолокон с гетеропереходом p-типа NiO / n-типа ZnO с использованием золь-гель процесса и технологии электроспиннинга и их использовании в качестве фотокатализаторов. Последние проявляли более высокую каталитическую активность, чем чистые нановолокна NiO и ZnO. Луо и др. [33] сообщили, что наноиглы ZnO, выращенные непосредственно из пористой пены Ni или поверхности NiO, показали в 2,5 раза более высокие фотокаталитические характеристики, чем чистый ZnO. Lei et al. изготовили иерархические пористые полые микросферы ZnO / NiO, которые обладают превосходной адсорбционной способностью по отношению к Конго [34]. Несмотря на сообщенную улучшенную фотокаталитическую эффективность, использование существующих гетероструктур ZnO @ NiO в качестве фотокатализаторов все еще страдает недостатками, такими как сложный процесс синтеза, сложность отделения фотокатализатора от реакционной среды и последующее повторное использование фотокатализаторов. В частности, отделение фотокатализаторов от раствора после реакции является проблемой в практических фотокаталитических процессах.
В настоящей работе ткань из углеродного волокна выбрана в качестве подложки для синтеза гетероструктур ZnO @ NiO методом электрохимического осаждения. Такая конфигурация позволяет легко отделить фотокатализатор от раствора и переработать фотокатализатор. Также обсуждается характеристика отклика фототока иерархических гетероструктур ZnO @ NiO ядро – оболочка.
Методы
Подготовка материалов
Наностержни ZnO были выращены на ткани из углеродного волокна методом электрохимического осаждения. Перед использованием ткань из углеродного волокна была очищена последовательной обработкой ультразвуком в ацетоне, этаноле и деионизированной воде. Смешанный водный раствор (электролит) 5 мМ гексагидрата нитрата цинка (Zn (NO 3 ) 2 · 6H 2 О) и 5 мМ гексаметилентетрамин, ткань из углеродного волокна, платиновая пластина 2 см × 2 см и Ag / AgCl в насыщенном растворе KCl использовали в качестве рабочего, противодействующего и контрольного электродов соответственно. Электролитическая ячейка помещалась в водяную баню для поддержания постоянной температуры 90 ° C. Реакцию проводили в течение 30 мин при постоянном потенциале –0,9 В относительно электрода сравнения. После реакции образцы несколько раз промывали деионизированной водой и сушили в печи при 60 ° C в течение 24 часов.
Слой нанолистов NiO был нанесен на ткань из углеродного волокна с помощью электрохимического осаждения и 0,01 моль гексагидрата нитрата никеля (Ni (NO 3 ) 2 · 6H 2 О) растворяли в 500 мл деионизированной воды. Реакцию проводили при постоянном потенциале -1 В относительно электрода сравнения в течение 10 мин. После реакции образцы вынимали из раствора и несколько раз промывали деионизированной водой с последующим отжигом при 400 ° C в печи в течение 2 ч на воздухе.
Для приготовления гетероструктур ZnO @ NiO на наностержни ZnO методом электрохимического осаждения наносился слой NiO. Время напыления варьировалось от 5 до 10 и 15 мин. Полученные образцы обозначаются соответственно как ZN1, ZN2 и ZN3. Процесс изготовления гетероструктур ZnO @ NiO представлен на рис. 1. Был использован тот же процесс, который использовался для нанесения слоя NiO на подложку из углеродной ткани.

Процесс изготовления иерархических гетероструктур ZnO @ NiO
Характеристика материала
Морфология и структура наностержней ZnO, нанолистов NiO и гетероструктур ZnO @ NiO были охарактеризованы методами автоэмиссионной сканирующей электронной микроскопии (FESEM; NoVaTM Nano SEM 250, FEI), дифракции рентгеновских лучей (XRD; Bruker D8 Advance) и пропускания электронная микроскопия (ТЕМ; Tecnai G2 F20, FEI). Химический состав поверхности и состояния ZN2 определяли с помощью рентгеновского фотоэлектронного спектрометра (Thermo ESCALAB 250XI), снабженного монохроматическим источником Al Kα (1486,6 эВ). Измерения фотолюминесценции (ФЛ) проводились с помощью микро-рамановского спектрометра JY-630 с использованием линии 325 нм He – Cd-лазера в качестве источника возбуждения.
Фотокаталитическая активность
Фотокаталитическая активность образцов (ZnO, NiO и ZnO @ NiO) была исследована путем изучения фотодеградации родамина B (RhB) и метилового оранжевого (MO). Фотокаталитическая установка (XPA series-7, Nanjing) была оборудована ртутной лампой мощностью 500 Вт в качестве источника света. Обычно образец фотокатализатора, выращенный на тканевой подложке из углеродного волокна (2 см × 1,5 см), помещали в кварцевую трубку, заполненную 20 мл водного раствора RhB или MO (5 мг / л). Раствор сначала выдерживали в течение 60 мин в темноте для обеспечения адсорбционно-десорбционного равновесия между фотокатализатором и красителем, после чего начинали облучение УФ-светом. При заданных интервалах освещения концентрацию красителя определяли путем измерения оптической плотности раствора красителя при 464 нм (для MO) и 554 нм (для RhB) на спектрофотометре UV-Vis (TU-1900/1901, Пекин). . Эксперименты проводились при комнатной температуре.
Характеристика фототока
Все электрохимические измерения проводились с использованием типичной трехэлектродной системы. 0,5 М Na 2 SO 4 водный раствор (с pH, доведенным до ~ 7,0) использовался в качестве электролита. В качестве источника света для теста фототока использовалась УФ-лампа мощностью 10 Вт.
Результаты и обсуждение
Картины XRD наностержней ZnO, нанолистов NiO и нанокомпозитов ZnO @ NiO, выращенных на ткани из углеродного волокна, показаны на рис. 2. Широкие дифракционные пики, расположенные при 25,7 ° и 43,7 °, могут быть приписаны углеродной ткани. Дифракционные пики, наблюдаемые для наностержней ZnO, можно отнести к кристаллическим плоскостям (100), (002), (101), (102), (110), (103) и (112) гексагонального вюрцита ZnO. Дифракционные пики, наблюдаемые при 37,0 ° и 42,9 ° на дифрактограмме нанолистов NiO, могут быть отнесены к кристаллическим плоскостям (111) и (200) кубического NiO. На рентгенограммах гетероструктур ZN1, ZN2 и ZN3 наблюдались дифракционные пики гексагональной структуры ZnO и кубической структуры NiO. Кроме того, дифракционные пики NiO постепенно усиливаются по мере увеличения времени осаждения для получения композитных гетероструктур с 5 до 15 мин. Кроме того, не наблюдались никакие другие характерные пики, а также не наблюдались кристаллические фазовые превращения ZnO после осаждения NiO, что подтверждает высокую чистоту полученных композитов.
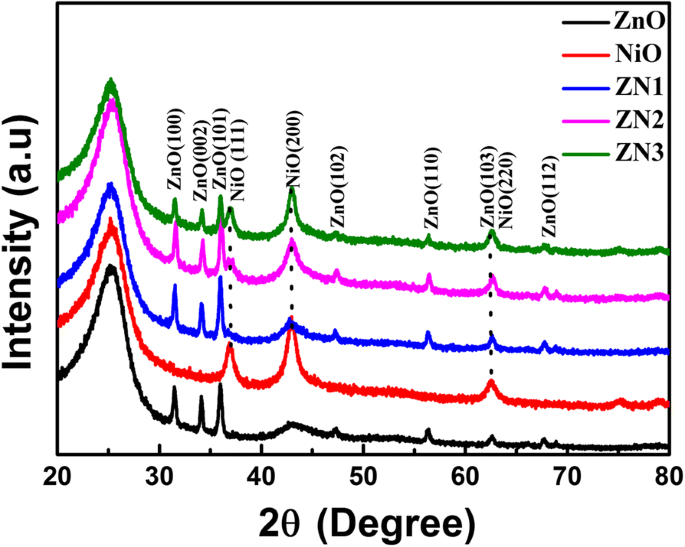
Рентгенограммы композитов ZnO, NiO и ZnO @ NiO
На рис. 3а показаны типичные СЭМ-изображения вида сверху тканевой основы из углеродного волокна. Волокна имели гладкую поверхность (вставка на рис. 3а). Как видно на рис. 3b, NiO с пластинчатой структурой равномерно растет на ткани из углеродного волокна. Напротив, ZnO рос в виде наностержней на ткани из углеродного волокна (рис. 3c). Наностержни ZnO с гладкой поверхностью и диаметром 200 нм были получены с большим выходом (вставка на рис. 3в). FESEM-изображения композитов ZnO @ NiO представлены на рис. 3d – f. Диаметр гетероструктур увеличивался при нанесении нанолистов NiO. Увеличение времени осаждения NiO до 10 мин (рис. 3д) увеличивает плотность нанесенных нанолистов NiO. Когда время осаждения было увеличено до 15 минут (рис. 3f), верхняя часть нанокомпозитов была соединена между собой, что указывает на дальнейшее увеличение количества нанесенного NiO, что согласуется с результатами XRD.

SEM-изображения a углеродная ткань, b Нанолисты NiO, c Наностержни ZnO, d ZN1, e ZN2 и f ZN3
Отображение элементов EDS на рис. 4b и c, соответствующее SEM на рис. 4a образца ZN2, ясно показывает однородное пространственное распределение элементов цинка (Zn), никеля (Ni) и кислорода (O), что указывает на то, что NiO нанолисты, равномерно распределенные на поверхности наностержней ZnO. Вышеупомянутые элементы в иерархическом ZnO @ NiO также подтверждаются измерением EDX на рис. 4, что согласуется с наблюдениями SEM.
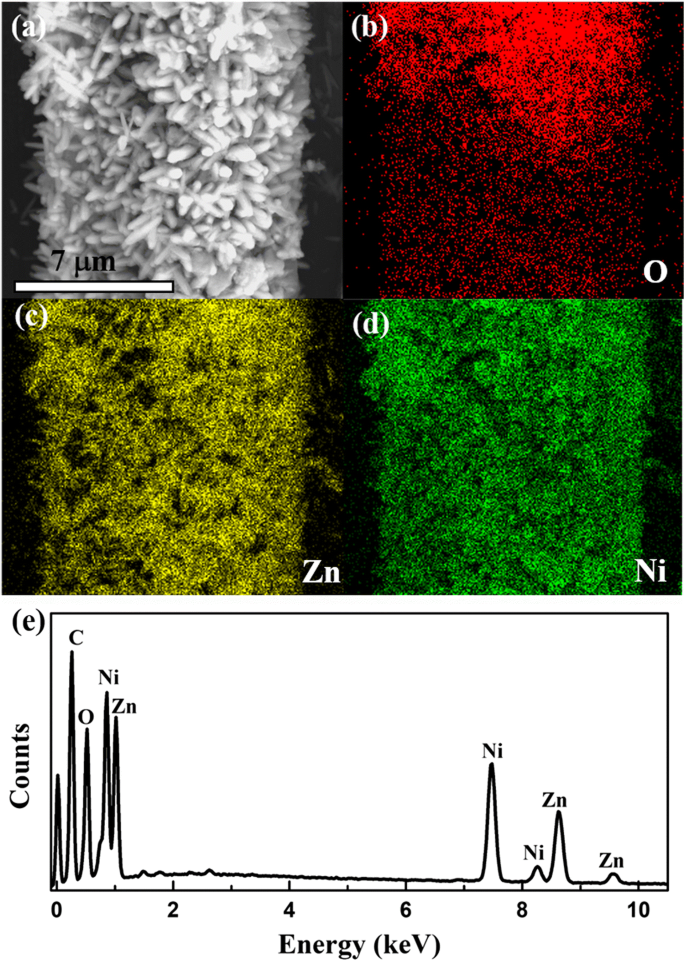
Типичные изображения элементарного картирования ZN2, полученные методом энергодисперсионной рентгеновской спектроскопии (EDS). а Соответствующее СЭМ-изображение области картирования. б О отображение. c Zn отображение. г Отображение Ni. е Изображения EDS
Как видно на типичном изображении ПЭМ на рис. 5, гетероструктуры ZnO @ NiO (ZN2) имеют структуру ядро-оболочка, которая состоит из наностержней ZnO в качестве ядра и нанолистов NiO в качестве оболочки. Диаметр стержневидных морфологий составлял ~ 200–300 нм. На изображении ПЭМ высокого разрешения на рис. 5b показаны границы раздела кристаллических решеток ZnO и NiO. Межплоскостное расстояние 0,26 нм совпадает с шагом решетки плоскости (002) гексагонального вюрцита ZnO, а шаг решетки 0,241 нм соответствует межплоскостному расстоянию плоскости (111) кубического NiO. Более того, четкая граница раздела и непрерывность полос решетки, наблюдаемые между наноструктурами NiO и ZnO на рис. 5b, указывают на образование p – n-гетероперехода между NiO и ZnO в наноструктуре ZN2.

а ПЭМ-изображение гетероструктуры ZnO @ NiO (ZN2). б ПЭМ высокого разрешения изображения ЗН2
Картины рентгеновской фотоэлектронной спектроскопии (XPS) ZN2 показаны на рис. 6. Пики, соответствующие четырем элементам, Zn, O, Ni и C, наблюдались в обзорных спектрах XPS (рис. 6a). Пик C1s с энергией связи 284,6 эВ использовался в качестве стандартного эталона для калибровки и в основном связан с углеводородными загрязнителями, обычно присутствующими в спектрах XPS [15]. На рис. 6b пики XPS, расположенные при 529,5 эВ, были приписаны решеточному кислороду, тогда как пик энергии при 532,2 эВ был приписан неадсорбированному O 2 или поверхностные гидроксильные частицы [35]. На рис. 6c два пика с центрами энергии связи 1022,3 и 1045,2 эВ были отнесены к Zn 2p 3/2 и Zn 2p 1/2 утверждает [36], предполагая, что Zn существовал в форме Zn 2+ . На рисунке 6d показаны XPS-сигналы Ni 2p ZN2, которые можно разложить на пять пиков. Пики при 854,0, 856,1 и 861,1 эВ, соответствующие Ni 2p 3/2 состояние, можно отнести к Ni – O. Оставшиеся два пика при 873,1 и 879,6 эВ были отнесены к Ni 2p 1/2 состояние [32].
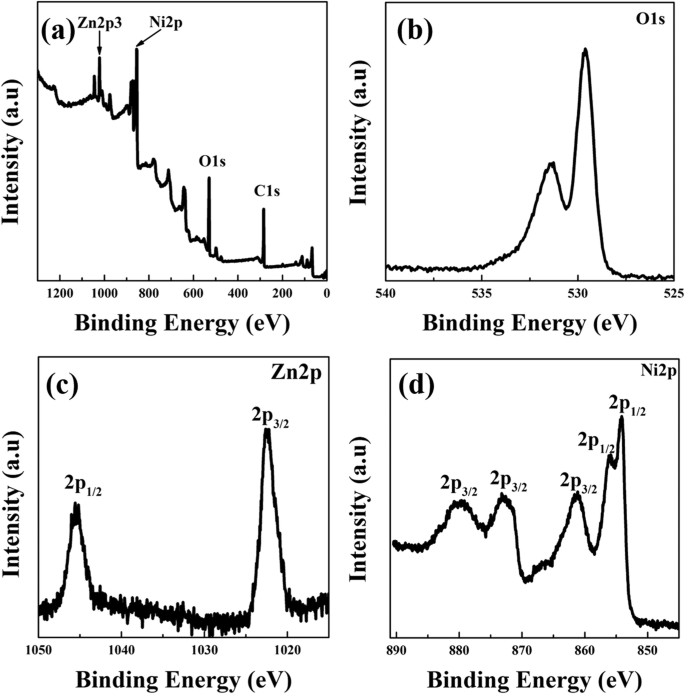
XPS-спектры ZN2. а Обзорные спектры. б О 1с. c Zn 2p. г Спектры Ni 2p
Чтобы исследовать потенциальную применимость нанокомпозитов ZnO @ NiO, фотокаталитическую активность образцов исследовали путем измерения разложения красителя RhB под воздействием ультрафиолетового излучения. Характеристическое поглощение RhB при 554 нм использовали для контроля его концентрации в процессе разложения. Через 180 мин 95% RhB разложилось в присутствии ZN2. Для сравнения, наностержни ZnO и нанолисты NiO соответственно разрушили только 38% и 33% RhB (рис. 7a). Более того, активность фотодеградации нанокомпозитов ZnO @ NiO была намного выше, чем у наностержней ZnO и нанолистов NiO. Для измерения активности фотодеградации использовали график константы скорости фотодеградации RhB в зависимости от времени разложения. Реакцию можно описать как модель кинетики псевдопервого порядка следующим образом [9]:
$$ \ ln \ left (\ frac {C} {C_0} \ right) =- kt, $$где C 0 представляет собой начальную концентрацию RhB, C относится к концентрации RhB при разном времени облучения t , и k - константа скорости реакции. Линейные графики ln ( C / C 0 ) от времени фотодеградации RhB на ZnO, NiO, ZN1, ZN2 и ZN3 показаны на рис. 7b. Константа скорости ( k ) соответствует наклону линейных аппроксимаций. Расчетное k для разложения RhB над ZN2 было 0,01656 мин -1 , что выше расчетных значений для реакций на наностержнях ZnO (0,00257 мин −1 ) и нанолистов NiO (0,00208 мин -1 ). В целом фотокаталитическая активность снижалась в следующем порядке:ZN2> ZN3> ZN1> наностержни ZnO> нанолисты NiO. Экспериментальные результаты показывают, что нанесение слоя NiO на наностержни ZnO способствует переносу заряда, тем самым значительно улучшая фотокаталитическую активность. Согласно результатам БЭТ (показаны в дополнительном файле 1), удельные площади поверхности композитов ZnO @ NiO сначала увеличиваются по мере увеличения времени осаждения NiO, а затем уменьшаются по мере дальнейшего увеличения времени осаждения; таким образом, ZN2 проявляет наивысшую фотокаталитическую активность.
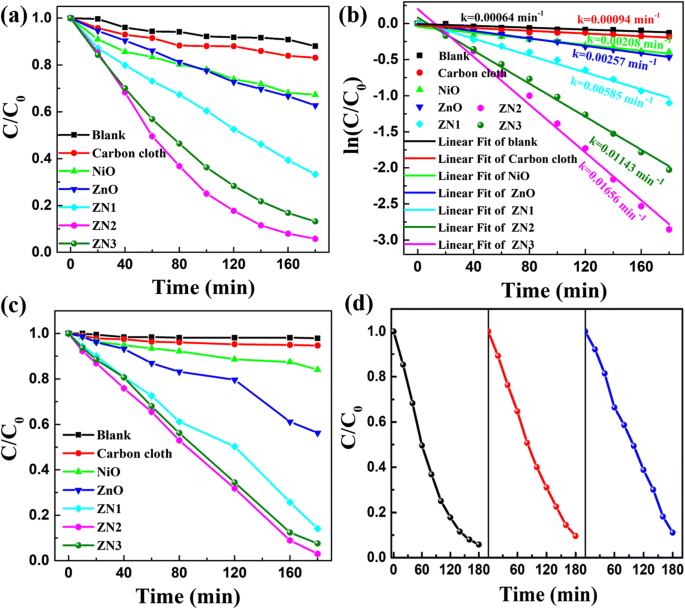
а Графики относительной концентрации (C / C 0 ) RhB в зависимости от времени деградации RhB на наностержнях ZN1, ZN2, ZN3 и ZnO и нанолистах NiO под воздействием УФ-излучения. б Соответствующие графики - ln ( C т / C 0 ) от времени облучения. c Графики относительной концентрации ( C / C 0 ) зависимости МО от времени для деградации МО на гетероструктурах ZnO, NiO и ZnO @ NiO при УФ-облучении. г Повторяющаяся фотокаталитическая деградация RhB над ZN2
Фотокаталитическая деградация МО красителя под воздействием ультрафиолетового излучения также была исследована, и результаты показаны на рис. 7c. Аналогичным образом фотокаталитическая активность снижалась в следующем порядке:ZN2> ZN3> ZN1> наностержни ZnO> нанолисты NiO. Можно сделать вывод, что нанокомпозиты ZnO @ NiO демонстрируют более высокую фотокаталитическую активность по сравнению с наностержнями ZnO и нанолистами NiO. Фотокаталитическую стабильность ZN2 оценивали, проводя повторную фотокаталитическую деградацию RhB при облучении ультрафиолетовым светом. Как видно на рис. 7d, выход разложения оставался высоким (~ 95%) в течение повторных циклов с небольшим снижением до 90%, наблюдаемым после третьего цикла. Эти результаты демонстрируют высокую фотокаталитическую эффективность и возможность повторного использования гетероструктур ZnO @ NiO, которые являются важными атрибутами для их практического использования в реальных приложениях для удаления органических загрязнителей из сточных вод.
Соответствующие отклики фототока показаны на рис. 8а. Несколько световых циклов включения-выключения были использованы для исследования эффективности разделения носителей заряда. Нанолисты NiO не показали изменений в токе как в темных условиях, так и при световом освещении, тогда как наностержни ZnO показали небольшой отклик фототока при ультрафиолетовом облучении. Напротив, композиты ZnO @ NiO показали более высокую плотность фототока. При этом плотность фототока уменьшалась в следующем порядке:ZN2> ZN3> ZN1> наностержни ZnO> нанолисты NiO. Быстрые отклики фототока предполагали, что перенос заряда в образцах был очень быстрым. Повышенный фототоковый отклик композитов ZnO @ NiO можно объяснить образованием плотных межфазных контактов между наностержнями ZnO и нанолистами NiO. Сделан вывод, что фотовозбужденные электроны в нанолистах NiO могут генерироваться и эффективно передаваться от CB NiO к соседним наностержням ZnO при ультрафиолетовом облучении, где ZnO служит эффективным стоком и переносчиком электронов, тем самым препятствуя рекомбинации фотогенерированных электрон-дырочных элементов. пары. Стоит отметить, что фототок композитов ZnO @ NiO первоначально увеличивался с увеличением времени осаждения NiO, а затем уменьшался при дальнейшем увеличении времени осаждения. Возможно, что площадь поверхности межфазного контакта между наностержнями ZnO и нанолистами NiO сначала увеличивается, а затем уменьшается по мере увеличения времени осаждения NiO, что согласуется с результатом фотокаталитической активности.
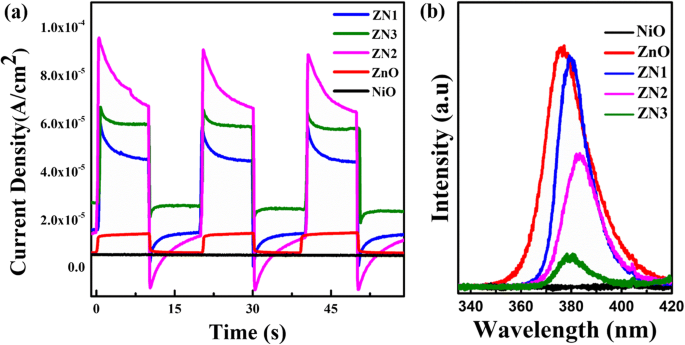
а Фототоковый отклик нанолистов NiO, наностержней ZnO и гетероструктуры ZnO @ NiO при облучении УФ-лампой (10 Вт). б Спектры ФЛ наностержней из чистого ZnO, нанолистов NiO и композита ZnO @ NiO
На рисунке 8b показаны типичные спектры ФЛ наностержней из чистого ZnO, нанолистов NiO и гетероструктур ZnO @ NiO, измеренные в тех же условиях при комнатной температуре. Для наностержней из чистого ZnO наблюдается сильный пик излучения при 378 нм, который соответствует излучению ZnO на ближнем крае полосы. Для нанолистов NiO не наблюдается пика излучения. Кроме того, интенсивность излучения ФЛ композита ZnO @ NiO явно ослаблена по сравнению с интенсивностью излучения наностержней чистого ZnO, что свидетельствует о сдерживании рекомбинации фотогенерированных электронно-дырочных пар. Результаты фототока и ФЛ показывают, что нанокомпозит ZnO @ NiO может значительно повысить эффективность разделения и эффективность межфазного переноса заряда фотогенерированных электронно-дырочных пар.
Повышенная фотокаталитическая активность гетероструктур ZnO @ NiO была приписана быстрому разделению носителей и транспорту на границе гетероструктур ZnO @ NiO из-за выравнивания полос типа II между ZnO и NiO. Этот предложенный механизм согласуется с предыдущими отчетами [8, 10, 22]. На рис.9 показана предложенная диаграмма энергетической зонной структуры гетероструктуры ZnO @ NiO. ZnO является полупроводником n-типа, тогда как NiO является полупроводником p-типа. При объединении ZnO и NiO образуется p − n-гетеропереход, а на границе раздела между NiO и ZnO создается внутреннее электрическое поле из-за переноса электронов и дырок. При облучении УФ-светом электроны в VB возбуждаются в CB, оставляя дырки в VB. Выравнивание зон гетеропереходов NiO p-типа и ZnO n-типа полезно для переноса фотогенерированных электронов от CB NiO к CB ZnO, тогда электроны могут объединяться с молекулами растворенного кислорода и образовывать анион-радикалы супероксида (• О 2 - ), которые играют важную роль в общей фотокаталитической реакции. И наоборот, фотогенерированные дырки могут переноситься из VB ZnO в VB NiO, и дырки легко захватываются OH - на поверхности катализатора с дальнейшим образованием гидроксильных радикалов (• ОН), которые являются чрезвычайно сильным окислителем для разложения органического красителя. Таким образом, нанокомпозиты ZnO @ NiO демонстрируют превосходные фотокаталитические характеристики по сравнению с наностержнями ZnO и нанолистами NiO.
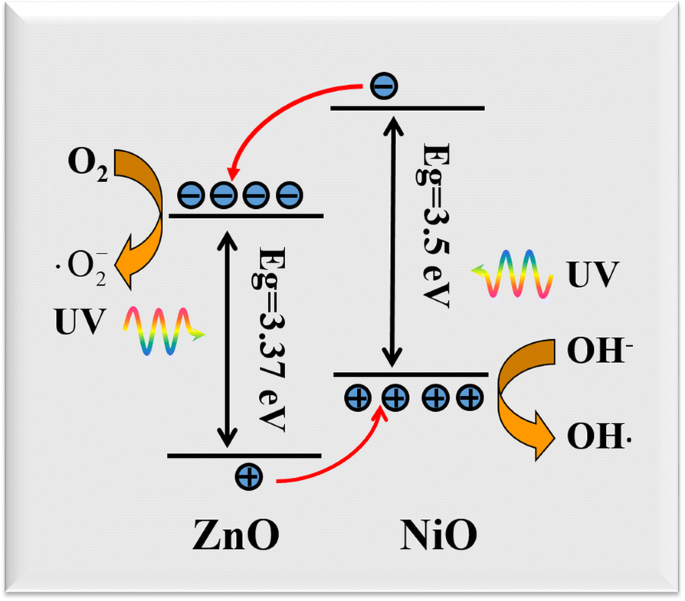
Схема выравнивания энергетических зон между ZnO и NiO
Выводы
Гетероструктуры ZnO @ NiO были успешно изготовлены простым методом электрохимического осаждения. Фотокаталитическая активность нанокомпозитов ZnO @ NiO превосходит активность наностержней ZnO и нанолистов NiO в отношении деградации красителей MO и RhB под воздействием УФ-излучения. Высокие фотокаталитические характеристики были приписаны высокой эффективности отделения фотогенерированных электронно-дырочных пар от p − n-гетероперехода, что подтверждено измерениями отклика фототока. Результаты показали, что в гетероструктурах ZnO @ NiO может быть сгенерировано и разделено больше свободных носителей, что приведет к более высокой эффективности разделения по сравнению с таковой, достигнутой в наностержнях ZnO и нанолистах NiO. Более того, гетероструктуры ZnO @ NiO могут быть легко переработаны с минимальным снижением фотокаталитической активности. Высокая фотокаталитическая эффективность и возможность повторного использования гетероструктур ZnO @ NiO, что позволяет легко отделить их от раствора, имеют важные применения для удаления органических загрязнителей из сточных вод.
Сокращения
- CB:
-
Полоса проводимости
- EDS:
-
Энергодисперсионная рентгеновская спектроскопия
- MO:
-
Метиловый апельсин
- PL:
-
Фотолюминесценция
- RhB:
-
Родамин Б
- SEM:
-
Сканирующая электронная микроскопия
- ТЕМ:
-
Просвечивающая электронная микроскопия
- VB:
-
Группа валентности
- XPS:
-
Рентгеновская фотоэлектронная спектроскопия
- XRD:
-
Рентгеновская дифракция
Наноматериалы
- Оценка эффективности смазки для повышения надежности
- 3 ключа для повышения производительности предприятия
- Гидротермальный синтез наночастиц In2O3, гибридные двойники, гексагональные дисковые гетероструктуры ZnO для по…
- Иерархическая гетероструктура полых сфер ZnO @ TiO2 для высокоэффективного фотокаталитического выделения водор…
- Видимые световые фотокаталитические характеристики нанокомпозитов ZnO / g-C3N4, легированных азотом
- Подготовка и фотокаталитические характеристики фотокатализаторов LiNb3O8 с полой структурой
- Подготовка гибридных микроматериалов MnO2 с полипропиленовым покрытием и их улучшенные циклические характери…
- Новый фотокатализатор на гетеропереходе Bi4Ti3O12 / Ag3PO4 с улучшенными фотокаталитическими характеристиками
- Изготовление и характеристики высокоэффективного поглощения электромагнитных волн структурированных нано…
- Изготовление и характеристика ZnO Nano-Clips с помощью процесса, опосредованного полиолом



