Высокоэффективный синтез углеродных наночастиц фосфида молибдена для электрокаталитического выделения водорода
Аннотация
Фосфид молибдена в составе фосфидов переходных металлов считается привлекательным электрокатализатором для реакции выделения водорода (HER). Однако его неудовлетворительная стабильность и проводимость в щелочной среде затянули его развитие. Здесь мы успешно ввели наночастицы MoP, со-легированные N, C (MoP-NC), с помощью простого и эффективного метода двухэтапного синтеза с использованием мочевины в качестве источника углерода в систему фосфида молибдена. Дешевизна мочевины и отличное соотношение углерода и азота устраняют препятствия на пути развития композитов MoP-NC. Полученные композиты обладают превосходной электрокаталитической активностью и стабильностью HER в 1-молярном растворе гидроксида калия (KOH), который требует всего лишь перенапряжения 131 мВ для достижения плотности тока 10 мА см −2 и демонстрирует незначительное снижение производительности после 1000 циклов CV.
Фон
В последние годы быстрое развитие человека привело к постепенному истощению ископаемой энергии [1,2,3]. Поэтому исследователи стремятся найти экологически чистый источник энергии, чтобы обуздать этот порочный круг и удержать водород на троне энергии. Однако традиционный фотолиз и электролиз воды для производства водорода являются узким местом с точки зрения эффективности. Принимая во внимание, что с внедрением высокоэффективных электролизованных катализаторов производства водорода, катализируемых водой, люди совершили качественный скачок в массовом производстве водорода. Этот опосредованный катализатором электрокаталитический процесс требует, чтобы сам катализатор имел низкое перенапряжение реакции выделения водорода (HER). Хотя благородные металлы, такие как Pt, на этой стадии имеют чрезвычайно низкое перенапряжение и превосходную стабильность, они дороги [4,5,6]. Недостаток доступной почвы ограничивает широкомасштабное применение таких катализаторов [7,8,9]. Поэтому поиск материала с низкой стоимостью и относительно хорошими характеристиками электрокаталитического выделения водорода был горячей точкой в последние несколько лет [10,11,12,13].
Стоит отметить, что недавно исследователи обнаружили, что некоторые катализаторы из неблагородных металлов имеют хорошее соотношение цена / качество в направлении выделения водорода, среди которых наиболее широко используемый фосфид молибдена (MoP) в фосфидах переходных металлов (TMP) [14 , 15,16,17]. Sun et al. смешанный (NH 4 ) 6 Пн 7 О 24 · 4H 2 О, (NH 4 ) 2 HPO 4 и лимонная кислота (CA) в различных молярных соотношениях, когда Mo:P:CA =1:1: x и x =2, образование сшитой сетевой структуры наночастицы MoP обладают лучшими характеристиками HER [18]. Джошуа и др. Получили аморфные наночастицы MoP с хорошими свойствами HER путем нагревания гексакарбонилмолибдена и триоктилфосфина (TOP) [19]. Однако электропроводность чистого фосфида молибдена неудовлетворительна, а характеристики выделения водорода и стабильность в щелочном растворе не так хороши, как в кислой среде, так что проводимость и стабильность можно повысить за счет введения материала на основе углерода [ 20,21,22].
Мы достигли высокоэффективного двухэтапного синтеза, введя мочевину в качестве источника углерода в систему фосфида молибдена, и успешно получили наночастицы MoP, со-легированные N, C (MoP-NC), которые обладают превосходной каталитической активностью и стабильностью даже в щелочных электролитах. . Кроме того, мы разработали две контрольные группы, которые исследовали действие мочевины, включая отсутствие источника углерода и глюкозу вместо мочевины в качестве источника углерода. Интересно, что первый всегда слабее второго при использовании глюкозы и мочевины в качестве источников углерода соответственно. Это можно объяснить ролью мочевины как источника углерода и азота для вспомогательного синтеза фосфида молибдена [23].
Презентация гипотезы
Фосфид молибдена широко используется в качестве катализатора из неблагородных металлов в направлении выделения водорода. Введение источника углерода может улучшить проводимость и стабильность электрокатализатора. Использование источника азота может улучшить характеристики выделения водорода в щелочном растворе.
Проверка гипотезы
Материалы
Мочевина (CH 4 N 2 O), глюкоза (C 6 H 12 О 6 ), дигидрофосфат аммония (NH 4 H 2 ЗП 4 ) и гептамолибдат аммония ((NH 4 ) 6 Пн 7 О 24 · 4H 2 O) были приобретены у Sinopharm Chemical Reagent Co., Ltd. КОН был приобретен у Aladdin Ltd. в Шанхае. В эксперименте использовалась деионизированная вода из оборудования для сверхчистой воды.
Подготовка образца
В типичном синтезе MoP-NC (NH4) 6 Пн 7 О 24 · 4H 2 O (0,240 г), NH 4 H 2 ЗП 4 (0,167 г) и CO (NH 2 ) 2 (2.000 г) растворяли в 50 мл деионизированной воды и подвергали обработке ультразвуком в течение 15 минут. После этого полученный раствор нагревали до 80 ° C и перемешивали на магнитной мешалке в течение 90 минут, оставался относительно закрытым на протяжении всей реакции, а затем сушили в лиофильном сушилке. Полученный белый порошок предшественника нагревали от комнатной температуры до 900 ° C со скоростью 5 ° C / мин в атмосфере N 2 . атмосфера на 120 мин. Чтобы изучить влияние источника углерода на синтез материала, MoP-C был приготовлен с использованием глюкозы вместо мочевины в качестве источника углерода. Когда не добавляли источник углерода или источник фосфора, получали соответственно Bulk-MoP и Mo-NC.
Характеристики
Информация о дифракции рентгеновских лучей (XRD) была собрана на дифрактометре рентгеновских лучей (XRD, дифрактометр Bruker D8-Advance с излучением Cu Kα ( λ =1,54056 Å)). Микроструктуру образца получали с помощью сканирующей электронной микроскопии с автоэмиссией (FE-SEM, S-4800, Hitachi, Япония). Изображения ПЭМ получали с помощью просвечивающей электронной микроскопии (ТЕМ, JEM-2100, JEOL, Япония). Химические компоненты были проанализированы с помощью рентгеновской фотоэлектронной спектроскопии (XPS) с Mg Kα в качестве источника монохроматического рентгеновского излучения.
Электрохимический тест
Все электрохимические измерения проводили на электрохимической рабочей станции (CHI 660E Chenhua, Шанхай), оснащенной традиционной трехэлектродной системой Pine Modulated Speed Rotator (PINE, США). Платиновая проволока и насыщенный каломельный электрод (SCE) соответствовали противоэлектроду и электроду сравнения, соответственно, а стеклоуглеродный электрод и вращающееся дисковое устройство были подключены в качестве рабочего электрода. Кроме того, для испытаний был предоставлен электролит 1 М КОН. Рабочий электрод готовили следующим образом. Сначала 5 мг катализатора растворяли в растворе, смешанном с 350 мкл изопропанола, 650 мкл деионизированной воды и 50 мкл 5 мас.% Нафиона. Затем, после того как упомянутый выше смешанный раствор обрабатывали ультразвуком в течение 30 минут, получали однородно диспергированные чернила. Наконец, 10 мкл чернил было нанесено на стеклоуглеродный электрод (диаметр 5 мм) для обработки естественной сушкой на воздухе, где катализатор имел поверхностную плотность 0,485 мг / см -2 . . Чтобы лучше описать рабочие параметры образца, мы использовали катализатор Pt / C (20 мас.%) Для сравнения, и процесс приготовления был таким же, как и у вышеуказанного рабочего электрода. Скорость развертки 10 мВ с −1 использовался для измерений вольтамперометрии с линейной разверткой (LSV). Тафель был получен путем аппроксимации кривой соответствующей области согласно уравнению Тафеля, а электрохимическая стабильность была получена путем выполнения 1000 циклов со скоростью развертки 100 мВ · с -1 . Емкость двойного слоя ( C dl ) данные получены из циклической вольтамперометрии (CV), которая выполняется в одном и том же диапазоне напряжений (0,847–0,947 В относительно RHE) в разных диапазонах скорости сканирования (20–200 мВ). Электрохимическая спектроскопия импеданса (EIS) измерения проводились при постоянной амплитуде потенциала 10 мВ в диапазоне частот по умолчанию (1–10 5 Гц).
Следствия гипотезы
На рисунке 1а показана дифрактограмма MoP-NC с пиками дифракции при 27,95, 32,17, 43,15, 57,48, 57,95, 64,93, 67,03, 67,86 и 74,33, соответствующих девяти различным кристаллическим граням MoP. СЭМ-изображения MoP-NC показали микроструктуры аморфных мелких частиц (рис. 1b). Частицы собирались вместе, образуя небольшие кластеры, но между кластерами все еще оставался определенный промежуток. Благодаря этой небольшой и плотной структуре MoP-NC обладают значительной каталитической активностью и хорошей стабильностью (рис. 1c). Из ПЭМ и ПЭМ высокого разрешения (ПЭМВР) (рис. 1d, e) видно, что эти наночастицы демонстрируют отчетливые полосы решетки, такие как полосы решетки из плоскости (100) с шагом 0,28 нм. Кроме того, за пределами этих четко определенных краевых областей решетки находились края наночастиц MoP-NC, которые решительно поддерживали включение наночастиц MoP-NC в углеродную матрицу. Соответствующее изображение отображения элементов EDS (рис. 1f – i) дополнительно подтвердило равномерное распределение четырех элементов в продукте MoP-NC.

а Диаграммы XRD для MoP. б , c СЭМ изображения MoP-NC. г , e Изображения MoP-NC с помощью ПЭМ и ВРТЭМ. е - я соответствующие изображения элементарного картирования EDS Mo, P, C и N
Чтобы лучше понять элементное распределение MoP-NC, был охарактеризован XPS. В области спектра Mo 3d Mo содержит два состояния Mo 3+ и Мо 6+ (Рис. 2а). Наличие Mo 3d 3/2 и Mo 3d 5/2 в Мо 3+ состояние привело к пикам микровибрации при 231,5 и 228,2 эв, в то время как пики 235,5 и 232,4 эв были отнесены к Mo 3d 3/2 и Mo 3d 5/2 в Мо 6+ состояние, поскольку поверхность материала MoP-NC неизбежно окислялась на воздухе [24, 25]. В области P 2p (рис. 2b) пики микровибрации 130,7 и 129,4 эВ были отнесены к P 2p 1/2 и P 2p 3/2 соответственно, обнаруживая присутствие P 3− [26]. Пик 133,9 эВ можно отнести к PO 4 3– [27]. В XPS-спектре C 1s (рис. 2c) основные пики, соответствующие трем химическим связям, составили 228,7 эВ (OC =O), 284,8 эВ (CN / C =C) и 286,3 эВ (CC) соответственно [28 ]. Появление C-N / C =N предполагает, что некоторые из атомов углерода в MoP-NC были заменены атомами азота с образованием углерода с примесью азота. В спектре N 1s (рис. 2d) из этой области могут быть решены три различных азотных окружения, где пики 398,4 и 402,1 эВ с более высокими энергиями связи соответствуют основным количествам пиридини и незначительному количеству четвертичного азота, соответственно. Кроме того, пик при 394,5 эВ был обозначен как комбинация N и Mo 3p [29].
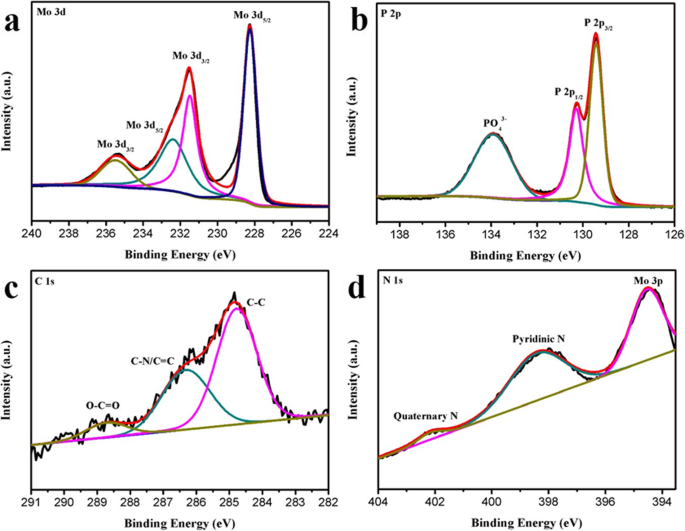
XPS-спектры ( a) Пн 3d, ( b) P 2p, ( c ) C 1s и ( d ) N 1с регионов
Электрокаталитическая активность HER MoP-NC в 1 М КОН (pH =14) с использованием типичной трехэлектродной системы со скоростью развертки 10 мВ с
-1
. Поскольку свойства приготовленных материалов требовали сравнительного анализа, также были изучены Mo-NC, Bulk-MoP и MoP-C. На рис. 3а изображены кривые LSV. Добавление Pt / C и чистого стеклоуглеродного электрода (Blank) сделало кривые в целом более иерархическими. Перенапряжение MoP-NC при плотности тока 10 мА см
−2
требуется всего 131 мВ, что значительно лучше, чем у Mo-NC и Bulk-MoP. Кроме того, эффективность LSV для MoP-C, полученного из глюкозы вместо мочевины в качестве источника углерода, также была невысокой у MoP-NC. Стоит отметить, что по сравнению с HER в кислотном растворе скорость образования ионов H при разложении воды HER в щелочной среде была медленнее (примерно на 2–3 порядка ниже, чем кислотная активность) и была более сложной [30 , 31,32]. На рисунке 3b показано уравнение подобранного графа Тафеля: η = а + b журнал j , где b - наклон Тафеля, а j - плотность тока [33]. Тафелевский наклон Pt / C составляет 58 мВ дек
−1
, по сравнению с Mo-NC (121 мВ разл
−1
), Bulk-MoP (135 мВ дек
−1
) и MoP-C (75 мВ дек
−1
), У MoP-NC был нижний параметр всего 66 мВ дек
−1
, что указывает на то, что каталитическая кинетика HER для электрода MoP-NC была быстрее. В то же время мы обнаружили, что MoP-NC в этой работе был вполне конкурентоспособен с характеристиками HER ранее описанного композитного / углеродного электрокатализатора на основе Mo (Таблица 1). Как видно из Таблицы 1, большинство материалов на основе MoP были основаны на кислотных условиях и редко тестировались в щелочных условиях [17,18,19, 22,23,24, 34,35,36,37]. Кроме того, некоторые из них были протестированы как в кислой, так и в щелочной среде [38,39,40,41]. Однако только материалы MoP с аморфным углеродным покрытием в этих материалах работают лучше в щелочной среде, чем в кислой. Причина, по которой MoP-NC в нашей работе может достичь хороших характеристик HER в щелочной среде, заключалась в том, что мочевина использовалась как в качестве источника углерода, так и источника азота в процессе синтеза, во время которого она также разлагала некоторое количество газа. Он замедляет полимеризацию MoP, легированного азотом и углеродом, который играет прекрасную вспомогательную роль в синтезе. Стабильность приготовленных материалов была непрерывной CV со скоростью сканирования 100 мВ с
-1
. . После 1000 циклов на кривой LSV наблюдалась небольшая потеря плотности тока по сравнению с исходным значением (рис. 3c). На рисунке 3d показаны графики CV MoP-NC, которые были выполнены в том же диапазоне напряжений (0,847–0,947 В относительно RHE) в разных диапазонах скорости сканирования (20–200 мВ). Для дальнейшего изучения емкости двойного слоя ( C dl ) материала, C dl серии контрольных групп показан на рис. 3д. C dl Mo-NC, Bulk-MoP и MoP-C составляли 0,8 мФ см
-2
, 60 мкФ см
−2
и 1,6 мФ см
−2
соответственно, а C dl MoP-NC составляло 10,9 мФ см
-2
который был намного больше, чем указанные выше материалы. Предположение показало, что MoP-NC имеет более высокую активную площадь поверхности. Кроме того, проводимость MoP-NC оценивали с помощью спектроскопии электрохимического импеданса (EIS). На рис. 3f показана диаграмма Найквиста для различных катализаторов. Сопротивление переноса заряда у катализатора MoP-NC было ниже, чем у других катализаторов, а это означало, что более высокая степень переноса электронов у катализатора MoP-NC после со-легирования N, C дополнительно улучшала электрокаталитические характеристики HER.> 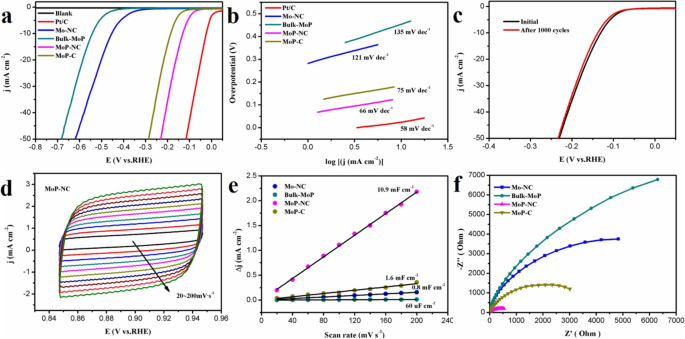
а Кривые LSV со скоростью сканирования 10 мВ с −1 при комнатной температуре в 1 М КОН. б Тафелевские графики синтезированных образцов. c Стабильность MoP-NC после 1000 циклов вольтамперометрии (CV). г Графики CV MoP-NC при скорости сканирования от 20 до 200 мВ с -1 . е Двухслойный конденсатор ( C dl ) Mo-NC, Bulk-MoP, MoP-NC и MoP-C с током конденсатора 0,1 В. f Спектры EIS Mo-NC, Bulk-MoP, MoP-NC и MoP-C
Выводы
Таким образом, мы синтезировали аморфные мелкие частицы MoP-NC простым и эффективным двухэтапным методом. Поскольку наночастицы MoP были покрыты углеродом, они частично агрегировались вместе. К счастью, эта структура не влияет на характеристики самого материала, но также способствует его устойчивости. Эта общая дисперсия, локально агрегированные мелкие частицы материала достигли плотности тока 10 мА см −2 . в 1 M KOH, для чего требуется только перенапряжение 131 мВ, что превосходит заявленные характеристики HER для одиночного фосфид молибдена в щелочной среде. Кроме того, материал демонстрировал незначительное ухудшение рабочих характеристик даже после сканирования 1000 циклов CV. Наши результаты показывают, что MoP с углеродным покрытием также может преодолевать щелочную среду, обеспечивая превосходную электрокаталитическую активность и стабильность HER.
Доступность данных и материалов
Все данные полностью доступны без ограничений.
Сокращения
- CA:
-
Лимонная кислота
- C dl :
-
Емкость двойного слоя
- Резюме:
-
Циклическая вольтамперометрия
- EIS:
-
Электрохимическая импедансная спектроскопия
- HER:
-
Реакция выделения водорода
- HRTEM:
-
Электронная микроскопия переходов высокого разрешения
- КОН:
-
Гидроксид калия
- LSV:
-
Вольтамперометрия с линейной разверткой
- MoP:
-
Фосфид молибдена
- MoP-NC:
-
MoP, со-легированный N, C
- SCE:
-
Насыщенный каломельный электрод
- SEM:
-
Сканирующая электронная микроскопия
- ТЕМ:
-
Переходная электронная микроскопия
- TMPs:
-
Фосфиды переходных металлов
- TOP:
-
Триоктилфосфин
- XPS:
-
Рентгеновская фотоэлектронная спектроскопия
- XRD:
-
Рентгеновская порошковая дифракция
Наноматериалы
- Высокоэффективный промывочный агент для выдувных полиолефинов
- MoS2 с контролируемой толщиной для электрокаталитического выделения водорода
- Композиты с квантовыми точками на S, N-графене / TiO2 для эффективного фотокаталитического производства водород…
- Простой синтез наночастиц SiO2 @ C, закрепленных на MWNT, в качестве высокоэффективных анодных материалов для лити…
- Синтез зеленого цвета в одной емкости микросферы SnO2, украшенной серебром:эффективный и многоразовый катализ…
- Наночастицы кремнезема для доставки внутриклеточного белка:новый подход к синтезу с использованием зеленог…
- Метод последующей обработки для синтеза монодисперсных бинарных наночастиц FePt-Fe3O4
- Исследование каркаса Zr – металл – органика как эффективного фотокатализатора для производства водорода
- Иерархическая гетероструктура полых сфер ZnO @ TiO2 для высокоэффективного фотокаталитического выделения водор…
- Функциональный пористый полимер на основе трифенилфосфина как эффективный гетерогенный катализатор синтез…



