Повышенное фотокаталитическое выделение водорода путем загрузки квантовых точек Cd0.5Zn0.5S на пористые нанолисты Ni2P
Аннотация
Ни 2 P был декорирован на нанопроводах или наностержнях CdS для эффективного фотокаталитического H 2 производство, в то время как удельная поверхность остается ограниченной из-за большого размера. Здесь композиты Cd 0,5 Zn 0,5 S квантовые точки (КТ) на тонком Ni 2 Пористые нанолисты P с высокой удельной поверхностью были созданы для фотокаталитического H 2 , не содержащего благородных металлов. поколение. Пористый Ni 2 Нанолисты P, которые были сформированы путем соединения Ni 2 размером 15–30 нм Наночастицы P, допускающие равномерную загрузку Cd размером 7 нм 0,5 Zn 0,5 S КТ и контролируемая плотность загрузки. Путем настройки содержания Ni 2 P, H 2 скорость образования 43,3 мкМ ч - 1 (1 мг фотокатализатора) и 700 мкМ ч - 1 (100 мг фотокатализатора) и эффективность преобразования солнечной энергии в водород 1,5% была достигнута для Ni 2 P-Cd 0,5 Zn 0,5 Композиты S. Эффект Ni 2 Систематически изучалось содержание Р на светопоглощение, фотолюминесценцию и электрохимические свойства композита. Вместе с расчетом зонной структуры на основе теории функционала плотности продвижение Ni 2 Выявлены P в переносе заряда и активность HER, а также влияние затенения на поглощение света. Такую стратегию можно применить к другим фотокатализаторам для эффективного производства водорода на солнце.
Фон
В качестве эффективной стратегии производства H 2 Фотокаталитическое производство водорода за счет использования солнечной энергии привлекло большое внимание с тех пор, как TiO 2 был описан как фотокатализатор в 1972 г. [1]. По сравнению с TiO 2 , Кд x Zn 1 − x S демонстрирует превосходную каталитическую активность, управляемую видимым светом, благодаря более узкой запрещенной зоне и хорошей фотохимической стабильности. A H 2 производительность до 1097 мкМ ч - 1 г - 1 было достигнуто с помощью Cd 0.5 Zn 0,5 S в качестве фотокатализатора [2], состав которого оказался оптимальным с точки зрения фотокаталитических свойств. Для уменьшения рекомбинации носителей и быстрого отделения носителей в реакции выделения водорода (HER) в качестве сокатализаторов использовались благородные металлы, такие как Pt, Co-Pt, Ru, Au и Pd [3,4,5,6,7, 8]. Например, при сокатализе с Co-Pt фотокаталитический H 2 скорость образования КД 0,5 Zn 0,5 S квантовые точки (КТ) могут быть увеличены в 4,7 раза [4]. A H 2 добыча достигает ~ 6.3 ммоль / час - 1 мг - 1 была достигнута при сочетании CdZnS с Au [9]. Однако высокая стоимость благородных металлов сильно ограничивает их будущее крупномасштабное применение, что делает недрагоценные сокатализаторы хорошими кандидатами на благородные для фотокаталитического H 2 поколение.
Среди различных неблагородных сокатализаторов, включая семейство углерода (графен, углеродные нанотрубки, восстановленный оксид графема, углеродные наноточки) [10,11,12,13,14,15], фосфиды [16,17,18,19,20 , 21,22] и TiO 2 [23, 24] и сульфиды [25,26,27,28,29,30,31,32], Ni 2 P и CoP широко комбинируются с нанопроволокой и / или наностержнями CdS для эффективного фотокаталитического H 2 производство [16,17,18, 33,34,35,36]. В этих композитах одномерный (1D) CdS всегда декорировался более мелкими наночастицами фосфидов или нанолистами с HER-активностью, и рекомбинация носителей может быть значительно уменьшена из-за большой длины диффузии носителей в одномерной структуре и ее четко определенных гетероструктур. интерфейс с сокатализаторами. Принимая во внимание преимущества квантовых точек, такие как высокая эффективность преобразования солнечной энергии в топливо, низкие затраты на производство [37, 38] и HER в основном возникает на границе раздела сокатализатор / электролит, рационально создавать гетеронаноструктуры с большой удельной поверхностью. область активных сайтов, сохраняя при этом быстрое разделение несущих. В этом случае для эффективного фотокаталитического H 2 сообщалось об обратной структуре с фотокатализаторами, загруженными на сокатализаторы. поколение [10, 13]. Например, скорость образования водорода составляет 2,08 и ~ 33,4 мМ ч - 1 мг - 1 были установлены загрузкой Cd 0.5 Zn 0,5 S QD на луковицеобразный углерод и двумерный графитовый нитрид углерода (g-C 3 N 4 ) микроленты соответственно. Это делает его весьма ожидаемым для фотокаталитического H 2 генерация при декорировании фосфидных наноструктур Cd 0,5 Zn 0,5 S КТ. Однако до сих пор о такой обратной структуре редко сообщалось.
Здесь обратная структура Cd 0,5 Zn 0,5 S QD на Ni 2 Массивы нанолистов P были синтезированы методом термического растворения для улучшенного фотокаталитического H 2 поколение. Скорость образования водорода 700 мкМ ч - 1 (с подачей 100 мг катализатора) и КПД от солнечной энергии к водороду (STH) 1,5% были достигнуты при 1,5 мас.% Ni 2 P. Эффект Ni 2 P на H 2 Систематически изучены скорость генерации, оптические и электрохимические свойства композита. Кроме того, зонная структура Ni 2 P был рассчитан на основе теории функционала плотности, вместе с фотоэлектрохимическими свойствами, детальной ролью Ni 2 P для H 2 было выявлено поколение.
Методы / экспериментальные
Синтез сокатализатора
Сначала 20 мл деионизированной воды, содержащей 2,61 г нитрата никеля и 2,52 г гексаметилентетрамина, переносили в тефлоновый автоклав и нагревали при 120 ° C в течение 10 часов для образования NiOOH. После охлаждения до комнатной температуры продукт NiOOH промывали спиртом и деионизированной водой путем центрифугирования при 2000 об / мин трижды и каждый раз по 5 мин. Затем смесь 0,22 г NiOOH и 0,44 г гипофосфита натрия помещали в трубчатую печь и нагревали при 500 ° C в течение 2 ч для фосфорирования. Когда он естественным образом остыл до комнатной температуры, черный Ni 2 Порошок Р. был получен и собран.
Синтез Ni 2 P-Cd 0,5 Zn 0,5 S Нанокомпозиты
Для приготовления Ni 2 P-Cd 0,5 Zn 0,5 Композит S, 100 мг Ni 2 Порошок P диспергировали в 20 мл этанола с помощью ультразвуковой обработки в течение 1 ч. Затем x мл ( x =0,48, 0,96, 1,4, 3, 5) высокодисперсный Ni 2 Раствор P добавляли в 20 мл раствора этиленгликоля, содержащего 272,6 мг ZnCl 2 . и 456,7 мг CdCl 2 ∙ 2,5 ч 2 O, и нагревали до 170 ° C при непрерывном перемешивании в атмосфере азота. После добавления 20 мл раствора этиленгликоля, растворяющего 960,7 мг Na 2 S ∙ 9H 2 O, раствор нагревали до 180 ° C и выдерживали 1 ч для роста Cd 0,5 Zn 0,5 S на Ni 2 P. Наконец, образцы трижды промывали спиртом и деионизированной водой соответственно. Взвесив окончательный xNi 2 P-Cd 0,5 Zn 0,5 S композиты, массовые проценты (мас.%) Были определены равными 0,5 ( x =0,48), 1 ( x =0,96), 1,5 ( x =1,4), 3 ( x =3), 5 ( x =5). Для сравнения чистый Cd 0,5 Zn 0,5 S КТ были синтезированы аналогичным методом, за исключением добавления Ni 2 П.
Характеристика морфологии, структуры и оптических свойств
Морфология, микроструктура и состав были охарактеризованы с помощью автоэмиссионной сканирующей электронной микроскопии (FESEM, JSM-7100F, JEOL) и просвечивающей электронной микроскопии (TEM, FEI Tecnai 20) с использованием сканирующей просвечивающей электронной микроскопии (STEM) и энергодисперсионной рентгеновской микроскопии. спектроскопия (EDX). Картины порошковой дифракции рентгеновских лучей (XRD) записывали на рентгеновском дифрактометре Bruker AXS D8 с Cu Kα (λ =1,54056 Å). Элементный состав, химические и валентные состояния были изучены с помощью рентгеновской фотоэлектронной спектроскопии (XPS) (валентная зона) (XPS, Escalab 250Xi) с излучением Al Kα. Поглощение в УФ-видимой области исследовали с помощью спектрофотометра УФ-видимой области (UV-3600, Shimadzu), снабженного устройством интегрирующей сферы, и соотношение массы / объема образца к деионизированной воде поддерживали на уровне 1 мг / 10 мл. Измерения фотолюминесценции (ФЛ) проводили на спектрофотометре 7000 FL (Hitachi, F7000) с длиной волны возбуждения 400 нм. Перед измерениями ФЛ чистый Cd 0,5 Zn 0,5 КТ S и композиты хорошо диспергировались в этаноле, а концентрация Cd 0,5 Zn 0,5 S поддерживали на уровне 0,5 мг / мл для всех образцов.
Измерения линейной вольтамперометрии (LSV) и спектров электрохимического импеданса (EIS)
Измерения LSV проводились в 1 М электролите NaOH (pH =14) на электрохимической рабочей станции (CHI 760E, CH Instruments) с типичной трехэлектродной конфигурацией. Pt фольга и насыщенный Ag / AgCl использовались в качестве противоэлектрода и электрода сравнения соответственно. Потенциалы были преобразованы в потенциалы обратимого водородного электрода (RHE) по уравнению E (vs RHE) =E (vs Ag / AgCl) + E Ag / AgCl (ref) + 0,0591 В × pH, где (E Ag / AgCl (ref) =0,1976 В по сравнению с NHE (нормальным водородным электродом) при 25 ° C) [39]. Измерения спектров электрохимического импеданса (EIS) проводили в темноте при 0,5 В по сравнению с RHE с амплитудой 5 мВ и электролитом 0,35 М Na 2 . SO 3 и 0,25 М Na 2 S с использованием аналогичной трехэлектродной системы. Рабочий электрод получали путем распределения ~ 2 мг продукта (диспергированного в 5 мл этанола) на 4 см 2 области подложки FTO и сушат при 70 ° C в течение 5 часов. Частотный диапазон находился в пределах 0,1 Гц ~ 100 кГц, а спектры анализировались программой Z-View (Scribner Associates Inc.).
Фотокаталитический (ПК) H 2 Поколение
Перед H 2 При производстве фотокатализаторы с разной массой (1, 5 и 10 мг) диспергировали в герметичном кварцевом реакторе (объем 40 мл, 5 см × 5 см × 1,6 см) с 15 мл 0,75 М Na 2 S и 1,05 М Na 2 SO 3 водный раствор. После 30-минутной дегазации азотом фотокаталитический эксперимент проводился при облучении Xe-лампой 300 Вт (PLS-SXE300 / 300UV, Perfect Light) с отсекающим фильтром 420 нм и падающей мощностью 300 мВт / см. 2 . Каталитический раствор постоянно перемешивали в течение всего эксперимента с ПК. Каждый час производился сбор газа объемом 1 мл и анализировался с помощью газового хроматографа (GC-2018, Shimadzu, Япония, TCD). Дальнейший эксперимент по стабильности при циклическом движении был проведен при тех же условиях. Параллельные эксперименты с дозировкой фотокализаторов от 15 до 100 мг были проведены в 100 мл электролита Na 2 . S и Na 2 SO 3 в реактор большего размера (объемом 150 мл) при таком же освещении. Эффективность преобразования солнечной энергии в водород (STH) рассчитывалась по уравнению протекания:
$$ {\ displaystyle \ begin {array} {l} \ mathrm {STH} \ \ left (\% \ right) =\ kern0.5em \ frac {\ mathrm {energy} \ \ mathrm {of} \ \ mathrm { сгенерировано} \ {\ mathrm {H}} _ 2} {\ mathrm {light} \ \ mathrm {energy} \ \ mathrm {on} \ \ mathrm {the} \ \ mathrm {surface} \ \ mathrm {of} \ \ mathrm {решение}} \ times 100 \% \\ {} \ kern6.5em =\ frac {237 \ mathrm {KJ} / \ mathrm {мол} \ kern0.5em \ times \ mathrm {moles} \ \ mathrm {из } \ {\ mathrm {H}} _ 2 \ \ mathrm {producted}} {\ mathrm {area} \ \ mathrm {of} \ \ mathrm {solution} \ \ mathrm {been} \ \ mathrm {irradiated} \ times 300 \ mathrm {mW} / {\ mathrm {cm}} ^ 2} \ times 100 \% \ end {array}} $$Вычислительные методы
Энергетические и электронные свойства объемного Ni 2 P рассчитывали с использованием метода теории функционала плотности (DFT). Венский пакет моделирования Ab-initio (VASP) [40] был принят во время расчетов с проектором расширенных волновых псевдопотенциалов (PAW) [41] и обобщенным градиентным приближением типа Perdew-Burke-Ernzerhof (PBE) (GGA) [42 ] обменно-корреляционные функциональные методы. Зона Бриллюэна с сеткой точек Монкхорста-Пак 9 × 9 × 9 [43], кинетической энергией, отсеченной на уровне 450 эВ, и энергетическим критерием 10 - 6 эВ применялись для геометрической оптимизации до тех пор, пока остаточные силы не сойдутся до менее 0,01 эВ / Å. Объемная модель гексагонального Ni 2 Учитывались П с симметрией П-62М. После полной оптимизации структуры параметр решетки Ni 2 P ( a = b =5,86918 Å, и c =3,37027 Å), что хорошо согласуется с указанными значениями [44].
Результаты и обсуждение
На рис. 1а, б показана морфология Ni 2 . P до и после композиции с Cd 0,5 Zn 0,5 S КТ (Ni 2 П мас.%:1,5%). Чистый Ni 2 P имеет морфологию, похожую на цветок, которая состоит из множества скрещенных нанолистов толщиной менее 20 нм и плоскими размерами от нескольких десятков нанометров до микрометра. Из рентгенограммы чистого Ni 2 P на рис. 1в, дифракционные пики плоскостей (111), (201), (210) и (300) отчетливо видны при 40,7 °, 44,6 °, 47,4 ° и 54,2 ° соответственно, что соответствует гексагональной Ни 2 P (JCPDF № 89-2742). После загрузки CD 0.5 Zn 0,5 S QD поверхность нанолистов становится довольно шероховатой, и на чистом Ni 2 можно различить множество наночастиц размером менее 10 нм. Скелет P. В то же время пики преломления XRD Cd 0,5 Zn 0,5 Плоскости S (JCPDF № 89-2943) (100), (002), (101) и (110) четко видны под 26,0 °, 27,8 °, 29,6 ° и 45,9 ° соответственно [6, 45] , а дифракционный сигнал Ni 2 P сильно снижен из-за низкого массового соотношения (1,5 мас.%) Ni 2 P в Cd 0,5 Zn 0,5 S. Сосуществование Cd 0.5 Zn 0,5 S и Ni 2 P был продемонстрирован с помощью рентгеновского фотоэлектронного спектрометра (XPS) и обзорных спектров на рис. 1d – f. За исключением сигналов кислорода и углерода, возникающих при абсорбции воздуха, могут быть обнаружены только Ni, P, Cd, Zn и S, что исключает возможность других примесей. Пики при 855,5 и 873,9 эВ можно отнести к Ni 2p 3/2 и 2р 1/2 соответственно, а пик P 2p 3/2 находится при 133,6 эВ [16, 46]. Одновременно пики дублетов Zn 2p, Cd 3d и S 2p указывают на двухвалентный Zn 2+ , CD 2+ , и S 2− с компакт-диска 0,5 Zn 0,5 S КТ [3, 34, 47]. Вкратце, рост Cd 0,5 Zn 0,5 S на Ni 2 Нанолисты P были созданы для образования Ni 2 P-Cd 0,5 Zn 0,5 Нанокомпозиты S.
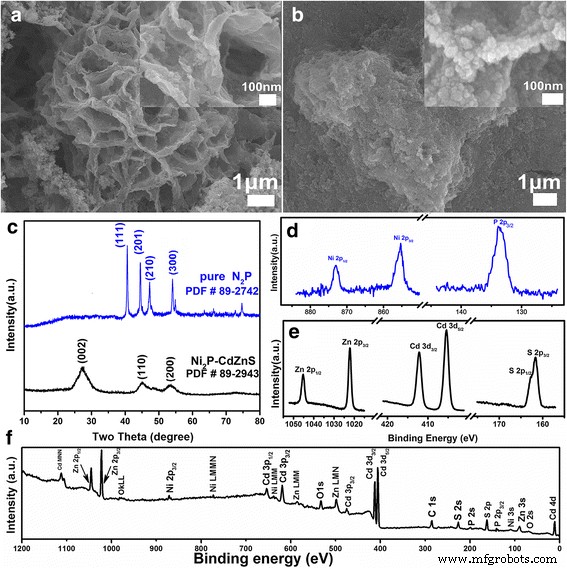
Морфология, кристаллические свойства и химическое состояние Ni 2 P-Cd 0,5 Zn 0,5 Композиты S (1,5 мас.% Ni 2 П). а – б СЭМ-изображения Ni 2 с малым и большим (вставка) увеличения P до и после загрузки Cd 0,5 Zn 0,5 S, c Рентгенограмма Ni 2 P и Ni 2 P-Cd 0,5 Zn 0,5 S, d – f XPS тонкие и обзорные спектры Ni 2 P-Cd 0,5 Zn 0,5 S композит
Микроструктура и элементный состав образцов были дополнительно исследованы методами просвечивающей электронной микроскопии. Из изображений ПЭМ с разным увеличением чистого Ni 2 P (рис. 2а, б), нанолисты пористые и состоят из сшитых наночастиц неправильной формы размером ~ 15–30 нм. Выбранная область электронограммы (SAED) на рис. 2c показывает дифракционное кольцо Ni 2 P (111), (201), (210) и (300) плоскости. Дифракционные сигналы плоскостей с высоким показателем преломления, таких как (222), (402) и (420), также могут быть обнаружены из-за сильного многократного рассеяния электронов высоких энергий. После компоновки с Cd 0.5 Zn 0,5 S, перекрещенные Ni 2 Нанолисты P были покрыты множеством более мелких наночастиц размером ~ 7 нм (рис. 2d). Спектры EDX (вставка, рис. 2f) ясно показывают сигнал Ni, P, Cd, Zn и S, что указывает на сосуществование Ni 2 P и Cd 0,5 Zn 0,5 S. По картине SAED (рис. 2е) сильные дифракционные кольца Cd 0,5 Zn 0,5 Плоскости S (002), (110) и (200) (обозначенные желтыми пунктирными линиями) можно четко различить вместе со слабыми сигналами Ni 2 P (300), (402) и (420) (отмечены белыми пунктирными линиями), что свидетельствует о хорошем составе Ni 2 P с квантовыми точками. Примечательно, что Ni 2 Кольцо P (300) перекрывается с Cd 0,5 Zn 0,5 S (110) и (200), что затрудняет различение. Электронно-микроскопическое изображение Ni 2 с высоким разрешением. P-Cd 0,5 Zn 0,5 Образец S на рис. 2e также показывает полосы решетки с шагом 0,34 и 0,22 нм, что соответствует Cd 0,5 Zn 0,5 S (002) и Ni 2 Плоскости кристалла P (111) соответственно. Элементные отображения EDX (рис. 2h – l), взятые из области, показанной изображением высокоуглового кольцевого темного поля (HAADF) (рис. 2g), показывают, что Ni, P, Cd, Zn и S равномерно распределены между образец, дополнительно демонстрирующий успешную композицию Cd 0,5 Zn 0,5 S КТ с пористым Ni 2 Нанолисты П.

Микроструктура Ni 2 P и Ni 2 P-Cd 0,5 Zn 0,5 S композит. а – в и d – f ПЭМ-изображения с разным увеличением и SAED-изображение Ni 2 P и Ni 2 P-Cd 0,5 Zn 0,5 S, вставка f - спектр EDX, где желтые и белые пунктирные линии обозначают Cd 0,5 Zn 0,5 S и Ni 2 P соответственно. г Изображение STEM с высокоугловым кольцевым темным полем (HAADF) и h – l соответствующие EDX-отображения Ni 2 P-Cd 0,5 Zn 0,5 S композит
На рисунке 3а показан H 2 скорость эволюции Ni 2 P-Cd 0,5 Zn 0,5 Нанокомпозиты S варьировались в зависимости от содержания Ni 2 P при дозировке питания 1 мг в реакторе на 40 мл. Чистый Cd 0,5 Zn 0,5 S показывает фотокаталитический H 2 скорость эволюции 12,6 мкМ ч - 1 мг - 1 , и чистый Ni 2 P показывает незначительное образование водорода. С добавлением Ni 2 P, фотокаталитическая активность Ni 2 P-Cd 0,5 Zn 0,5 Композиты S, очевидно, были улучшены и достигли максимального значения 43,3 мкМ h - 1 мг - 1 при 1,5 мас.% Ni 2 P, почти в 3,4 раза выше, чем у чистого Cd 0,5 Zn 0,5 S. Дальнейшее добавление Ni 2 P (≥ 3 мас.%) Приведет к быстрому ухудшению свойств, а H 2 скорость эволюции меньше чистого Cd 0,5 Zn 0,5 S, когда Ni 2 P увеличивается до 5 мас.%. Такое нелинейное поведение предполагает, что существует оптимальный Ni 2 Содержание P, а именно подходящая плотность загрузки Cd 0,5 Zn 0,5 S на Ni 2 P для фотокаталитического свойства. В то же время стабильность 1,5 мас.% Ni 2 P-Cd 0,5 Zn 0,5 S изучали с помощью велосипедного теста (рис. 3b). В течение четырех последовательных циклов, которые длились в общей сложности 16 ч, H 2 поколение сохранялось относительно стабильным с незначительной деградацией, что указывает на хорошую фотокаталитическую стабильность композита.
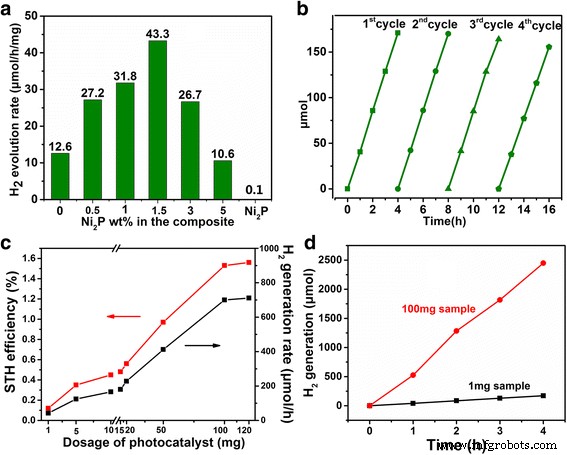
Фотокаталитические свойства Ni 2 P-Cd 0,5 Zn 0,5 Композиты S. а Фотокаталитическое получение водорода при разном весовом% Ni 2 P и b циклическое испытание композита с 1,5 мас.% Ni 2 P тестировали в небольшом реакторе (40 мл, 1,0 мг фотокатализатора). c Скорость производства водорода и эффективность преобразования солнечной энергии в водород (STH) при различном количестве фотокатализатора. Испытания фотокатализатора с дозировкой от 15 до 100 мг проводили в реакторе объемом 150 мл, а испытания с дозировкой от 1 до 10 мг - в реакторе на 40 мл. г Скорость образования водорода для композитных образцов 1 и 100 мг (1,5 мас.% Ni 2 P)
Влияние количества катализатора на эффективность STH и H 2 Генерация была систематически изучена (рис. 3c – d) для 1,5 мас.% Ni 2 P-Cd 0,5 Zn 0,5 Образец S. Были приняты два типовых реактора объемом 40 и 150 мл при одинаковой плотности мощности освещения. При испытании в меньшем реакторе (40 мл), хотя и STH, и H 2 скорость образования увеличивается с дозировкой катализатора от 1 до 10 мг, шаг увеличения намного меньше, чем при дозировке. STH и H 2 скорость генерации всего 0,45% и 166 мкМ ч - 1 когда дозировка катализатора увеличилась до 10 мг, почти в 3,8 раза по сравнению с образцом 1 мг. Для реактора большего размера (150 мл) отчетливое увеличение STH и H 2 поколение можно найти с дозировкой, увеличенной с 15 до 100 мг, и 1,53% STH и 700 мкМ ч - 1 из H 2 генерация может быть достигнута при дозировке 100 мг, что почти в 3,1 раза больше, чем у 15 мг катализатора. Учитывая, что падающий свет имеет более длинный путь, когда он проходит через более глубокий реактор, такой результат показывает, что более крупный реактор будет более выгодным для использования падающего света. Однако эффективность СТГ достигнет насыщения после увеличения дозировки до примерно 100 мг, что позволяет предположить, что существует оптимальная дозировка для использования света. Оптимальный H 2 скорость генерации превосходит CdZnS QDs-2D g-C 3 N 4 микроленты (H 2 скорость образования 33,4 мМ ч - 1 г - 1 ) [10], Cd 0,1 Zn 0,9 Наночастицы S-углеродные нанотрубки (скорость:1563 мкМ ч - 1 г - 1 ) [11], C 3 с сэндвич-структурой N 4 / Au / CdZnS фотокатализатор (расход 6,15 мМ ч - 1 г - 1 ) [9], и сенсибилизированный КТ CdS Zn 1 − x Компакт-диск x Твердые растворы S (скорость 2128 мкМ ч - 1 г - 1 ) [48].
Выявить механизм улучшенных фотокаталитических свойств и подробно изучить роль Ni 2 P, как оптические, так и электрохимические свойства чистого Ni 2 P, Cd 0,5 Zn 0,5 S, а композиты исследованы на рис. 4. Из спектров поглощения (рис. 4а) чистый Cd 0,5 Zn 0,5 S имеет край поглощения при 506 нм, соответствующий ширине запрещенной зоны 2,45 эВ [13, 49]. Для чистого Ni 2 P (вставка) видно широкое поглощение во всем видимом диапазоне. После состава, помимо поглощения в диапазоне <506 нм, можно обнаружить очевидные хвосты в видимой области спектра> 506 нм, что можно отнести к вкладу Ni 2 P. Поскольку видимое поглощение на более длинных волнах увеличивается с Ni 2 P, композит показывает пониженное поглощение Cd 0,5 Zn 0,5 S (<506 нм). В то же время спектры фотолюминесценции (рис. 4б) показывают, что чистый Cd 0,5 Zn 0,5 S имеет интенсивную краевую люминесценцию на длине волны ~ 620 нм при возбуждении на длине волны 400 нм. После композиции он будет постепенно разлагаться при добавлении Ni 2 П. Учитывая, что более высокое содержание Ni 2 P вызовет больше Ni 2 P / Cd 0,5 Zn 0,5 S-интерфейсов, которые помогают улучшить перенос заряда и подавить рекомбинацию зарядов, уменьшение интенсивности ФЛ можно понять по уменьшению рекомбинации носителей и усилению переноса заряда на Ni 2 P / Cd 0,5 Zn 0,5 Интерфейс S.
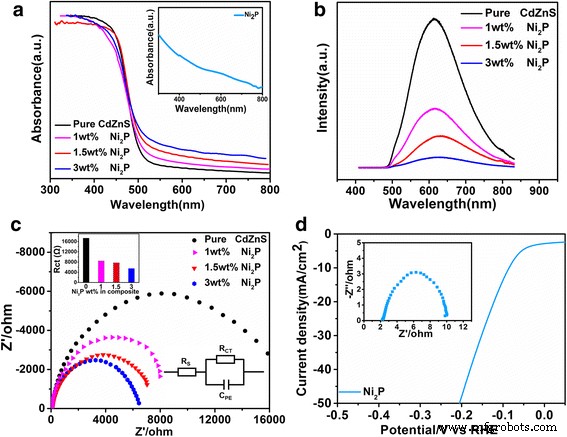
Эффект Ni 2 Содержание P от оптических и электрохимических свойств Ni 2 P-Cd 0,5 Zn 0,5 S композит. а Спектры поглощения в УФ и видимой областях (вставка чистый Ni 2 P), b спектры фотолюминесценции и c Спектры ЭИС. г Кривая LSV и спектр EIS (вставка) чистого Ni 2 П
Эффективная роль Ni 2 P в подсказке переноса заряда также может отражаться в спектрах EIS в зависимости от Ni 2 Содержание P (рис. 4в). Как показано эквивалентной схемой (вставка, рис. 4c), сопротивление переносу заряда (Rct) на границе раздела катализатор / электролит можно оценить по радиусу полукруга графиков Найквиста на основе эквивалентной схемы R-C. Эквивалентное последовательное сопротивление (ESR) может быть получено из пересечения кривой и реального сопротивления ( Z ’), А сопротивление переносу заряда (Rct) соответствует ширине полукруга, нанесенного на более высокие частоты. R CT чистого Cd 0,5 Zn 0,5 S составляет 17 320 Ом, что указывает на его полупроводниковую природу. После композиции с 1, 1,5 и 3 мас.% Ni 2 P, R CT постепенно уменьшается до 8432, 7721 и 5473 Ом соответственно, что свидетельствует об усилении Ni 2 P в электропроводности. Действительно, Ni 2 P считается хорошим электрокатализатором для HER [44, 50, 51]. Из кривой LSV чистого Ni 2 P на пене Ni, показанной на рис. 4d, Ni 2 P имеет хорошую активность HER с перенапряжениями 84 мВ и 201 мВ, чтобы добавить плотность тока 10 и 50 мА / см 2 (без iR-коррекции) соответственно. Спектр EIS (вставка на рис. 4d) показывает, что Ni 2 P имеет очень низкий R CT (~ 7,3 Ом), что указывает на металлический характер Ni 2 P. Следовательно, Ni 2 P может не только увеличивать электрическую проводимость при Cd 0,5 Zn 0,5 S / Ni 2 P, но также обеспечивает эффективные активные центры для HER, что приводит к улучшенным фотокаталитическим свойствам композита.
Учитывая, что добавление Ni 2 P уменьшил поглощение на длине волны <506 нм, необходимо продемонстрировать, действительно ли поглощение света Ni 2 P можно использовать для получения водорода. Зонная структура Ni 2 Затем P исследовали расчетом DFT. На рис. 5а, б представлена шариковая модель массивного Ni 2 . P и рассчитанная зонная структура. Из рис. 5b нельзя обнаружить запрещенную зону, что свидетельствует о металлических характеристиках Ni 2 P, что хорошо согласуется с приведенным выше результатом EIS. Это указывает на то, что фотоэлектроны в основном связаны с фотовозбуждением Cd 0,5 Zn 0,5 S вместо Ni 2 P. Кроме того, уровень Ферми Ni 2 P (полученный из нашего автомобильного файла) находится на уровне 1,03 В по сравнению с NHE, что намного ниже, чем уровень минимума полосы проводимости (CBM) (- 1,04 В по сравнению с NHE) для Cd 0,5 Zn 0,5 S QDs [13].
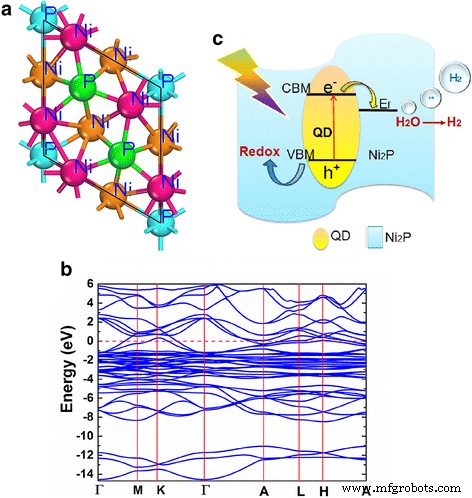
Зонная диаграмма и механизм разделения и переноса заряда для фотокаталитического H 2 эволюция. а Вид сверху на модель шара и клюшки (001) объемного Ni 2 с концевыми поверхностями. П. б Расчетная зонная структура Ni 2 P, где красная пунктирная линия представляет уровень Ферми. c Схематический механизм, иллюстрирующий разделение и перенос заряда для фотокаталитического H 2 поколение
Соответственно, схематический механизм был продемонстрирован для фотокаталитического H 2 эволюция композита по рис. 5в. Расположение уровня Ферми Ni 2 P делает его энергетически выгодным для передачи фотогенерированных электронов от Cd 0,5 Zn 0,5 S в Ni 2 P, затем вызывает разделение фотовозбужденных электронов и дырок на границе раздела, что приводит к подавлению рекомбинации заряда. Одновременно H 2 будет эффективно развиваться на активных центрах Ni 2 P из-за хорошей активности HER и большой удельной поверхности композитов. Положительные роли Ni 2 P в переносе заряда и активность HER будут преобладать при более низком содержании Ni 2 P (≤ 1,5 мас.%). Когда содержание превышает 1,5 мас.%, Эффект затенения Ni 2 P в поглощении света преодолеет положительный аспект, что приведет к деградации H 2 поколение. Оптимальные фотокаталитические свойства будут достигнуты при 1,5 мас.% Ni 2 . P, когда два эффекта достигают баланса.
Выводы
Обратная структура Cd 0,5 Zn 0,5 S QD на Ni 2 Были изготовлены пористые нанолисты P для эффективного фотокаталитического H 2 производство. Ни 2 Пористые нанолисты P состоят из наночастиц размером 15–30 нм, что позволяет эффективно загружать Cd размером 7 нм 0,5 Zn 0,5 S КТ. Поскольку свойства разделения и переноса зарядов улучшаются с добавлением Ni 2 P от 0 до 5 мас.%, Конкурентный эффект затенения, который неблагоприятен для поглощения света Cd 0,5 Zn 0,5 S индуцирован. Оптимальный фотокаталитический H 2 получение 43,3 мкМ ч - 1 (дозировка 1 мг) будет достигнута при 1,5 мас.% Ni 2 P. На основании оптимального содержания фотокаталитическая зависимость от подаваемой дозировки катализатора показывает, что эффективность STH достигнет максимального значения 1,5% при дозировке 100 мг. The high HER activity and band structure of Ni2 P were revealed, confirming the effective role of Ni2 P in prompting photocatalytic H2 evolution dynamics from both experimental and theoretical aspects. The heterostructure of Cn0.5 Zn0.5 S QDs-Ni2 P porous nanosheets can not only help to prompt the photo-excited charge separation and transfer, but also speed up the dynamics of hydrogen evolution reaction via the co-catalytic role of Ni2 P, thus enhances the photocatalytic hydrogen generation property. Such a method can be applied to other catalysts toward efficient photocatalytic property.
Сокращения
- CBM:
-
Conductive band minimum
- DFT:
-
Функциональная теория плотности
- EDX:
-
Энергодисперсионная рентгеновская спектроскопия
- EIS:
-
Electrochemical impedance spectra
- FESEM:
-
Field emission scanning electron microscopy
- FTO:
-
Fluorine-doped tin oxide
- GGA:
-
Generalized gradient approximation
- HER:
-
Hydrogen evolution reaction
- LSV:
-
Linear sweep voltammetry
- NHE:
-
Normal hydrogen electrode
- PBE:
-
Perdew-Burke-Ernzerhof type
- ПК:
-
Photocatalytic
- PL:
-
Фотолюминесценция
- QDs:
-
Квантовые точки
- RHE:
-
Реверсивный водородный электрод
- STEM:
-
Сканирующая просвечивающая электронная микроскопия
- STH:
-
Solar to hydrogen
- ТЕМ:
-
Просвечивающая электронная микроскопия
- VASP:
-
Vienna Ab-initio Simulation Package
- XPS:
-
Рентгеновская фотоэлектронная спектроскопия
- XRD:
-
Рентгеновская дифракция
Наноматериалы
- MoS2 с контролируемой толщиной для электрокаталитического выделения водорода
- Композиты с квантовыми точками на S, N-графене / TiO2 для эффективного фотокаталитического производства водород…
- Раскрытие морфологической эволюции и кинетики травления пористых кремниевых нанопроволок во время химическ…
- Фотокаталитическая активность, усиленная Au-плазмонными наночастицами на фотоэлектроде нанотрубки TiO2, покры…
- Иерархическая гетероструктура полых сфер ZnO @ TiO2 для высокоэффективного фотокаталитического выделения водор…
- Новый фотокатализатор на гетеропереходе Bi4Ti3O12 / Ag3PO4 с улучшенными фотокаталитическими характеристиками
- Синергетические эффекты наночастиц Ag / BiV1-xMoxO4 с повышенной фотокаталитической активностью
- Модификация сокатализатора сплава PtNi сенсибилизированного эозином Y гибрида g-C3N4 / GO для эффективного фотокат…
- Легкий синтез и повышенная фотокаталитическая активность в видимом свете новых композитов с гетеропереходо…
- Влияние легирования магнием на наночастицы ZnO для расширенной фотокаталитической оценки и антибактериально…



