Наночастицы альбумина, содержащие ресвератрол, с длительным кровообращением и улучшенной биосовместимостью для высокоэффективной таргетной терапии опухолей поджелудочной железы
Аннотация
Сывороточный альбумин человека (HSA) является внутренним белком и важным носителем, который переносит как эндогенные, так и экзогенные вещества через клеточные мембраны. Здесь мы разработали и приготовили нагруженные ресвератролом (RV) наночастицы HSA, конъюгирующие RGD (аргинин-глицин-аспартат) через полиэтиленгликоль (PEG) «мост» (HRP-RGD NP) для высокоэффективной направленной терапии опухолей поджелудочной железы. НЧ HRP – RGD обладают средним размером 120 ± 2,6 нм с узким распределением, гомодисперсной сферической формой, эффективностью инкапсуляции RV 62,5 ± 4,21% и максимальной степенью высвобождения RV 58,4,2 ± 2,8% при pH 5,0 и 37 ° С. Биосовместимость RV in vitro улучшается после покрытия HSA и PEG. Конфокальные флуоресцентные изображения показывают, что у НЧ HRP-RGD самый высокий коэффициент поглощения клетками 47,3 ± 4,6% по сравнению с НЧ HRP и НЧ HRP-RGD со свободным блокированием RGD, что объясняется RGD-опосредованным эффектом. Набор для подсчета клеток-8 (CCK-8) показывает, что HRP – RGD NP без RV (HP – RGD NP) почти не обладают цитотоксичностью, но HRP – RGD NP значительно более цитотоксичны для клеток PANC-1 по сравнению со свободным RV и НЧ HRP в зависимости от концентрации, демонстрируя апоптотическую морфологию. Кроме того, с составом покрытия PEG и HSA, НЧ HRP – RGD продлевают кровообращение правого желудочка, увеличиваясь примерно в 5,43 раза (t 1/2 ). После внутривенной инъекции мышам с опухолью содержание НЧ HRP – RGD в опухолевой ткани оказалось примерно в 3,01 и 8,1 раза выше, чем содержание НЧ HRP и свободного ПЖ, соответственно. Основываясь на этих результатах, НЧ HRP – RGD были использованы в противораковом исследовании in vivo и продемонстрировали лучший эффект подавления роста опухоли из всех протестированных препаратов без рецидива, высокой биосовместимости in vivo и отсутствия значительной системной токсичности в течение 35 дней лечения. Эти результаты демонстрируют, что НЧ HRP – RGD с длительным кровообращением и улучшенной биосовместимостью обладают высокими противораковыми эффектами и имеют многообещающее применение в будущем в терапии рака.
Фон
Рак поджелудочной железы представляет собой разрушительное заболевание, при котором средняя выживаемость составляет менее 6 месяцев, а коэффициент выживаемости только 5 лет составляет 6% [1]. Традиционным клиническим лечением рака поджелудочной железы является хирургическое удаление, лучевая терапия и химиотерапия [2, 3]. Однако эти методы могут быть ограничены серьезными побочными эффектами, такими как распространение раковых клеток после неполного иссечения, серьезная токсичность для нормальных клеток во время лучевой терапии и низкая выживаемость [4]. Хотя низкие целевые эффекты и высокие побочные эффекты также ограничивают применимость противораковых препаратов в химиотерапии, разрабатывается все больше новых химиотерапевтических агентов. Помимо синтетических лекарств, многие экстракты китайских трав эффективны против определенных типов рака. Ресвератрол (RV), натуральный экстракт растений, таких как виноград и соевые бобы [5], широко используется в агрегации тромбоцитов и ингибировании вазодилатации, а также снижении вязкости крови [6, 7]. А в последние десятилетия было обнаружено, что он оказывает сильное противораковое действие при некоторых видах рака, таких как рак печени, груди и яичников [8, 9]. Однако использование RV в качестве потенциального противоракового препарата имеет некоторые недостатки для дальнейшего клинического применения, такие как плохая растворимость, слабое кровообращение и отсутствие селективности [4, 10].
С точки зрения защиты структурной целостности лекарственного средства, стратегия инкапсуляции привлекла интерес многих исследователей, которая продемонстрировала свою эффективность в преодолении некоторых из вышеупомянутых недостатков по сравнению с обычными «бесплатными» лекарствами [11]. Например, он может улучшить плохую растворимость и низкую биодоступность, снизить быстрый почечный клиренс, а также повысить селективность клеток [12]. В настоящее время используются многие методы инкапсуляции, такие как липосомы, наночастицы на основе полимеров, гидрогели и сывороточный альбумин [13,14,15,16]. Среди этих методов использование сывороточного альбумина стало одним из наиболее интересных носителей для доставки нерастворимых противораковых препаратов. Человеческий сывороточный альбумин (HSA), эндогенный белок, не токсичен, не иммуногенен и обладает высокой биосовместимостью [17]. Он широко используется в качестве макромолекулярного белка-носителя для доставки лекарств [18]. Таким образом, HSA способен улучшать растворимость липофильных лекарств. Кроме того, наличие функциональных карбоксильных и аминогрупп на поверхности способствует функционализации поверхности наночастиц альбумина [19, 20]. Например, за счет ковалентного связывания поверхность наночастиц альбумина можно декорировать флуоресцентными красителями, молекулами-мишенями и функциональной РНК [21, 22]. Кроме того, он может быть легко функционализирован гидрофильными полимерами, такими как PEG, для продления кровообращения [23].
В этом исследовании HSA используется для инкапсуляции липофильного RV в виде нанопрепарата, который функционализирован на поверхности молекулой, направленной на опухоль, аргинин-глицин-аспартат (RGD) через «мостик» PEG (HRP-RGD NP). Приготовленные НЧ HRP – RGD демонстрируют высокую биосовместимость in vitro и in vivo, а также пролонгированное кровообращение. Поглощение клетками и биораспределение опухолей in vivo также оценивали для подтверждения его целевого потенциала в клетках PANC-1. Более того, целенаправленная противораковая эффективность НЧ HRP – RGD была исследована in vitro и in vivo. Эти результаты показывают, что НЧ HRP – RGD могут быть универсальной наноплатформой для потенциальных противоопухолевых терапевтических агентов для целевого применения химиотерапии.
Методы
Материалы
Сывороточный альбумин человека (HSA, лиофилизированный порошок, ≥96%), ресвератрол (RV, ≥99%), 1-этил-3- (3-диметиламинопропил) карбодиимид (EDC), изотиоцианат флуоресцеина (FITC), Arg – Gly – Asp (RGD, ≥97%), 3- (2-пиридилдитио) пропионовая кислота N -гидроксисукцинимидный эфир (SPDP), краситель Hoechst 33258 и 4 ', 6-диамидино-2-фенилиндол (DAPI) были получены от Sigma Aldrich (Сент-Луис, Миссури, США). NH 2 –ПЭГ 2000 –COOH был куплен у Seebio Biotech Inc. (Шанхай, Китай). N -Сукцинимидил S -ацетилтиоацетат (SATA) был приобретен у Pierce Biotech Inc. (Рокфорд, Иллинойс, США). ДМСО, раствор трипсина-ЭДТА, фосфатный буфер (PBS), фетальная бычья сыворотка (FBS), раствор пенициллина-стрептомицина и среды DMEM были приобретены у Sigma.
Синтез наночастиц HSA – RV
Наночастицы HSA – RV были синтезированы простым методом десольватации [24]. Более подробно, 6 мг RV растворяли в ДМСО до 1 мг / мл и смешивали с 10 мг HSA в 1 мл воды при слабом перемешивании с образованием затвердевших коацерватов после перемешивания в течение 6 часов при комнатной температуре, а затем обрабатывали перекрестным способом. -сшивание 0,5% глутаровым альдегидом (100 мкл). После этого органические растворители удаляли диализом в воде в течение 1 дня, в результате чего получали наночастицы HSA – RV. Пустые наночастицы HSA получали, как указано выше, за исключением того, что ДМСО без RV смешивали с раствором HSA в течение 6 часов.
Синтез и характеристика НЧ HRP – RGD
Наночастицы HSA-RV были конъюгированы с HS-PEG-RGD с помощью традиционного кросслинкера SPDP, как описано в литературе [25]. Вкратце, 20 мг NH 2 –ПЭГ 2000 –COOH обрабатывали 2 мг SATA в течение 3 ч и очищали путем обессоливания. Полученный SATA-PEG добавляли к 10 мг пептида RGD и 8 мг EDC в течение 3 часов. Затем PEG-RGD, защищенный SATA, подвергали взаимодействию с 1 мл гидроксиламина в фосфате натрия в течение 3 часов. После очистки путем обессоливания ему вводили HS – PEG – RGD. Затем полученный HS-PEG-RGD конъюгировали с наночастицами HSA-RV через дисульфидные связи. Вкратце, аминогруппы наночастиц HSA-RV сначала были активированы SPDP, а затем повторно суспендированы в 10 мл PBS и прореагировали с избытком HS-PEG-RGD или HS-PEG в течение 24 часов. Полученный раствор повторно промывали PBS и фильтровали через фильтр Millipore (100 кДа) для удаления любых оставшихся PEG-RGD и других органических растворителей, в результате чего получали НЧ HRP-RGD. Морфологию и размер наночастиц определяли с помощью сканирующей электронной микроскопии (SEM, Philips XL-30 FEG, Эйндховен, Нидерланды) и системы Zetasizer Nano ZS (Malvern Instruments, Малверн, Великобритания) соответственно. Спектры поглощения регистрировали на спектрофотометре UV-Vis (UV1800, Shimadzu, Япония). Спектры флуоресценции регистрировали на флуоресцентном спектрометре (F-4500, Hitachi, Япония).
Загрузка и выдача лекарств
Шесть миллиграммов RV растворяли в ДМСО до 1 мг / мл и смешивали с 10 мг HSA в 1 мл воды при слабом перемешивании с образованием затвердевших коацерватов после перемешивания в течение 6 часов при комнатной температуре, а затем обрабатывали поперечным сшиванием. с 0,5% глутаровым альдегидом (100 мкл). После этого органические растворители и свободный RV удаляли диализом в воде в течение 1 дня. Диализат использовали для количественного определения свободного RV с помощью спектрометра UV-Vis при 306 нм в соответствии с калибровочной кривой. Количество препарата в HRP – RGD NP было общим добавленным RV за вычетом количества свободного RV.
Высвобождение RV из HRP – RGD NPs было обнаружено с помощью метода динамического диализа (диализный мешок с пороговой молекулярной массой 8–12 кДа) при pH 5,0, 7,4 и 9,0 PBS, соответственно, при 37 ° C. Концентрацию лекарственного средства рассчитывали с использованием стандартной калибровочной кривой. Эффективность инкапсуляции = Вт 1 / Вт 2 × 100%, где W 1 представляет собой вес RV в HRP – RGD NP, а W 2 - добавленный вес жилого автофургона. Совокупный выпуск = Вт а / Вт b × 100%, где W а представляет собой количество выпущенных RV, а W b - общее количество RV, присутствующее в HRP – RGD NP.
Анализ гемолиза in vitro
Анализ гемолиза in vitro проводили, как описано в предыдущей работе [26]. Более подробно, 0,2 мл эритроцитов (эритроцитов в PBS) смешивали с 0,8 мл HRP – RGD NP (в PBS) в заранее определенных концентрациях (10, 50, 100 и 200 мкг / мл). Эритроциты, инкубированные с деионизированной водой или PBS, были установлены как положительный или отрицательный контроль соответственно. После инкубирования при 37 ° C в течение 3 часов вышеуказанный набор суспензий центрифугировали при 10 000 об / мин в течение 1 мин и оптическую плотность супернатантов при 541 нм контролировали с помощью спектрометра UV-Vis. Гемолитический коэффициент =(OD t - OD nc ) / (OD pc - OD nc ) × 100%, где OD t , OD pc , и OD nc - абсорбция супернатанта исследуемого образца, положительного и отрицательного контролей соответственно.
Культура клеток
Клетки опухоли поджелудочной железы человека PANC-1 были приобретены из банка клеток коллекции типовых культур Китайской академии наук (Шанхай, Китай) и культивированы в среде DMEM с добавлением 10% FBS и 1% пенициллина-стрептомицина в увлажненном инкубаторе (5%). CO 2 ) при 37 ° С.
Использование сотовой связи
Для клеточного поглощения, FITC был использован для мечения НЧ HRP – RGD. Клетки PANC-1 прилипали к предметным стеклам в 6-луночных планшетах и инкубировали с НЧ HRP, НЧ HRP – RGD + блокирование свободного RGD и НЧ HRP – RGD при той же концентрации меченого FITC в течение 5 ч соответственно. Затем клетки трижды промывали PBS и фиксировали 0,2 мл глутарового альдегида с последующим окрашиванием DAPI в течение 10 мин. Флуоресцентные изображения клеток получали с помощью конфокального лазерного сканирующего микроскопа (Leica TCS SP8 CARS, Вецлар, Германия).
Кроме того, отношения поглощения НЧ HRP, НЧ HRP – RGD + блокирование свободного RGD и НЧ HRP – RGD при одинаковой концентрации меченого FITC клетками PNAC-1 были проанализированы с помощью проточной цитометрии (FCM, FACSCalibur, FACSCanto II). путем измерения флуоресценции FITC. Для каждого анализа FCM регистрировали десять тысяч клеток. Флуоресценцию FITC возбуждали лазером с длиной волны 488 нм.
Цитотоксичность in vitro
Цитотоксичность НЧ HP – RGD, носителя RV, определяли с использованием стандартного набора для подсчета клеток-8 (CCK-8) (Bestbio, Китай). Ячейки PNAC-1 (1 × 10 5 клеток / мл, 0,5 мл) высевали в 96-луночный планшет и культивировали в течение 24 часов. После удаления старых сред свежие среды, содержащие 10, 50, 100 и 200 мкг / мл НЧ HRP – RGD, инкубировали с клетками PNAC-1 в течение 24 часов. PBS использовали для трехкратной мягкой промывки клеток. Затем в каждую лунку добавляли 100 мкл рабочего раствора CCK-8 (10% CCK-8 + 90% DMEM) с последующей инкубацией при 37 ° C в течение 0,5 часа. Величину поглощения при 450 нм определяли с помощью считывающего устройства для микропланшетов (Infinite 200 Pro, Tecan, Австрия). Кроме того, in vitro противораковая эффективность ПЖ (растворенного в ДМСО), НЧ HRP и НЧ HRP – RGD с той же концентрацией ПЖ в отношении клеток PNAC-1 оценивалась с помощью анализа CCK-8, упомянутого выше. Все эксперименты проводились в 4 раза. Кроме того, морфологическое исследование апоптоза было обнаружено окрашиванием Hoechst 33258. Флуоресценцию Hoechst 33258 в клетках наблюдали и регистрировали с помощью лазерного сканирующего конфокального микроскопа.
Модель животного
Голых мышей Balb / c в возрасте 4–5 недель покупали в Shanghai Slac Laboratory Animal Co. Ltd. (Шанхай, Китай). Все эксперименты на животных проводились в соответствии с Руководством по уходу и использованию лабораторных животных, одобренным Управлением лабораторных животных Тайшаньского медицинского университета. Модели подкожного ксенотрансплантата опухоли были созданы в правой области спины мышей путем инъекции 1 × 10 6 Клеток PNAC-1 на мышь, и когда опухоли имели объем около 80 мм 3 , эти мыши были случайным образом разделены на разные группы ( n =5) для дальнейшего использования.
Кровообращение и биораспределение опухоли
Нормальным мышам внутривенно вводили RV, НЧ HRP и НЧ HRP – RGD. После этого в разное время были взяты образцы крови из глазничного сплетения. Каждый образец крови растворяли в 900 мкл буфера для лизиса. Концентрацию RV, НЧ HRP и НЧ HRP – RGD в крови определяли по спектрам поглощения RV каждого солюбилизированного образца крови с помощью спектрометра UV-Vis. Концентрация образца определяется как процент введенной дозы на грамм ткани (ID% / г).
Биораспределение в опухоли было выполнено на мышах с опухолью. Ткани опухоли взвешивали и переваривали раствором царской водки в течение ночи через 24 часа после внутривенной инъекции RV, HRP NP и HRP – RGD NP соответственно. Концентрацию RV, HRP NP и HRP-RGD NP в опухоли определяли по спектрам поглощения RV каждой солюбилизированной опухолевой ткани с помощью спектрометра UV-Vis. Концентрация образца определяется как процент введенной дозы на грамм ткани (ID% / г).
Противораковая эффективность in vivo
Мышам разных групп внутривенно вводили физиологический раствор, ПЖ, НЧ HRP и НЧ HRP – RGD (доза, равная RV, n =5,10 мг / кг). Во время лечения размер опухоли и массу тела мышей с опухолью контролировали каждые 3 дня. Объем опухоли рассчитывали по формуле: V =(Длина × ширина 2 ) / 2. Относительный объем опухоли = V / V 0 , где V 0 был объем опухоли до первоначального лечения.
Гистологическое исследование
Здоровым голым мышам Balb / c из разных групп внутривенно вводили физиологический раствор (контроль), ПЖ, НЧ HRP и НЧ HRP – RGD (доза, равная RV, n =5, 5 мг / кг). Через 35 дней мышей умерщвляли и собирали сердце, печень, селезенку, легкие и почки. Полученные основные органы фиксировали 4% параформальдегидом в течение ночи. После этого эти органы обезвоживали в 25% сахарозе, разрезали на срезы 5 мкм и окрашивали гематоксилином и эозином (H&E). Окрашенные срезы получали под инвертированным фазово-контрастным микроскопом.
Результаты и обсуждение
Синтез и характеристика НЧ HRP – RGD
Согласно простому методу десольватации [24], RV был инкапсулирован с помощью HSA, в результате чего были получены наночастицы HSA – RV. После этого поверхность наночастиц HSA – RV была ковалентно функционализирована с помощью HS – PEG – RGD с помощью традиционного сшивающего агента SPDP [25], образуя нанокомпозитные НЧ HRP – RGD. НЧ HRP и НЧ HRP – RGD показали одномодальное и узкое распределение частиц по размерам (рис. 1а, б). После конъюгирования RGD на поверхности НЧ HRP средний размер наночастиц увеличился со 113 ± 3,1 нм до 120 ± 2,6 нм. Кроме того, НЧ HRP и НЧ HRP – RGD имели гомодисперсную сферическую морфологию (рис. 1c, d).
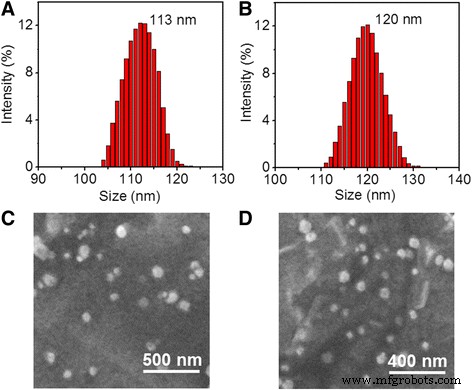
Гранулометрический состав НЧ HRP ( a ) и НЧ HRP – RGD ( b ). СЭМ-изображения НЧ HRP ( c ) и НЧ HRP – RGD ( d )
Спектры УФ-видимой и флуоресценции были сняты для подтверждения присутствия РВ в НЧ HRP-RGD. Как показано на рис. 2а, НЧ HRP и НЧ HRP – RGD имели пики поглощения для RV при 304 нм, что указывает на присутствие RV в обеих наночастицах. Кроме того, НЧ HRP и НЧ HRP-RGD показали сигналы флуоресценции RV на длине волны возбуждения 325 нм, что согласуется со спектрами флуоресценции RV (Рис. 2b). Эти результаты демонстрируют, что RV сохраняет свои оптические свойства после конъюгации с НЧ HRP и НЧ HRP – RGD.
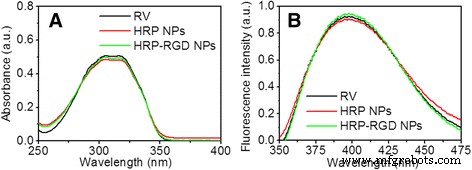
а Спектры поглощения свободных RV, НЧ HRP и НЧ HRP – RGD. б Спектры флуоресценции свободных RV, НЧ HRP и НЧ HRP – RGD
Загрузка и выпуск автофургона
На рис. 3а показана кривая изменения эффективности инкапсуляции ПЖ в НЧ HRP – RGD при увеличении концентрации ПЖ. Максимальный RV EE полученных НЧ HRP – RGD составил 62,5 ± 4,21%. Кроме того, как видно на рис. 3b, НЧ HRP-RGD показали самую высокую скорость высвобождения RV 58,4,2 ± 2,8% через 60 ч при 37 ° C и pH 5,0 по сравнению со скоростью высвобождения, полученной при pH 6,5, pH 7,4, и pH 9,0 при 37 ° C. Сообщалось, что в норме pH крови составляет 7,4, тогда как ткань опухоли имеет слабокислый характер [27]. Это оказалось полезным признаком использования НЧ HRP – RGD в терапии опухолей.
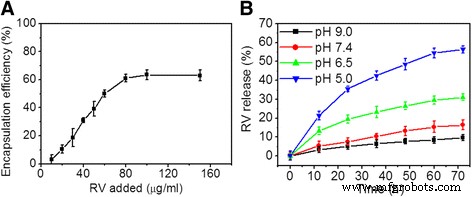
а Эффективность инкапсуляции RV как функция добавленных концентраций RV. б Профиль высвобождения RV из HRP – RGD НЧ in vitro при pH 5,0, 6,5, 7,4 и 9,0 при 37 ° C
Биосовместимость in vitro
На рис. 4a, b показаны изображения RV, растворенных в ДМСО, и НЧ HRP – RGD в PBS при 4 ° C через 7 дней. Первый показывает твердое вещество, подобное игольчатому кристаллу, тогда как последний имеет много микро- и гомодисперсных сферических частиц, что указывает на улучшенную стабильность RV после инкапсуляции наночастицами HSA. Кроме того, средний размер НЧ HRP-RGD в воде, DMEM, PBS и FBS практически не изменялся в течение 4 недель (рис. 4c), демонстрируя высокую коллоидную стабильность НЧ HRP-RGD, которая, скорее всего, приписывалась PEG и Инкапсуляция HSA.
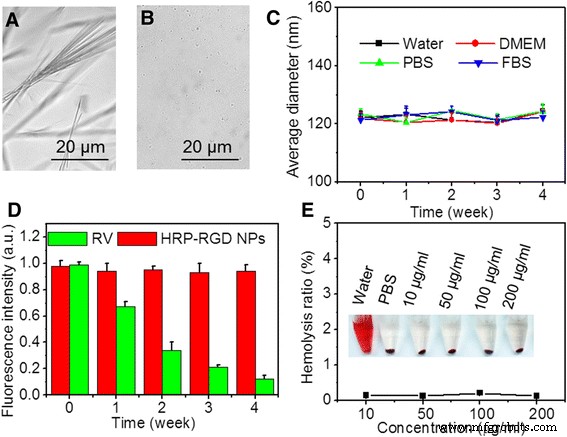
Изображение a , полученное с микроскопа свободный RV (растворенный в DMSO) в PBS и b НЧ HRP – RGD в PBS через 7 дней. c Тест коллоидной стабильности НЧ HRP – RGD в различных средах (вода, DMEM, PBS и FBS). г Стабильность флуоресценции RV в НЧ HRP – RGD через 4 недели. е Коэффициент гемолиза эритроцитов после 1 ч инкубации с НЧ HRP – RGD в различных концентрациях. вставка показывает фотографию эритроцитов, подвергнутых воздействию дистиллированной воды, PBS и НЧ HRP – RGD с различными концентрациями с последующим центрифугированием
На рис. 4d показана флуоресцентная стабильность НЧ RV и HRP – RGD в водном растворе при 4 ° C. После 4 недель хранения интенсивность флуоресценции ПЖ НЧ HRP – RGD оставалась более 96,8% от исходной интенсивности; однако флуоресценция RV быстро падала до 12,1% от начальной интенсивности, вероятно, из-за преципитации RV из раствора [10], что дополнительно указывает на стабильность HRP – RGD NP по сравнению со свободным RV. Более того, как показано на рис. 4e, не было обнаружено значительного явления гемолиза для эритроцитов, обработанных HRP-RGD NPs, ниже 200 мкг / мл, как и в группе, получавшей PBS отрицательного контроля, что свидетельствует о превосходной гемосовместимости HRP-RGD NPs. . Эти результаты позволяют предположить, что инкапсуляция HSA улучшила стабильность и биосовместимость RV in vitro, что полезно для биомедицинских применений.
Использование сотовой связи
НЧ HRP и НЧ HRP – RGD были маркированы FITC. Как показано на фиг. 5а, ядра проявляли синюю флуоресценцию, которые были окрашены DAPI. Интенсивная зеленая флуоресценция (сигнал FITC) наблюдалась в перинуклеарной области клеток PANC-1, обработанных НЧ HRP-RGD, показывая, что достаточное количество НЧ HRP-RGD попало в цитоплазму. Напротив, очень слабая зеленая флуоресценция проявлялась в клетках PANC-1, обработанных НЧ HRP. Более того, клетки PANC-1, предварительно обработанные свободным RGD, также проявляли мягкую зеленую флуоресценцию, вероятно, связанную с блокировкой рецептора RGD на поверхности PANC-1 свободным RGD. Коэффициент клеточного поглощения наночастиц был обнаружен с помощью FCM, который составлял 16,2 ± 4,9%, 7,1 ± 5,1% и 58,5 ± 3,5% для НЧ HRP, НЧ HRP-RGD с блокировкой RGD и НЧ HRP-RGD, обработанных PANC- 1 соответственно (рис. 5б). Эти результаты демонстрируют, что целевая молекула RGD может способствовать высокоэффективному захвату HRP – RGD NP клетками PANC-1 [28, 29].
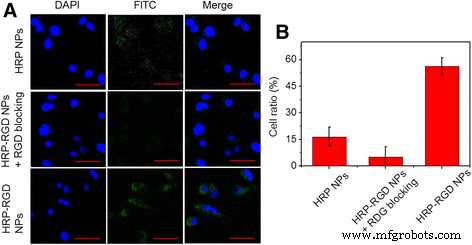
а Конфокальные флуоресцентные изображения клеток PANC-1 после инкубации с НЧ HRP, НЧ HRP – RGD с блокировкой RGD и НЧ HRP – RGD, меченных FITC. Зеленый и синие цвета представляют собой ядра клеток, окрашенные флуоресценцией FITC и DAPI, соответственно. Шкала масштаба =20 мкм. б Количественное поглощение клетками PANC-1 НЧ HRP, НЧ HRP – RGD с блокировкой RGD и НЧ HRP – RGD с помощью проточной цитометрии
Цитотоксичность in vitro
На рис. 6а показана цитотоксичность НЧ HP – RGD в диапазоне концентраций 0–200 мкг / мл по данным анализа CCK-8, в котором жизнеспособность клеток PANC-1 сохранялась выше 90%. Было высказано предположение, что уровни HP – RGD NP носителей RV ниже 200 мкг / мл не обладают значительной цитотоксичностью. Кроме того, также оценивали противораковый эффект НЧ HRP – RGD in vitro. Рисунок 6b показывает, что свободные RV, HRP NP и HRP-RGD NP при концентрациях RV в диапазоне от 0 до 50 мкг / мл вызывали снижение жизнеспособности клеток дозозависимым образом. По сравнению со свободными НЧ RV и HRP, НЧ HRP-RGD могут приводить к наибольшему снижению жизнеспособности клеток при всех тестируемых концентрациях, вероятно, из-за стабильности и эффектов нацеливания RGD НЧ HRP-RGD на клетки PANC-1 [30, 31] . Кроме того, ядра клеток PANC-1, обработанных свободным RV, HRP NP и HRP-RGD NP (все при 30 мкг / мл RV), были окрашены Hoechst 33258 и исследованы под конфокальным флуоресцентным микроскопом. Клетки, обработанные НЧ HRP и HRP-RGD, показали присутствие пикнотических ядер, что согласуется с клетками, обработанными RV (рис. 6c-f), что указывает на то, что типом гибели клеток, скорее всего, является апоптоз [32].
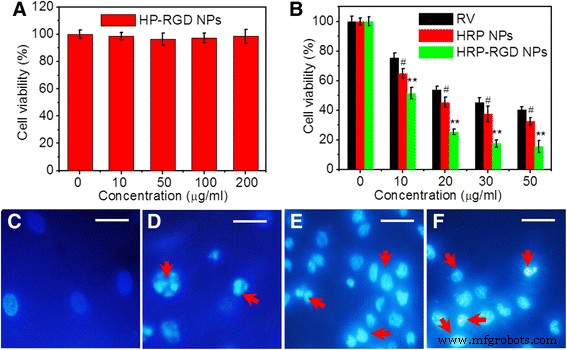
а Жизнеспособность клеток PANC-1 после обработки НЧ HP – RGD в течение 24 часов. б Жизнеспособность клеток PANC-1 после инкубации с различной концентрацией RV, HRP NP и HRP – RGD NP. Ядро клеток PANC-1, обработанных PBS ( c ), RV ( d ), HRP NP ( e ), НЧ HRP – RGD ( f ) окрашены Hoechst 33258 после обработки в течение 24 часов. Изображения были записаны с помощью цифровой камеры. Шкала масштаба =20 мкм. Красные стрелки представляют собой ядра пикнотических клеток
Кровообращение и биораспределение опухоли
На рис. 7а показано время циркуляции крови свободных RV, HRP NP и HRP – RGD NP после внутривенного введения мышам. Видно, что НЧ HRP и НЧ HRP – RGD имеют примерно одинаковое время полужизни ( t 1/2 ) 7,5 ± 0,5 ч и t 1/2 =6,57 ± 0,9 ч соответственно. В то время как свободный ПЖ был быстро удален из системы кровообращения и t 1/2 =1,21 ± 0,09 ч. НЧ HRP – RGD продлевали время циркуляции крови в ПЖ, примерно увеличиваясь в 5,43 раза ( t 1/2 ). Кроме того, через 24 часа после инъекции наночастиц содержание RV в опухолевой ткани в группе, получавшей HRP – RGD NP, было примерно в 3,01 и 8,1 раза выше, чем в группах, получавших HRP NPs и свободный RV. соответственно (рис. 7б). Эти результаты показывают, что инкапсуляция HSA и PEG может продлить время циркуляции, чтобы уменьшить элиминацию RV и продемонстрировать значительную эффективность избирательного накопления в опухолевой ткани [33, 34], вероятно, из-за повышенной проницаемости и удерживания (EPR) и нацеливания RGD эффект [35].
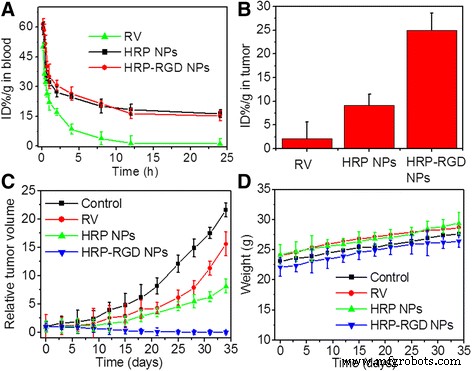
а Кривые кровообращения свободных ПЖ, НЧ HRP и НЧ HRP – RGD у мышей после внутривенной инъекции, определяемые по поглощению ПЖ из разбавленного тканевого лизата. б Содержание ПЖ в опухоли через 24 ч после обработки НЧ ПЖ, HRP и НЧ HRP – RGD. c Относительный объем опухоли мышей-опухоленосителей после внутривенной инъекции физиологического раствора (контроль), ПЖ, НЧ HRP и НЧ HRP – RGD. г Масса тела мышей с опухолью после внутривенной инъекции физиологического раствора (контроль), ПЖ, НЧ HRP и НЧ HRP – RGD
Противораковая эффективность in vivo
На рисунке 7c показана противораковая эффективность свободных RV, HRP NP и HRP – RGD NP при той же концентрации RV после внутривенной хвостовой инъекции. В качестве контроля мышей обрабатывали физиологическим раствором. У мышей, которым вводили НЧ HRP – RGD, наблюдалось значительное подавление роста опухоли и отсутствие рецидива после 35 дней лечения. В то время как в группах, получавших свободный RV, HRP NP, как и в контрольной группе, наблюдался постоянно увеличивающийся рост опухоли. Как и ожидалось, масса тела мышей во всех группах существенно не снизилась в течение 35 дней лечения (фиг. 7d). Более того, системную токсичность in vivo дополнительно оценивали путем окрашивания H&E основных органов (сердца, печени, селезенки, легких и почки) после 35 дней лечения (фиг. 8). Не было обнаружено заметной тканевой токсичности или аномалий на соответствующих изображениях окрашенных H&E тканей всех тестируемых групп, что дополнительно гарантировало безопасность in vivo НЧ HRP – RGD для биомедицинских применений.
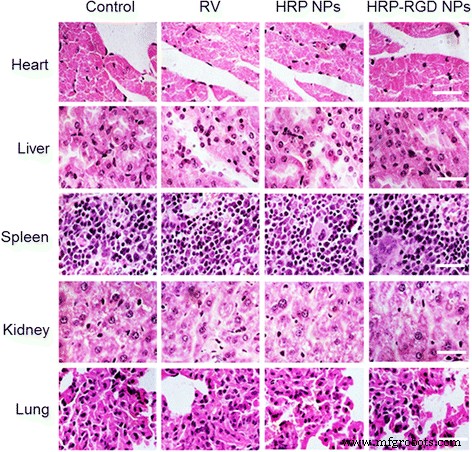
Репрезентативные изображения окрашивания HE сердца, печени, селезенки, почек и легких. Шкала масштаба =100 мкм
Выводы
Таким образом, мы проиллюстрировали, как HRP – RGD NPs могут быть использованы в качестве высокоэффективного терапевтического агента, направленного на опухоль поджелудочной железы. Было продемонстрировано, что НЧ HRP – RGD демонстрируют улучшенную коллоидную стабильность и биосовместимость in vitro по сравнению со свободным RV. RGD как молекула-мишень способствует высокоэффективному захвату клетками HRP – RGD NPs. В присутствии PEG и HSA, HRP-RGD NPs показали значительно увеличенное время циркуляции, которое может преодолеть короткую циркуляцию крови свободного RV. На основании нацеливания RGD, содержание НЧ HRP – RGD в опухолевой ткани было больше, чем содержание свободных НЧ RV и HRP. Более того, исследования in vitro и in vivo показали, что по сравнению со свободными НЧ RV и HRP, НЧ HRP – RGD обладают превосходным противораковым действием, вероятно, вызванным апоптозом. Наконец, НЧ HRP – RGD показали высокую биосовместимость и отсутствие значительной системной токсичности in vivo в течение 35 дней лечения. Эти результаты демонстрируют, что НЧ HRP – RGD могут быть многообещающим средством для химиотерапии опухолей в будущих биомедицинских приложениях.
Сокращения
- CCK-8:
-
Набор для подсчета клеток-8
- FBS:
-
Фетальная бычья сыворотка
- FITC:
-
Флуоресцеина изотиоцианат
- HSA:
-
Сывороточный альбумин человека
- PBS:
-
Фосфатный буфер
- PEG:
-
Полиэтиленгликоль
- RGD:
-
Аргинин-глицин-аспартат
- RV:
-
Ресвератрол
Наноматериалы
- Многофункциональные наночастицы золота для улучшенных диагностических и терапевтических применений:обзор
- Наночастицы для терапии рака:текущий прогресс и проблемы
- Модифицированный гиперразветвленный полиглицерин как диспергатор для контроля размера и стабилизации нано…
- Синтез и эффективность in vitro покрытых полипирролом железо-платиновых наночастиц для фототермической терапии…
- Наносборки 5-аминолевулиновой кислоты и сквалена для фотодетекции и терапии опухолей:исследования in vitro
- Оболочки диатомовых водорослей из кремнезема, адаптированные с использованием наночастиц Au, позволяют прово…
- Простой синтез безлигандных наночастиц иридия и их биосовместимость in vitro
- Наночастицы альбумина, содержащие артесунат и конъюгированные с красителем в ближнем инфракрасном диапазон…
- Украшение нанопузырьков с помощью вставляемого пептида с низким pH (pHLIP) для целевой доставки
- Хорошо выровненные массивы нанотрубок TiO2 с наночастицами Ag для высокоэффективного обнаружения ионов Fe3 +



