Наноканальный синтез сверхвысокой эффективности легирования азотом на мезопористых катализаторах Fe / N / C для реакции восстановления кислорода
Аннотация
Разработка соответствующих методов для эффективного повышения эффективности легирования азотом и плотности активных центров имеет важное значение для повышения активности реакции восстановления кислорода (ORR) неплатиновых электрокатализаторов Fe / N / C-типа. Здесь мы предлагаем простую и эффективную стратегию разработки мезопористого катализатора Fe / N / C для ORR со сверхвысокой площадью поверхности по БЭТ и выдающейся проводимостью через наноканалы пиролиза Fe 2 + в ограниченном молекулярном сите ионы, координированные с 2,4,6-три (2-пиридил) -1,3,5-триазиновыми комплексами, в качестве нового предшественника со стабильным координационным эффектом. Сочетание эффекта ограничения наноканала со стабильным координационным эффектом может синергетически улучшить термическую стабильность и стабилизировать активные центры, обогащенные азотом, а также помочь контролировать потерю активных атомов азота в процессе пиролиза и дополнительно получить высокую плотность активных центров для повышение активности ORR. Свежеприготовленный электрокатализатор Fe / N / C продемонстрировал превосходную каталитическую активность с начальным потенциалом ~ 0,841 В (по сравнению с RHE), близким к катализатору Pt / C, и высокой долговременной стабильностью в щелочном электролите. Кроме того, этот катализатор имеет низкий выход пероксида водорода (<6,5%) и высокое число переноса электрона (3,88–3,94), что указывает на то, что он является ценным заменителем традиционных катализаторов Pt / C. Эта работа открывает новый путь для разработки высокоэффективных электрокатализаторов Fe / N / C и углубляет понимание механизма катализа активного центра и ORR.
Введение
Исследование передовых экологически чистых энергетических устройств (например, топливных элементов и металл-воздушных батарей) в настоящее время является эффективным решением для решения проблемы загрязнения окружающей среды и энергетического кризиса. В этих системах реакция восстановления кислорода (ORR), обладающая характеристиками вялой кинетики и разнообразием путей реакции, является решающим процессом [1, 2]. В настоящее время первоклассными и широко используемыми электрокатализаторами для ORR являются наночастицы платины, закрепленные на различных углеродных материалах, но они обладают некоторыми недостатками (например, высокой стоимостью, редкостью, плохой стабильностью и легкостью отравления), что в значительной степени ограничивает крупномасштабные коммерческие приложения [3]. Таким образом, создание дешевых и высокоэффективных электрокатализаторов ORR на основе неплатиновых или неблагородных металлов является крайне необходимым.
В последние годы электрокатализаторы на основе легированного углерода рассматриваются как один из потенциальных неблагородных электрокатализаторов в качестве замены коммерческих катализаторов на основе Pt с точки зрения таких преимуществ, как низкая стоимость, высокие характеристики, устойчивость к коррозии и обильные ресурсы. [4, 5]. Переходные металлы / угли, легированные азотом (TM / N / C), служащие наиболее важным типом катализаторов ORR на основе легированного углерода, стали популярной областью исследований [4,5,6]. С одной стороны, синтез неплатиновых катализаторов TM / N / C, полученных из фталоцианина, порфирина и их производных, содержащих TM-N x ( x =2, 4, 6 и др.) В качестве многообещающих предшественников [4,5,6,7,8,9,10], но область, вызывающая беспокойство, обычно ограничивается причиной, по которой структура TM-N x является единственной предпосылкой для успешной разработки катализаторов TM / N / C. С другой стороны, некоторые исследователи предположили, что термообработка металл-макроциклических комплексов при высоких температурах может частично или полностью разрушить исходный TM-N x структура, а затем будут регенерированы эффективные структуры активного сайта [11]. Обнаружено, что включение TM-N x координационные структуры в прекурсорах не является необходимым условием, и почти прекурсоры, содержащие источники TM, N и C, могут быть использованы для катализаторов TM / N / C [12]. Этот прорыв способствует рациональной конструкции и контролю характеристик для различных катализаторов TM / N / C, особенно для катализаторов Fe / N / C как наиболее идеального производства для замены коммерческих катализаторов на основе Pt [13,14,15]. Однако из-за гетерогенной структуры катализаторов Fe / N / C идентификация активных центров ORR все еще остается спорной. Существует два мнения относительно структуры активных центров ORR катализатора Fe / N / C:(i) новый Fe-N x активные структуры реформируются из атомов Fe и N после термической обработки тройных прекурсоров при высоких температурах [2, 7, 10, 13, 14]; (ii) углеродные структуры, легированные азотом (NC), полученные из углеродных носителей, модифицированных атомами азота в процессе пиролиза, но атомы Fe рассматриваются как промоторы, способствующие образованию структур NC, и они имеют незначительный каталитический эффект или не имеют его вообще. Процесс ORR [16,17,18]. Хотя роль атомов Fe в катализаторах Fe / N / C четко не объяснена, однозначно, что легирование атомов N вносится в углеродный скелет углеродного носителя для повышения электрокаталитической активности.
Одной из проблем является то, что изготовление катализаторов Fe / N / C путем прямой карбонизации полимеров макромолекул [12, 19, 20], химических комплексов и биологических белков, содержащих Fe-N x структур [15, 21, 22] и других источников железа-азота [17, 23, 24] обычно осуществляется в открытой системе. Кроме того, большинство предшественников, обогащенных азотом, может легко образоваться при накоплении или агломерации в процессе карбонизации, что предотвратит эффективное экспонирование каталитически активных центров ORR, будет способствовать термической потере атомов N и уменьшит плотность активных центров, что приведет к ограничение производительности ORR катализаторов Fe / N / C [25]. Другая проблема заключается в том, что электронная проводимость синтезированных материалов Fe / N / C также определяет их активность ORR. Обычно, когда достигается высокая проводимость катализаторов Fe / N / C, активные атомы азота серьезно теряются в процессе прокаливания. Другими словами, в открытой системе нельзя одновременно учитывать проводимость и количество активных узлов. Контроль потери активных атомов азота в процессе пиролиза по-прежнему является актуальной проблемой повышения электрокаталитической активности. Несколько исследовательских групп предложили несколько эффективных стратегий ограниченной реакции для улучшения этого явления. Вот некоторые типичные образцы:(i) монтмориллонит с ограниченным межслоевым пространством ~ 1 нм используется в качестве 2D-реактора с ограниченным пространством, чтобы избежать упаковки и тепловых потерь активных атомов азота и повысить характеристики проводимости [26] , (i) перенасыщенные хлориды натрия появляются в виде полностью закрытого реактора для контроля потерь азота и увеличения плотности активного центра [27], и (iii) наша группа недавно использовала самоорганизующиеся агрегаты 3D-NaCl в качестве полузамкнутого закрытого реактора для эффективного снижения скорости разложения активных богатых азотом структур, что приводит к увеличению плотности активных центров и усилению активности ORR [25]. Однако эти методы обычно требуют громоздкой предварительной обработки, усложняют технологию или ограничивают устойчивость к чрезмерно высокой температуре.
Здесь мы предлагаем легкую и простую стратегию разработки нового катализатора Fe / N / C через наноканалы пиролиза в молекулярных ситах Fe, координированного с 2,4,6-три (2-пиридил) -1,3,5- триазиновые комплексы (Fe-TPTZ) как новый предшественник со стабильным координационным эффектом. В процессе карбонизации при высоких температурах этот ограниченный метод может уменьшить частичную потерю атомов N, улучшить площадь поверхности по БЭТ и мезопористые характеристики, повысить эффективность легирования азотом и плотность активных центров, а также повысить электронную проводимость, что может эффективно повысить электрокаталитическая активность ORR катализатора Fe / N / C. Кинетическое поведение ORR и механизм катализа Fe / N / C катализатора были дополнительно исследованы. Превосходная активность ORR с начальным потенциалом ~ 0,841 В (по сравнению с RHE), близкая к катализатору Pt / C, и высокая долговременная стабильность могут наблюдаться на катализаторе Fe / N / C, что указывает на то, что он является ценным заменителем традиционного Катализаторы Pt / C в щелочном растворе. Будущее влияние этого исследования дает новую идею или метод для разработки высокоэффективного неблагородного катализатора Fe / N / C путем интеграции стабильного эффекта координации на молекулярном уровне и эффектов, ограниченных наноканалом, и углубляет понимание активного центра и Механизм катализа ORR.
Методы
Синтез мезопористых катализаторов Fe / N / C
Для синтеза предшественника катализатора Fe / N / C использовали 0,2 г молекулярных сит KIT-6 (KIT-MS) (предоставленных Jiangshu Jichang Nano-Technology Co., Ltd.) с площадью поверхности по БЭТ 780 м 2 г -1 диспергируется ультразвуком в 0,2 моль л -1 Раствор HCl (общий объем 20 мл). Затем 0,2 г 2,4,6-три (2-пиридил) -1,3,5-триазина (TPTZ), предоставленного Shanghai Aladdin Biochemical Technology Co., Ltd., и 0,0423 г FeCl 2 · 4H 2 O были последовательно добавлены на основе фиксированного условия: n (Fe 2+ ): n (TPTZ) =1:3 и дополнительно перемешивали в течение 5 часов при 25 ° C, чтобы адекватно гарантировать координационную реакцию между Fe 2+ ионы и TPTZ и эффективно фиксируют образованные комплексы Fe-TPTZ в наноканалы (размер пор 4–10 нм) KIT-MS. После сушки при 80 ° C в сушильном шкафу полученный образец маркируется как прекурсор Fe-TPTZ @ KIT-MS, который далее нагревается при различных температурах (800 ° C, 900 ° C и 950 ° C). в течение 2 ч в трубчатой печи сопротивления с N 2 - расход 0,5 л мин -1 . Полученные образцы были полностью протравлены плавиковой кислотой (40 мас.%) И многократно промыты бидистиллированной водой с получением трех видов мезопористых катализаторов Fe / N / C (обозначенных как m -Fe / N / C-800, м -Fe / N / C-900 и m -Fe / N / C-950 соответственно). Разработанный процесс мезопористых катализаторов Fe / N / C с высокой плотностью активных центров показан на рис. 1. Примечательно, что KIT-MS можно рассматривать как новый реактор с ограниченным наноканалом для эффективного контроля потерь при термическом разложении атомы азота и дальнейшее улучшение плотности активных центров, легированных азотом, в процессе высокотемпературного пиролиза. Кроме того, основная причина использования комплекса Fe-TPTZ в качестве ценного исходного материала для производства электрокатализаторов Fe / N / C с мезопористой структурой с высокой плотностью активных центров связана с сильной координационной ролью между Fe 2+ ионы и атомы азота в лиганде TPTZ, которые могут термически стабилизировать структуру комплекса Fe-TPTZ и способствовать дисперсности Fe-содержащих частиц в конечных катализаторах Fe / N / C. Между тем, он может эффективно снизить скорость термического разложения атомов азота в процессе пиролиза и повысить плотность каталитически активных центров, легированных азотом, для оптимизации характеристик ORR. В качестве контроля мы подготовили m -Ni / N / C-900 и м -Cu / N / C-900 с использованием того же метода синтеза при 900 ° C и с использованием KIT-MS в качестве нового реактора с ограниченным наноканалом. Мы также синтезировали катализаторы Fe / N / C-900 и N / C-900 при той же температуре термообработки, полученные из комплекса Fe-TPTZ и лиганда TPTZ, соответственно, без использования KIT-MS в качестве реактора с ограниченным наноканалом. .
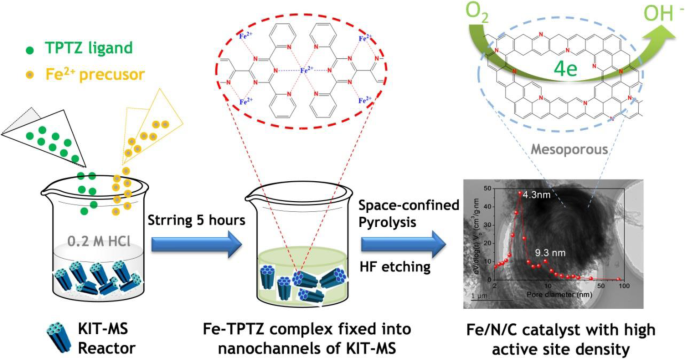
Схема синтеза мезопористых катализаторов Fe / N / C
Характеристика мезопористых катализаторов Fe / N / C
Данные термогравиметрического анализа были получены на дифференциальном термическом анализаторе Shimadzu DTG-60H в атмосфере азота при скорости нагрева 10 ° C мин -1 . Данные рентгеновской фотоэлектронной спектроскопии (XPS) собирали на спектрометре Kratos XSAM800. Изображения высокого разрешения с помощью сканирующей и просвечивающей электронной микроскопии были получены на приборах Hitachi UHR S4800 и FEI Tecnai-G2 F30 соответственно. Изотермы адсорбции / десорбции азота тестировали на анализаторе Micromeritics ASAP 2010 при 77 К. Данные рентгеновской дифракции (XRD) получали на рентгеновском дифрактометре Shimadzu XRD-6000 (Cu Ka 1 излучение, λ =1,54178 Ǻ) при скорости сканирования 4 ° мин -1 . Рамановская система Horiba HR800 использовалась для измерения рамановской спектроскопии с длиной волны возбуждения 532 нм.
Электрохимические тесты
Все электрохимические данные были собраны на бипотенциостате CHI760E (Shanghai Chenhua Instruments Co. Ltd., Китай) с трехэлектродной системой, которая состоит из вращающегося кольца (Pt) -диска (стеклоуглерод, Φ =5 мм) рабочий электрод (RRDE, American Pine Instrument Co., Ltd.), насыщенный каломельный электрод сравнения (SCE) и противоэлектрод из Pt-фольги (1 см 2 ). Приготовление RRDE с покрытием из катализатора относится к предыдущим сообщениям [21, 25]. Обычно 10 мкл 10 мг / мл -1 Дисперсию катализатора наносили по каплям на RRDE и сушили естественным путем. Массовая загрузка катализатора была ограничена примерно 600 мкг / см -2 . . Все электродные потенциалы относительно SCE в щелочном электролите были преобразованы в потенциалы относительно обратимого водородного электрода (RHE) на основе уравнения Нернста. Другими словами, преобразование потенциала следует этому уравнению:E (по сравнению с RHE) / V =E (по сравнению с SCE) / V + 1,0 В. Перед проведением электрохимического испытания активация RRDE, покрытого катализатором, проводилась с помощью испытание циклической вольтамперометрии от 1,2 до 0,2 В относительно RHE в 0,1 моль л -1 Раствор КОН, насыщенный азотом, 20 циклов. Скорость сканирования 5 мВ с -1 а электролит 0,1 моль л -1 КОН во всех тестах вольтамперометрии.
Результаты и обсуждение
Термогравиметрический анализ (ТГА) трех прекурсоров (Fe-TPTZ @ KIT-MS, Fe-TPTZ и TPTZ) впервые показан на рис. 2а. Видно, что термическое разложение лиганда TPTZ происходит быстро после того, как температура превышает 300 ° C, и может быть сохранено только ~ 9,0% остаточной массы. Однако остаточная масса составляет ~ 40,3% на кривой ТГА комплекса Fe-TPTZ, что свидетельствует об образовании относительно стабильного координационного взаимодействия Fe 2+ ионы и атомы азота, такие как атомы азота пиридиновой группы на краю или атомы азота ароматического кольца в лиганде TPTZ [28]. Этот эффект комплексообразования на молекулярном уровне может в основном улучшить термическую стабильность комплекса Fe-TPTZ, а также способствовать образованию мостиковых и сшитых молекул TPTZ. Поведение Fe-TPTZ при разложении может быть дополнительно замедлено благодаря использованию ограниченного пространства роли наноканалов KIT-MS в качестве нового нанореактора, что приводит к наибольшей остаточной массе (47,4%) Fe-TPTZ @ KIT- РС. Эта роль может быть в пользу увеличения эффективности легирования азотом и плотности активных центров во время высокотемпературного пиролиза, что способствует оптимизации характеристик ORR мезопористых катализаторов Fe / N / C. Для дальнейшего изучения того, было ли полностью сформировано стабильное координационное взаимодействие, мы сначала охарактеризовали TPTZ, Fe-TPTZ и Fe-TPTZ @ KIT-MS с помощью XPS-спектров N1s высокого разрешения (рис. 2b). Очевидно, энергия связи (B.E.) пиридинового азота положительно сдвинулась с 398,8 эВ для лиганда TPTZ до 399,1 эВ для комплекса Fe-TPTZ или предшественника Fe-TPTZ @ KIT-MS. Это является прямым доказательством уменьшения электронной плотности вокруг атомов пиридинового N после Fe 2+ вводятся ионы, поскольку положительный сдвиг в B.E. можно отнести к взаимодействию комплексообразования, которое произошло между Fe 2+ ионы и пиридиновые атомы N на краю молекулы TPTZ, в которых 3d-незанятые орбитали Fe 2+ ионы могут быть эффективно заполнены неподеленной парой электронов атомов пиридинового азота. Образование комплекса Fe-TPTZ может дополнительно побудить большее количество атомов пиридинового азота собраться вокруг атомов Fe, что может быть полезно для производства большего количества Fe-N x структуры активных центров, приводящие к усилению электрокаталитической активности ORR исходных катализаторов Fe / N / C с мезопористой структурой.
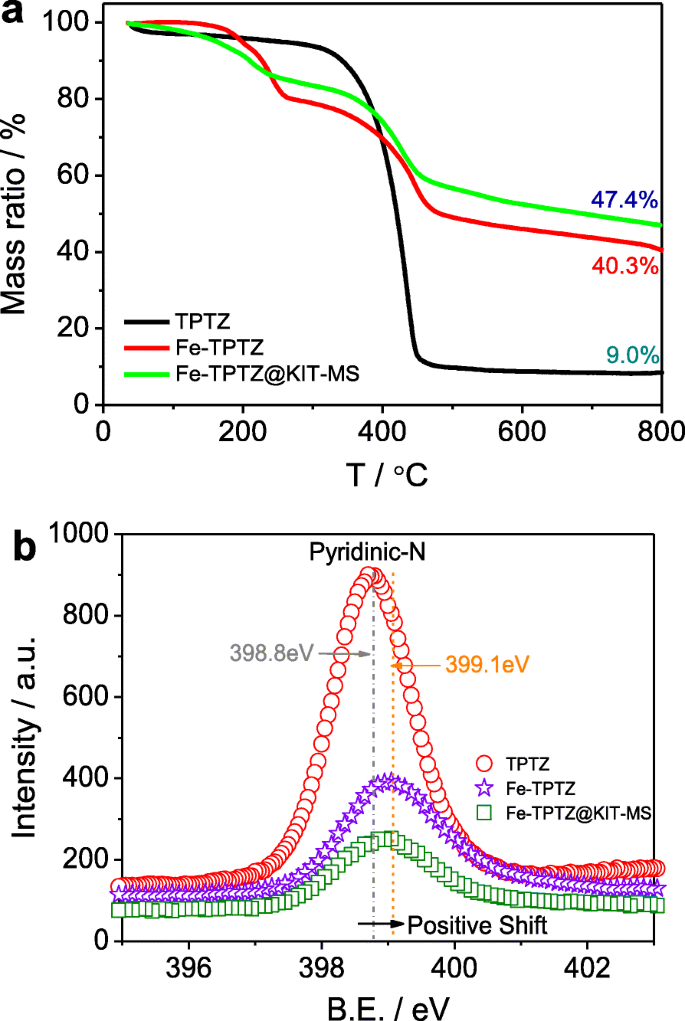
а Кривые ТГА и b высокое разрешение N1 s XPS-спектры прекурсоров TPTZ, Fe-TPTZ и Fe-TPTZ @ KIT-MS
Основываясь на том, что характеристика проводимости электрокатализаторов типа Fe / N / C поддерживает тесную связь с их каталитическими характеристиками ORR, мы измерили электронную проводимость m -Fe / N / C-800, м -Fe / N / C-900 и m -Fe / N / C-950 методом спектроскопии электрохимического импеданса (EIS). Данные EIS были получены в смешанном растворе, состоящем из 0,1 М KCl в качестве электролита и 1 мМ [Fe (CN) 6 ] 3- / [Fe (CN) 6 ] 4- как датчик окислительно-восстановительного потенциала. Результаты Боде показаны на рис. 3а, а графики Найквиста указаны на вставке к рис. 3а. Графики Найквиста аппроксимируются эквивалентной схемой (см. Дополнительный файл 1:Рисунок S1) с пятью компонентами R s , C dl , R p , R int , и C ϕ , где R s представляет собой сопротивление электролита между электродом сравнения и рабочим электродом. C dl представляет собой емкость двойного слоя на границе раздела твердое тело электрода / электролит, C ϕ релаксация заряда, связанная с образованием поверхностных промежуточных продуктов, R p представляет сопротивление переносу заряда во время ORR, а R int представляет собой легкость образования промежуточных продуктов. Сумма R p и R int связано со скоростью ORR. Соответствующие результаты предлагаются в Дополнительном файле 1:Таблица S1. Можно найти, что сумма R p и R int составляет всего 2232,2 Ом для м -Fe / N / C-900, но составляет около 2475,5 Ом на м -Fe / N / C-800 и до 4418,6 Ом на м -Fe / N / C-950 соответственно. Меньшая сумма предполагает относительно более высокую скорость ORR, что означает, что соответствующий катализатор ( m -Fe / N / C-900) показал лучшую электрокаталитическую активность ORR.
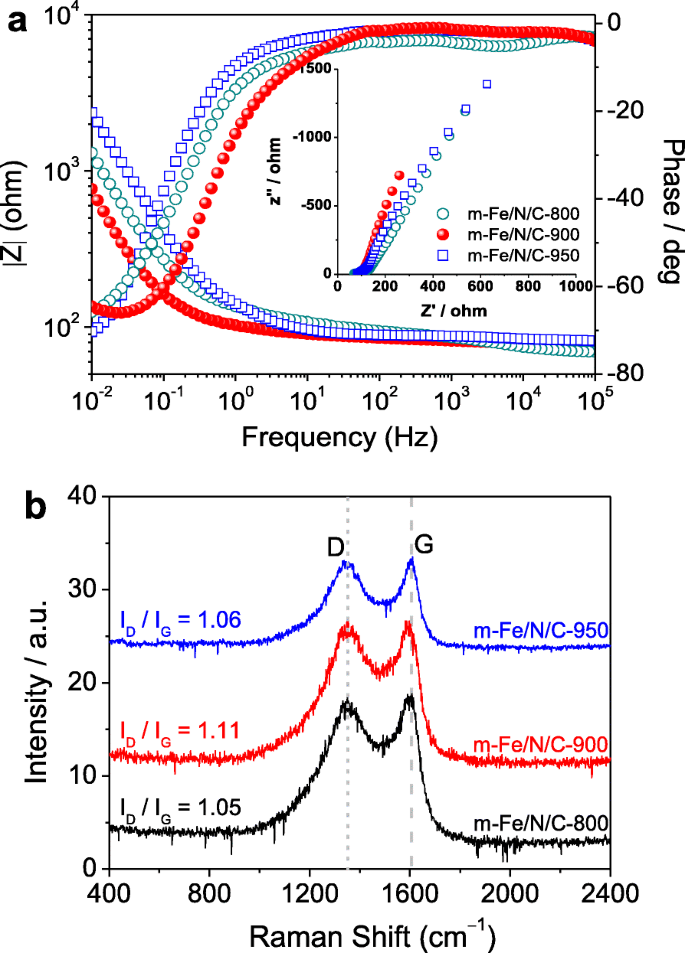
а График Боде EIS для m-Fe / N / C-800, m-Fe / N / C-900 и m-Fe / N / C-950; на вставке - соответствующий график Найквиста. б Рамановские спектры m-Fe / N / C-800, m-Fe / N / C-900 и m-Fe / N / C-950
Рамановские спектры м -Fe / N / C-800, м -Fe / N / C-900 и m -Fe / N / C-950 (см. Рис. 3b) были измерены, а затем были подогнаны к двум пикам Лоренца. Пик с центром ~ 1350 см -1 соответствует индуцированной неупорядоченной структурой D-полосе, которая обычно возникает из-за появления различных плоских дефектов, легированных гетероатомами [18]. Пик с центром ~ 1600 см -1 представляет всю G-полосу, индуцированную графитовой структурой, с плоскостью E 2 г режим вибрации [25]. Их соотношение интенсивности ( I D / Я G ) в значительной степени использовался для различения степеней беспорядка и графитизации. Установлено, что I D / Я G значение на м -Fe / N / C-900 составляет около 1,11, что явно выше, чем на m -Fe / N / C-800 ( I D / Я G =1,05) или м -Fe / N / C-950 ( I D / Я G =1,06). Это означает, что в м может существовать больше азотсодержащих дефектных структур и более высокое содержание легирования атомов азота. -Fe / N / C-900, что хорошо согласуется с результатами анализа XPS. В этом исследовании мы непосредственно закрепили комплексы Fe-TPTZ в наноканалах молекулярных сит, поскольку новый реактор наноконфайнмента может значительно защитить их от пирогенного разложения. Кроме того, сильный эффект координации на молекулярном уровне между Fe 2+ ионы и атомы азота в лиганде TPTZ могут также в определенной степени стабилизировать предшественник Fe-TPTZ и дополнительно способствовать общему содержанию N и эффективности легирования N во время процесса пиролиза. Некоторые ранее опубликованные результаты предполагают, что содержание легирования N-атомов может положительно влиять на электрическую проводимость катализаторов с легированным углеродом [22, 26], адекватно подтверждая оптимальную характеристику проводимости и наивысшую эффективность легирования N для m -Fe / N / C-900 электрокатализатор подготовлен в данной работе.
Анализ рентгеновской фотоэлектронной спектроскопии (XPS) был применен для изучения электронной структуры и химического состава на поверхности m -Fe / N / C-800, м -Fe / N / C-900 и m -Fe / N / C-950. Согласно обзорным XPS-спектрам (рис. 4 и дополнительный файл 1:рис. S2), мы обнаруживаем, что все катализаторы типа Fe / N / C в значительной степени содержат элементы C, N, O и Fe, что доказывает, что Fe и N атомы были успешно легированы в углеродную структуру. Общее содержание Fe, C и N из анализа поверхности XPS и все отношения N / C в мезопористых электрокатализаторах ORR Fe / N / C-типа в исходном состоянии приведены в таблице 1. Показано, что соотношение N / C в м -Fe / N / C-900 до 10,3, что явно больше, чем в m -Fe / N / C-800 (~ 10,0) или м -Fe / N / C-950 (~ 4,4), что дополнительно указывает на наивысшую эффективность легирования азотом и общее содержание азота в м -Fe / N / C-900. C1 s XPS-анализ м -Fe / N / C-900 (рис. 4b) также одобряет легирование атомов азота благодаря появлению характерного пика, соответствующего sp 2 Связь C =N при энергии связи (Б.Э.) ~ 286,5 эВ. Кроме того, сигнал Fe-элемента в обзорных XPS-спектрах электрокатализаторов Fe / N / C-типа в исходном состоянии относительно слаб, поскольку содержание Fe очень низкое после выщелачивания в кислотном растворе. Чтобы изучить электронное состояние атомов Fe, мы проанализировали Fe 2 p Спектр XPS м -Fe / N / C-900 на рис. 2b, который был подогнан к четырем пикам с помощью B.E. 710,3, 712,9, 716,8 и 725,3 эВ соответственно. Пик, расположенный при ~ 710,3 эВ, может быть отнесен к характеристическому пику связи Fe – N, что свидетельствует о наличии Fe 2+ состояние в м -Fe / N / C-900 [29, 30]. Бытие. расположенная примерно при 712,9 эВ и 725,3 эВ, соответствует Fe 3+ 2 п 3/2 и Fe 3+ 2 п 1/2 соответственно (рис. 4в), что позволяет предположить, что атомы Fe из комплекса Fe-TPTZ могут быть частично окислены; однако пик, расположенный при 716,8 эВ, может представлять собой сателлитный пик связи Fe – N. Чтобы еще больше убедиться в химическом состоянии оксидов Fe, мы проанализировали O1 s спектр м -Fe / N / C-900 (рис. 4d). Он разделен на три вершины с Б.Е. 531.0, 532.3 и 533.2 эВ, что соответствует C – O – C, C =O и Fe – O по отдельности [31]. Приведенные выше результаты могут указывать на то, что существующее состояние атомов Fe в основном состоит из связей Fe – N и Fe – O в m -Электрокатализатор Fe / N / C-900.
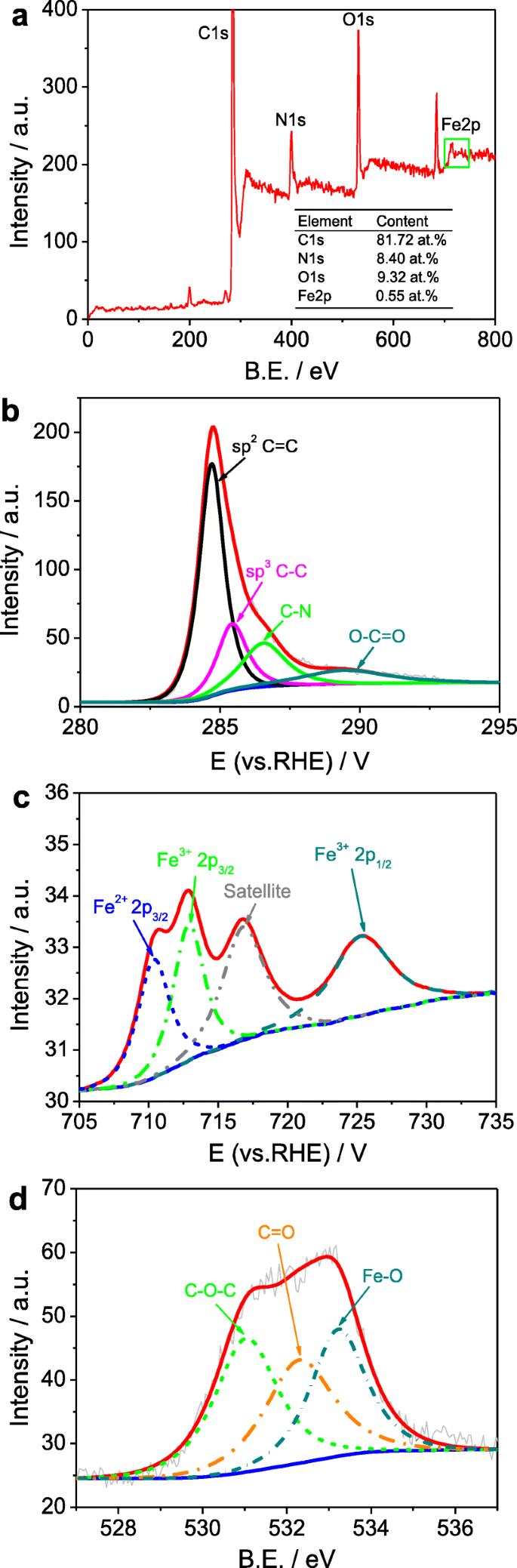
Обзор ( а ), Fe 2 p ( б ), O 1 с ( c ) и C 1 s ( д ) XPS-спектры м -Fe / N / C-900
Оборудованный N1 s XPS-спектры м -Fe / N / C-800 и m -Fe / N / C-900 (см. Рис. 5a, b) отображают четыре пика с B.E. 398,3, 399,5, 401,1 и 406,1 эВ, которые по отдельности можно отнести к пиридиновому N, Fe – N, графитному N и окисленному N (–NO 2 ) [10, 16, 25, 26, 32, 33]. Однако подогнанный N1 s Спектр XPS м -Fe / N / C-950 (рис. 5c) показал только три пика с B.E. 399,2, 401,4 и 406,4 эВ, что соответствует Fe – N, графитному N и окисленному N (–NO 2 ), соответственно. Отмечено, что плотность электронного облака атомов азота смещена из-за более сильной электроотрицательности атомов кислорода, в результате чего пик окисления появляется на стадии высоких энергий. Относительное соотношение графитовых групп N доминирует в общем содержании азота, но относительное соотношение неактивных окисленных N (–NO 2 ) увеличивается с 17,8 до 38,7 ат.% с увеличением температуры пиролиза, как показано на рис. 5d. Кроме того, более высокая температура пиролиза приведет к исчезновению пиридиновой группы N в m -Fe / N / C-950. Приведенные выше результаты показывают, что группа Fe – N может быть образована в катализаторах типа Fe / N / C в исходном состоянии, но активные пиридиновые и графитовые группы N имеют большое значение для определения активности ORR Fe / N / C- типа электрокатализаторов.
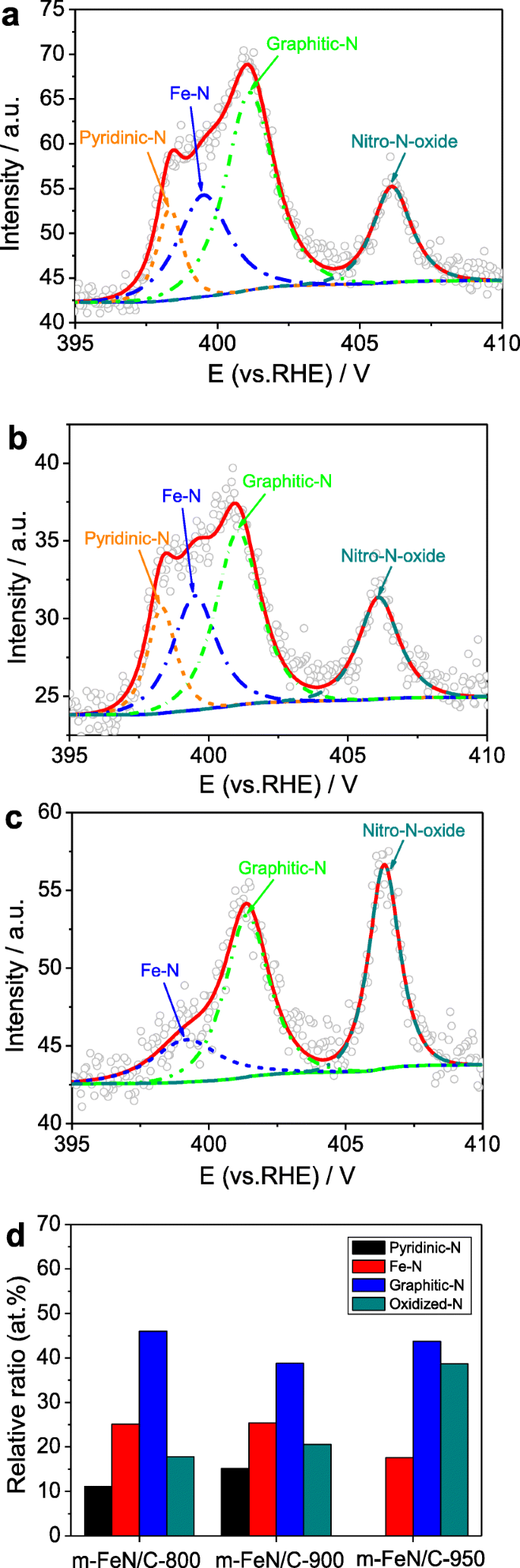
N 1 s XPS-спектры м -Fe / N / C-800 ( a ), м -Fe / N / C-900 ( b ), м -Fe / N / C-950 ( c ), и их относительное содержание в общем содержании N ( d )
Анализ морфологии m Катализатор -Fe / N / C-900 изображен на рис. 6 и в дополнительном файле 1:на рис. S3. На м может существовать большое количество губчатых форм. -Fe / N / C-900 (рис. 6a, b), синтезированный высокотемпературным пиролизом металлоорганических (Fe-TPTZ) комплексов, ограниченно закрепленных в наноканалах молекулярных сит. ПЭМ-изображения с высоким разрешением (рис. 6c, d) убедительно демонстрируют наличие множества высокоупорядоченных мезопористых структур внутри m -Fe / N / C-900, который в значительной степени может быть получен в результате удаления молекулярного сита в качестве реактора с ограниченным наноканалом. Кроме того, на рис. 6д отчетливо видны неупорядоченные углеродные структуры на краю и несколько мезопор, что связано с легированием атомов азота. По этой причине характеристики пористости и площадь поверхности Брунауэра-Эмметта-Теллера (БЭТ) м -Fe / N / C-900 также исследовали с помощью изотерм адсорбции / десорбции азота (вставка на рис. 6f). Можно наблюдать изотермическую кривую типа Ленгмюра IV, что указывает на высокую мезопористость m Электрокатализатор -Fe / N / C-900. Это может быть дополнительно подтверждено распределением пор BJH по размерам m . -Fe / N / C-900 (рис. 6f), который показал высокую площадь поверхности BET ( A СТАВКА ~ 1035 м 2 г -1 ) и общий объем пор ( V всего ~ 1,22 см 3 г -1 ) со средним диаметром пор ( D p ) около 4,7 нм. Представленные два максимальных размера пор (4,3 и 9,3 нм) приписываются максимальному положению мезопор в м -Fe / N / C-900. Эти мезопоры могут обеспечить более удобные наноканалы для быстрой транспортировки электролита, реагентов и продуктов; уменьшить сопротивление транспортировке молекулы кислорода к активным центрам, легированным азотом; и повысить каталитическую эффективность ORR на м -Fe / N / C-900. Кроме того, использование наноканалов молекулярного сита в качестве наноконфликтного реактора выгодно для получения губчатых трехмерных мезопористых углеродов со сверхвысокой площадью поверхности, способствуя увеличению воздействия каталитически активных центров ORR. Изображения элементарного картирования (рис. 7) отображают однородное распределение четырех видов основных элементов (Fe, N, C и O) на поверхности m -Fe / N / C-900, что может быть результатом синергетической роли ограниченного наноканалами эффекта молекулярных сит и стабильного молекулярно-координационного эффекта комплексов Fe-TPTZ в определенной степени.
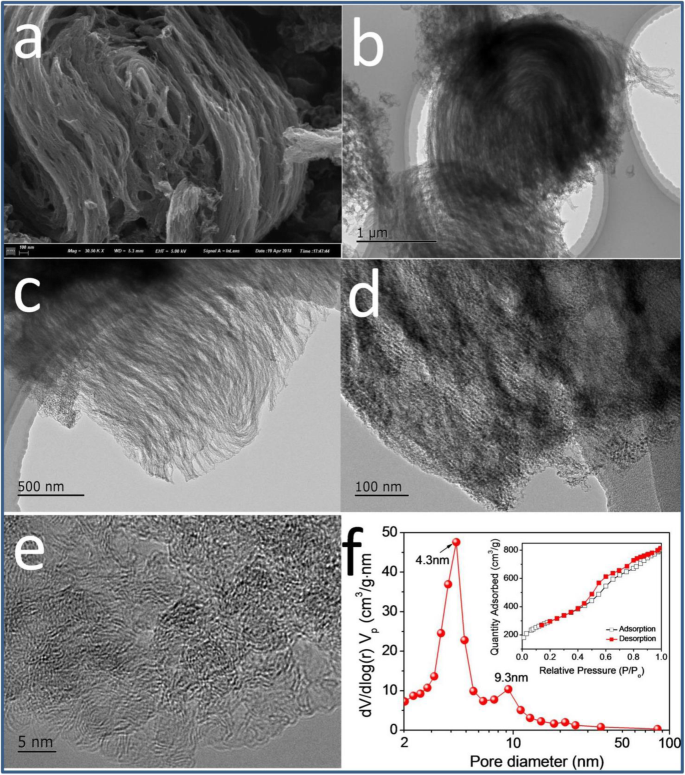
SEM ( a ) и ПЭМ-изображения высокого разрешения ( b - е ) м -Fe / N / C-900; е распределение пор по размерам м -Fe / N / C-900; на вставке изотермы адсорбции-десорбции азота

Изображение TEM ( a ) м -Fe / N / C-900 и соответствующие изображения элементарного отображения C, O, Fe и N ( b - е )
Электрокаталитическую активность по отношению к ORR всех приготовленных катализаторов проверяли с помощью циклической вольтамперограммы (CV) или линейной сканирующей вольтамперограммы (LSV). На рисунке 8a показаны CV для м -Fe / N / C-900 в N 2 против O 2 -насыщенный 0,1 моль л -1 Электролит КОН. Резкий пик ORR произошел при 0,86 В по сравнению с RHE в O 2 -насыщенный электролит; однако в N 2 наблюдалась безликая CV-кривая. -насыщенный электролит, предполагающий каталитическую активность ORR m -Fe / N / C-900 с начальным потенциалом ( E начало ) 1,0 В. Кроме того, влияние температуры термообработки (800–950 ° C) на производительность ORR было исследовано на рис. 8b. Более высокая или более низкая температура термообработки препятствует увеличению активности на основе максимальной пиковой плотности тока ( j p ), и потенциал наиболее положительного пика ( E p ) можно получить на м -Fe / N / C-900. Активность ORR m -Fe / N / C-900 может быть сопоставим с другими известными катализаторами на основе легированного углерода (см. Дополнительный файл 1:Таблица S2). Чтобы получить представление о кинетическом поведении ORR электрокатализаторов типа Fe / N / C, мы дополнительно протестировали поляризационные кривые ORR методом LSV в сочетании с RRDE, как показано на рис. 8c. На основании данных RRDE перенесенный номер электрона ( n ) и H 2 О 2 доходность (H 2 О 2 %) во время ORR были оценены с помощью следующих уравнений. (1) и (2) соответственно. Вычисленные уравнения выглядят следующим образом [34]:
$$ \% H {O} _2 ^ {-} =100 \ times \ frac {2 {I} _r / N} {I_d + \ left ({I} _r / N \ right)} $$ (1) $$ n =4 \ times \ frac {I_d} {I_d + {I} _r / N} $$ (2)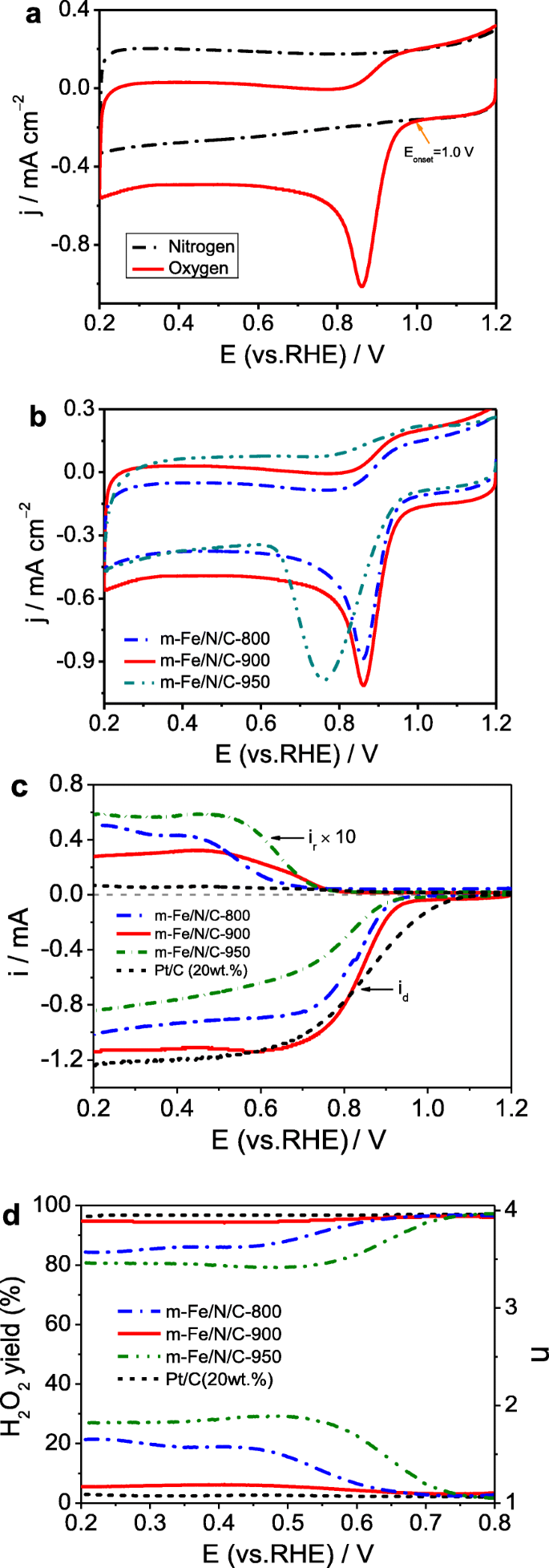
а Кривые CV м -Fe / N / C-900 в N 2 против O 2 -насыщенный 0,1 М раствор КОН. б Кривые CV м -Fe / N / C-800, м -Fe / N / C-900 и m -Fe / N / C-950 в O 2 -насыщенный 0,1 моль л -1 Раствор КОН. c Disk and ring currents obtained with LSVs on RRDE for m -Fe/N/C-800, m -Fe/N/C-900, and m -Fe/N/C-950 in O2 -saturated 0.1 mol l -1 KOH solution. г The corresponding electron transfer numbers and H2 О 2 yields of m -Fe/N/C-800, m -Fe/N/C-900, and m -Fe/N/C-950 derived from c
где I d is the Faradaic disk-current, I r is the Faradaic ring-current, and N is the collection efficiency of ring electrode (0.38). The Pt-ring potential was set at 1.5 V (vs. RHE) as reported elsewhere. Figure 8d displays the relatively calculated results. H 2 О 2 yield (<6.5%) and n value (3.88–3.94) are obtained on m -Fe/N/C-900, dominating a four-electron ORR pathway. It suggests that this catalyst is a valuable substitute for the traditional 20 wt.% Pt/C catalyst (purchased from Aladdin Industrial Co. Ltd.), although the H2 О 2 yield on m -Fe/N/C-900 is slightly higher. In addition, the half-wave potential (E 1/2 ) for ORR of m -Fe/N/C-900 is about 0.841 V approaching that of 20 wt.% Pt/C (~ 0.848 V), and the limited current density (j d ) of m -Fe/N/C-900 is almost identical to that of 20 wt.% Pt/C. Compared to the m -Fe/N/C-900 catalyst, higher H2 О 2 yield and smaller n value can be gained on both m -Fe/N/C-800 and m -Fe/N/C-950, but the electron transfer number on both m -Fe/N/C-800 and m -Fe/N/C-950 still belongs to the range (3.4–4.0), showing that the ORR on two Fe/N/C-type happens with a mixed process of two and four-electron transfer pathways. The above results further approve that the m -Fe/N/C-900 synthesized by nanochannel-confined control of the pyrolysis process to improve the nitrogen-doping efficiency and increase the nitrogen-doped active-site density has exhibited the optimal ORR catalytic performance in alkaline electrolyte.
We also discuss the effect of different transition metals on the ORR catalytic activity of Fe/N/C-type electrocatalysts. The obtained LSV curves on the RRDE are indicated in Fig. 9a, and the corresponding n value and H2 О 2 yield are demonstrated in Fig. 9b. E 1/2 values are about 0.785 V for m -Cu/N/C-900 and 0.780 V for m -Ni/N/C-900, respectively, which are lower compared to the m -Fe/N/C-900. The j d follows the order of m -Fe/N/C-900> m -Cu/N/C-900> m -Ni/N/C-900, further suggesting the best ORR catalytic activity of m -Fe/N/C-900 in 0.1 mol l -1 KOH solution. Compared to the m -Fe/N/C-900 catalyst, higher H2 О 2 yield and smaller n value are obtained on both m -Cu/N/C-900 and m -Ni/N/C-900. What is noteworthy is that the H2 О 2 yield on m -Cu/N/C-900 and m -Ni/N/C-900 is over twice as large as that on m -Fe/N/C-900. However, the n value on both m -Cu/N/C-900 and m -Ni/N/C-900 is 3.5–4.0, indicating that the ORR process on two Fe/N/C-type electrocatalysts follows a two- and four-electron mixed transfer pathway but is dominant in a four-electron reaction pathway. Besides, the electrochemical long-term stability for ORR catalysis of m -Fe/N/C-900 is of great significance in the practical applications. An accelerated aging test (AAT) was carried out by successive CV scanning tests from 0.2 to 1.2 V vs RHE for 5000 cycles at 200 mV s -1 in oxygen-saturated 0.1 M KOH electrolyte. The ORR electrocatalytic behavior of m -Fe/N/C-900 has been further evaluated under the same conditions as above experiments. CV curves for ORR activity of m -Fe/N/C-900 before and after doing the AAT are almost unchanged on the E p (~ 0.86 V), but the j p is slightly reduced (Fig. 9c). LSV curves of m -Fe/N/C-900 (Fig. 9d) also reveal an only ~ 12 mV negative shift in the E 1/2 and a negligible decrease in the j d . However, the commercial Pt/C (20 wt.% Pt) catalyst after doing the AAT has exhibited about 55 mV of the negative shift in E 1/2 and an obvious reduction in the j d (Fig. 9d). Results show that the m -Fe/N/C-900 has more excellent electrocatalytic stability compared to the Pt/C catalyst, further suggesting that it is a valuable and promising substitute for the conventional Pt-based materials in alkaline electrolytes.
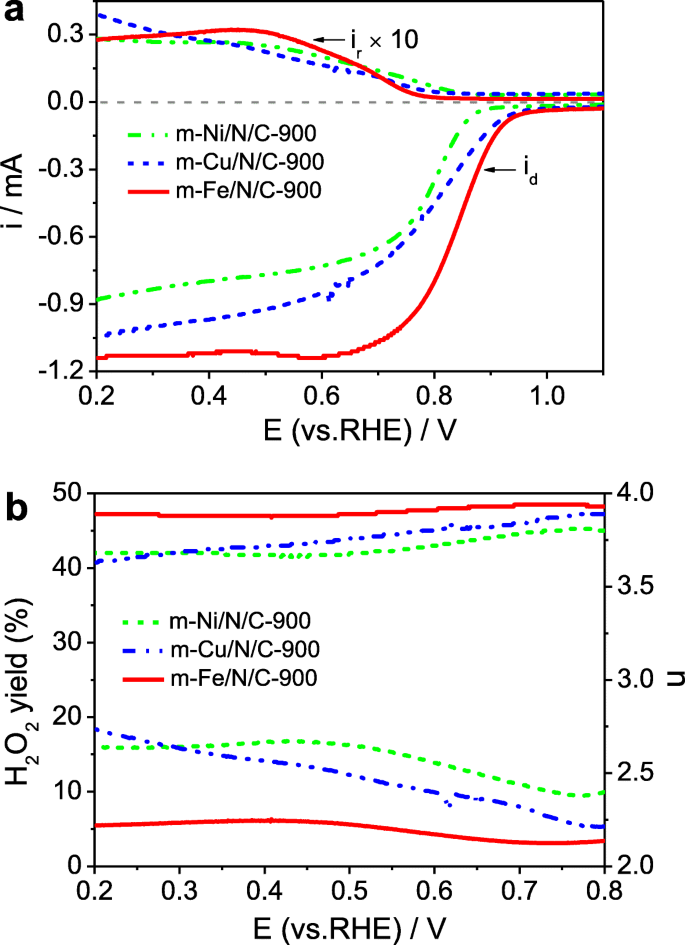
а Disk and ring currents obtained with LSVs on RRDE for m -Ni/N/C-900, m -Cu/N/C-900, and m -Fe/N/C-900 in O2 -saturated 0.1 mol l -1 KOH solution. б The corresponding electron transfer number and H2 О 2 yield of m -Ni/N/C-900, m -Cu/N/C-900, and m -Fe/N/C-900 derived from a . c CV curves and d LSV curves of m -Fe/N/C-900 before and after continuous scanning for 5000 cycles in O2 -saturated 0.1 M KOH solution
In order to discuss the catalytically active sites of Fe/N/C-type catalysts and study the role of the molecular coordination and nanochannel-confined effects, we have further examined the N/C-900, Fe/N/C-900, and 20 wt.% Pt/C catalysts for comparison of the ORR catalytic behavior. The tested results of the ORR activity are indicated in Fig. 10a. The onset potentials of ORR are about 0.683 V for N/C-900 and 0.740 V for Fe/N/C-900, being largely lower than those of m -Fe/N/C-900 (0.841 V) and 20 wt.% Pt/C catalysts (0.848 V). Figure 10b shows the corresponding H2 О 2 yields and transferred electron numbers in the ORR process. Given other Fe/N/C-type catalysts and the Pt/C catalyst, the H2 О 2 yield on N/C-900 is the highest and the transferred electron number on N/C-900 is the smallest, suggesting the worst ORR catalytic activity of N/C-900. In addition, the H2 О 2 yield on Fe/N/C-900 is mainly higher than that on m -Fe/N/C-900 and the transferred electron number on Fe/N/C-900 is far lower than that on m -Fe/N/C-900 in the same range (0.2–0.8 V vs RHE), indicating a relatively inferior ORR activity. Thus, it can be concluded that the ORR performance complies with the sequence of Pt/C> m -Fe/N/C-900> Fe/N/C-900> N/C-900. These results show that the formation of Fe-TPTZ compounds with the strong molecular-level coordination effect is beneficial to produce the Fe/N/C-type catalysts with high ORR activity, and the utilization of the nanochannel-confined effect can reduce the decomposition speed of Fe-TPTZ compounds and protect the nitrogen-rich active sites (e.g., Fe–N, graphitic-N, or pyridinic-N) from the thermal loss during the pyrolysis process (see the TG analysis, Fig. 2a), which can enhance the ORR performance of Fe/N/C-type catalysts in alkaline medium.
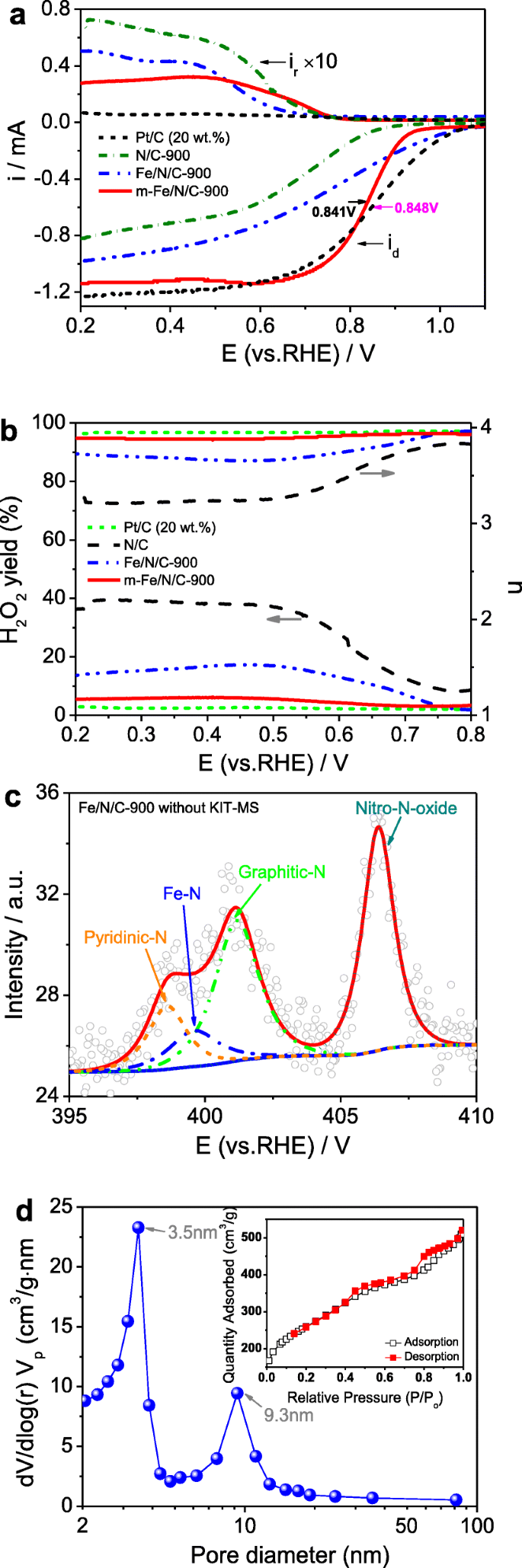
а Disk and ring currents obtained with LSVs on RRDE for N/C-900, Fe/N/C-900, m -Fe/N/C-900, and Pt/C (20 wt.%) in O2 -saturated 0.1 mol l -1 KOH solution. б The corresponding electron transfer number and H2 О 2 yield of N/C-900, Fe/N/C-900 m -Fe/N/C-900, and Pt/C (20 wt.%) derived from a
To deepen the understanding of active sites and their ORR catalysis mechanism, we also characterized the prepared Fe/N/C-type catalysts by the spectra of X-ray diffraction (XRD) and X-ray photoelectric spectroscopy (see Additional file 1:Figures S4 and S5). The XRD data display that the density of carbon (002) peak follows the sequence of N/C-900> Fe/N/C-900> m -Fe/N/C-900, and the positions for carbon (002) peak in three catalysts are negatively shifted because of the production of more sp 2 C–N groups into the graphitic layers and the decrease of graphitization. It also implies that the different N content may be doped into the carbon skeleton in the catalyst, and both N-doping efficiency and N content can follow the similar order with their ORR activity. More significantly, we further compare the structural and porous differences between Fe/N/C-900 and m -Fe/N/C-900 to better study the nanochannel-confined effect of molecular sieves. The tested XPS survey spectrum of Fe/N/C-900 was indicated in Additional file 1:Figure S5, and its surface contents of Fe, C, and N and the N/C ratio were summarized in Table 1. The Fe content and N content are ~ 0.41 at.% and ~ 4.48 at.%, but the N/C ratio is only 5.1 in the Fe/N/C-900, being lower compared to the m -Fe/N/C-900. It suggests the N-doping efficiency was improved by introducing the nanochannel-confined protection strategy into the carbonization process, which can prove our key views of this work. Besides, the fitted N1s XPS spectrum of Fe/N/C-900 is indicated in Fig. 10c. It displays the existence of four peaks with B.E. of 398.6, 399.6, 401.2, and 406.4 eV, which still correspond to the pyridinic-N, Fe–N, graphitic-N, and oxidized-N (–NO2 ) with a relative percentage of 14.0, 10.2, 35.4, and 40.4 at.%, respectively. Compared with the m -Fe/N/C-900, the total ratio of active N-rich groups such as pyridinic-N, Fe–N, and graphitic-N obviously decreases about 19.8 at.%; however, the relative ratio of Fe–N groups is reduced about 15.2 at.%. Thus, associating with fore-mentioned XPS data and the catalytic activity data, we conclude that the electrocatalytically active sites may be pyridinic- and graphitic-N groups for holding the ORR performance, but the enhancement of the ORR activity may be related to the relative ratio of Fe–N groups for our system. The role of the nanochannel-confined effect cannot only reduce the loss of total N content, but also can largely increase the N-doping efficiency and improve the effective ORR active-site density in the catalyst. Besides, we further analyzed porous characteristic and BET specific surface area of Fe/N/C-900 without the usage of the KIT-MS nanoreactor. The nitrogen adsorption/desorption isotherms with a similar Langmuir IV-type isotherm curve are seen in the inset of Fig. 10d. It suggests that highly mesoporous characteristic is still existed in Fe/N/C-900, supported by the analysis of BJH pore-size distribution (Fig. 10d). The A СТАВКА (~ 875 m 2 g -1 ) and V всего (~ 0.76 cm 3 g -1 ) with an average D P of only ~ 3.5 nm are obtained on the Fe/N/C-900, which are obviously lower than those on the m -Fe/N/C-900. The large difference on pore structures between Fe/N/C-900 and m -Fe/N/C-900 can be derived from the stable coordination effect and the nanochannel-confined role of a KIT-MS reactor in the preparation of m -Fe/N/C-900. It will also influence their inherent ORR performance because higher A СТАВКА и V всего can help to supply abundant catalytic sites and increase the exposed surface active-site density, being beneficial to the adsorption and electro-reduction process of O2 molecule [35]. Notably, we should pay much attention to the effect of the conductivity characteristic. Generally, a higher conductivity characteristic of m -Fe/N/C-900 corresponds to a relatively faster ORR electron transportation process. Therefore, facile design and control of active nitrogen-rich groups (pyridinic-N, graphitic-N, and Fe–N, etc.) is of great importance to fabricate mesopore-structured Fe/N/C electrocatalysts for the ORR, but further improving the conductance, N-doped active-site density, and mesoporous characteristic is another key issue of concern to obtain the high performance.
Выводы
In conclusion, here, we propose a new and effective strategy to design a Fe/N/C-type electrocatalyst (m -Fe/N/C-900) with ultrahigh BET surface area (1035 m 2 g -1 ) and total pore volume (1.22 cm 3 g -1 ) via nanochannel-confined high-temperature carbonization of Fe 2+ ions coordinated with 2,4,6-tri(2-pyridyl)-1,3,5-triazine compound as a single-source Fe, N, and C precursor. The elemental mapping images of m -Fe/N/C-900 further prove the homogeneous distribution of Fe, N, C, and O elements on its surface. On the one hand, the strong molecular-coordination role in Fe-TPTZ complex can enhance the thermal stability and stabilize higher contents of Fe–N active sites during pyrolysis process. On the other hand, the utilization of abundant nanochannels of molecular sieve as a novel nanoconfined reactor does not only benefit to produce spongy-like mesoporous carbons with excellent pore structure and conductivity characteristic, but also facilitate to decrease the loss of N atoms and improve the N-doping efficiency and N-doped active-site density, resulting in the ORR activity enhancement. Electrochemical tests indicate the m -Fe/N/C-900 displays unexpected catalytic performance with an ORR half-wave potential of ~ 0.841 V versus RHE and high limited current density approaching the commercial Pt/C catalyst. Additionally, low H2 О 2 yield (<6.5%) and high electron transfer number (3.88–3.94) on m -Fe/N/C-900, indicating that it is a valuable substitute for the traditional Pt/C catalyst. The comparison analysis of XPS data and electrocatalytic activity data can point out that active pyridinic and graphitic-N groups may be the electrocatalytically ORR-active sites, but the enhancement of the ORR activity may be related to the relative ratio of Fe–N groups for our system. This study provides a new idea or method for the synthesis of high-performance Fe/N/C electrocatalysts via integrating molecular-level coordination and nanochannel-confined effects and does also help the researchers better deepen the understanding of nitrogen-doped active sites and their ORR catalysis mechanism for Fe/N/C-type electrocatalysts to a certain extent. However, what cannot be ignored is that effective improvement and optimization of nitrogen-doping active site density, conductivity, and porous characteristics is essential to boost the ORR electrocatalytic activity.
Доступность данных и материалов
The authors declare that the materials and datasets used or analyzed during the current study are available from the corresponding author on reasonable request.
Сокращения
- AAT:
-
Accelerated aging test
- AE:
-
Auxiliary electrode
- СТАВКА:
-
Брунауэр-Эмметт-Теллер
- Резюме:
-
Циклическая вольтамперометрия
- E 1/2 :
-
Half-wave potential
- E p :
-
Peak potential
- Fe/N/C catalyst:
-
Iron/nitrogen/carbon catalyst
- Fe-TPTZ:
-
Fe coordinated with 2,4,6-tri(2-pyridyl)-1,3,5-triazine complexes
- GC:
-
Glassy carbon
- HR-TEM:
-
Просвечивающая электронная микроскопия высокого разрешения
- KIT-MS:
-
KIT-6 molecular sieves
- LSV:
-
Вольтамперометрия с линейной разверткой
- ORR:
-
Реакция восстановления кислорода
- Pt/C:
-
Platinum/carbon catalyst
- RDE:
-
Rotation disk electrode
- RE:
-
Reference electrode
- RHE:
-
Реверсивный водородный электрод
- RRDE:
-
Rotation ring-disk electrode
- SCE:
-
Насыщенный каломельный электрод
- SEM:
-
Сканирующая электронная микроскопия
- TGA:
-
Термогравиметрический анализ
- TPTZ:
-
2,4,6-Tri(2-pyridyl)-1,3,5-triazine
- WE:
-
Working electrode
- XPS:
-
Рентгеновская фотоэлектронная спектроскопия
- XRD:
-
Рентгеновская дифракция
Наноматериалы
- Достижения и проблемы флуоресцентных наноматериалов для синтеза и биомедицинских приложений
- Синтез зеленого цвета в одной емкости микросферы SnO2, украшенной серебром:эффективный и многоразовый катализ…
- Метод последующей обработки для синтеза монодисперсных бинарных наночастиц FePt-Fe3O4
- Самолегированный высокопористый углерод графитового азота для электрокатализа реакции восстановления кисл…
- Синтез и активность окисления CO 1D смешанного бинарного оксида CeO2-LaO x, нанесенного золотыми катализаторами
- Нанопетали из мезопористого оксида никеля (NiO) для сверхчувствительного определения уровня глюкозы
- Сапонины Platycodon из Platycodi Radix (Platycodon grandiflorum) для зеленого синтеза наночастиц золота и серебра
- Простой синтез поверхностно-функционализированных магнитных нанокомпозитов для эффективной селективной ад…
- Реакция восстановления кислорода на PtCo Нанокатализатор:отравление (Bi) сульфат-анионами
- Двумерные мезопористые микрочипы VO2 для высокопроизводительного суперконденсатора



