Модификация сокатализатора сплава PtNi сенсибилизированного эозином Y гибрида g-C3N4 / GO для эффективного фотокаталитического выделения водорода в видимом свете
Аннотация
Экономичный и эффективный сокатализатор из сплава на основе Pt привлек значительное внимание благодаря своей превосходной каталитической активности и сокращению использования Pt. В этом исследовании сокатализатор из сплава PtNi был успешно декорирован на g-C 3 N 4 / GO гибридный фотокатализатор с помощью простого метода химического восстановления. Сенсибилизированный эозином Y g-C 3 N 4 Композитный фотокатализатор /PtNi/GO-0.5% дает примерно в 1,54 и 1178 раз более высокую скорость выделения водорода, чем сенсибилизированный эозином Y g-C 3 N 4 /Pt/GO-0.5% и g-C 3 N 4 /Ni/GO-0.5% соответственно. Механизм повышения производительности для g-C 3 N 4 Композит / PtNi / GO также был исследован с помощью различных характеристик, таких как фотолюминесценция, переходный отклик фототока и ПЭМ. Эти результаты показали, что повышенная эффективность разделения зарядов и большее количество реактивных центров ответственны за улучшенные характеристики выделения водорода из-за положительного синергетического эффекта между Pt и Ni. Это исследование предполагает, что сплав PtNi может быть использован в качестве экономичного и эффективного сокатализатора в реакции выделения водорода.
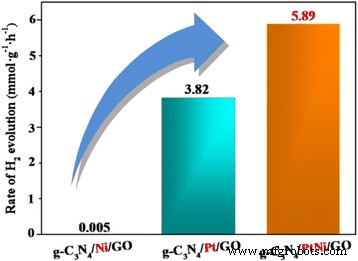
Значительное увеличение фотокаталитического H 2 эволюция осуществляется через сенсибилизированный эозином Y g-C 3 N 4 / PtNi / GO композит со сплавом PtNi в качестве эффективного сокатализатора.
Фон
Устойчивое и крупномасштабное выделение водорода из воды с использованием солнечной энергии считается одним из многообещающих методов решения энергетического кризиса и загрязнения окружающей среды [1, 2]. Для достижения этой цели требуются фотокатализатор, реагирующий на видимый свет, и эффективный сокатализатор [3,4,5]. Обычно загрузка благородного металла Pt в качестве эффективного сокатализатора крайне необходима для достижения высокой скорости выделения водорода [6,7,8]. Однако платина встречается редко и дорого, что затрудняет ее практическое применение. Желательно снизить количество используемой Pt при одновременном сохранении ее превосходной каталитической активности в отношении выделения водорода. Замена части Pt переходным металлом (Ni, Co, Cu, Fe и т. Д.) С образованием сокатализатора из биметаллического сплава является многообещающим потенциальным способом достижения превосходной каталитической активности и сокращения использования Pt [9,10,11]. В некоторых случаях каталитические характеристики сокатализатора из биметаллического сплава на основе Pt сравнимы с чистой Pt из-за положительного синергетического эффекта между двумя металлами. Поэтому в последнее время все больше внимания уделяется фотокатализатору, реагирующему на видимый свет, с добавлением сокатализатора из биметаллического сплава.
Yu et al. сообщили, что Cu 2 , модифицированный сокатализатором из сплава PtCo или сплава PtNi ZnSnS 4 показал более высокий H 2 эффективность производства по сравнению с загрузкой чистой Pt Cu 2 ZnSnS 4 [12]. Пт 3 Ко-биметаллический сокатализатор, украшенный CdS, был приготовлен Hu et al. и показали улучшенные характеристики выделения водорода [13]. PtCo и / или PtFe загрузка Zn 1 - x Компакт-диск x S также оценивались в предыдущих исследованиях [14, 15]. Однако низкие фотокаталитические характеристики Cu 2 в видимом свете ZnSnS 4 или высокая токсичность Cd препятствует их практическому применению в больших масштабах. Нитрид углерода (g-C 3 N 4 ) привлекла внимание своей невысокой стоимостью [16]. Han et al. сообщил, что H 2 скорость эволюции 960 мкмоль г -1 ч −1 был получен над PtCo / g-C 3 N 4 фотокатализатор под λ > Облучение 400 нм [17]. PtNi x / g-C 3 N 4 Фотокатализатор hybird был также изучен Би и др., а H 2 скорость эволюции 8456 мкмоль г -1 ч −1 достигается при полном спектральном облучении [18]. Однако фотокаталитические характеристики в видимом свете для биметаллического сплава, модифицированного сокатализатором g-C 3 N 4 фотокатализатор все еще находится на низком уровне из-за широкой запрещенной зоны 2,7 эВ и плохой способности к переносу электронов. Эозин Y-сенсибилизированный g-C 3 N 4 может собирать широкий диапазон видимого света [19, 20]. Оксид графена (GO) обладает высокой способностью к переносу электронов и широко используется в качестве акцептора электронов [21,22,23,24,25]. Объединение g-C 3 N 4 и GO может способствовать передаче электронов в g-C 3 N 4 и, таким образом, улучшить разделение электронно-дырочных пар для улучшения фотокаталитических характеристик выделения водорода [26,27,28,29,30,31]. Недавно мы сообщили об эффективном сенсибилизированном эозином Y g-C 3 N 4 Композитный фотокатализатор выделения водорода / Pt / GO [23]. Дорогой Pt сокатализатор играет одну из важных ролей в относительно высоких характеристиках производства водорода. Для уменьшения дорогостоящего использования Pt и дальнейшего улучшения ее видимых фотокаталитических характеристик используется недорогой g-C, сенсибилизированный эозином Y 3 N 4 Композитный фотокатализатор / GO, содержащий сокатализатор из сплава на основе Pt, является полезным.
Здесь сенсибилизированный эозином Y g-C 3 N 4 Составной фотокатализатор / PtNi / GO был приготовлен для выделения водорода из воды. Самая высокая скорость выделения водорода 5,89 ммоль г -1 ч −1 получается над сенсибилизированным эозином Y g-C 3 N 4 / PtNi / GO фотокатализатор, который намного превосходит сенсибилизированный эозином Y g-C 3 N 4 / Pt / GO и g-C 3 N 4 / Образцы композитов Ni / GO. Насколько нам известно, ранее не сообщалось о том, что сенсибилизированный эозином Y g-C 3 N 4 Композит / PtNi / GO используется для получения водорода из воды. Оптимальное молярное соотношение Pt / Ni и количество сокатализатора PtNi были подробно рассмотрены. Кроме того, механизм улучшенных фотокаталитических характеристик для g-C 3 N 4 Композит / PtNi / GO также был исследован с помощью различных методов определения характеристик.
Экспериментальный раздел
Синтез g-C 3 N 4
g-C 3 N 4 порошки были синтезированы, как описано в предыдущем исследовании [32]. В типичной процедуре мочевину (8 г) помещали в тигель из оксида алюминия с крышкой. Тигель нагревали до 600 ° C со скоростью нагрева 5 ° C / мин и выдерживали в течение 2 ч в трубчатой печи. После термической обработки светло-желтый g-C 3 N 4 порошки были собраны для дальнейшего использования.
Подготовка GO
ГО был приготовлен по модифицированной методике Хаммерса [33]. Природный графит (10 г) и NaNO 3 (5 г) помещали в химический стакан. Затем добавили 230 мл концентрированной серной кислоты, и процесс должен быть как можно медленнее. Вышеуказанную реакцию проводили при перемешивании на бане с ледяной водой. Затем 10 г KMnO 4 добавляли к раствору смеси и оставляли реагировать в течение 3 часов. Температуру раствора повышали до 35 ° C и поддерживали в течение 4 ч. Затем в полученный раствор выливали 460 мл дистиллированной воды и нагревали до примерно 98 ° C в течение 3 часов. После реакции определенное количество H 2 О 2 (30%) и концентрированную соляную кислоту добавляли при перемешивании с целью удаления избытка KMnO 4 и SO 4 2– . Наконец, образец GO был получен путем сублимационной сушки в течение 24 часов.
Синтез g-C 3 N 4 / Ni / GO, г-Ц 3 N 4 / Pt / GO и g-C 3 N 4 / Pt x Ни y / GO Композитные фотокатализаторы
Синтез g-C 3 N 4 / PtNi / GO- X ( X представляет собой массовое отношение сокатализатора PtNi к г-C 3 N 4 / GO и молярное отношение Pt к Ni составляет 1:1):в типичном случае 133 мг г-C 3 N 4 диспергировали в 50 мл безводного этанола. Превышение NaBH 4 восстановитель добавляли в раствор смеси при перемешивании. Затем определенный объем NiCl 2 · 6H 2 Раствор O (0,1 моль / л) и H 2 PtCl 6 раствор (1,0 ммоль / л) по каплям добавляли к вышеуказанному раствору. Чтобы исследовать добавленную процедуру NiCl 2 · 6H 2 O и H 2 PtCl 6 Были выбраны три метода, включая одновременную загрузку Pt и Ni, загрузку Pt, а затем Ni или наоборот. Затем суспензионный раствор перемешивали в течение 5 часов для достижения однородной дисперсии сокатализатора PtNi в g-C 3 N 4 . После этого g-C 3 N 4 / Образцы PtNi-X были собраны центрифугированием, чтобы смыть избыток NaBH 4 несколько раз. После этого 67 мг GO и g-C 3 N 4 / PtNi-X одновременно диспергировали в 100 мл дистиллированной воды. Суспензионный раствор обрабатывали ультразвуком при 500 Вт в течение 10 часов. После этого серия g-C 3 N 4 / PtNi / GO- X Композитные фотокатализаторы получали центрифугированием, а затем сушили при 60 ° C в вакуумной печи в течение одной ночи. Другие сокатализаторы из биметаллического сплава PtNi с другим молярным соотношением Pt / Ni (9:1, 3:1, 1:3, 1:9) также были приготовлены таким же образом, как и вышеупомянутый метод, который назван Pt 9 Ни 1 , Pt 3 Ни 1 , Pt 1 Ни 3 , и Pt 1 Ни 9 соответственно, соотношение M Pt / Ni 1:1 называют PtNi.
Синтез g-C 3 N 4 /Ni/GO-0.5% и g-C 3 N 4 /Pt/GO-0,5% образцов (0,5% представляет собой массовое отношение Ni или Pt к г-C 3 N 4 / GO композит):g-C 3 N 4 /Ni/GO-0.5% и g-C 3 N 4 Образцы /Pt/GO-0,5% были приготовлены с использованием той же процедуры подготовки, что и g-C 3 N 4 / PtNi / GO-X, за исключением добавления другого объема NiCl 2 · 6H 2 Раствор O или H 2 PtCl 6 решение. Весовое соотношение г-С 3 2:1 N 4 to GO выбран во всех g-C 3 N 4 / Ni / GO, г-Ц 3 N 4 / Pt / GO и g-C 3 N 4 / Pt x Ни y Составные образцы / GO в соответствии с нашим предыдущим исследованием [32].
Методы характеризации
Рентгенограммы получали с использованием рентгеновского дифрактометра (Bruker D8-Advance, Германия) с использованием Cu-Kα-излучения. ПЭМ-изображения образцов регистрировали с помощью просвечивающей электронной микроскопии (JEM-2100, Япония). Химические состояния поверхности фотокатализаторов измеряли с помощью рентгеновской фотоэлектронной спектроскопии (XPS, AXISULTRA) с монохроматическим рентгеновским излучением Al Ka (1486,6 эВ). Спектры фотолюминесценции (ФЛ) измеряли на спектрометре JY HORIBA FluoroLog-3, длина волны возбуждения была выбрана 460 нм. Кривые отклика фототока получали на электрохимической рабочей станции (CHI660E, Ченхуа, Китай) с использованием стандартной стандартной трехэлектродной ячейки при облучении видимым светом (λ> 420 нм). 0,1 моль / л Na 2 SO 4 раствор использовался в качестве электролита.
Измерение фотокаталитической активности
Фотокаталитические эксперименты проводились в ячейке из пирекса с плоским верхним окном при 6 ° C. Обычно 50 мг порошка фотокатализатора и 50 мг красителя эозина Y добавляли в 100 мл H 2 O, содержащий 20 об.% ( v / v) триэтаноламин (TEOA, pH =7). В качестве источника света использовалась ксеноновая лампа мощностью 300 Вт (D59, Beijing China Education Au-light Co., Ltd) в сочетании с УФ-фильтром (> 420 нм). Количество водорода измеряли с помощью газовой хроматографии (GC-7920, TCD, Ar-носитель).
Результаты и обсуждение
Диаграммы XRD g-C 3 N 4 /Ni/GO-0.5%, g-C 3 N 4 /Pt/GO-0.5% и g-C 3 N 4 Образцы /PtNi/GO-0.5% показаны на рис. 1. Для трех образцов наблюдаются два очевидных дифракционных пика. Небольшой пик с центром при 2θ =13,8 ° соответствует пику (100) g-C 3 N 4 , который возникает из-за мотива структурной упаковки в плоскости [34]. Пик сильной дифракции при 27,4 ° обозначен как пик (002) g-C 3 N 4 , что соответствует межслоевой укладке сопряженной ароматической системы [35]. Для трех оцениваемых образцов дифракционный сигнал сокатализатора GO, Pt и / или Ni обнаружен не был. Достаточное расслоение GO в композите может привести к отсутствию информации GO [28]. Пока количество Pt и / или Ni слишком мало для обнаружения методом XRD. Как показано на рис. 2, три разных образца после ультразвуковой обработки демонстрируют аналогичную более тонкую ламинарную структуру. Тесный контакт между двухмерной слоистой структурой g-C 3 N 4 и нанолистовая структура ГО. На рис. 2a, b наночастицы Ni или Pt немного большего размера диспергированы на промежуточном слое или на поверхности g-C 3 N 4 . По сравнению с чистыми Ni и Pt размер частиц сокатализатора сплава PtNi уменьшается, а дисперсия сокатализатора сплава PtNi улучшается (см. Рис. 2c). Небольшой размер сокатализатора из сплава PtNi будет обеспечивать больше реакционных центров для выделения водорода, а высокая дисперсность сокатализатора из сплава PtNi способствует передаче электронов от g-C 3 N 4 и / или перейти к сокатализатору PtNi. Улучшенная дисперсия сокатализатора сплава PtNi также наблюдалась в предыдущем исследовании [36]. Причина точности требует дальнейшего изучения.
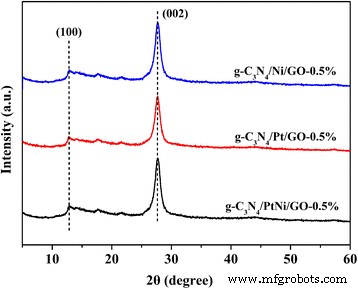
Диаграммы XRD g-C 3 N 4 /Ni/GO-0.5%, g-C 3 N 4 /Pt/GO-0.5% и g-C 3 N 4 /PtNi/GO-0.5% образцы

ПЭМ изображения g-C 3 N 4 /Ni/GO-0.5% ( а ), г-Ц 3 N 4 /Pt/GO-0.5% ( b ) и g-C 3 N 4 /PtNi/GO-0.5% ( c )
Для исследования поверхностного химического элемента и валентных состояний g-C 3 N 4 / Ni / GO, г-Ц 3 N 4 / Pt / GO и g-C 3 N 4 / PtNi / GO, были измерены XPS-спектры высокого разрешения трех различных образцов, и результаты показаны на фиг. 3. На фиг. 3a XPS-спектр C 1 s можно сопоставить с двумя сильными пиками со связыванием энергии около 284,8 эВ и 288,2 эВ, которые относятся к CC и N =CN соответственно [37]. Два пика характерны для разновидностей углерода в g-C 3 N 4 . Также получены два небольших пика при 286,7 эВ и 287,7 эВ, которые принадлежат функциональным группам C-O и C =O на поверхности GO соответственно [38]. На рис. 3 (b) характеристические пики C-N-C, N- (C) 3 , и группы C-N-H в g-C 3 N 4 были обнаружены, которые расположены при энергиях связи 398.7, 400.3 и 401.4 эВ соответственно [39]. На рис. 3 (c) энергии полос для O 1 s находятся при 532,4 и 533,8 эВ, которые относятся к кислородсодержащим функциональным группам в композитном образце и поверхностной адсорбции разновидностей кислорода, соответственно [40]. На рис. 3 (d) представлены спектры РФЭС дублета Pt 4f (4f 7/2 и 4f 5/2 ). Пт 4f 7/2 и 4f 5/2 пики расположены при 70,97 и 74,28 эВ для g-C 3 N 4 /Pt/GO-0.5% выборки, соответственно, которые представляют сигнал Pt 0 [41, 42]. Для g-C 3 N 4 /PtNi/GO-0.5%, орбитальные энергии связи Pt 4f сдвигаются примерно на 0,42 эВ в сторону высокой энергии связи по сравнению с чистой Pt. Очевидный сдвиг пика предполагает, что электрон Pt представляет собой небольшую потерю, что указывает на то, что сокатализатор сплава PtNi образуется в g-C 3 N 4 /PtNi/GO-0.5% образец. Как показано на рис. 3e, энергии связи 852,54 и 870,18 эВ могут быть отнесены к Ni 2p 3/2 и Ni 2p 1/2 для g-C 3 N 4 / Ni / GO-2% образца, соответственно, которые являются характеристическим сигналом Ni 0 [43]. По сравнению с g-C 3 N 4 / Ni / GO-2%, энергии связи Ni 2p смещены в сторону низкой энергии связи для g-C 3 N 4 / PtNi / GO-2% образец. Результат предполагает, что происходит изменение окружения атомов Ni, что дополнительно подтверждает успешность синтеза сокатализатора из сплава PtNi [41]. Точное молярное отношение Pt к Ni в г-C 3 N 4 Образец /PtNi/GO-0,5% составляет 9:11 по данным измерения XPS. На основании приведенного выше анализа можно сделать вывод, что g-C 3 N 4 Композит / PtNi / GO со сплавом PtNi в качестве сокатализатора был получен путем сочетания легкого жидкофазного сонохимического способа с методом химического восстановления.
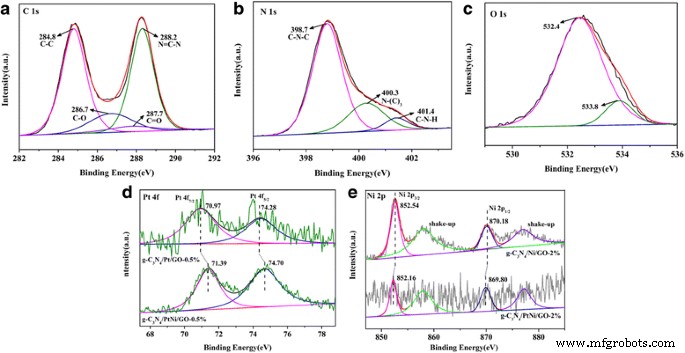
XPS-спектры ( a ) C 1 с, ( b ) N 1 с и ( c ) O 1 с для g-C 3 N 4 /PtNi/GO-0.5% образец. г XPS-спектры Pt 4f для g-C 3 N 4 /Pt/GO-0.5% и g-C 3 N 4 /PtNi/GO-0.5% образцов. е XPS-спектры Ni 2p для g-C 3 N 4 / Ni / GO-2% и g-C 3 N 4 / PtNi / GO-2% образцы
На рисунке 4 показан H 2 . скорость эволюции серии g-C 3 N 4 /PtNi/GO-0,5% образцов, загруженных сокатализатором разного типа. Одновременная загрузка названий Pt и Ni как g-C 3 N 4 /PtNi/GO-0.5%; Загрузка имен Pt, а затем Ni как g-C 3 N 4 /Pt-Ni/GO-0.5%; Загрузка Ni, а затем Pt имен как g-C 3 N 4 /Ni-Pt/GO-0.5%. Для g-C, сенсибилизированного эозином Y 3 N 4 /Ni/GO-0,5% образец с чистым Ni в качестве сокатализатора, H 2 скорость эволюции очень низкая и достигает всего 0,005 ммоль г -1 ч −1 . После замены Ni на Pt в качестве сокатализатора значительное увеличение H 2 наблюдается скорость эволюции, которая резко возрастает до 3,82 ммоль г -1 ч −1 для сенсибилизированного эозином Y g-C 3 N 4 /Pt/GO-0.5% образец. Результат предполагает, что загрузка эффективного сокатализатора Pt необходима для достижения отличных характеристик для H 2 . поколение. При использовании сплава PtNi в качестве сокатализатора сенсибилизированный эозином Y g-C 3 N 4 /PtNi/GO-0.5% композит показывает самый высокий H 2 скорость эволюции 5,89 ммоль г -1 ч −1 , что примерно в 1,54 и 1178 раз выше, чем у сенсибилизированного эозином Y g-C 3 N 4 /Pt/GO-0.5% и g-C 3 N 4 /Ni/GO-0.5% соответственно. Повышенные характеристики можно отнести к положительному синергетическому эффекту между Pt и Ni. По сравнению с чистым сокатализатором Pt, сокатализатор из сплава PtNi ускоряет накопление фотогенерированных электронов, которые обеспечивают большее количество электронов для выделения водорода [18]. Кроме того, небольшой размер и высокая дисперсность сокатализатора из сплава PtNi могут обеспечить больше H 2 сайтов эволюции и увеличивают перенос электронов соответственно. При загрузке Pt, а затем Ni или наоборот очевидное уменьшение H 2 наблюдается эволюционная активность. Фактически, загрузка Pt, а затем Ni или наоборот не приводит к образованию сокатализатора сплава PtNi [44]. Результат показывает, что достижение высокого H 2 скорость образования сильно зависит от использования эффективного сокатализатора из сплава PtNi.
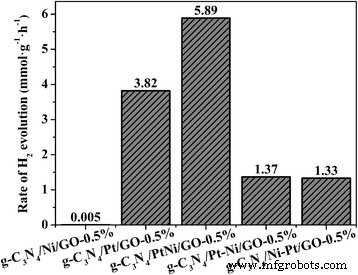
H 2 скорость эволюции серии g-C 3 N 4 /PtNi/GO-0,5% образцов, загруженных сокатализатором разного типа. Источник света:ксеноновая лампа 300 Вт ( λ > 420 нм). Реакционный раствор:100 мл 20% ( v / v) водный раствор ТЭОА (pH =7)
Состав сокатализатора из сплава PtNi оказывает важное влияние на каталитическую активность H 2 эволюция. Следовательно, H 2 скорость продукции сенсибилизированного эозином Y g-C 3 N 4 / Pt x Ни y Были исследованы образцы /GO-0,5%, нагруженные различным молярным соотношением Pt / Ni, результаты представлены на рис. 5а. H 2 производительность увеличивается постепенно с увеличением молярного отношения Ni / Pt. Когда молярное соотношение Ni / Pt составляет 1:1, максимальная скорость производства водорода составляет 5,89 ммоль г -1 ч −1 получается. Дальнейшее увеличение количества Ni приводит к падению H 2 эволюционная деятельность. Деградация H 2 производительность генерации может происходить из-за уменьшения количества активных сайтов Pt для H 2 эволюция. Активные центры Pt адсорбируют ионы водорода сильнее, чем Ni [12]. Следовательно, H 2 эволюция преимущественно идет на Pt, а не на Ni. На рисунке 5b показан H 2 скорость продукции сенсибилизированного эозином Y g-C 3 N 4 / PtNi / GO образцы, нагруженные различным количеством сокатализатора сплава PtNi. Когда массовое содержание сокатализатора из сплава PtNi составляет 0,5%, скорость выделения водорода составляет 2,45 ммоль г -1 . ч −1 получается для g-C 3 N 4 /PtNi/GO-0.25% образец. Скорость выделения водорода увеличивается с 2,45 ммоль г -1 . ч −1 до максимального значения 5,89 ммоль г -1 ч −1 после количества сокатализатора сплава PtNi до 0,5%. При дальнейшем увеличении количества сокатализатора из сплава PtNi характеристики выделения водорода незначительно снижаются. Избыток сокатализатора из сплава PtNi может препятствовать поглощению света эозином Y и g-C 3 N 4 и, таким образом, ухудшают фотокаталитические характеристики. Стабильность образования водорода для g-C 3 N 4 Образец /PtNi/GO-0,5% был также измерен, и результат показан на рис. 6. После 4-х циклового испытания скорость образования водорода для g-C 3 N 4 /PtNi/GO-0.5% образец показывает небольшое уменьшение, что указывает на то, что g-C 3 N 4 Композитный образец /PtNi/GO-0.5% относительно устойчив к выделению водорода. Сильная ковалентная связь между углеродом и нитридом в C 3 N 4 и слабая деградация эозина Y являются двумя основными причинами устойчивости g-C 3 к выделению водорода. N 4 /PtNi/GO-0.5% образец [19, 45].
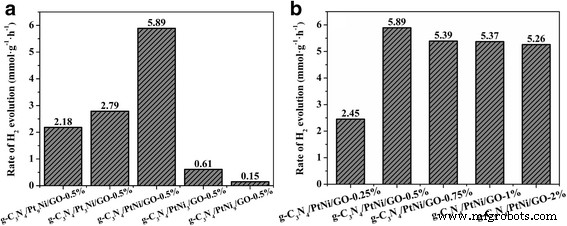
а H 2 скорость производства г-C 3 N 4 / Pt x Ни y /GO-0,5% образцы, нагруженные разным мольным соотношением Pt / Ni. б H 2 скорость производства г-C 3 N 4 / PtNi / GO образцы, нагруженные различным количеством сокатализатора сплава PtNi. Источник света:ксеноновая лампа 300 Вт ( λ > 420 нм). Реакционный раствор:100 мл 20% ( v / v ) Водный раствор ТЭОА (pH =7)
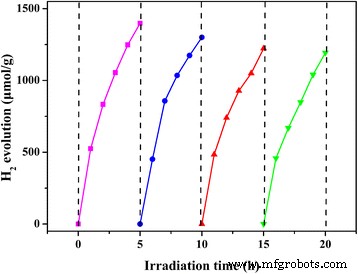
Циклический H 2 производство для G-C 3 N 4 /PtNi/GO-0.5% образец. Источник света:ксеноновая лампа 300 Вт (λ> 420 нм), реакционный раствор:100 мл 20% (об. / Об.) Водного раствора TEOA (pH =7), фотокатализатор, 50 мг, массовое отношение эозина Y к фотокатализатору составляет 1 :1
Чтобы исследовать механизм улучшенных фотокаталитических характеристик g-C 3 N 4 / PtNi / GO со сплавом PtNi в качестве сокатализатора, были оценены две возможные причины поглощения света и эффективности разделения заряда. На рисунке 7 показаны спектры диффузного отражения в УФ и видимой областях g-C 3 . N 4 /Ni/GO-0.5%, g-C 3 N 4 /Pt/GO-0.5% и g-C 3 N 4 /PtNi/GO-0.5% образцов. Три разных образца демонстрируют очевидное поглощение после примерно 450 нм, которое происходит от металлического сокатализатора [18]. G-C 3 N 4 Образец /Ni/GO-0,5% с чистым Ni в качестве сокатализатора показывает самое сильное поглощение примерно после 450 нм. Однако H 2 скорость эволюции g-C 3 N 4 /Ni/GO-0.5% выборка - самая низкая. Результат предполагает, что улучшенный H 2 эффективность эволюции не происходит из-за повышенного поглощения света.
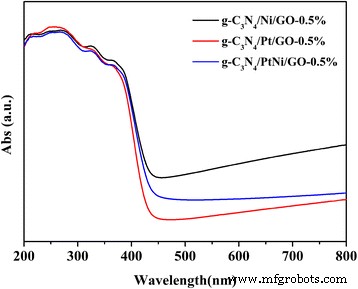
Спектры диффузного отражения в УФ и видимой областях g-C 3 N 4 /Ni/GO-0.5%, g-C 3 N 4 /Pt/GO-0.5% и g-C 3 N 4 /PtNi/GO-0.5% образцы
Эффективность разделения зарядов можно охарактеризовать по спектрам тушения фотолюминесценции (ФЛ) [46, 47]. В целом сильная интенсивность спектров ФЛ свидетельствует о серьезной рекомбинации носителей заряда. На рис. 8а показаны спектры тушения фотолюминесценции (ФЛ) эозина Y за счет g-C 3 N 4 /Ni/GO-0.5%, g-C 3 N 4 /Pt/GO-0.5% и g-C 3 N 4 /PtNi/GO-0.5% образцов. Только раствор Eosin Y без фотокатализатора демонстрирует обширный пик эмиссии около 540 нм из-за структуры конъюгированного ксантена Eosin Y и сильной рекомбинационной способности фотогенерированных электронно-дырочных пар в возбужденном Eosin Y. Очевидное гашение флуоресценции наблюдается после добавления в него фотокатализаторов различного типа. раствор Eosin Y. Тушение флуоресценции предполагает, что электроны передаются фотокатализаторам от возбужденного эозина Y, а затем мигрируют в сокатализатор для восстановления протонов. Кроме того, наблюдается небольшой синий сдвиг (примерно 1,3 нм) спектров тушения ФЛ для трех различных оцененных композитных фотокатализаторов, который можно отнести к нековалентному π-π-стэкинговому взаимодействию между Eosin Y, gC 3 N 4 и GO [48]. Спектры тушения ФЛ g-C 3 N 4 Образец /Pt/GO-0.5% показывает умеренную интенсивность, которая ниже, чем g-C 3 N 4 /Ni/GO-0.5% проба. Важно отметить, что g-C 3 N 4 Образец /PtNi/GO-0,5% демонстрирует самую низкую интенсивность флуоресценции, что означает, что сокатализатор из сплава PtNi является наиболее эффективным сокатализатором для повышения эффективности разделения заряда, чем чистые Pt или Ni. Результат согласуется с активностью выделения H2 (см. Рис. 4). Для дополнительной проверки процесса переноса заряда, переходные реакции фототока g-C 3 N 4 /Ni/GO-0.5%, g-C 3 N 4 /Pt/GO-0.5% и g-C 3 N 4 Были измерены образцы /PtNi/GO-0,5%, результаты показаны на рис. 8b. G-C 3 N 4 Образец /PtNi/GO-0,5% демонстрирует самый высокий отклик фототока при облучении видимым светом (λ> 420 нм), что дополнительно подтверждает, что использование сокатализатора из сплава PtNi необходимо для повышения эффективности разделения заряда. Основываясь на приведенных выше результатах, улучшенная активность выделения H2 для сенсибилизированного эозином Y g-C 3 N 4 Композитный материал /PtNi/GO-0.5% обеспечивает повышенную эффективность разделения заряда.
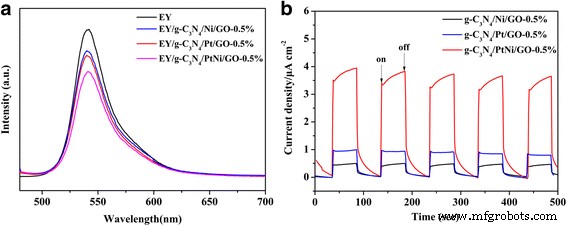
а Спектры тушения фотолюминесценции (ФЛ) g-C 3 N 4 /Ni/GO-0.5%, g-C 3 N 4 /Pt/GO-0.5% и g-C 3 N 4 /PtNi/GO-0,5% образцов в 20% (об. / Об.) Водном растворе TEOA (pH =7). Раствор эозина Y:0,01 мМ ( b ) Переходные реакции фототока g-C 3 N 4 /Ni/GO-0.5%, g-C 3 N 4 /Pt/GO-0.5% и g-C 3 N 4 /PtNi/GO-0.5% образцы
Согласно приведенным выше результатам и анализу механизма, мы предлагаем схематическую диаграмму для понимания H 2 процесс эволюции сенсибилизированного эозином Y g-C 3 N 4 Композитный образец / PtNi / GO (рис.9). При облучении видимым светом фотогенерированные электроны в НСМО возбужденного эозина Y переходят на g-C 3 N 4 и / или GO, а затем к сокатализатору из сплава PtNi для восстановления протонов. Между тем фотовозбужденные электроны в КП g-C 3 N 4 также поступают в сокатализатор из сплава PtNi для H 2 реакция эволюции. В то же время фотогенерированные дырки или окисленные красители Eosin Y непосредственно окисляют жертвенный агент TEOA.
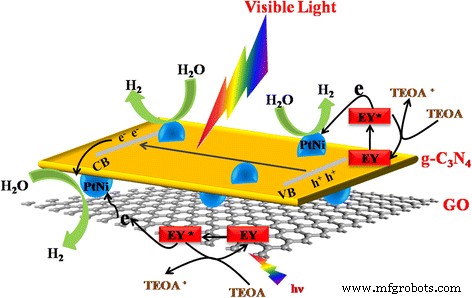
Принципиальная схема H 2 процесс эволюции сенсибилизированного эозином Y g-C 3 N 4 / PtNi / GO композитный образец при облучении видимым светом
Заключение
Тернарный g-C 3 N 4 Композит / PtNi / GO был синтезирован путем сочетания легкого жидкофазного сонохимического метода с методом химического восстановления. Сенсибилизированный эозином Y g-C 3 N 4 Композит /PtNi/GO-0.5% показывает самую высокую скорость выделения водорода 5,89 ммоль г -1 . ч −1 , что примерно в 1,54 и 1178 раз выше, чем у сенсибилизированного эозином Y g-C 3 N 4 /Pt/GO-0.5% и g-C 3 N 4 /Ni/GO-0.5% соответственно. Повышенная фотокаталитическая активность может быть приписана положительному синергетическому эффекту между Pt и Ni, а также более активным центрам, что приводит к эффективному разделению фотовозбужденных электронно-дырочных пар. Это исследование демонстрирует, что сплав PtNi может использоваться в качестве экономичного и эффективного сокатализатора для фотокаталитического выделения водорода.
Наноматериалы
- MoS2 с контролируемой толщиной для электрокаталитического выделения водорода
- Композиты с квантовыми точками на S, N-графене / TiO2 для эффективного фотокаталитического производства водород…
- Углеродные наноточки как двухрежимные нанодатчики для селективного обнаружения перекиси водорода
- Определение перекиси водорода на основе модификации внутренней поверхности твердотельных нанопор
- Температурная кристаллизация нанофлексов MoS2 на графеновых нанолистах для электрокатализа
- Гидротермальный синтез наночастиц In2O3, гибридные двойники, гексагональные дисковые гетероструктуры ZnO для по…
- Исследование каркаса Zr – металл – органика как эффективного фотокатализатора для производства водорода
- Иерархическая гетероструктура полых сфер ZnO @ TiO2 для высокоэффективного фотокаталитического выделения водор…
- Видимые световые фотокаталитические характеристики нанокомпозитов ZnO / g-C3N4, легированных азотом
- Последовательно выращенный из пара гибридный перовскит для плоских солнечных элементов с гетеропереходом



