Углеродные наноточки как двухрежимные нанодатчики для селективного обнаружения перекиси водорода
Аннотация
Перекись водорода (H 2 О 2 ) является важным продуктом ферментативных реакций на основе оксидазы, таких как реакция глюкоза / глюкозооксидаза (GOD). Следовательно, зондирование сгенерированного H 2 О 2 для достижения обнаружения различных углеводов и их оксидаз очень важно. Здесь мы сообщаем об одном виде углеродных наноточек с двойным излучением (CD), которые могут служить в качестве новых двухрежимных наносенсоров с флуорометрическим и колориметрическим выходом для селективного обнаружения H 2 О 2 . Двухмодельные наносенсоры устанавливаются только на недекорированных компакт-дисках с двойной эмиссией, на которых наблюдаются значительные флуорометрические и колориметрические изменения при добавлении различных концентраций H 2 О 2 в решении для компакт-дисков, что способствует обнаружению H 2 невооруженным глазом. О 2 . Механизм действия наносенсоров можно объяснить тем фактом, что внешние химические стимулы, такие как гидроксильные радикалы из H 2 О 2 вызывают изменение свойств поверхности и агрегацию компакт-дисков, которые доминируют в излучении и поглощении компакт-дисков. Созданные двухрежимные наносенсоры обладают хорошей биосовместимостью и высокой селективностью по отношению к H 2 . О 2 с линейным диапазоном обнаружения от 0,05 до 0,5 M и позволяют обнаруживать H 2 О 2 всего 14 мМ.
Фон
Флуоресцентные углеродные наноточки (CD) привлекли внимание исследователей из-за их уникальных физико-химических свойств, таких как хорошая биосовместимость, низкая токсичность, настраиваемая фотолюминесценция (PL) и высокий квантовый выход. Из-за вышеперечисленных символов компакт-диски нашли потенциальное применение в различных областях, включая, помимо прочего, биоимиджинг, биосенсоры и светоизлучающие устройства [1,2,3,4,5,6,7,8,9]. Более того, из-за их способности повышающего и понижающего преобразования, отсутствия оптического мерцания и высокой фотостабильности по сравнению с органическими красителями или полупроводниковыми квантовыми точками (КТ) компакт-диски более подходят для применения в флуоресцентных наносенсорах за счет увеличения или гашения флуоресценции [10 , 11,12,13,14,15,16,17,18,19].
Перекись водорода (H 2 О 2 ) - это один из распространенных окислителей, который всегда используется в качестве медицинского дезинфицирующего средства для стерилизации. Кроме того, H 2 О 2 также является важным продуктом ферментативных реакций на основе оксидазы, таких как реакция глюкоза / глюкозооксидаза (GOD). Следовательно, стратегия зондирования посредством зондирования H 2 О 2 может быть использован как перспективный подход для обнаружения углеводов и их оксидаз. По этой причине обнаружение H 2 О 2 может использоваться для наблюдения за заболеваниями углеводного обмена, такими как диабет. В настоящее время, хотя различные сенсоры глюкозы, основанные на определении H 2 О 2 были разработаны с использованием различных аналитических методов, ранее описанные сенсорные системы в основном основаны на одном сигнале, таком как кондуктометрические, флуорометрические или колориметрические изменения [20,21,22]. В последнее время достижения в области нанотехнологий, особенно в области флуоресцентных наночастиц, таких как полупроводниковые квантовые точки и новые углеродные наночастицы, привели к появлению нового H 2 О 2 наносенсоры. Лу и др. разработали один вид микрогибридов с двойной эмиссией (DEMB), объединив квантовые точки CdTe и родамина для ратиометрического флуоресцентного определения глюкозы посредством мониторинга образования H 2 О 2 [20]. Zhang et al. сообщил о флуоресцентном наносенсоре, который показал селективный и чувствительный ответ на H 2 О 2 через тушение флуоресценции ЦД [21, 22]. Однако эти работы неизбежно привели к внутренним дефектам КТ на основе полупроводников с дорогими химическими составляющими и загрязнению тяжелыми металлами. Более того, наносенсоры, основанные на считывании одиночного сигнала, тушения флуоресценции или изменения цвета, могут иметь плохую стабильность анализа из-за колебаний факторов окружающей среды и ошибок экспериментальной работы. Учитывая вышеизложенное, мы хотим разработать новый класс флуоресцентных компакт-дисков, флуоресценция и цвет раствора которых очень чувствительны к изменению концентраций H 2 О 2 . Таким образом, на основе этих компакт-дисков может быть создан двухрежимный наносенсор для четкого и точного определения H 2 О 2 путем одновременной проверки флуорометрических и колориметрических изменений раствора CD, что полезно для реализации обнаружения H 2 невооруженным глазом О 2 .
В этом исследовании мы разработали простой и удобный метод синтеза компакт-дисков нового типа, которые демонстрируют темно-красный цвет раствора в видимом свете и двойное флуоресцентное излучение под УФ-лампой 365 нм (синее и зеленое флуоресцентное излучение). Компакт-диски просто синтезируются сольвотермическим методом с использованием лимонной кислоты, мочевины и N . , N -диметилформамид (ДМФ) в качестве источника углерода, источника азота и реакционного растворителя соответственно. Флуоресценция и цвет раствора очень чувствительны к изменению концентрации H 2 . О 2 . Таким образом, на основе этих компакт-дисков может быть создан двухрежимный наносенсор для четкого и точного определения H 2 О 2 путем одновременной проверки флуорометрических и колориметрических изменений раствора CD, что полезно для реализации обнаружения невооруженным глазом H 2 О 2 . Без внедрения каких-либо дорогостоящих инструментов на основе этих компакт-дисков был создан двухрежимный наносенсор. Эта сенсорная система может эффективно избежать потенциальных ошибок в работе и значительно повысить надежность измерения. Кроме того, наносенсоры на основе CD являются многообещающими в применении для определения уровня глюкозы в крови как in vivo, так и in vitro благодаря их хорошей биосовместимости и высокой растворимости в воде.
Методы
Синтез компакт-дисков
Компакт-диски были приготовлены с использованием сольвотермического метода с лимонной кислотой в качестве источника углерода, мочевиной в качестве источника азота и ДМФ в качестве сореагента. В типичном эксперименте лимонную кислоту (1 г) и мочевину (2 г) растворяли в 10 мл ДМФ. Затем раствор переносили в автоклав с поли (тетрафторэтиленом) объемом 25 мл и нагревали при 160 ° C в течение 4 часов. После реакции автоклав естественным образом охладили до комнатной температуры. Получился темно-красный раствор. Компакт-диски осаждали добавлением 5 мл реакционного раствора в 25 мл большого количества этанола и центрифугировали при 7500 об / мин в течение 30 минут. Затем осадок подвергали диализу для получения чистых CD. Приготовленные компакт-диски собирали и сушили в вакуумном сушильном шкафу при 60 ° C и менее 1 Па в течение 12 часов. Затем компакт-диски повторно растворяли в деионизированной воде с образованием 0,75 мг / мл -1 CD решение для дальнейших исследований. И последующие H 2 О 2 -обработанные компакт-диски были собраны и высушены тем же методом для определения морфологии поверхности и структурных свойств.
Измерения
Морфология поверхности компакт-дисков была охарактеризована с помощью просвечивающего электронного микроскопа высокого разрешения (HRTEM, JEOL JSM-IT100). Структурные свойства компакт-дисков определяли с помощью рентгеновского дифрактометра (XRD, PA National X’Pert Pro) и спектрометра микро-комбинационного рассеяния (Renishaw RM 2000). Спектры поглощения компакт-дисков измеряли на спектрофотометре Hitachi U-3900 UV-Vis-NIR. Спектры флуоресценции компакт-дисков измеряли на спектрофотометре (Hitachi F-7000). Квантовый выход флуоресценции CD был получен на спектрометре Horiba FL-322 с калиброванной интегрирующей сферой. Кривые затухания флуоресценции компакт-дисков были также измерены Horiba FL-322 с использованием 405-нм NanoLED, контролирующего излучение при 450 и 500 нм, соответственно. Инфракрасный спектр с преобразованием Фурье (FTIR) компакт-дисков записывали на спектрометре Bio-Rad Excalibur (Bruker Vector 22). Рентгеновская фотоэлектронная спектроскопия (XPS) была записана на рентгеновском фотоэлектронном спектрометре ESCALAB MK II с использованием Mg в качестве источника возбуждения.
Создание нанодатчиков компакт-диска
Для обнаружения H 2 О 2 , спектры флуоресценции и поглощения CD в присутствии H 2 О 2 были исследованы в буфере PBS (pH =7,4, при 25 ° C). В типичном эксперименте разное количество H 2 О 2 сначала смешивали с дистиллированной водой, а затем с 20 мкл 0,75 мг / мл -1 Раствор CD вводили в 4 мл H 2 . О 2 раствор с разной концентрацией (0, 0,05, 0,1, 0,15, 0,25, 0,5, 1,0 и 2,0 М). Затем были сделаны фотографии, спектры флуоресценции и поглощения после добавления компакт-дисков в H 2 О 2 решение.
Также оценивалась селективность наносенсоров на основе CD. Раствор CD (20 мкл, 3,75 мкг мл -1 ) смешивали с различными видами катионов и окислителей (4 мл, 0,1 М), а затем раствор встряхивали в течение 1 мин. Наконец, спектры поглощения и флуоресценции раствора в УФ-видимой области были записаны после того, как компакт-диски были добавлены в H 2 . О 2 решение.
Результаты и обсуждение
Описание компакт-дисков
Морфологию приготовленных компакт-дисков измеряли с помощью просвечивающего электронного микроскопа (ТЕМ). Как показано на рис. 1a, компакт-диски хорошо диспергированы с однородным диапазоном размеров 2,5–6,5 нм и средним диаметром около 5 нм (дополнительный файл 1:рисунок S1b). Кроме того, изображение ПЭМВР (вставка к рис. 1а) показывает дифракционные полосы около 0,21 нм, что согласуется с (100) графита. На дифрактограммах компакт-дисков, показанных на рис. 1b, наблюдается широкий пик около 23,4 °, который соответствует сильно разупорядоченным атомам углерода с графитоподобной углеродной структурой. Спектры комбинационного рассеяния компакт-дисков (рис. 1c) показывают две полосы:полосу D (около 1347 см -1 , что было связано с колебаниями sp 3 -гибридизированный углерод с дефектами и беспорядком) и полоса G (около 1577 см -1 , который был связан с E 2g режимы вибрации ИП 2 -гибридизированный углерод в двумерной гексагональной кристаллической структуре). Спектры FTIR компакт-дисков (рис. 1d) представляют широкие полосы поглощения колебаний O – H / N – H при 3100–3600 см −1 . , валентные колебания C =O / C =C в области 1690–1610 см −1 и валентные колебания N – O на отметке 1350–1390 см −1 . Приведенные выше данные показывают, что на поверхности компакт-дисков могут быть некоторые функциональные группы, и эти функциональные группы могут играть важную роль в высокой гидрофильности и стабильности компакт-дисков в водном растворе.
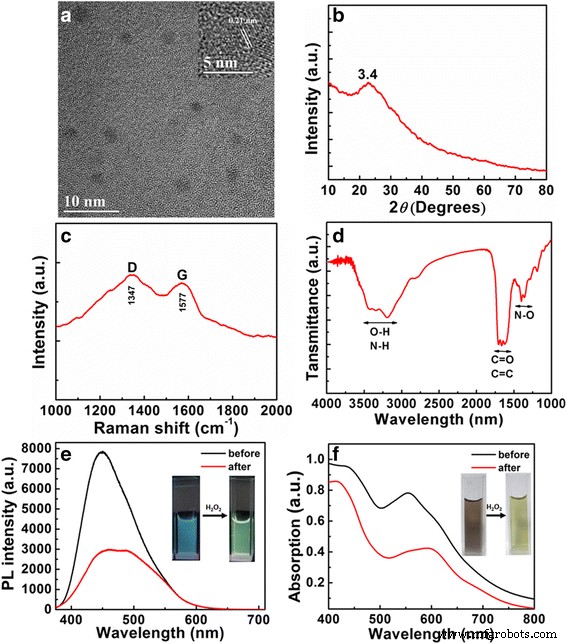
а ТЕМ-образ компакт-дисков. Вставки покажите изображения компакт-дисков в формате HRTEM. б Рентгенограмма компакт-дисков. c Рамановская спектроскопия компакт-дисков. г ИК-Фурье спектроскопия компакт-дисков. е Изменение флуоресценции CD после добавления 0,5 M H 2 О 2 . Вставки показать фотографии компакт-дисков до ( слева ) и после ( справа ) добавив H 2 О 2 под УФ-светом. е Колориметрическая вариация CD после добавления 0,5 M H 2 О 2 . Вставки показать фотографии компакт-дисков до ( слева ) и после ( справа ) добавив H 2 О 2 при дневном свете
Флуоресцентное поведение наносенсоров на основе CD по отношению к H 2 О 2 был измерен в водных растворах ЦД, показанных на рис. 1д. При возбуждении с одной длиной волны при 365 нм растворы CD демонстрируют асимметричные спектры излучения, которые можно сопоставить с флуоресцентными полосами с двойным излучением с центрами 450 и 500 нм, соответствующими синим и зеленым флуоресцентным полосам соответственно. Когда растворы CD смешиваются с H 2 О 2 , интенсивность синей полосы падает сильнее, чем зеленой. Соответственно, самые сильные выбросы компакт-дисков сдвигаются от 450 до 500 нм по результатам матриц возбуждения-излучения компакт-дисков после добавления H 2 О 2 (Дополнительный файл 1:Рисунок S2). В результате цвет флуоресценции растворов КД изменяется с синего на зеленый при освещении УФ лампой 365 нм (вставка к рис. 1д). Более того, растворы CD одновременно испытывают колориметрическое изменение с темно-красного на зеленый после добавления H 2 О 2 (вставка к рис. 1е). Это изменение цвета можно объяснить изменением интенсивности полос поглощения около 555 и 595 нм, вызванным добавлением H 2 О 2 в растворе КД (рис. 1е). Взятые вместе, эти результаты подтверждают, что компакт-диски можно использовать в качестве двухрежимного наносенсора для обнаружения H 2 О 2 .
Механизм распознавания
Чтобы исследовать механизм восприятия, морфологию и флуоресцентные свойства CD после добавления H 2 О 2 также были охарактеризованы. Как показано в Дополнительном файле 1:Рисунки S1a и S1c, добавление H 2 О 2 в раствор CD может привести к агрегации CD, размер которых составляет от 30 до 60 нм. H 2 О 2 -индуцированная агрегация CD также была выявлена в нормализованных спектрах поглощения (дополнительный файл 1:Рисунок S3); а именно, полоса поглощения КД сдвигается в красную сторону от 555 до 595 нм в видимой области [15]. Соответственно, цвет раствора КД изменяется от темно-красного до зеленого, а также состояние дисперсности КД, переходящее в состояние агрегации. Спектры XRD (рис. 1b и дополнительный файл 1:рисунок S4) компакт-дисков до и после добавления H 2 О 2 мало изменяются, что указывает на отсутствие изменений в кристаллической структуре компакт-дисков.
Эволюция флуоресценции свежеприготовленных компакт-дисков с добавлением H 2 О 2 исследовали по спектрам флуоресценции. Матрицы возбуждения-излучения показывают, что добавление H 2 О 2 изменяет центры эмиссии компакт-дисков с 450 до 500 нм (дополнительный файл 1:Рисунок S2). Кривые затухания флуоресценции, показанные на рис. 2а для компакт-дисков с излучением при 450 и 500 нм, могут быть хорошо аппроксимированы моноэкспоненциальной функцией затухания со средним временем жизни 7,96 и 7,12 нс соответственно (при возбуждении 365 нм). Напротив, время затухания флуоресценции компакт-дисков после H 2 О 2 обработка составила 4,53 и 4,83 нс (рис. 2б и таблица 1). Между тем, квантовый выход ФЛ ( η int ) компакт-дисков изменилось с 5,5 до 4,6%, когда H 2 О 2 был добавлен в раствор компакт-диска. Учитывая изменение времени жизни флуоресценции и квантового выхода ФЛ, можно сделать вывод, что перенос заряда (ПЗ) может происходить между КД и H 2 О 2 , что могло быть триггером для изменения спектров ФЛ компакт-дисков.
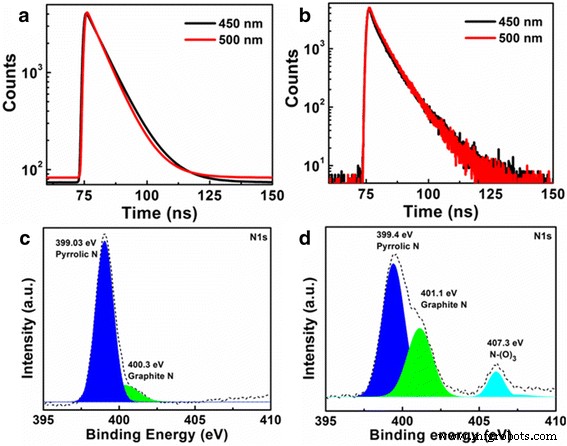
а , b Затухание флуоресценции компакт-дисков до ( a ) и после ( b ) добавляя 0,5 М H 2 О 2 . c , d XPS (N1s) компакт-дисков до ( c ) и после ( d ) добавляя 0,5 М H 2 О 2
Спектры FTIR и XPS компакт-дисков были измерены, чтобы дать представление о химическом составе и изменениях окружающей среды, вызванных H 2 О 2 . Спектры FTIR CD до и после добавления H 2 О 2 показано в Дополнительном файле 1:Рисунок S7 показывает, что валентные колебания N – O на отметке 1350–1390 см −1 увеличиваются с добавлением H 2 О 2 , что также подтверждается результатами РФЭС-спектров. Из полного обзора XPS-спектров (Дополнительный файл 1:Рисунок S8) видно, что отношение O к N компакт-дисков до и после H 2 О 2 курс лечения составил 1,57 и 3,85 соответственно. Увеличение отношения O / N показывает, что состояния связывания N в CD могут измениться с добавлением H 2 О 2 , что согласуется с XPS-спектрами высокого разрешения N1s, показанными на рис. 2в, г. По результатам XPS-спектров N1s, содержание графита N в компакт-дисках было увеличено с добавлением H 2 О 2 . Кроме того, есть дополнительный пик состояния N – O при 407,3 эВ в спектрах N1s после добавления H 2 О 2 , что явно демонстрирует, что импорт H 2 О 2 приводит к изменению поверхностных состояний в КД. Все исследования показывают, что кадр поверхности N может быть изменен добавлением H 2 O 2
Предыдущие сообщения предполагают, что полосы излучения CD связаны с поверхностными состояниями, такими как радикалы с примесью азота и группы мочевины [5, 9, 12, 23,24,25]. Между тем эти поверхностные состояния чувствительны к внешним физическим или химическим раздражителям. На основе фотофизического анализа и анализа окружающей среды на поверхности мы предлагаем механизм эволюции флуоресценции с введением H 2 О 2 (Рис. 3). Краевое состояние свежеприготовленных компакт-дисков состоит из конъюгированных пиррольных N-групп. Этот тип состояния N может быть в основном локализован на высоком энергетическом уровне. Таким образом, возбужденный электрон может безызлучательно релаксировать в высокоуровневое поверхностное состояние N, а затем излучательно переходить в основное состояние, сопровождаемое полосами излучения флуоресценции около 450 нм. Напротив, интенсивность флуоресценции раствора CD немного уменьшается из-за динамического тушения между H 2 О 2 и компакт-диски, где CT возникает между компакт-дисками и H 2 О 2 аналогично предыдущим отчетам [26,27,28,29]. В противном случае можно было бы сделать вывод, что радикалы флуоресценции с высокой энергией (связанное с ними состояние N) трансформируются в состояние с более низкой энергией N – O в результате воздействия гидроксильного радикала из H 2 О 2 . Таким образом, возбужденный электрон может в основном релаксировать с излучательным переходом из состояния N – O с более низкой энергией в основное состояние с зеленой полосой излучения при 500 нм, что также приводит к статическому тушению флуоресценции на 450 нм. Следовательно, основные полосы излучения компакт-дисков могут показывать изменение с синего излучения на зеленое.
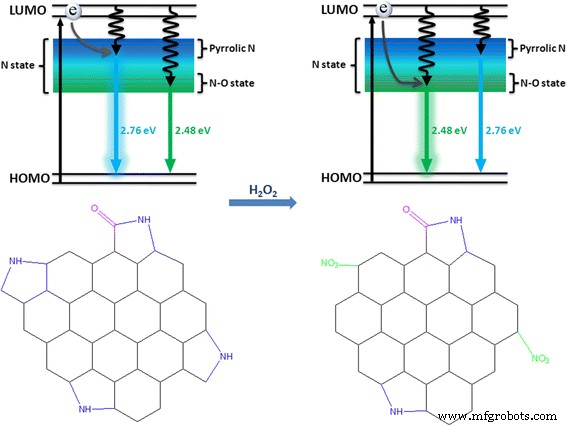
Возможный механизм распознавания компакт-дисков до ( слева ) и после ( справа ) добавление H 2 О 2
Оценка нанодатчиков компакт-дисков
На основе описанных выше флуоресцентных и колориметрических характеристик компакт-дисков мы разработали наносенсор для обнаружения H 2 О 2 на компакт-дисках. Предлагаемая сенсорная система состоит из компакт-дисков с надлежащей концентрацией в водном растворе (3,75 мкг мл -1 , Дополнительный файл 1:Рисунок S9), где компакт-диски выполняют двойную функцию как колориметрические, так и флуорометрические репортеры в этой системе.
Предлагаемая система наносенсинга на основе раствора CD проиллюстрирована на рис. 4. Флуорометрические и колориметрические изменения, вызванные H 2 О 2 может быть отчетливо визуализирована невооруженным глазом (рис. 4c, f), где ряд заметных изменений цвета от синего к зеленому и от темно-красного к зеленому можно наблюдать при УФ-свете и дневном освещении. Кроме того, добавление H 2 О 2 в раствор CD также можно выразить количественно с помощью спектров флуоресценции и поглощения (рис. 4a, d). Как показано на рис. 4а, полоса флуоресценции с центром при 450 и 500 нм постепенно уменьшается с увеличением H 2 О 2 концентрации от 0 до 2 М. Однако увеличение H 2 О 2 концентрация приводит к разному снижению интенсивности флуоресценции при 450 нм ( I 450 ) и 500 нм ( I 500 ), что хорошо согласуется с изменением цвета флуоресценции в растворе ЦД (рис. 4в). Следовательно, отношение интенсивности флуоресценции при 500 нм к интенсивности при 450 нм выбрано для контроля H 2 О 2 концентрации (рис. 4а, б). Более низкое отношение связано с синим излучением, в то время как зеленая флуоресценция может наблюдаться невооруженным глазом при более высоком соотношении I 500 Я 450 . Диапазон линейного обнаружения с помощью этих средств составляет от 0,05 до 0,5 M с линейной корреляцией R 2 =0,987. Точно так же колориметрическое изменение происходит в растворе ЦД из-за неоднородного уменьшения полосы поглощения при 555 и 595 нм. Как показано на рис. 4d, интенсивность поглощения уменьшается в видимой области, но увеличивается H 2 О 2 концентрация приводит к тому, что поглощение около 595 нм уменьшается медленнее, чем около 555 нм. Следовательно, коэффициент поглощения при 595 нм ( A 595 ) до 555 нм ( A 555 ) также можно использовать для измерения H 2 О 2 концентрация. Соотношение A 595 в A 555 экспоненциально возрастает от 0,05 до 2 M с экспоненциальной корреляцией R 2 =0,999, и изменение колориметра хорошо коррелирует с H 2 О 2 диапазон концентраций от 0,05 до 0,25 М с линейным пределом обнаружения (LOD) 14 мМ (дополнительный файл 1:рисунок S11 и таблица S1). Двухрежимные наносенсоры обладают надлежащей чувствительностью этого метода, удовлетворяющей клиническим и медицинским требованиям, благодаря концентрации H 2 О 2 через реакцию GOD в диапазоне миллимолярных (~ 10 мМ) в плазме [20]. Кроме того, двухрежимные наносенсоры имеют собственный встроенный эталон калибровки, поэтому колебания интенсивности и другие внешние факторы могут быть устранены, что способствует повышению точности тестирования.
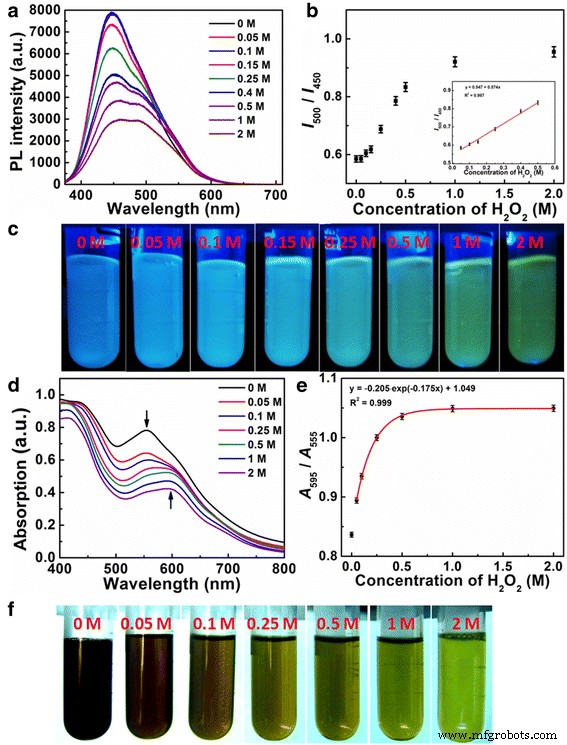
а Спектры флуоресценции CD в присутствии различных H 2 О 2 концентрации. б Калибровочная кривая I 500 / Я 450 компакт-дисков по сравнению с H 2 О 2 концентрация. Вставки показать линейную дальность обнаружения I 500 / Я 450 компакт-дисков по сравнению с H 2 О 2 концентрация. c Фотографические изображения флуоресцентного раствора CD при различных концентрациях H 2 О 2 . г УФ-видимые спектры компакт-дисков в присутствии различных H 2 О 2 концентрации. е Калибровочная кривая A 595 / А 555 компакт-дисков по сравнению с H 2 О 2 концентрация. е Фотографические изображения раствора КД при различных концентрациях H 2 О 2
Для оценки селективности наносенсоров по отношению к H 2 О 2 , анализы интерференции были выполнены в идентичных условиях с использованием некоторых общих катионов, таких как Na + , K + , NH 4+ , Ca 2+ , Zn 2+ , и Fe 2+ . Как показано на рис. 5a, b, флуорометрические и колориметрические изменения CD были исследованы в присутствии различных катионов. В присутствии Na + , K + , NH 4 + , Ca 2+ , Zn 2+ , и Fe 2+ , коэффициент флуоресценции I 500 Я 450 и коэффициент поглощения A 595 в A 555 появляются только как незначительные отклонения по сравнению с холостым образцом, что означает, что эти катионы мало влияют на обнаружение H 2 О 2 . Кроме того, мы также сравнили воздействие на компакт-диски с другими окислителями, такими как HNO 3 , KClO 3 , FeCl 3 , NaClO, K 2 Cr 2 О 7 , и KMnO 4 (Рис. 5c, d и Дополнительный файл 1:Рисунки S12 и S13), и мы обнаружили, что цвет флуоресценции изменяется с синего на зеленый при добавлении этих окислителей, кроме K 2 Cr 2 О 7 и КМно 4 . Итак, мы можем исключить вмешательство со стороны K 2 Cr 2 О 7 и КМно 4 через изменение флуоресценции. Кроме того, мы можем легко исключить влияние других окислителей, таких как HNO 3 , KClO 3 , FeCl 3 , и NaClO в результате коэффициента поглощения A 595 в A 555 . Следовательно, двухрежимные наносенсоры, продемонстрированные в этой статье, могут быть очень многообещающими с точки зрения высокой селективности определения из-за синергетического эффекта двух независимых методов обнаружения [30,31,32,33]. Кроме того, мы измерили время отклика флуорометрического изменения при добавлении H 2 О 2 и обнаружили, что флуоресценция уменьшается после введения H 2 О 2 и стабильно держится около 3,3 с (дополнительный файл 1:рисунок S14).
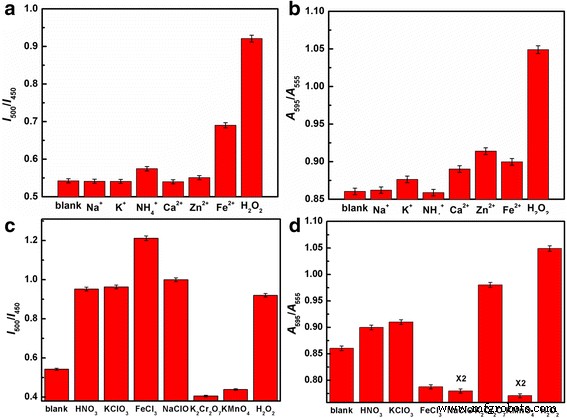
а , c Коэффициент флуоресценции I 500 / Я 450 раствора, содержащего компакт-диски и различные интерферентные катионы ( a ) и окислители ( c ). б , d Коэффициент поглощения A 595 / А 555 раствора, содержащего компакт-диски и различные интерферентные катионы ( b ) и окислители ( d )
Жизнеспособность клеток A549 исследовали с использованием стандартного анализа CCK-8 для оценки цитотоксичности CD. Как показано на рис. 6, мы обнаружили, что около 80% жизнеспособности достигается путем инкубации клеток A549 с CD в течение 48 часов даже при высокой концентрации CD, например 500 мкг мл
-1
. Подсчитано, что 50% ингибирующая концентрация (IC50) CD составляет около 1106 мкг / мл
-1
. с помощью GraphPad Prism 5.0, который определяет, что компакт-диски обладают хорошей биосовместимостью и очень низкой цитотоксичностью при высокой концентрации. Кроме того, мы сравнили аналитические характеристики наносенсоров, о которых сообщалось ранее, для H 2 О 2 определение показано в Дополнительном файле 1:Таблица S2. Биосовместимость, простота и визуализация обнаружения сопоставимы или даже лучше, чем у большинства из этих описанных H 2 О 2 анализы. Учитывая, что двухрежимные наносенсоры на основе компакт-дисков обладают хорошей селективностью по отношению к H 2 О 2 Обнаружение, надлежащий предел обнаружения (LOD =14 мМ) в том же порядке, что и уровень глюкозы в крови, и очень низкая цитотоксичность при высокой концентрации CD, наносенсоры многообещают для использования в тесте уровня глюкозы в крови и других клинических требованиях. / P> 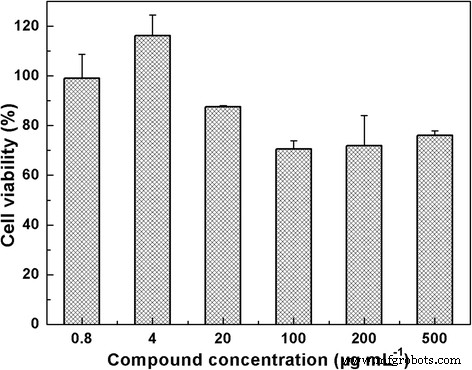
Жизнеспособность клеток A549 после 48-часовой инкубации при различных концентрациях CD
Выводы
В заключение мы предлагаем двухрежимный наносенсор на основе компакт-дисков с колориметрическим и флуорометрическим выходом для количественного определения H 2 О 2 на основе флуорометрического и колориметрического изменения раствора CD при введении H 2 О 2 . Наносенсоры просты и удобны для обнаружения невооруженным глазом для H 2 О 2 . Механизм действия наносенсоров можно объяснить тем фактом, что внешние химические стимулы, такие как гидроксильные радикалы из H 2 О 2 вызывают изменение свойств поверхности и агрегацию компакт-дисков, которые доминируют в излучении и поглощении компакт-дисков. Предлагаемые наносенсоры обладают хорошей биосовместимостью, высокой селективностью по отношению к H 2 . О 2 с линейным диапазоном обнаружения от 0,05 до 0,5 М и пределом обнаружения около 14 мМ, что сопоставимо с уровнем H 2 О 2 произведенные реакциями БОГА. Считается, что стратегия, описанная в этой статье, может обеспечить многообещающий подход к разработке нового датчика уровня глюкозы в крови, который может быть ценным для диагностики заболеваний и тестирования окружающей среды.
Наноматериалы
- Устройства из углеродного волокна для вашего дома
- Инновационные способы использования углеродного волокна
- 5 забавных вариантов использования листов из углеродного волокна
- Для чего используется обертка из углеродного волокна?
- MoS2 с контролируемой толщиной для электрокаталитического выделения водорода
- Графен и полимерные композиты для суперконденсаторов:обзор
- Определение перекиси водорода на основе модификации внутренней поверхности твердотельных нанопор
- Новый магнитоупругий нанобиосенсор для высокочувствительного обнаружения атразина
- Фотоприемники из кремния с резонансной полостью для поляриметрического обнаружения в ближнем инфракрасном …
- Трехмерный каркас из нанопроволоки из нитрида углерода для гибких суперконденсаторов



