Оценка биоразложения поли (молочной кислоты), наполненного функционализированными наночастицами титана (PLA / TiO2), в условиях компоста
Аннотация
В этой статье представлено исследование биодеградации, проведенное в течение 90 дней в стандартных контролируемых условиях компостирования поли (молочной кислоты) (PLA), наполненного функционализированным нанонаполнителем анатаза и диоксида титана (PLA / TiO 2 нанокомпозиты). Морфология поверхности, термические свойства, процент биодеградации и изменения молекулярной массы в разное время инкубации оценивались с помощью визуального осмотра, сканирующей электронной микроскопии (SEM), дифракции рентгеновских лучей (XRD), дифференциальной сканирующей калориметрии (DSC) и проницаемости геля. хроматография (GPC) путем взятия образцов деградированного компоста в конце заданного интервала времени биоразложения. Быстрое увеличение кристалличности показало, что PLA и PLA / TiO 2 нанокомпозиты обладают гетерогенными механизмами разложения в контролируемых условиях компостирования. Скорость биоразложения PLA / TiO 2 нанокомпозитов был выше, чем у чистого PLA, потому что молекулы воды легко проникали в нанокомпозиты. Дисперсия наночастиц в PLA / TiO 2 нанокомпозиты влияли на скорость биодеградации PLA. Более того, биоразложение PLA можно контролировать, добавляя некоторое количество диспергированного TiO 2 нанонаполнители в контролируемых условиях компостирования.
Введение
Поли (молочная кислота) (PLA), синтетический биоразлагаемый полимер, исследуется во всем мире для биомедицинских и потребительских приложений из-за растущей потребности в возобновляемых материалах, которые являются устойчивыми альтернативами продуктам, полученным из нефтехимии [1,2,3,4]. PLA - это продукт, который получается в результате полимеризации лактида или молочной кислоты, которая является наиболее широко производимой карбоновой кислотой в природе путем микробной ферментации углеводов [5]. Однако применение PLA относительно ограничено, поскольку его температура тепловой деформации, ударная вязкость и скорость разрушения неудовлетворительны [6, 7]. Один из методов устранения этих недостатков - модифицировать PLA путем добавления неорганических наночастиц, включая типичную наноглину, углеродные нанотрубки, оксид цинка и анатаз (A-TiO 2 ) [8,9,10,11,12,13,14,15]. Недавно PLA / TiO 2 нанокомпозиты были получены нами путем плавления смешения PLA с химически модифицированным TiO 2 (раствор молочной кислоты с привитым TiO 2 , в дальнейшем именуемый g-TiO 2 ) [16]. Результаты показали, что TiO 2 наночастицы оказали значительное влияние на улучшение механических свойств PLA / TiO 2 смеси, такие как деформация при разрыве и эластичность, по сравнению с чистым PLA. В то же время g-TiO 2 наночастицы оказали сильное влияние на гидролитическую деградацию и фотодеградацию PLA [17, 18].
Изучение биоразлагаемости и механизма биоразложения биоразлагаемых материалов с использованием лабораторных испытаний является чрезвычайно важным методом с промышленной и научной точки зрения, который обеспечивает понимание срока службы этих материалов [15]. В настоящее время доступно несколько методов оценки биоразлагаемости биоразлагаемых материалов, которые, как правило, основаны на косвенных измерениях, таких как производство углекислого газа, производство биогаза или потребление кислорода [19, 20].
Характеристики биоразложения PLA в компосте были изучены и опубликованы [21,22,23]. Компостирование - это ускоренное биоразложение органических материалов в теплой, влажной и аэробной среде в сочетании с микробной популяцией и контролируемыми условиями компостирования [24, 25]. Более того, биодеградация PLA в условиях компостирования, процесс, зависящий от температуры и влажности, включает несколько процессов, а именно поглощение воды, расщепление сложного эфира, а также образование и растворение фрагментов олигомеров [26]. Наиболее распространенный механизм биодеградации PLA включает двухэтапный процесс разложения. Первоначально тепло и влага в компосте атакуют цепи PLA и расщепляют их, образуя полимеры с небольшой молекулярной массой и, в конечном итоге, молочную кислоту. После этого микроорганизмы в компосте и почве минерализуют олигомерные фрагменты и молочную кислоту с образованием метана и диоксида углерода (CO 2 ) в анаэробных и аэробных условиях соответственно [27,28,29].
В последнее время влияние наполнителей на биодеградацию PLA привлекло большое внимание, и особое внимание было сосредоточено на нанонаполнителях, таких как наноглины, углеродные нанотрубки и гидроксиапатит [23, 30, 31, 32, 33, 34, 35, 36, 37,38]. Некоторые авторы [32,33,34] обнаружили, что добавление наночастиц может ускорить биодеградацию PLA, что объясняется высокой относительной гидрофильностью наночастиц, что обеспечивает легкую проницаемость воды в полимерную матрицу и запускает гидролитическую деградацию. Однако в других исследованиях [35,36,37,38] сообщается, что биодеградация замедляется из-за улучшенных барьерных свойств нанокомпозитов.
Несмотря на то, что в некоторых публикациях основное внимание уделялось биоразложению материалов PLA, роль TiO 2 играет в деградацию PLA остается спорным. Как появился TiO 2 Наночастицы влияют на биодеградацию PLA, пока не ясно. Итак, исследование биодеградации PLA, модифицированного TiO 2 нанонаполнители в состоянии компоста по-прежнему необходимы. Текущее исследование, основанное на оценке эволюционирующего CO 2 , оценили биоразложение PLA / TiO 2 нанокомпозиты широко в контролируемых лабораторных условиях компоста, дополняют способность PLA / TiO 2 разлагаться нанокомпозиты в различных условиях разложения могут расширить использование PLA в различных конечных приложениях в будущем.
Методы
Материалы
PLA (производство Natureworks @ (4032D)) показал средневесовую молекулярную массу (Mw) 19 600 кДа и полидисперсность 1,89, как определено с помощью гель-проникающей хроматографии (GPC). PLA сушили при 65 ° C в течение 24 ч при пониженном давлении и хранили в вакууме с поглотителем влаги перед использованием. Молочную кислоту (88%, Guangshui National Chemical Co.) перегоняли при 80 ° C для удаления воды перед использованием. Наночастицы диоксида титана анатаза со средним размером первичных частиц прибл. 20 нм, поставлялись Pangang Co., Ltd. Толуол и хлороформ использовали в полученном виде. Микрокристаллическая целлюлоза хроматографической чистоты была поставлена Shanghai Chemical Reagent Co., Ltd. CPPIA).
Подготовка образца
Подробная информация о функционализации TiO 2 наночастицы и получение PLA / TiO 2 о нанокомпозитах [16]. G-TiO 2 нанонаполнители получали путем прививки олигомера молочной кислоты на поверхность анатаза. PLA / TiO 2 нанокомпозиты были получены смешиванием расплава с помощью вращающегося двухшнекового экструдера. Чистый PLA был подвергнут такой же обработке смешиванием, чтобы иметь такую же термическую историю, что и нанокомпозиты. Образцы с 0, 0,5, 1,0, 2,0, 5,0, 8,0 и 15,0 мас.% G-TiO 2 были приготовлены и обозначены как PLA, PLA / TiO 2 –0,5, PLA / TiO 2 –1, PLA / TiO 2 –2, PLA / TiO 2 –5, PLA / TiO 2 –8 и PLA / TiO 2 –15 нанокомпозитов.
Небольшие образцы микросхем PLA и g-TiO 2 при различных соотношениях были преобразованы в листы толщиной приблизительно 0,5 мм путем прессования при 190 ° C в течение 4 минут под давлением 10 МПа с последующим охлаждением при комнатной температуре в течение 5 минут под давлением 5 МПа. После этого отформованные под давлением образцы разрезали на размер 5 мм × 5 мм и взвесили.
Тесты на деградацию
Испытание на биоразложение проводилось в лабораторном масштабе на основе стандартных методов испытаний, разработанных для биоразлагаемых пластиков (GB / T19277–2003 / ISO 14855-1:2005) (определение предельной аэробной биоразлагаемости пластиковых материалов в контролируемых условиях компостирования - метод путем анализа образовавшегося CO 2 ). Большая часть углерода в метаболизируемых субстратах генерирует энергию за счет химического превращения в CO 2 в аэробных средах [39]. Следовательно, измерения генерации CO 2 считаются наиболее подходящей мерой биоразложения в большинстве случаев. Стандарт определяет процедуру определения максимальной аэробной биоразлагаемости путем измерения количества выделившегося CO 2 и процент степени биоразложения исследуемых материалов в контролируемых условиях компостирования. Инокулят для компостирования получали из органической фракции ТБО, которую просеивали до размеров менее 5 мм. После этого мелкую фракцию использовали в качестве посевного материала. В таблице 1 показаны определенные физико-химические свойства посевных материалов для компостирования. В каждом тесте в серию реакторов для компостирования (каждый образец в трех экземплярах) загружали 15 г контрольного материала (например, микрокристаллической целлюлозы (MCE), что было рекомендовано стандартом) или исследуемого материала (каждая пленка взвешивалась и помечалась ранее. деградации), 85 г посевного материала и 320 г сухого морского песка (обеспечивает хорошие однородные условия и улучшенную аэробную среду внутри посевного материала). После этого реакторы помещали в инкубатор без света при 58 ± 2 ° C на время эксперимента 90 дней. Аэрация была инициирована насыщенным водой CO 2 -бесплатный воздух; скорость потока через каждый реактор была установлена на уровне 25 мл · мин -1 . Влажность, перемешивание и аэрация во всех реакторах контролировались в соответствии с требованиями GB / T19277–2003 / ISO 14855-12,005. В определенное время отбирали от трех до четырех образцов каждого образца, промывали дистиллированной водой и сушили при комнатной температуре не менее 24 часов до постоянного веса.
СО 2 образовавшиеся в процессе биодеградации улавливались растворами NaOH и измерялись через регулярные промежутки времени с помощью метода титрования. NaOH титровали стандартным раствором HCl до конечной точки фенолфталеина. Общий CO 2 количество выделившихся во время биодеградации рассчитывали относительно контрольной колбы. Данные, представленные для каждого образца, представляют собой среднее значение, полученное для трех образцов.
Характеристика
Исследование под микроскопом
Изображения, полученные с помощью сканирующей электронной микроскопии (СЭМ), получали с использованием прибора Philips FEI INSPECT F, работающего при 5 кВ. Перед анализом все образцы были покрыты золотом.
Термический анализ
Тепловые свойства образцов изучали методом дифференциальной сканирующей калориметрии (ДСК) (TA Q20, TA Instruments). Термограммы были получены в потоке азота (50 мл / мин) при скоростях нагрева и охлаждения 10 ° C / мин в диапазоне температур от комнатной до 200 ° C и от 200 до - 50 ° C соответственно.
Исследования XRD
Рентгеноструктурный анализ (XRD) проводили с использованием рентгеновского дифрактометра DX-1000 (Dandong Fanyuan Instrument Co. LTD. Китай), оборудованного Cu K α ( λ =0,154 нм) источника. Генератор работал при 25 мА и 40 кВ. Образцы сканировали под разными углами (т. Е. От 2 до 70 °) со скоростью сканирования 6 ° / мин.
Определение процента биоразложения ( D т ,%)
Процент биоразложения ( D т ,%) можно рассчитать по формуле. 1, который был принят как для уравнения. 2 [1, 40].
$$ {D} _t \ left (\% \ right) =\ frac {{\ left ({\ mathrm {CO}} _ 2 \ right)} _ T - {\ left ({\ mathrm {CO}} _ 2 \ right )} _ B} {{\ mathrm {Th}} _ {\ mathrm {CO} 2}} \ times 100 $$ (1)где (CO 2 ) Т количество CO 2 (в г / колбу) выделился из исследуемых материалов, (CO 2 ) B количество CO 2 (в г / колбу) выделяется в контрольной колбе, и Th CO2 это теоретический CO 2 количество произведенных полимерных материалов.
Теоретический CO 2 количество, которое может быть произведено в каждой колбе (Th CO2 , г 2 / г образца) рассчитывали по следующей формуле:
$$ {\ mathrm {Th}} _ {\ mathrm {CO} 2} ={M} _ {\ mathrm {TOT}} \ times {C} _ {\ mathrm {TOT}} \ times \ frac {44} {12} $$ (2)где M TOT - общий вес (г) сухого полимерного твердого материала, добавленного в колбу для компостирования в начале эксперимента, C TOT - это масса (г) общего органического углерода в общем количестве сухих полимерных твердых веществ в образце, а 44 и 12 - молекулярная масса CO 2 и атомная масса C соответственно.
Измерение молекулярной массы
Молекулярные массы нанокомпозитов PLA до и после компостирования определялись методом ГПХ. Система ГПХ была оборудована насосом для изократической ВЭЖХ Waters 1515, детектором показателя преломления Waters 2414 и автоматическим пробоотборником Waters 717 plus. Хлороформ использовали в качестве элюента со скоростью потока 0,8 мл / мин при 30 ° C. Калибровка проводилась по стандартам из полистирола.
Результаты и обсуждение
Деградация полимера связана с изменением характеристик, таких как цвет, морфология поверхности и механические свойства. Временные изменения внешнего вида чистого PLA и PLA / TiO 2 нанокомпозиты были разными в лабораторных условиях. Поверхность чистой матрицы PLA, которая изначально была прозрачной в соответствии с аморфной структурой, стала относительно беловатой через 2 дня биодеградации [41]. Эта особенность увеличивалась с увеличением времени инкубации до полной непрозрачности через 10 дней. Бляшки от желтого до темно-коричневого цвета, вызванные проникновением воды и инкубацией микроорганизмов, начали наблюдаться на поверхности чистой поверхности пленок PLA через 30 дней. Однако через 6 дней на поверхности нанокомпозита PLA появилась большая площадь темно-коричневых бляшек (рисунок не показан). Коричневые пятна указывают на колонии микроорганизмов, а трещины представляют собой эффект биоразложения. На рисунке 1 показана морфология поверхности PLA и его TiO 2 . нанокомпозиты под наблюдением СЭМ. Перед деградацией поверхность чистая и PLA / TiO 2 нанокомпозиты были гладкими. Чистый PLA не вызывал значительных изменений на поверхности после 5 дней биоразложения в условиях компоста. Через 20 дней шероховатость поверхности чистого PLA увеличилась (рис. 1а, а ’). Однако PLA / TiO 2 нанокомпозит демонстрирует прогрессивные изменения, ясно показывая, что значительная деградация PLA / TiO 2 сложный произошел. На поверхности нанокомпозитов наблюдались явные трещины и пустоты (рис. 1b, b ’; c, c’; и d, d ’; соответственно). Это могло быть связано с гидролизом PLA и активностью микроорганизмов. По мере увеличения времени инкубации трещины и пустоты становились существенно глубокими и большими (рис. 1 b ’, c’ и d ’, соответственно), тем самым предполагая потерю цепи и поверхностную эрозию с течением времени. Явление объемной эрозии для всех исследуемых материалов было аналогично процессу гидролитического разложения PLA и PLA / TiO 2 нанокомпозиты [17].

СЭМ-фотография поверхности чистого PLA ( a 0 , а , a ’ ), PLA / TiO 2 –2 ( b 0 , b , b ’ ), PLA / TiO 2 –5 ( c 0 , c , c ’ ) и PLA / TiO 2 –8 ( д 0 , d , d ’ ) нанокомпозитов как функция времени инкубации. а 0 , b 0 , c 0 , d 0 :0 день; а , b , c , d :5 дней; а ' , b ’ , c ’ , d ’ :20 дней
Для оценки кристалличности PLA и PLA / TiO 2 нанокомпозитов во время биодеградации, образцы, отобранные в разное время инкубации, были проанализированы на их термические свойства (рис. 2 и 3). На рис. 2 показано, что температура стеклования ( T г ) немного уменьшился для всех образцов со временем деградации. Уменьшение T г очевидно, из-за повышенной подвижности молекул в результате процесса гидролиза и пластифицирующего действия фрагментов олигомера и воды во время биодеградации [33, 42]. Исчезновение пика холодной кристаллизации ( T копия ) для всех образцов только через 2 дня можно было объяснить гидролизом PLA и быстрым увеличением кристалличности полимерной матрицы [43]. Уменьшение T м было приписано быстрое снижение молекулярной массы [44, 45]. Бимодальный пик плавления постепенно сменялся мономодальным пиком, тем самым подразумевая, что маленькие и несовершенные кристаллы исчезали со временем разложения. Этот результат доказал, что разложение PLA происходило быстро в аморфных областях на ранней стадии разложения в контролируемых условиях компостирования. Сканирование при охлаждении (см. Рис. 3) показывает, что пик кристаллизации чистого PLA постепенно увеличивается. Однако пики кристаллизации PLA / TiO 2 количество нанокомпозитов первоначально значительно увеличилось, а затем немного уменьшилось с увеличением времени инкубации. Причем, чем выше было содержание нанонаполнителей, тем раньше пики кристаллизации достигли своего пика. Уменьшение пика кристаллизации дополнительно подтвердило, что кристаллическая область начала разрушаться после разрушения аморфной области. Джулиана и Роберто [42] сообщили, что за короткие промежутки времени для образца PLA некоторые аморфные области превращаются в кристаллы, затем степень кристалличности увеличивается из-за эффекта эрозии аморфных частей. Более того, кристаллические области в течение длительного времени подвергаются гидролизу.
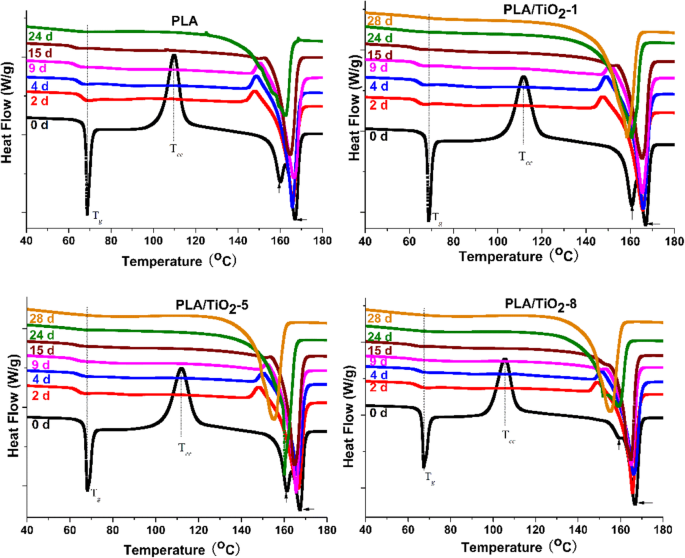
Термограммы ДСК продуктов биоразложения чистого PLA и PLA / TiO 2 нанокомпозиты в разное время инкубации, первое сканирование при нагревании
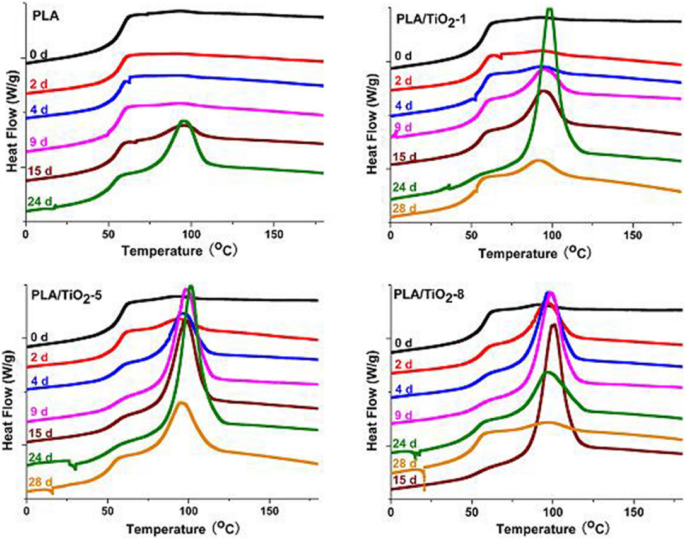
Термограммы ДСК биоразложенного чистого PLA и PLA / TiO 2 нанокомпозиты в разное время инкубации, сканирование при охлаждении
XRD представляет собой идеальный метод для отслеживания изменений кристаллизации полимеров во время разложения. Картины XRD PLA и его нанокомпозитов (рис. 4) показывают, что полимерная матрица сохраняет аморфную структуру до биоразложения. Только через 2 дня два сильных пика на 2 θ =16,4, 18,5 °, 20,9 ° и 23,6 °, и их интенсивность увеличивалась со временем инкубации. Этот результат означал формирование кристаллических структур поли (L-лактида) или поли (D-лактида) типа [46, 47]. Изменение кристаллического пика указывает на то, что аморфные области разлагаются быстрее, чем кристаллические области, что увеличивает значение отношения кристаллических и аморфных областей. Этот результат соответствовал результатам ДСК и изменению прозрачности образцов.
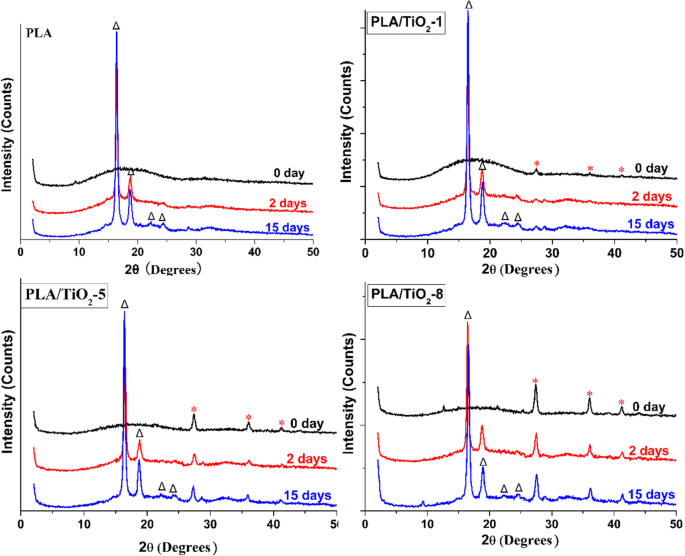
Картины XRD чистого PLA и PLA / TiO 2 нанокомпозиты в разное время инкубации
Оценка валидации инокулята имеет решающее значение во время биоразложения в условиях компостирования. Активность посевного материала измеряли, как требуется, стандартным методом: D т стандартного материала должно составлять не менее 70% в конце 45 дней тестирования. Вставка на рис. 5 показывает, что MCE начинает биоразлагаться через 5 дней, а процент биоразложения достигает 72% в конце 45 дней инкубации. Эти результаты показали, что MCE в эксперименте был эффективным в качестве справочного материала. В эксперименте дублированные емкости для компостирования показали хорошую воспроизводимость (стандартное отклонение ± 1,3%). На рисунке 5 показан D . т для чистого PLA и PLA / TiO 2 нанокомпозиты во время инкубации. Аналогичное поведение наблюдалось для PLA и PLA / TiO 2 . нанокомпозитов, то есть сначала наблюдалась лаг-фаза, за которой следует резкое линейное увеличение биоразложения, а затем фаза плато для всех образцов. Крутизна увеличения должна указывать на усиление деградации. Однако кривые показали, что лаг-фаза нанокомпозитов была немного короче, чем у чистого PLA. Этот результат указывает на присутствие TiO 2 , в некоторой степени, ускоряет начальную фазу разложения и увеличивает процентное содержание CO 2 производится в конце инкубационного периода. После 80 дней инкубации в контролируемых условиях компостирования D т для PLA, PLA / TiO 2 –1, PLA / TiO 2 –2, PLA / TiO 2 –5, PLA / TiO 2 –8 и PLA / TiO 2 –15 достигло 78,9, 86,9, 92,0, 97,8, 91,3 и 85,0% соответственно. Куниока и др. [48] сообщили, что окончательная биоразлагаемость PLA составила 80%. Результаты нашего эксперимента показали, что D т коммерчески чистого продукта PLA также составляла почти 80% в конце 80 дней. Уменьшение D т начиная с PLA / TiO 2 –8 приписывается интенсивной агломерации TiO 2 при его содержании более 8 мас.% [16]. Более подробная информация представлена в следующем разделе.
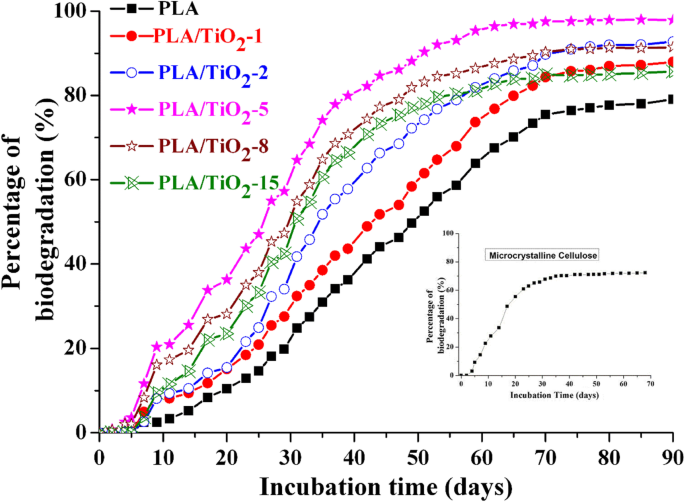
Процент биоразложения как функция времени инкубации для чистого PLA и PLA / TiO 2 нанокомпозиты. Вставка представляет собой процент биоразложения как функцию времени для микрокристаллической целлюлозы
Различные проценты биоразложения связаны с различными изменениями молекулярной массы полимерной матрицы. На рис. 6 показано изменение молекулярной массы образцов в зависимости от времени инкубации. Кривые показывают, что изменения Mn в PLA / TiO 2 нанокомпозиты были аналогичными (то есть быстрое уменьшение Mn с последующей фазой плато почти постоянного Mn), по крайней мере, в течение определенного времени инкубации. Чтобы исследовать механизмы разложения, вызванные добавлением нанонаполнителей, модель, которая учитывает автокатализ за счет генерируемых концевых групп карбоновых кислот, была использована для расчета константы скорости катализированной деградации согласно [17, 49]:
$$ \ ln {M} _ {nt} =\ ln {M} _ {n0} - kt $$ (3)где k - константа скорости катализируемого гидролитического разложения, M n0 - среднечисловая молекулярная масса до разложения, M нет - это среднечисловая молекулярная масса в любой момент времени.
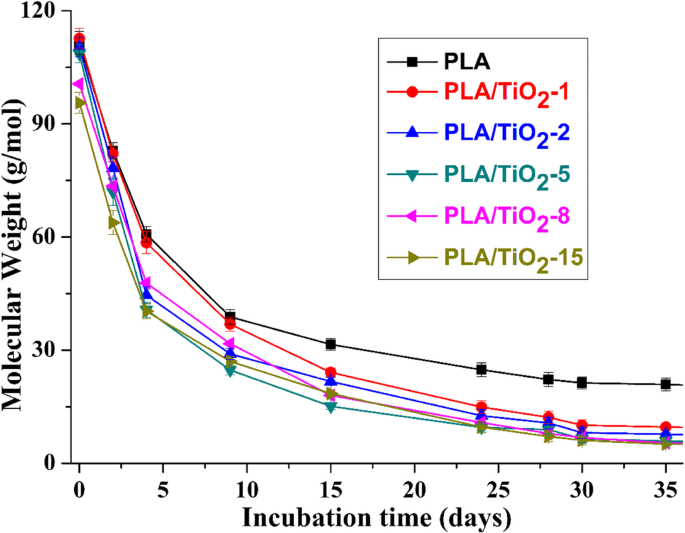
Изменение Mn как функция времени для чистого PLA и PLA / TiO 2 нанокомпозиты
k значения, оцененные по формуле. (3) представлены на рис. 7. Из рис. 7 скорость деградации нанокомпозитов PLA и PLA может быть идентифицирована до двух и трех фаз, соответственно. Mn быстро снижался в течение первых 8 дней, после чего следовала фаза плато для чистого PLA. Для PLA / TiO 2 нанокомпозиты, самые высокие значения k означает, что M n быстро снизилась в первой фазе (т.е. с 0 до 4 дней). Следующие от 5 до 24 дней относятся ко второй фазе, и значения k немного снизился по сравнению с первым этапом. Немногочисленные исследования [13, 50] показали, что кристаллическая часть PLA более устойчива к деградации, чем аморфная часть; таким образом, уменьшение k в этой фазе может быть вызвано увеличением кристалличности матрицы PLA. Через 24 дня (т.е. последняя фаза) значение k снова уменьшилось. На этой стадии полимер полностью разложился на фрагменты олигомера или молочную кислоту, и микроорганизмы минерализовали оставшиеся материалы для непрерывного образования CO 2 .
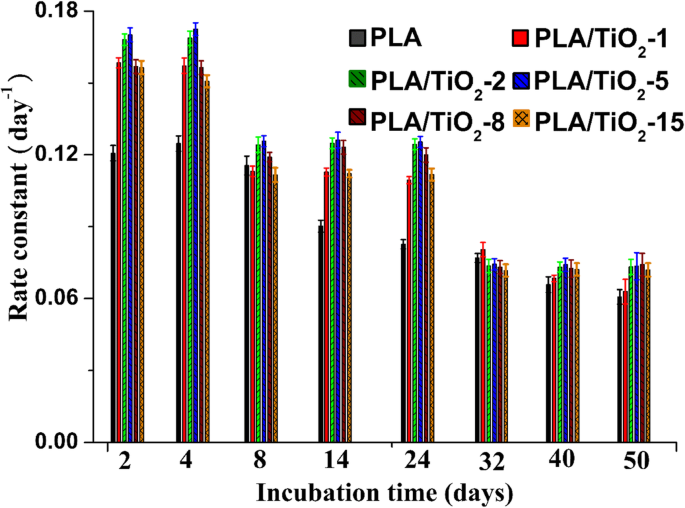
Скорость биодеградации в зависимости от времени инкубации для чистого PLA и PLA / TiO 2 нанокомпозиты
В условиях компостирования факторы, влияющие на склонность PLA к биоразложению, будут контролировать разложение PLA / TiO 2 нанокомпозиты. Когда количество g-TiO 2 был гомогенно диспергирован в матрице PLA, молекулы воды легко проникали внутрь образцов, вызывая процесс деградации [17]. Следовательно, на первом этапе Mn существенно снизился. Эволюция лаг-фазы CO 2 Исследование PLA и его нанокомпозитов в этот период показало, что микроорганизмы нуждаются в подходящих полимерных цепях для минерализации. По мере увеличения времени инкубации полимерные цепи в аморфных областях разлагаются, и количество аморфных областей уменьшается; таким образом, процентное соотношение кристаллической и аморфной области (т.е. χ c ) увеличилось [39], что привело к уменьшению k на втором этапе. Однако на этой стадии фрагменты олигомера начали минерализоваться микроорганизмами, что указывает на то, что произошла продуктивная фаза минерализации PLA. При уменьшении количества оставшихся фрагментов олигомера и увеличении χ c , k и D т уменьшилась, и наблюдалась почти длинная фаза плато для k и D т на третьем этапе. В нашем предыдущем исследовании [16] морфология каждого нанокомпозита была описана и определена с помощью SEM и TEM; результаты показали, что дисперсия g-TiO 2 с менее 5 мас.% в PLA / TiO 2 нанокомпозиты были лучше, чем полученные с высокой концентрацией нанонаполнителей. По дисперсности и содержанию TiO 2 , PLA / TiO 2 –5 имел наибольшее значение k и D т по сравнению с другими нанокомпозитами в нашем эксперименте.
Выводы
PLA / TiO 2 были приготовлены нанокомпозиты (на основе PLA и функционализированного g-TiO 2 ) и подвергаются биоразложению в контролируемых условиях компостирования. Использование такого стандарта, информация о узорах на поверхности образцов и быстрое увеличение кристалличности показали, что PLA и PLA / TiO 2 нанокомпозиты обладают гетерогенными механизмами биодеградации. Исследование деструкции нанокомпозитов в условиях компостирования показало, что присущий PLA характер разложения сохранился после включения функционализированных наночастиц диоксида титана (PLA / TiO 2 ). Добавление TiO 2 наночастицы увеличивают скорость разложения матрицы PLA, поскольку молекулы воды легко проникают в PLA / TiO 2 нанокомпозитов, тем самым активируя процесс деградации. Это явление было особенно очевидно для PLA / TiO 2 –5 из-за высокого содержания TiO 2 содержание и хорошая дисперсия TiO 2 нанонаполнители в матрице PLA по сравнению с другими нанокомпозитами.
Сокращения
- DSC:
-
Дифференциальная сканирующая калориметрия
- D т :
-
Процент биоразложения
- GPC:
-
Гель-проникающая хроматография
- g-TiO 2 :
-
Привитой TiO 2
- MCE:
-
Микрокристаллическая целлюлоза
- Mn:
-
Среднечисленная молекулярная масса
- Mw:
-
Средневесовая молекулярная масса
- PLA:
-
Поли (молочная кислота)
- SEM:
-
Сканирующая электронная микроскопия
- T cc :
-
Пик холодной кристаллизации
- Т g :
-
Температура стеклования
- XRD:
-
Рентгеновская дифракция
Наноматериалы
- ADM и LG Chem исследуют производство молочной кислоты и PLA в США
- Улучшенное фотоэлектрохимическое определение мочевой кислоты на электроде из стеклоуглерода, модифицирова…
- Электроспряденные полимерные нановолокна, украшенные наночастицами благородных металлов для определения х…
- Простой синтез окрашенного и проводящего композита CuSCN, покрытого наночастицами CuS
- Новые нанокомпозиты полистирола с полианилином, легированным лаурилсерной кислотой
- Нацеливание на эндотелиальные клетки с помощью многофункциональных наночастиц GaN / Fe
- Фотокаталитическая активность, усиленная Au-плазмонными наночастицами на фотоэлектроде нанотрубки TiO2, покры…
- Повышенная стабильность магнитных наночастиц золота с помощью сополимера поли (4-стиролсульфоновой кислоты …
- Синергетические эффекты наночастиц Ag / BiV1-xMoxO4 с повышенной фотокаталитической активностью
- Токсичность наночастиц CoFe2O4, покрытых ПЭГ, с лечебным эффектом куркумина



