Источник органического фосфора и кальция индуцирует синтез микросфер фосфата кальция со структурой желточной оболочки с высокой удельной площадью поверхности:применение в адсорбции HEL
Аннотация
Микросферы фосфата кальция со структурой желточной оболочки имеют большой потенциал для медицинского применения благодаря своим превосходным физико-химическим свойствам и биосовместимости. Однако разработка фосфата кальция со структурой желточной оболочки с высокой адсорбционной способностью остается сложной задачей. Здесь представлена пористая микросфера со структурой желточной оболочки (ATP-CG) фосфата кальция с высокой удельной площадью поверхности [ S СТАВКА =143 м 2 г −1 , который примерно в три раза выше, чем у микросфер АТФ-CL, синтезированных путем замены источника кальция на пентагидрат l-лактата кальция (CL)], был успешно синтезирован с использованием динатриевой соли аденозин-5'-трифосфата (АТФ) в качестве источника фосфора и моногидрат глюконата кальция (CG) в качестве источника кальция с помощью самовоспроизводящегося подхода. Также было исследовано влияние молярного отношения Ca к P (Ca / P), гидротермальной температуры и времени на морфологию микросфер ATP-CG. Установлено, что источник органического кальция и источник органического фосфора играют жизненно важную роль в формировании структуры желточной оболочки. Кроме того, была исследована серия экспериментов по адсорбции, чтобы выяснить механизм адсорбции двух видов микросфер со структурой желточной оболочки, синтезированных с использованием различных источников кальция. Результаты показывают, что адсорбционная способность микросфер ATP-CG (332 ± 36 мг / г) примерно в два раза выше, чем у микросфер ATP-CL (176 ± 33 мг / г). Более того, более высокая удельная поверхность, обусловленная источником кальция, и уникальные химические свойства поверхности для микросфер ATP-CG играют важную роль в улучшении адсорбционной способности HEL. Исследование показывает, что готовые микросферы со структурой желточной оболочки перспективны для применения в областях доставки лекарств и обеспечивают эффективный подход для улучшения адсорбционной способности лекарств.
Введение
Фосфат кальция привлек значительное внимание в течение последних нескольких лет благодаря своей превосходной биосовместимости [1], высокой нагрузочной способности и эффективности доставки. Биоматериалы, связанные с фосфатом кальция, широко используются в различных областях биомедицины, таких как тканевая инженерия [2], восстановление костей [3] и доставка лекарств [4]. Для расширения области применения и улучшения характеристик материалов на основе фосфата кальция используются различные материалы из фосфата кальция с различными морфологиями и микроструктурами, включая микросферы из карбонизированного гидроксиапатита (HAp) [5], микротрубки HAp [6], полые микросферы HAp [7] ], мезопористые наносферы из аморфного фосфата кальция (ACP) [8] «желток @ клетка-оболочка».
Среди различных морфологий микросферы со структурой желточной оболочки привлекают все больше и больше внимания, поскольку они не только являются передовым материаловедом, но также обладают уникальными морфологическими особенностями. В микросферах со структурой желточной оболочки пустое пространство между ядром желтка и оболочкой может служить резервуаром для хранения различных грузов, а оболочка с пористой структурой может обеспечивать путь диффузии для гостевых молекул, что дает им большой потенциал для различных применений, включая катализ [9], литий-ионные батареи [10], фотокатализатор [11] и биомедицина [12]. Традиционно методы принесения в жертву темплатов являются основными для получения микросфер со структурой желточной оболочки [13, 14]. Эти стратегии шаблонов достигли большого успеха в настройке структуры и свойств. Однако у этих подходов есть некоторые недостатки. Например, утомительные технологические операции и поверхностно-активные вещества или реагенты, регулирующие структуру, которые могут быть опасны для здоровья человека. В настоящее время методы самотемплинга широко используются при исследовании микросфер со структурой желточной оболочки [15, 16]. В отличие от традиционных подходов к созданию шаблонов, шаблоны, используемые в подходах с автоматическим созданием шаблонов, являются не только шаблонами для формирования пустот, но и предшественниками микросфер со структурой желточной оболочки. Таким образом, самовоспроизводящиеся методы являются удобными подходами для получения микросфер со структурой желточной оболочки. Тем не менее, внедрение самовоспроизводящихся подходов к синтезу микросфер фосфата кальция со структурой желтка и оболочки остается интересной задачей.
Кроме того, материалы из фосфата кальция использовались для переноса различных типов грузов, таких как белки [17], ДНК [18] и миРНК [19]. Однако необходимо срочно решить проблему плохой адсорбционной способности фосфата кальция к лекарствам. Как правило, подходы к иммобилизации молекул лекарств на поверхности носителя зависят от свойств поверхности, включая поверхностный потенциал [20], гидрофобность / гидрофильность [21], водородную связь [22] и удельную поверхность [23]. Таким образом, улучшение свойств поверхности и удельной площади поверхности является действенным подходом к увеличению способности носителя к адсорбции лекарств.
В данном случае мы приготовили своего рода пористые микросферы фосфата кальция со структурой желточной оболочки, используя динатриевую соль аденозин-5'-трифосфата (АТФ) в качестве источника фосфора и моногидрат глюконата кальция (CG) в качестве источника кальция с помощью самовоспроизводящегося подхода. Без какого-либо добавления темплатного агента полученные микросферы из фосфата кальция со структурой желточной оболочки демонстрируют особенно высокую удельную поверхность. Кроме того, поведение микросфер ATP-CG при адсорбции лизоцима куриного яйца (HEL) было исследовано в сравнении с микросферами ATP-CL, полученными путем замены источника кальция на пентагидрат l-лактата кальция (CL). Результаты показывают, что разница в удельной площади поверхности, вызванная источником кальция и химическими свойствами поверхности, играет жизненно важную роль в улучшении адсорбционной способности HEL.
Методы
Материалы
Динатриевая соль аденозин-5'-трифосфата (АТФ) была получена от Macklin Biochemical Co., Ltd (Шанхай, Китай). Моногидрат глюконата кальция (CG) и пентагидрат (l) -лактата кальция (CL) были приобретены у Sangon Biotech Co., Ltd (Шанхай, Китай). Лизоцим куриных яиц (HEL, ~ 70000 Ед / мг) был приобретен у Sigma-Aldrich (Тауфкирхен, Германия).
Синтез и характеристика микросфер ATP-CG и ATP-CL со структурой желтка и оболочки
Микросферы фосфата кальция со структурой желтка и оболочки ATP-CG получали следующим образом:вкратце, 0,9 г CG растворяли в 20 мл сверхчистой воды с образованием раствора C при 60 ° C и 0,11 г ATP растворяли в 5 мл. сверхчистой воды с образованием раствора P. Затем раствор C охлаждали до комнатной температуры и смешивали с раствором P при интенсивном перемешивании, и pH раствора доводили 2 М раствором NaOH до 5. Конечный объем раствора составлял 30 мл с дополнительным добавлением сверхчистой воды, и молярное отношение Ca к P (Ca / P) составило 3,3. Конечный раствор переносили в систему для микроволнового разложения для микроволновой гидротермальной реакции и обрабатывали при 120 ° C в течение 15 минут. Полученные осадки собирали центрифугированием (4500 об / мин, 10 мин), промывали сверхчистой водой и лиофилизировали в течение 48 часов. Микросферы ATP-CL были приготовлены в соответствии с описанными в литературе процедурами [24].
Кристаллическая фаза микросфер была охарактеризована дифракцией рентгеновских лучей (XRD, Cu K α источник, λ =0,154). Морфологию микросфер наблюдали с помощью сканирующей электронной микроскопии (SEM), просвечивающей электронной микроскопии (TEM) и TEM высокого разрешения (HRTEM). Состав микросфер изучали на инфракрасном спектрофотометре с преобразованием Фурье (FTIR). Удельную поверхность микросфер определяли методом Брунауэра-Эмметта-Теллера (БЭТ). Термогравиметрический анализ (ТГА) был использован для изучения термических свойств образцов при скорости нагрева 10 ° C / мин в атмосфере азота.
Адсорбция и характеристика HEL
Эксперименты по адсорбции HEL двух видов микросфер были проведены следующим образом:определенное количество микросфер желточной оболочки (ATP-CG, Ca / P =3,3, 120 ° C, 15 мин и ATP-CL, Ca / P =2,5, 120 ° C, 30 мин) диспергировали в воде при постоянной ультразвуковой обработке в течение 10 мин с образованием суспензии микросфер с концентрацией 1,5 мг / мл. Затем 0,5 мл водных растворов, содержащих различные концентрации HEL, были немедленно добавлены к 1 мл вышеупомянутой суспензии, и конечные концентрации лекарственного средства составили 1–7,5 мг / мл. Каждый раствор встряхивали (200 об / мин) при 37 ° C в течение 6 часов. Позже растворы центрифугировали и количество HEL в супернатантах измеряли с помощью УФ-видимого спектрофотометра при 280 нм. Дзета-потенциалы и состав микросфер до и после загрузки лекарственного средства были охарактеризованы анализатором дзета-потенциала, ИК-Фурье спектрометром и термогравиметрическим анализатором (ТГА, скорость нагрева 10 ° C мин -1 , азотная атмосфера).
Изотерма адсорбции
Для изучения адсорбционного поведения в нашем исследовании была использована модель изотермы Дубинина-Радушкевича (D-R). Модель D-R основана на теории заполнения микропор, которая используется для описания неидеальной сорбции на гетерогенной поверхности, а также для выделения механизма сорбции (физическая сорбция или химическая сорбция). Модель выражается следующим уравнением:где Q eq - адсорбционная емкость адсорбента при равновесии (мг / г), C eq - концентрация адсорбата в водной фазе при равновесии (мл / л). Q м максимальная адсорбционная способность. R - газовая постоянная, 8,314 Дж / (моль ∙ k). Т абсолютная температура. E представляет собой среднюю свободную энергию для оценки типа адсорбции. Если E значение ниже 8 кДж / моль, тип адсорбции можно объяснить физической адсорбцией, от 8 до 16 кДж / моль, тип адсорбции относится к ионному обмену и превышает 16 кДж / моль, тип адсорбции можно описать химической адсорбцией .
$$ {Q} _ {\ mathrm {eq}} ={Q} _m \ exp \ left (- {K} _ {\ mathrm {DR}} \ {\ varepsilon} ^ 2 \ right) $$ (1) $$ \ varepsilon =\ text {RT1n} (1+ \ frac {1} {{C} _ \ text {eq}}) $$ (2) $$ \ mathrm {E} =\ frac {1} {\ sqrt {K _ {\ mathrm {DR}}}} $$ (3)Статистический анализ адсорбции лекарств
Данные были представлены как среднее значение ± стандартное отклонение (SD). Значительные различия ( p <0,05) были статистически рассчитаны среди различных групп с использованием однофакторного дисперсионного анализа. Все эксперименты были проведены в трех экземплярах, и данные были проанализированы с помощью программного обеспечения DPS.
Результаты и обсуждение
Морфология и химическая характеристика микросфер
Структурированные микросферы ATP-CG, состоящие из желтка и оболочки
СЭМ-изображения на рис. 1 показывают морфологию различных образцов, полученных при различных условиях реакции. В t =5 мин или 15 мин, все продукты состоят из однородных микросфер. Однако при дальнейшем увеличении гидротермического времени до 30 мин образовывались самособирающиеся микросферы нанолистов (как показано на рис. 1 f, i, l). Между тем влияние Ca / P на морфологию продуктов также наблюдается при t =30 мин. По мере увеличения Ca / P постепенно образовывались самособирающиеся микросферы нанолистов (как показано на рис. 1 f, i, l). Формирование самосборных микросфер нанолистов можно объяснить следующими причинами. Во-первых, в микроволновом гидротермальном процессе молекулы АТФ могут гидролизоваться с образованием молекул на основе аденозина, включая аденозиндифосфат (АДФ), аденозинмонофосфат (АМФ) и аденозин, и одновременно высвобождать ионы фосфата (PO 4 3– ). Между тем, молекулы CG могут гидролизоваться с образованием глюконата и ионов кальция (Ca 2+ ). Затем ионы фосфата будут реагировать с ионами кальция с образованием первичных ядер ACP [25]. Затем начальные ядра ACP растут и собираются, чтобы сформировать микросферы ACP. Следовательно, при дальнейшем увеличении гидротермального времени молекулы АТФ и CG в растворе дополнительно гидролизуются и выделяют больше PO 4 3– и Ca 2+ ионы, которые вызывают образование самосборных микросфер нанолистов за счет улучшения перенасыщения системы и скорости зародышеобразования. Кроме того, за счет увеличения Ca / P локальная высокая концентрация Ca 2+ также ускоряет преобразование морфологии продуктов таким же образом, как указано выше. Приведенный выше анализ показывает, что гидротермальное время и Ca / P имеют важное влияние на морфологию продуктов.

СЭМ-изображения микросфер ATP-CG, полученных микроволновым гидротермальным методом при 120 ° C
Затем исследуются FTIR-спектры микросфер, синтезированных с различными Ca / P при 120 ° C в течение 15 мин (рис. 2). Пики на 1620 см −1 , 1383 см −1 , и 912 см −1 приписываются характерным пикам C =O, C – O групп CG и P – O АТФ [26] соответственно, что означает, что негидролизованные молекулы CG и АТФ или их производные абсорбируются на поверхности микросфер. Слабый характерный пик РО 4 3– от ГАП находится на высоте 1035 см −1 [27] и пики поглощения при 1122 см −1 и 567 см −1 присвоены ЗП 4 3– ионы ACP [28], что указывает на то, что продукты состоят из ACP и HAp. Результаты FTIR предполагают, что фосфат кальция успешно получен с использованием АТФ в качестве источника фосфора и ХГ в качестве источника кальция.
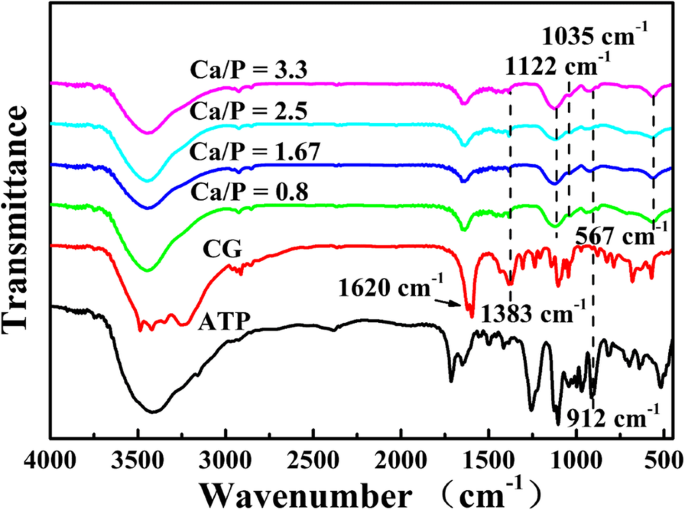
FTIR-спектры микросфер ATP-CG, синтезированных с различными Ca / P при 120 ° C в течение 15 мин
Кроме того, изображения SEM и TEM образцов, синтезированных с использованием различных Ca / P с помощью микроволнового гидротермального метода при 120 ° C в течение 15 минут, показаны на рис. 3. Когда Ca / P составляет 0,8 или 1,67, образцы состоят из пористых микросфер ( Рис. 3б, г). Когда Ca / P составляет 2,5, морфология продуктов начинает трансформироваться в микросферы со структурой желточной оболочки (рис. 3f). При дальнейшем увеличении Ca / P до 3,3 продукты полностью состоят из микросфер со структурой желточной оболочки (рис. 3h). Кроме того, некоторые из сломанных сфер и обнаженные ядра микросфер желточной оболочки (вставка на рис. 3g) наблюдаются после механического разрушения, что свидетельствует о полой структуре между желтком и скорлупой. Основываясь на вышеизложенном, мы предположительно предлагаем механизм образования микросфер со структурой желточной оболочки, синтезированных с использованием различных Ca / P. Когда Ca / P ниже, сначала образуются пористые микросферы ACP, что объясняется эффектом ингибирования молекул АТФ и CG или их производных, адсорбированных на поверхности микросфер. Затем, по мере дальнейшего увеличения Ca / P, метастабильный ACP будет расти, что обусловлено высоким пересыщением системы. Наконец, кристаллические ГАП образуются на внешней поверхности, что подтверждается изображением микросфер с высоким разрешением (ПЭМВР) на рис. 3i (межплоскостное расстояние 0,308 нм можно индексировать как (210) ГАП). В результате образуются полые структуры между желтком и скорлупой из-за разницы в объеме или плотности между HAp и ACP [24]. Соответствующее отображение EDS показывает, что элементы Ca, P и O равномерно распределены по микросферам. Спектры EDS на рис. 3k и спектр XPS на рис. 3l показывают, что химические элементы микросфер в основном включают Ca, P и O, что согласуется с результатом FTIR (рис. 2).

SEM и TEM изображения микросфер ATP-CG, синтезированных с различными Ca / P. а , b Са / Р =0,8. c , d Са / Р =1,67. е , f Са / Р =2,5. г , ч Са / Р =3,3. я HRTEM, j EDS-мэппинг, k Спектры ЭДС, л XPS-спектры микросфер ATP-CG с Ca / P =3,3
Влияние гидротермального времени и температуры с помощью микроволнового излучения на морфологию микросфер, синтезированных с Ca / P =3,3, далее исследуется. Как показано на рис. 4a-b, когда гидротермальное время составляет 5 минут, образцы состоят из пористых микросфер. Как обсуждалось выше, когда t =15 мин, продукт также состоит из микросфер со структурой желточной оболочки (рис. 4c-d). Когда гидротермальное время увеличивается до 60 минут или температура повышается до 160 o C, наблюдаются перемычки листов или стержней (рис. 4e-l). Преобразование морфологии от пористой оболочки к желточной оболочке к листу или стержню объясняется дальнейшим ростом ACP с непрерывным гидролизом молекул ATP и CG в растворе. Более того, гидролиз молекул АТФ и CG или их производных, адсорбированных на поверхности микросфер ACP, также ускоряет рост ACP. Интересный феномен проявился на 60 мин или 160 o C, эти листы или стержни также созданы из наночастиц ACP (как показано в красных прямоугольниках), что подтверждается анализом DTA на рис. S1. На кривых ДТА [29, 30] наблюдается экзотермический пик при 650 ° C, который связывают с кристаллизацией ACP. Экзотермический пик постепенно ослабевает с увеличением гидротермического времени или температуры, что означает превращение ACP в продуктах в кристаллический фосфат кальция.

SEM и TEM изображения микросфер ATP-CG, синтезированных с Ca / P =3,3 в различных экспериментальных условиях. а , b Т =120 ° C, t =5 мин. c , d Т =120 ° C, t =15 мин. e – h Т =120 ° C, t =60 мин. я – л Т =160 ° C, t =15 мин.
Химический состав и структура образцов, синтезированных с Ca / P =3,3 при различном гидротермальном времени или температуре, исследуются методами FTIR и XRD. Как показано на рис. 5а, характеристические пики PO 4 3– ионы HAp расположены на 1037 см −1 и 603 см −1 [27]. Пик на 1122 см −1 присваивается характеристическому пику ПО 4 3– ионы от ACP. Пики поглощения при 1620 см −1 и 1383 см −1 относятся к характерному пику групп C =O и C – O из КГ соответственно. Пик поглощения при 912 см −1 относится к асимметричному валентному колебанию P – O АТФ. При увеличении гидротермального времени или температуры интенсивность характерных пиков CG и ATP постепенно уменьшается, указывая на то, что молекулы ATP и CG или их производные, адсорбированные на поверхности микросфер, подвергаются дальнейшему гидролизу. Между тем, интенсивность характерного пика ПО 4 3– ионы в HAp представляют собой постепенно увеличивающуюся тенденцию с уменьшением интенсивности характеристического пика ACP, освещая превращение кристаллической фазы продуктов в фазу HAp.
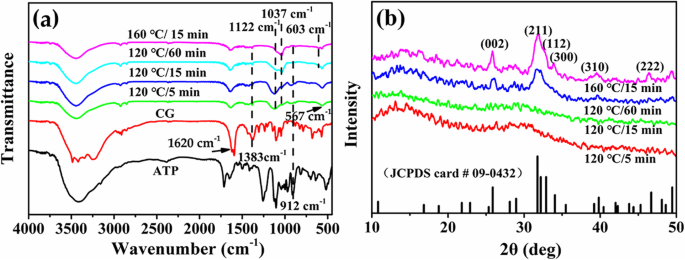
а Спектры FTIR и b Рентгенограммы микросфер ATP-CG, синтезированных с Ca / P =3,3 в различных экспериментальных условиях
На рис. 5b показаны рентгенограммы различных образцов. Характерный выступ аморфной фазы около 2 θ =30 ° микросфер, синтезируемых за 5 или 15 мин. Однако, когда гидротермальное время увеличивается до 60 минут или температура повышается до 160 ° C, кристаллическая фаза микросфер полностью превращается в HAp, который может быть проиндексирован как стандартные данные (JDCPS № 09-0432). Улучшение относительной интенсивности плоскостей решетки (211), (300) и (002) могло бы дополнительно объяснить увеличение кристалличности продуктов. Таким образом, результаты XRD и FTIR дополнительно подтверждают кристаллическое фазовое превращение продуктов с увеличением гидротермальной температуры или времени.
Микросферы, структурированные из желтка и скорлупы АТФ-ХЛ
Чтобы сравнить характеристики адсорбции лекарств, другие микросферы со структурой желточной оболочки были приготовлены с использованием ХЛ в качестве органического источника кальция с помощью микроволнового гидротермального метода [24]. С точки зрения морфологии, образцы по-прежнему состоят из микросфер со структурой желточной оболочки, что подтверждается сломанными сферами (вставка на рис. 6а) и изображениями ПЭМ (рис. 6b, c). Результат показывает, что изменение источника кальция не оказывает значительного влияния на морфологию продуктов. Кроме того, электронная дифракция на выбранной площади (SAED) показывает дискретные пятна SAED (рис. 6d), демонстрируя, что получаются хорошо кристаллизованные микросферы. Кроме того, EDS-картирование показывает равномерное распределение элементов Ca, P и O в микросферах (рис. 6e). Соответствующие спектры EDS также подтверждают присутствие элементов Ca, P и O в микросферах (рис. 6f), что указывает на то, что полученные микросферы представляют собой фосфат кальция.

а SEM . б , c Изображения ТЕА . г S электронная дифракция на выборочной площади (SAED) . е EDS-мэппинг и f EDS-спектры микросфер ATP-CL
Механизм адсорбции и адсорбции микросфер HEL
Как показано на рис. 7, адсорбционная способность двух видов микросфер увеличивается с увеличением начальной концентрации HEL. Когда начальная концентрация HEL увеличивается до 6,5 мг / мл, адсорбционная способность микросфер ATP-CG выходит на плато, а максимальная адсорбционная способность микросфер составляет около 332 ± 36 мг / г (рис. 7a), что примерно вдвое больше. выше, чем у микросфер ATP-CL (176 ± 33 мг / г, 6 мг / мл, рис. 7b).
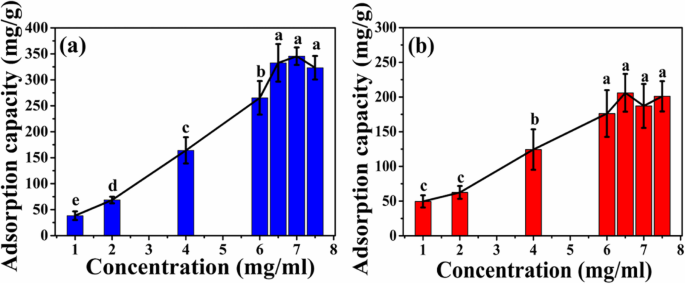
Кривая адсорбции микросфер при различной начальной концентрации HEL. а Микросферы ATP-CG. б Микросферы ATP-CL
Результат адсорбции HEL дополнительно подтверждается спектрами FTIR и кривыми TG. Как показано на рис. 8a, b, поглощение достигает максимума при 1134 см −1 . (1139 см −1 ) и 563 см −1 (568 см −1 ) присвоено характеристическому пику РО 4 3– ионы ACP и 1039 см −1 (1040 см −1 ) присвоено характеристическому пику ПО 4 3– ионы HAp наблюдаются в HEL-адсорбированных микросферах, что указывает на то, что введение HEL в микросферы не вызывает каких-либо значительных изменений в структуре микросфер. Пики адсорбции при 1542 см -1 и 1545 см −1 приписываемые амидной группе HEL наблюдаются в HEL-адсорбированных микросферах, подтверждая, что HEL успешно адсорбируется на микросферах. Между тем, полосы адсорбции при 2966, 2962, 2935 и 2927 см −1 происходит от –CH 3 и –CH 2 группы HEL также обнаруживаются в HEL-адсорбированных микросферах, что дополнительно подтверждает наличие HEL на микросферах. Кривые ТГА показывают, что потеря массы микросфер ATP-CG до и после адсорбции HEL составляет 11,3% и 36,7% соответственно (рис. 8c). Следовательно, адсорбционная способность HEL микросфер ATP-CG составляет приблизительно 340 мг / г. Однако потеря массы АТФ-CL составляет 21,1% до адсорбции HEL, и 37% появляется на микросферах, адсорбированных HEL (рис. 8d). Так, адсорбционная емкость HEL составляет 189 мг / г для микросфер ATP-CL. Результаты ТГА близки к результатам на рис. 7.
ИК-Фурье спектры и кривые ТГА микросфер до и после адсорбции HEL . а Спектры FTIR и c Кривые ТГА микросфер ATP-CG, b Спектры FTIR и d Кривые ТГА микросфер АТФ-ХЛ
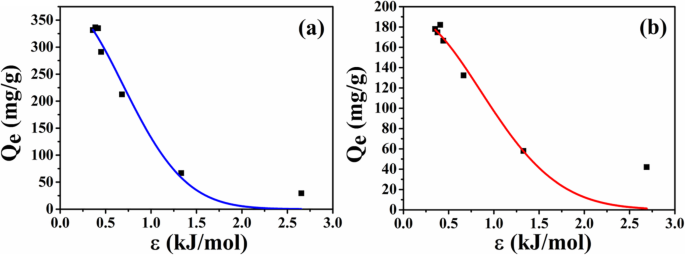
Чтобы исследовать причину разницы в адсорбционной способности между двумя типами микросфер, данные о равновесной адсорбции микросфер дополнительно анализируются в соответствии с моделью изотермы D-R. Подгоночные кривые показаны на рис. 9, а подгоночные параметры перечислены в таблице 1 соответственно. Исходя из результатов подгонки, коэффициент корреляции от ATP-CG выше, чем от ATP-CL, предполагая, что модель D-R подходит для описания поведения адсорбции лекарства микросферами ATP-CG. Поскольку E ниже 8 кДж / моль, адсорбция HEL на микросферы ATP-CG является физической сорбцией. Максимальная вместимость ( Q м ) микросфер ATP-CG для HEL может достигать 381 мг / г, что близко к результату на рис. 7a.

а Модель изотерм адсорбции HEL на микросферах ATP-CG. б Модель изотерм адсорбции HEL на микросферах ATP-CL
Поскольку адсорбция HEL на микросферах ATP-CG является физической сорбцией, исследуется поверхностный потенциал микросфер. Как показано на фиг. 10a, величина дзета-потенциала микросфер ATP-CG, ATP-CL и HEL в сверхчистой воде составляет -17 мВ, -22 мВ и 20 мВ, соответственно. После адсорбции HEL значение дзета-потенциала микросфер ATP-CG и ATP-CL изменяется до 2,7 мВ и 1,5 мВ, соответственно, указывая на адсорбцию молекул HEL на поверхность микросфер за счет электростатической силы притяжения. Однако притягивающая электростатическая сила не является основной причиной разницы в адсорбционной способности между двумя типами микросфер, потому что нет значительной разницы в значениях дзета-потенциала (-17 мВ и -22 мВ) между микросферами.
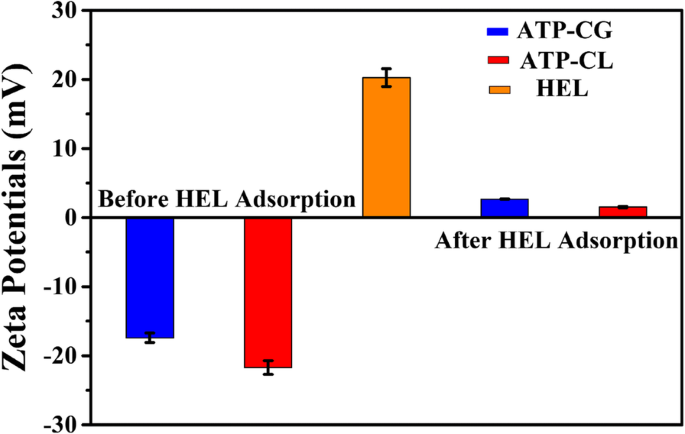
Дзета-потенциалы HEL и микросфер до и после адсорбции HEL
Поэтому, чтобы дополнительно выяснить причину, вызывающую разницу в абсорбционной способности микросфер, исследуют удельную поверхность микросфер. Как показано на фиг. 11a, удельная поверхность по БЭТ ( S СТАВКА ) микросфер ATP-CG составляет 143 м 2 г −1 , что примерно в три раза выше микросфер АТФ-CL (55 м 2 г −1 , Таблица 2). Таким образом, удельная площадь поверхности может способствовать разнице в абсорбционной способности микросфер. Такая высокая удельная поверхность микросфер ATP-CG в основном объясняется низкой кристалличностью [31]. Из фиг. 11b микросферы ATP-CG обладают более низкой кристалличностью, чем микросферы ATP-CL. Более того, разница в кристалличности между ATP-CG и ATP-CL в основном связана с разными условиями синтеза. Обычно кристалличность продукта увеличивается с увеличением степени гидролиза реагентов при определенном давлении и температуре. Здесь кислотность глюконовой кислоты (pKa =3,39) выше, чем l-молочной кислоты (pKa =3,86), что может вызвать более медленную скорость гидролиза и, в конечном итоге, иметь более низкую кристалличность. В результате за счет замены источника кальция получают микросферы ATP-CG с более высокой удельной поверхностью.
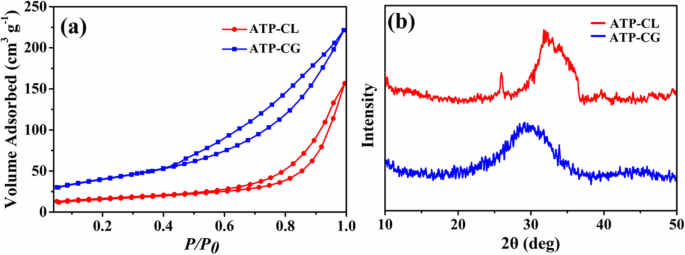
а Изотермы адсорбции-десорбции азота. б Рентгенограммы микросфер
Выводы
Микросферы желточной оболочки ATP-CG были разработаны с использованием АТФ в качестве источника органического фосфора и CG в качестве источника органического кальция с помощью гидротермального метода с использованием микроволн. Микросферы обладают высокой удельной поверхностью и высокой адсорбционной способностью. Также было исследовано влияние Ca / P, гидротермальной температуры и времени на морфологию и структуру микросфер. Исследование показывает, что органический источник фосфора и органический источник кальция оказывают значительное влияние на образование микросфер со структурой желточной оболочки. Более того, гидротермальные условия, включая Ca / P, гидротермальные и температурные, ответственны за образование микросфер желточной оболочки. Кроме того, мы обнаружили, что удельная площадь поверхности и химические свойства поверхности, такие как поверхностный потенциал, являются двумя ключевыми факторами, которые влияют на адсорбционную способность микросфер, путем сравнения адсорбционного поведения HEL двух видов микросфер, синтезированных с разными источниками кальция.
Доступность данных и материалов
Все данные, подтверждающие выводы этой статьи, включены в статью.
Сокращения
- СТАВКА:
-
Измерения Брунауэра-Эммета-Теллера
- FTIR:
-
Инфракрасная спектроскопия с преобразованием Фурье
- ТЕМ:
-
Просвечивающая электронная микроскопия
- XRD:
-
Рентгеновская дифракция
- TGA:
-
Термогравиметрический анализ
- HRTEM:
-
ТЕМ высокого разрешения
- SAED:
-
Электронная дифракция на выделенной области
Наноматериалы
- Получение наночастиц mPEG-ICA, нагруженных ICA, и их применение в лечении LPS-индуцированного повреждения клеток H9c2…
- Ультратонкий идеальный поглотитель и его применение в качестве плазмонного датчика в видимой области
- Простой синтез окрашенного и проводящего композита CuSCN, покрытого наночастицами CuS
- Влияние контактной неравновесной плазмы на структурные и магнитные свойства шпинелей Mn Х Fe3 - X О4
- Влияние отжига in situ на подвижность и морфологию органических полевых транзисторов на основе TIPS-пентацена
- Настройка морфологии поверхности и свойств пленок ZnO путем создания межфазного слоя
- Настройка трибологических характеристик слоистых нанопластинок фосфата циркония в масле с помощью поверхно…
- Синтез нанокристаллов ZnO и применение в инвертированных полимерных солнечных элементах
- Лазерные и транспортные свойства поли [(9,9-диоктил-2,7-дивиниленфлуоренилен) -альт-со- (2-метокси- 5- (2-этилгексило…
- Эффекты взаимодействия поверхностных плазмонных поляритонов и магнитных дипольных резонансов в метаматери…



