Стержневидный нанопористый CeO2, модифицированный наночастицами PdO, для окисления CO и сжигания метана с высокой каталитической активностью и водостойкостью
Аннотация
PdO / CeO 2 композит со стержнеобразной нанопористой каркасной структурой был получен путем комбинирования удаления легирования лент сплава Al-Ce-Pd с прокаливанием. Для окисления CO и CH 4 горения нанопористый PdO / CeO 2 композит демонстрирует превосходную каталитическую активность, а полные температуры реакции CO и CH 4 составляют 80 ° C и 380 ° C соответственно. Кроме того, композит обладает отличной циклической стабильностью, CO 2 токсичность и водостойкость, а каталитическая активность практически не снижается после 100 часов испытаний долгосрочной стабильности в присутствии водяного пара (2 × 10 5 промилле). Результаты серии характеристик показывают, что повышенная каталитическая активность может быть объяснена хорошей дисперсией наночастиц PdO, большой удельной поверхностью, высокой окислительно-восстановительной способностью, взаимодействием между PdO и CeO 2 , и больше поверхностно-активного кислорода на PdO. Результаты характеризации и экспериментов также показывают, что наночастицы PdO, полученные путем комбинирования деаллорирования и прокаливания, обладают более сильной каталитической активностью, чем наночастицы Pd. Наконец, простая модель используется для резюмирования каталитического механизма PdO / CeO 2 композитный. Мы надеемся, что эта работа поможет лучше понять разработку высокоактивных катализаторов.
Фон
В настоящее время все большее число людей обращают внимание на экологические проблемы и сосредотачиваются на смягчении некоторых важных экологических проблем, таких как выбросы выхлопных газов и глобальное потепление [1, 2]. В частности, устранение токсичного CO и парникового газа CH 4 является предметом множества исследований. Среди таких исследований низкотемпературный катализ оказался эффективным способом устранения этих загрязняющих газов [3,4,5,6].
Хотя многие исследования доказали, что дешевые металлы и их оксиды металлов (например, переходные металлы и оксиды, а также редкоземельные металлы и оксиды) могут использоваться в качестве катализаторов для окисления CO и CH 4 при горении, бесспорно, что использование благородных металлов обычно значительно улучшает каталитические характеристики [7, 8]. В последние годы катализаторы Pd и PdO были тщательно изучены и считаются одними из самых эффективных катализаторов окисления CO и CH 4 горение. Они проявляют не только низкую летучесть при высоких температурах, но и высокую каталитическую активность при низких температурах [9, 10].
Однако с точки зрения применения, поскольку содержание драгоценных металлов в земле относительно невелико, катализаторы Pd и PdO, которые обычно используются в практических промышленных приложениях, загружаются на носители, такие как оксиды металлов, цеолиты, углеродные материалы и металлоорганические каркасы. Эта конфигурация также соответствует тенденции развития устойчивого катализа за счет сохранения благородных металлов и использования взаимодействия носитель-благородный металл для улучшения каталитической активности [11, 12]. Среди видов опор CeO 2 считается многообещающим носителем из-за его сильных свойств хранения / выделения кислорода и превосходной термической стабильности. Например, MacLachlan et al. использовали комбинацию пропитки до начальной влажности и восстановления с помощью поверхности для получения наноструктурированного PdO / CeO 2 композит, который показал хорошую активность в качестве катализатора горения метана после прокаливания [13]. Луо и др. сообщил о приготовлении PdO-CeO 2 катализатора методом сжигания раствора и доказали, что синергетические эффекты PdO и CeO 2 являются причиной повышенной каталитической активности [14].
Несмотря на то, что было достигнуто много хороших результатов, все еще есть некоторые проблемы. Например, многие органические химические вещества или поверхностно-активные вещества могут загрязнять наноматериалы, что приводит к недостаточной каталитической активности, что характерно для влажной химии [15]. Кроме того, процесс приготовления катализатора на основе метода старения жидкого прекурсора сложен, а выход невелик [16]. Поэтому разработка экологически чистых материалов с высоким выходом и высокой каталитической активностью остается сложной задачей.
В этой работе мы разработали метод получения PdO / CeO 2 композиты путем удаления легирования лент из сплава Al-Ce-Pd и последующего прокаливания. Метод приготовления прост, структуру материала легко контролировать, и не требуются органические реагенты [17, 18], что особенно подходит для крупномасштабного промышленного производства и устойчивого будущего [19, 20]. Однако, насколько нам известно, в литературе не было сообщений об использовании удаления легирования для приготовления катализаторов для сжигания метана. Поэтому есть надежда, что эта работа может дать понимание и помочь в синтезе и получении наноматериалов.
Методы
Материалы
Все химические вещества и металлы использовали без дополнительной очистки в исходном состоянии. Чистый Al (99,90 вес.%), Чистый Ce (99,90 вес.%) И чистый Pd (99,90 вес.%) Были от Sino-Platinum Metals Co., Ltd. Гранулированный NaOH (AR) был от Shanghai Aladdin Biochemical Technology Co., Ltd. . Аргон высокой чистоты был от компании Xi'an Jiahe Co., Ltd.
Синтез PdO / CeO 2 Составной
Al 92− X Ce 8 Pd X ( X =0, 0,1, 0,3, 0,5, 0,7, 0,9 и 1,1) сплавы-предшественники были приготовлены дуговой плавкой чистого Al, чистого Ce и чистого Pd в атмосфере аргона. Полученный сплав-прекурсор Al-Ce-Pd переплавляли высокочастотным индукционным нагревом в кварцевой трубке под защитой аргона. Расплавленный сплав был выдут на высокоскоростной вращающийся медный валок аргоном для быстрого затвердевания, и была получена лента из сплава Al-Ce-Pd шириной приблизительно от 3 до 4 мм и толщиной приблизительно от 20 до 30 мкм.
Подготовленную ленту из сплава Al-Ce-Pd помещали в раствор гидроксида натрия с концентрацией 20 мас.% И удаляли сплав при температуре окружающей среды в течение 2 часов, затем нагревали до 80 ° C и удаляли сплавы в течение 10 часов. Образец с удаленным слоем многократно промывали деионизированной водой и сушили на воздухе при комнатной температуре. Высушенный образец прокаливали в O 2 . при 200 ~ 600 ° C в течение 2 часов и расходе O 2 составляет 18 мл мин -1 . Метод получения и структурная эволюция PdO / CeO 2 составные представлены на рис. 1.
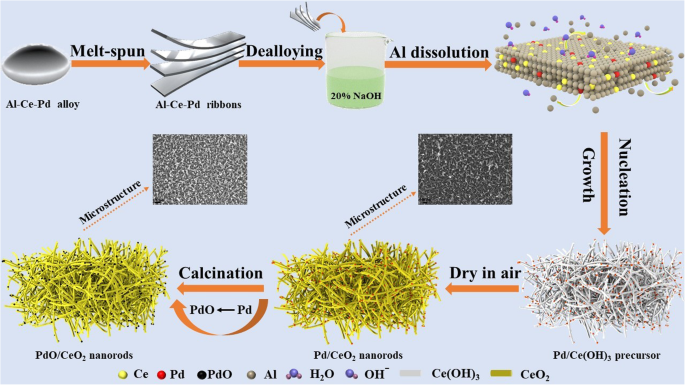
Схема приготовления стержневидного нанопористого PdO / CeO 2 составной
Образец характеристики
Картины дифракции рентгеновских лучей (XRD) получали с использованием дифрактометра Shimadzu XRD-6100 с Cu Kα-излучением (20 кВ и 40 мА). Морфология и элементный состав образцов были получены с помощью сканирующего электронного микроскопа (SEM) JSM-7000F и энергодисперсионного спектрометра (EDS) INCA X-Sight Oxford. Изображения просвечивающего электронного микроскопа (ПЭМ), изображения просвечивающего электронного микроскопа высокого разрешения (HRTEM) и изображения сканирующей просвечивающей электронной микроскопии в сочетании с энергодисперсионными рентгеновскими спектрами (STEM-EDX) были записаны на электронном микроскопе JEOL JEM-200. Удельная поверхность ( S СТАВКА ), размер пор ( D p ) и объем пор ( V p ) образцов определяли на приборе Micromeritics ASAP 2020 при 77,4 К. Анализ рентгеновской фотоэлектронной спектроскопии (XPS) выполняли на многофункциональном спектрометре модели Axis Ultra Kratos. Восстановление с запрограммированной температурой водорода (H 2 -TPR) проводили на приборе Quantachrome Autosorb-iQC-TPX, в котором образец массой 50 мг нагревали от 50 до 800 ° C со скоростью 10 ° C / мин в 10 об.% H 2 / Газовая смесь Ar, текущая со скоростью 40 мл мин -1 .
Тестирование катализатора
Каталитическую активность образцов оценивали по окислению CO и CH 4 горение. Катализатор (100 мг) загружали в трубчатый реактор из нержавеющей стали, и реактор помещали в трубчатую печь с точным контролем температуры. Исходный газ, состоящий из 1 об.% CO, 10 об.% O 2 , и 89 об.% N 2 или 1 об.% CH 4 , 10 об.% O 2 , и 89 об.% N 2 вводили в реактор с общим расходом 50 мл мин -1 . (объемная скорость =30000 ч −1 ), а расход реакционного газа контролировали и регулировали с помощью массового расходомера (Brooks 5850E). Подробная информация о подготовке исходного газа с 20 об.% H 2 O показаны в Дополнительном файле 1:Рисунок S1. CO и CH 4 Концентрации во время процесса нагрева анализировались на линии с помощью газового хроматографа Agilent GC-7890B, оборудованного пламенно-ионизационным детектором (FID). Конверсия CO и CH 4 был рассчитан в соответствии с формулой. (1):
$$ X =\ frac {C _ {\ mathrm {in}} - {C} _ {\ mathrm {out}}} {C _ {\ mathrm {in}}} \ times 100 \% $$ (1)где X представляет собой преобразование CO или CH 4 , C в представляет собой входную концентрацию CO или CH 4 , и C вне представляет собой выходную концентрацию CO или CH 4 .
Скорости реакции CO и CH 4 были рассчитаны по формуле. (2) [14, 21]:
$$ {r} _ {\ mathrm {CO} / {\ mathrm {CH}} _ 4} =\ frac {C _ {\ mathrm {CO} / {\ mathrm {CH}} _ 4} \ cdot {X} _ { \ mathrm {CO} / {\ mathrm {CH}} _ 4} \ cdot P \ cdot V} {m _ {\ mathrm {cat}} \ cdot {W} _ {\ mathrm {Pd}} \ cdot R \ cdot T } \ left (\ mathrm {mol} \ cdot {\ mathrm {s}} ^ {- 1} \ cdot {\ mathrm {g}} _ {\ mathrm {Pd}} ^ {- 1} \ right) $$ (2)где r CO / CH4 представляет собой скорость реакции CO или CH 4 ; концентрация CO или CH 4 выражается как C CO / CH4 в исходном газе; преобразование CO или CH 4 выражается как X CO / CH4 ; P - атмосферное давление, равное 101,3 кПа; V - общий расход; м кот - масса катализатора в реакторе; Вт Pd - загрузка Pd; R - молярная газовая постоянная, равная 8,314 Па · м 3 моль −1 К -1 ; и T - температура окружающей среды (293 К).
Результаты и обсуждение
Характеристики катализатора
Спектры XRD образцов показаны на рис. 2. Четкий набор дифракционных пиков для CeO 2 (JCPDS № 34-0394) был обнаружен, как показано на фиг. 2а, но дифракционные пики, связанные с Pd, не были обнаружены во всех образцах с удаленным слоем, которые были прокалены при 400 ° C. Распакованный Al 91,3 Ce 8 Pd 0,7 Сплав прокаливали при разных температурах, как показано на рис. 2б. По мере постепенного повышения температуры дифракционные пики CeO 2 постепенно становился резким и узким; однако даже после прокаливания при 800 ° C дифракционные пики, относящиеся к Pd, обнаружить не удалось. Этот результат может быть связан с относительно низкой концентрацией Pd в образце, который может быть сильно диспергирован в образце в форме аморфной фазы или мелких кристаллических зерен. Никаких дифракционных пиков, связанных с Al, не наблюдалось в спектрах XRD для любого из образцов, что указывает на то, что остаточное содержание Al в образцах после удаления сплава было либо очень низким, либо Al присутствовал в образцах в аморфной форме.
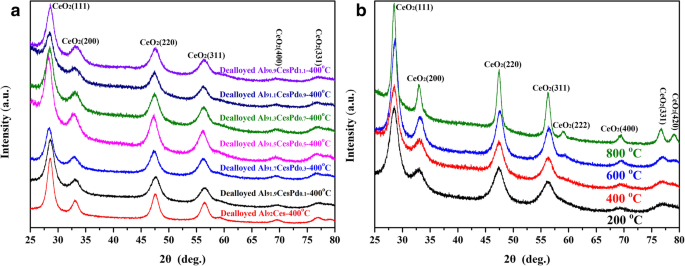
Картины XRD Al 92− X Ce 8 Pd X ( X =0,1, 0,3, 0,5, 0,7, 0,9 и 1,1), удаляется при 400 ° C ( a ) и дифрактограммы удаленного Al 91,3 Ce 8 Pd 0,7 сплавы, прокаленные при разных температурах ( b )
Результаты EDS и микроструктуры расплавленного Al 91,3 Ce 8 Pd 0,7 прокаленные при 400 ° C показаны на рис. 3. После удаления легирования содержание Ce и Pd в образце было очень близко к таковому в сплаве-предшественнике, как показано на рис. 3a, что указывает на то, что потери Ce и Pd были small в процессе разгрузки. Остаточный Al в удаленном Al 91,3 Ce 8 Pd 0,7 сплава, прокаленного при 400 ° C, было очень низким, всего 2,73%, что согласуется с результатами XRD. На рисунках 3b и c показаны изображения поверхности образца, полученные с помощью СЭМ, и образец демонстрирует однородную, неупорядоченную, тканую пористую структуру, состоящую из множества наностержней диаметром приблизительно 10 нм; наностержни уложены друг на друга, образуя несколько микропор и мезопор. Поперечное сечение SEM-изображения образца показано на рис. 3d, и наностержни соединены друг с другом, чтобы сформировать трехмерную каркасную структуру, которая способствует стабилизации наночастиц через большую площадь контакта, что приводит к большему количеству взаимодействующих наноразмеров. интерфейсы.
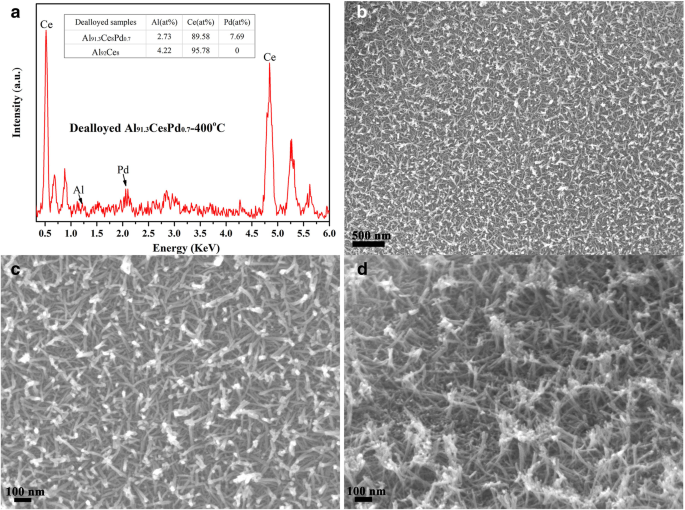
Образец ЭЦП ( а ), СЭМ-изображения поверхности ( b , c ) и изображение поперечного сечения SEM ( d ) расплавленного Al 91,3 Ce 8 Pd 0,7 сплав прокаленный при 400 ° C
Изображения ПЭМ и картографирование ПЭМ-EDX были дополнительно использованы для характеристики структур и распределения частиц в образце, как показано на рис. 4. Удаленный Al 91,3 Ce 8 Pd 0,7 Прокаленный при 400 ° C состоит из множества наностержней, как показано на рис. 4а, и наностержни уложены друг на друга, образуя множество микропор и мезопор, что согласуется с результатами СЭМ. На поверхности наностержней распределено несколько более темных частиц, как показано в красных прямоугольниках на рис. 4а. На рис. 4б показано изображение образца, полученное методом ПЭМВР. Значения шага решетки наностержней составляют примерно 0,314 нм и 0,193 нм, что соответствует плоскостям (111) и (220) CeO 2 . , соответственно. Красный прямоугольник на рис. 4b представляет собой изображение ПЭМВР более темных частиц, показанных на рис. 4а, которые имеют диаметр приблизительно 5 нм и распределены на поверхности CeO 2 наностержни. Однако значение шага решетки более темных частиц (0,201 нм) аналогично значению для плоскости (220) CeO 2 (0,193 нм) и трудно различить. Для идентификации этих частиц было выполнено отображение характеристик TEM-EDX. Как показано на фиг. 4c и d, частицы, распределенные на CeO 2 наностержни связаны с Pd, и, учитывая значение шага решетки 0,201 нм, более темные частицы определяются как наночастицы PdO, которые равномерно диспергированы на поверхности CeO 2 наностержни (рис. 4d), образующие ряд шероховатых поверхностей раздела.
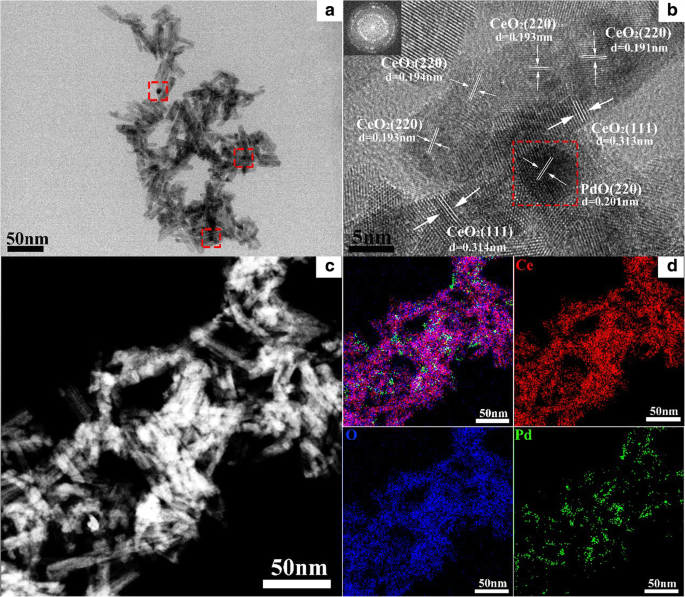
ТЕА ( а ), HRTEM ( b ) и отображение TEM-EDS ( c , d ) изображения расплавленного Al 91.3 Ce 8 Pd 0,7 сплав прокаленный при 400 ° C
Испытания BET и BJH проводились на расплавленном Al 91.3 Ce 8 Pd 0,7 прокаливают при различных температурах, и соответствующие результаты показаны на рис. 5 и в таблице 1. Все образцы демонстрировали изотермы типа IV с H 2 и H 3 петли гистерезиса, как показано на рис. 5а. Этот результат указывает на то, что образцы представляют собой мезопористые структуры, что согласуется с результатами SEM и TEM. Кроме того, кривая распределения пор по размерам, показанная на фиг. 5b, дополнительно доказывает, что все образцы обладают мезопористой структурой, а кальцинированные образцы демонстрируют аналогичное узкое распределение пор по размерам со средним диаметром пор приблизительно 12 ~ 14 нм. Удельная поверхность ( S СТАВКА ), размер пор ( D p ) и объем пор ( V p ) образцов при соответствующих температурах прокаливания перечислены в таблице 1. Прокаленный образец при 400 ° C демонстрирует наибольшую удельную поверхность и наибольший объем пор, равный приблизительно 102 м 2 г −1 и 0,362 см 3 г −1 , соответственно. Поскольку температура прокаливания непрерывно повышалась, удельная поверхность немного уменьшалась; однако даже после прокаливания при 600 ° C удельная поверхность образца все еще составляла 84 м 2 г −1 . Эти результаты показывают, что стержнеобразный нанопористый CeO 2 скелетная структура обладает отличной антиспекающей способностью. Этот вывод также подтверждается размерами кристаллов в Дополнительном файле 1:Таблица S1 и изображениями SEM и TEM в Дополнительном файле 1:Рисунок S2.
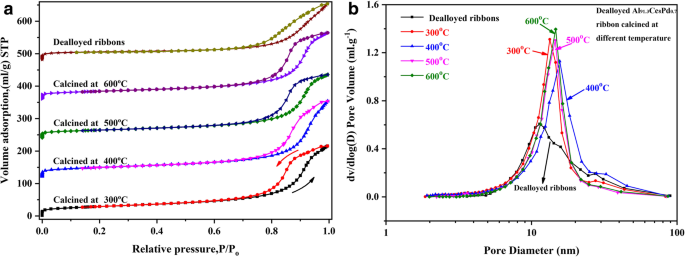
Кривые изотермы адсорбции-десорбции азота ( a ) и кривые распределения пор по размерам ( b ) нелегированного Al 91,3 Ce 8 Pd 0,7 ленты, прокаленные при разных температурах
Спектры РФЭС расплавленного Al 91.3 Ce 8 Pd 0,7 образец и кальцинированный очищенный от сплава Al 91,3 Ce 8 Pd 0,7 Образцы показаны на рис. 6, чтобы дополнительно охарактеризовать валентный состав элементов поверхности образцов. Спектр XPS Ce 3d показан на рис. 6a, где U представляет собой Ce 4+ . и V представляет собой Ce 3+ [22]. Как правило, наличие Ce 3+ тесно связан с кислородными вакансиями. Результаты расчетов показывают, что концентрации Ce 3+ в расплавленном Al 91,3 Ce 8 Pd 0,7 образец и кальцинированный очищенный от сплава Al 91,3 Ce 8 Pd 0,7 Образец составлял 21,15% и 23,33%, соответственно, с небольшой разницей, как показано в Таблице 2. Этот результат показывает, что прокаливание практически не влияет на концентрацию поверхностных кислородных вакансий. Чтобы понять влияние загрузки PdO на концентрацию кислородных вакансий в образце, XPS-спектр деалгированного Al 92 Ce 8 образец прокаленный при 400 ° C (чистый CeO 2 ) показан в Дополнительном файле 1:Рисунок S3. Ce 3+ Расчетная концентрация составила примерно 14,27%, что намного меньше, чем у образца, загруженного PdO. Это явление указывает на взаимодействие между PdO и CeO 2 и что присутствие PdO может изменить валентное состояние CeO 2 поверхностные элементы и увеличивают концентрацию поверхностных кислородных вакансий.
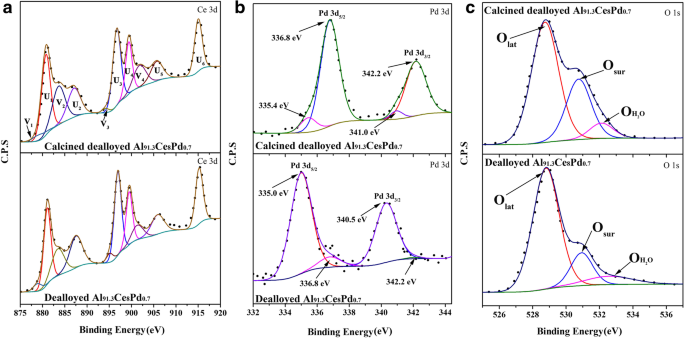
XPS-спектры Ce 3d ( a ), Pd 3d ( b ) и O 1s ( c ) области расплавленного Al 91,3 Ce 8 Pd 0,7 образец и расплавленный Al 91,3 Ce 8 Pd 0,7 образец прокаленный при 400 ° C
Для дальнейшего исследования эффектов прокаливания на поверхности наночастиц PdO были получены XPS-спектры Pd 3d для деалегированного Al 91,3 Ce 8 Pd 0,7 образец и кальцинированный очищенный от сплава Al 91,3 Ce 8 Pd 0,7 Образцы показаны на рис. 6б. В кальцинированном очищенном от сплава Al 91,3 есть две формы Pd. Ce 8 Pd 0,7 Лента; сильные пики при 336,8 эВ и 342,2 эВ можно отнести к PdO (Pd 2+ ) [23], а слабые пики при 335,4 эВ и 341,0 эВ можно отнести к металлическому Pd (Pd 0 ) [24]. Таблица 2 показывает, что концентрации Pd 2+ и Pd 0 составляли примерно 91,25% и 8,75% соответственно. Однако результаты анализа расплавленного Al 91.3 Ce 8 Pd 0,7 образец наоборот, и концентрации Pd 2+ и Pd 0 составляли примерно 6,45% и 93,55% соответственно. Это открытие указывает на то, что Pd присутствует в форме металлического Pd в очищенном образце, тогда как после прокаливания Pd окислился до PdO и равномерно диспергировался на поверхности CeO 2 , что согласуется с результатами изображений HRTEM.
Хорошо известно, что поверхностно-активный кислород (O sur ) обычно является активным кислородом для каталитических реакций. На рис. 6c показаны XPS-спектры O 1s двух катализаторов. Для кальцинированного деалегированного алюминия 91,3 Ce 8 Pd 0,7 В образце пики при 528,9 эВ, 530,6 и 532,1 эВ соответствуют решеточному кислороду (O lat ), поверхностно-активный кислород (O sur ) и слабоадсорбированный H 2 O (O H2O ) соответственно [25, 26]. Соотношение O sur (O sur / (O шир + O sur + O H2O )) был рассчитан и приведен в таблице 2. Отношения O sur для расплавленного Al 91,3 Ce 8 Pd 0,7 образец и кальцинированный очищенный от сплава Al 91,3 Ce 8 Pd 0,7 образец составлял приблизительно 16,2% и 29,3% соответственно, что указывает на присутствие более поверхностно-активных форм кислорода в кальцинированном деаллорированном Al 91,3 Ce 8 Pd 0,7 образец. Концентрации Ce 3+ в этих двух катализаторах были похожи (рис. 6а), предполагая, что PdO имеет более сильную способность адсорбировать и активировать O 2 чем металлические наночастицы Pd. Отдельный эксперимент (Дополнительный файл 1) был разработан для устранения влияния термической активации на результаты экспериментов, как показано в Дополнительном файле 1:Рисунок S4, и полученные результаты также подтверждают вышеприведенный вывод.
Чтобы сравнить различия в восстанавливаемости образцов до и после прокаливания, H 2 -TPR использовался для испытания как кальцинированного очищенного алюминия 91,3 Ce 8 Pd 0,7 образец и расплавленный Al 91,3 Ce 8 Pd 0,7 образец, и результаты показаны на рис. 7. На двух кривых TPR есть три основных пика, но их интенсивности и положения различаются. Два набора пиков, P 2 , P 2 ′ И P 3 , P 3 ′, В высокотемпературном диапазоне (> 300 ° C) объясняются восстановлением поверхности CeO 2 и навалом CeO 2 , соответственно [27], а P 1 и P 1 'Пики в низкотемпературном диапазоне (<300 ° C) объясняются снижением содержания частиц PdO и Pd 2+ -O-Ce 4+ структура [28]. Площадь P 1 пик значительно больше, чем у P 1 'Пик, который указывает на то, что кальцинированный образец с удаленным слоем содержал больше частиц PdO, что согласуется с результатами XPS. Тот факт, что P 1 площадь пика больше, чем у P 1 'Пик также указывает на то, что для кальцинированного образца с удаленным сплавом больше Ce 4+ ионы, связанные с частицами PdO, могут восстанавливаться при низких температурах, что является преимуществом для реакции каталитического окисления. P 2 и P 2 'Пики, расположенные около 470 ° C, также подтверждают эту гипотезу. Площадь P 2 'Пик значительно больше, чем у P 2 пик, указывающий на то, что для кальцинированного образца с удаленным легированием концентрация поверхностного CeO 2 количество частиц, которые могут быть восстановлены только при высоких температурах, было меньше, чем в образце, подвергнутом удалению сплава; другими словами, часть Ce 4+ ионы, связанные с PdO, восстанавливались при низких температурах. В сочетании с анализом XPS окислительно-восстановительная способность PdO / CeO 2 композитов выше, чем у Pd / CeO 2 , что предполагает, что PdO / CeO 2 композиты обладают более высокими каталитическими характеристиками.
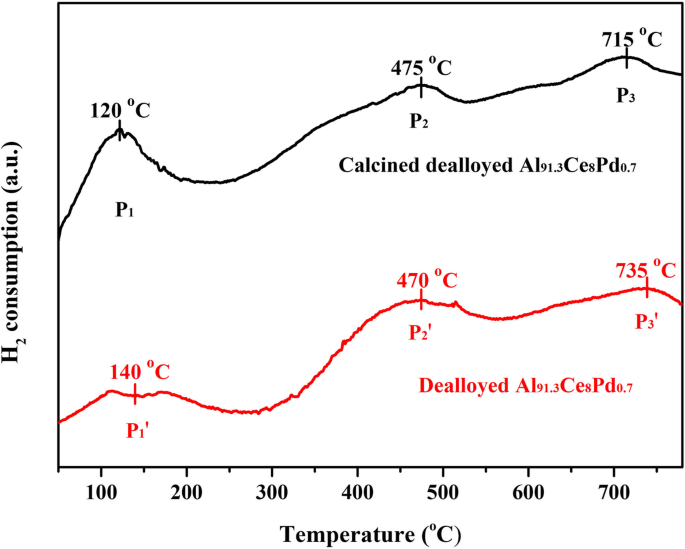
H 2 Кривые TPR расплавленного Al 91,3 Ce 8 Pd 0,7 ленты и необработанный Al 91,3 Ce 8 Pd 0,7 ленты, прокаленные при 400 ° C
Основываясь на приведенных выше результатах характеризации, возможный механизм образования PdO / CeO 2 композитов (рис. 1). Сначала в растворе NaOH растворяется Al, и Ce реагирует с OH - при 80 ° C с образованием стержневидного нанопористого Ce (OH) 3 скелетная структура из-за анизотропии Ce (OH) 3 рост. В то же время атомы Pd диффундируют к поверхности Ce (OH) 3 наностержни. Поскольку Ce (OH) 3 крайне нестабилен, легко обезвоживается и окисляется до CeO 2 при сушке на воздухе. После прокаливания под O 2 , большая часть наночастиц Pd на поверхности CeO 2 наностержни окислились с образованием PdO (рис. 6b) и были частично внедрены в CeO 2 наностержни (рис. 4) при высокой температуре для создания сильного взаимодействия металл-оксид-носитель. В результате PdO / CeO 2 были сформированы композиты.
Тест каталитической активности
Зависимость между содержанием Pd в прекурсоре и каталитической активностью катализаторов показана на рис. 8 а и б. Как показано на рис. 8а, CeO 2 наностержни проявляют плохую каталитическую активность по отношению к окислению CO (вставка), а T 99 (соответствующая температура реакции при конверсии 99%) достигает 280 ° C. Каталитическая активность при окислении CO была значительно увеличена из-за загрузки PdO. Образец расплавленного Al 91,3 Ce 8 Pd 0,7 показал лучшую каталитическую активность CO, а T 50 (соответствующая температура реакции при конверсии 50%) и T 99 составляли 15 ° C и 80 ° C соответственно. Температура выключения также была ниже минус 20 ° C. Однако при дальнейшем увеличении содержания Pd в предшественнике каталитическая активность несколько снизилась. Каталитическая активность по отношению к CH 4 сгорание катализаторов, образованных из прекурсоров с различным содержанием Pd, показано на рис. 8b. Подобно тому, которое наблюдается для окисления CO, чистый CeO 2 наностержни проявляют слабую каталитическую активность по отношению к CH 4 сгорание, а конверсия при 600 ° C составила всего 65%. После добавления PdO каталитическая активность значительно улучшилась. Аналогичным образом расплавленный Al 91,3 Ce 8 Pd 0,7 образец показал лучшую каталитическую активность по отношению к CH 4 сгорание, с температурой зажигания около 250 ° C, и T 50 и T 99 были 305 ° C и 380 ° C соответственно.
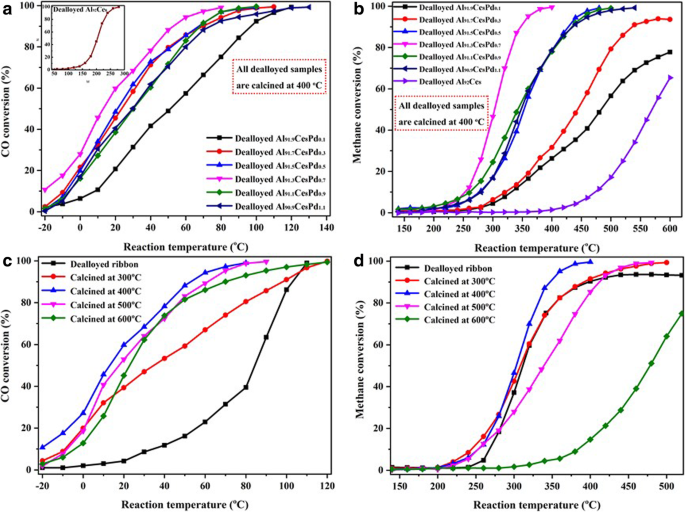
Конверсия CO ( a ) и CH 4 преобразование ( b ) как функции температуры реакции на удаленном Al 90 Ce 10 ленты и ленты из удаленного сплава Al-Ce-Pd с различным содержанием Pd, прокаленные при 400 ° C. Конверсия CO ( c ) и CH 4 преобразование ( d ) как функции температуры реакции на удаленном Al 91,3 Ce 8 Pd 0,7 кальцинирован при разных температурах
CO и CH 4 конверсии в зависимости от температуры реакции над удаленным Al 91,3 Ce 8 Pd 0,7 ленты, прокаленные при разных температурах, показаны на рис. 8c и d. Лента с удаленным слоем (без прокаливания) показала низкую каталитическую активность СО по сравнению с прокаленными образцами, как показано на фиг. 8с. В сочетании с анализом XPS эти результаты показывают, что PdO поддерживается на CeO 2 наностержни проявляют лучшую каталитическую активность CO, чем у Pd, что согласуется с H 2 -TPR анализ. Ниже 400 ° C каталитическая активность по отношению к CO постепенно возрастает с увеличением температуры прокаливания; однако при прокаливании при температурах выше 400 ° C каталитическая активность по отношению к CO снижалась с увеличением температуры прокаливания. Для канала 4 При сжигании аналогично образец, прокаленный при 400 ° C, показал лучшую каталитическую активность, как показано на рис. 8d. Тем не менее, ленточка с пропиткой имела температуру выключения и T . 50 аналогично кальцинированному образцу, и конверсия CH 4 всегда был ниже 93%. Согласно результатам экспериментов и анализу каталитической активности ленты с удаленным сплавом и кальцинированной ленты с удаленным сплавом при различных значениях O 2 атмосфер (Дополнительный файл 1:Рисунок S5), причины этого явления могут быть связаны с температурой выключения CH 4 был высоким (> 240 ° C), и часть Pd окислилась до PdO; таким образом, образец показывает хороший CH 4 каталитическая активность. Однако, поскольку композит не кальцинируется в чистом O 2 атмосфере окисление было недостаточным до такой степени, что не удалось полностью преобразовать CH 4 . Для расплавленного Al 91,3 Ce 8 Pd 0,7 прокаленные при разных температурах, порядок каталитической активности по отношению к CH 4 выглядит следующим образом:очищенный образец (без кальцинирования) <кальцинированный при 600 ° C <кальцинированный при 500 ° C <кальцинированный при 300 ° C <кальцинированный при 400 ° C. Результаты экспериментов показывают, что температура прокаливания имеет важное влияние на каталитическую активность образца.
Испытания на стабильность цикла были также выполнены на очищенном от сплава Al 91.3 Ce 8 Pd 0,7 ленты, прокаленные при 400 ° C, как показано на рис. 9а и б. Будь то окисление CO или сжигание CH 4 , результаты показывают, что аналогичные кривые могут быть получены для этих трех последовательных тестов активности и что катализатор стабилен и не дезактивирован. Этот результат показывает, что катализатор, полученный прокаливанием удаленного сплава Al 91,3 Ce 8 Pd 0,7 ленты при температуре 400 ° C имеют практическое значение и могут использоваться многократно.
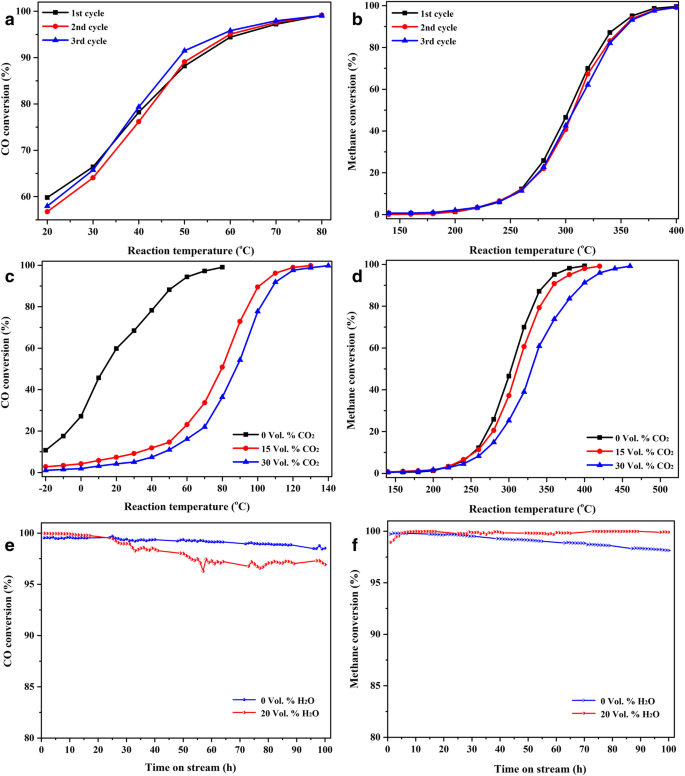
Циклические испытания стабильности ( a , b ), устойчивость к CO 2 тесты на токсичность ( c , d ) и испытания на водонепроницаемость ( e , f ) расплавленного Al 91,3 Ce 8 Pd 0,7 ленты, прокаленные при 400 ° C
Как правило, катализаторы, имеющие практическое применение, должны быть стабильными в присутствии CO 2 . и H 2 О. Реакционные газы, содержащие CO 2 или H 2 O пропускали над катализатором для исследования CO 2 и H 2 O допуски расплавленного алюминия 91,3 Ce 8 Pd 0,7 ленты, прокаленные при 400 ° C, как показано на рис. 9c – f. По сравнению с ответом при отсутствии CO 2 в реакционном газе добавление 15 об.% CO 2 снижает активность катализатора по отношению к окислению CO, как показано на фиг. 9c, с T 50 и T 99 80 ° C и 130 ° C соответственно. Однако при дальнейшем увеличении CO 2 до 30 об.% активность катализатора по отношению к окислению CO снижается незначительно, а T 50 и T 99 составляют 88 ° C и 140 ° C соответственно. При сжигании метана наличие 15 об.% CO 2 в реакционном газе мало влияет на каталитическую активность, и T 50 и T 99 увеличились всего на 5 ° C и 30 ° C, соответственно, по сравнению с таковыми в отсутствие CO 2 , как показано на рис. 9d. Когда концентрация CO 2 был удвоен (30 об.% CO 2 ), каталитическая активность продолжает снижаться с T 50 и T 99 350 ° C и 460 ° C соответственно. Таким образом, в случаях, когда концентрация реагента постоянна, увеличение концентрации CO 2 продукты будут формировать прочные конкурентные отношения с CO и CH 4 для адсорбции на наночастицах PdO и на его границах раздела, тем самым уменьшая количество CO или CH 4 адсорбируется в единицу времени и, следовательно, коэффициент конверсии. Однако из-за более высокой температуры реакции, необходимой для сжигания метана, десорбция CO 2 улучшается так, что CO 2 влияние на горение метана оказывается слабее, чем на окисление CO.
Результаты испытаний катализатора на долговременную стабильность и водостойкость показаны на рис. 9e и f. Для окисления CO каталитическая активность практически не снижается после 100 часов испытаний, независимо от наличия или отсутствия высокой концентрации водяного пара (20 об.%), Что указывает на то, что катализатор имеет превосходную долгосрочную стабильность и водостойкость при окислении CO. . Для сжигания метана с высокой степенью конверсии (99%) катализатор обладает аналогичными свойствами в отношении окисления CO. В то же время влияние водяного пара на горение метана при низкой конверсии (30%, 50% и 85%) также обсуждается в Дополнительном файле 1:Рисунок S6. Влияние водяного пара на каталитическую активность при низкой конверсии больше, чем при высокой. Подробные описания и обсуждения представлены в Дополнительном файле 1:Рисунок S6. Полученные выводы аналогичны сделанным Burch et al. [29]. По сравнению с водостойкостью некоторых недавно описанных катализаторов на основе Pd для сжигания метана (дополнительный файл 1:Таблица S2), PdO / CeO 2 Катализатор, приготовленный в этом исследовании, сохраняет относительно превосходную каталитическую активность после более высокой концентрации водяного пара (20 об.%) и более длительного времени реакции (100 ч), что очень полезно для дальнейшего практического применения сжигания метана.
Расход реакционного газа и концентрация O 2 известно, что они оказывают важное влияние на каталитическую активность катализатора. Здесь влияние скорости потока на каталитические характеристики очищенного от сплава Al 91,3 Ce 8 Pd 0,7 ленты, прокаленные при 400 ° C, были сначала исследованы, как показано на рис. 10а и б. Как показано на рис. 10a, для окисления CO, когда общий расход увеличился с 20 мл мин -1 (объемная скорость 12000 ч −1 ) до 100 мл мин −1 (объемная скорость 60 000 ч −1 ) конверсия CO постепенно снижалась с исходных 78 до 31%. Однако стоит отметить, что, хотя конверсия CO снижалась с увеличением скорости потока, скорость реакции ( r CO ) постепенно увеличивалась. Это явление было вызвано уменьшением времени контакта газов с активными участками при увеличении расхода газа, что привело к снижению конверсии; однако фактическое количество реагента, протекающего через активные центры в единицу времени, было увеличено, что привело к увеличению скорости реакции. Аналогичное явление наблюдалось при горении метана. Однако, похоже, что скорость потока имела немного меньшее влияние на преобразование CH 4 чем при конверсии CO. При увеличении скорости потока с 20 до 100 мл мин -1 конверсия метана снизилась с начального значения 84 до 53%. Причем скорость реакции горения метана ( r CH4 ) демонстрирует линейное увеличение скорости потока, а не имеет тенденцию оставаться стабильным, как это наблюдается для r CO . Это указывает на то, что катализатор имеет более широкий диапазон расходов при сжигании метана, чем при окислении CO. В этом исследовании рассчитанные значения r CO и r CH4 при различных условиях испытаний были в диапазоне 1,40 ~ 2,87 \ (\ left (\ times {10} ^ {- 5} \ mathrm {mol} \ cdotp {\ mathrm {g}} _ {\ mathrm {Pd}} ^ {-1} \ cdotp {\ mathrm {s}} ^ {- 1} \ right) \) и 1.51 ~ 4.70 \ (\ left (\ times {10} ^ {- 5} \ mathrm {mol} \ cdotp { \ mathrm {g}} _ {\ mathrm {Pd}} ^ {- 1} \ cdotp {\ mathrm {s}} ^ {- 1} \ right) \) соответственно.
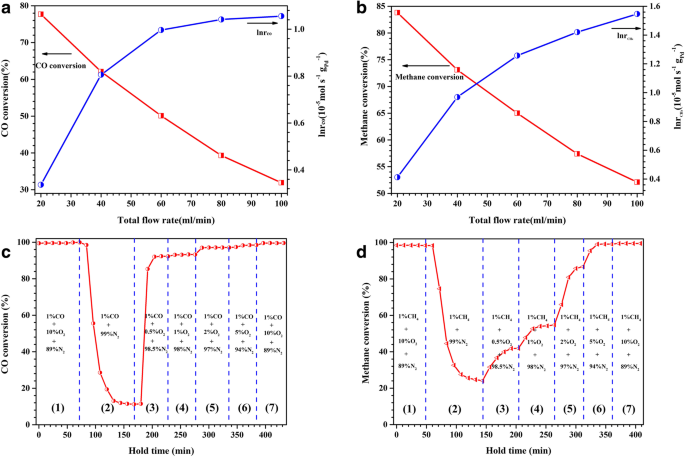
Каталитическая активность и скорость реакции освобожденного от сплава Al 91,3 Ce 8 Pd 0,7 ленты, кальцинированные при 400 ° C для окисления CO с различными расходами при 20 ° C ( a ) и для сжигания метана с разными расходами при 320 ° C ( b ) (реакционный газ 1 об.% CO / CH 4 , 10 об.% O 2 , и 89% об.% N 2 .). Каталитическая активность очищенного от сплава Al 91,3 Ce 8 Pd 0,7 ленты, прокаленные при 400 ° C для окисления CO в присутствии различных O 2 концентрации при 80 ° C ( c ) и для сжигания метана в присутствии различных O 2 концентрации при 380 ° C ( d )
Затем эффект O 2 Концентрация в реакционном газе на каталитическую активность катализатора была исследована. Для окисления CO, как показано на рис. 10c, в условиях, богатых кислородом (10 об.% O 2 ) конверсия CO поддерживалась на уровне 99%, а поскольку O 2 концентрация внезапно снизилась до 0 (анаэробные условия), конверсия CO быстро снизилась, прежде чем в конечном итоге стабилизировалась на уровне примерно 12%. Причина этого явления заключалась в том, что поверхностный решеточный кислород участвовал в реакции окисления CO. Как правило, путь окисления CO с участием решеточного кислорода на поверхности носителя является медленным и неэффективным по сравнению с прямой адсорбционной активацией O 2 молекула [30]. Следовательно, в этом исследовании конверсия CO оставалась на более низком уровне в анаэробных условиях. Этот результат также показал, что CeO 2 носитель имеет сильную способность накапливать / выделять кислород. Впоследствии 0,5% O 2 был введен в реакционный газ, и конверсия CO быстро восстановилась до 90%. Как O 2 концентрация продолжает увеличиваться, конверсия CO в конечном итоге достигла начальных 99%, и было установлено новое устойчивое состояние. Для сжигания метана (рис. 10d) наблюдали результат, аналогичный результату окисления CO, но с двумя разными точками. Во-первых, в анаэробной среде конверсия CH 4 наконец, стабилизировалась на уровне 25%, что выше, чем у анаэробной конверсии CO, что указывает на то, что высокая температура реакции может ускорить миграцию кислорода поверхностной решетки, тем самым улучшая эффективность преобразования. Второй момент заключался в том, что как O 2 концентрация увеличилась, скорость увеличения CH 4 конверсия и окончательное установление устойчивого состояния происходили медленнее, чем конверсия CO, что может быть связано с неполным сгоранием метана в условиях недостатка кислорода (0,5 ~ 2 об.% O 2 ). Этот результат также показывает, что горение метана является более сложной реакцией по сравнению с окислением CO.
На основе результатов характеризации и экспериментов предлагается простой механизм окисления CO и сжигания метана, как показано на рис. 11.
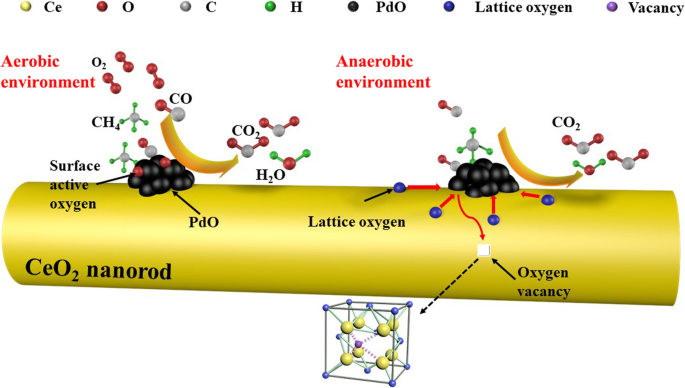
Схематическое изображение окисления CO и горения метана над стержневидным нанопористым PdO / CeO 2 катализаторы
Во-первых, CO и CH 4 Молекулы реакционного газа адсорбируются на поверхности PdO, быстро реагируя с адсорбированным и активированным кислородом на поверхности PdO, а затем с CO 2 и H 2 O продуцируются и десорбируются. Активные центры снова становятся доступными, и высокая скорость реакции окисления CO и CH 4 горение поддерживается. Стоит отметить, что реакция каталитического окисления все еще может протекать медленно в анаэробных условиях, что, как показано, связано с участием кислорода поверхностной решетки наностержней в каталитической реакции (рис. 10c, d), как показано на рис. . 11.
Большое количество экспериментальных результатов показало, что PdO / CeO 2 Катализатор, полученный удалением сплава в сочетании с прокаливанием, продемонстрировал отличную каталитическую активность в отношении окисления CO и сжигания метана и обладает выдающейся стабильностью цикла, стойкостью к CO 2 токсичность и водостойкость. Помимо присущей ему простоты, «зеленый» метод подготовки удаления легирования может эффективно избежать загрязнения наноматериалов органическими химическими веществами и другими поверхностно-активными веществами, которые являются обычными для методов мокрого химического синтеза. Кроме того, PdO / CeO 2 Катализатор, приготовленный удалением сплава в сочетании с прокаливанием, демонстрирует отличную воспроизводимость, и повторные эксперименты, подробно описанные в Дополнительном файле 1:Рисунки S7 – S10, Таблицы S3 и S4, очень хорошо доказали это. Таким образом, эта работа может дать представление о приготовлении других новых катализаторов.
Выводы
Таким образом, простой метод удаления легирования ленты Al-Ce-Pd в сочетании с прокаливанием был разработан для получения PdO / CeO 2 стержневой нанопористый композит. Результаты экспериментов показывают, что образец, полученный удалением сплава Al 91,3 Ce 8 Pd 0,7 лента в растворе 20 мас.%, а затем прокаливание при 400 ° C показало лучшую каталитическую активность в отношении окисления CO и горения метана, а также температуры реакции для полного превращения CO и CH 4 составляют 80 ° C и 380 ° C соответственно. Высокая каталитическая активность может быть объяснена хорошей дисперсией наночастиц PdO (имеющих большую удельную поверхность 102 м 2 г −1 ), сильная окислительно-восстановительная способность, взаимодействие между PdO и CeO 2 , и больше поверхностно-активного кислорода на PdO. Кроме того, катализатор также показал отличную стабильность цикла, устойчивость к CO 2 . токсичность и водостойкость, где после 100 часов испытаний каталитическая активность практически не снижалась в присутствии H 2 О. Кроме того, каталитические реакции могут происходить даже в анаэробных условиях. Эти результаты демонстрируют возможность использования комбинированного метода кальцинирования с удалением легирования для приготовления новых катализаторов. Ожидается, что метод может быть применен для изготовления аналогичных композиционных материалов.
Доступность данных и материалов
Наборы данных, подтверждающие выводы этой статьи, включены в статью.
Сокращения
- CH 4 :
-
Метан
- CO:
-
Окись углерода
- D p :
-
Размер пор
- EDS:
-
Энергодисперсионный спектрометр
- EDX:
-
Энергодисперсионные рентгеновские спектры
- FID:
-
Детектор ионизации пламенем
- H 2 -TPR:
-
Восстановление с запрограммированной температурой водорода
- S СТАВКА :
-
Удельная поверхность
- SEM:
-
Сканирующий электронный микроскоп
- ТЕМ:
-
Просвечивающий электронный микроскоп
- V p :
-
Объем пор
- XPS:
-
Рентгеновская фотоэлектронная спектроскопия
- XRD:
-
Рентгеновская дифракция
Наноматериалы
- Наночастицы для терапии рака:текущий прогресс и проблемы
- Получение и повышенная активность каталитического гидрирования наночастиц Sb / палигорскита (PAL)
- Наночастицы альбумина, содержащие ресвератрол, с длительным кровообращением и улучшенной биосовместимостью…
- Модифицированный гиперразветвленный полиглицерин как диспергатор для контроля размера и стабилизации нано…
- Синергетические эффекты наночастиц Ag / BiV1-xMoxO4 с повышенной фотокаталитической активностью
- Стимуляция роста клеток SH-SY5Y наночастицами золота, модифицированными 6-меркаптопурином и проникающим в нейро…
- Оболочки диатомовых водорослей из кремнезема, адаптированные с использованием наночастиц Au, позволяют прово…
- Переохлаждение воды, контролируемое наночастицами и ультразвуком
- Свойства наночастиц оксида цинка и их активность против микробов
- Простой подход к получению наноразмерного оксида цинка в воде / глицерине с чрезвычайно концентрированными и…



