Естественная степень диссоциации высокодисперсных наночастиц серебра с контролируемыми карбоксильными группами на микросферах PSA и их каталитические характеристики
Аннотация
Нанокомпозиты сополимера стирола и акриловой кислоты (nAg @ PSA) с высокодисперсными наночастицами серебра были получены и охарактеризованы методами просвечивающей электронной микроскопии и термогравиметрии. Количество и распределение коллоидного серебра на частицу зависело от степени диссоциации карбоксильных групп в сфере PSA. Количество карбоксильных групп оценивали по кривой титрования по электропроводности. Однако диссоциацию карбоксильных групп на PSA трудно точно определить существующими методами, поскольку степень диссоциации будет увеличиваться с увеличением примесных ионов во время титрования. Нами разработана методика определения степени диссоциации ЧСА без примесных ионов. При этом используется новая система параллельных электродов с регулируемым расстоянием. Таким образом, впервые исследована связь между распределением наносеребра и естественной диссоциацией карбоксильных групп на поверхности сфер PSA. Точное измерение и контроль диссоциации облегчили производство сфер PSA, содержащих высокодисперсные наночастицы серебра. Каталитические свойства свежеприготовленных катализаторов nAg @ PSA изучали путем восстановления 4-нитрофенола. Контролируя степень естественной степени диссоциации карбоксильной группы на сфере PSA, можно управлять и получать дисперсию наночастиц серебра. Они обеспечивают легкий синтез, высокие каталитические характеристики и хорошую пригодность для вторичной переработки.
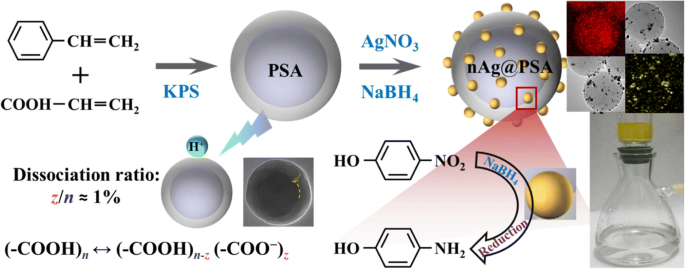
Введение
В последнее время большое внимание привлекает получение композитных микросфер ядро-оболочка, содержащих диэлектрическую твердую сферу, покрывающую металлическую оболочку. Этот интерес был вызван их уникальными каталитическими и оптическими свойствами. Эти микросферы ядро-оболочка обладают значительным потенциалом в широком диапазоне применений, таких как комбинационное рассеяние света с усилением поверхности (SERS) [1,2,3,4,5], катализ [6,7,8,9,10], наноинженерия оптических резонансов [11, 12], фотонных кристаллов [13,14,15] или биохимии [16, 17] для таких приложений, как химические сенсоры. Многие усилия были сосредоточены на получении композитных наносфер ядро-оболочка с благородными металлическими оболочками благодаря их новым оптическим и каталитическим свойствам [18]. Одна из наиболее часто изучаемых систем - композитные микросферы с серебряной оболочкой. Были изучены различные методы синтеза, в том числе самосборка [19], нанесение затравки [18], последовательная адсорбция и реакция ионного слоя (SILAR) [20] и осаждение восстановления на месте [21].
Однако имеется немного сообщений о контролируемом приготовлении серебряных оболочек на поли (стироле- co -акриловая кислота) поверхности микросфер. Количество наночастиц серебра, нанесенных на поли (стирол- co -акриловая кислота) композитных наносфер определяется несколькими факторами, включая температуру, количество карбоксильных групп и количество диссоциированных зарядов вокруг сфер PSA. Влияние температуры на осаждение наночастиц Ag исследовано и описано в литературе [22]. Количество карбоксильных групп изучено методами кондуктивного титрования [19]. Число диссоциированных зарядов обычно меньше стехиометрического числа, потому что поведение слабой кислоты зависит от ионной силы. Добавление солей электролита во время электрохимических измерений неизмеримо увеличивает степень диссоциации карбоксильных групп. Следовательно, количественная оценка количества диссоциированных зарядов в латексных суспензиях затруднительна. Тем не менее количество диссоциированных карбоксильных групп на частицу влияет на осаждение наночастиц серебра и было изучено здесь с использованием системы параллельных электродов с регулируемым расстоянием. Это облегчает контролируемое получение наночастиц серебра.
Некоторые области применения поли (стирола- co , содержащего наночастицы серебра) -акриловая кислота) наносферы [22,23,24]. Ли и его сотрудники [22] получили покрытый наночастицами серебра поли (стирол- co -акриловая кислота) композитных наносфер, а затем использовали эти наносферы в качестве подложек для спектроскопии комбинационного рассеяния с усилением поверхности (SERS). Сонг и соавторы [24] синтезировали поли (стирол- co ), содержащий наночастицы серебра. -акриловая кислота) наносферы в качестве антибактериальных агентов. Тем не менее, мало исследований было проведено в отношении каталитического применения полистирола, содержащего наночастицы серебра, co -акриловая кислота). Удивительно, но нет сообщений о связи между дисперсией наночастиц Ag и степенью диссоциации карбоксильных групп. В нашей предыдущей работе [23] сообщалось о грубой взаимосвязи между карбоксильными группами и наночастицами серебра по результатам термогравиметрии и ПЭМ. На этот раз мы поднимаем новую точку зрения, основанную на естественном соотношении диссоциации карбоксильной группы, путем разработки нового точного электрохимического измерения.
В этом отчете описывается точная характеристика естественной степени диссоциации карбоксильной группы сфер PSA с помощью двух проволочных электродов для предотвращения проникновения примесей. Мы синтезировали четыре размера латексных частиц, чтобы варьировать величину диссоциированных зарядов. Затем было исследовано формирование хорошо распределенных наночастиц серебра, расположенных на наносферах PSA. Поли (стирол- co -акриловая кислота) наносферы предлагают большую площадь поверхности для иммобилизации наночастиц серебра и контролируемое количество диссоциированных карбоксильных групп для хорошего распределения наночастиц серебра. Эта часть кажется похожей на нашу предыдущую работу [23]. Тем не менее, есть один важный прогресс в этой работе, который необходимо отметить:это естественная степень диссоциации карбоксильной группы, которая в основном определяет количество наночастиц Ag, а не общее количество карбоксильных групп. Этот вывод может быть установлен только при точном измерении степени естественной диссоциации карбоксильной группы. Такие высокодисперсные наночастицы серебра на нанокомпозите nAg @ PSA демонстрируют высокие каталитические характеристики при использовании восстановления 4-нитрофенола в качестве модельной реакции. Это имеет интересный потенциал для будущих исследований.
Результаты и обсуждение
Количество карбоксильных групп в наносферах PSA
На рис. 1 показаны микрофотографии, полученные с помощью сканирующего электронного микроскопа, и соответствующие распределения частиц по размерам четырех видов наносфер PSA. Частицы были сферическими с хорошо контролируемым распределением частиц по размерам. Размеры частиц были исследованы с помощью SEM, и был рассчитан объем наносфер. Размеры приведены в таблице 1. Объем наносферы, плотность суспензии суспензии PSA и количество сфер в исходных суспензиях определялись ранее опубликованным методом [23, 25, 26, 27].
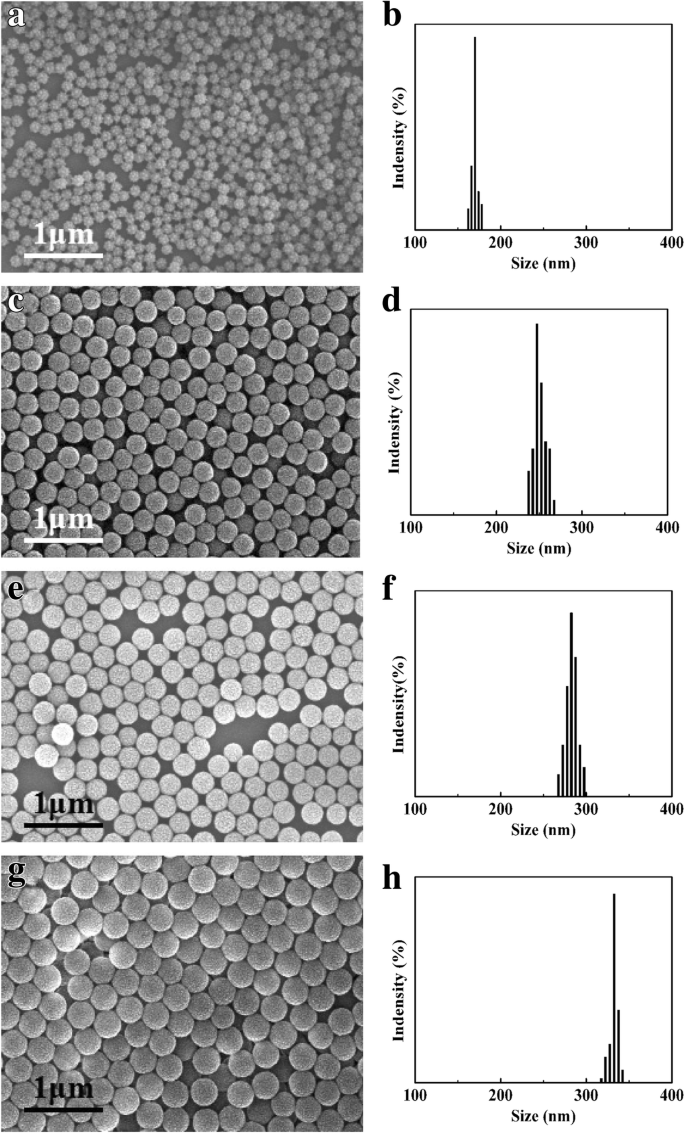
СЭМ-микрофотографии и гистограммы распределения частиц по размерам наносфер PSA: a , b PSA1; c , d PSA2; е , f PSA3; г , ч PSA4
Количество карбоксильных групп на частице определяли титрованием по проводимости, о котором сообщалось ранее [23]. Уровни карбоксильной нагрузки (на частицу) перечислены в таблице 1. На рисунке 2 показан логарифмический график общего количества карбоксильных групп на частицу с диаметрами сферы PSA. График показывает линейную зависимость с наклоном 2,0. Это свидетельствует о том, что карбоксильная группа может в основном распределяться на сферической поверхности, а не в фазовом объеме.
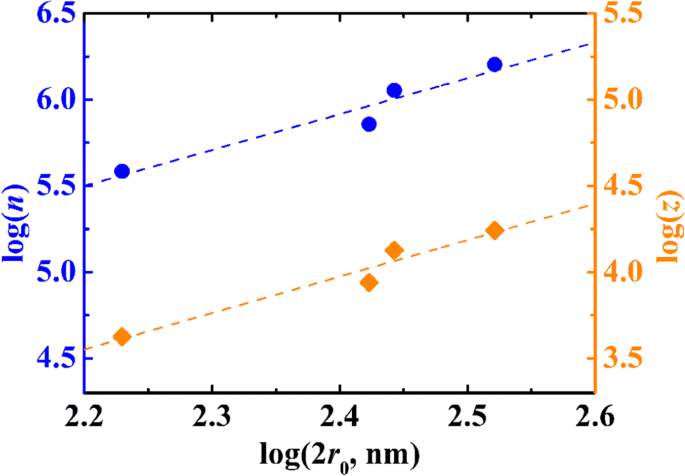
Логарифмические графики количества −COOH и −COO + на частицу относительно диаметра сфер PSA
Коэффициент естественной диссоциации карбоксильных групп на наносферах PSA
Ячейку заполняли суспензией PSA с известной концентрацией латекса. Затем прикладывали переменное напряжение 10 мВ, чтобы получить переменное сопротивление подвески между параллельными проволочными электродами. Выражение для сопротивления раствора между двумя параллельными проводами приблизительно равно [22]
$$ {R} _S =0.916 \ frac {\ log \ left (d / a-1 \ right)} {Lc \ varLambda} $$ (1)Здесь Λ - молярная проводимость суспензии PSA с концентрацией c , d расстояние между двумя электродами, a - радиус Pt проволоки, а L - длина Pt проволоки, погруженной в суспензию. Сопротивление суспензии получали с помощью графиков Найквиста. Значения Z 1 были нанесены на график ( d / а - 1) для некоторых частот на рис. 3. График для заданной частоты попал на линию с общим наклоном. Это показывает положительные перехваты в log ( d / а - 1) =0 или d =2 а . Линейный график частично поддерживается формулой. (1), и это не удовлетворяет пропорциональности уравнения. (1) по внешнему виду (положительные значения точек пересечения). Перехват означает, что сопротивление появится, если два электрода войдут в контакт друг с другом. Это сопротивление должно быть расположено на границе раздела или включено в двойной слой. Наклон линейности, равный 0,916 / LcΛ , согласно формуле. (1), не должно зависеть от частоты. Значения молярной проводимости (основанные на молярной концентрации сфер PSA, рассматривая сферу PSA как огромный носитель заряда) были рассчитаны и усреднены по частотам более 150 Гц от наклона; они перечислены в таблице 1. Поскольку одна сфера PSA несет огромное количество -COOH, эти значения намного больше, чем у обычных ионов. На рис. 3 представлена зависимость молярной проводимости от диаметров сферы ЧСА. Они лежат на прямой с наклоном 2,9, что означает \ (\ varLambda ={kr} _0 ^ 3 \). Это означает, что крупные частицы должны значительно увеличивать молярную проводимость, поскольку заряды аккумулируются на одной сфере.
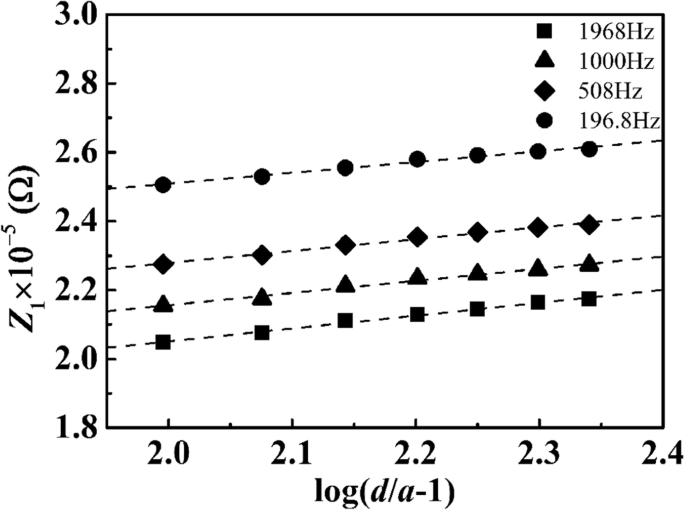
График зависимости реальной части импеданса переменного тока типичной подвески ВАБ от log ( d / а - 1) для частот f =196,8, 508, 1000 и 1968 Гц соответственно
Как мы описали ранее [23, 26], молярная проводимость латексной суспензии на N A частицы латекса были определены как сумма молярной проводимости z свободные ионы водорода, zλ H , а проводимость N A слева z заряжен −COO - несущая сфера PSA, λ L :
$$ {\ varLambda} _ {\ mathrm {L}} =z {\ lambda} _ {\ mathrm {H}} + {\ lambda} _ {\ mathrm {L}} $$ (2)Ионная проводимость выражается через коэффициент диффузии D , через
$$ \ lambda =\ frac {Dz ^ 2 {F} ^ 2} {RT} $$ (3)Когда уравнение. (3) для иона водорода λ H = F 2 Д H / RT , и частица латекса λ L = F 2 г 2 Д L / RT вставлены в формулу. (2) получаем
$$ {\ varLambda} _ {\ mathrm {L}} =\ left ({F} ^ 2 / RT \ right) \ left ({zD} _ {\ mathrm {H}} + {z} ^ 2 {D } _ {\ mathrm {L}} \ right) $$ (4)Здесь D H и D L представляют собой коэффициенты диффузии иона водорода и −COO - несущая сфера PSA соответственно. Д L был оценен уравнением Стокса-Эйнштейна, а затем вставлен в уравнение. (4) с D H (9,3 × 10 −9 м 2 s −1 ), решая уравнение для z . Результаты приведены в таблице 1. На рисунке 4 показан график z с диаметрами сферы PSA. Наклон линии равен 2,1, что почти равно наклону линейности n . против 2 r 0 . Значение z / н было 0,01. Это было рассчитано в соответствии с таблицей 1, которая представляет диссоциацию карбоксила в частице как
$$ {\ left (- \ mathrm {COOH} \ right)} _ n \ leftrightarrow {\ left (- \ mathrm {COOH} \ right)} _ {nz} \ {\ left (- {\ mathrm {COO}} ^ {-} \ right)} _ z + z {\ mathrm {H}} ^ {+} \ \ left (100 \ leftrightarrow 99:1:1 \ right) $$ (5A)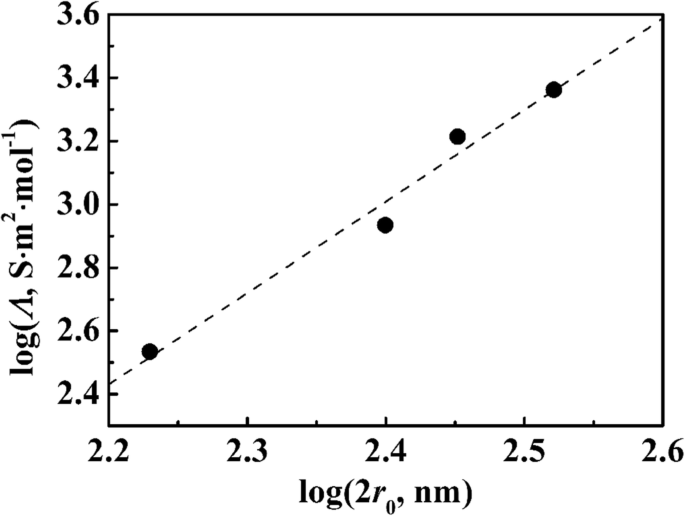
Изменение молярной проводимости от диаметров для суспензий PSA в логарифмическом масштабе
Это значение указывает на то, что естественная степень диссоциации –COOH составляла всего 1%. Другая часть находится в нейтральной форме –COOH.
Вставив этот результат в уравнение. (5A):
$$ {\ left (- \ mathrm {COOH} \ right)} _ {100} \ leftrightarrow {\ left (- \ mathrm {COOH} \ right)} _ {99} {\ mathrm {COO}} ^ {- } + {\ mathrm {H}} ^ {+}. $$ (5B)Проводимость в основном вызвана образованием (AH) 99 A - и H + через реакцию (5B).
Чтобы подтвердить надежность этих методов и полученных результатов, мы построили рассчитанные значения λ L / D против z 2 для четырех частиц латекса и одновалентных материалов (для z =1) в логарифмическом масштабе на рис. 5. Как и ожидалось, это показывает, что прямая линия прошла через значения одновалентных материалов. Согласно формуле. (3) значения λ / Dz 2 (= F 2 / RT ) должен быть постоянным и не зависеть от диаметра или других свойств частиц.
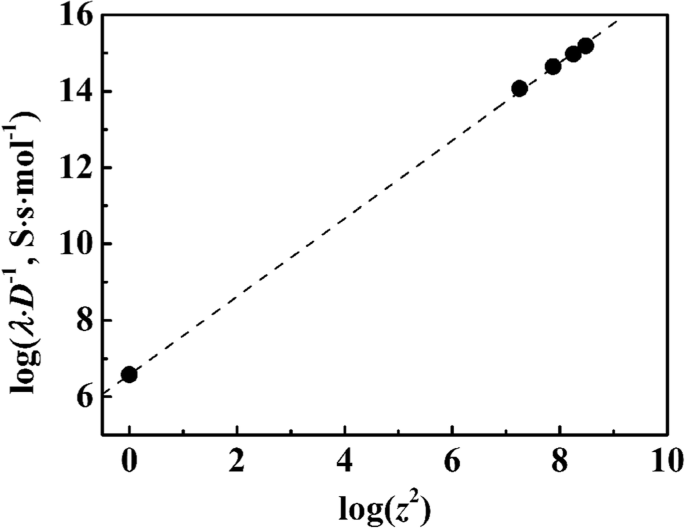
Логарифмический график λ · D -1 против z 2 для четырех суспензий PSA и галогенид-ионов
Механизм наночастиц серебра, поддерживаемых на наносферах PSA
PSA1 – PSA4 был выбран в качестве базальных сфер для приготовления композитных наносфер nAg @ PSA1 – nAg @ PSA4 при сохранении постоянных всех остальных параметров (часть «Материалы и методы»). ПЭМ-микрофотографии нанокомпозитов nAg @ PSA1 – nAg @ PSA4 показаны на рис. 6. Из микрофотографий видно, что PSA, покрытый наночастицами серебра, был очевиден. По мере того, как наносферы PSA становились больше, все большее количество наночастиц серебра закреплялось на наносферах PSA. Соответственно увеличивалось покрытие и однородность наночастиц серебра на наносферах PSA. На рис. 7а представлена микроструктура наночастиц Ag, покрытых наносферами PSA. Шаг решетки наночастицы серебра составляет 0,23 нм, что соответствует плоскости (111) кристалла серебра. Это подтвердило успешное осаждение наночастиц Ag. Осаждение наночастиц Ag также можно проверить по данным энергодисперсионной рентгеновской спектроскопии (EDX). EDX-картирование соответствующих элементов Ag и C, представленное на рис. 7b, показало однородное распределение этих элементов. Спектр EDX подтвердил присутствие Ag, C и O (рис. 7c). Медь из поддерживающей медной сетки.

ПЭМ-изображения нанокомпозитов nAg @ PSA. а - г , что соответствует nAg @ PSA1 – nAg @ PSA4
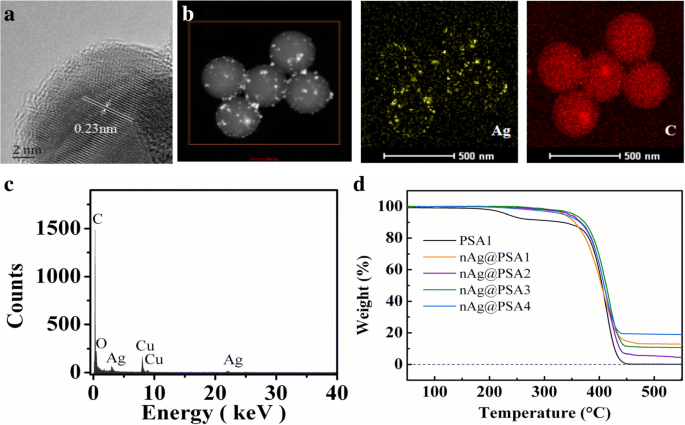
а ПЭМ-изображение Ag на наносферах PSA4. б EDX-картирование композитных наносфер nAg @ PSA4. c EDX-спектр композитных наносфер nAg @ PSA4. г Кривые ТГ композитных сфер nAg @ PSA1-nAg @ PSA
Термогравиметрический анализ был использован для дальнейшей количественной характеристики наночастиц серебра, покрытых наносферами PSA. Кривые ТГ наносфер PSA1 и композитных наносфер nAg @ PSA, полученных из наносфер PSA1 – PSA4, показаны на рис. 6d. Данные ТГ позволили рассчитать весовой вклад наночастиц серебра в состав композитных наносфер. Затем мы могли бы оценить количество наночастиц серебра с помощью веса p . Взаимосвязь между распределением наночастиц серебра и степенью диссоциации карбоксильных групп показана на рис. 8. Очевидно, что среднее количество частиц серебра на одну частицу PSA линейно увеличивается с количеством диссоциированных карбоксильных групп. Этот результат может быть связан с образованием наночастиц серебра на поверхности композита. Отрицательно заряженные карбоксильные группы притягивают положительно заряженные катионы серебра за счет образования ионных пар. Присоединенные ионы серебра восстанавливаются боргидридом натрия, и это быстродействующий восстанавливающий агент, который может вызвать образование ядер серебра. Образовавшиеся ядра серебра действуют как центры зародышеобразования; рост происходит за счет диффузии ионов серебра в растворе к поверхности частиц. Их можно интерпретировать как гетерогенные центры зародышеобразования / роста, в конечном итоге образующие наночастицы серебра. Формирование наночастиц серебра во многом определяется балансом скорости зародышеобразования и роста частиц.
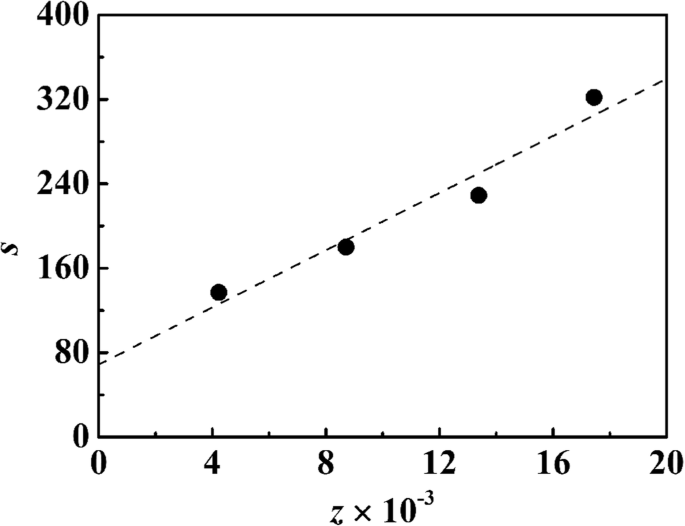
Изменение количества наночастиц серебра в зависимости от числа −COO + на частицу
Каталитическая производительность
Восстановление 4-нитрофенола до 4-аминофенола является модельной каталитической реакцией и использовалось для оценки каталитической активности нанокомпозитов nAg @ PSA. Каталитическую реакцию контролировали с помощью УФ-видимой спектроскопии. Смесь NaBH 4 и 4-нитрофенол показал полосу поглощения при 400 нм, соответствующую 4-нитрофенолят-иону. На рис. 9a – c проиллюстрирована реакция восстановления 4-нитрофенола, наблюдаемая в разное время с использованием различных количеств nAg @ PSA4 в качестве катализатора. Интенсивность полосы поглощения при 400 нм постепенно уменьшалась и со временем исчезла. Это сопровождается появлением новой полосы около 300 нм, соответствующей 4-аминофенолу. Это указывает на превращение 4-нитрофенола в 4-аминофенол. Во время этого процесса реакции общие концентрации NaBH 4 и 4-нитрофенол составляли 36 мМ и 0,12 мМ соответственно. Концентрация 4-нитрофенола пропорциональна его оптической плотности; концентрация во время реакции t ( C t ) и время t =0 ( C 0 ) эквивалентны поглощению во время реакции t ( А t ) и время t =0 ( A 0 ). На рис. 9d показаны графики ln ( A t / А 0 ) от времени реакции в секундах. Результаты показали, что ln ( A t / А 0 ) линейно уменьшалась со временем. Это следует за кинетическим поведением псевдопервого порядка. Константа скорости k при комнатной температуре рассчитывали по наклону, и константы nAg @ PSA4, содержащего 0,0041 мг Ag, nAg @ PSA4, содержащего 0,0054 мг Ag, и nAg @ PSA4, содержащего 0,0068 мг Ag, составили 1,66 × 10 - 3 s −1 , 4,52 × 10 −3 s −1 , и 6.80 × 10 −3 s −1 , соответственно. Эти результаты показали, что чем больше количество катализатора, тем выше скорость реакции. Наибольшая константа скорости k при комнатной температуре сопоставим с аналогом ранее описанных нанокомпозитных катализаторов Ag, например 0,7 × 10 -2 s −1 из G 4 -ПАМАМ-NH 2 (Ag 12 ) [28], 1,274 × 10 −2 s −1 из Ag 10 @ SBA-15 [29], 6,2 × 10 −3 s −1 CNFs / AgNPs [30], и 31.64 × 10 −2 мин −1 из [AgCl 2 ] - сложный [31].
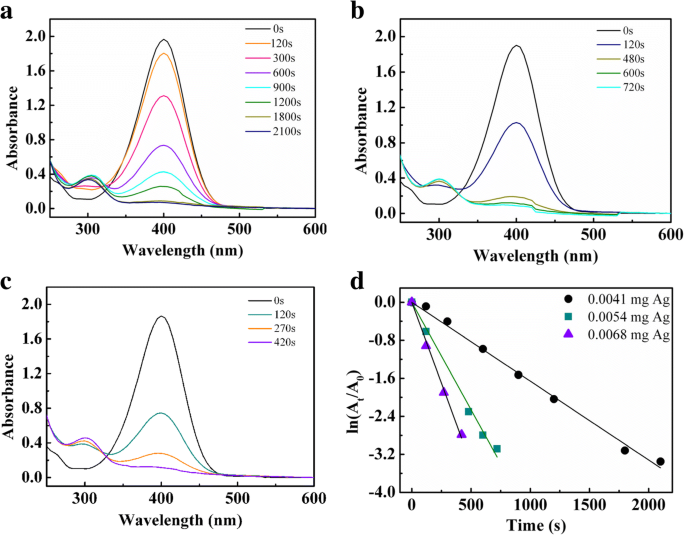
а УФ-видимые спектры 0,12 мМ 4-NP с 36 мМ NaBH 4 в присутствии нанокомпозитов nAg @ PSA4 (содержащих 0,0041 мг Ag). б УФ-видимые спектры 0,12 мМ 4-NP с 36 мМ NaBH 4 в присутствии нанокомпозитов nAg @ PSA4 (содержащих 0,0054 мг Ag). c УФ-видимые спектры 0,12 мМ 4-NP с 36 мМ NaBH 4 в присутствии нанокомпозитов nAg @ PSA4 (содержащих 0,0068 мг Ag). г График ln (A t / A 0 ) от времени реакции в присутствии nAg @ PSA4 в качестве катализатора
Реакции восстановления 4-нитрофенола с использованием nAg @ PSA2 и nAg @ PSA3 в качестве катализатора показаны на рис. 10a, b. При таком же добавлении серебра константы скорости nAg @ PSA2, nAg @ PSA3 и nAg @ PSA4 составили 2,92 × 10 3 s −1 , 5,07 × 10 3 s −1 , и 6.80 × 10 3 s −1 соответственно (рис. 10в). Эти результаты демонстрируют, что каталитические характеристики nAg @ PSA возрастают с увеличением диаметра наносфер PSA или количества частиц серебра на частицу PSA. С увеличением диаметра сферы PSA изготовленная каталитическая пленка будет более полипористой с более высокой дисперсностью наночастиц Ag. Более высокая дисперсность дает больше возможностей для реагентов, достигающих поверхности наночастиц Ag. Рисунок 10d, e показывает, что скорости реакции увеличиваются с увеличением размера частиц серебра и количества серебра на квадратный сантиметр поверхности наносфер PSA, соответственно. Рисунок 10f показывает, что скорость реакции увеличивается с уменьшением количества наносфер на кубический сантиметр суспензии nAg @ PSA.
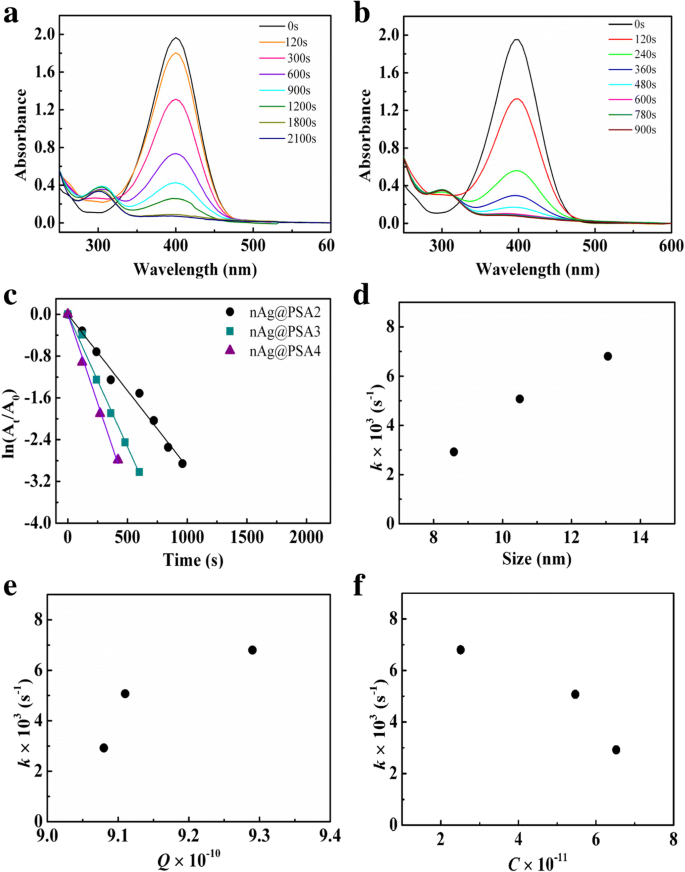
а УФ-видимые спектры 0,12 мМ 4-NP с 36 мМ NaBH 4 в присутствии нанокомпозитов nAg @ PSA2 (содержащих 0,0068 мг Ag). б УФ-видимые спектры 0,12 мМ 4-NP с 36 мМ NaBH 4 в присутствии нанокомпозитов nAg @ PSA3 (содержащих 0,0068 мг Ag). c Участок ln (A t / A 0 ) от времени реакции в присутствии нанокомпозитов nAg @ PSA (содержащих 0,0068 мг Ag), полученных из наносфер PSA2 – PSA4. г Влияние размера наночастиц серебра на константу скорости. е Влияние количества серебра на квадратный сантиметр поверхности наносфер PSA на константу скорости. е Влияние количества наносферы на кубический сантиметр суспензии nAg @ PSA на константу скорости
Для оценки возможности повторного использования нанокомпозиты nAg @ PSA были нанесены на воронку из стеклянного песка, чтобы сформировать каталитическую мембрану. Когда реакционная смесь (36 мМ NaBH 4 и 0,12 мМ 4-NP), прошедшего через мембрану, желтый цвет в реакционной смеси исчез, что свидетельствует о быстрой каталитической реакции (фиг. 11a). Степень превращения 4-нитрофенола определяли по A t / А 0 при λ =400 нм. Согласно фиг. 11b, степень конверсии составила 96% после прохождения через каталитическую мембрану. Более того, из рис. 11c видно, что каталитическая мембрана была активна до восьми циклов восстановления 4-нитрофенола - это подтверждает высокую возможность повторного использования катализатора.
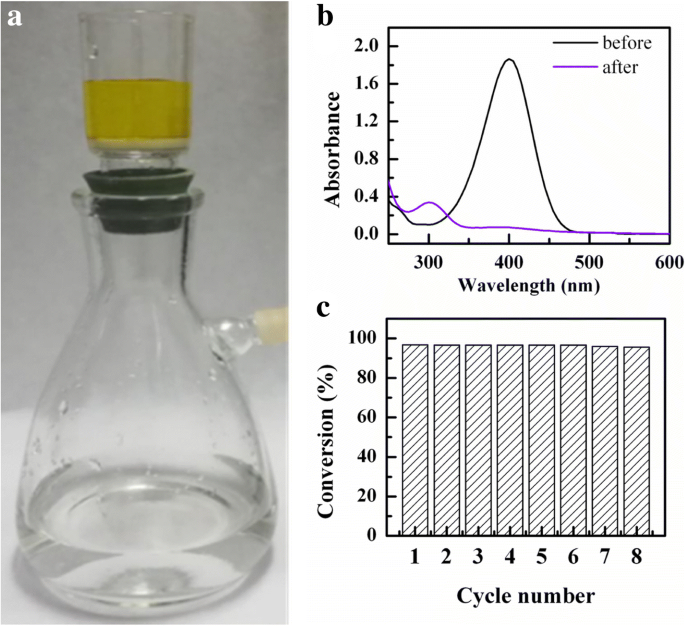
а Фотография, показывающая быстрое восстановление 4-NP, проходящего через каталитическую мембрану nAg @ PSA. б УФ-видимые спектры 0,12 мМ 4-NP с 36 мМ NaBH 4 до и после прохождения через каталитическую мембрану nAg @ PSA. c Коэффициент конверсии 4-НП при циклическом тестировании
Выводы
Мы синтезировали монодисперсный поли (стирол- co -акриловая кислота) (PSA) посредством эмульсионной полимеризации без мыла, а композитные наносферы nAg @ PSA могут быть легко получены путем восстановления нитрата серебра in situ с помощью боргидрида натрия в водном растворе. СЭМ-микрофотографии наносфер PSA показали, что наносферы PSA были сферическими с узким распределением частиц по размерам. График зависимости карбоксила от диаметров был линейным с наклоном 2,0. Это указывает на то, что карбоксильные группы в основном распределены на поверхности наносфер PSA. Диссоциация должна происходить на поверхности частицы, а не внутри частицы по объему, потому что количество диссоциированных карбоксильных групп пропорционально площади поверхности латексной частицы. Сумма ( z ) диссоциированных карбоксильных групп составляет 1% от количества ( n ) карбоксильных групп. ПЭМ подтвердила образование наночастиц серебра, нанесенных на наносферы PSA. Диссоциированные заряды на поверхности наносфер PSA оказали большое влияние на покрытие наночастиц Ag на наносферах PSA. Каталитические свойства наносфер nAg @ PSA были исследованы при катализе восстановления 4-нитрофенола. Эти синтезированные наносферы nAg @ PSA содержали высокодисперсные наночастицы серебра с высокой каталитической активностью и хорошей пригодностью для вторичной переработки.
Материалы и методы
Материалы
Акриловая кислота (AA), персульфат калия (KPS), боргидрид натрия (NaBH 4 ), нитрат серебра (AgNO 3 ) и гидроксид натрия были приобретены у Aladdin Chemical Reagent Co., Ltd. (Шанхай, Китай). Стирол (St) был поставлен компанией Tokyo Chemical Industry Co., Ltd. (Токио, Япония). Все химические вещества были аналитической чистоты и использовались в том виде, в котором они были получены, если не указано иное.
Синтез наносфер PSA
Наносферы PSA были приготовлены согласно литературным данным [22,23,24, 32, 33]. Обычно AA и H 2 Первоначально в стеклянную колбу загружали O (130 мл). Стирол добавляли после растворения подаваемого АК. Затем колбу нагревали до 75 ° C при перемешивании в условиях азота. Полимеризация была инициирована после того, как раствор KPS (20 мл) был впрыснут, а затем выдержан при 75 ° C в течение 12 часов. Остальные рабочие параметры приведены в таблице 2. Продукты очищали семью циклами центрифугирования-редиспергирования в дистиллированной воде, а затем окончательно диспергировали в воде.
Подготовка композитных наносфер nAg @ PSA
Типичная процедура изготовления нанокомпозитов nAg @ PSA [22,23,24] описывается следующим образом:дисперсия PSA (500 мл, 0,3 мг мл -1 ) смешивали с водным раствором AgNO 3 (12,5 мл, 10 мМ) в стеклянной колбе. Дисперсию смеси перемешивали при 300 об / мин -1 . в течение 5 ч при комнатной температуре. После этого NaBH 4 (12,5 мл, 10 мМ) добавляли к дисперсии и полученной смеси давали возможность реагировать при 0 ° C в течение 2 часов при перемешивании. Суспензию центрифугировали (20 мин, 12000 об / мин -1 ), осадок промывали 30 мл дистиллированной воды. Этот цикл центрифугирования-редиспергирования повторяли четыре раза для удаления примесей.
Эксперименты по каталитической производительности
Реакцию 4-нитрофенола боргидридом натрия, катализируемую нанокомпозитами nAg @ PSA, проводили в водном растворе. Процедура реакции была следующей:NaBH 4 водный раствор (4,5 мл, 80 мМ) смешивали с раствором 4-NP (0,5 мл, 2,4 мМ) в 10-мл пробирке Эппендорфа. Затем в раствор смеси добавляли нанокомпозиты nAg @ PSA и доводили объем до 10 мл дистиллированной водой. Сразу после этого аликвоту помещали в кварцевую кювету с длиной пути 1 см для УФ-видимой спектроскопии.
Суспензию nAg @ PSA4 (содержащую 1,3538 мг Ag) фильтровали через воронку из стеклянного песка, снабженную фильтровальной конической колбой, наносили на фильтровальную бумагу и промывали дистиллированной водой (100 мл). 10 мл раствора (36 мМ NaBH 4 и 0,12 мМ 4-NP) подвергали вакуумной фильтрации в воронке, покрытой мембраной nAg @ PSA4. Собранный раствор в конической колбе охарактеризовали с помощью УФ-видимой спектроскопии. Чтобы оценить возможность повторного использования катализатора nAg @ PSA4, мембрану промыли дистиллированной водой и использовали повторно.
Система и инструменты параллельных электродов с регулируемым расстоянием
Системы параллельных электродов с регулируемым расстоянием состояли из двух платиновых проволок диаметром 0,1 мм и позиционера xz. Как показано на рис. 12, один из проводов был закреплен, и расстояние d было скорректировано перемещением y ось позиционера xz. Длина погружена в раствор, контролируемая z ось позиционера xz. Импеданс переменного тока на другом расстоянии был получен согласно нашим предыдущим работам [25,26,27].
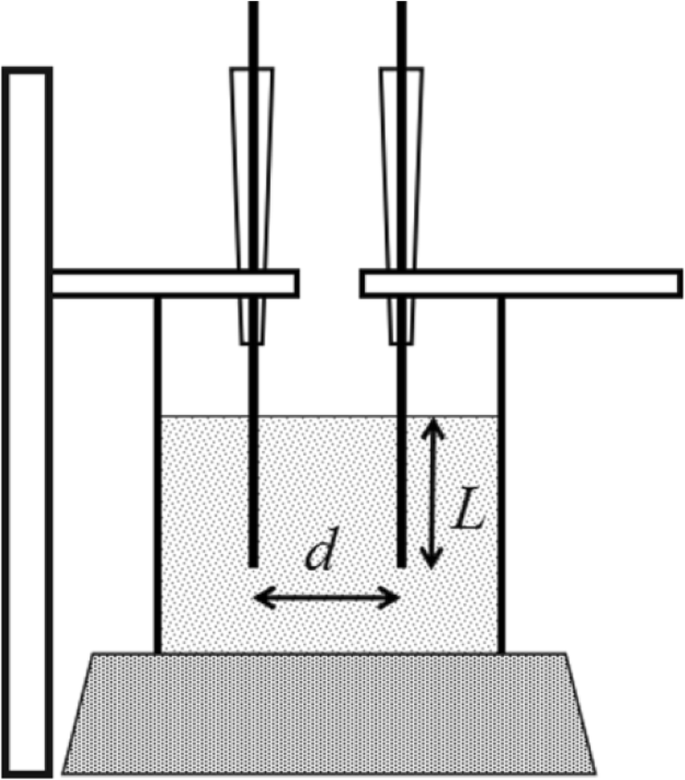
Иллюстрация параллельной системы электродов с регулируемым расстоянием
The nanoparticle features and the location of the silver particles on the latex surface were investigated by SEM and TEM (JEOL JEM-2010, JEOL Ltd., Tokyo, Japan). The content of silver nanoparticle coatings on PSA nanospheres was analyzed by thermogravimetric analysis (Perkin Elmer Pyris 1, Perkin-Elmer Co., USA). The UV-Vis spectra were recorded on Shimadzu UV-2550 spectrophotometer (Shimadzu, Kyoto, Japan) at room temperature.
Сокращения
- a :
-
The radius of Pt wire
- d :
-
The distance between two electrodes
- D H and D L :
-
The diffusion coefficients of hydrogen ion and −COO — carrier PSA sphere, respectively
- L :
-
The length of Pt wire immersed in suspension
- n :
-
The number of −COOH per PSA microsphere
- nAg@PSA:
-
Silver nanoparticle-loaded poly(styrene-co-acrylic acid) nanocomposites
- PSA:
-
Poly(styrene-co-acrylic acid) nanospheres
- z :
-
The number of –COO — per PSA microsphere
- Λ :
-
The molar conductivity of the PSA suspension with concentration c
Наноматериалы
- Многофункциональные наночастицы золота для улучшенных диагностических и терапевтических применений:обзор
- Получение наночастиц mPEG-ICA, нагруженных ICA, и их применение в лечении LPS-индуцированного повреждения клеток H9c2…
- Получение и повышенная активность каталитического гидрирования наночастиц Sb / палигорскита (PAL)
- Влияние отношения Li / Nb на получение и фотокаталитические характеристики соединений Li-Nb-O
- Синтез и эффективность in vitro покрытых полипирролом железо-платиновых наночастиц для фототермической терапии…
- Высокоэффективное определение H2 для многослойных гетеропереходов MoS2 / SiO2 / Si за счет декорирования поверхнос…
- Зеленая способность к синтезу и стабилизации наночастиц меди:каталитическая, антибактериальная, цитотоксич…
- Последние достижения в синтетических методах и применении серебряных наноструктур
- Влияние кислотного пептизирующего агента на соотношение анатаз-рутил и фотокаталитические характеристики н…
- Сапонины Platycodon из Platycodi Radix (Platycodon grandiflorum) для зеленого синтеза наночастиц золота и серебра



