Синтез квантовых точек ZnSe / CdS / ZnS Core / Shell с подавленной реабсорбцией и их применение для иммуносорбентного анализа
Аннотация
Мы сообщаем о бесфосфиновом однореакторном методе синтеза квантовых точек (КТ) ядро-оболочка ZnSe / CdS / ZnS с составными структурами типа II / типа I и соответствующими свойствами подавления реабсорбции. Синтезированные КТ обладают высокой эффективностью красного излучения (с квантовым выходом 82%) и высокой оптической стабильностью. По сравнению с квантовыми точками типа I, квантовые точки ZnSe / CdS / ZnS демонстрируют больший стоксов сдвиг и меньшую реабсорбцию, что может снизить потери на эмиссию и улучшить уровень флуоресцентного выхода. КТ ZnSe / CdS / ZnS используются в качестве флуоресцентных меток для использования их в иммуноферментном анализе с флуоресценцией (FLISA), впервые при обнаружении C-реактивного белка (CRP) с пределом обнаружения (LOD) 0,85. нг / мл, что более чувствительно, чем у КТ CdSe / ZnS типа I на основе FLISA (1,00 нг / мл). Результаты показывают, что КТ ZnSe / CdS / ZnS типа II / типа I могут быть хорошими кандидатами для применения в обнаружении биомедицинской информации.
Фон
Флуоресцентные полупроводниковые квантовые точки (КТ) ядро / оболочка характеризуются превосходными оптическими свойствами, такими как более широкий диапазон излучения, более высокие квантовые выходы (QY) фотолюминесценции (ФЛ) и более высокая оптическая и химическая стабильность, чем у традиционных органических красителей. Эти преимущества открывают возможности для революционных достижений в области флуоресцентных меток для биомедицинской диагностики, молекулярной визуализации и фотоэлектрического поля [1,2,3,4,5,6,7]. В соответствии с выравниванием полос между материалами ядра и оболочки КТ ядро / оболочка можно разделить на структуры типа I, обратного типа I и типа II. КТ типа I, характеризующиеся «вложенной» структурой выравнивания полос, которая может ограничивать как электроны, так и дырки в области сердцевины, чтобы усилить излучательную рекомбинацию и физически отделить поверхность оптической активной сердцевины от окружающей среды и, таким образом, улучшить интенсивность ФЛ. и оптическая стабильность [6,7,8,9]. Несмотря на эти благоприятные свойства, небольшой стоксов сдвиг (всего несколько десятков нанометров), называемый разницей между спектром поглощения и спектром ФЛ, вызывает серьезное реабсорбцию, что приводит к общим потерям излучения и ограничивает их применение в количественном определении [10, 11]. Напротив, квантовые точки типа II с шахматным выравниванием запрещенной зоны способствуют пространственному разделению электрона и дырки в различных областях структуры ядро / оболочка. Последующая энергия рекомбинационного перехода края зоны e – h меньше ширины запрещенной зоны любого из составляющих компонентов материала, что приводит к значительному смещению в красную область излучения, которое недоступно для любого из монокомпонентных материалов. Сила осциллятора первой особенности экситонного поглощения квантовых точек второго типа резко уменьшается по сравнению с остовными квантовыми точками [12,13]. Сильно смещенное в красную область излучение и сплющенный пик поглощения первого экситона уменьшают перекрытие спектров поглощения и излучения, что подавляет реабсорбцию, и способствует количественному биологическому обнаружению. Типичные квантовые точки ZnSe / CdS типа II имеют перестраиваемое излучение от синевато-фиолетового до красного диапазона и подавленное реабсорбцию [13]. Однако электроны, делокализованные в оболочке CdS, уязвимы для захвата поверхностными дефектами или окружающей средой, что приводит к низкому квантовому выходу флуоресценции. Возможным решением является покрытие КТ ZnSe / CdS самой внешней оболочкой из ZnS не только для пассивирования поверхности для увеличения квантового выхода и оптической стабильности, но и для ограничения утечки токсичного элемента Cd, что снижает биотоксичность. До сих пор большинство исследований было сосредоточено на квантовых точках типа I, и лишь некоторые из них были выполнены на квантовых точках ZnSe / CdS / ZnS типа II / типа I [12,13,14,15]. Более того, во всех исследованиях процесса синтеза квантовых точек ZnSe / CdS / ZnS использовалось двухэтапное приготовление путем предварительной очистки сырых квантовых точек ядра ZnSe и использовались токсичные и дорогие фосфины. Кроме того, ни в одном из них не использовались квантовые точки ZnSe / CdS / ZnS для биологического обнаружения.
Здесь мы сообщаем о бесфосфиновом однореакторном методе синтеза высококачественных красных эмиссионных КТ ZnSe / CdS / ZnS типа II / типа I с ядром / оболочкой с функцией подавления реабсорбции и первым использованием квантовых точек для изготовить иммуноферментный анализ, связанный с флуоресценцией (FLISA). Мы использовали высокореакционный и малотоксичный прекурсор Se (ODE-Se) и олеат цинка для синтеза высококачественных квантовых точек ZnSe с ядром, а затем добились роста с несколькими оболочками без очистки основных квантовых точек. Это показывает большие перспективы для крупномасштабного синтеза квантовых точек ядро / оболочка. Квантовый выход готовых КТ ZnSe / CdS / ZnS типа II / типа I с красным излучением может достигать 82% при более низком содержании токсичного кадмия, что особенно важно для снижения биотоксичности в биомедицинской области. Кроме того, КТ имеют большой стоксов сдвиг, а также сглаженный первый пик поглощения, что приводит к небольшому перекрытию спектров ФЛ и поглощения и подавлению эффекта реабсорбции.
C-реактивный белок (CRP) как белок острой фазы из клеток печени считается ранним индикатором инфекции и аутоиммунных заболеваний. Такие заболевания часто начинаются при очень низких уровнях CRP. Следовательно, чувствительный количественный иммуноферментный анализ уровней CRP в биологических образцах имеет решающее значение для диагностики и мониторинга развития заболеваний [16]. По сравнению с традиционным иммуноферментным анализом (ELISA), FLISA экономит время без ферментативной реакции и менее чувствителен к условиям окружающей среды, обусловленным оптическим качеством флуоресцентных квантовых точек [17]. Таким образом, FLISA стала новым центром исследований в области количественного иммуноанализа [2, 18,19,20,21]. Здесь мы впервые продемонстрировали количественный иммуноферментный анализ FLISA с использованием водорастворимых КТ ZnSe / CdS / ZnS типа II / типа I с ядром / оболочкой в качестве флуоресцентного зонда. Предел обнаружения (LOD) для количественного определения белка CRP достиг 0,85 нг / мл, что на 15% более чувствительно, чем у КТ CdSe / ZnS типа I на основе FLISA в контрольных экспериментах. Высокий QY, превосходная оптическая стабильность и низкий эффект реабсорбции могут способствовать применению квантовых точек ZnSe / CdS / ZnS типа II / типа I в биомедицине и фотоэлектрическом поле.
Методы
Химические вещества
Оксид кадмия (CdO, 99,99%), оксид цинка (ZnO, 99,9%, порошок), селен (Se, 99,9%, порошок), 1-октадецен (ODE, 90%), 1-октантиол (OT, 98%), олеиновая кислота (OA, 90%), поли (малеиновый ангидрид-альт-1-октадецен) (PMAO) и 2- (N-морфолино) этансульфоновая кислота (MES) были приобретены у Aldrich. Парафиновое масло (аналитическая чистота), ацетон (аналитическая чистота), гексаны (аналитическая чистота) и метанол (аналитическая чистота) были получены от Beijing Chemical Reagent Co., Ltd, Китай. NaOH, HCl, Na 2 CO 3 , NaHCO 3 , KH 2 ЗП 4 , Na 2 HPO 4 , H 3 БО 3 , Na 2 В 4 О 7 · 10H 2 О и Твин-20 были закуплены у Shanghai Sangon Co., Ltd, Китай. Бычий сывороточный альбумин (BSA) и телячья сыворотка были приобретены у Sigma. 1-этил-3- (3- (диметиламино) пропил) карбодиимид (EDC), N-гидроксисульфосукцинимид (сульфо-NHS) и микропланшеты были приобретены у Thermo Fisher Scientific (США). Мышиные моноклональные антитела против белка С-реакции и антиген CRP были получены от Abcam (США). Все химические вещества и растворители использовались в том виде, в котором они были получены, без дополнительной очистки.
Стандартный раствор для прекурсора Se (0,1 M)
Se (6 ммоль) и ODE (60 мл) загружали в трехгорлую колбу на 100 мл, а затем нагревали до 220 ° C в течение 180 минут в атмосфере азота с получением желтого прозрачного раствора.
Стандартный раствор для прекурсора Zn (0,4 M) и прекурсора Cd (0,2 M)
ZnO (30 ммоль), олеиновая кислота (30 мл) и 45 мл ODE загружали в трехгорлую колбу на 100 мл и нагревали до 310 ° C в атмосфере азота с получением прозрачного раствора. Полученному раствору давали остыть до 140 ° C для инъекции. Процесс приготовления предшественника Cd был таким же, как и предшественника Zn, за исключением того, что концентрация была доведена до 0,2 M, а температура реакции была установлена на 240 ° C.
Типичный синтез квантовых точек ZnSe / CdS / ZnS типа II / типа I
В качестве типичной процедуры синтеза 4 мл предшественника Se и 15 мл ODE помещали в круглую колбу на 100 мл. Смесь нагревали до 310 ° C. При этой температуре в реакционную колбу быстро вводили 2 мл прекурсора Zn. Аликвоты были извлечены через различные интервалы времени для отслеживания эволюции положения PL, которое координируется с размером частиц QD. Когда нанокристаллы ядра достигли желаемого размера, температура реакции была снижена до 230 ° C для роста оболочки CdS. Без каких-либо стадий очистки, поскольку смесь предшественника Cd и 1-октантиола (молярное радио ОТ и катиона составляет 1:1,2) начали добавляться по каплям с помощью шприцевого насоса со скоростью 3 мл / ч, в то время как температура была повышен до 310 ° C. Тот же процесс был применен к росту оболочки ZnS. Аликвоты КТ были взяты во время реакции для анализа развития КТ ZnSe / CdS / ZnS ядро / оболочка. Свежеприготовленные КТ ядро / оболочка очищали, добавляя ацетон, а затем повторно диспергировали в хлороформе.
Типичный синтез квантовых точек CdSe / ZnS типа I
КТ CdSe / ZnS были синтезированы, как описано в наших предыдущих отчетах [7]. Впоследствии процесс фазового переноса, зонды обнаружения квантовых точек и антител и приготовление FLISA были такими же, как и в случае с квантовыми точками ZnSe / CdS / ZnS, которые будут описаны ниже.
Фазовый перенос квантовых точек ZnSe / CdS / ZnS для биоприложения
Поли (малеиновый ангидрид-альт-1-октадецен) (ПМАО) - амфифильный олигомер, гидрофобные концы которого чередуются с органическим покрытием на КТ, а гидрофильные концевые группы могут свободно взаимодействовать с окружающим буфером, - был использован для переноса гидрофобных КТ в чистые вода. КТ ZnSe / CdS / ZnS и ПМАО смешивали и растворяли в хлороформе с обработкой ультразвуком (молярное соотношение КТ / ПМАО составляло 1:7). После этого хлороформ удаляли на роторном испарителе при 45 ° C. Затем равный объем 0,1 М NaHCO 3 водный раствор (pH =8,5) добавляли для растворения QD-PMAO. Инкапсулированные в ПМАО КТ ZnSe / CdS / ZnS типа II / типа I не демонстрируют потери флуоресценции и обладают высокой стабильностью в водном растворе в широком диапазоне pH среды.
Подготовка зондов для обнаружения квантовых точек и антител
Эта процедура широко описывалась в предыдущих публикациях [1,2,3]. QDs-PMAO сначала конъюгировали с моноклональным антителом CRP посредством активации этих групп -COOH с помощью EDC и сульфо-NHS. Затем в QD добавляли определенное количество моноклональных антител CRP и растворяли в буфере BS, а затем блокировали BSA. Наконец, продукт промывали 5 мМ BS-буфером (pH 8,0) при центрифугировании. QDs-mAb хранили в 50 мкл буфера BS (5 мМ, pH =8,0).
Приготовление флуоресцентного микропланшета, покрытого антителами
Первичное антитело (концентрация моноклонального антитела CRP составляла 1,8 мг / мл) разбавляли карбонатно-бикарбонатным буфером (50 мМ pH =9,6, буфер CB) в каждой лунке микропланшета. Затем микропланшет закрывали герметизирующей пленкой и инкубировали при 4 ° C в течение 24 часов. Чтобы удалить лишнее покрытие антител, микропланшет трижды промывали промывочным буфером (0,05% Твин-20 в 10 мМ PBS, pH =7,4). Затем избыточные сайты связывания блокировали 0,5% (мас. / Об.) BSA в 10 мМ PBS (pH =7,4) для инкубации в течение ночи при 4 ° C. Этот процесс гарантировал, что все доступные и оставшиеся связывающие стороны лунок микропланшета были закрыты. Планшет сушили в камере с постоянной температурой и влажностью в течение 24 часов, затем хранили при 4 ° C для дальнейшего использования.
Количественное определение CRP с помощью флуоресцентного иммуноанализа
В каждую лунку 96-луночного микропланшета, содержащего покрывающее антитело, добавляли 100 мкл стандартного антигена и разбавляли до ряда концентраций буфером для образца. Планшеты инкубировали при 37 ° C в течение 30 мин, а затем пять раз промывали промывочным буфером. Затем 100 мкл зондов QDs-mAb разводили буфером для зондов (10% телячьей сыворотки (об. / Об.) В 0,1 М PBS) в каждую лунку инкубировали и промывали так же, как в вышеупомянутом процессе.
Характеристика
Спектры поглощения в УФ-видимой области и ФЛ при комнатной температуре измеряли с помощью спектрофотометра Ocean Optics (режим PC2000-ISA). Квантовые выходы ФЛ (QY) определяли путем сравнения интегральной интенсивности флуоресценции образцов QD в растворе со стандартом известных QY (этанольный раствор родамин 101 (R101) (0,01% HCl, QY =100%) в качестве стандарта). . Исследования методом просвечивающей электронной микроскопии (ПЭМ) проводили на электронном микроскопе JEOL JEM-2010, работающем при 200 кВ. Определение фазы продуктов проводили на рентгеновском дифрактометре (D8-ADVANCE) с использованием излучения Cu-Ka (длина волны =1,54 Å). Размеры КТ и зонда КТ-антитело регистрировали с помощью динамического светорассеяния (Nano-ZS 90, Malvern Instruments, UK).
Результаты и обсуждение
Спектры УФ-видимого поглощения и ФЛ процесса роста оболочки показаны на рис. 1. Стоксов сдвиг ядра ZnSe составляет всего 8 нм с первым пиком поглощения при 420 нм и пиком излучения при 428 нм, а полная ширина излучения равна половине максимум (FWHM) 17 нм. Однако, когда на ядре ZnSe вырос только один монослой (МС) оболочки CdS, стоксов сдвиг значительно увеличился до 54 нм с первым пиком поглощения на 497 нм и пиком излучения на 551 нм с полной шириной излучения на полувысоте (FWHM). 38 нм. Из-за делокализации электронной волновой функции излучение фотолюминесценции квантовых точек ZnSe / CdS (629 нм) смещено в красную сторону по сравнению с квантовыми точками ядра ZnSe (428 нм), а полуширина расширяется до 52 нм с осаждением оболочки CdS. Уширенная ФЛ на полувысоте возникла из-за усиленного фрелихоподобного экситон-фононного взаимодействия [22, 23]. Более того, сила осциллятора первого пика поглощения быстро ослабевает из-за пространственно непрямого перехода типа II из валентной зоны ZnSe в зону проводимости CdS. Это обычное явление для квантовых точек II типа [24,25,26]. В то время как резкое увеличение поглощения в синей области спектра (<500 нм) было приписано запрещенной зоне массивного материала CdS (2,42 эВ). Как следствие, красное излучение, плоский пик поглощения первого экситона и устойчивое поглощение в коротковолновой области (<500 нм) квантовых точек ZnSe / CdS типа II привели к большому стоксовому сдвигу и подавлению реабсорбции. При последовательном росте оболочки ZnS ФЛ смещалась в коротковолновую область, а ширина на полувысоте сужалась с 52 нм до 43 нм. Это явление было приписано тому факту, что атомы Zn диффундируют в богатые кадмием области, образуя градиентную оболочку при высокой температуре, тем самым увеличивая смещение полосы оболочки. QY может увеличиться с 20 до 82% в процессе роста оболочки CdS и ZnS на ядрах ZnSe.
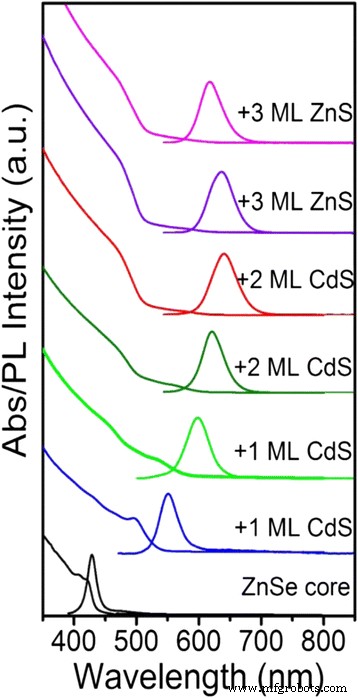
Эволюция УФ-видимых спектров поглощения и ФЛ при последовательном росте КТ ZnSe / CdS / ZnS ядро / оболочка
Следует отметить, что избыток прекурсора Zn-OA по сравнению с прекурсором Se в растворе ядра был необходим для получения высококачественных и монодисперсных квантовых точек ядра ZnSe. В результате оболочка из сплава ZnCdSeS неизбежно будет образовываться во время добавления предшественника оболочки Cd-OT на начальной стадии, поскольку высокая температура (> 200 ° C) способствует катионному обмену и диффузии между Zn 2 + и компакт-диск 2+ , а богатый октантиол в предшественнике Cd-OT также может реагировать с избытком Zn-OA [7, 12, 27, 28]. Оболочка из сплава может не только снизить межфазное натяжение и уменьшить количество дефектов для увеличения QY, но также создать энергетический барьер для дырок. Край зоны проводимости материала оболочки сплава ZnCdSeS находился между ZnSe и CdS, а край валентной зоны был глубже, чем CdS. Это сформировало больший потенциальный провал на краю валентной зоны как дополнительный блокирующий слой для дырок (Схема 1) [12]. Эта структура энергетической зоны может дополнительно уменьшить перекрытие электронов и дырок, чтобы уменьшить силу первого пика экситонного поглощения и подавить реабсорбцию.
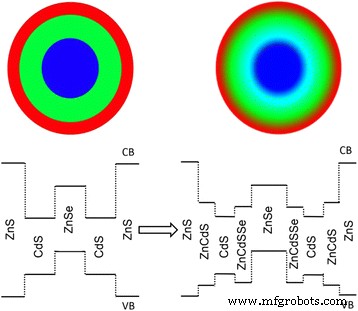
Схема структуры ( вверх ) и выравнивание полосы ( снизу ) для квантовых точек ZnSe / CdS / ZnS типа II / типа I на соответствующих резких и легированных границах раздела соответственно
Информация о полосовой структуре ядро / оболочка и эволюция ФЛ и оптической плотности во время роста оболочки может быть дополнительно проверена путем сравнения XRD, TEM и HRTEM нанокристаллов ядра и ядра / оболочки. На порошковых дифрактограммах ядра ZnSe, ZnSe / CdS и ZnSe / CdS / ZnS ядро / оболочка (левый рисунок на рис.2) видно, что дифракционные пики становятся резкими и смещаются в положения, соответствующие объемному вюрциту (WZ) CdS. или кристаллические структуры ZnS. Этот результат согласуется с предсказанными значениями для большего объема оболочки CdS или ZnS по сравнению с ядром ZnSe в конечных квантовых точках ядро / оболочка и свидетельствует о росте мультиоболочек. Кроме того, произошел переход от ядер ZnSe типа цинковой обманки (ZB) к ядру / оболочке типа WZ с покрытием CdS и ZnS. Об этом явлении сообщалось в системах КТ CdSe / CdS ядро / оболочка [29, 30]. ПЭМ-изображения основных квантовых точек и нескольких квантовых точек типа ядро / оболочка показаны на рис. 2a - 2 F. Все изображения ПЭМ показывают почти монодисперсные сферические квантовые точки с постепенно увеличивающимся средним диаметром от исходного ядра ZnSe (3,90 нм) до типа ZnSe / 6CdS. II (7.98 нм) и ZnSe / 6CdS / 6ZnS type-II / type-I (11.92 nm). Как показано на ПЭМ-изображении КТ ZnSe с ядром (вставка на рис. 2а), период решетки плоскостей (111) составляет 0,32 нм, а КТ обладают хорошей кристалличностью и монодисперсностью. С ростом оболочек параметр решетки показал соответствующее изменение (0,35 нм для CdS и 0,31 нм для ZnS) в соответствии с данными XRD. Результаты ясно показали контролируемый рост CdS и последующих материалов оболочки ZnS.
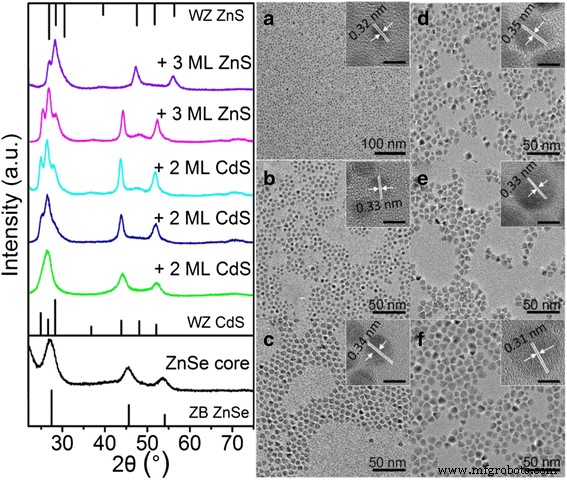
Влево :Рентгенограммы квантовых точек ZnSe / CdS / ZnS типа II / типа I с разными стадиями роста оболочки. Дифракционные линии для цинковой обманки (ZB) ZnSe (внизу), WZ CdS ( в середине ) и WZ ZnS ( вверх ) проиндексированы. Право :соответствующие ПЭМ и ВРЭМ ( вставка , полоса 5 нм) изображения ядра ZnSe ( a ), КТ ZnSe / CdS типа II с 2 ML ( b ), 4 мл ( c ) и 6 мл ( d ) CdS оболочки соответственно и КТ ZnSe / CdS / ZnS типа II / типа I с 3 ML (E) и 6 ML (F) соответственно
Между тем, чтобы подтвердить эволюцию состава во время роста мультиоболочки, был проведен анализ энергодисперсионной рентгеновской спектроскопии (EDS) для различных стадий роста ядра / оболочки, как показано в Дополнительном файле 1:Таблица S1. Данные EDS показывают, что соответствующие изменения содержания Cd, Se, Zn и S соответствуют стадии роста оболочки. Но стоит отметить, что молярное соотношение Cd / (Zn + Cd) в полученных КТ ZnSe / CdS выше, чем соотношение сырья Cd / (Zn + Cd) из-за катионного обмена между Zn 2 + и компакт-диск 2+ в процессе нанесения оболочки из CdS на ядро из ZnSe при температуре выше 200 ° C. По сравнению с опубликованной литературой о типичных квантовых точках CdSe / CdS / ZnS типа I (мольное отношение Cd ~ 40%) [31], квантовые точки ZnSe / CdS / ZnS типа II / типа I содержали гораздо меньше элемента Cd (~ 13%).
Визуальное сравнение гидрофобных КТ в хлороформе и КТ, закрытых ПМАО, в воде под солнечным светом и УФ-светом показано в Дополнительном файле 1:Рисунок S1 (A). Похоже, что оба раствора КТ не возмущены и агрегация наночастиц отсутствует. Обе КТ излучали одинаковый красный свет при освещении ручной УФ-лампой (365 нм). Дополнительный файл 1:На рисунке S1 (B) показаны спектры поглощения в УФ-видимой области и спектры ФЛ квантовых точек до и после фазового переноса. По сравнению с гидрофобными квантовыми точками в хлороформе, спектр ФЛ квантовых точек, закрытых ПМАО, имеет незначительные изменения, что указывает на отсутствие очевидных изменений в размере частиц и свойствах ФЛ. Дополнительный файл 1:На рис. S1 (C) и (D) представлены ПЭМ-изображения квантовых точек до и после фазового перехода, которые дополнительно определяют морфологию и состояние квантовых точек, покрытых PMAO. Похоже, что КТ, закрытые ПМАО, хорошо изолированы и редко наблюдаются в виде агрегатов.
Чтобы подтвердить образование КТ, инкапсулированных в ПМАО, в процессе фазового переноса, была использована ИК-Фурье спектроскопия для характеристики функциональных групп на поверхности КТ (показано в Дополнительном файле 1:Рисунок S2). Уменьшение пика на 1777 см −1 (сравнил PMAO с QDs-PMAO) и увеличение пика на 1715 см −1 (сравнили три образца) были отнесены к разложению ангидрида и образованию -COOH. Результаты FTIR показали, что амфифильный полимер ПМАО успешно нанесен на поверхность КТ ZnSe / CdS / ZnS.
Стабильность полученных КТ очень важна для последующей обработки. На рис. 3а показано изменение относительной стабильности ФЛ гидрофобных КТ ZnSe / CdS / ZnS после стадий очистки. Интенсивность ФЛ КТ ZnSe / CdS / ZnS ядро / оболочка могла сохраняться на уровне 85% после многих циклов очистки в гексане. Как показано на фиг. 3b, коллоидная стабильность QD-PMAO в BS-буфере (pH =7,2) оценивалась как функция времени при 25 ° C. Интенсивность ФЛ практически не изменялась, и раствор был прозрачным даже через 400 ч. Это указывает на то, что QDs-PMAO стабилен в растворе BS без каких-либо повреждений. На рис. 3c показано изменение интенсивности ФЛ QD-PMAO, которые были погружены в раствор от кислого до основного (pH =1-14, отрегулированный с помощью HCl или NaOH) на 30 мин. Интенсивность ФЛ гидрофильных КТ может сохраняться более 85%, за исключением случая, когда PH =14. На рис. 3d показано влияние температурного параметра на относительную интенсивность флуоресценции КТ-ПМАО. Интенсивность флуоресценции постепенно уменьшалась с повышением температуры, но все еще оставалась 76% при 90 ° C, в то время как пики ФЛ постепенно сдвигались в сторону более длинных волн из-за теплового расширения и эффекта электрон-фононной связи. Все оценки стабильности показывают, что КТ ZnSe / CdS / ZnS типа II / типа I и КТ-ПМАО были очень стабильными и, таким образом, подходили для биологических применений.
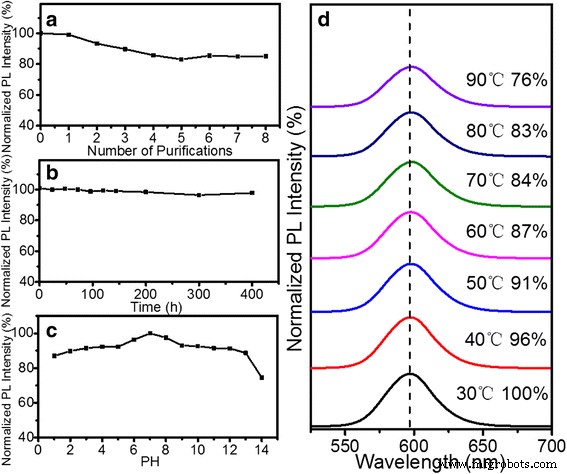
Тест на стабильность гидрофобных квантовых точек при ( a ) повторяющиеся стадии процесса очистки; тест на стабильность QDs-PMAO при ( b ) BS буфер, ( c ) PH и ( d ) температура
CRP - это белок острой фазы из клеток печени, и его уровень считается ранним индикатором инфекции и аутоиммунных заболеваний. Здесь КТ ZnSe / CdS / ZnS в исходном состоянии с блокированными PMAO соединяют с CRP, чтобы продемонстрировать возможность применения в количественном иммуноанализе. Диаграмма сравнения спектров флуоресценции водных КТ ZnSe / CdS / ZnS и КТ-мАт показана на рис. 4а. Ясно, что форма пика ФЛ обоих образцов примерно идентична, за исключением того, что интенсивность флуоресценции снижается до 60% после реакции сочетания из-за неизбежной потери образца во время процесса разделения на центрифуге. Это доказывает превосходную оптическую стабильность квантовых точек ZnSe / CdS / ZnS типа II / типа I даже после процесса связывания антител с белками.
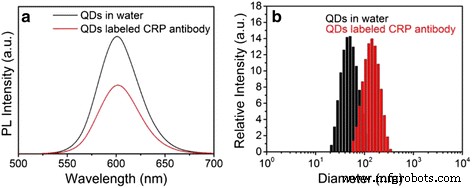
Спектры флуоресценции ( a ) и динамическое рассеяние света ( b ) QDs-PMAO и QDs-mAb в буфере
Для дальнейшего исследования влияния конъюгации на размер КТ водные КТ и КТ-мАт характеризуются динамическим светорассеянием (DLS). Результаты DLS (рис. 4b) ясно показывают, что оба образца имеют узкое распределение по размерам с хорошей монодисперсностью и сохраняют дискретную форму без агрегации, в то время как гидродинамический размер увеличивается с 46 до 120 нм после процесса связывания. Это демонстрирует успех конъюгации с антителами к CRP.
Кроме того, мы использовали составные квантовые точки ZnSe / CdS / ZnS типа II / типа I вместо КТ CdSe / ZnS типа I в качестве флуоресцентного зонда, чтобы установить FLISA для количественного обнаружения CRP. Процесс сборки показан в Дополнительном файле 1:Схема S1. На рис. 5а показана относительная интенсивность флуоресценции флуоресцентной метки QD для иммуноанализа при обнаружении различных концентраций антигенов CRP (стандартный антиген CRP разбавлен до 0, 1, 5, 10, 50, 100, 200, 400 нг / мл). Очевидно, что интенсивность PL постепенно увеличивается с увеличением концентрации CRP. На рисунке 5b показано, что корреляция между интенсивностью флуоресценции и целевыми концентрациями CRP подчиняется уравнению кривой квадратичной регрессии y =44230 + 8121,1x-10,3x 2 с коэффициентом корреляции 0,9991, который чем ближе к 1, тем лучше. Диапазон рабочих концентраций от 0 до 400 нг / мл. LOD является одним из ключевых параметров иммуноанализа на FLISA. При использовании композитных КТ ZnSe / CdS / ZnS типа II / типа I в качестве флуоресцентного зонда чувствительность количественного определения CRP составляет 0,85 нг / мл, что на 15% более чувствительно, чем у FLISA на основе типа CdSe / ZnS. -I QD (1,00 нг / мл) (в дополнительном файле 1:рисунок S3).
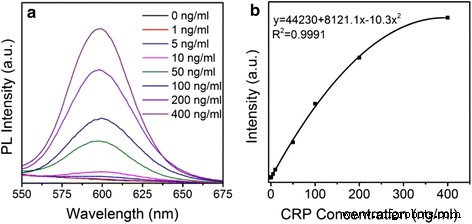
Спектры фотолюминесценции FLISA для определения различной концентрации антигена CRP ( a ) и стандартные кривые ( b )
Кроме того, были использованы эксперименты по восстановлению для оценки матричного эффекта FLISA с рядом известных стандартных антигенов CRP для анализа, и конечные концентрации охватывали уровни низкого, среднего и высокого риска. Как показано в Таблице 1, все коэффициенты извлечения находятся в диапазоне 83,61-105,9%. Эти результаты показывают, что FLISA на основе квантовых точек ZnSe / CdS / ZnS типа II / типа I со свойством подавления реабсорбции имеет высокую точность и дает большие преимущества при количественном обнаружении иммуноанализа.
Выводы
Мы сообщаем о бесфосфиновом однореакторном методе синтеза КТ ZnSe / CdS / ZnS типа II / типа I с ядром / оболочкой с большим стоксовым сдвигом и плоским первым пиком поглощения с подавлением реабсорбции. Эти характеристики уменьшают реабсорбцию и улучшают уровень флуоресценции. Квантовые точки в исходном состоянии имеют высокий QY (82%) и высокую стабильность в различных условиях испытаний. Затем мы сначала используем QD ZnSe / CdS / ZnS в качестве флуоресцентного зонда в FLISA для количественного определения белка CRP с высокой чувствительностью (LOD 0,85 нг / мл). Это указывает на то, что КТ ZnSe / CdS / ZnS типа II / типа I с ядром / оболочкой с подавленной реабсорбцией имеют многообещающий потенциал для применения в биомедицине и фотоэлектрических областях.
Сокращения
- BSA:
-
Бычий сывороточный альбумин
- CRP:
-
С-реактивный белок
- DLS:
-
Динамическое рассеяние света
- EDC:
-
1-этил-3- (3- (диметиламино) пропил) карбодиимид
- EDS:
-
Энергодисперсионная рентгеновская спектроскопия
- ELISA:
-
Иммуноферментный анализ
- FLISA:
-
Иммуноферментный анализ, связанный с флуоресценцией
- FWHM:
-
Полная ширина на половине максимальной
- LOD:
-
Предел обнаружения
- MES:
-
2- (N-морфолино) этансульфоновая кислота
- OT:
-
1-октантиол
- PMAO:
-
Поли (малеиновый ангидрид-альт-1-октадецен)
- QD:
-
Квантовые точки
- QYs:
-
Квантовые выходы
- sulfo-NHS:
-
N-гидроксисульфосукцинимид
Наноматериалы
- Достижения и проблемы флуоресцентных наноматериалов для синтеза и биомедицинских приложений
- Синтез обогащенных пиридином N, S-углеродных квантовых точек как эффективных имитаторов ферментов
- Зеленый синтез квантовых точек InP / ZnS Core / Shell для применения в светоизлучающих диодах, не содержащих тяжелых м…
- Синтез нанокристаллов ZnO и применение в инвертированных полимерных солнечных элементах
- Синтез композита поли (3,4-этилендиокситиофен) / золото / графен в твердом состоянии и его применение для амперо…
- Синтез водорастворимых квантовых точек сульфида сурьмы и их фотоэлектрические свойства
- Обратимый электрохимический контроль фотовозбужденной люминесценции пленки CdSe / ZnS с квантовыми точками ядр…
- Экологичный и простой синтез нанопроволок Co3O4 и их перспективное применение с графеном в литий-ионных батаре…
- Простой одностадийный сонохимический синтез и фотокаталитические свойства композитов на квантовых точках г…
- Синтез и характеристика модифицированного BiOCl и их применение при адсорбции низкоконцентрированных красите…



