Экологичный и экономичный синтез наночастиц оксида олова:обзор методологий синтеза, механизма образования и их потенциального применения
Аннотация
Нанотехнология стала наиболее многообещающей областью исследований с ее важным применением во всех областях науки. В последние годы оксид олова привлек огромное внимание из-за его удивительных свойств, которые были улучшены с синтезом этого материала в нанометровом диапазоне. В наши дни для производства наночастиц оксида олова используются многочисленные физические и химические методы. Однако эти методы дороги, требуют больших затрат энергии, а также используют различные токсичные химические вещества во время синтеза. Возросшая озабоченность по поводу здоровья человека и воздействия на окружающую среду привела к разработке экономичного и экологически безопасного процесса его производства. Недавно наночастицы оксида олова были успешно синтезированы экологически чистыми методами с использованием различных биологических объектов, таких как экстракт растений, бактерии и природные биомолекулы. Однако производство в промышленных масштабах с использованием подходов зеленого синтеза остается проблемой из-за сложности биологических субстратов, что затрудняет выяснение реакций и механизма образования, которые происходят во время синтеза. Таким образом, в настоящем обзоре суммируются различные источники биологических объектов и методологии, используемые для зеленого синтеза наночастиц оксида олова, а также влияние на их свойства. В этой работе также описываются достижения в понимании механизма образования, описанные в литературе, и различные аналитические методы, используемые для характеристики этих наночастиц.
Введение
В последние несколько десятилетий нанотехнология превратилась в новую область исследований, связанных с синтезом, характеристикой, модификацией и использованием наноматериалов для их огромного применения в таких областях, как фармацевтика, пищевая промышленность, косметика, текстильная промышленность, медицина, оптика, электроника и т. Д. энергетика и электрохимические приложения [1,2,3,4]. Наноматериалы - это материалы, имеющие один размер в диапазоне размеров 1–100 нм. Очень большое отношение площади поверхности к объему и чрезвычайно малый размер этих материалов могут привести к совершенно новой или усиленной электрической, оптической, магнитной, каталитической и антимикробной активности по сравнению с их объемными материалами [5,6,7]. Благодаря этим уникальным свойствам наночастицы находят применение в различных областях современной науки и техники, таких как наномедицина, фотокатализ, биосенсоры, чистящие средства и текстильная промышленность [1, 8]. Среди наночастиц оксид олова (IV) (SnO 2 ), в частности, получили огромное внимание благодаря их универсальному применению, например, оптоэлектронным устройствам [9], твердотельным датчикам газа [10], электродам для литий-ионных аккумуляторов [11], автоэмиссионным дисплеям [12], светодиодам. [13], катализ [14], солнечные элементы на основе красителей [15], медицина [16], фотодатчики и антистатические покрытия [17].
В материаловедении SnO 2 считается дефицитным по кислороду полупроводником n-типа, который кристаллизуется в виде тетрагональной структуры рутила с постоянными решетки a = b =4,7374 Å и c =3,1864 Å. Элементарная ячейка состоит из двух шестикоординированных атомов олова и четырех трехкоординированных атомов кислорода [18, 19]. Широкая запрещенная зона (от 3,6 до 3,8 эВ), высокая термическая стабильность (до 500 ° C), высокая степень прозрачности в видимой области спектра, сильные химические и физические взаимодействия с адсорбированными частицами делают SnO 2 многообещающий кандидат для потенциального применения в литий-ионных батареях, датчиках, катализаторах, накопителях энергии, стеклянных покрытиях, медицине и восстановлении окружающей среды [20,21,22,23]. SnO 2 используется в качестве сенсора для улучшения времени отклика и чувствительности благодаря своей высокой удельной площади, высокой химической стабильности, низкому электрическому сопротивлению и низкой плотности [24]. За последние несколько лет SnO 2 был тщательно исследован на предмет его применения в солнечных элементах [25] и газовых датчиках для обнаружения горючих газов, таких как CO, NO, NO 2 , H 2 S и C 2 H 5 ОН [26,27,28,29]. Благодаря уникальным физико-химическим свойствам и потенциальному применению наночастиц (НЧ) научное сообщество разработало несколько методов производства наночастиц. Однако химические и физические методы, используемые для синтеза наночастиц металлов и оксидов металлов, довольно дороги и используют токсичные вещества, опасные для окружающей среды и здоровья человека [30]. В последние годы большинство исследователей изменили свой исследовательский интерес в сторону зеленого синтеза наночастиц, поскольку он имеет множество преимуществ, таких как экономичная, простая процедура производства, воспроизводимость в производстве и часто приводит к более стабильным наночастицам [31]. В течение последнего десятилетия было проведено несколько исследований зеленого синтеза SnO 2 Сообщалось о НП. Однако в литературе нет ни одной обзорной статьи, демонстрирующей методологию синтеза и механизм образования. Следовательно, в этой статье описывается зеленый синтез, механизм образования, методы определения характеристик и потенциальные применения SnO 2 НП.
Экологический синтез наночастиц оксида олова
SnO 2 НЧ синтезируются различными физическими, химическими и зелеными методами. К химическим методам относятся золь-гель, гидротермальные, осаждения, механохимические, микроэмульсионные и так далее [31,32,33,34,35,36,37]. Среди химических методов наиболее широко используется золь-гель синтез, в котором используется соль-предшественник олова и химические реагенты, регулирующие образование оловосодержащего геля. После этого гель подвергают термообработке при температуре до 800 ° C с получением SnO 2 НП [32, 38]. Химические стабилизаторы и укупорочные агенты, такие как щавелевая кислота или этиленгликоли, могут быть добавлены во время синтеза SnO 2 НЧ для контроля размера и предотвращения агломерации наночастиц [32, 39]. PH раствора, концентрация химикатов, время реакции и температура прокаливания также могут влиять на размер и морфологию наночастиц [31, 34,35,36,37]. Вышеупомянутые методы синтеза SnO 2 В НП используются различные опасные химические реагенты, растворители и поверхностно-активные вещества, которые создают серьезную угрозу окружающей среде и здоровью человека [4, 30].
SnO 2 НЧ также можно синтезировать физическими методами, такими как пиролиз распылением, термическое окисление, химическое осаждение из паровой фазы, лазерная абляция и обработка ультразвуком [40,41,42,43,44]. Среди этих методов лазерная абляция считается экономичным и простым методом синтеза наночастиц металлов и оксидов металлов в жидкости [44, 45]. В отличие от других традиционных методов, этот метод не требует блокирующих / восстанавливающих агентов, высокой температуры или высокого давления и позволяет нам получать наночастицы высокой чистоты [44, 45]. Изменение параметров импульсов, подаваемых лазерным лучом, и времени абляции являются важными параметрами, которые определяют размер частиц, морфологию и химию поверхности наночастиц [44]. Однако для большинства физических методов требуется сложное оборудование, высокая энергия и квалифицированный персонал [46]. Поэтому очень важно разработать методы синтеза, которые были бы экологически чистыми, дешевыми, эффективными и работали бы в условиях окружающей среды. Одним из таких решений является «зеленый» синтез, и многие исследователи разработали подход «зеленой химии» для синтеза наночастиц оксида олова. В стратегии зеленого синтеза биологические объекты, такие как экстракт растений, микроорганизмы или другие зеленые источники, могут использоваться в качестве альтернативы обычным физическим и химическим методам [47]. В наши дни биологически вдохновленные методы синтеза также известны как зеленый синтез, потому что они согласуются с двенадцатью принципами зеленой химии [48]. Некоторые из явных преимуществ биологического синтеза перед физическими и химическими методами:(а) чистый и экологически безопасный метод, поскольку используются нетоксичные химические вещества, (б) использование возобновляемых источников, (в) активные биологические компоненты, такие как сам фермент в качестве а также фитохимические вещества действуют как восстанавливающий и укупоривающий агент, тем самым сводя к минимуму общую стоимость процесса синтеза; (d) не требуются внешние экспериментальные условия, такие как высокое давление и температура, что приводит к значительной экономии энергии [49, 50].
В последнее десятилетие интерес к синтезу SnO 2 Количество NP, полученных биологическим методом, значительно увеличилось, поскольку этот процесс является более надежным, экологичным, рентабельным, с низким уровнем затрат и высоким выходом, а также с простыми процедурами, не вызывающими какого-либо вредного воздействия на окружающую среду. Разнообразные биологические субстраты, такие как экстракты растений, бактерии и природные биомолекулы, были успешно использованы для зеленого синтеза SnO 2 НП. Фитохимические вещества различных растений и ферменты бактерий в первую очередь ответственны за синтез зелени. Активные соединения, присутствующие в зеленых источниках, также играют роль восстанавливающего, укупоривающего и стабилизирующего агента во время синтеза. Желаемые НЧ часто получают после прокаливания или отжига при определенных температурах [51,52,53,54].
Опосредованный растениями синтез наночастиц оксида олова
Опосредованный растениями синтез стал лучшей платформой для синтеза по сравнению с обычными физико-химическими методами, потому что он не содержит токсичных химикатов и обеспечивает естественное покрытие, а также восстанавливающие агенты. Кроме того, это легко и экологично, а также дает качественный продукт без примесей. В этом методе нет необходимости использовать высокую температуру, высокое давление и дорогостоящее оборудование. Кроме того, опосредованный растениями синтез приводит к крупномасштабному производству более стабильных наночастиц различной формы и размера [55, 56]. Экстракты большого количества частей различных видов растений были использованы для зеленого синтеза SnO 2 НП. В общем, опосредованный растениями синтез SnO 2 НЧ - это очень простой процесс, при котором к ранее приготовленному экстракту добавляется тонкая соль. По окончании реакции раствор подвергают центрифугированию. Наконец, гранулы затем подвергаются термической обработке с последующей характеристикой с использованием различных аналитических методов, таких как инфракрасная спектроскопия с преобразованием Фурье (FTIR), рентгеновский дифрактометр (XRD), энергодисперсионный рентгеновский анализ (EDS), сканирующая электронная микроскопия ( SEM), просвечивающая электронная микроскопия (TEM), анализатор размера частиц (PSA) и динамическое рассеяние света (DLS). УФ – видимая спектроскопия (УФ – видимая) используется для контроля образования наночастиц. Подробный протокол опосредованного растениями синтеза SnO 2 НЧ схематически изображен на рис. 1. Diallo et al. сообщил о зеленом синтезе SnO 2 НП с использованием Aspalathus linearis и пентагидрат хлорида олова (SnCl 4 · 5H 2 O) в качестве предшественника [51]. Соль растворяли в растительном экстракте, и через 10 мин наблюдали образование белого налета. Белый осадок собирали после процесса центрифугирования и сушили при температуре около 80 ° C. Порошок отжигали при различных температурах в течение примерно 4 часов и подвергали различным аналитическим методам, таким как просвечивающая электронная микроскопия высокого разрешения (HR-TEM), EDS, XRD и рентгеновская фотоэмиссионная спектроскопия (XPS). НЧ имели квазисферическую форму со средним размером в диапазоне 2,5–11,40 нм. Было обнаружено, что размер частиц и кристаллическая природа наночастиц увеличиваются с увеличением температуры отжига. Более того, биоактивные компоненты, такие как аспалатин, нотофагин и аспалалинин, присутствующие в растительном экстракте, действуют как хелатирующие, так и восстанавливающие агенты. Camellia sinensis экстракт листьев также использовался для синтеза SnO 2 НП [53]. Полифенолы, присутствующие в экстракте листьев, действуют как стабилизирующие, так и покрывающие агенты. Сканирующая электронная микроскопия высокого разрешения (HR-SEM) и XRD-анализ показали сферическую форму SnO 2 НЧ размером от 5 до 30 нм. Кроме того, было обнаружено, что ширина запрещенной зоны наночастиц уменьшается с увеличением температуры отжига. Catunaregam spinosa -опосредованный зеленым синтезированным SnO 2 НЧ показали отличную фотокаталитическую активность в отношении красителя Конго красный [57]. Биосинтезированные НЧ имеют сферическую форму и средний размер 47 нм.
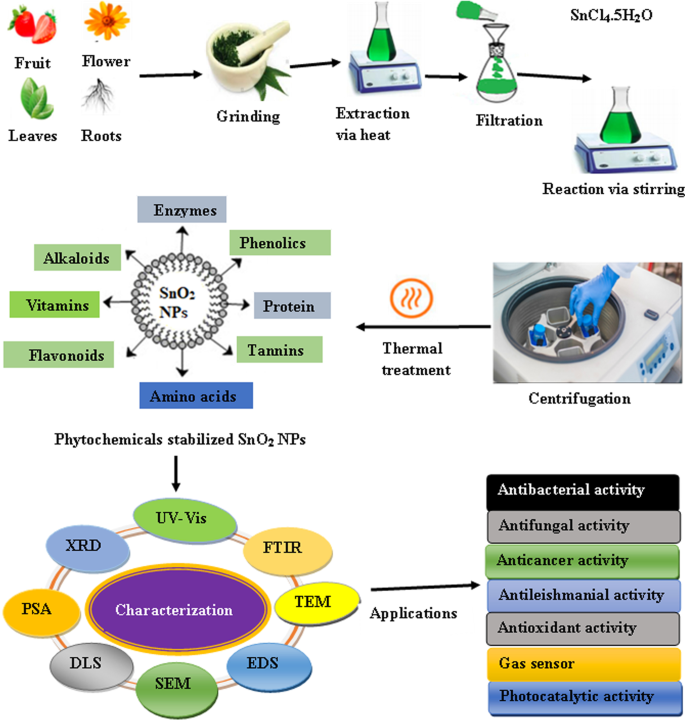
Схематическая диаграмма опосредованного растительным экстрактом синтеза SnO 2 НП
Экстракт листьев Aloe barbadensis miller был использован для синтеза SnO 2 НП из SnCl 2 · 2H 2 О в качестве предшественника [58]. Полученные НЧ оказались сферическими со средним размером от 50 до 100 нм. Более того, синтезированные наночастицы проявили отличную антибактериальную активность против S. золотистый и Э. coli.
В другом исследовании зеленый синтез SnO 2 НЧ были получены эффективным и дешевым методом с использованием Plectranthus amboinicus экстракт листьев и SnCl 2 · 2H 2 О в качестве исходного материала [59]. Растительный экстракт действует как восстанавливающий и стабилизирующий агент. Полученные НЧ были охарактеризованы с помощью SEM, EDX, XRD и PSA. НЧ имели тетрагональную форму со средним размером частиц 63 нм. Кроме того, авторы обнаружили, что биосинтезированные НЧ проявляют большую фотокаталитическую активность против родамина B по сравнению с коммерческим SnO 2 . Зеленый синтез SnO 2 Сообщалось о НЧ при использовании Nyctanthes arbor-tristis (Париджатака) экстракт цветов [60]. Как видно из анализа SEM и PSA, синтезированные наночастицы демонстрируют морфологию мелких гранул с крошечной стадией агломерации и средним размером зерна 2-8 нм. В исследовании также изучался гидролизный и улавливающий потенциал растительного экстракта.
Зеленый синтез SnO 2 NP было выполнено с помощью недорогого и экологически чистого процесса с использованием Psidium guajava экстракт листьев [61]. Результат в УФ-видимом диапазоне показал пик поверхностного плазмонного резонанса при 314 нм, подтверждающий образование SnO 2 НП. Кроме того, НЧ имели сферическую форму размером от 8 до 10 нм. Исследование также показало, что НЧ демонстрируют 90% -ную деградацию реактивного желтого 186 в течение 180 минут под воздействием солнечного излучения. Bhosale et al. [62] идентифицировали экстракт листьев Calotropis gigantea как естественный источник для синтеза SnO 2 НП. Вторичные метаболиты экстракта действуют как стабилизатор и блокирующий агент при превращении хлорида олова в SnO 2 НП. Авторы предположили, что НЧ имели сферическую форму и средний размер от 30 до 40 нм. Синтезированные НЧ разлагают краситель метиловый оранжевый до 80% за 120 мин. Singh et al. [63] сообщили о биосинтезе SnO 2 . НП, использующие Piper Betle листовой экстракт. СЭМ и ПЭМ анализ выявили образование сферических НЧ со средним размером 8,4 нм. НЧ разрушают реактивный желтый 186 в псевдопервом порядке с эффективностью 92,17%. Кроме того, НЧ показали превосходную селективность в отношении удаления реактивного желтого 186 по сравнению с реактивным красным 120 и реактивным зеленым 119. В литературе для получения SnO 2 использовались различные растения и растительные экстракты. (Таблица 1). Из таблицы видно, что природа видов растений и условия реакции влияют на размер и форму SnO 2 НП.
Бактериальный синтез наночастиц оксида олова
Микробы - важные нанофабрики, которые приобретают огромный потенциал в качестве экологически чистых и экономичных инструментов, избегая токсичных химикатов и высокой энергии, необходимой для физико-химического синтеза. Различные микробы, такие как бактерии, грибы и дрожжи, были использованы для синтеза металлов и наночастиц оксидов металлов внутриклеточно или внеклеточно. Внутриклеточный синтез включает транспортировку ионов металлов в микробную клетку и образование НЧ в присутствии фермента, коферментов и других биомолекул внутри клетки. При внеклеточном синтезе ионы металлов задерживаются на поверхности микробной клетки. Ферменты и белки, доступные на поверхности, восстанавливают ионы металлов и отвечают за стабилизацию НЧ [73]. Однако внеклеточный синтез более выгоден по сравнению с внутриклеточным путем, потому что его можно использовать для производства больших количеств НЧ и устраняет различные стадии синтеза, необходимые для восстановления НЧ [74].
Биологический синтез с использованием бактерий - это экологически чистый и экономичный подход по сравнению с химическим синтезом. Однако этот метод имеет несколько недостатков:(а) скрининг микробов - это трудоемкий процесс, (б) требуется тщательный мониторинг культурального бульона и всего процесса, и (в) трудно контролировать размер и морфологию микробов. НП. Не все бактерии могут синтезировать НЧ из-за собственного метаболического процесса и ферментативной активности. Следовательно, необходим тщательный отбор подходящих бактерий для получения НЧ с четко определенным размером и морфологией [74]. Например, в исследовании, проведенном Шриваставой и Мухопадхьяем [54], сообщается о недорогой, экологически чистой и простейшей процедуре синтеза SnO 2 НЧ, использующие свежие и чистые Erwinia herbicola бактериальные клетки и водный раствор хлорида олова (II). Синтезированный SnO 2 НЧ в основном имели сферическую форму размером от 10 до 42 нм. Сообщалось, что бактериальный белок и другие биомолекулы служат в качестве восстанавливающего и стабилизирующего агента во время синтеза SnO 2 НП. Эти биомолекулы также помогли контролировать размер и агрегацию SnO 2 НП.
Биомолекулы и другой синтез наночастиц оксида олова, опосредованный зеленым источником
Помимо опосредованного растениями и бактериями синтеза SnO 2 Исследователи разработали нетоксичный, экологически чистый и экологически чистый химический подход, используя другие биомолекулы, такие как аминокислоты, витамины, ферменты и сахара (таблица 2). Ян и др. [75] синтезировали SnO 2 НЧ с использованием недорогого и экологически чистого метода с использованием витамина С (аскорбиновая кислота), естественной биомолекулы. ПЭМ-анализ показал образование сферических НЧ со средним размером около 30 нм. Витамин C действует как блокирующий и восстанавливающий агент во время синтеза. Исследование показало, что витамин С на поверхности SnO 2 НЧ снижали окислительный стресс, вызванный SnO 2 НЧ на клетках, что приводит к снижению потери веса у новорожденных мышей. Сферический SnO 2 НЧ со средним размером частиц 13 нм были приготовлены с использованием углеводов (крахмала) [76]. Было высказано предположение, что углевод действует как матрица, которая может связывать несколько катионов металлов через их функциональные группы, и, следовательно, наблюдается однородная дисперсия катионов. В другом исследовании остатки воды, собранные из замоченных бенгальских бобов ( Cicer arietnum L.) был использован для синтеза нелегированного SnO 2 , а также SnO, легированный Ni, Fe и Au 2 НП [77,78,79]. Авторы предположили, что пектин в экстракте отвечает за синтез SnO 2 НП. Средний размер кристаллитов нелегированного SnO сферической формы 2 , SnO, легированный никелем 2 , и SnO, легированный Au 2 Было обнаружено, что размер НЧ составляет 11, 6 и 25 нм соответственно.
Другое исследование показало зеленый подход к синтезу SnO 2 НЧ, использующие мембрану из яичной скорлупы (ESM) [80], естественные биоотходы из куриной яичной скорлупы. Было высказано предположение, что ESM составляют биомолекулы, такие как уроновая кислота и сахариды, содержащие альдегидные фрагменты, которые действуют как восстанавливающий агент во время синтеза. Морфологический анализ показал образование SnO 2 стержневой, гексагональной и сферической формы. НЧ с размером частиц 13–40 нм.
Различные аминокислоты, такие как глицин, аргинин, аспарагиновая кислота, лизин и тирозин [81,82,83,84,85], были использованы для зеленого синтеза SnO 2 НЧ из-за их хороших улавливающих или комплексообразующих агентов. Синтез, опосредованный аминокислотами, исключает использование токсичных химикатов во время синтеза. Сферический SnO 2 НЧ были синтезированы с использованием аргинина [81]. Морфологические исследования показывают, что синтезированный SnO 2 НЧ имели сферическую форму со средним размером в диапазоне 4–5 нм. Bhattacharjee et al. [83] использовали глицин для производства SnO 2 НЧ хлорида олова. Было высказано предположение, что НЧ, образующиеся при 200 ° C, 400 ° C и 600 ° C, имеют сферическую, поликристаллическую и монодисперсную природу со средним размером 6, 16 и 33 нм соответственно. Кроме того, наночастица, полученная при 400 ° C, была люминесцентной. Аналогичным образом, Begum et al. [84] продемонстрировали синтез тетрагональной структуры рутила SnO 2 НЧ с L-лизином размером от 4 до 17 нм.
Механизм образования наночастиц оксида олова посредством зеленого синтеза
В последние несколько лет различные экстракты растений, микроорганизмы и другие биологические производные использовались в зеленом синтезе металлов и наночастиц оксидов металлов. Исследования показали, что вторичные метаболиты, такие как фенолы, флавоноиды, дубильные вещества, сапонины, терпеноиды и углеводы, присутствующие в растительном экстракте, играют важную роль, действуя как восстанавливающие, так и стабилизирующие агенты в синтезе металлов или наночастиц оксидов металлов [87]. Кроме того, опосредованный микробами синтез может осуществляться внутриклеточно или внеклеточно в зависимости от места, где образуются NP. При внеклеточном синтезе биоредукция происходит на поверхности микробных клеток в присутствии ферментов, доступных на поверхности. Кроме того, при внутриклеточном биосинтезе ионы металлов транспортируются в микробную клетку, и НЧ легко образуются там в присутствии ферментов внутри клетки [73]. Selvakumari et al. [53] использовали Camellia sinensis экстракт для биосинтеза SnO 2 НП. В ходе своих исследований они продемонстрировали, что полифенольные соединения (эпикатехин, эпигаллокатехин, эпикатехин галлат и эпигаллокатехин галлат), присутствующие в экстракте, действуют как блокирующие, так и стабилизирующие агенты. SnO 2 НЧ, сформированные этим методом, состоят из нескольких основных этапов, включая (i) восстановление Sn 2+ в Sn 0 , (ii) восстанавливающий эффект фенольных соединений (–OH) экстракта на образование форм Sn, и (iii) термическое превращение форм Sn в SnO 2 НП. В SnO 2 НЧ синтезированы с использованием Calotropis gigantean экстракт листьев, полифенольные соединения ответственны за биохимические превращения ионов олова [62]. Сферический SnO 2 НЧ размером 3,62–6,34 нм были синтезированы с использованием экстракта цветной капусты [52]. Было высказано предположение, что полифенолы и флавоноиды экстракта координируются с ионами металлов, что приводит к образованию Sn (OH) 2 промежуточные продукты, которые при прокаливании приводят к образованию SnO 2 НП. В другом исследовании Srivastava и Mukhopadhyay [54] сообщили как о внутриклеточном, так и о внеклеточном синтезе сферического SnO 2 НЧ ферментами, секретируемыми бактерией E. гербикола . В этом методе Sn 2+ ионы улавливаются внеклеточными ферментами, секретируемыми бактериальной клеткой, или ассоциированными с мембранами белками на поверхности клетки, и восстановление было инициировано ферментами дегидрогеназы. Sn 2+ ионы восстанавливаются за счет получения двух электронов и молекулы НАД + окисляется с образованием НАДН, что в конечном итоге приводит к образованию внеклеточных Sn NP. Биосинтезированные наночастицы Sn затем окисляются кислородом, присутствующим в растворе, что приводит к образованию SnO 2 НП. Анализ FTIR выявил присутствие на поверхности белковоподобных молекул, которые обеспечивают естественную поддержку и стабильность SnO 2 НП. Кроме того, аминокислоты играют роль укупорочных или комплексообразующих агентов, тем самым сводя к минимуму использование токсичных химикатов во время синтеза. Возможный механизм зеленого синтеза SnO 2 НП показан на рис. 2:
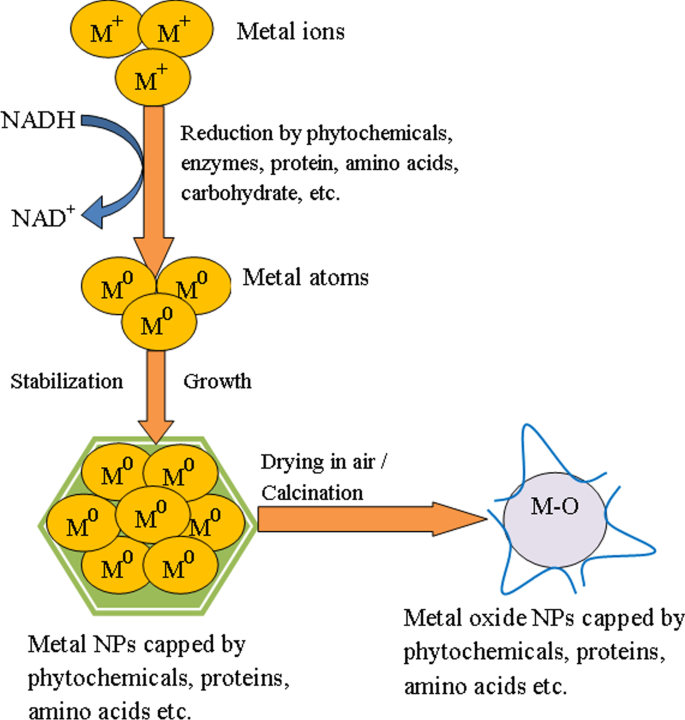
Диаграмма, показывающая возможный механизм биологически опосредованного синтеза оксида металла (SnO 2 ) НП
Характеристика наночастиц оксида олова
Характеристика наночастиц очень важна для знания и контроля процедуры синтеза и применения. Морфология поверхности и детали конформации, касающиеся размера, формы, кристалличности и площади поверхности синтезированных наночастиц, изучаются с использованием различных методов. Некоторые из методов, используемых для характеристики SnO, синтезированного в зеленом цвете 2 НЧ являются УФ-видимыми, ИК-Фурье, XRD, EDS, SEM и TEM. УФ-видимая спектроскопия используется для мониторинга образования наночастиц путем изучения их оптических свойств. УФ – видимые спектры SnO 2 НЧ синтезированы с использованием Catunaregam spinosa экстракт показал самый высокий пик поглощения 223 нм из-за его поверхностного плазмонного резонанса [57]. XRD - это мощный метод, используемый для изучения кристаллической структуры материалов. Bhattacharjee et al. [81] охарактеризован SnO 2 НЧ с пиками XRD при углах дифракции (2 θ ) 26.7, 34.2, 38.07, 51.9, 54.9, 58.1, 62.1, 64.9, 66.08, 71.6 и 79.07, соответствующие (110), (101), (200), (211), (220), (002), (310), (112), (301), (202) и (321) соответственно (рис.3). Стандартные дифракционные пики показывают тетрагональную рутильную структуру SnO 2 НЧ со средним размером кристаллитов 4,6 нм, рассчитанным по уравнению Дебая – Шерера [81].
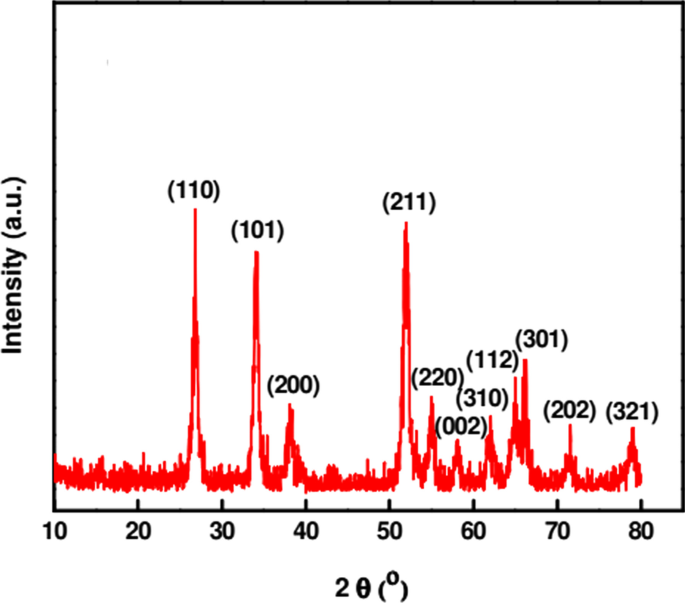
Диаграммы XRD SnO 2 НЧ, синтезированные с использованием аргинина под воздействием микроволнового излучения [81]
ИК-Фурье спектроскопия используется для исследования химии поверхности и идентификации функциональных групп, присутствующих на поверхности наночастиц, которые могут быть ответственны за восстановление, блокирование и стабилизацию наночастиц [88]. FTIR-анализ SnO 2 НЧ синтезированы с использованием Pruni flos экстракт показал основные полосы поглощения при 3308, 2153, 1634, 423, 403 и 383 см -1 . Сильные полосы, наблюдаемые при 3308, 2153 и 1634 см −1 были отнесены к валентным колебаниям групп Sn – OH за счет молекул воды, адсорбированных на SnO 2 поверхность, валент C – H алкинов и колебания C =O флавоноидов соответственно. Полосы от 423 до 383 см −1 объясняются антисимметричным растяжением Sn – O – Sn [70]. Методы, основанные на микроскопии, такие как SEM и TEM, широко используются для определения морфологических свойств наночастиц. Однако ПЭМ дает лучшее разрешение и информацию о внутренней структуре, такой как кристаллическая структура и морфология, по сравнению с СЭМ. Более точные результаты свойств поверхности можно получить с помощью FE-SEM. Эти методы также полезны для оценки среднего размера синтезированных наночастиц [89]. Анализ FE-SEM и TEM показал образование слегка агломерированного SnO сферической формы 2 НЧ со средним размером 30–40 нм (рис. 4) [62].

а ПЭМ-изображения биосинтезированного SnO 2 НП; б ВР-ТЕМ изображения SnO 2 НП; c FE-SEM изображения SnO 2 НП и д Паттерны SAED SnO 2 НП
Кроме того, анализ селективной дифракции электронов (SAED) показал, что частицы имеют нанокристаллическую природу (рис. 4) [62]. Формирование сферической формы SnO 2 НЧ синтезированы с использованием Piper betle водный экстракт был определен методом FE-SEM [63]. По данным ПЭМ и рентгеноструктурного анализа, средний размер наночастиц составил 8,4 нм.
EDS - это аналитический метод, используемый для анализа элементного состава образца. Спектры ЭДС SnO 2 НЧ синтезированы с использованием Psidium Guajava экстракт листьев показал присутствие пиков Sn и O, что подтверждает образование чистого SnO 2 НП [61].
Биологическое применение наночастиц зеленого синтезированного оксида олова
Синтезированный зеленым SnO 2 НЧ показали повышенную фотокаталитическую, антимикробную, антиоксидантную и противоопухолевую активность по сравнению с их основной формой. В этом разделе мы обсудили применение синтезированного зеленым светом SnO 2 НП в различных областях как руководство для новых исследователей на будущее.
Противомикробное действие
Многие исследователи наблюдали антимикробную активность SnO 2 НП. Например, антибактериальная активность SnO 2 НЧ синтезированы с использованием алоэ вера растительный экстракт изучали с использованием E. coli и С. золотистый . Было высказано предположение, что НП были более активны против S. золотистый чем E. coli [58]. Это может быть связано с тем, что клеточная стенка E. coli сложнее, чем S. золотистый . С. золотистый имеет мембрану, состоящую из толстого пептидогликана. Однако клеточная стенка E. coli имеет пептидогликановый слой плюс внешнюю мембрану, состоящую из липополисахарида. Наружная мембрана E. coli acts as a barrier that lowers the penetration level of ROS into the cell [90,91,92]. Another reason could be the difference in the polarity of their cell membrane. The membrane of S aureus has a more positive charge than E. coli , which result in greater penetration level of negatively charged free radicals causing more cell damage and death in S. золотистый than in E. coli [93, 94]. The antibacterial activity of SnO2 NPs synthesized using Punica granatum seed extract has been tested against E. coli. The bactericidal effect increased with increasing the concentration of the nanoparticles [95]. SnO 2 NPs synthesized using Trigonella foenum-graecum seed extract also showed similar antibacterial activity against E. coli [72]. In a recent study, Clerodendrum inerme leave extract was used for the synthesis of un-doped and Co-doped SnO2 NPs [96]. The green synthesized un-doped and Co-doped SnO2 NPs were subjected toward antimicrobial activity against five disease-causing pathogens such as E. coli , B. subtillis , A. niger , A. flavus , and C. Albicans, , and their zone of inhibition diameters (ZOIs), minimum inhibitory concentration (MIC), and minimum bactericidal concentration (MBC) were calculated. The Co-doped SnO2 NPs showed substantial antibacterial activity against E. coli and B. subtillis in a concentration-dependent manner compared to the un-doped SnO2 NPs, plant extract, and standard drugs in terms of their MIC (22 ± 0.7, 18 ± 0.8 mg/mL) and MBC (31 ± 0.9, 21 ± 0.6 mg/mL) as well as ZOIs (30 ± 0.08, 26 ± 0.06 nm), respectively. The authors suggested that the broad-spectrum antibacterial activity of Co-doped SnO2 NPs is due to cobalt doping, which leads to increased grain size and surface area of the NPs as compared to un-doped SnO2 НП. As more is the surface area with smaller particle sizes, the greater will be the antimicrobial activity. The associations of biomolecules like flavonoids and phenolic compounds with Co-doped SnO2 NPs are also responsible for the enhancement of their antimicrobial activity. Furthermore, the green synthesized Co-doped SnO2 NPs showed extraordinary antifungal activity with maximum ZOIs of 17 ± 0.04, 23 ± 0.08, and 26 ± 0.06 nm against A. niger , A. flavus, and C. Albicans, respectively, in comparison with plant extract, un-doped SnO2 NPs, and standard drugs [96].
The actual mechanism of action of SnO2 NPs against microbial strains is still unknown. However, several mechanisms of action against bacteria have been suggested for metal oxide nanoparticles, such as the decomposition of nanoparticles, electrostatic interaction of nanoparticles with the cell wall of microorganisms, and formation of reactive oxygen species (ROS) by the effect of light radiation [97,98,99]. One possible cause for the antibacterial effect of SnO2 NPs may be the accumulation of the NPs on the surface of the bacterial cell membrane. The ROS generated due to the presence of SnO2 NPs interacts with the cell membrane and disturbs the membrane permeability and respiration system of the bacteria, which leads to cell death [72, 95, 100]. For instance, Khan et al. suggested that the release of Sn 4+ и Co 2+ is responsible for the damage of bacterial DNA and mitochondria, which inactivates the bacterial enzyme and finally leads to cell death [96].
Antioxidant Activity
Many researchers examined the antioxidant activity of NPs by monitoring the ability in quenching of stable DPPH (2,2-diphenyl-1-picrylhydrazyl) radical into non-radical form (DPPH-H). Kamaraj et al. [101] reported the antioxidant activity of SnO2 NPs biosynthesized using Cleistanthus Collinus leaves extract. The antioxidant activity of SnO2 NPs increased with increasing concentration of SnO2 NPs and reaction time. In another study [95], the free radical scavenging activity of green synthesized SnO2 NPs increased in a dose-dependent manner. However, the annealed sample exhibited a lower scavenging activity as compared to the as-prepared sample. The decrease in scavenging activity with increasing annealing temperature may be due to a decrease in surface area-to-volume ratio of the NPs. Moreover, the antioxidant efficacy of SnO2 NPs against DPPH is due to the transfer of electron density between the NPs and the free radical located at nitrogen in DPPH. A similar result was found for SnO2 NPs synthesized using Trigonelle foenum-graecum aqueous extract [72]. Hong et al. [67] reported significant antioxidant properties of biosynthesized SnO2 НП. The antioxidant activity of the biosynthesized SnO2 increased with increasing concentration of the NPs, with IC50 (half-maximal inhibitory concentration) value of 2257.4 µg/ml. Recently, Khan et al. reported significant antioxidant activity of Co-doped SnO2 NPs, as compared to un-doped SnO2 NPs and plant extract [96].
Cytotoxic Activity
SnO 2 NPs synthesized using an aqueous extract of agricultural waste of dried peel of Annona squamosa were evaluated for cytotoxicity test against the hepatocellular carcinoma cell line (HepG2) [64]. TEM results revealed the loss of cell volume, considerable swelling of the cells, and nuclear condensation. The nuclear condensation seen in SnO2 NP-treated HepG2 cells might be due to the breakdown of chromatin in the nucleus. SnO 2 NPs inhibited cell proliferation in a dose- and time-dependent manner with an IC50 value of 148 µg/mL. SnO 2 NPs synthesized using piper nigrum seed extract exhibited higher cytotoxic activity against colorectal (HCT116) and lung (A549) cancer cell lines [69]. The proliferation of both cancer cell lines increased with increasing NPs size. Besides, a gradual decline in cell viability was observed with increasing dosage of SnO2 НП. The authors concluded that the cytotoxic effect was associated with the generation of oxidative stress from reactive oxygen species (ROS). SnO 2 NPs fabricated by using Pruni spinosae flos aqueous extract revealed an excellent cytotoxic effect against non-small cell lung cancer cell A549 and lung fibroblast CCD-39Lu cells, in concentration- and time-dependent manner [70]. Recently, Khan et al. [96] investigated the in vitro cytotoxic effect of green synthesized un-doped SnO2 NPs and Co-doped SnO2 NPs against mammary gland breast cancer (MCF-7), human amnion (WISH), and human lung fibroblast (WI38) cell lines by a colourimetric technique 3-(4,5-dimethylthiazol-2yl)-2,5-diphenyl tetrazdium bromide (MTT) assay. The green synthesized Co-doped SnO2 NPs showed significant and substantial mortality rate compared to un-doped SnO2 NPs, plant extract, and standard drug 5-FU (5-5-5-fluorouracil), while un-doped SnO2 NPs exhibited a similar mortality rate to that of the standard drug, but the lowest cytotoxicity against breast cancer cell line was observed with the plant extract. The cytotoxic effect of the plant extract, green synthesized un-doped SnO2 , and Co-doped SnO2 NPs was performed with IC50 values of 31.56 ± 1.4, 26.99 ± 1.9, and 18.15 ± 1.0 µg/mL for MCF-7, and 40.69 ± 0.9, 38.97 ± 0.8, and 36.80 ± 0.6 µg/mL for WI38, and 38.56 ± 0.8, 35.56 ± 0.9, and 31.10 ± 0.7 µg/mL, respectively, and depicted that the cytotoxicity of Co-doped SnO2 NPs was more proficient as compared to plant extract and un-doped SnO2 NPs alone. Additionally, the authors reported excellent observational results showing greater in vitro inhibition of breast cancer MCF-7 cell lines in a concentration- and dose-dependent manner. The green synthesized NPs also showed robust cytotoxicity against MCF-7 as compared to WI38 and WISH normal cell lines with Co-doped SnO2 NPs unveiling higher ROS generation than the un-doped SnO2 НП. Figure 5 shows the probable cytotoxicity mechanism of green synthesized SnO2 NPs.
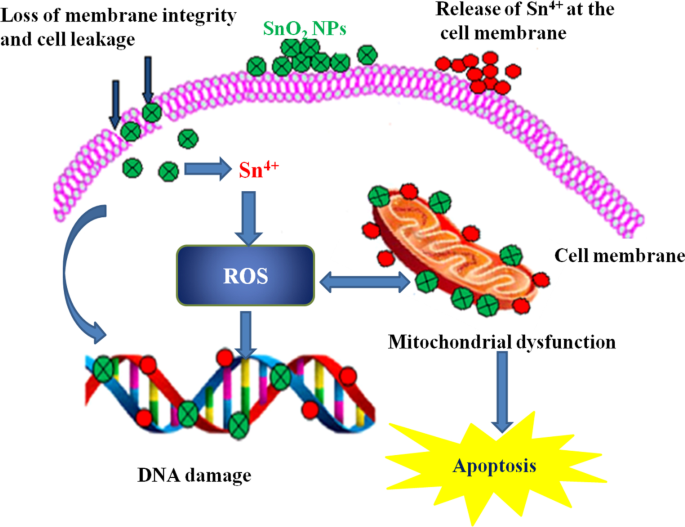
Mechanism during cytotoxicity of green synthesized SnO2 НП
Photocatalytic Activity
The uncontrolled release of toxic chemicals, hazardous textile dyes, and pesticides from various industries into the running water has led to severe environmental problems. These superfluous water contaminants cause long-term adverse effects and pose a real threat to aquatic and human life. Besides, some organic dyes are carcinogenic and toxic. Hence, treating water that contains poisonous chemicals before disposal to the environment is very crucial to reduce environmental pollution. Recent studies have shown that nanostructured semiconductor metal oxides act as an excellent photocatalyst for the removal of various water pollutants [102,103,104,105]. Among the semiconductor metal oxides, SnO2 is extensively used in the removal of common textile dyes and organic compounds owing to its beneficial characteristics, which include physical and chemical stability, high surface reactivity, high photocatalytic efficiency, low cost, and low toxicity [68, 106]. Manjula et al. [107] synthesized SnO2 nanoparticles using glucose. The NPs were effectively used as a catalyst in degrading methyl orange (MO) dye. The effect of calcination temperature (150–500 °C) on the photocatalytic activity of the NPs was investigated, and the results revealed that the as-synthesized SnO2 NPs calcinated at 150 °C is the best photocatalyst for the reaction under study among the studied materials. Moreover, the as-prepared SnO2 nanoparticles degraded methyl orange completely in 30 min, and also, the nanomaterials may be recycled with enhanced efficiency a minimum of five times. In another study [108], the photocatalytic activity of the SnO2 QDs (quantum dots) synthesized by using serine was evaluated by monitoring the optical absorption spectra of eosin Y solution under direct sunlight. It was observed that the rate of degradation of eosin Y using SnO2 QDs (98%) is higher than that using commercial SnO2 (96%) and P25 (88%). Begum et al. [84] reported the synthesis of SnO2 NPs using an amino acid, L-lysine monohydrate. The synthesized nanoparticles were evaluated for their photocatalytic behavior toward toxic organic dyes, namely malachite green oxalate (MGO) and Victoria blue B (VBB) under direct sunlight. The absorption peak of these dyes has begun to reduce, which shows that the chromophore structure has been demolished (Fig. 6). Furthermore, the as-prepared SnO2 NPs exhibited an outstanding photocatalytic degradation of MGO (97.3%) and VBB (98%) dye within 120 min. Literature reports on the photocatalytic activity of green synthesized SnO2 NPs are summarized in Table 3.
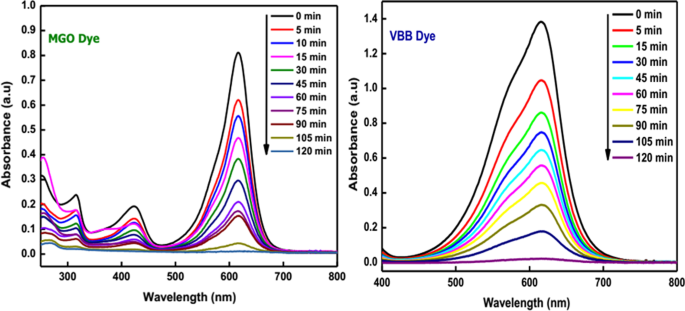
Photocatalytic degradation of malachite green oxalate dye under solar irradiation using SnO2 НП
Gas-Sensing Property
Many metal oxide-based gas sensors are widely used for gas-sensing applications. However, SnO2 NPs has gained tremendous attention in gas sensing under atmospheric conditions because of its beneficial properties, which include high sensitivity, high selectivity, easy reversibility, and cheap manufacturing costs. Green synthesized porous SnO2 nanospheres demonstrated excellent gas sensing capabilities [107]. It was observed that the assimilation of 0.5 wt% Pd into the SnO2 matrix improved the sensitivity and made it highly selective for low-temperature hydrogen detection. Moreover, the fabric was able to respond to even 50 ppm H2 in N2 at room temperature with an interval of 10 s. These sensing properties are due to the synergetic effect of both the porous structure of SnO2 nanospheres and also the catalytic property of Pd nanoparticles. Gattu et al. [77] reported the gas-sensing behavior of biosynthesized and chemically synthesized Ni-doped SnO2 NPs thin films. The biosynthesized Ni-doped SnO2 NPs thin film showed higher NO2 gas-sensing response as compared to the chemically synthesized ones. The sensor response was found to be increased with Ni doping for both biosynthesized and chemically synthesized Ni-doped SnO2 НП. This may be due to the reduction of particle size with Ni-doping, which results in increased surface area for adsorption of NO2 газ. Furthermore, the Ni-doped SnO2 thin film exhibited excellent selectivity toward NO2 gas when put next to other gases like NH3 , LPG and H2 S. In another study [78], the gas-sensing properties of un-doped and Fe-doped SnO2 NPs synthesized using Cicer arietnum L. extract were reported. The gas response within the presence of 100 ppm NH3 gas at 200 °C operating temperature was found to be 28% for un-doped SnO2 and 46% for Fe-doped SnO2 thin films. Moreover, the Fe-doped SnO2 -based sensor was found to be more selective for NH3 gas as compared to the un-doped SnO2 датчик. The biosynthesized Au-doped SnO2 NPs were found to be highly sensitive to NO2 gas at 200 °C operating temperature [79]. Gas sensor supported Au-doped SnO2 NPs showed the gas response of ~ 30% for 100 ppm of NO2 газ. Additionally, the gas sensor of Au-doped SnO2 NPs showed excellent selectivity toward NO2 gas when put next to other gases like H2 S, LPG, and NH3 . The improved gas response and selectivity toward NO2 gas are because of the lattice distortion induced by Au-doping and also the oxygen vacancies generation within the SnO2 lattice.
Выводы
The use of green methods for the production of NPs has been the area of focused research because it is an eco-friendly, inexpensive, nontoxic, and sustainable method. Numerous studies report the possibility of producing SnO2 NPs via a green protocol using a range of plant materials, bacteria, and natural biomolecules. The literature survey shows that the green substrates act as reducing and stabilizing agents or capping agents regardless of their source. Among the various green methods of SnO2 synthesis, plant-mediated synthesis is cost-effective, easy to process, and less hazardous than microorganisms. However, the plant extracts consist of a large number of active compounds in a different composition, which makes it difficult to know the exact amount of the molecules responsible for the reduction of metal ions. Due to this complexity, it is difficult to evaluate the synthesis of nanoparticles. Therefore, further study on the mechanism of formation of SnO2 NPs is required to understand the chemical reactions that occur during the synthesis. With the knowledge of the actual reaction mechanism, it will be possible to monitor and optimize the biosynthesis process, which is essential for the large-scale production of SnO2 НП. Hence, understanding of the rapidly growing method of synthesis discussed herein will help facilitate future research progress on SnO2 NPs and their enormous potential for industrial-scale production in the near future.
Доступность данных и материалов
Not available.
Сокращения
- НП:
-
Наночастицы
- SnO2 НП:
-
Tin oxide nanoparticles
- УФ-видимый:
-
Ультрафиолетовая и видимая спектроскопия
- SEM:
-
Сканирующая электронная микроскопия
- FE-SEM:
-
Автоэмиссионная сканирующая электронная микроскопия
- ТЕМ:
-
Просвечивающая электронная микроскопия
- HR-TEM:
-
Просвечивающая электронная микроскопия высокого разрешения
- FTIR:
-
Инфракрасная спектроскопия с преобразованием Фурье
- EDS:
-
Энергодисперсионный рентгеновский анализ
- PSA:
-
Particle size analyzer
- XPS:
-
X-ray photoemission spectroscopy
- SAED:
-
Selective area electron diffraction
Наноматериалы
- Специальные оксидные огнеупоры и их применение
- Многофункциональные наночастицы золота для улучшенных диагностических и терапевтических применений:обзор
- Получение наночастиц mPEG-ICA, нагруженных ICA, и их применение в лечении LPS-индуцированного повреждения клеток H9c2…
- Биогенный синтез, характеристика и оценка антибактериального потенциала наночастиц оксида меди против Escheric…
- Потенциальная токсичность наночастиц диоксида титана для печени, мозга и эмбрионов у мышей
- Формирование и люминесцентные свойства нанокомпозитов Al2O3:SiOC на основе наночастиц оксида алюминия, модифици…
- Получение наноструктуры Au @ TiO2 - оболочка и ее применение для разложения и обнаружения метиленового синего
- Легкий синтез червоточиноподобного мезопористого оксида олова за счет самосборки, вызванной испарением, и у…
- Зеленая способность к синтезу и стабилизации наночастиц меди:каталитическая, антибактериальная, цитотоксич…
- Сапонины Platycodon из Platycodi Radix (Platycodon grandiflorum) для зеленого синтеза наночастиц золота и серебра



