Повышенная протонная проводимость и снижение проницаемости для метанола с помощью биомембраны из альгината натрия, электролита и сульфированного оксида графена
Аннотация
Высокая степень кроссовера метанола и высокая стоимость мембраны Nafion® являются основными проблемами при использовании топливных элементов с прямым метанолом. С целью решения этих проблем была создана мембрана из полимерного электролита, отличного от Nafion, с низкой проницаемостью для метанола и высокой протонной проводимостью на основе полимера альгината натрия (SA) в качестве матрицы и сульфированного оксида графена (SGO) в качестве неорганического наполнителя (0,02-0,2 % масс.) получали простым методом литья из раствора. Сильное электростатическое притяжение между -SO 3 H SGO и полимер альгината натрия увеличивают механическую стабильность, оптимизируют водопоглощение и, таким образом, ингибируют кроссовер метанола в мембране. Оптимальные свойства и рабочие характеристики были продемонстрированы мембраной SA / SGO с загрузкой 0,2 мас.% SGO, которая дала протонную проводимость 13,2 × 10 −3 . Scm −1 , а проницаемость для метанола составляла 1,535 × 10 −7 см 2 s −1 при 25 ° C, что намного ниже, чем у Нафиона (25,1 × 10 −7 см 2 s −1 ) при 25 ° C. Механические свойства полимера альгината натрия с точки зрения прочности на разрыв и удлинения при разрыве были улучшены добавлением SGO.
Фон
Простое преобразование химической энергии топлива посредством химической реакции в электричество может быть выполнено только с помощью устройства на топливных элементах. Что касается этой возможности, топливный элемент с прямым метанолом (DMFC) получил большое внимание, потому что он может работать с использованием только 17% метанола в качестве топлива для производства электроэнергии с меньшими выбросами загрязняющих веществ по сравнению с другими методами, а также безопасен для использования во время полета [1] . DMFC имеет широкие возможности во многих приложениях, таких как медицинские инструменты, слуховые аппараты и портативные инструменты. К сожалению, его применение было затруднено из-за отсутствия коммерциализации, что объясняется такими проблемами, как высокая стоимость производства (примерно 1000 долларов США за метр −2 ) [2], высокая проницаемость для метанола серийно выпускаемых мембран (нафион) и низкая реакционная способность и низкая стойкость действующих электрокатализаторов (палладий и рутений) [3]. Протонно-электролитная мембрана является наиболее важным компонентом DMFC, поскольку она действует как сепаратор топлива и окислителя, а также как путь для проведения протонов; следовательно, это может иметь существенное влияние на общую эффективность системы. Среди требуемых характеристик мембраны мембрана должна иметь высокую протонную проводимость и способность эффективно блокировать прохождение метанола через мембрану, чтобы избежать отравления катодной стороны [4]. Кроме того, важно обеспечить использование безопасного недорогого сырья для мембраны. Текущая коммерческая мембрана (Nafion) не отвечает этим основным требованиям; следовательно, это не лучшая мембрана для применений DMFC из-за ее высокой проницаемости для метанола, высокой стоимости и использования опасных материалов. Кроме того, эти проблемы влияют на его протонную проводимость, что, следовательно, ограничивает его эффективность в приложениях DMFC. В настоящее время биоматериалы привлекают внимание, потому что они безопасны и экологически чисты, что относит их к материалам экологически чистых технологий. В качестве нового и превосходного биоматериала альгинаты заинтриговали многих исследователей из различных областей применения, включая тканевую инженерию, биомедицину, средства доставки лекарств, упаковку пищевых продуктов и DMFC [5]. Альгинат - это известный водорастворимый полисахарид, содержащийся в коричневых морских водорослях, и он состоит из (1-4) -связанных звеньев β-d-маннуроновой кислоты (M) и α-1-гулуроновой кислоты (G). Он имеет очень высокое водопоглощение и может поглощать воду в 200–300 раз больше своего собственного веса [6]. Способность чистого альгината к протонной проводимости низкая из-за отсутствия путей непрерывного переноса и слабой проводящей способности полимера [6,7,8,9]. Предыдущие исследования показали, что наиболее эффективным методом улучшения механических свойств и уточнения других свойств этого полимерного материала является введение неорганического материала и полимерной основы [7]. Композиционные материалы могут расширять или предоставлять новые возможности, которые трудно получить, используя каждый компонент по отдельности. Например, механическая прочность альгината была успешно увеличена за счет введения углеродных нанотрубок и оксида графена в матрицу альгинатного полимера [3, 10, 11]. Предыдущие исследования по разработке мембран на основе биополимеров показали хороший потенциал в сочетании с другими материалами, такими как неорганические или синтетические полимеры, например, двухслойный хитозан (1,67 × 10 −6 см 2 s −1 ) [12], хитозан-ПВС / нафион (2.2 × 10 −6 см 2 s −1 ) [13], хитозан-SHNT (0,76 × 10 −2 Scm −1 ) [14], хитозан-цеолит (2,58 × 10 -2 См см −1 ) [15], хитозан-ПМА (1,5 × 10 -2 См см −1 ) [16], хитозан-альгинат натрия (4,2 × 10 -2 См см −1 ) [17], альгинат-каррагинан (3,16 × 10 -2 См см −1 ) [18], сульфированный хитозан-SGO (72 × 10 -2 См см −1 ) [19], PVA-альгинат натрия (9,1 × 10 −2 См см −1 ) [20], биоцеллюлоза-нафион (7,1 × 10 −2 См см −1 ) [21], хитозан-SPSF (4,6 × 10 -2 См см −1 ) [22], хитозан-диоксид кремния / углеродные нанотрубки (УНТ) (2,5 × 10 −2 См см −1 ), хитозан-ПВП (2,4 × 10 -2 См см −1 ) [23], наноцеллюлоза / полипиррол (1,6 мВт см −2 ) для ферментативных топливных элементов [24], нановолокна целлюлозы (УНВ) (0,05 × 10 −3 См см −1 ) и нанокристаллы целлюлозы (ЧПУ) (4,6 × 10 −3 См см −1 ) [25], бактериальная целлюлоза (BC) / поли (4-стиролсульфоновая кислота) (PSSA) (0,2 См см -1 ) [26], и нанокристаллической целлюлозы, легированной имидазолом (2,79 × 10 −2 См см −1 ) [27]. Однако количество разработанных мембран на основе биополимеров слишком мало по сравнению с исследованиями с участием синтетических полимеров во многих областях, включая топливные элементы. Кроме того, бесспорно, хитозану уделялось больше внимания, чем другим углеводным полимерам.
Оксид графена является многообещающим материалом на основе углерода с большим потенциалом для многих приложений, включая электронику, нанокомпозиты, биомедицину и топливные элементы. Оксид графена обладает превосходными свойствами, такими как высокое удлинение, высокая проводимость, высокая механическая прочность, уникальная графитированная плоская структура и электроизоляционные свойства [28]. В качестве добавочного материала в гидрофильной полимерной матрице он обеспечивает высокую упругость, чтобы противостоять набуханию, вызванному влагой. Кроме того, оксид графена был бы предпочтительнее УНТ из-за его гораздо более низкой стоимости, что делает его наиболее подходящим кандидатом для мембран в приложениях DMFC [29]. Предыдущие исследования показали, что ОГ усиливает природные полимеры, такие как хитозановые пленки и пористые монолиты хитозан-желатин [19, 30]. Bayer et al. [31] подготовили статью GO, которая показала проницаемость для водорода в три раза ниже, чем нафион, и протонную проводимость 49,9 мСм −1 . используя технику в плоскости. Характеристики жидкостных топливных элементов прямого действия (DLFC) были превосходными, когда Lue et al. [32] представил ГО в Нафион. Однако эффективность ГО в качестве проводника протонов ограничена, поскольку в нем отсутствуют функциональные группы, которые могут быть переносчиками протонов в мембране, что отрицательно влияет на протонную проводимость и снижает производительность топливного элемента [19]. Карим и др. [33] сообщили, что проводимость нанолиста GO в их исследовании составляла 15 мСм см −1 . и проводимости GO, сообщенные Hatakeyama et al. [34] и Bayer et al. [35] составляли 0,4 мСм −1 . и 0,55 мСм −1 , соответственно. Основываясь на этих недостатках, сульфированный ГО считается лучшим вариантом, чем ГО для этого приложения, поскольку сульфированный ГО показал повышенную протонную проводимость и способствует образованию гомогенной мембраны из-за высокой совместимости между ГОС и SO 3. H [19]. Кейт и др. [36] представили документ SGO, который показал высокую максимальную плотность мощности 113 мВт · см −2 . при 0,39 В для топливного элемента с мембраной с полимерным электролитом (PEMFC). Преимущества –SO 3 Включение H заключается в следующем:(i) кислотные группы могут предлагать дополнительные места перескока для движения протонов, и (ii) электростатическое притяжение улучшит термическую и механическую стабильность, препятствуя подвижности и упаковке альгинатной цепи. На основании наших исследований, ни один нанокомпозитный альгинатный / SGO материал еще не был произведен с использованием этого метода. Использование биоматериалов в электрических устройствах приведет к междисциплинарным исследованиям между биологическими науками и устойчивыми энергетическими технологиями. Таким образом, это исследование объединит преимущества альгината и SGO для формирования новой биомембраны с высокой прочностью, хорошей протонной проводимостью и проницаемостью для метанола с целью, чтобы она работала лучше, чем Nafion или другие коммерческие протонообменные мембраны (PEM) в качестве кроме того, его производство намного дешевле, чем на Nafion.
Методы
Материалы
Природный графит TIMREX PG25 был приобретен у TIMCAL Ltd. Концентрированная серная кислота (H 2 SO 4 , 95%), метанол (CH 3 ОН, 99,7%), перманганат калия, соляная кислота, водный раствор перекиси водорода (H 2 О 2 , 35%), хлорид кальция, этанол, сульфаниловая кислота, раствор нитрита натрия и глицерин были получены от Sigma Aldrich. Эти химические вещества использовали в том виде, в котором они были получены, без дополнительной очистки. Во всех экспериментах использовалась деионизированная (ДИ) вода через систему Millipore (Milli-Q).
Подготовка мембраны
Метод Хаммера был модифицирован и применен для получения ГСН из природного графита [10, 37]. Сначала 2 г графита были смешаны со 150 мл H 2 . SO 4 (95%) в колбе емкостью 500 мл. Смесь перемешивали 30 мин на ледяной бане. При непрерывном и энергичном перемешивании к смеси добавляли 15 г перманганата калия. Скорость добавления тщательно контролировали, чтобы поддерживать температуру реакции на уровне 20 ° C. Затем смесь перемешивали и оставляли на ночь при комнатной температуре с последующим добавлением 180 мл воды при интенсивном перемешивании и кипячении с обратным холодильником при 98 ° C в течение 24 часов; это привело к тому, что раствор стал желтым. Восемьдесят миллилитров 35% H 2 О 2 добавляли к реакционной смеси, которой давали остыть до комнатной температуры, чтобы погасить реакцию с помощью KMnO 4 . Полученный GO промывали 5% HCl с последующим центрифугированием. Наконец, продукт несколько раз промывали деионизированной водой, фильтровали и сушили в условиях вакуума.
Пятьдесят миллилитров оксида графена добавляли к 8 мл 0,06 М раствора сульфаниловой кислоты при 70 ° C. При непрерывном перемешивании к смеси по каплям добавляли 2 мл раствора нитрита натрия и оставляли на 12 ч при постоянной температуре 70 ° C. После завершения реакции смесь промывали и собирали центрифугированием. Собранный SGO еще несколько раз промывали водой до достижения pH 7. Частицы SGO были охарактеризованы с помощью рентгеновской фотоэлектронной спектроскопии (XPS). Альгинат натрия растворяли в 1% ( w / v бидистиллированная вода для получения раствора альгината. Содержание SGO, добавляемого в раствор альгината, варьировалось со значениями 0,02, 0,05, 0,09, 0,13, 0,17 и 0,2 мас.% Для получения композитной пленки. Смесь непрерывно перемешивали в течение 60 мин с помощью магнитной мешалки. Гетерогенный раствор переносили на стеклянную подложку и оставляли при 60 ° C на 72 часа, чтобы обеспечить процесс формирования тонкой пленки. Затем высушенная мембрана из альгината / сульфированного оксида графена была сшита с использованием раствора хлорида кальция / глицерина для увеличения механической прочности и снижения гидрофильных свойств альгината. Мембрану погружали на 30 минут в 100 мл сшивающего раствора, концентрация катионов которого поддерживалась на уровне 1,5% w / v . Наконец, все свободные катионы удаляли с поверхности мембраны промыванием деионизированной водой, и мембрану сушили при 25 ° C. Методика приготовления представлена на схеме 1.
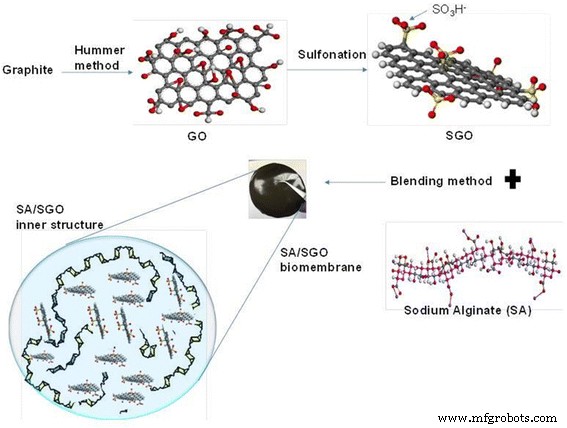
Наполнитель сульфированного оксида графена (SGO) и способ получения биомембраны SA / SGO
Характеристика мембраны
Были проанализированы инфракрасные спектры с преобразованием Фурье (FTIR PERKIN ELMER) оксида графена, сульфированного оксида графена и мембраны. Длина волны FTIR находилась в диапазоне 4000–500 см −1 . . Микроструктуру пленочных мембран исследовали с помощью автоэмиссионного сканирующего электронного микроскопа (FEI QUANTA 400 FESEM) с рабочим напряжением 5 кВ в качестве меры предосторожности для образца на основе биоматериала. Анализ просвечивающей электронной микроскопии высокого разрешения (HRTEM) проводился с использованием o Digital TEM HT7700, работающего при ускоряющем потенциале 300 кВ.
Образцы готовили на сетках с кружевной углеродной опорной пленкой. XPS использовался для определения химического состава поверхности образца с помощью Axis Ultra DLD. Механическая прочность мембраны SA / SGO была проверена на универсальной испытательной машине, включая предел прочности на разрыв, модуль Юнга и удлинение при разрыве. Используемая нагрузка составляла 3 кН при комнатной температуре. Изменения веса и длины (или толщины) влажных и сухих мембран могут определять скорость водопоглощения и коэффициент набухания мембраны. Обычно мембрану замачивали в воде на 2 дня при 30 ° C. Для влажной мембраны регистрировали вес и длину, а затем удаляли воду в мембране и капли жидкости на поверхности мембраны. Кроме того, влажную мембрану сушили под вакуумом и температурой 120 ° C в течение не менее 24 часов. Также регистрировали вес и длину мембраны в сухом состоянии. Используя уравнения. 1 и 2, можно определить водозабор (WU%) и коэффициент набухания (SW%), где L мокрый представляет влажную массу и л сухой представляет собой сухую массу, полученную из длины влажной и сухой мембран соответственно.
$$ \ mathrm {WU} \% =\ frac {{\ mathrm {mass}} _ {\ mathrm {wet}} - {\ mathrm {mass}} _ {\ mathrm {dry}}} {{\ mathrm { масса}} _ {\ mathrm {dry}}} \ times 100 $$ (1) $$ \ mathrm {SW} \% =\ frac {L _ {\ mathrm {wet}} - {L} _ {\ mathrm { dry}}} {L _ {\ mathrm {dry}}} \ times 100 $$ (2)Расчет поглощения метанола аналогичен расчету поглощения воды, за исключением того, что раствор для иммерсии заменяется на метанол, а не на деионизированную воду.
Протонную проводимость приготовленной мембраны рассчитывали с использованием четырехэлектродной ячейки для измерения проводимости, подключенной к потенциостату / гальваностату (WonATech), работающей в диапазоне частот от 1 МГц до 50 Гц. Мембраны (размером 1 см × 4 см) необходимо замачивать в воде на 24 часа для измерения проводимости в полностью гидратированном состоянии. Для получения графика зависимости напряжения от тока использовали потенциостат. Наклон прямой линии - это сопротивление мембраны. На схеме 1 представлена ячейка теста протонной проводимости. Протонную проводимость можно рассчитать по следующей формуле:
$$ \ sigma =\ frac {L} {RWT} $$ (3)где L расстояние между двумя электродами, W ширина мембраны, T - толщина мембраны, а R - сопротивление мембраны, аналогично методу в предыдущих работах [38, 39].
Две ячейки жидкостной проницаемости резервуара с 20 v / v % метанола использовали для определения проницаемости мембраны для метанола. Различия в концентрации метанола приводят к прохождению метанола через мембрану, и может быть определена проницаемость для метанола. Уравнение 3 используется для расчета проницаемости метанола:
$$ P =\ frac {1} {Ca} \ left (\ frac {\ Delta Cb (t)} {\ Delta t} \ right) \ left (\ frac {LVb} {A} \ right) $$ ( 4)где P - диффузионная проницаемость мембраны для метанола (см 2 s −1 ), C a - концентрация метанола в загрузочной камере, т.е. ячейке A (моль л −1 ), ∆Cb ( т ) / ∆t - изменение молярной концентрации метанола в ячейке B как функция времени (моль л −1 s), V b - объем каждого диффузионного резервуара (см 3 ), А - площадь мембраны, а L толщина мембраны (см).
Характеристики мембраны можно определить путем расчета селективности мембраны, которая может быть достигнута за счет высокой протонной проводимости и низкой проницаемости для метанола. Формула, используемая для расчета селективности, выглядит следующим образом:
$$ \ varphi =\ frac {\ sigma} {P} $$ (5)где φ представляет селективность, σ представляет ионную проводимость, а P представляет проницаемость для метанола.
Результаты и обсуждение
Характеристика сульфированного оксида графена (SGO) и биомембраны SA / SGO
Спектры FTIR на рис. 1a, b показывают разницу между GO и SGO, которую можно отчетливо наблюдать. Рис. 1b - увеличенное изображение Рис. 1a, чтобы получить более четкое представление пиков в спектрах SGO. В спектре SGO появляется новая полоса при 1244 см -1 . , который представляет собой типичное поглощение группы сульфоновой кислоты (-SO 3 H), тогда как спектр GO не содержит этой полосы [40]. Кроме того, в спектре видны новые пики на длинах волн 1012, 1036 и 1125 см -1 . , которые считаются симметричными и асимметричными валентными колебаниями SO 3 H - группы. Этот новый спектр показывает, что раствор оксида графена был успешно модифицирован в сульфированный оксид графена с использованием простого метода, описанного выше. В то же время модификация сульфирования все еще сохраняет функциональные группы в GO, такие как гидроксильная группа, на уровне 3319 см -1 . и карбоксильная группа при 1636 см -1 . Дальнейшее подтверждение наличия SO 3 H - группы можно определить с помощью анализа XPS.
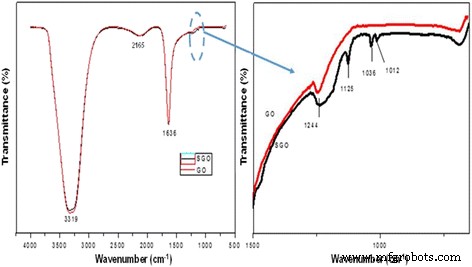
а , b FTIR-спектры оксида графена (GO) и сульфированного оксида графена (SGO)
На рис. 2 показаны XPS-спектры мембран GO и SGO, в которых спектры сканирования находятся в диапазоне 0–800 эВ для распознавания поверхности существующих элементов с помощью измеримого анализа. Видно, что сигналы C1s и O1s проявляются при 286 и 531 эВ соответственно как в спектрах GO, так и в спектрах SGO. Также замечено, что после введения групп сульфоновой кислоты в ГО появился новый пик S2p при 168 эВ. Сульфоновые группы в SGO способствовали незначительному увеличению интенсивности в спектрах O1s по сравнению со спектрами GO. Спектр высокого разрешения C1s, который называют гауссовой спектральной деконволюцией, подтвердил, что GO был успешно адаптирован с помощью химической модификации [41]. На рисунке внутри рис. 2b показаны спектры S2p функционализированного GO при большем увеличении. Энергия связи сульфогрупп способствовала появлению пика S2p при 168 эВ, и этот пик подтвердил, что группы сульфоновой кислоты были успешно прикреплены к основной цепи нанолиста GO [41, 42].
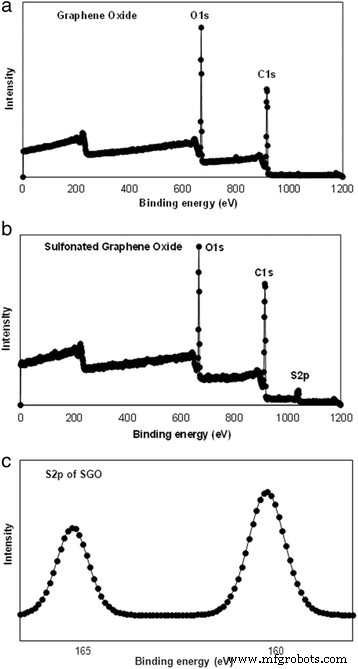
XPS из а , b широкие спектры ГО и СГО и c Спектры S2p SGO
Успешное производство ГО с помощью метода Хаммера было подтверждено листовой морфологией ГО, как показано на изображении FESEM (рис. 3а). Bai et al. [43] также сгенерировали GO методом Хаммера. Результаты их исследований показали, что морфология как GO, так и RGO оказалась слегка изогнутой и образовала несколько складок, которые напоминают морфологию GO в этом исследовании.

а FESEM изображение GO. б , c FESEM-изображения SGO с разным увеличением и d EDX СГО
Изображение SGO с помощью FESEM на рис. 3b, c имеет скомканную и более шероховатую поверхность по сравнению с поверхностью GO, что, скорее всего, связано с эффектами процесса сульфирования, подтверждая, что метод модификации также был успешно применен [41, 44 ]. Это коррелирует с наличием нового пика в спектрах пропускания FTIR, который принадлежит к сульфоновой группе. Более того, присутствие сульфогрупп было также подтверждено в листе GO с помощью анализа XPS. СГО отличалось от ГО, которое имело многослойную структуру без какой-либо агрегации. Применяемый метод модификации приводит к формированию слоистой и переупакованной структуры; Таким образом, СГО продемонстрировало свою гибкость. Результат энергодисперсионного рентгеновского излучения (EDX) показывает, что 1,76 мас.% Серы содержится в листах SGO (рис. 3d).
Изображение поверхности и поперечное сечение биомембран SA и SA / SGO показаны на рис. 4. Рис. 4a – c представляет собой изображение поверхности, а рис. 4d – f - изображение поперечного сечения мембран с различным содержанием SGO. И малое, и большое увеличение показывают, что лист SGO полностью однородно диспергирован в общей полимерной матрице и управляется межмолекулярными взаимодействиями; признано, что водородные связи возникают между группами сульфоновой кислоты в SGO и полярными группами (-O-, C =O) в мембране SA / SGO [45]. SGO помещается в полимерную матрицу и действует как барьер для молекул метанола. Изображение для SA / SGO6 выглядит лучше при полном распространении на всю полимерную матрицу альгината натрия. Фиг. 5 представляет собой ПЭМ-изображение сформированного композита, в котором нанолисты SGO хорошо распределены в полимерной матрице альгината натрия. Альгинат натрия присутствует в структуре частиц наносферы, которая аналогична предыдущему исследованию, опубликованному Marrella et al. [46].
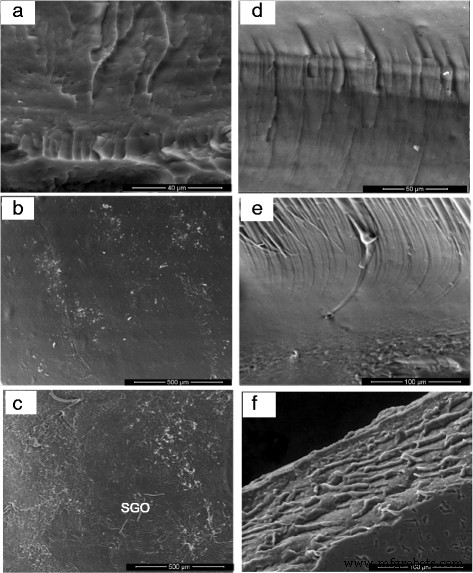
FESEM-изображения морфологии поверхности и поперечного сечения для a , d альгинат натрия, b , e SA / SGO4 и c , f Биомембраны SA / SGO6

ПЭМ-изображение нанолистов SGO, распределенных в полимерной матрице альгината натрия
Наличие взаимодействий водородных связей между SGO и альгинатной полимерной матрицей показано анализом FTIR. Результаты FTIR для альгинатных и альгинатных мембран SGO показаны на рис. 6. По-видимому, происходит небольшой сдвиг в спектрах сайтов водородных связей в соответствии с взаимодействиями водородных связей. Полосы группы O-H в альгинатной мембране появились при 1413 и 3440 см -1 .; однако полосы были сдвинуты на 1406 и 3404 см -1 в мембране SA / SGO за счет водородной связи между полярными группами в SGO и группами O – H в альгинате [45]. Полосы группы C =O в альгинатной мембране также сдвинулись до 1046 с 1082 см -1 . . Расположение сульфоновой группы (–SO 3 H) полосы в альгинатной мембране также изменились с 1284 до 1277 см −1 . Таким образом, результаты показывают, что существует водородная связь между SGO и альгинатом [47]. Полная дисперсия частиц SGO в полимерной матрице может облегчить путь протонной проводимости во всех направлениях мембраны. В результате было сделано предположение, что свойства мембран из SA / SGO превосходят свойства чистых альгинатных мембран в соответствии с внутренней структурой SEM и спектрами FTIR.
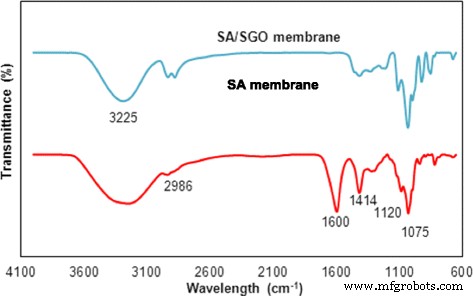
ИК-Фурье спектры мембран SA и SA / SGO
Термическая стабильность и механические свойства
На рисунке 7 показано сравнение анализа ТГА для всех биомембран SA / SGO с различным содержанием SGO. Потери на первом этапе происходили ниже 200 ° C из-за высвобождения молекул воды, что известно как процесс испарения. Обычно термическое разложение GO происходит при температуре около 200 ° C из-за разложения кислородно-лабильной группы, в то время как для альгинатных полимеров тепловое разложение на первой стадии происходит при 178 ° C [48, 49]. Биомембрана SA / SGO показывает большие потери при более высокой температуре 198 ° C. Эта повышенная температура указывает на то, что существует взаимодействие между альгинатом натрия и SGO, которое увеличивает термостойкость биомембраны SA / SGO. Это показывает, что присутствие SGO увеличило термическую стабильность биомембраны из-за благоприятных межфазных взаимодействий, таких как водородные связи или электростатические взаимодействия между матрицей альгината натрия и нанолистами сульфированного оксида графена, что делает эту мембрану пригодной для применения DMFC. Вторая стадия потери веса происходит при температуре 250 ° C из-за разложения боковой цепи альгината натрия. Третья стадия (> 400 ° C) включает процесс разложения основной цепи полимера [50].
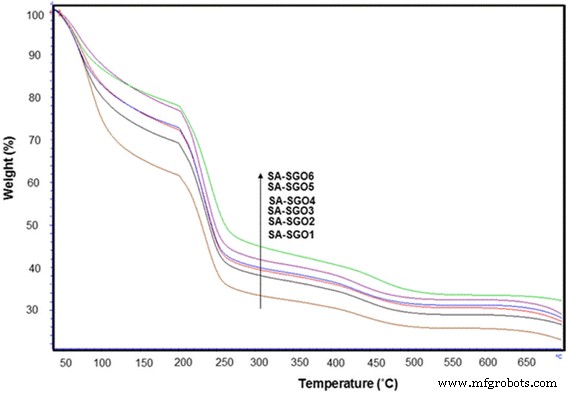
Кривая ТГА для биомембран SA / SGO с различным вес.% SGO
На рис. 8 представлены значения растягивающего напряжения и удлинения при разрыве мембраны при изменении массового процента SGO. От 0,02 до 0,13 мас.% SGO растягивающее напряжение увеличивалось, а затем незначительно снижалось при 0,17 мас.%. Это может быть связано с переупаковкой листов оксида графена, что может быть связано с силами Ван-дер-Ваальса в нанолистах GO. Большая часть нанолистов из оксида графена приводит к скольжению и снижает влияние оксида графена на улучшение механических свойств мембраны. Напряжения при растяжении Нафиона и других биомембран в предыдущих исследованиях перечислены в Таблице 1 [51,52,53,54,55]. Мембрана Nafion имеет более высокое растягивающее напряжение по сравнению с биомембраной SA / SGO6. Однако он сопоставим между категориями биомембран. Сам оксид графена имеет очень хорошие механические свойства, с модулем упругости 1100 ГПа и внутренней прочностью 125 ГПа; это основная причина, по которой SGO может увеличивать механические свойства альгинатной мембраны [45].
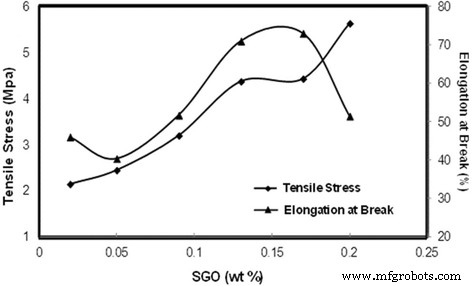
Напряжение при растяжении и удлинение при разрыве биомембраны с различными мас.% SGO
Более того, образование водородных связей между SGO и чистым альгинатным матричным полимером также может привести к хорошим механическим свойствам. Более сильное образование водородных связей приводит к более сильной межфазной адгезии, следовательно, к повышению механической прочности мембраны. Модель удлинения при разрыве отличается от модели растягивающего напряжения. Более низкое растягивающее напряжение приводит к более высокому относительному удлинению при разрыве. Удлинение при разрыве указывает, до какой степени мембранная пленка может быть растянута до максимальной точки, которая также известна как гибкость. В таблице 1 сравниваются несколько мембран из предыдущих исследований с мембраной из текущего исследования с точки зрения удлинения при разрыве [51,52,53,54,55,56]. Логичны различные закономерности между растягивающим напряжением и удлинением при разрыве. Как упоминалось выше, присутствие SGO в мембране увеличивает межфазную связь из-за водородной связи, тем самым снижая гибкость мембраны.
Поглощение жидкости и коэффициент набухания мембраны
Признано, что вода является важным компонентом протонообменной мембраны, поскольку она действует как проводник протонов, в котором адсорбированная вода способствует переносу протонов [39]. На рисунке 9 представлены результаты поглощения воды и метанола мембраной SA / SGO с различными значениями весовых процентов SGO. Как показано, мембрана SA / SGO имеет более низкую водопоглощающую способность при различном содержании сульфированного GO (самое низкое WU - 57,9% по SA / SGO6) в мембране по сравнению с чистым альгинатом. Увеличение количества SGO снижает поглощение воды из-за его блокирующей способности в качестве наполнителя в мембране [5]. Добавление SGO способствует сокращению ионных путей, препятствуя движению воды и метанола. Более высокое содержание SGO обеспечивает более прочный барьер для водопоглощения мембраны. Водородная связь между наполнителем SGO и полимером альгината натрия усиливает межфазную адгезию мембранного композита, тем самым снижая водопоглощающую способность [19]. В образовании водородных связей в мембране SA / SGO участвуют группы –OH в GO, группы –O- и C =O на цепях SA и вклад сульфонатных групп (–SO 3 З) [3, 19]. Подобно картине результата поглощения воды, поглощение метанола мембраной SA / SGO также снижалось с увеличением% мас. SGO в мембране. Наличие той же тенденции показывает, что между SGO и альгинатным полимером была хорошая сеть и связь, что препятствовало пересечению топлива. По результатам экспериментов, присутствие материалов на основе оксида графена снижает водопоглощающую способность мембраны SA и сохраняет ее механическую прочность. Степень набухания снижалась с 106% до 61,12% с увеличением мас.% SGO в альгинатной полимерной матрице (рис. 9) из-за блокирующего эффекта [10]. The strong hydrogen bonding also diminished the pathways for absorbance of the ionic group into the polymer [32].
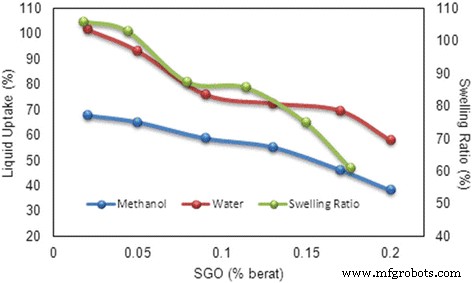
Liquid uptake and swelling ratio of SA/SGO membrane with wt.% of SGO
IEC, Proton Conductivity, Methanol Permeability, and Selectivity
Ion exchange capacity (IEC) calculation is important since it is responsible for measuring the number of milliequivalents ions in 1 g of the prepared membranes and is an indicator for proton conductivity in DMFCs.
Table 2 shows the IEC values of the membranes. A higher IEC value is achieved by the SA/SGO membrane containing a higher wt% of SGO. This is due to the function of sulfonic acid groups in the SGO nanosheets. An increment in the IEC value increases the proton conductivity value of the SA/SGO biomembrane. The proton conductivities of the SA/SGO membrane versus temperature are presented in Fig. 10. Increasing the temperature leads to the enhancement of proton conductivity. The SA/SGO membrane features a consistently increasing pattern in proton conductivity as the SGO particle amount increases, with a maximal value of 13.2 mS cm −1 at 0.2 wt% of SGO loading at temperature of 30 °C. The ln σ vs. 1000/T plot is also shown in Fig. 11. Assuming that the conductivity follows an Arrhenius behavior, the ion transport activation energy E а of the SA/SGO membranes can be obtained according to the Arrhenius equation:
$$ {E}_a=-b\ x\ R $$where b is the slope of the line regression of ln σ (S/cm) vs. 1000/T (K −1 ) plots, and R is the gas constant (8.314472 JK −1 mol −1 ). The ion transport activation energy of the SA/SGO6 composite membrane is 8.17 kJ mol −1 , which is slightly greater than the E а of Nafion® 115 (6.00 kJ mol −1 ) [57] and lower than that of Nafion 117 (12 kJ mol −1 ) [58]. This can be attributed to the hydrophilic properties of the sodium alginate matrix, which provide high water content, and the introduction of SGO still allows this property to remain due to the hydrophilic properties of oxygenated functional groups. The abundant water forms a continuous transferring channel and makes the movement of ion easy.
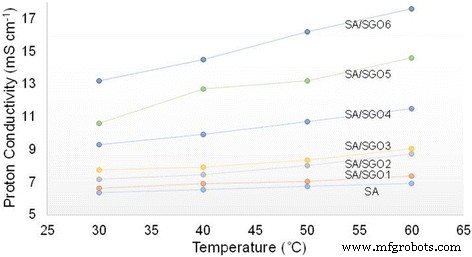
Proton conductivity of SA/SGO biomembranes with various content of SGO at different temperature
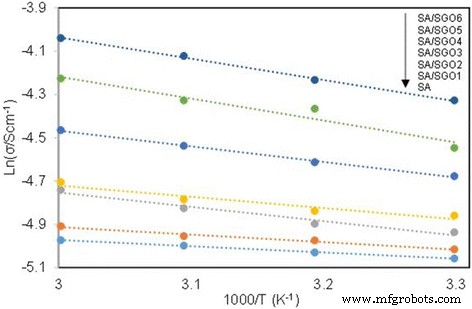
ln σ vs. 1000/T plot for the cross-linked QAPVA membranes, the lines indicate the linear regression
Figure 13a presents the suggested proton mobility mechanism in SA/SGO plasticized with glycerol in which high synchronization exists between H + and electron lone pairs belonging to the oxygen atoms carrier in glycerol and the hydrophilic sulfonic acid groups in SGO nanosheets. We believe that the proton transport applies both Grotthus and vehicle mechanisms, strengthened by the SGO particles.
The SA/SGO biomembranes show very low methanol permeability, and the lowest was achieved by SA/SGO6 (1.535 × 10 −7 см 2 s −1 ), as listed in Table 2. The low methanol permeability can be explained in terms of the membrane microstructure between sodium alginate, SGO, and glycerol plasticizer. The introduced SGO particles serving as fillers in the SA polymer create substantial obstacles to the linked hydrophilic passages. The SGO filler blocks the migration of methanol passing through the membrane, and this is known as the blocking effect, which reduces the methanol permeability. The methanol permeability also decreases because of the interfacial interaction between the SGO and SA biopolymer [41]. The methanol permeability of the SA/SGO6 bio membrane at four different temperature conditions is shown in Fig. 12. As seen, the methanol permeability increases at a higher temperature, which can be related to the structure changes of the bio membrane. The higher temperature provides more heat, which can shake the membrane chains and molecules, thus leading to more free volume, which consequently reduces the methanol blocking effect. Less resistance causes easier movement of methanol diffusion [59]. Mu et al. [60] reported the decrease in methanol crossover in the presence of Au nanoparticles self-assembled on a Nafion membrane, which consequently improved the overall performance.
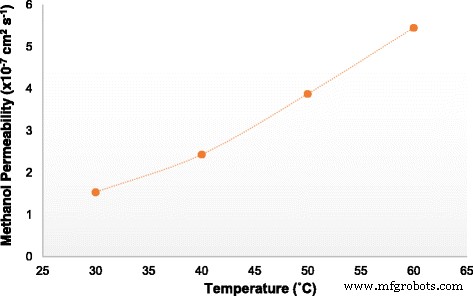
Methanol permeability of membrane SA/SGO6 vs. temperature
The interfacial interaction between SGO filler, glycerol, and SA polymer confines the hydrophilic passage formation in the membrane, and this wide hydrophilic passage is a significant factor in methanol migration [19]. Thus, the presence of SGO facilitates methanol permeability reduction [6]. The proposed mechanism of methanol rejection is presented in Fig. 13b.
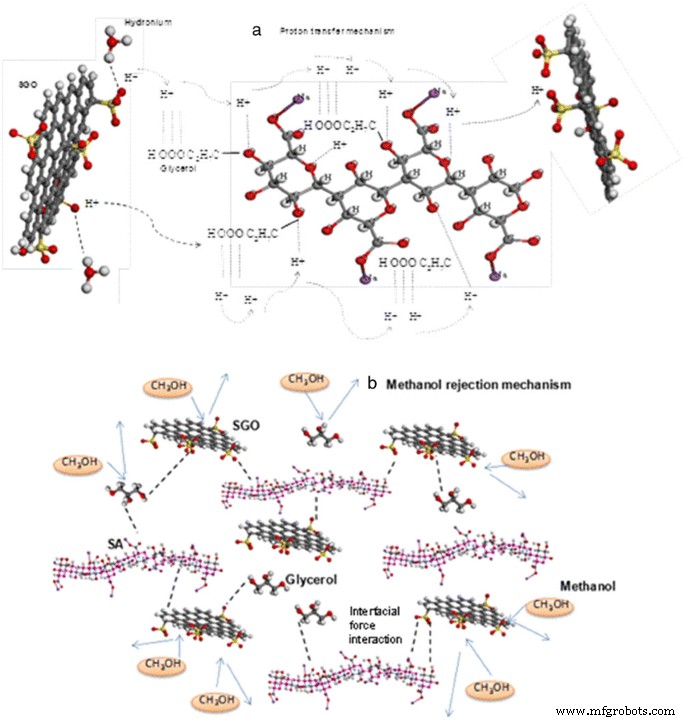
Suggested mechanism of a proton mobility and b methanol rejection
It was noticed that a higher selectivity value resulted in a higher DMFC capability. The selectivity values of the SA/SGO can be observed in Table 2, which compares the selectivity among SA and SA/SGO biomembranes as well as Nafion 117 membranes from previous work. The presence of SGO enhanced the selectivity of the SA/SGO polymer membrane (8.555 × 10 4 S s cm −3 for 0.2 wt% SGO loading), which is higher than that of SA (3.7678 × 10 4 S s cm −3 ) and fortunately also higher than that of Nafion 117 (7.99 × 10 4 S s cm −3 ) [38], 4.05 × 10 4 S s cm −3 [61], and 4.22 × 10 4 S s cm −3 [62], in which the low methanol permeability is the main factor to be considered.
Single Cell
Single-Cell Performance Evaluation
Figure 14 indicates the cell polarization result for pure alginate, SA/SGO6 composite biomembrane and Nafion 117 under ambient temperature, 4 M methanol concentration and passive mode condition. The SA/SGO6 composite biomembrane was applied due to the high selectivity factor and obviously had a higher open-circuit voltage (0.63 V), which can be related to the low methanol permeability equaling to that the sodium alginate biomembrane. The OCV of Nafion 117 (0.52 V) in the current study is lower than SA/SGO and sodium alginate, which might be due its higher methanol permeability. The crossing of methanol through the membrane leads to the reduction in the OCV value. The higher OCV of SA/SGO and alginate membrane is the big indicator that synthesized membrane has lower methanol permeability compared to Nafion, which the main objective of this study is successfully achieved. The improvement in the power density of SA/SGO6 is due to the sulfonic acid group that functions as a proton transferral pathway as well as a methanol inhibitor, thus achieving 5.9 mW cm −2 compared to the sodium alginate, which achieved only 2.83 mW cm −2 . However, Nafion 117 achieved a higher power density, which was 6.62 mW cm −2 . Thiam et al. [38] reported the performance of Nafion 117 membrane under the same condition with a power density of 7.95 mW cm −2 . No doubt, Nafion achieves a better performance in DMFC application due to the excellent proton conduction. However, the power density performance between Nafion 117 and SA/SGO biomembranes does not show a big difference quantitatively. Hence, SA/SGO can be an alternative membrane for DMFC in the future. However, the properties of the membrane still need to be enhanced, and higher wt% of SGO filler can probably be used to obtain a higher power density. To the best of our knowledge, there is only one previous work by Pasini Cabello et al. that has examined the single-cell performance in DMFC application using an alginate biopolymer-based membrane [18]. They tested an alginate/carrageenan membrane at temperatures of 50, 70, and 90 °C in 2 M methanol concentration in the active mode, which achieved maximum power densities of 10.4, 13.9, and 17.3 mW/m 2 , соответственно. The active mode has an advantage due to the continuous flow of the methanol feed into the cell that allows the reaction to occur continuously and thus is capable of achieving a higher power density. The higher power density could be achieved at a higher temperature due to the higher number of activated protons. Nevertheless, this work is an indicator that biopolymer-based membrane has a big potential that can be explored and applied in DMFC systems.
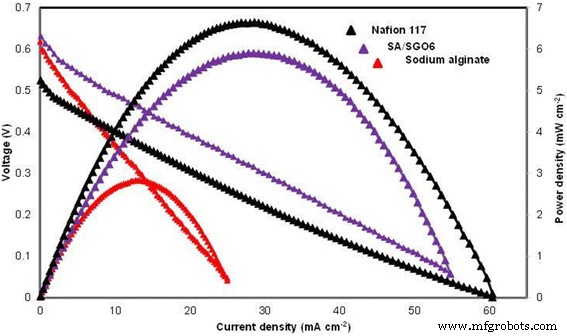
Single-cell performance test for sodium alginate, SA/SGO6, and Nafion 117 (4 M methanol and 25 °C temperature, passive mode)
Conclusions
In conclusion, a membrane with low methanol permeability, high proton conductivity, and high selectivity was successfully prepared through the simple technique known as the blending method. The presence of sulfonated graphene oxide enhanced the properties of the alginate-based polymer membrane in terms of proton conductivity and methanol permeability. The sulfonate groups facilitated the networking between the alginate polymer and the graphene oxide filler. The blocking effect of SGO also reduced the methanol crossover in the membrane. The primary weaknesses of the alginate polymer, which are its mechanical properties of tensile strength and elongation at break, were also improved by the addition of SGO into the polymer matrix. The presence of SGO improved the SA/SGO membrane to a high level comparable to commercial membranes.
Сокращения
- BC:
-
Bacterial cellulose
- CNC:
-
Cellulose nanocrystal
- CNFs:
-
Cellulose nanofibers
- CNT:
-
Углеродные нанотрубки
- DI:
-
Деионизированный
- DLFC:
-
Direct liquid fuel cell
- DMFC:
-
Direct methanol fuel cell
- EDX:
-
Energy dispersive X-ray
- FESEM:
-
Field emission scanning electron microscope
- FTIR:
-
Fourier transform infrared
- GO:
-
Оксид графена
- GOS:
-
Graphene oxide sheet
- HRTEM:
-
Просвечивающая электронная микроскопия высокого разрешения
- IEC:
-
Ion exchange capacity
- L :
-
Distance between the two electrodes
- OCV:
-
Open circuit voltage
- P:
-
Membrane diffusion permeability for methanol
- PEMFC:
-
Polymer electrolyte membrane fuel cell
- PEMs:
-
Proton exchange membrane
- PMA:
-
Phospho molybdic acid
- PSSA:
-
Poly-styrene sulfonic acid
- PVA:
-
Poly vinyl alcohol
- PVP:
-
Poly (vinyl pyrrolidone)
- R :
-
Resistance of the membrane
- RGO:
-
Reduced graphene oxide
- SA:
-
Sodium alginate
- SA/SGO:
-
Sodium alginate/sulfonated graphene oxide membrane
- SGO:
-
Sulfonated graphene oxide
- SHNT:
-
Sulfonated halloysite nanotube
- SPSF:
-
Sulfonated polysulfone
- SW%:
-
Swelling ratio percentage
- T :
-
Membrane thickness
- TGA:
-
Thermal gravimetric analysis
- W :
-
Width of the membrane
- WU%:
-
Water uptake percentage
- XPS:
-
Рентгеновская фотоэлектронная спектроскопия
Наноматериалы
- Графен в динамиках и наушниках
- Нановолокна и нити для улучшенной доставки лекарств
- Нанокомпозиты из оксида графена, украшенные титанатом:получение, огнестойкость и фотодеградация
- Биобезопасность и антибактериальная способность графена и оксида графена in vitro и in vivo
- Изготовление и определение характеристик нового композитного катализатора из углеродного нановолокна Tio2 дл…
- Легкий синтез червоточиноподобного мезопористого оксида олова за счет самосборки, вызванной испарением, и у…
- Разработка и регулировка работы выхода графена с помощью размера, модификации, дефектов и легирования:исслед…
- Оценка структур графен / WO3 и графен / CeO x как электродов для применения в суперконденсаторах
- Получение наноразмерного CL-20 / оксида графена в один этап с помощью шаровой мельницы для значительного уменьш…
- Получение нанокомпозита сверхвысокой молекулярной массы полиэтилен / графен Полимеризация на месте с помощь…



