Сравнительное исследование биосинтезированных наночастиц оксида меди и цинка in vivo путем внутрибрюшинного и внутривенного введения у крыс
Аннотация
В настоящее время антимикробные свойства наночастиц (НЧ) меди (Cu) и оксида цинка (ZnO) широко используются для борьбы с ростом патогенных микробов. CuNP и ZnONP постоянно используются в косметике, медицине и пищевых добавках, и их потенциал токсического воздействия на человека и экосистему вызывает серьезную озабоченность. В этом исследовании судьба и токсичность биосинтезированной меди (Bio-CuNP) и оксида цинка (Bio-ZnONP) в диапазоне от 16 до 96 нм оценивалась на самцах крыс Wistar. Воздействие двух наночастиц in vivo достигается двумя разными путями введения, а именно внутрибрюшинными (в / б) и внутривенными (в / в) инъекциями. Три различных концентрации:концентрация без наблюдаемого побочного эффекта (NOAEC), ингибирующая концентрация (IC 50 ) и общую летальную концентрацию (ТСХ) оценивали в диапазоне доз от 6,1 до 19,82 мкг / кг и от 11,14 до 30,3 мкг / кг для Bio-CuNP и Bio-ZnONP, соответственно, как для в / в, так и для в / в путей введения. 14-й и 28-й день наблюдения. Эти диапазоны доз считаются основанными на предыдущем исследовании доз антибактериальных препаратов на патогенных бактериях с множественной лекарственной устойчивостью. В этом исследовании мы исследовали токсическое действие Bio-CuNP и Bio-ZnONP на поведение животных, массу животных, гематологические индексы, индексы органов и гистопатологию печени, селезенки, почек и органов мозга. Мы обнаружили, что в / в и в / б введение Био-ЗнОНП в трех разных дозах не вызывало смертности, а масса тела немного снижалась до второй недели приема по сравнению с контрольной группой носителя. В диапазонах доз 11–16 мкг / кг (в / в) и 24–30 мкг / кг (в / б) не наблюдалось значительных изменений уровня креатинина в сыворотке, а также уровней АЛТ в сыворотке крови, уровня АСТ в сыворотке и ЩФ. уровень, который составлял 40,7 мг / дл, 37,9 МЕ / л и 82,4 МЕ / л в норме по сравнению с контролем с носителем на 14-й и 28-й дни наблюдения. Эти данные подтверждаются исследованиями показателей печени, почек и селезенки, а также гистопатологическими исследованиями. Кроме того, повреждение печени и почек происходило, когда концентрация Bio-CuNP составляла 9,5 мкг / кг (IC 50 ) и 11,7 мкг / кг (ТСХ) для в / в введения. Аналогичным образом наблюдалось повышение сывороточного уровня АЛТ (67,7 мг / дл), уровня AST (70 МЕ / л) и ЩФ (128 МЕ / л). И масса тела была значительно ниже, чем в контрольной группе после 14-го дня, и наблюдались статистически значимые различия при использовании этого пути; Интересно, что токсичность Bio-CuNPs в сыворотке пролонгирована (до 28-го дня). Эффект Bio-CuNP через в / б путь был значительно ниже по сравнению с контролем. Результаты настоящего исследования показали, что Био-ЗнОНП не влияют на биомаркеры функции почек и печени (как в / в, так и в / б) по сравнению с Био-CuNP.
Как показано в графическом аннотации (рис. 1), наша цель - оценить токсичность Bio-CuNP и Bio-ZnONP с помощью протокола in vivo. Согласно обзорам Kahru и Dubourguier, AgNP, CuNP и ZnONP исторически использовались в качестве биоцидов для предотвращения роста микроорганизмов и водорослей (Kahru and Dubourguier 2010). Поэтому, как и пестициды, наноматериалы следует контролировать на предмет их токсической реакции на нецелевые виды, включая людей и животных. Чтобы лучше понять, может ли случайный выброс металлсодержащих НЧ представлять угрозу для нецелевых видов, необходима оценка токсического эффекта. «Нецелевой организм» - это организм, который будет подвергаться воздействию НЧ после их случайного попадания. выпустить в окружающую среду.
Фон
Некоторые металлы необходимы для нормальных физиологических функций живых организмов. С последнего десятилетия наблюдается рост использования наночастиц на основе металлов в биомедицинских приложениях, экспоненциальное использование наночастиц предупреждает о проблемах безопасности для уменьшения и / или предотвращения побочных эффектов, вызываемых наночастицами, на живую систему [1]. Среди НЧ Cu и ZnO обычно содержатся в пищевых добавках и в организме человека [2, 3]. Уникальные физико-химические свойства Cu и ZnONP находят функциональное применение в физиологических метаболических процессах, что увеличивает их коммерческую ценность в промышленности [4,5,6]. Однако при избыточном потреблении Cu и ZnONP наблюдались побочные эффекты, включая гемолиз, желудочно-кишечные расстройства, повреждение печени и почек [7].
В частности, всасывание CuNP легко происходит после приема внутрь, ингаляции и воздействия на кожу [8, 9], в значительной степени через желудочно-кишечный тракт [8, 10]. CuNP нацелены на клетки слизистой оболочки и удерживаются внутри, связываясь с металлотионеином или глутатионом [11]. Он хранится в основном в печени, мозге, сердце, почках и мышцах. Сообщалось, что 98% Cu связывается с церулоплазмином, сывороточным белком, который приводит к клеточной токсичности. [12, 13]. Cu является каталитическим индуктором супероксидных радикалов, гидроксильных радикалов и перекиси водорода посредством реакции Габера-Вейсса [14], более высокие концентрации Cu могут вызывать окислительный стресс.
По степени растворимости ZnONP рассматривались как отдельная группа НЧ в составе НЧ оксидов металлов [15]. Элемент цинк содержится в организме человека, а ZnONP, как известно, менее токсичны [3]. Однако сообщается, что избыток цинка вызывает токсические эффекты [16]. Высвобождение металлических катионов Zn 2 из ZnONP также оказались токсичными для микроорганизмов и грызунов [17]. НЧ ZnO могут проникать разными путями, достигая кровотока и оказывая неблагоприятное воздействие на органы [18]. Предварительные результаты показали, что пораженные ZnONP системы органов могут проявлять воспаление, изменение частоты сердечных сокращений и функций, а также окислительный стресс [19, 20]. Согласно [21], вдыхание 20 нм ZnONP (2,5 мг / кг массы тела) крысами дважды в день приводило к увеличению содержания цинка в печени через 12 часов и в почках через 36 часов.
Повышение осведомленности о нанотоксичности, сообщалось об исследованиях in vivo токсичности CuNP и ZnONP для интраназальной инстилляции [22, 23], интратрахеальной инстилляции [24, 25] и перорального введения [26, 27, 28], воздействия на кожу [29, 30]. Чтобы оценить токсичность, необходимо провести внутривенное (в / в) и внутрибрюшинное (в / б) введение. Насколько нам известно, имеются минимальные отчеты о токсичности CuNP и ZnONP при внутривенном и внутрибрюшинном введении. Более того, токсикологический механизм и тканевое распределение двух НЧ еще не были систематически изучены после в / в и в / б инъекций.
Таким образом, мы продемонстрировали токсичность биосинтезированных CuNP и ZnONP в диапазоне 16–96 нм у самцов крыс линии Wistar посредством внутрибрюшинных (в / б) и внутривенных (в / в) инъекций по желанию на 14 и 28 день наблюдения.
Метод
Биосинтез био-CuNP и био-ZnONP
Биологический синтез CuNP и ZnONP из непатогенных Enterococcus faecalis адаптирован внеклеточным ферментативным методом [31, 32]. Кроме того, форма и размер синтезированных наночастиц были подтверждены с помощью автоэмиссионной сканирующей электронной микроскопии (FeSEM) и просвечивающей электронной микроскопии (TEM).
Исследования in vivo
Экспериментальные животные и животноводство
Особо здоровых самцов крыс линии Wistar в возрасте от 12 до 13 недель были приобретены у Mahaveera Enterprises, Хайдарабад, Индия. Животных отбирали в диапазоне веса 160–200 г для каждой группы и акклиматизировали в течение 1 недели до начала лечения, а состояние здоровья крыс контролировали ежедневно. Животных содержали в стандартных условиях температуры (24 ± 1 ° C) и относительной влажности (55 ± 10%) соответственно с 12-часовыми циклами свет / темнота. Во время лечения животных содержали в клетках с крышками из нержавеющей стали. Животных кормили коммерчески доступным стандартным гранулированным рационом (VRK Nutrition Solutions, Sangli, Maharashtra, India Ltd.). Питьевая вода давалась животным ad libitum.
Исследования токсичности проводились в фармацевтическом колледже Лукмана, Калабураги, Индия. Работа с животными проводилась в соответствии с надлежащей лабораторной практикой. Протокол исследования был одобрен этическим комитетом Института животных (номер одобрения:346 / CPCSEA).
Приготовление и введение Bio-Cu и ZnONP
Исходные суспензии Bio-CuNP и Bio-ZnONP (50 мг / мл) готовили путем раздельного растворения в бидистиллированной воде в течение ночи и фильтровали с использованием шприцевых фильтров 0,22 мкм. Фильтраты используются для приготовления рабочего стандарта в диапазоне концентраций 1,25–175 мкг / мл.
Животные были разделены на три группы по три различных концентрации для каждого типа наночастиц. Принимая во внимание шесть крыс / группу для внутривенного введения (обозначено как набор эксперимента A) и шесть крыс / группу для внутрибрюшинного пути (обозначено как набор эксперимента B), согласно таблицам 1 и 2. В обоих наборах экспериментов группа A служил контролем (носитель дистиллированная вода).
Пункты наблюдения и проверки
Клинические признаки
Во время теста наблюдение после лечения проводилось один раз в день для отслеживания признаков клинической токсичности и / или смерти.
Расход корма и воды
Потребление корма и воды регистрировалось ежедневно после даты начала обработки, рассчитывалось по разнице между поданными и оставшимися количествами.
Поведение и вес животного
Каждые два дня после инъекции крыс взвешивали и оценивали изменения в поведении.
Гематологические индексы
Кровь была взята для гематологического анализа с использованием стандартной техники взятия крови из подкожной вены (с использованием пробирок для сбора калий-метилендиаминтетрауксусной кислоты). Согласно стандартному гематологическому анализу у крысы было собрано 300 мкл крови, и на 14 и 28 дней были проанализированы стандартные гематологические параметры, то есть количество тромбоцитов, гематокрит, гемоглобин, количество эритроцитов и количество лейкоцитов [33].
Биохимический панельный анализ сыворотки
Для определения биохимических уровней сыворотки, включая аланинаминотрансферазу (ALT / GPT), креатинин (CRE), аспартатаминотрансферазу (AST) и щелочную фосфатазу (ALP), контрольных и обработанных крыс умерщвляли и собирали образцы цельной крови для центрифугирования (3000 об / мин. ) в течение 15 минут. Оценка проводилась автоматическим биохимическим анализатором для образцов 14 и 28-го дня [34].
Определение веса органелл
Через 14 и 28 дней крыс анестезировали эфиром с забуференным фосфатом физиологическим раствором и вскрывали. Органы контрольной и обработанной групп забирали немедленно. Сердце, легкие, тимус, мозг, почки, печень и селезенка были осторожно отделены и промыты раствором хлорида натрия, промыты ледяной деионизированной водой и высушены фильтровальной бумагой. Исследовали морфологию и цвет рассеченных органов и измеряли вес каждого органа. Чтобы изучить степень изменений, явно вызванных Bio-Cu и ZnONP, индекс органов (O X ) рассчитывалась отдельно по формуле [35]:
$$ \ mathrm {Organ} \ \ mathrm {index} \ \ left ({\ mathrm {O}} _ {\ mathrm {X}} \ right) =\ frac {\ mathrm {Weight} \ \ mathrm {of} \ \ mathrm {экспериментальный} \ \ mathrm {орган} / \ mathrm {вес} \ \ mathrm {of} \ \ mathrm {экспериментальный} \ \ mathrm {животное}} {\ mathrm {Weight} \ \ mathrm {of} \ \ mathrm {control} \ \ mathrm {organ} / \ mathrm {weight} \ \ mathrm {of} \ \ mathrm {control} \ \ mathrm {animal}} $$Где указатель органов (O X ) может измениться как:
Индекс сердца (H X ), Индекс печени (Li X ), Индекс селезенки (S X ), Индекс легких (Lu X ), Почечный индекс (K X ), Индекс вилочковой железы (T X ), Индекс мозга (B X ).
Гистология
Одну крысу из каждой группы, включая контроль, фиксировали 10% забуференным формалином после обескровливания забуференным фосфатом физиологическим раствором. Небольшой кусочек печени, почки, селезенки и мозга фиксировали 10% формалином и заливали парафином. Парафиновые блоки были разрезаны и обработаны для окрашивания гематоксилином и эозином. Окрашенные срезы наблюдали с помощью светлопольной микроскопии [36].
Статистический анализ
Все данные выражены в виде среднего значения ± стандартное отклонение среднего значения трех независимых экспериментов; каждый был проведен в трех экземплярах, N =6 крыс в группе.
Результаты и обсуждение
Синтез био-CuNP и био-ZnONP проводили внеклеточным ферментативным методом при воздействии на реагенты Enterococcus faecalis супернатант. Анализ FeSEM Bio-CuNPs и Bio-ZnONPs можно увидеть с размером в диапазоне от 1 до 100 нм в распределении (дополнительный файл 1). Анализ ПЭМ сообщает о присутствии биосинтезированных CuNP и ZnONP с морфологией сердцевины оболочки размером 12–90 нм и сферической формой для CuNP [31] и ZnONP в диапазоне от 16 до 96 нм [32] (дополнительный файл 2).
Оценка Bio-Cu и ZnONP на самцах крыс линии Вистар была исследована без признаков смертности при лечении NP. Кроме того, после лечения и до конца эксперимента наблюдали за частым исследованием белых фекалий после в / в введения Bio-CuNP в дозировке от 9,5 до 11,5 мкг / кг. Между третьей и четвертой неделями у крыс, получавших Bio-CuNPs, наблюдалось значительное увеличение потребления корма, а потребление воды в / в составило 9,5 мкг / кг (IC 50 ) и 11,5 мкг / кг (ТСХ), тогда как для внутривенного введения (диапазон доз:от 24,8 до 30,3 мкг / кг) и крыс контрольной группы с 3-й по 4-ю неделю. Изменение массы тела крыс после в / в и в / в Введение Bio-CuNPs и Bio-ZnONPs показано в таблицах 3 и 4. Снижение и увеличение массы тела являются ценными показателями при оценке токсичности исследуемого образца [37]. Предыдущие сообщения, подтвержденные в исследованиях токсичности, на 13,5 нм золота [33] и серебра 100 нм [38], влияние НЧ на массу тела при в / в инъекции было меньше, чем при в / в и пероральном введении. По словам Риуани и др. , небольшое снижение веса после 4 дней лечения во всех обработанных группах может указывать на неблагоприятное воздействие токсичных веществ на животных [39].
Можно видеть, что в / в и в / в введение Био-ZnONP в трех разных дозах (NOAEC, IC 50 и TLC) масса тела была немного снижена до второй недели приема по сравнению с контрольной группой. Однако через 14 дней масса тела восстановилась. В случае в / б введения снижение массы тела было вызвано био-ZnONP (30,3 мкг / кг) при общей летальной концентрации и было ниже, чем в контрольной группе, что указывает на тривиальную токсичность через в / б путь по сравнению с внутривенным путем. (Таблица 4, рис. 1а). Аналогичным образом, у крыс, получавших Bio-CuNP в концентрации 9,5 мкг / кг и 11,7 мкг / кг с помощью в / в введения, было замечено небольшое снижение массы тела. До 14 дней лечения Bio-CuNP не наблюдалось никаких отрицательных эффектов на рост и прибавку массы тела. Изменение массы тела в течение 28 дней при дозе 11,7 мкг / кг (в / в способ) показано в таблице 3. После 14-го дня лечения было обнаружено значительное снижение массы тела при в / в введении по сравнению с контролем. группа. Таким образом, указывает на токсичность Bio-CuNPs через этот путь (рис. 1b). Крысы, обработанные Bio-CuNP посредством в / б введения, вызывали незначительное снижение массы тела, и никаких признаков смертности не наблюдали ни при в / б, так и в / в введениях. Таким образом, внутрибрюшинные инъекции вызывают меньшую токсичность (см. Таблицу 4 и Рис. 1а).
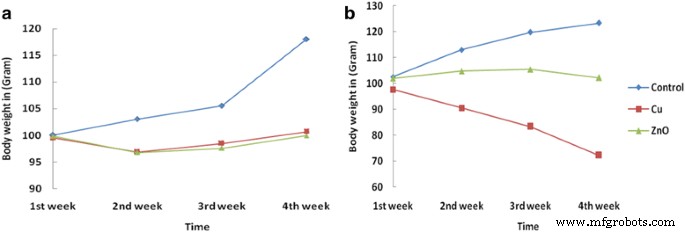
Изменение массы тела необработанных (контроль) и обработанных крысами Bio-CuNP и Bio-ZnONP. Био-CuNP и Bio-ZnONP, обработанные (А) внутрибрюшинным (в / б) и (В) внутривенным (в / в) путями введения до 28-го дня наблюдения. Все обработки Bio-CuNP (Cu) и Bio-ZnONP (ZnO) вводили при их общей летальной концентрации и наблюдали в течение 28 дней; N =6 крыс в группе
Гематологические индексы
Оценка гематологических параметров, таких как количество эритроцитов, количество лейкоцитов, количество тромбоцитов, уровень гемоглобина и время свертывания крови, являются важными объектами для измерения токсичности обработанных НП. На 14-й и 28-й день гематологические результаты в зависимости от концентрации представлены в таблицах 5 и 6 для в / б и в / в путей введения. Дозировка Bio-CuNP при 9,5 мкг / кг (IC 50 ) и 11,7 мкг / кг (TLC) при в / в введении показали снижение количества эритроцитов в отличие от Bio-ZnONP. Однако тенденции, зависящей от концентрации, замечено не было. У крыс, получавших Био-ЗнОНП с помощью в / в введения, уровень гемоглобина, количество тромбоцитов и лейкоцитов изменились, но не наблюдается значительных различий между всеми тремя концентрациями (NOAEC, IC 50 и ТСХ). Но в случае внутрибрюшинного пути введения на 14-й день наблюдения было обнаружено значительное снижение и изменение количества эритроцитов, лейкоцитов, уровня гемоглобина и количества тромбоцитов (таблица 5) по сравнению с контролем и биологическими препаратами. Леченые CuNP. Удивительно, но гематологические эффекты оказались нормальными на 28-й день (таблица 6).
Гематологические эффекты различных методов инъекций (в / в, в / б) для двух разных Био-НП на 14-й и 28-й день наблюдений различны. Можно наблюдать, что гемоглобин, красные кровяные тельца, лейкоциты и тромбоциты уменьшаются посредством в / в пути при лечении Bio-CuNP и через i / p путь у крыс, обработанных Bio-ZnONP. Но наблюдалось значительное снижение количества эритроцитов. Это указывает на то, что разные пути инъекции не вызвали значительных различий в количестве тромбоцитов, гемоглобине или лейкоцитах, за исключением крыс, которым вводили Bio-CuNP (в / в путь). Эритроциты показывают значительную разницу после в / б и в / в инъекций (как показано в таблицах 5 и 6).
Биохимический анализ сыворотки
Креатинин сыворотки - продукт жизнедеятельности; более высокая выработка креатинина указывает на повреждение почек. Био-ЗнОНП (в / в путь:доза 11-16 мкг / кг, в / в путь:доза 24-30 мкг / кг) существенно не влияли на уровень креатинина в сыворотке по сравнению с контролем на 14-й и 28-й день. (Таблицы 7 и 8, рис. 2а, б). Крысы, получавшие Bio-CuNP (в / в путь:доза 06-12 мкг / кг), показали повышение уровня креатинина в сыворотке до 2,3 мг / дл по сравнению с контролем. Однако внутрибрюшинный способ введения не показал значительных изменений (таблицы 7 и 8). Сыворотка крови содержит большое количество ферментов, но для оценки нормальных и патологических симптомов печени полезны аланинтрансаминазы (глутаматпируваттрансаминаза) и аспартаттрансаминазы (глутаматоксалат-ацетаттрансаминаза). Аспартаттрансаминаза митохондриального происхождения присутствует в больших количествах в печени, сердце, почках и скелетных мышцах. Щелочная фосфатаза сыворотки - это глобулиновый фермент с низким молекулярным весом, более высокая концентрация которого обнаруживается в костях, гепатобилиарном тракте и почках. Активность этого фермента может быть определена путем оценки органического фосфата, высвобождаемого из глицеринфосфата. Уровень ферментов в сыворотке повышен как при гепатоцеллюлярной, так и при механической желтухе. При в / в введении Био-ЗнОНП (40,7 мг / дл, 37,9 МЕ / л, 82,4 МЕ / л) не оказывают значительного воздействия на уровни АЛТ, АСТ и ЩФ в сыворотке по сравнению с контролем. Хотя внутрибрюшинное введение показало значительное повышение уровня АЛТ, АСТ и ЩФ по сравнению с контролем на 14 и 28 день (рис. 2а и б). Результаты исследования токсичности сыворотки показали, что Био-ЗнОНП не изменяют уровни креатинина, АЛТ, АСТ и ЩФ при в / в введении до 28 дней.
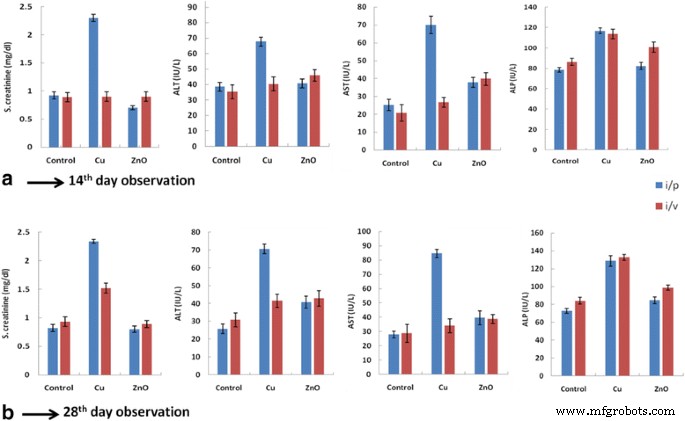
Биохимические результаты крыс, получавших Bio-CuNPs и Bio-ZnONPs. Уровни S. креатинина, АЛТ, АСТ и ЩФ измеряли у крыс, получавших Bio-CuNP и Bio-ZnONP внутрибрюшинным (в / б) и внутривенным (в / в) путями введения на (A) 14-й день и (B) 28 день. Все данные выражены в виде среднего значения ± стандартное отклонение среднего значения трех независимых экспериментов; каждый был проведен в трех экземплярах, N =6 крыс на группу. Примечание:Cu:Bio-CuNPs, ZnO:Bio-ZnONPs, в / б:внутрибрюшинно, в / в:внутривенно
Напротив, крысы, получавшие Bio-CuNP через в / в введения, показали значительное повышение сывороточного АЛТ (67,7 мг / дл), уровня АСТ (70 МЕ / л) и ЩФ (128 МЕ / л). Эффект Bio-CuNPs через i / p-путь был значительно ниже по сравнению с контролем. Различие результатов может быть связано с различием в способах дозирования, токсичностью наночастиц, а также продолжительностью введения. Мы обнаружили, что Bio-ZnONP не влияют на биомаркеры функции почек и печени (как в / в, так и в / в) по сравнению с Bio-CuNP.
Определение веса органелл и гистологическое исследование
Изменения веса органов крыс при различных дозах биопрепаратов иллюстрируют неблагоприятное воздействие этих наночастиц на органы. Можно видеть, что вес сердца, печени, селезенки, легких, почек и мозга снижается у крыс при лечении био-ZnONP, как показано в таблицах 9 и 10. Кроме того, рассмотрение реакции органа и степени изменений были исследованы путем расчета индекса органа (O X ) каждого органа в отдельности. Индексы органов для сердца, печени, селезенки, легких, почек, головного мозга и тимуса представлены в таблицах 9 и 10.
Разницу в массе селезенки и тимуса наблюдали после в / в и в / б введения у крыс, обработанных Bio-CuNP и Bio-ZnONP. На 14-й день Bio-ZnONPs показал снижение индекса селезенки при в / в введении и повышение при в / в введении (таблица 9). В случае крыс, обработанных Bio-CuNP посредством в / в введения, наблюдалось значительное снижение индекса селезенки на 14-й (0,265) и 28-й день (0,49). Это указывает на то, что иммунная система была затронута в / в введением Bio-CuNP и в / в введением Bio-ZnONP. В случае в / п введения Био-ЗнОНП иммунная система крысы возвращается к нормальному состоянию через 14 дней и доказывает, что эффект не продлевается. В совокупности с предыдущими вариациями массы тела кажется, что в / в путь введения Bio-CuNP может влиять на сердце, печень, легкие, почки и мозг; кроме того, это может повредить иммунную систему. Из рис. 3а следует, что селезенка и тимус являются основными мишенями для органов Bio-CuNP.
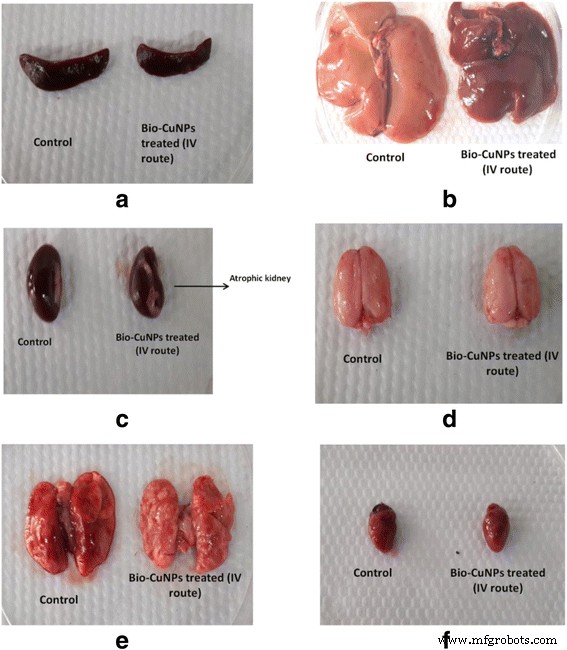
Изменение морфологии органелл. Где а селезенка, b печень, c почка, d мозг, е легкие и е сердце крыс-самцов Wistar, получавших Bio-CuNP внутривенно, по сравнению с контролем на 28-й день наблюдения
В случае групп, получавших i / v и i / p Bio-CuNPs, очевидные эффекты на индекс органа наблюдались при обоих IC 50 и дозы ТСХ. Более того, из двух разных способов введения внутрибрюшинная инъекция показывает умеренную токсичность в группах, обработанных Bio-ZnONP, и самую высокую токсичность в группах, обработанных Bio-CuNP. Было известно, что эффективное всасывание лекарств при в / б инъекции происходит быстро из-за плотных кровеносных сосудов и лимфы в брюшине мыши [40]. Соответственно, внутривенная инъекция показывает наименьшую токсичность в группах, обработанных Bio-ZnONP, и самую высокую токсичность в группах, обработанных Bio-CuNP.
Токсикологические изменения у крыс
Мы попытались тщательно изучить эффекты токсичности при различных дозах и временных интервалах Bio-NP. Ткани, обработанные Био-ЗнОНП (в / в путь:диапазон доз 11-16 мкг / кг, путь в / в:диапазон доз 24-30 мкг / кг), не показали изменений в печени, почках, селезенке и головном мозге по сравнению с контрольные ткани (рис. 4, 5, 6 и 7). Наблюдения при вскрытии трупа (вскрытие:вскрытие мертвой крысы) показали, что все органы крыс, обработанных Bio-NP, обладали анатомическими особенностями (например, характеристиками цвета, формы и размера), которые можно было ожидать, исходя из их внешнего вида у необработанных животных. По сравнению с Bio-ZnONP, крысы, обработанные Bio-CuNP, показали более значительные изменения анатомических характеристик тканей почек, печени, селезенки и мозга по сравнению с контролем (рис. 4, 5, 6 и 7).
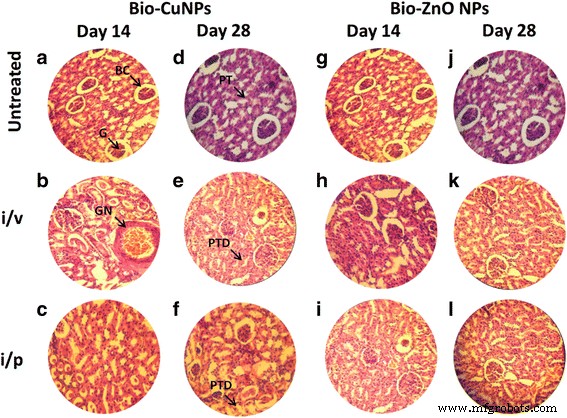
H &E-окрашенные срезы почки крысы. Крысам вводили в / в и в / б пути введения Bio-Cu и ZnONP; необработанные образцы считались контролем. Срезы, обработанные Bio-CuNP, наблюдались на 14-й день (A – C) и 28-й день (D – F). Срезы, обработанные био-ZnONP, на 14 день (G – I) и 28 день (J – L). Капсула Боумена BC, клубочки G, проксимальные канальцы PT, некроз клубочков GN, повреждение проксимальных канальцев PTD
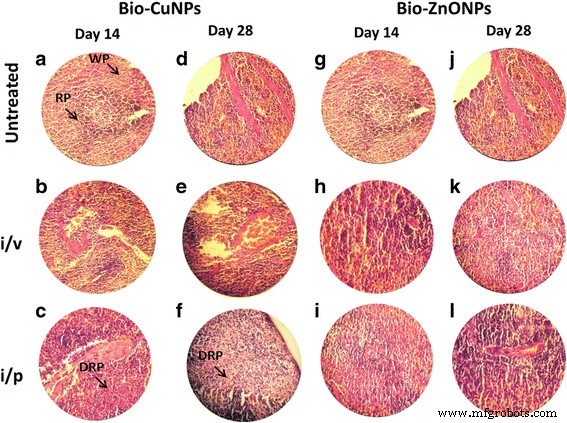
H &E-окрашенные срезы селезенки крысы. Крысам вводили в / в и в / б пути введения Bio-Cu и ZnONP; необработанные образцы считались контролем. Срезы, обработанные Bio-CuNP, наблюдались на 14-й день (A – C) и 28 день (D – F). Срезы, обработанные био-ZnONP, на 14 день (G – I) и 28 день (J – L). Белая целлюлоза WP, красная мякоть RP, снижение DRP красной мякоти
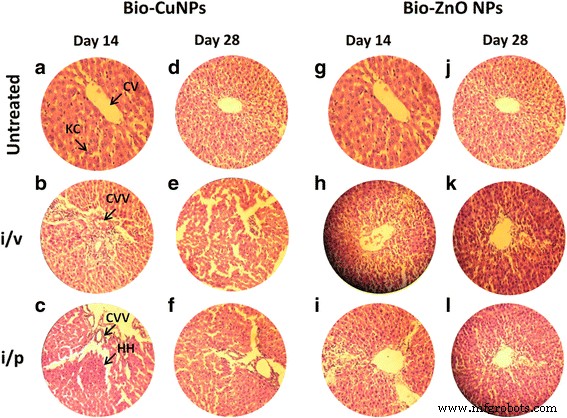
H &E-окрашенные срезы печени крысы. Крысам вводили в / в и в / б пути введения Bio-Cu и ZnONP; необработанные образцы считались контролем. Срезы, обработанные Bio-CuNP, наблюдались на 14-й день (A – C) и 28 день (D – F). Срезы, обработанные био-ZnONP, на 14 день (G – I) и 28 день (J – L). Центральная вена CV, клетки KC Купфера, вакуолизация центральной вены CVV (вакуолизация цитоплазмы), кровоизлияние в печень HH
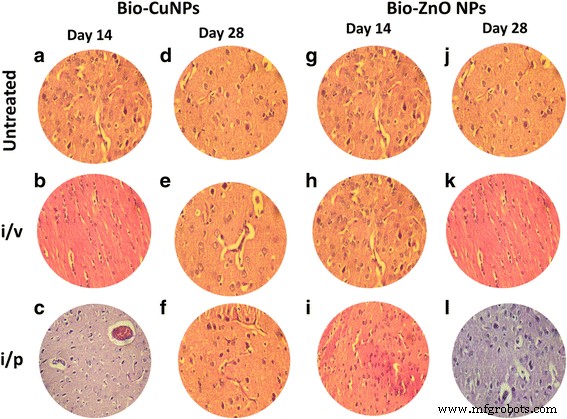
H &E-окрашенные срезы мозга крысы. Крысам вводили в / в и в / б пути введения Bio-Cu и ZnONP; необработанные образцы считались контролем. Срезы, обработанные Bio-CuNP, наблюдались на 14-й день (A – C) и 28 день (D – F). Срезы, обработанные био-ZnONP, на 14 день (G – I) и 28 день (J – L). [Все слайды наблюдаются при увеличении × 40, NIKON eclipse E200 (тринакулярный микроскоп)]
Био-CuNPs вызывали повреждения при в / в введении и демонстрировали дозозависимую тенденцию в тканях. При концентрации ТСХ (11,7 мкг / кг) Bio-CuNPs показали серьезное повреждение тканей печени и почек крыс Wistar. Кроме того, Bio-CuNP, обработанные как в / в, так и в / в пути, индуцировали некроз клубочковых клеток (атрофия клубочков), капсулы Боумена и проксимальных канальцев у крыс 14-го и 28-го дня в группах (рис. 4b, e, c и f). ) по сравнению с необработанным контролем. Некроз клубочков возникает из-за иммунологической компенсации, но повреждения канальцев в основном связаны с токсическим действием НЧ. Повреждение канальцев, вызванное токсическим действием Bio-CuNP как в / в, так и в / в, также увеличивает давление в клубочках и вызывает атрофию клубочков.
Нормальная контрольная группа показала нормальное гистологическое строение печеночной дольки и центральной вены, окруженной нормальными гепатоцитами (рис. 6). Био-CuNP, обработанные внутрибрюшинным путем (19,82 мкг / кг), показали умеренные гистологические изменения, включая активацию клеток Купфера, как на 14-й, так и на 28-й день наблюдения (фиг. 6b, e). У крыс, получавших Bio-CuNP внутривенно, наблюдались серьезные изменения, включая цитоплазматическую вакуолизацию гепатоцитов, окружающих центральную вену, и кровоизлияние в печень на 14-й день наблюдения (фиг. 6c). Удивительно, но 28-дневная группа показала умеренные изменения, включая жировые изменения гепатоцитов и пикноз ядер гепатоцитов (рис. 6f). Ткань печени, обработанная Био-ЗнОНП, в течение 14-го дня группы, которым вводили внутрибрюшинный путь, показала умеренные изменения, продемонстрированные жировыми изменениями гепатоцитов (фиг. 6i). Группы, обработанные био-ZnONP, показали небольшое улучшение, и значительная гепатопротекторная активность наблюдалась на 28-й день по сравнению с 14-м днем (фиг. 6l). На 14-й день и далее у животных, получавших Био-ЗнОНП, произошло восстановление нормальной архитектуры печени.
Было замечено уменьшение количества клеток селезенки (красная пульпа) и увеличение лимфоцитов (белая пульпа) в ткани селезенки, выделенной у крыс, получавших Bio-CuNP через в / в введения (рис. 5c, f). При первичном наблюдении увеличение количества Bio-CuNPs в селезенке было замечено в красной пульпе и было связано с умеренной потерей клеточной массы; reduced cell mass was obvious on the 28th day time point when compared with 14th day of i/v administration (Fig. 5f), whereas minor changes were observed in red pulp depletion when rats were treated with Bio-CuNPs via i/p route on both 14th and 28th day time point. Structural changes were not seen in the white pulp or in splenic blood vessels (arteries or venous sinuses) and intravascular erythrocytes (Fig. 5b, e). No morphological changes have been found in spleen tissues treated with Bio-ZnONPs (Fig. 5). The H&E-stained brain sections of rats, treated (i/v and i/p) with NPs, showed no changes in brain region, olfactory bulb (perivascular localization) and the choroid plexus and ependyma of the lateral ventricles (Fig. 7).
Conclusion
Animal toxicity studies using 16- to 96-nm-ranged biosynthesized copper (Bio-CuNPs) and zinc oxide (Bio-ZnONPs) was assessed in male Wistar rat at the dose range of 6.1 to 19.82 μg/kg and 11.14 to 30.3 μg/kg respectively for both i/p and i/v routes on 14th and 28th day of observation. We observed no mortality and normal behaviour in the animals treated with Bio-CuNPs and Bio-ZnONPs in their specific dose range. The results also verified the Bio-CuNPs and Bio-ZnONPs at low concentrations do not cause identifiable toxicity even after their breakdown in vivo over time. Increased concentrations of these Bio-NPs induce weight reduction, but no significant statistical difference was observed for Bio-ZnONPs’ treated animals. In the case of i/v and i/p Bio-CuNPs’ treated groups, obvious effects on organ index have been observed at both IC50 and TLC doses. Moreover, of the two different administration routes, the intraperitoneal injection shows the modest toxicity in Bio-ZnONPs’ treated groups and highest toxicity in Bio-CuNPs’ treated groups. Correspondingly, the intravenous injection shows the least toxicity in Bio-ZnONPs’ treated groups and highest toxicity in Bio-CuNPs’ treated groups. Considering all the results of studies, targeting Bio-ZnONPs by intravenous injection is promising for possible biomedical application.
Сокращения
- ±:
-
Plus or minus
- ALP:
-
Alkaline phosphatase
- ALT:
-
Alanine aminotransferase
- AST:
-
Aspartate aminotransferase
- Bio-CuNPs:
-
Biogenic copper nanoparticles
- Bio-ZnONPs:
-
Biogenic zinc oxide nanoparticles
- BX :
-
Brain index
- CRE:
-
Creatinine
- Cu:
-
Copper
- FesEM:
-
Автоэмиссионная сканирующая электронная микроскопия
- H&E:
-
Haematoxylin eosin
- Hb:
-
Haemoglobin
- HX :
-
Heart index
- i.e.:
-
That is
- i/p route:
-
Intraperitoneal route
- i/v route:
-
Intravenous route
- IC:
-
Inhibitory concentration
- KX :
-
Kidney index
- LiX :
-
Liver index
- LuX :
-
Lung index
- NOAEC:
-
No observable adverse effect concentration
- NPs:
-
Nanoparticles
- Ox :
-
Organ index
- RBC:
-
Red blood cell
- SD:
-
Standard deviation
- SX :
-
Spleen index
- ТЕМ:
-
Просвечивающая электронная микроскопия
- TLC:
-
Total lethal concentration
- TX :
-
Thymus index
- WBC:
-
White blood cell
- ZnO:
-
Оксид цинка
Наноматериалы
- Биосовместимые наночастицы FePO4:доставка лекарств, стабилизация РНК и функциональная активность
- Биогенный синтез, характеристика и оценка антибактериального потенциала наночастиц оксида меди против Escheric…
- Наночастицы альбумина, содержащие ресвератрол, с длительным кровообращением и улучшенной биосовместимостью…
- Новые биосовместимые наночастицы Au Nanostars @ PEG для КТ-визуализации in vivo и свойства очищения почек
- Биобезопасность и антибактериальная способность графена и оксида графена in vitro и in vivo
- Модифицированный гиперразветвленный полиглицерин как диспергатор для контроля размера и стабилизации нано…
- Синтез и эффективность in vitro покрытых полипирролом железо-платиновых наночастиц для фототермической терапии…
- Зеленая способность к синтезу и стабилизации наночастиц меди:каталитическая, антибактериальная, цитотоксич…
- Сравнительное исследование биосинтезированных наночастиц оксида меди и цинка in vivo путем внутрибрюшинного и…
- Зеленый синтез металлов и наночастиц оксидов металлов и их влияние на одноклеточную водоросль Chlamydomonas reinhardtii



