Водорастворимый фуллеренол с зависимостью от гидроксильных групп для эффективной фотодинамической инактивации инфекционных микробов с двухфотонным возбуждением
Аннотация
Мы успешно получили водорастворимый фуллеренол [C 60 (ОН) 46 ], который показал высокий квантовый выход синглетного кислорода и эффективно генерировал активные формы кислорода. Кроме того, водорастворимый C 60 (ОН) 46 с более высоким составом экспонированных гидроксильных групп имел превосходную двухфотонную стабильность и характеристики по сравнению с таковым с более низким составом таких групп. Таким образом, полученный фуллеренол может быть эффективным двухфотонным фотосенсибилизатором. Водорастворимый C 60 (ОН) 46 имел благоприятные двухфотонные свойства. Во время двухфотонной фотодинамической терапии водорастворимый C 60 (ОН) 46 обладают значительной антимикробной активностью в отношении Escherichia coli на сверхнизком уровне энергии 211,2 нДж пиксель −1 при 800 сканированиях и длине волны фотовозбуждения 760 нм.
Введение
За последние несколько десятилетий были синтезированы различные молекулы фотосенсибилизаторов (ФС) [1]. Однако клиническое применение существующих PS связано с рядом проблем. Большинство молекул ПС гидрофобны и могут легко агрегировать в водной среде, что снижает их квантовый выход (QY) [2]. Более того, агрегированные PS нельзя просто вводить внутривенно. Селективное накопление молекул PS в отмерших тканях также необходимо для предотвращения повреждения здоровых клеток. Из-за этих проблем разработка эффективного носителя PS остается серьезной проблемой для фотодинамической терапии (PDT). Соответственно, растет интерес к использованию наночастиц в качестве носителей ПС.
Прогресс в нанобиотехнологии стимулировал интерес к биомедицинским применениям нового класса наноструктур [3,4,5,6,7,8,9,10,11], которые состоят исключительно из атомов углерода, а именно фуллерена C 60. , которые представляют собой сфероидальные молекулы (диаметром 0,72 нм), которые не токсичны и обладают уникальными физико-химическими свойствами. Небольшой размер липофильного C 60 молекул отвечает за их стерическую совместимость с биологическими молекулами и способствует их интеграции в гидрофобные области мембран [12, 13]. Из-за расширенного π -сопряженная система его молекулярных орбиталей, фуллерен C 60 поглощает ультрафиолетовый-видимый (УФ-видимый) свет и может генерировать активные формы кислорода (АФК) с почти 100% синглетным кислородом QY ( Φ Δ ). Кроме того, физико-химические свойства фуллерена C 60 позволить ему генерировать ROS и служить PS для PDT. Фуллерены также могут вызывать прооксидантные эффекты, и это может быть продиктовано используемым фуллереном, типом исследованных клеток и экспериментальной установкой [14,15,16,17]. С 60 имеет чрезвычайно низкую растворимость в полярных растворах, что значительно ограничивает его применение в медицине. Однако из-за наличия двойных связей C 60 может быть легко модифицирован с помощью химических групп для увеличения его растворимости в воде. Следовательно, водорастворимый C 60 производные имеют расширенные возможности для медицинского применения, включая нейрозащиту, доставку лекарств и генов, фотосенсибилизацию и биосенсибилизацию.
Многофотонная лазерная микроскопия (также известная как двухфотонная лазерная микроскопия) влечет за собой использование локализованного «нелинейного» возбуждения для возбуждения флуоресценции только в тонкой плоскости растрового сканирования. Двухфотонная лазерная микроскопия использовалась в различных исследованиях изображений [18]. Обычно он сочетается с возбуждением лазером в ближней инфракрасной области (NIR), чтобы извлечь выгоду из присущего ему максимального пропускания ткани для биовизуализации; Это связано с тем, что NIR имеет преимущества небольшого рассеяния, поглощения низкой энергии, оптимального проникновения излучения и уменьшения фотообесцвечивания образцов. Сочетание двухфотонной лазерной микроскопии с возбуждением лазером NIR стало предпочтительным методом для флуоресцентной микроскопии толстых тканей и более глубоких биологических образцов [19, 20] и широко применяется в других методах лечения фотовозбуждением [21, 22]. Более того, из-за сверхнизкой энергии и короткого фотовозбуждения двухфотонная лазерная микроскопия считается альтернативным подходом к проведению ФДТ [23]. Хотя некоторые PS токсичны [24, 25], те, у которых высокий Φ Δ являются приоритетными для проведения PDT. Высокая Φ Δ значение особенно желательно, когда двухфотонные методы используются для оценки молекулярной активности в фотосвойствах и эффективного проведения нелинейных микроскопических исследований; такое значение желательно, потому что отношение поглощенной энергии к потоку энергии, подводимой к образцу, велико, что сводит к минимуму возможное фотоповреждение образца [26]. Однако в литературе нет исследований, в которых рассматривалось использование материалов с двухфотонными свойствами для PDT. Чтобы восполнить этот пробел, в настоящем исследовании применялся водорастворимый гидроксилированный фуллеренол с сильной способностью к донорству электронов и большим π -сопряженная система для повышения эффективности переноса заряда, тем самым улучшая двухфотонные свойства. В частности, водорастворимый гидроксилированный C 60 (ОН) 46 был разработан и применен в качестве двухфотонного PS для эффективного удаления микробов с использованием сверхнизкоэнергетического фемтосекундного лазерного излучения и всего 800 сканирований при двухфотонном возбуждении (TPE; длина волны возбуждения 760 нм). Для фемтосекундного лазерного излучения сверхнизкой энергии энергия составила 211,2 нДж на пиксель −1 . и мощность составила 2,112 мВт (относительно расчета мощности лазера после объектива см. раздел «Материалы и методы» и рис. 1а, где x - г фокус и z -осевое разрешение лазерной системы составляет примерно 0,37538 и 0,90159 мкм соответственно); кроме того, для процесса сканирования общее эффективное время экспозиции составляло приблизительно 3,2621 с, скорость сканирования составляла 4,0776 мс сканирование −1 , а область сканирования составляла 200 × 200 мкм 2 (Подробнее о расчетах см. в разделе «Материалы и методы»). Водорастворимый гидроксилированный C 60 (ОН) 46 удалось почти на 100% устранить Escherichia coli ( E. coli , грамотрицательный бактериальный штамм). Кроме того, водорастворимый C 60 (ОН) 46 с более высоким составом гидроксильных групп демонстрирует превосходные двухфотонные фотосвойства по сравнению с таковым с более низким составом гидроксильных групп под TPE; следовательно, производное водорастворимого C 60 (ОН) 46 можно рассматривать как имеющий значительный потенциал для использования при одновременной ФДТ для уничтожения злокачественных микробов.
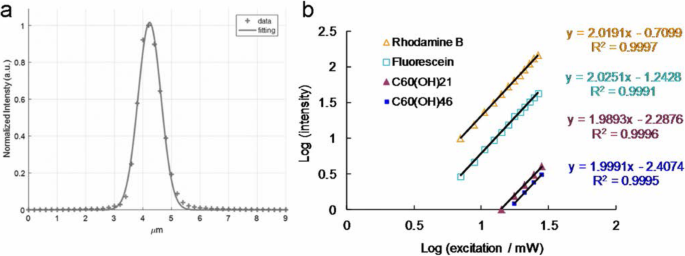
а Согласно z -осевое сканирование тонкой золотой пленки, используемой для измерения сигнала генерации второй гармоники в различных положениях, z -осевое разрешение лазерной системы (полная ширина на половине высоты) составляет приблизительно 0,90159 мкм (аппроксимация с использованием функции Гаусса). б Зависимость интенсивности ТФЛ от мощности (логарифма) возбуждения материалов и флуорофоров; Экспозиция TPE от 704,0 до 2816,0 нДж на пиксель −1 для родамина B и флуоресцеина от 1408,0 до 2816,0 нДж на пиксель −1 для водорастворимого C 60 (ОН) 21 фуллеренол, и от 1760,0 до 2816,0 нДж на пиксель −1 для водорастворимого C 60 (ОН) 46 фуллеренол. Длина волны возбуждения 760 нм. Доставленная доза:OD 600 0,05 из E. coli и 3 мкг мл -1 материалы. Данные представлены в виде средних значений ± стандартное отклонение ( n =6)
Материалы и методы
Получение и характеристика водорастворимых фуллеренолов, C 60 (ОН) 21 и C 60 (ОН) 46 [27]
Фуллерен-сырец был коммерчески доступен (Sigma-Aldrich, Сент-Луис, Миссури, США), а C 60 (ОН) 12 предшественник был произведен, как описано ранее. Сначала к исходному материалу добавляли 30% раствор перекиси водорода (100 мл; Sigma-Aldrich, Сент-Луис, Миссури, США), 0,5-1,0 г C 60 (ОН) 12 , и смесь интенсивно перемешивали при 60 ° C на воздухе. После охлаждения в раствор добавляли смесь растворителей, включающую 2-пропанол, диэтиловый эфир и гексан (по 100–200 мл для каждого; Sigma-Aldrich, Сент-Луис, Миссури, США), который затем центрифугировали и декантировали. Оставшееся твердое вещество дважды промывали 200 мл диэтилового эфира посредством процедур центрифугирования и декантации. Наконец, конечные продукты водорастворимого C 60 (ОН) 21 и C 60 (ОН) 46 были получены сушкой остатка в вакууме при комнатной температуре в течение ночи соответственно. Вес конечного продукта был откалиброван с помощью термогравиметрического анализа. Морфологию конечного продукта наблюдали с помощью просвечивающей электронной микроскопии высокого разрешения (HR-TEM, JEOL 3010, Акишима, Токио, Япония) с разрешением приблизительно 1,11 ± 0,03 нм и 1,13 ± 0,04 нм для C 60. (ОН) 21 и C 60 (ОН) 46 , соответственно. Динамическое рассеяние света (DLS, Malvern Nano-ZS90, Вустершир, Уэст-Мидлендс, Великобритания) также использовалось для определения размера материалов. Экспонированные функциональные группы материалов, как только они были приготовлены, сначала исследовали с помощью инфракрасной спектроскопии с преобразованием Фурье (FTIR) (RX1, PerkinElmer, Waltham, MA, USA). УФ – видимая спектроскопия материалов проводилась на спектрометре (U-4100, Hitachi, Chiyoda-ku, Tokyo, Japan). Химию поверхности фуллеренола исследовали с помощью рентгеновской фотоэлектронной спектроскопии (XPS, спектрометр PHI 5000 (VersaProbe, Chanhassen, MN, США)). Молекулярную массу фуллеренола определяли с помощью масс-спектрометра с полевой десорбцией (FD) (AccuTOF, GCx-plus, JEOL, Akishima, Tokyo, Japan), и на основании результатов было подтверждено, что количество гидроксильных групп составляет 21 и 46. соответственно.
Бактериальные культуры [28]
Э. coli , полученные из нашей собственной лаборатории, были выращены в питательном агаре LB (на литр:триптон 10 г, дрожжевой экстракт 5 г, хлорид натрия 8 г, агар 15 г, pH доведен до 7,5) (Sigma-Aldrich, St. Louis, Миссури, США) и инкубировали при 37 ° C.
Анализ биосовместимости с методом подсчета колониеобразующих единиц (КОЕ) [28]
Э. coli (OD 600 ~ 0,05) был добавлен материал (0–9 мкг мл -1 ) и инкубировали в течение 3 ч при 37 ° C (дополнительный файл 1:рис. S1). После инкубации смесь центрифугировали и осадки бактерий разбавляли (OD 600 ~ 0,05). Фактор разбавления 10 −5 до 10 −8 затем проводили с инкубированными бактериями и высевали на чашки с агаром. Планшеты оставляют в инкубаторе (при 37 ° C) на ночь. Количество выживших бактерий определяли и выражали в процентах (%), что соответствовало единице КОЕ / мл -1 . после инкубации. Данные представляют собой средние значения ± стандартное отклонение ( n =6).
ψ Δ Измерение [29, 30]
Согласно предыдущему исследованию, ψ Δ может быть получен. ψ Δ измерения проводились в D 2 O на 355 нм, используя мезо -тетра (4-сульфонатофенил) порфина дигидрохлорид (TSPP; Sigma-Aldrich, Сент-Луис, Миссури, США) в качестве эталона ( ψ Δ =0,64).
Измерение QY флуоресценции [31, 32]
Относительная фотолюминесценция (PL) QY контрастного вещества обычно представляет собой отношение испускаемых фотонов к поглощенным фотонам и определяется следующим образом:
$$ \ mathrm {QY} ={\ mathrm {QY}} _ {\ mathrm {ref}} \ \ left ({\ eta} ^ 2 / {\ eta _ {\ mathrm {ref}}} ^ 2 \ right) \ left (I / A \ right) \ left ({A} _ {\ mathrm {ref}} / {I} _ {\ mathrm {ref}} \ right) $$ (1)где QY ref =0,28 - QY Cy5.5, растворенного в диметилсульфоксиде (ДМСО; Sigma-Aldrich, Сент-Луис, Миссури, США) в качестве эталона, η - показатель преломления ddH 2 O =1,33 ( η ссылка ДМСО =1,48), I - интегральная интенсивность флуоресценции, а A - поглощение на длине волны возбуждения. Однофотонное возбуждение (OPE) или TPE дает тот же QY.
Фемтосекундная лазерная оптическая система для измерения двухфотонного поглощения (TPA) и двухфотонной люминесценции (TPL) [23, 28, 33,34,35 , 36,37,38]
Самодельная фемтосекундная лазерная оптическая система титан-сапфир (ti-sa) (частота повторения 80 МГц; Tsunami, Spectra-Physics, Санта-Клара, Калифорния, США) использовалась в соответствии с предыдущими исследованиями.
Измерение TPA
Со скоростью сканера гальванометра 2 м мс −1 спектр возбуждения был измерен как 720–820 нм с мощностью возбуждения 2,8 мВт [это мощность перед объективом; мощность после объектива (или на образце) составляет 0,9856 мВт или 98,56 нДж на пиксель −1 ]. Поэтому были измерены относительные спектры TPA как функция длины волны возбуждения для фуллеренолов.
Измерение спектров TPL
Материал подвергали ТПЭ фемтосекундным лазером при длине волны возбуждения 760 нм, область сканирования 200 × 200 мкм 2 , частота 10 кГц, время экспозиции 1,638 с / (сканирование, пиксель) =100 мкс, сканирование 128 × 128 пикселей −1 и площадь пикселя 1562,5 × 1562,5 нм 2 . Площадь фокусного пятна рассчитывалась как π d 2 / 4, где d =0,61 λ / числовая апертура ( NA ) - полная ширина на половине высоты перетяжки луча. Например, на x - г осевое фокальное пятно с возбуждением 760 нм и масляно-иммерсионным объективом × 40 с NA из 1,3, d =0,61 × 800 нм / 1,3 =375,38 нм =0,37538 мкм, а z -осевое разрешение составило 0,90159 мкм. Для возбуждения 760 нм время экспозиции на сканирование для отдельного наноматериала выражается как (площадь фокусного пятна / площадь пикселя) × 100 =4,0776 мс, а общее время экспозиции t =4,0776 мс × количество сканирований. Маслоиммерсионный объектив A × 40 ( NA 1.3) использовался для сбора сигналов, а диапазон обнаружения спектрального фотометра составлял 300–695 нм.
Кроме того, расчеты мощности лазера (мВт или нДж пиксель −1 ), использованные на образце, были следующими. Для масляно-иммерсионного объектива × 40 ( NA 1.3), скорость передачи на длине волны 760 нм в этой оптической системе составляет примерно 88%, а мощность лазера передавалась от выхода к объективу только с 40% исходной выходной мощности из-за потери мощности. В результате расчетная энергия после объектива (на образце) составляет P вывод (мВт) * 40% * 88% =0,352 × P вывод (мВт). Например, P вывод =2,8 мВт, расчетная энергия после объектива (на образце) составляет 3,0 мВт * 40% * 88% =0,9856 мВт. При частоте сканирования 10 кГц (каждый импульс остается пикселем 0,1 мс −1 ), рассчитанная энергия на образце (Дж пиксель −1 ) было около P вывод (мВт) * 40% * 88% * 0,1 мс =0,0352 * P вывод (J пиксель −1 ). Например, P вывод =2,8 мВт, энергия (Дж пиксель −1 ) на образце =2,8 мВт * 40% * 88% * 0,1 мс =0,09856 мкДж пиксель −1 =98,56 нДж пиксель −1 . Мощность после объектива (на образце) была использована и отмечена пропускной способностью данной рукописи.
Измерение абсолютного поперечного сечения TPE [24, 36,37,38,39,40,41,42,43,44,45,46,47, 48]
Абсолютное сечение ТПЭ измеряли по сигналу люминесценции через фемтосекундная лазерная оптическая система в соответствии с предыдущими исследованиями. TPL флуоресцеина и родамина B (Sigma-Aldrich, Сент-Луис, Миссури, США) требовали проверки. Результаты показаны на рис. 1b и были получены путем измерения зависимости интенсивности излучения в диапазоне мощности возбуждения 704 нДж на пиксель −1 . (7,04 мВт) до 2816 нДж пиксель −1 (28,16 мВт). Квадратичная зависимость с показателями степени 2,03 для флуоресцеина и 2,02 для родамина B была измерена для увеличения мощности возбуждения для определения люминесценции от TPE. Согласно предыдущим исследованиям, сечения действия TPE для флуоресцеина и родамина B составляют 36,4 и 68,0 GM (1 GM =10 -50 см 4 s фотон −1 ) соответственно для возбуждения 760 нм. Мы также сослались на бесплатный веб-сайт http://www.drbio.cornell.edu/cross_sections.html, любезно предоставленный профессором Крисом Сюй (Корнельский университет, Нью-Йорк, США). Поперечные сечения действия TPE для флуоресцеина и родамина B были рассчитаны и составили 36,5 и 66,1 ГМ соответственно (таблица 1), что указывает на ошибку менее 5% по сравнению с данными лаборатории профессора Сюй. В этом исследовании родамин B был выбран в качестве стандартного эталона для определения поперечного сечения, а рассчитанные абсолютные поперечные сечения TPE для водорастворимого C 60 (ОН) 21 и C 60 (ОН) 46 фуллеренолы составляли приблизительно 1230,51 гм и 1037,21 гм соответственно. Измеренные параметры для расчета абсолютных поперечных сечений TPE образцов показаны в таблице 3. Для материалов двухфотонных свойств и двухфотонной фотодинамической способности не наблюдалось изменений от партии к партии.
Фемтосекундная лазерная оптическая система (для флуоресцентной микроскопии с визуализацией продолжительности жизни, FLIM) [39, 45]
Самодельная фемтосекундная лазерная оптическая система ти-са (частота следования 80 МГц; Tsunami, Spectra-Physics, Санта-Клара, Калифорния, США) использовалась в соответствии с предыдущими исследованиями. Данные и параметры срока службы генерируются с использованием аппроксимации тройным экспоненциальным уравнением при мониторинге эмиссии в условиях TPE (Ex, 760 нм).
Расчет скоростей радиационного и безызлучательного распада [46]
PL QY и время жизни являются основными параметрами при исследовании характеристик излучения флуоресцентных красителей в различных средах. QY ( Q ) можно выразить следующим образом:
$$ Q =\ frac {\ varGamma} {\ varGamma + k} $$ (2)где Γ - скорость радиационного распада, а k - скорость безызлучательного распада. Время жизни флуоресценции обычно определяется как среднее время, необходимое электрону в возбужденном состоянии для распада в основное состояние. Срок действия TPL τ также может относиться к скорости распада и описывается следующим образом:
$$ \ tau =\ frac {1} {\ varGamma + k} $$ (3)Следуя уравнениям. По формулам (2) и (3) скорости радиационного и безызлучательного распада могут быть рассчитаны.
При поглощении фотона один из слабосвязанных электронов флуоресцентной молекулы - флуорофор - перемещается на более высокий энергетический уровень. В этом случае флуорофор находится в возбужденном состоянии, A * . Это состояние метастабильно; следовательно, флуорофор вернется в свое стабильное основное состояние, A . Он может делать это либо излучательно, испуская фотон флуоресценции hν
$$ A \ ast -> A + h \ nu $$или безызлучательно, рассеивая энергию возбужденного состояния в виде тепла:
$$ A \ ast -> A + \ mathrm {heat} $$Депопуляция возбужденного состояния зависит от имеющихся путей снятия возбуждения. Флуоресценция - это радиационная деактивация самого низкого уровня колебательной энергии первого электронно-возбужденного синглетного состояния, S 1 , обратно в основное электронное состояние, S 0 . Синглетные состояния - это уровни энергии, которые могут быть заселены слабосвязанным электроном без переворота спина. Процессы поглощения и излучения иллюстрируются диаграммой уровней энергии имени Александра Яблонского.
Время жизни флуоресценции, τ , - среднее время, в течение которого флуорофор остается в электронно-возбужденном состоянии S 1 после возбуждения. τ определяется как величина, обратная сумме параметров скорости для всех процессов депопуляции возбужденного состояния:Ур. (3), где безызлучательная константа скорости k представляет собой сумму константы скорости внутреннего преобразования k ic и константа скорости межсистемного перехода в триплетное состояние k isc такое, что k = k ic + к isc . Излучение флуоресценции всегда происходит с самого низкого колебательного уровня S . 1 , правило, известное как правило Каши, указывающее на то, что флуорофор не помнит свой путь возбуждения; например, OPE и TPE дают одинаковый спектр флуоресценции, QY и время жизни.
Определение уровня жизнеспособности бактерий после лазерного воздействия [28]
Метод подсчета КОЕ
Бактерии (OD 600 ~ 0,05) был добавлен материал (3 или 6 мкг мл -1 ) путем инкубации в течение 3 ч при 37 ° C в темноте. После инкубации смесь центрифугировали и осадки бактерий разбавляли (OD 600 ~ 0,05) при мощности TPE 211,2 нДж на пиксель −1 при 800 сканированиях (приблизительно 3,2621 с общего эффективного времени экспозиции; Ex, 760 нм). Затем коэффициент разбавления 10 −5 до 10 −8 затем проводили с инкубированными бактериями и высевали на чашки с агаром. Планшеты оставляют в инкубаторе (при 37 ° C) на ночь. Количество выживших бактерий определяли и выражали в процентах (%), что соответствовало единице КОЕ / мл -1 . после инкубации. Данные представляют собой средние значения ± стандартное отклонение ( n =6).
LIVE / DEAD Kit
Бактерии (OD 600 ~ 0,05) был добавлен материал (3 или 6 мкг мл -1 ) путем инкубации в течение 3 ч при 37 ° C в темноте. После инкубации смесь центрифугировали и осадки бактерий разбавляли (OD 600 ~ 0,05) при мощности TPE 211,2 нДж на пиксель −1 при 800 сканированиях (приблизительно 3,2621 с общего эффективного времени экспозиции; Ex, 760 нм). Затем гранулы окрашивали с использованием LIVE (SYTO 9, как показано зеленой флуоресценцией) / DEAD ( йодид пропидия, PI, как показано с красной флуоресценцией) (Thermo Fisher Scientific, Уолтем, Массачусетс, США) в соответствии с инструкцией. Жизнеспособность бактерий была определена количественно с помощью антимикробных тестов, которые показали, что почти все обработанные наноматериалом бактерии умерли после обработки. Сходная жизнеспособность была определена количественно с помощью метода подсчета КОЕ для определения эффективных антибактериальных эффектов материалов при ФДТ. Данные представлены как среднее ± стандартное отклонение ( n =6).
Обнаружение ROS [23, 29, 34, 35, 49,50,51,52,53,54,55]
Синглетный кислород ( 1 О 2 )
(а) Материал (3 или 6 мкг мл -1 ) обрабатывали бактериями (OD 600 ~ 0,05), после чего подвергали 3 ч инкубации при 37 ° C в темноте. Затем смесь подвергали фотовозбуждению TPE (211,2 нДж пиксель −1 , 800 сканирований; Ex, 760 нм) и, наконец, смешали с реагентом Singlet Oxygen Sensor Green (SOSG) (1 мкМ; Thermo Fisher Scientific, Уолтем, Массачусетс, США) (Ex / Em:488/525 нм). Для измерений использовался флуоресцентный спектрометр. Для нейтрализации ROS смесь смешивали с 30 ppm антиоксиданта α -токоферол / метиллинолеат (Sigma-Aldrich, Сент-Луис, Миссури, США) в темноте и подвергнутый фотовозбуждению TPE с такой же обработкой. (б) Материал (3 или 6 мкг мл -1 ) обрабатывали бактериями (OD 600 ~ 0,05), после чего подвергали 3 ч инкубации при 37 ° C в темноте. Затем смесь подвергали фотовозбуждению TPE (211,2 нДж пиксель −1 , 800 сканирований; Ex, 760 нм) и, наконец, смешали с 10 мкМ транс-1- (2'-метоксивинил) пирена ( t -MVP, Thermo Fisher Scientific, Уолтем, Массачусетс, США) / 0,10 M SDS (Sigma-Aldrich, Сент-Луис, Миссури, США) (Ex / Em:352/465 нм). Для нейтрализации ROS смесь смешивали с 30 ppm антиоксиданта α -токоферол / метиллинолеат (Sigma-Aldrich, Сент-Луис, Миссури, США) в темноте. Реакция t -MVP с 1 О 2 дает промежуточный диоксетан, который флуоресцирует при разложении на 1-пиренкарбоксальдегид. Кроме того, этот высокоселективный флуоресцентный зонд не реагирует с другими активированными формами кислорода, такими как гидроксильные радикалы, супероксид или перекись водорода. Для измерений использовался флуоресцентный спектрометр. Нейтрализацию АФК проводили так же, как описано ранее.
Радикальный анион супероксида (O 2 .- )
(а) Материал (3 или 6 мкг мл -1 ) обрабатывали бактериями (OD 600 ~ 0,05), после чего подвергали 3 ч инкубации при 37 ° C в темноте. Затем смесь подвергали фотовозбуждению TPE (211,2 нДж пиксель −1 , 800 сканирований; Ex, 760 нм) и, наконец, смешали с 2,3-бис (2-метокси-4-нитро-5-сульфофенил) -2H-тетразолий-5-карбоксанилидом (XTT, 0,45 мМ; Sigma-Aldrich, St. Louis, MO , США). Целью этого материала было взаимодействие с O 2 . - и произвел XTT-формазан, что привело к сильному поглощению (длина волны 470 нм). Для контроля этого поглощения использовался УФ-видимый спектрометр. Для нейтрализации ROS смесь смешивали с 30 ppm антиоксиданта α -токоферол / метиллинолеат (Sigma-Aldrich, Сент-Луис, Миссури, США) в темноте и подвергнутый фотовозбуждению TPE с такой же обработкой. (б) Материал (3 или 6 мкг мл -1 ) обрабатывали бактериями (OD 600 ~ 0,05), после чего подвергали 3 ч инкубации при 37 ° C в темноте. Затем смесь подвергали фотовозбуждению TPE (211,2 нДж пиксель −1 , 800 сканирований; Ex, 760 нм) и, наконец, смешанный с 50 мМ бикарбонатным буфером (pH 8,60) и глутатионом ( γ -1-глутамил-1-цистеинил-глицин, GSH, Sigma-Aldrich, Сент-Луис, Миссури, США) / 0,80 мМ бикарбонатный буфер (анализ Эллмана для O 2 . - обнаружение). Впоследствии следующие эксперименты были проведены в соответствии с процедурой, описанной в предыдущем исследовании. Потеря GSH (%) рассчитывалась как разница в оптической плотности между образцом и отрицательным контролем, деленная на оптическую плотность отрицательного контроля. Сигнал генерируемого O 2 . - был получен, как описано в предыдущем расчете. Данные представляют собой средние значения ± стандартное отклонение ( n =6).
Анализ поглощения [35]
Э. coli (OD 600 ~ 0,05) инкубировали с 3 мкг мл -1 материал. Поглощение количества 3 мкг мл -1 Материал регистрировали методом УФ-видимой спектроскопии (Abs, примерно 203 нм). Материалы были смешаны с E. coli (OD 600 ~ 0,05) при 37 ° C с 1-го по 10-й час, соответственно, и центрифугировали (1200 об / мин) для удаления лишних материалов и удержания супернатанта и измерения его поглощения. Оценивали разницу в поглощении между собранным супернатантом и исходными материалами, в результате чего определяли процент поглощения в каждый момент времени. Данные представляют собой средние значения ± стандартное отклонение ( n =6).
Статистический анализ [56]
Статистическая значимость определялась дисперсионным анализом. p значение считалось статистически значимым для всех обработок.
Результаты и обсуждение
Характеристика водорастворимого фуллеренола
Водорастворимый C 60 (ОН) 46 (фуллеренол), который был определен как кольцевой и монодисперсный, был синтезирован в соответствии с предыдущим исследованием [27]. Средний латеральный размер фуллеренола составлял приблизительно 1,13 ± 0,04 нм, как было определено с использованием изображений с малым увеличением (фиг. 2a) и изображений HR-TEM (фиг. 2b). Кроме того, было отмечено, что фуллеренол проявляет благоприятную кристалличность наряду с хорошим шагом решетки, который соответствует d -размещение полос решетки фуллеренола {1 \ (\ overline {1} \) 00}. Однако эти частицы могут образовывать агрегаты за счет водородных связей в водном растворе с pH 7,0. Средний размер образовавшихся агрегатов составлял приблизительно 130 нм, как показал анализ DLS. Более того, агрегаты оставались очень стабильными в течение 3 месяцев в различных физиологических средах, таких как водный раствор с pH 7,0, 1 × фосфатно-солевой буфер и питательная среда (дополнительный файл 1:таблица S1). В УФ-видимом спектре поглощения фуллеренола пики поглощения наблюдались примерно при 216 и 309 нм, и эти пики были отнесены к π - π * переход ароматических связей C =C и n - π * переходы плеча C =O соответственно. π -электронный переход в фуллереноле, содержащем кислород (рис. 2c), что обычно наблюдается для водных дисперсий, тем самым подтверждая присутствие фуллеренола. Дополнительные характеристики были выполнены с использованием FTIR, XPS и масс-спектрометрии для подтверждения свойств приготовленных материалов. FTIR был использован для анализа экспонированных функциональных групп приготовленных материалов. Результаты анализа выявили следующие характерные полосы материала:валентную полосу C – O примерно при 1109 см −1 (полоса 1), фенольная полоса валентных колебаний C – OH примерно при 1271 см −1 (полоса 2), валентная полоса третичного спирта C =O примерно при 1422 см -1 (полоса 3), полоса растяжения C =C приблизительно при 1674 см -1 (полоса 4), полоса растяжения C =O примерно при 1721 см -1 (полоса 5) и межмолекулярная водородная связь C – H и валентная полоса карбоксилатного O – H примерно при 3318 см -1 (полоса 6). Кроме того, полоса CO 2 интерференция не наблюдалась. Эти полосы выявили открытые гидроксильные и карбонильные группы, а также ароматические связи C =C (рис. 2d). XPS был выполнен для изучения химического состава поверхности фуллеренола, который преимущественно содержит атомы углерода в целом. Спектры C (1s) фуллеренола после деконволюции выявили отсутствие кислорода в кольце (C – C / C =C, 286,1 эВ), связь C – O (286,9 эВ) и связь C =O (288,0 эВ). Кроме того, отношение O (1s) / C (1s) составляло приблизительно 35,8% (рис. 2e). Молекулярную массу фуллеренола также определяли с помощью масс-спектрометрии FD (дополнительный файл 1:рис. S2); the number of hydroxyl groups (C–OH) was confirmed to be 46, which was consistent with the atomic ratios and bonding compositions of the fullerenol summarized in Fig. 2. These characterization results confirm the successful synthesis of fullerenol.
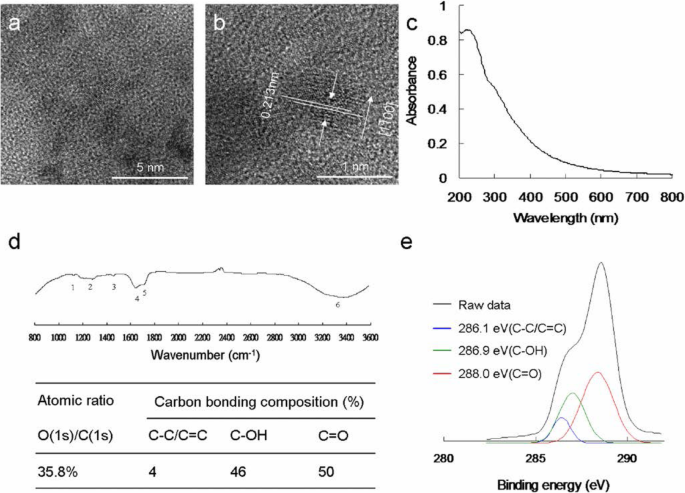
Functional characterization of the synthesized water-soluble C60 (OH)46 fullerenol. а Low-magnified TEM image and b HR-TEM image of a water-soluble fullerenol illustrating the materials {1\( \overline{1} \)00} lattice planes and the mean size of 1.11 ± 0.03 nm with a d -spacing of 0.213 nm. c UV–vis and d FTIR spectra of nanomaterial. е Deconvoluted C(1s) XPS spectra and fitted peaks obtained using Gaussian function:nonoxygenated ring (C–C/C=C), C–O bond, and C=O bond, respectively. The atomic ratio and bonding composition of fullerenol are shown as summarized in the table. The O(1s)/C(1s) atomic ratio is 35.8%
ROS Generation of Water-Soluble Fullerenol Under TPE
A PS absorbs and transfers light energy to other nonabsorbing molecules to generate ROS, which kill targeted cells, damage tumor vasculature, and activate an antitumor immune response. PSs have a particular arrangement of electrons in their molecular orbitals. Similar to nearly all molecules, at ground (singlet) state, PSs have couples of electrons with opposite spins in low-energy molecular orbitals. The absorption of light at an appropriate wavelength lifts an electron to a high-energy orbital without changing its spin. This is a short-lived (nanoseconds) excited singlet (S1 ) state, and the PS can lose its energy and return to the ground state by emitting light (fluorescence) or heat. Alternatively, intersystem crossing, wherein the spin of the excited electron is inverted, can occur in the S1 государство. This electron spin inversion is responsible for the relatively long life (lasting microseconds) of the excited triplet (T1 ) state. Radiative triplet-to-singlet transitions are inhibited because they require a change in electron spin, which is a slow process. From the T1 state, the PS can return to the ground state by emitting light (phosphorescence) or transferring energy to another molecule. It can also lose energy through internal conversion or radiationless transitions when colliding with other molecules. The longer the life of the PS in the T1 state is, the higher are its chances of colliding with another molecule, resulting in ROS production [57,58,59]. The photosensitization of water-soluble fullerenols results in their transition to a long-lived T1 state and subsequent energy or electron transfer to molecular oxygen, yielding ROS such as 1 О 2 и O 2 . - , which have major roles in PDT. Therefore, 1 О 2 и O 2 . - produced by water-soluble C60 (OH)46 must be detected directly using laser irradiation. To detect 1 О 2 и O 2 . - formation during PDT, in this study, PDT was initiated by combining excited the triplet water-soluble C60 (OH)46 , oxygen, and light configured to a suitable wavelength and energy as well as by introducing SOSG, t -MVP, XTT, and GSH reagents [33, 34, 49,50,51]. To exploit the potential bactericidal capability of the materials, a wavelength of approximately 760 nm was determined to be the most efficient for deriving the relative maximum TPA ratio of the water-soluble C60 (OH)46 under TPE (Fig. 3a); this is attributable to the interband transitions involved [52]. This wavelength was used in subsequent experiments in this study. The water-soluble C60 (OH)46 was photoexcited through TPE at a power of 211.2 nJ pixel −1 with 800 scans (Ex, 760 nm; total effective exposure time, ~ 3.2621 s) and delivered dose of 3 or 6 μg mL −1 (Additional file 1:Table S2). Furthermore, to confirm the involvement of ROS in the PDT effects of the water-soluble C60 (OH)46 , α -tocopherol was used for ROS neutralization [49, 53]. The quantity of generated ROS was reduced after the addition of α -tocopherol, but the observed bacterial viability increased as expected. Additionally, the quantity of generated ROS depended on the delivered dose. To prevent 1 О 2 и O 2 . - production possibly engendered by inadvertent exposure of water-soluble C60 (OH)46 to white light—which could have compromised the experiments in this study [60]—subsequent PDT experiments were conducted in the dark. This study focused on the quantities of generated 1 О 2 и O 2 . - . The water-soluble C60 (OH)46 exhibited considerable antibacterial effects, demonstrating its potential for application in PDT. Notably, after the same experiment, the water-soluble C60 (OH)21 (Additional file 1:Figs. S3, S4; Fig. 3a) was less effective in forming 1 О 2 и O 2 . - when compared with the water-soluble C60 (OH)46 (Additional file 1:Table S2). The water-soluble C60 (OH)46 generated more 1 О 2 и O 2 . - than did the water-soluble C60 (OH)21; additionally, the water-soluble C60 (OH)46 and water-soluble C60 (OH)21 had Φ Δ values of approximately 0.93 and 0.85, respectively (for reference, Φ Δ =0.64 is the QY of TSPP dissolved in D2 O [29, 30]).
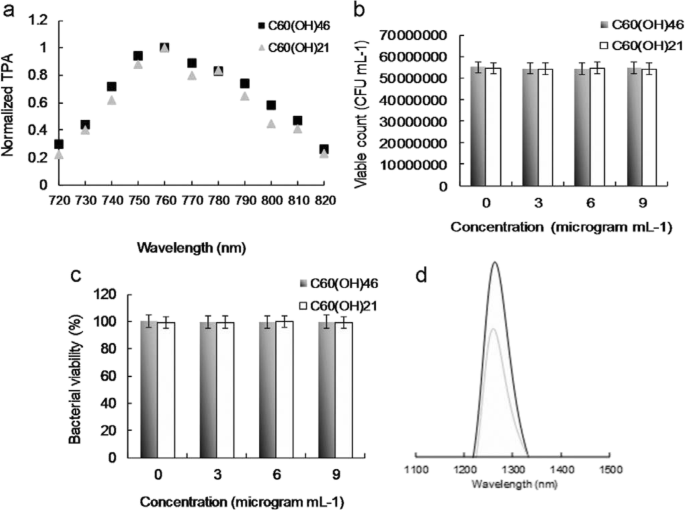
а Relative TPA spectra of the material. TPE as a function of the wavelength (720–820 nm) at 98.56 nJ pixel −1 that was used to monitor the signals. Delivered dose, 3 μg mL −1 water-soluble C60 (OH)46 or C60 (OH)21 fullerenol. The number of surviving b material-treated bacteria was determined by CFU counting assay and is expressed as the percentage (%) for c bacteria that corresponds to the unit of CFU mL −1 . Delivered dose, OD600 ~ 0.05 of E. coli and 0–9 μg mL −1 water-soluble fullerenol. г Measurement of phosphorescence spectra at 1270 nm for material. Delivered dose, 3 μg mL −1 water-soluble fullerenol. Data are means ± SD (n =6)
Antimicrobial Ability Determination Using TPE
Before the execution of antimicrobial experiments, the toxicity of water-soluble fullerenols must be examined to exclude factors that could contribute to bacterial elimination and confound experimental results. In addition, to prevent possible ROS production engendered by the inadvertent exposure of experimental materials to white light, which could confound experimental results [35], PDT experiments must be conducted in the dark. This study applied Gram-negative E. coli as the experimental template. A CFU counting assay was conducted to determine the number of surviving bacteria (expressed herein as a percentage, corresponding to CFU mL −1 ). The bacteria were treated with two types of the prepared water-soluble fullerenols (dose range, 0 to 9 μg mL −1 ) and incubated in the dark for 3 h at 37 °C to determine absorbance at 600 nm (OD600 ~ 0.05; Additional file 1:Fig. S1). The growth levels of the bacteria treated with the water-soluble fullerenols were first monitored by measuring absorbance at 600 nm. The initial absorbance was 0.05 OD600 , and the absorbance associated with both materials reached approximately 0.37 over time. Accordingly, neither material inhibited bacterial proferation. Moreover, the materials engendered a nearly 0 log10 reduction in the number of surviving bacteria (Fig. 3b), corresponding to a viability of approximately 100% (Fig. 3c). Accordingly, the materials were determined to exhibit excellent biocompatibility with the bacteria. Consequently, the materials subjected to 3 h of incubation in the dark at 37 °C were used to conduct experiments. Although the water-soluble fullerenol could generate ROS, interactions between materials and reagents (i.e., SOSG, t -MVP, XTT, and GSH) may result in false-positive ROS signals, thereby confounding PDT results [52]. Therefore, to exclude this possibility, bacteria were introduced and treated with materials in the present study. The amount of ROS generated from the photoexcited material-treated E. coli was observed. Table 2 presents the observed amount of ROS, revealing a similar trend to that in Tables S2–S3 (Additional file 1:materials alone and material-treated-Gram-positive Bacillus subtilis (B. subtilis )); these results were consistent with the 1 О 2 phosphorescence signal emitted from the materials at 1270 nm (Fig. 3d). PDT against E. coli was performed using irradiation with a low dose of energy (211.2 nJ pixel −1 with 800 scans, total effective exposure time ~ 3.2621 s; Ex, 760 nm). The effects PDT on the viability of E. coli treated with two-photon photoexcited materials were then determined (Fig. 4). No bactericidal effects were observed on bacteria alone (with or without laser exposure) or on the panel of material-treated bacteria without laser treatment (Fig. 4a). After TPE, bacterial viability was relatively low; specifically, the viability observed for the panel that was treated with the water-soluble C60 (OH)21 was nearly 15%, corresponding to an approximately 0.823 log10 reduction (Fig. 4b). By contrast, the bacterial viability observed for the panel treated with the water-soluble C60 (OH)46 was approximately 0 (100% elimination efficiency, corresponding to a ~ 7.736 log10 reduction). When the dose was increased, complete bactericidal effects were observed for both materials (Fig. 4c, d). However, antimicrobial effects did not differ by bacteria type (Gram-negative E. coli or Gram-positive B. subtilis ) after photoexcitation (Additional file 1:Fig. S5). In addition, regarding the fullerenols that eliminated bacteria, a higher composition of hydroxyl groups increased bactericidal capability when compared with a lower composition under identical treatment conditions.
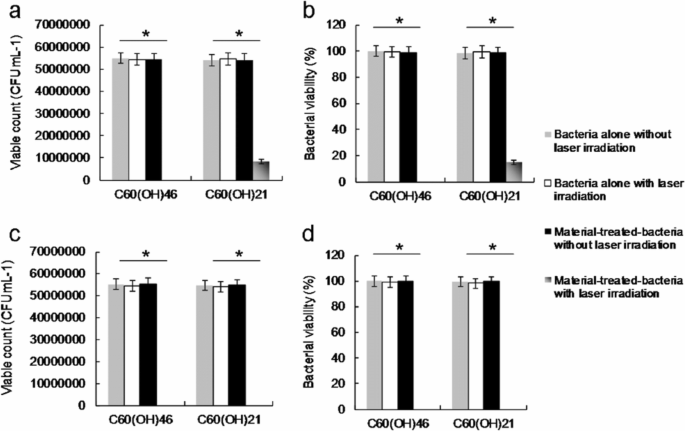
Viability (%) was quantified according to the determined viable count of material-treated bacteria through a CFU assay conducted using short excitation with a TPE power of 211.2 nJ pixel −1 with 800 scans (approximately 3.2621 s of total effective exposure time; Ex, 760 nm) to deliver a dose of a , b 3 or c , d 6 μg mL −1 . Delivered dose, OD600 0.05 of E. coli . Data are presented as means ± SD (n =6). For C60 (OH)46 - and C60 (OH)21 -treated E. coli with photoexcitation, a p <0.001 and p =0.662, b p <0.001 and p =0.658, c p <0.001 and p <0.001, and d p <0.001 and p <0.001. * p value obtained by Student’s t test
Observation of Water-Soluble Fullerenol-Treated E. coli Using TEM and Investigation of Two-Photon Properties
To observe the disruption of material-treated bacteria after photoexcitation, the water-soluble C60 (OH)46 with high PDT efficiency was selected, and bacteria were imaged using TEM. Bare E. coli (Fig. 5a) were incubated with the water-soluble fullerenol for 3 h, resulting in the substantial adsorption of materials on the bacterial surfaces. Nevertheless, no unusual morphologies were observed, indicating normal live bacterial morphology (Fig. 5b). Uptake assay results revealed the adsorption of materials onto the bacterial surface, with the corresponding burst rate being approximately 85% within the first 3 h of incubation (Fig. 5c); the rate reached saturation from the 3rd to the 10th hour. Therefore, the materials were adsorbed and formed an external barrier on the bacterial surface. However, the E. coli exhibited a distorted appearance and severe morphological changes over 3 days of incubation (Fig. 5d), resulting in a 0.940 log10 reduction that corresponded to a nearly 18% viability (Fig.5f; Additional file 1:Fig. S6). Material absorption and coating on the bacterial surface suppressed the absorption of nutrients essential for microbial growth and engendered changes in membrane (wall) permeability, thereby inducing internal osmotic imbalances and inhibiting microbial growth. In other words, the water-soluble fullerenol had antibacterial (bacteriostatic or bactericidal) effects after 3 days of incubation. Furthermore, the photoexcited material-treated bacteria, particularly E. coli , exhibited unique morphologies with severe damage after 3 h of incubation (Fig. 5e, f; Additional file 1:Fig. S6). No heat-generated bubbles formed on the bacterial surface incurred damage, indicating that the water-soluble fullerenol did not have photothermal-mediated heat properties after photoexcitation (Additional file 1:Fig. S7). The viability of E. coli was also determined through fluorescence and quantification (Fig. 6). The green fluorescence indicative of living bacteria in Fig. 6a reveals that the bacteria exposed to laser treatment alone were largely undamaged, which is consistent with the results presented in Fig. 5a. Dead bacteria were detectable after treatment with the materials and laser exposure (red fluorescence in Fig. 6b), a finding that is also consistent with that in Fig. 5e. Bacterial viability was quantified for further antimicrobial testing. Nearly complete elimination of the material-treated bacteria (Fig. 6c) was observed. Viability was also quantified using a CFU assay (Figs. 4a, b and 5f, and Additional file 1:Fig. S6) to demonstrate the antibacterial efficiency of the water-soluble C60 (OH)46 in PDT. According to the results in Figs. 4, 5, and 6; Table 2; and Table S2 (Additional file 1), E. coli treated with the water-soluble C60 (OH)46 was susceptible to photoexcitation, leading to a higher death rate, increased ROS generation, and more severe morphological collapse compared with E. coli treated with the water-soluble C60 (OH)21 . In general, the absolute cross section for TPE makes fluorophores efficient for nonlinear microscopic studies because the ratio of the energy absorbed to the input energy flux to a specimen is high, thereby minimizing possible photodamage to specimens [39, 40]. When two-photon techniques are used to image molecular activities in living biological preparations and turbid tissues, a favorable cross section is desirable [61]. In the present study, the absolute cross section for TPE calculated for the water-soluble C60 (OH)46 was approximately 1037 GM (Goeppert-Mayer unit, with 1 GM =10 −50 cm 4 s photon −1 ) at a 760-nm excitation wavelength (fluorescein was the standard reference for the cross section [39, 40]; Fig. 1b and Tables 1 and 3); the absolute cross section calculated for the water-soluble C60 (OH)21 was approximately 1230 GM, which is similar to values obtained in relevant studies [62, 63]. These absolute cross sections could facilitate the two-photon process. Moreover, the fluorescence of the water-soluble C60 (OH)46 was illuminated through a two-photon process (Fig. 1b). The relative fluorescence QY was approximately 0.02 (the QY of Cy5.5 in dimethyl sulfoxide [31] served as a reference:QYref =0.28); similarly, the absolute QY [64] was approximately 0.01, and the same QYs were derived for one-photon excitation and TPE [31]. By contrast, the water-soluble C60 (OH)21 had lower relative and absolute QYs (0.06 and 0.05, respectively). In addition, this study investigated the lifetime of the fullerenols. The effects of radiative and nonradiative decay rates on QY and lifetime were calculated. The average lifetime of the water-soluble C60 (OH)46 was approximately 7.797 ns, as calculated from observed lifetimes of 0.149, 1.775, and 19.679 ns; the average lifetime of the water-soluble C60 (OH)21 was approximately 5.251 ns (Fig. 7 and Table 4). Therefore, the ratio of radiative to nonradiative decay rates of the water-soluble C60 (OH)46 was approximately0.020 (derived from rates of approximately 2.565 × 10 6 s −1 to 1.257 × 10 8 s −1 ), whereas that of the water-soluble C60 (OH)21 was approximately 0.064 (approximately 1.143 × 10 7 s −1 and 1.790 × 10 8 s −1 ; Additional file 1:Table S4). This finding is attributable to the existence of a hydroxyl group on the surface of the water-soluble fullerenol, which induced the nonradiative recombination of electron–hole pairs, leading to the inhibition of intrinsic state emission. However, hydroxylgroups at the edge of the water-soluble fullerenol may have a high occupied molecular orbital. This can be attributed to the strong orbital interaction between hydroxyl groups, which could thus increase the efficiency of intersystem crossing (rather than fluorescence generation) and generate numerous nanomaterial triplets with a high composition of hydroxyl groups; therefore, this would result in a high Φ Δ value for the water-soluble fullerenol and induce the fullerenol to react with oxygen according to the Jablonski diagram [65]. Consequently, two-photon PDT can be effectively performed using ultralow energy in an extremely short time, thereby providing an alternative approach to killing malignant species.
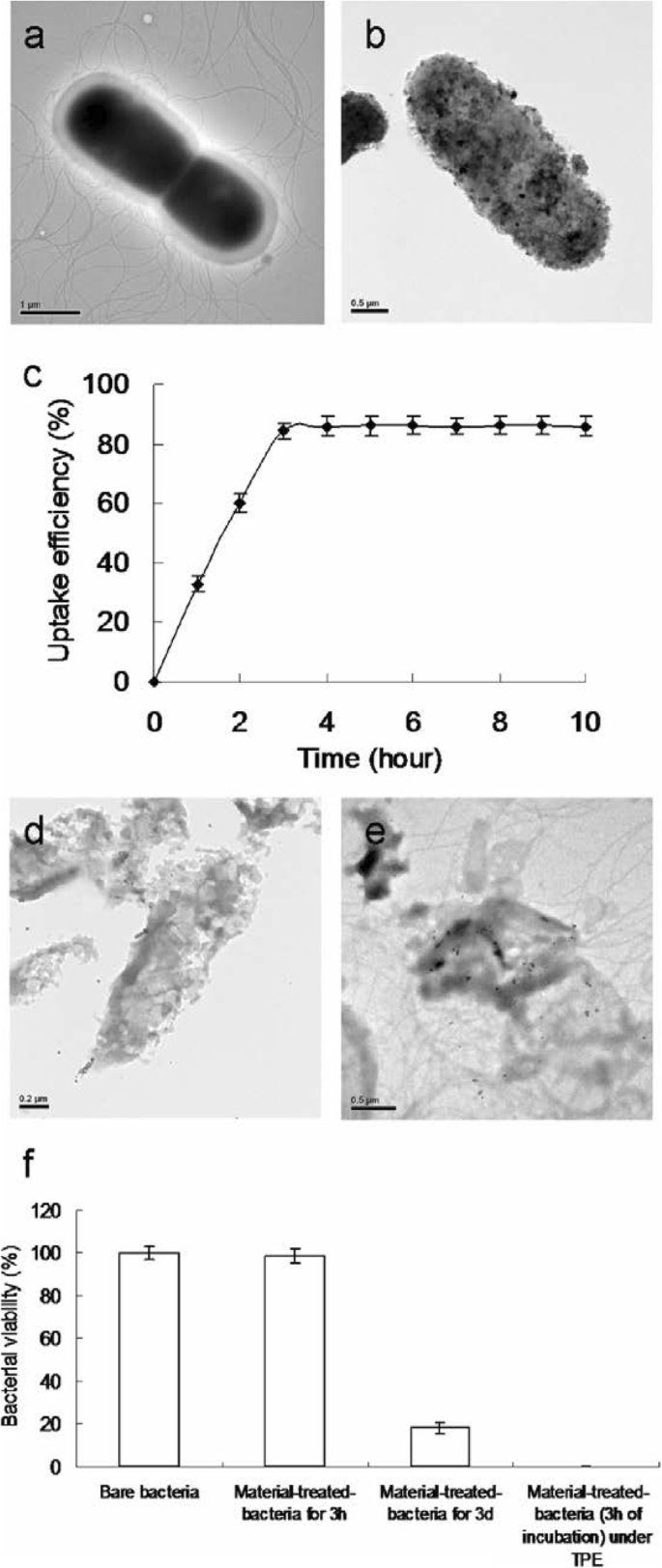
Изображения ПЭМ. а Showing bare bacteria without any treatment. Bacteria treated with material for b 3 h and d 3 days of incubation. е The photoexcited material-treated bacteria (3 h of incubation) with a TPE power of 211.2 nJ pixel −1 with 800 scans (approximately 3.2621 s of total effective exposure time; Ex, 760 nm). c Uptake assay of bacteria and material at 37 °C. е Viability (%) was quantified following the determined viable count of material-treated bacteria via CFU assay by short excitation with the same treatment. Delivered dose OD600 ~ 0.05 of E. coli and 3 μg mL −1 water-soluble fullerenol C60 (OH)46 . Data are means ± SD (n =6)

Images obtained after laser photoexcitation exposure (211.2 nJ pixel −1 ) with 800 scans (approximately 3.2621 s of total effective exposure time; Ex, 760 nm) of a , b material-treated bacteria. The Live/Dead kit was used to stain bacteria before images were obtained. Scale bar, 50 μm. c Viability (%) determination results. Delivered dose, OD600 ~ 0.05 of E. coli and 3 μg mL −1 water-soluble fullerenol C60 (OH)46 . For the percentages alive and dead, p <0.001. * p value obtained using Student’s t контрольная работа. Data are presented as mean ± SD (n =6)
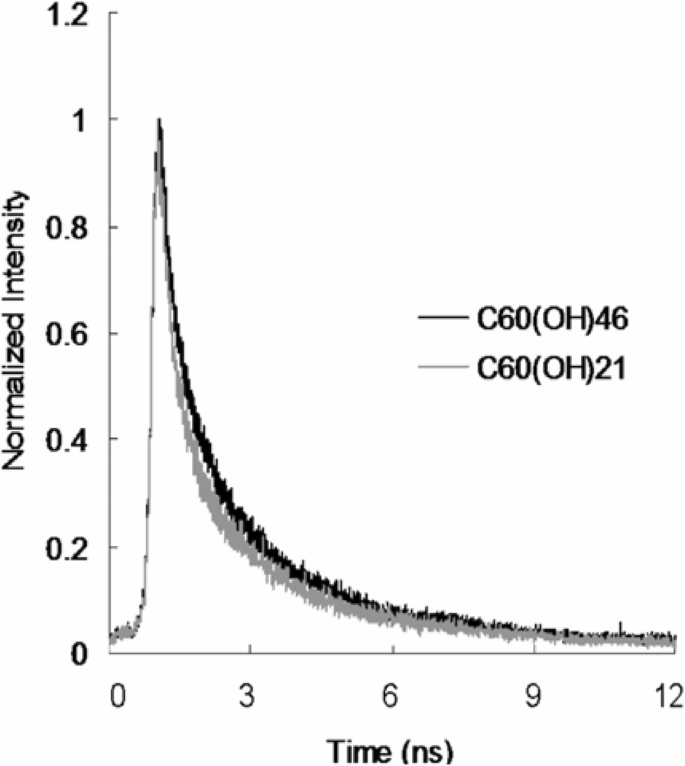
Time-resolved room-temperature PL decay profiles of material (98.56 nJ pixel −1 ). Excitation wavelength, 760 nm. Delivered dose, OD600 ~ 0.05 of E. coli and 3 μg mL −1 материалы. Data are presented as means ± SD (n =6)
Conclusions
This study revealed that a water-soluble fullerenol material with a higher composition of hydroxyl groups had superior photoproperties to those of a fullerenol material with a lower composition of hydroxyl groups; the superior photoproperties can be attributed to the reduced laser exposure and materials used for treatment. Furthermore, the water-soluble fullerenol with a higher composition of hydroxyl groups exhibited high TPA, a favorable absolute cross section for TPE, and high two-photon stability. Therefore, this fullerenol has potential as a two-photon PS in two-photon PDT coupled with TPE. This property is probably due to the presence of a hydroxyl group on the surface of the water-soluble fullerenol, which caused the nonradiative recombination of electron–hole pairs, leading to the inhibition of intrinsic state emission. Moreover, hydroxyl groups at the edge of the water-soluble fullerenol may have a high occupied molecular orbital; this may be ascribed to the strong orbital interaction between the hydroxyl groups, thereby increasing intersystem crossing (rather than fluorescence generation) efficiency and generating numerous material triplets with a high composition of hydroxyl groups. Therefore, the water-soluble fullerenol would have a high Φ Δ value and react with oxygen according to the Jablonski diagram. Consequently, two-photon PDT can be effectively performed using ultralow energy in an extremely short time. Accordingly, this efficient alternative approach to managing malignant species presents possibilities for future clinical applications.
Доступность данных и материалов
All datasets are presented in the main paper.
Сокращения
- PS:
-
Фотосенсибилизаторы
- КГ:
-
Квантовый выход
- PDT:
-
Фотодинамическая терапия
- UV–vis:
-
Ультрафиолет - видимый
- ROS:
-
Активные формы кислорода
- ψ Δ :
-
Singlet oxygen QY
- NIR:
-
Ближний инфракрасный порт
- TPE:
-
Two-photon excitation
- E. coli :
-
кишечная палочка
- HR-TEM:
-
Просвечивающая электронная микроскопия высокого разрешения
- DLS:
-
Динамическое рассеяние света
- FTIR:
-
Инфракрасное преобразование Фурье
- XPS:
-
Рентгеновская фотоэлектронная спектроскопия
- FD:
-
Field desorption
- CFU:
-
Colony forming unit
- TSPP:
-
Meso -tetra(4-sulfonatophenyl)porphine dihydrochloride
- PL:
-
Фотолюминесценция
- DMSO:
-
Диметилсульфоксид
- OPE:
-
One-photon excitation
- TPA:
-
Two-photon absorption
- TPL:
-
Two-photon luminescence
- ti-sa:
-
Titanium-sapphire
- NA :
-
Числовая апертура
- FLIM:
-
Fluorescence lifetime imaging microscopy
- 1 О 2 :
-
Singlet oxygen
- SOSG:
-
Singlet Oxygen Sensor Green
- t -MVP:
-
Trans-1-(2′-methoxyvinyl)pyrene
- O 2 . - :
-
Superoxide radical anion
- XTT:
-
2, 3-Bis (2-methoxy-4-nitro-5-sulfophenyl)-2H-tetrazolium-5-carboxanilide
- GSH:
-
Glutathione, γ -l-glutamyl-l-cysteinyl-glycine
- S1 :
-
Singlet
- T1 :
-
Triplet
- B. subtilis :
-
Bacillus subtilis
- GM:
-
Goeppert-Mayer
Наноматериалы
- MoS2 с контролируемой толщиной для электрокаталитического выделения водорода
- Композиты с квантовыми точками на S, N-графене / TiO2 для эффективного фотокаталитического производства водород…
- Электроспряденные полимерные нановолокна, украшенные наночастицами благородных металлов для определения х…
- Монодисперсные углеродные наносферы с иерархической пористой структурой в качестве материала электродов дл…
- Исследование каркаса Zr – металл – органика как эффективного фотокатализатора для производства водорода
- Иерархическая гетероструктура полых сфер ZnO @ TiO2 для высокоэффективного фотокаталитического выделения водор…
- Эффективный и действенный дизайн нанопроволок InP для максимального сбора солнечной энергии
- Нанокристалл Sb2O3, легированный S:эффективный катализатор в видимом свете для разложения органических веществ
- Fox Chase сотрудничает с Rodon Group в разработке мазка для тестирования на COVID для здоровья храма
- Volvo Group сотрудничает с Nvidia в разработке платформы искусственного интеллекта для автономных грузовиков



