Фотофентоновая деградация AO7 и фотокаталитическое восстановление Cr (VI) над наночастицами BiFeO3, декорированными CQD, под воздействием видимого и ближнего инфракрасного света
Аннотация
В этой работе углеродная квантовая точка (ККТ) - украшенная BiFeO 3 Фотокатализаторы из наночастиц были приготовлены гидротермальным методом. Наблюдение с помощью просвечивающего электронного микроскопа и определение характеристик методом XPS показывают, что CQD хорошо закреплены на поверхности BiFeO 3 наночастицы. Кислотный оранжевый 7 (AO7) и шестивалентный хром (Cr (VI)) были выбраны в качестве модельных загрязнителей для исследования характеристик фотокаталитического / фото-фентонового разложения и фотокаталитического восстановления готовых CQD / BiFeO 3 композиты под воздействием видимого и ближнего инфракрасного (NIR) света. По сравнению с голым BiFeO 3 наночастицы, CQD / BiFeO 3 композиты демонстрируют значительно улучшенную фотокаталитическую и фото-каталитическую активность Фентона. Кроме того, композиты обладают хорошей каталитической стабильностью. Эффективное разделение фотогенерированных зарядов в композитах было продемонстрировано измерениями отклика фототока и спектроскопии электрохимического импеданса (EIS). Основные активные частицы, участвующие в реакции каталитического разложения, были выяснены с помощью экспериментов по улавливанию и обнаружению радикалов. Основные фотокаталитические и фото-фентоновые механизмы систематически исследуются и обсуждаются.
Фон
В последние десятилетия сточные воды, содержащие ионы тяжелых металлов и органические соединения, наносят серьезный ущерб окружающей среде и людям. Как один из распространенных ионов тяжелых металлов, шестивалентный хром (Cr (VI)), получаемый при гальванике, дублении кожи и печати, представляет серьезную угрозу для нашего здоровья из-за своей высокой токсичности [1]. С другой стороны, большинство органических загрязнителей (таких как красители) также токсичны и не поддаются биологическому разложению, что разрушает нашу среду обитания [2]. До настоящего времени было разработано множество методов удаления органических загрязнителей и восстановления Cr (VI) до Cr (III) [3,4,5]. Среди этих методов фотокаталитические и фото-фентоноподобные каталитические методы считаются многообещающими методами эффективного разложения органических загрязнителей и снижения содержания Cr (VI) в сточных водах из-за их недорогой стоимости, неселективности и простоты эксплуатации [6 , 7,8,9]. Основные этапы процесса фотокаталитического разложения можно описать следующим образом:возбуждение фотокатализаторов, разделение и миграция фотогенерированных зарядов, образование активных частиц на поверхности катализаторов и разложение органического соединения, а также восстановление Cr (VI ), вызванные окислительно-восстановительной реакцией активных частиц и фотоиндуцированными зарядами [10, 11]. Каталитическая реакция, подобная фото-Фентону, основана на синергетическом эффекте реакции Фентона и фотокаталитического процесса. Генерация активных частиц в процессе реакции Фентона может быть ускорена после введения подходящего светового излучения, что приводит к улучшенной каталитической активности [12, 13]. Однако широкое применение фотокаталитических и фото-фентоноподобных каталитических методов ограничено из-за большой ширины запрещенной зоны фотокатализаторов, реагирующих только на УФ-свет (который составляет ~ 5% энергии солнечного света), и их низкой эффективности разделения заряда [14]. В целом известно, что видимый свет и ближний инфракрасный (NIR) свет занимают ~ 45% и ~ 46% солнечной энергии соответственно, и их применение вызвало большой интерес [15, 16]. В результате разработка активных катализаторов широкого спектра (УФ- и БИК) с эффективным разделением фотогенерированных зарядов очень важна для их практического применения [17,18,19,20]. До сих пор железосодержащие катализаторы с узкой запрещенной зоной рассматриваются как идеальные кандидаты для фотокаталитических и фото-фентоноподобных каталитических применений [21,22,23,24,25].
В качестве одного из типичных железосодержащих катализаторов BiFeO 3 со структурой типа перовскита, как известно, представляет собой интересный фотокаталитический материал, управляемый видимым светом, и фото-фентоноподобный каталитический материал для разложения красителей [26,27,28,29,30,31,32,33,34]. Тем не менее, его каталитическая активность не настолько высока для удовлетворения требований применения из-за высокой скорости рекомбинации фотогенерированных зарядов. Более того, световой диапазон BiFeO 3 необходимо расширить до ближней инфракрасной области света для эффективного использования солнечной энергии. Поэтому для преодоления этих недостатков использовалось множество стратегий [35,36,37,38,39,40].
Углеродные квантовые точки (ККТ), являясь важным классом нульмерных наноуглеродных материалов, привлекли значительное внимание благодаря своим отличительным свойствам, таким как большая площадь поверхности, низкая токсичность, высокая биосовместимость, хорошая растворимость в воде, высокая химическая стабильность, хорошие электрические характеристики. проводимость и прекрасные оптические свойства [41,42,43,44]. Эти выдающиеся свойства делают его многообещающим кандидатом для практического применения в различных областях [41,42,43,44]. Что еще более важно, фотовозбужденные ККТ являются отличными донорами и акцепторами электронов, способствующими разделению фотогенерированных зарядов в фотокатализаторах [45]. С другой стороны, было обнаружено, что CQD представляют собой уникальный фотолюминесцентный материал с повышающим преобразованием, который позволяет генерировать коротковолновый эмиссионный свет (от 450 до 750 нм) путем возбуждения длинноволнового света (ближний инфракрасный свет, от 700 до 750 нм). 1000 нм) [42, 44]. Эмиссионный свет с повышенным преобразованием может использоваться в качестве возбуждающего света для производства фотогенерированных зарядов в полупроводниках, что расширяет область их светового отклика [45]. В результате показано, что включение CQD с фотокатализаторами является многообещающим способом создания превосходных гибридных композитных фотокатализаторов [46,47,48,49,50,51,52]. Chen et al. подготовил CQD / BiFeO 3 нанокомпозитов и обнаружили их повышенную фотокаталитическую активность в видимом свете для разложения красителя [53]. Однако, насколько нам известно, нет работ, посвященных деградации фото-фентонового красителя и фотокаталитическому восстановлению Cr (VI) CQD / BiFeO 3 композитные фотокатализаторы при облучении видимым или ближним инфракрасным светом.
В этой работе CQD / BiFeO 3 Композитные фотокатализаторы были приготовлены гидротермальным способом. Их фотокаталитические и фото-фентоноподобные каталитические свойства для разложения кислотного оранжевого 7 (AO7), а также фотокаталитическая активность по восстановлению Cr (VI) при облучении видимым и ближним инфракрасным светом были систематически исследованы. Предложен соответствующий каталитический механизм.
Методы
Подготовка CQD
ККТ были приготовлены гидротермальным методом [54]. Глюкозу (1 г) добавляли в дистиллированную воду (80 мл) при перемешивании магнитной мешалкой и ультразвуковой обработке до получения гомогенного раствора. Затем этот раствор переносили в автоклав из нержавеющей стали с тефлоновым покрытием объемом 100 мл и нагревали при 180 ° C в течение 4 часов. После реакции полученный раствор дважды фильтровали через фильтровальную бумагу, а затем получали красновато-коричневую суспензию CQD.
Изготовление CQD / BiFeO 3 Композиты
BiFeO 3 наночастицы были получены с использованием полиакриламидного геля, как описано в литературе [55]. CQD / BiFeO 3 композиты были изготовлены следующим образом (рис. 1):BiFeO 3 Наночастицы (0,1 г) вводили в дистиллированную воду (70 мл) с последующей обработкой ультразвуком в течение 0,5 ч до получения однородной суспензии. После этого в BiFeO 3 по каплям добавляли определенное количество суспензии CQD. суспензия при магнитном перемешивании. Смесь перемещали в автоклав из нержавеющей стали с тефлоновым покрытием (100 мл) и нагревали при 130 ° C в течение 4 часов. Наконец, продукт собирали центрифугированием, промывали деионизированной водой и сушили при 60 ° C в течение 8 часов. Чтобы изучить влияние содержания CQD на каталитические активные компоненты композитов, серия CQD / BiFeO 3 композиты с разным массовым содержанием ККТ были приготовлены путем добавления различных объемов суспензии ККТ (3, 6, 12 и 24 мл). Эти композиты получили названия 3C / BFO, 6C / BFO, 12C / BFO и 24C / BFO.
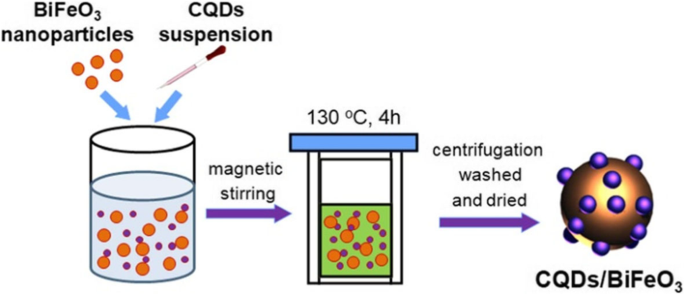
Схематическое изображение процесса подготовки CQD / BiFeO 3 составной
Каталитическое и фотокаталитическое разложение красителя на основе фотофентона
Каталитические характеристики фотофентона исходного CQD / BiFeO 3 композиты исследовали в отношении разложения AO7, отдельно облучаемого видимым светом (ксеноновая лампа мощностью 300 Вт с фильтром отсечки 420 нм) и ближним ИК-светом (ксеноновая лампа мощностью 300 Вт с фильтром отсечки 800 нм). В типичном эксперименте фотокатализатор (0,1 г) помещали в раствор AO7 (200 мл, 5 мг / л) и перемешивали с помощью магнитной мешалки в темноте в течение 0,5 ч для достижения адсорбционно-десорбционного равновесия между фотокатализатором и молекулами AO7. Впоследствии определенное количество H 2 О 2 раствор добавляли в суспензию и включали ксеноновую лампу для начала каталитической реакции. В каталитическом процессе отбирали небольшое количество реакционного раствора (2 мл) и центрифугировали для удаления катализатора. Оптическую плотность супернатанта измеряли спектрофотометром УФ-видимой области при 484 нм для определения концентрации АО7. С другой стороны, фотокаталитическое разложение AO7 на образцах было выполнено для оценки их фотокаталитической активности в тех же условиях в отсутствие H 2 О 2 .
Каталитические эксперименты по рециркуляции были проведены для проверки каталитической возможности повторного использования образцов. После первого каталитического эксперимента катализатор отделяли от раствора центрифугированием, промывали деионизированной водой и сушили. Собранный катализатор добавляли в новый раствор красителя для следующей каталитической реакции в тех же условиях.
Чтобы подтвердить, что реакционноспособные частицы участвуют в процессах фотокаталитического разложения и каталитического разложения фотофентона, эксперименты по улавливанию активных частиц были выполнены путем добавления нескольких поглотителей в тех же условиях, что и упомянутые выше. Этанол (10% по объему) и оксалат аммония (AO, 2 мМ) использовали в качестве поглотителей гидроксила (· OH) и фотогенерированных дырок (h + ) соответственно [56]. N 2 продувка может удалить растворенный O 2 в растворе, что приводит к ингибированию супероксида (· O 2 - ) поколения.
Фотокаталитическое восстановление Cr (VI)
Cr (VI) был использован в качестве другого модельного загрязнителя для измерения фотокаталитической активности образцов. Процесс фотокаталитического восстановления Cr (VI) до Cr (III) был аналогичен процессу разложения красителя. Начальная концентрация Cr (VI) составляла 10 мг / л, а дозировка фотокатализатора составляла 0,2 г в 200 мл раствора Cr (VI) (т.е. 1 г / л). Начальное значение pH раствора Cr (VI) регулировали с помощью H 2 . SO 4 до 2 ~ 3. Остаточная концентрация раствора Cr (VI) определялась УФ-видимым спектрофотометром с использованием метода дифенилкарбазида (DPC) [57].
Обнаружение гидроксильных радикалов
Флуориметрию использовали для обнаружения радикалов · ОН, образующихся на облученных образцах, с использованием терефталевой кислоты (ТА) в качестве молекулы зонда. Обычно · OH будет реагировать с TA с образованием сильно флуоресцентного соединения, 2-гидрокситерефталевой кислоты (TAOH). Информация о · OH может быть обнаружена путем измерения интенсивности фотолюминесценции (ФЛ) TAOH с длиной волны возбуждения ~ 315 нм. Обычно ТА вводили в раствор NaOH (1,0 ммоль л -1 ) для получения раствора ТА (0,25 ммоль л -1 ). Катализатор (60 мг) помещали в раствор ТА (100 мл) при перемешивании магнитной мешалкой в течение нескольких минут. После этого определенное количество H 2 О 2 растворяли в указанной выше смеси, которую облучали видимым светом (ксеноновая лампа 300 Вт с фильтром отсечки 420 нм) или ближним ИК-светом (ксеноновая лампа 300 Вт с фильтром отсечки 800 нм). Через заданные интервалы облучения отбирали 3 мл реакционного раствора и центрифугировали для удаления катализатора. Спектры ФЛ супернатанта определяли на флуоресцентном спектрофотометре. С другой стороны, образование · OH в фотокаталитической реакции также измеряли в тех же условиях без добавления H 2 О 2 .
Характеристика
Фазовую чистоту образцов исследовали с помощью порошковой рентгеновской дифракции (XRD) и инфракрасной спектроскопии с преобразованием Фурье (FTIR). Морфологию и микроструктуру образцов наблюдали с помощью автоэмиссионной просвечивающей электронной микроскопии (ПЭМ). Химическое состояние элементов поверхности на образцах было обнаружено с помощью рентгеновской фотоэлектронной спектроскопии (XPS). Спектры диффузного отражения образцов в ультрафиолетовой и видимой области (УФ-видимая область) регистрировали с помощью двухлучевого УФ-видимого спектрофотометра TU-1901. Спектры ФЛ образцов определяли на флуоресцентном спектрофотометре. Измерения нестационарного фототока и спектроскопии электрохимического импеданса (EIS) проводили на электрохимической рабочей станции с трехэлектродной системой. Изготовление рабочего электрода и процедуры испытаний были аналогичны описанным ранее [56]. В частности, измерение отклика фототока проводилось при облучении видимым светом (ксеноновая лампа мощностью 300 Вт с фильтром отсечки 420 нм).
Результаты и обсуждение
XRD-анализ
На рисунке 2 представлены дифрактограммы BiFeO 3 . , CQD и 24C / BFO. BiFeO 3 и образец 24C / BFO демонстрируют аналогичные дифракционные картины, которые можно легко проиндексировать как ромбоэдрический BiFeO 3 этап (номер файла JCPD:74-2016). Никаких следов примесей, таких как Fe 2 О 3 и Bi 2 О 3, находится. Результаты показывают, что BiFeO 3 высокой чистоты получено, и введение УКТ и гидротермальная обработка явно не меняют кристаллическую структуру BiFeO 3 . Из рентгенограммы ККТ видно, что широкий дифракционный пик наблюдается при ~ 23,5 °, что в основном объясняется аморфной структурой ККТ. Примечательно, что для композита не обнаруживаются характерные дифракционные пики CQD из-за низкого содержания CQD в образце 24C / BFO. Чтобы подтвердить наличие CQD в композите, выполняется характеристика FTIR.
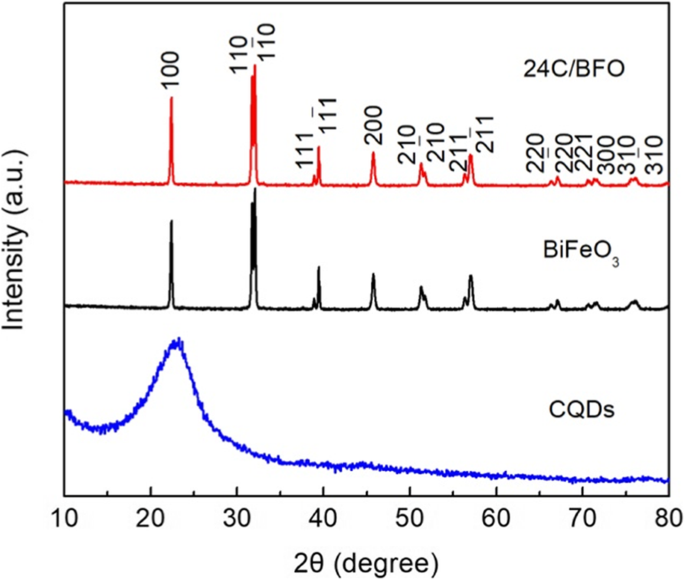
Рентгенограммы BiFeO 3 , CQD и композиты 24C / BFO
Анализ FTIR
На рисунке 3 показаны ИК-Фурье-спектры BiFeO 3, . Композиты CQD и 12C / BFO. В случае голого BiFeO 3 пики на ~ 440 см −1 и ~ 560 см −1 относятся к валентным и деформационным колебаниям Fe – O, что согласуется с опубликованным результатом [55]. Для ККТ деформационное колебание для C – H при ~ 638 см −1 , валентное колебание для C – C при ~ 1630 см −1 , и растяжение C – OH на ~ 1120 см −1 найдены [58]. Кроме того, характерные пики BiFeO 3 и CQD обнаруживаются в спектре композита 12C / BFO. Результаты предполагают существование CQD и BiFeO 3 в композите. Причем пик, расположенный на ~ 1380 см −1 объясняется валентным колебанием O – H от поглощенного H 2 O [59].
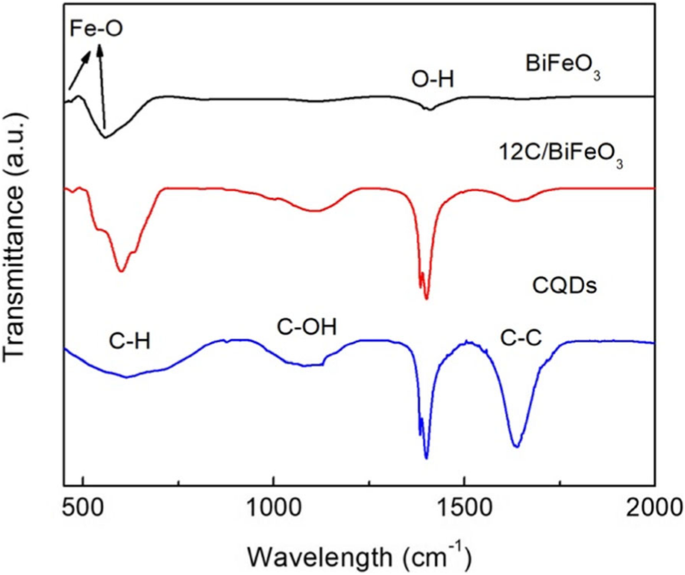
ИК-Фурье спектры BiFeO 3 , CQD и композиты 12C / BFO
Свойство оптического поглощения
Хорошо известно, что свойство оптического поглощения наноматериалов оказывает важное влияние на их характеристики [60, 61]. Свойство оптического поглощения BiFeO 3 , CQD и CQD / BiFeO 3 композиты были исследованы по спектрам диффузного отражения в УФ-видимой области, как показано на рис. 4а. По сравнению с BiFeO 3 , CQD / BiFeO 3 композиты демонстрируют явно повышенную оптическую абсорбционную способность во всем диапазоне УФ-видимого света. Следует отметить, что интенсивность оптического поглощения композитов постепенно увеличивается с увеличением содержания УКТ. Это явление можно объяснить сильным поглощением света УКТ в УФ-видимой области. Чтобы получить край поглощения света образцами, строят кривые первой производной спектров диффузного отражения в УФ-видимой области (рис. 4b), на которых длина волны пика считается границей поглощения образцов [62]. Обнаружено, что края поглощения BiFeO 3 и CQD / BiFeO 3 композиты расположены на длине волны ~ 588 нм, что позволяет предположить, что декорирование ККТ не изменяет ширину запрещенной зоны BiFeO 3 .
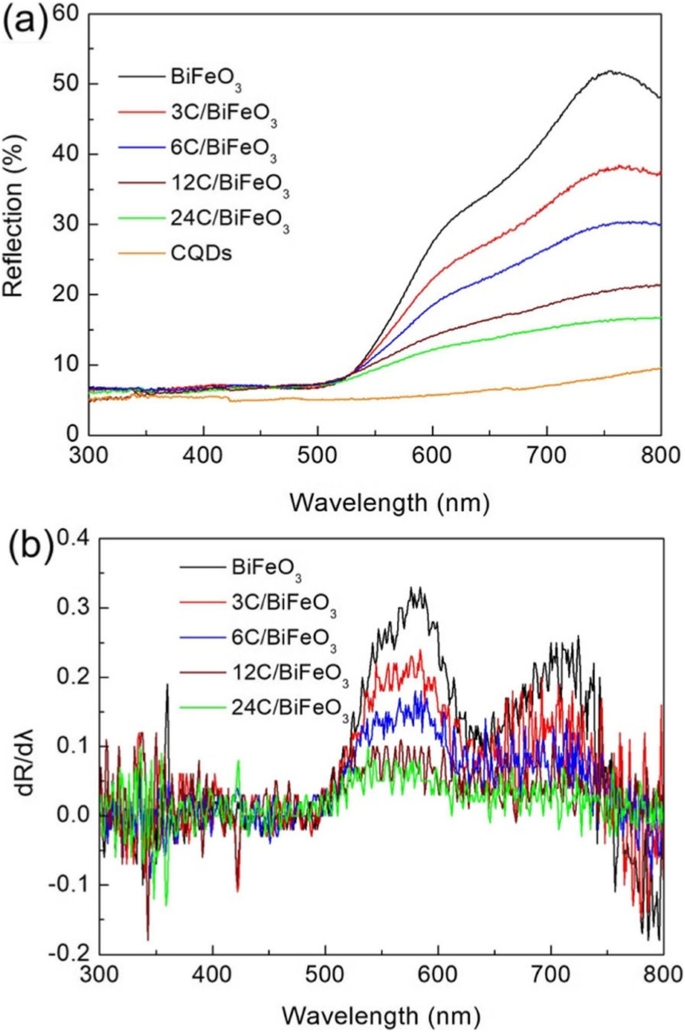
а УФ-видимые спектры диффузного отражения BiFeO 3 , CQD и CQD / BiFeO 3 композиты. б Соответствующая первая производная спектров диффузного отражения
Анализ XPS
Химическое состояние элементов в образце 12C / BFO контролировали с помощью XPS, и результаты представлены на рис. 5. На спектре Bi 4f XPS (рис. 5a) наблюдались два сильных пика при 164,1 (Bi 4f 5/2 ) и 158,8 эВ (Bi 4f 7/2 ) демонстрируют существование Bi 3+ в композиции [63]. На рис. 5b XPS-спектр Fe 2p показывает два очевидных пика при 723,6 и 709,6 эВ, которые приписываются Fe 2p 1/2 и Fe 2p 3/2 . Примечательно, что широкий пик Fe 2p 3/2 можно разделить на два пика при 712,0 и 709,6 эВ, соответствующих Fe 3+ и Fe 2+ соответственно [40]. Кроме того, видно, что сателлитный пик Fe 2p 3/2 находится при 717,8 эВ. Как показано на XPS-спектре O 1s (рис. 5c), очевидный пик, расположенный при 529,6 эВ, приписывается решеточному кислороду, а плечевой пик при 531,3 эВ принадлежит хемосорбированному кислороду поверхностных вакансий [64]. Для XPS-спектра C 1s (рис. 5d) сигнал C 1s можно разделить на два отдельных пика. Основной пик при ~ 284,9 эВ приписывается связи C – C с sp 2 орбиталь, тогда как пик при 287,7 эВ вызван кислородсодержащим углеродом. Результаты дополнительно демонстрируют сосуществование CQD и BiFeO 3 в композите [65].
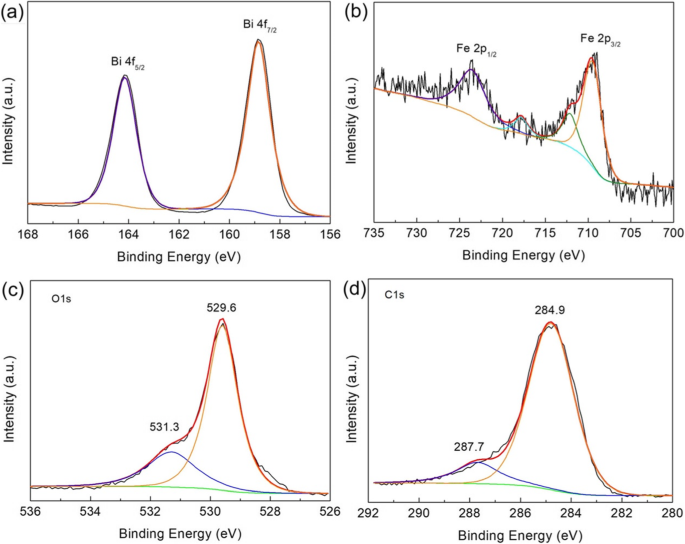
Спектры XPS высокого разрешения a Bi 4f, b Fe 2p, c O 1s и d C 1 для композита 12C / BFO
Наблюдение за морфологией
Изображения BiFeO 3 ПЭМ и ПЭМ высокого разрешения (ВРТЭМ) наночастицы показаны на рис. 6а и б соответственно. Видно, что голый BiFeO 3 имеет сферическую форму и гладкую поверхность со средним диаметром ~ 120 нм. Шаг решетки 0,288 нм принадлежит к шагу (110) BiFeO 3 . Изображение ПЭМ на рис. 6с показывает, что ККТ состоят из сферических частиц со средним размером частиц ~ 15 нм. Из изображения TEM CQD / BiFeO 3 композитов (рис. 6г – ж) видно, что УКТ декорированы на поверхности BiFeO 3 наночастицы. Изображение ВРЭМ 12C / BiFeO 3 образец (рис. 6h) показывает межплоскостное расстояние 0,389 нм, соответствующее плоскости (012) BiFeO 3 . Наряду с BiFeO 3 , декорированные ККТ обладают аморфной характеристикой. Этот результат предполагает образование гибридной композитной структуры между BiFeO 3 и CQD.

а и b ПЭМ и ВРТЭМ изображения чистого BiFeO 3 наночастицы соответственно; c ТЕМ изображение CQD; г - г ПЭМ-изображения 3C / BFO, 6C / BFO, 12C / BFO и 24C / BFO соответственно; ч ВРЭМ изображение 12C / BFO
Сканирующее темнопольное изображение с помощью просвечивающего электронного микроскопа (DF-STEM) и соответствующие сопоставления элементов образца 12C / BFO показаны на рис. 7a – e, соответственно. Результаты показывают, что образец представляет не только однородное распределение элементов Bi / Fe / O, но также равномерное распределение элемента C. Это подтверждает, что ККТ равномерно собраны на поверхности BiFeO 3 наночастицы.
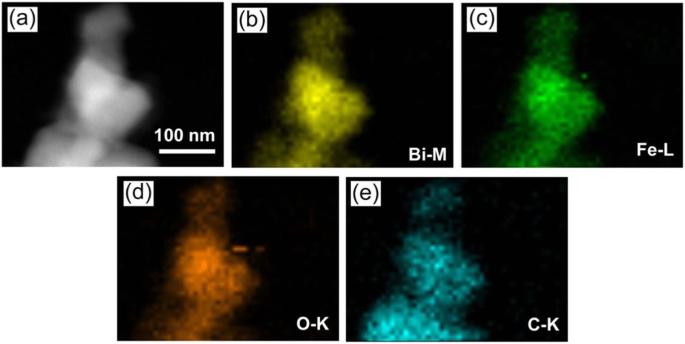
а DF-STEM изображение композита 12C / BFO. б - е Соответствующие энергодисперсионные рентгеновские элементарные изображения
Каталитические и фотокаталитические характеристики Фото-Фентона
Фотокаталитические характеристики образцов сначала оценивали по разложению AO7 под воздействием видимого света, и результат показан на рис. 8а. Перед фотокаталитической реакцией проводили адсорбционный (в темноте) и холостой (без катализатора) эксперименты. Небольшое количество AO7 (~ 5%) разлагается после 3-часового облучения без катализатора, что указывает на то, что саморазложением красителя можно пренебречь. В фотокаталитической реакции способность чистого BiFeO 3 к фотодеградации является слабым, и только ~ 33% AO7 разлагается после 3-часовой выдержки. Когда BiFeO 3 наночастицы декорированы CQD, CQD / BiFeO 3 композиты проявляют явно повышенную фотокаталитическую активность. Более того, обнаружено, что каталитическая активность композитов сильно зависит от содержания CQD. Среди этих композитов 12C / BiFeO 3 композит показывает оптимальный процент деградации ~ 73% после 3-часового облучения, что в 2,2 раза выше, чем у чистого BiFeO 3 . Однако при дальнейшем увеличении содержания CQD (например, 24C / BFO) избыточные CQD, декорированные на поверхности BiFeO 3 наночастицы могут защищать BiFeO 3 от поглощения видимого света, что приводит к снижению фотокаталитической активности.
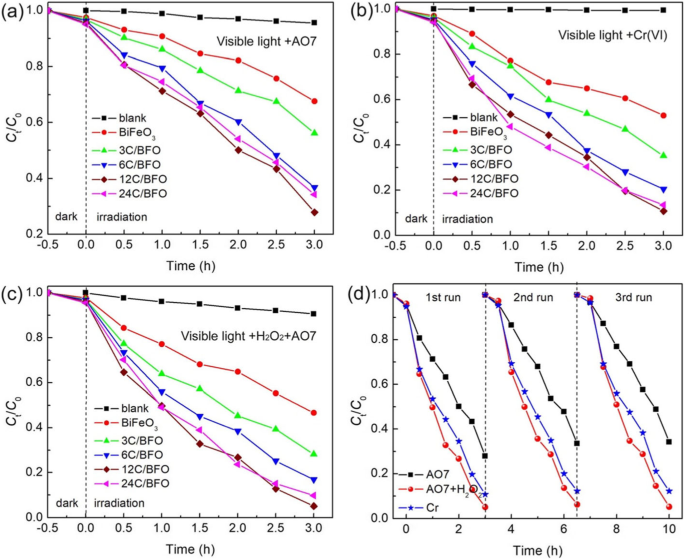
а Фотокаталитическая деструкция AO7, b фотокаталитическое восстановление Cr (VI) и c фото-Фентоновское каталитическое разложение AO7 над BiFeO 3 и CQD / BiFeO 3 композиты при облучении видимым светом. г Возможность вторичного использования композита 12C / BFO для фотокаталитического разложения AO7, фотокаталитического восстановления Cr (VI) и каталитического разложения AO7 фотофентоном под облучением видимым светом
В этой работе также изучалась фотокаталитическая способность образцов к восстановлению Cr (VI) при облучении видимым светом, как показано на рис. 8b. Холостой эксперимент показывает, что восстановление Cr (VI) после 3-часового освещения в отсутствие катализаторов незначительно. Видно, что CQD / BiFeO 3 композиты обладают гораздо более высокой способностью к фотокаталитическому восстановлению, чем чистый BiFeO 3 . Эффективность восстановления Cr (VI) по образцам увеличивается в следующем порядке:BiFeO 3 <3C / BFO <6C / BFO <24C / BFO <12C / BFO. Результат демонстрирует свойство фотокаталитического восстановления BiFeO 3, под действием видимого света. что, очевидно, может быть улучшено декорированием CQD.
Помимо фотокаталитической активности, показано, что BiFeO 3 также демонстрирует многообещающую способность к фотофентоноподобному катализу. На рисунке 8c показано фото-фентоновское разложение AO7 над образцами при облучении видимым светом с добавлением H 2 . О 2 , из которого видно, что процент разложения AO7 в фото-фентоноподобном каталитическом процессе намного выше, чем в голой фотокаталитической реакции. Например, около 96% AO7 представляет собой фото-фентон, каталитически разложенный на образце 12C / BFO при 3-часовом облучении, что дает ~ 23% улучшение по сравнению с фотокаталитическим разложением AO7 (~ 73%). Кроме того, установлено, что каталитическая активность фото-Фентона между образцами имеет такой же порядок, как и фотокаталитическая активность между образцами. Это говорит о том, что CQD / BiFeO 3 композиты могут быть использованы в качестве эффективных фото-катализаторов Фентона для разложения красителей.
Как правило, возможность повторного использования катализаторов рассматривается как важный параметр для их практического применения. Согласно приведенным выше каталитическим результатам, образец 12C / BFO был выбран в качестве катализатора для исследования фотокаталитической и фото-каталитической стабильности Фентона. На рис. 8d представлена каталитическая активность образца 12C / BFO во время трех последовательных фотокаталитических процессов и фото-каталитических процессов Фентона под воздействием видимого света. После трех последовательных циклов каталитическая активность образца 12C / BFO не претерпевает явного снижения. Это указывает на то, что CQD / BiFeO 3 композит демонстрирует хорошую каталитическую способность многократного использования при облучении видимым светом.
В этой работе фотокаталитическая и фото-фентоновая каталитическая активность BiFeO 3 , управляемая светом в ближнем инфракрасном диапазоне. и 12C / BFO. На рисунках 9a – c показано зависящее от времени фотокаталитическое разложение AO7, фотокаталитическое восстановление Cr (VI) и каталитическое разложение AO7 фотофентоном над BiFeO 3 и 12C / BiFeO 3 при облучении ближним инфракрасным светом соответственно. Видно, что голый BiFeO 3 почти не проявляет фотокаталитической активности в ближнем ИК-диапазоне, потому что не может реагировать на ближний ИК-свет, в то время как около 22% AO7 разлагается BiFeO 3 во время фото-каталитической реакции Фентона. Напротив, образец 12C / BFO демонстрирует очевидную каталитическую активность, управляемую светом в ближнем ИК-диапазоне. После 3-часового облучения БИК-светом фотокаталитическая деградация AO7, фотокаталитическое восстановление Cr (VI) и фото-фентоновая деградация AO7 на образце 12C / BFO достигают ~ 35%, ~ 63% и ~ 49% соответственно. . Результат показывает, что введение УКТ на поверхность BiFeO 3 играет важную роль в усилении его каталитической активности, управляемой светом в ближнем инфракрасном диапазоне. Каталитическая стабильность образца 12C / BFO для света в ближнем инфракрасном диапазоне также была изучена с помощью каталитических экспериментов по рециркуляции, как показано на рис. 9d. Обнаружено, что CQD / BiFeO 3 композит также обладает устойчивой каталитической активностью в ближнем ИК-диапазоне.
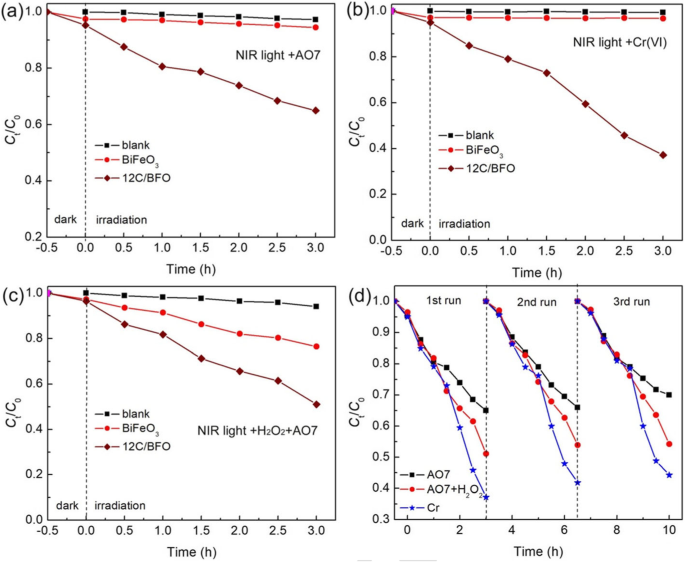
а Фотокаталитическая деструкция AO7, b фотокаталитическое восстановление Cr (VI) и c фото-Фентоновское каталитическое разложение AO7 над BiFeO 3 и CQD / BiFeO 3 композиты под действием ближнего инфракрасного излучения. г Возможность вторичного использования композита 12C / BFO для фотокаталитического разложения AO7, фотокаталитического восстановления Cr (VI) и каталитического разложения AO7 фото-Фентоном под облучением NIR светом
Отлов активных видов
Чтобы изучить влияние активных частиц на реакцию каталитического разложения, были проведены эксперименты по улавливанию активных частиц. На рис. 10а и б показано фотокаталитическое и фотофентоновское каталитическое разложение AO7 с использованием образца 12C / BFO с добавлением гасителей при освещении видимым светом, соответственно. Из рис. 10а видно, что введение этанола и АО приводит к относительно небольшому ингибированию разложения АО7. Напротив, фотокаталитическое разложение AO7 резко подавляется с помощью N 2 продувка. Это говорит о том, что · O 2 - является первичным реактивным веществом, тогда как · OH и h + являются вторичными реактивными частицами, ответственными за разложение красителя. Как показано на фиг. 10b, процент разложения АО7 снижается с 96% (без поглотителей) отдельно до ~ 60% (N 2 продувка), ~ 71% (добавление АО) и ~ 45% (добавление этанола). Это показывает, что · O 2 - , h + , и · OH участвуют в управляемой видимым светом фото-каталитической реакции Фентона, и · OH играет относительно большую роль в этом процессе. На рисунках 10c и d представлены фотокаталитическая и фотофентоновская каталитическая деградация AO7 на образце 12C / BFO в присутствии поглотителей при облучении ближним инфракрасным светом, соответственно. Видно, что в обоих каталитических процессах разложение красителя зависит от · O 2 - , h + , и · ОН. В частности, · O 2 - продемонстрировано, что является основным активным веществом в фотокаталитическом процессе, управляемом светом в ближней инфракрасной области, тогда как · OH играет ключевую роль в каталитической реакции фото-Фентона в ближнем инфракрасном диапазоне.
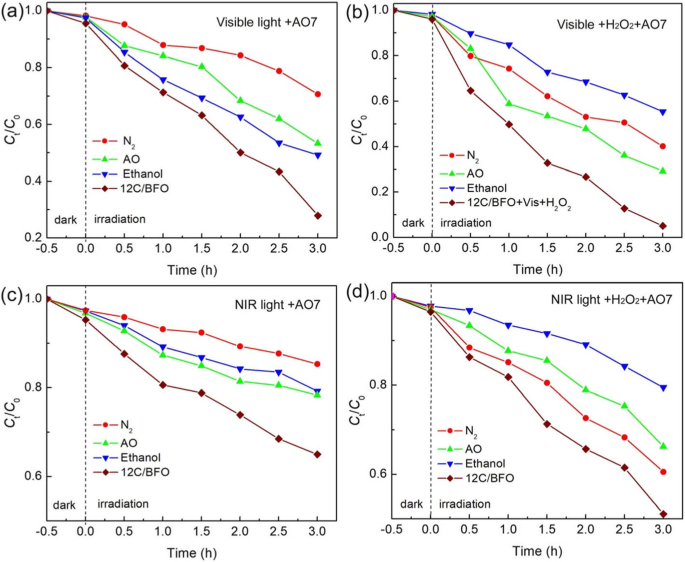
а и b Действие этанола, N 2 продувка и АО на фотокаталитическом и фотофентоновом каталитическом разложении AO7 над 12C / BFO при облучении видимым светом соответственно. c и d Действие этанола, N 2 продувка и АО на фотокаталитическом и фотофентоновом каталитическом разложении AO7 над 12C / BFO при облучении светом в ближней инфракрасной области, соответственно
На рисунке 11 показаны зависящие от времени спектры ФЛ раствора TPA с использованием образца 12C / BFO в качестве катализатора в фотокаталитической и фото-каталитической реакции Фентона при освещении видимым и ближним инфракрасным светом. Видно, что во всех случаях каталитических процессов пик излучения ФЛ, расположенный при ~ 429 нм, постепенно становится интенсивным с увеличением времени освещения, что свидетельствует о генерации радикалов · OH. Основываясь на интенсивности сигнала ФЛ, можно сделать вывод, что в фото-фентоновом процессе образуется больше радикалов · OH, чем в фотокаталитическом процессе, а облучение видимым светом приводит к увеличению генерации радикалов · OH по сравнению с облучением ближним инфракрасным светом. .
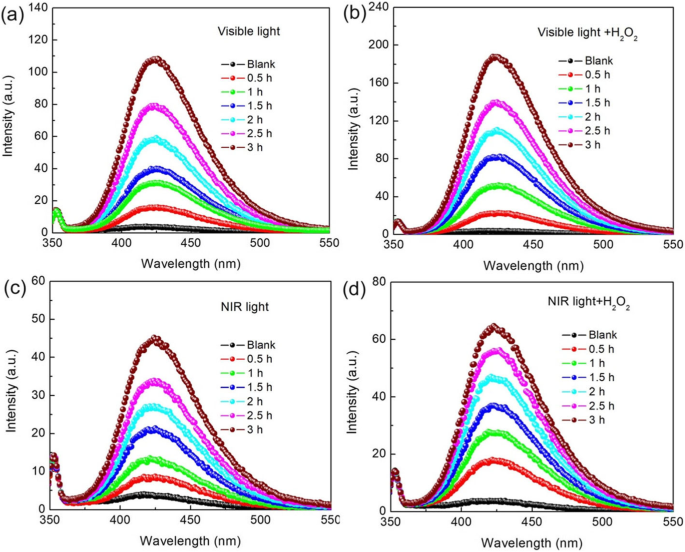
а и b Спектры ФЛ раствора ТА в зависимости от времени облучения видимым светом образца 12C / BFO в фотокаталитических и фото-каталитических реакциях Фентона соответственно. c и d Спектры ФЛ раствора ТА в зависимости от времени облучения светом в ближней инфракрасной области образца 12C / BFO в фотокаталитических и фото-каталитических реакциях Фентона соответственно
Эффективность снятых платежей
Фотоэлектрохимические измерения очень полезны для исследования характеристик миграции и рекомбинации фотогенерированных зарядов. Переходные токи фотоотклика BiFeO 3 и 12C / BFO при облучении видимым светом с несколькими циклами включения / выключения показаны на фиг. 12a. Видно, что плотность фототока 12C / BFO намного выше, чем у чистого BiFeO 3 , что указывает на эффективное разделение фотогенерированных зарядов в ККТ / BiFeO 3 композитный. На рисунке 12b показаны кривые EIS для BiFeO 3 . и 12C / BFO. Хорошо известно, что полукруг на графике Найквиста в высокочастотной области отражает процесс межфазного переноса заряда, а меньший диаметр полукруга означает меньшее сопротивление переноса заряда [66]. Образец 12C / BFO имеет меньший диаметр полукруга по сравнению с чистым BiFeO 3 , предполагая, что миграция фотогенерируемых зарядов может стимулироваться в CQD / BiFeO 3 композиты.
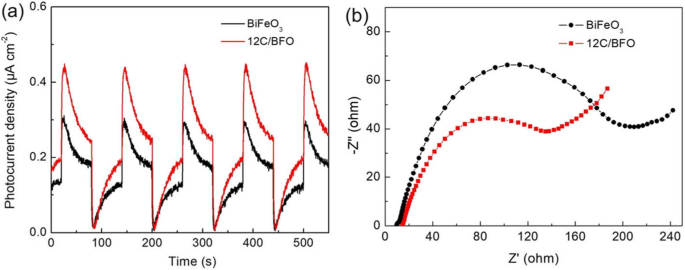
а Графики реакции фототока BiFeO 3 и 12C / BFO при облучении видимым светом. б Спектры ЭИС BiFeO 3 и 12C / BFO
Каталитический механизм
Возможный управляемый видимым светом фотокаталитический механизм CQD / BiFeO 3 для деградации красителя и восстановления Cr (VI) предлагается, как показано на рис. 13a. Когда CQD / BiFeO 3 композит облучается видимым светом, BiFeO 3 наночастицы будут возбуждены, чтобы генерировать фотогенерированные электроны и дырки. С другой стороны, электроны в ККТ также можно возбуждать от их π орбитальный или σ орбитали к самой низкой незанятой молекулярной орбитали (НСМО) для получения фотовозбужденных электронов. Было продемонстрировано, что возбужденные ККТ могут действовать как отличные доноры электронов и акцепторы электронов. Следовательно, фотогенерированные электроны в зоне проводимости (ЗП) BiFeO 3 наночастицы легко переместятся в π орбитальный или σ орбитали ККТ, в то время как фотовозбужденные электроны ККТ перейдут на CB BiFeO 3 . Во время описанного выше процесса обратной миграции электронов разделение фотогенерированных зарядов в BiFeO 3 может быть повышена, как показывают фотоэлектрохимические измерения (см. рис. 12a). Таким образом, больше фотогенерируемых зарядов доступно для участия в фотокаталитической реакции, что приводит к улучшению фотокаталитической активности.
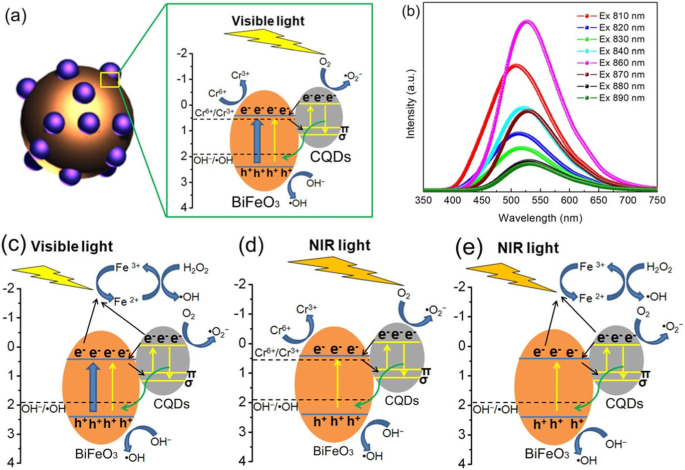
а Механизм фотокаталитического разложения AO7 над CQD / BiFeO 3 композитные фотокатализаторы при облучении видимым светом. б Спектры ФЛ с повышением конверсии ККТ при различных длинах волн возбуждения. c Фотофентоновский каталитический механизм разложения AO7 над CQD / BiFeO 3 композиты при облучении видимым светом. г Фотокаталитический механизм БИК света CQD / BiFeO 3 композиты. е БИК свет фото-Фентоновый механизм CQD / BiFeO 3 композиты
Что еще более важно, свойство PL с повышенным преобразованием CQD также играет важную роль в усилении фотокаталитической активности. На рисунке 13b представлены преобразованные с повышением частоты спектры ФЛ CQD с длиной волны возбуждения от 810 до 890 нм, из которых видно, что пики излучения после преобразования с повышением частоты центрированы на более коротких длинах волн в диапазоне 400–680 нм. Поскольку светопоглощающий край свежеприготовленного BiFeO 3 наночастицы расположены на ~ 588 нм (см. рис. 4), излучение с повышенным преобразованием (400–588 нм) ККТ может быть использовано для возбуждения BiFeO 3 наночастицы для производства фотогенерированных электронов и дырок, которые обеспечивают дополнительные фотогенерируемые заряды для фотокаталитической реакции. Это также способствует повышению фотокаталитической активности BiFeO 3 наночастицы.
Помимо выхода фотогенерированных зарядов, окислительно-восстановительная способность фотогенерированных зарядов считается еще одним важным фактором для понимания каталитического механизма катализаторов. В нашей предыдущей работе потенциалы CB и VB подготовленного BiFeO 3 Наночастицы рассчитаны как + 0,4 и + 2,47 В относительно NHE, соответственно [55]. С термодинамической точки зрения, образование · OH будет происходить плавно, потому что потенциал VB BiFeO 3 положительнее, чем окислительно-восстановительный потенциал OH - / · OH (+1,99 В по сравнению с NHE) [67]. По сравнению с окислительно-восстановительным потенциалом Cr (VI) / Cr (III) (+ 0,51 В по сравнению с NHE) [57] фотогенерированные электроны в CB BiFeO 3 является достаточно отрицательным, чтобы восстановить Cr (VI) до Cr (III). Другой активный вид · O 2 - может быть получен из реакции между фотовозбужденными электронами ККТ и O 2 [68].
На рисунке 13c представлен механизм каталитической деградации фото-Фентона под действием видимого света красителя над CQD / BiFeO 3 . композиты. В этом случае одновременно будут протекать фотокаталитическая реакция и реакция Фентона. Когда H 2 О 2 введен в фотокаталитическую систему, управляемую видимым светом, H 2 О 2 может реагировать с Fe 2+ на поверхности BiFeO 3 для получения дополнительных · OH вместе с образованием Fe 3+ . Одновременно Fe 3+ будет уменьшено до Fe 2+ фотогенерированными электронами BiFeO 3 и CQD [69]. Во время этой циклической реакции образуется больше · ОН, что способствует повышению каталитической эффективности.
На рисунках 13d и e показан фотокаталитический и фото-каталитический механизм Фентона CQD / BiFeO 3 . композит при облучении ближним инфракрасным светом. Известно, что BiFeO 3 не реагируют на ближний инфракрасный свет (> 800 нм). В результате в двух каталитических процессах под действием ближнего инфракрасного излучения могут быть возбуждены только CQD. Миграция фотогенерируемых зарядов и возбуждение CQD с преобразованием вверх аналогичны тем, которые изображены на рис. 13a и b. Поскольку BiFeO 3 не может быть напрямую возбужден NIR-светом, NIR-возбужденный CQD / BiFeO 3 композит имеет относительно более низкий выход фотогенерируемых зарядов по сравнению с композитом, возбуждаемым видимым светом. Вот почему фотокаталитическая и фотофентоновая каталитическая активность CQD / BiFeO 3 композиты при облучении ближним инфракрасным светом слабее, чем при облучении видимым светом.
Выводы
CQD были успешно декорированы на поверхности BiFeO 3 наночастицы через гидротермальный путь для получения CQD / BiFeO 3 композиты. Под воздействием видимого и ближнего инфракрасного излучения эти композиты демонстрируют заметно усиленное фотокаталитическое разложение AO7, фотокаталитическое восстановление Cr (VI) и каталитическое разложение AO7 фото-Фентоном по сравнению с чистым BiFeO 3 наночастицы. Их можно использовать повторно без очевидного снижения каталитической активности. Установлено, что введение ККТ приводит к эффективному разделению фотогенерированных зарядов в композитах. Повышенная каталитическая активность CQD / BiFeO 3 Композиты можно отнести к двум факторам:превосходной фотолюминесценции с повышенным преобразованием и способности ККТ к фотогенерированному переносу электронов.
Доступность данных и материалов
Все данные, проанализированные в ходе этого расследования, представлены в этой статье.
Сокращения
- АО:
-
Оксалат аммония
- AO7:
-
Кислотный апельсин 7
- CB:
-
Полоса проводимости
- CQD:
-
Квантовые точки углерода
- Cr (VI):
-
Шестивалентный хром
- DF-STEM:
-
Сканирующий просвечивающий электронный микроскоп в темном поле
- DPC:
-
Дифенилкарбазидный метод
- DRS:
-
Спектры диффузного отражения в УФ-видимой области
- E g :
-
Энергия запрещенной зоны
- EIS:
-
Электрохимическая импедансная спектроскопия
- FTIR:
-
Инфракрасная спектроскопия с преобразованием Фурье
- h + :
-
Фотогенерация дырок
- HRTEM:
-
Просвечивающий электронный микроскоп высокого разрешения
- LUMO:
-
Самая низкая незанятая молекулярная орбиталь
- NIR:
-
Ближний инфракрасный свет
- O 2 - :
-
Супероксидный радикал
- OH:
-
Гидроксильный радикал
- PL:
-
Фотолюминесценция
- TA:
-
Терефталевая кислота
- TAOH:
-
2-гидрокситерефталевая кислота
- ТЕМ:
-
Просвечивающий электронный микроскоп
- VB:
-
Группа валентности
- XPS:
-
Рентгеновская фотоэлектронная спектроскопия
- XRD:
-
Рентгеновский дифрактометр
Наноматериалы
- Получение и повышенная активность каталитического гидрирования наночастиц Sb / палигорскита (PAL)
- Синтез зеленого цвета в одной емкости микросферы SnO2, украшенной серебром:эффективный и многоразовый катализ…
- Гидротермальный синтез наночастиц In2O3, гибридные двойники, гексагональные дисковые гетероструктуры ZnO для по…
- Получение наноструктуры Au @ TiO2 - оболочка и ее применение для разложения и обнаружения метиленового синего
- Зеленая способность к синтезу и стабилизации наночастиц меди:каталитическая, антибактериальная, цитотоксич…
- Влияние кислотного пептизирующего агента на соотношение анатаз-рутил и фотокаталитические характеристики н…
- Фотокаталитическая активность тройного нанокомпозита аттапульгит – TiO2 – Ag3PO4 для разложения родамина B при мод…
- Получение иерархических пористых инкапсулированных силикалит-1 НЧ серебра и его каталитические характерист…
- Переохлаждение воды, контролируемое наночастицами и ультразвуком
- Нанотрубки из диоксида титана, полученные путем быстрого разрушающего анодирования для фотокаталитического…



