Зеленый синтезированный фитохимически (Zingiber officinale и Allium sativum) с пониженным содержанием наночастиц оксида никеля подтвержден бактерицидный и каталитический потенциал
Аннотация
Фитосинтезированные наночастицы (НЧ), обладающие пониженной химической токсичностью, были сосредоточены во всем мире и в последнее время стали важным компонентом нанотехнологий. Мы подготовили зеленые фитохимически восстановленные (имбирь и чеснок) NiO-NP для замены синтетических бактерицидных и каталитических агентов в текстильной промышленности. НЧ были охарактеризованы с помощью ультрафиолетовой видимой спектроскопии (UV-Vis), рентгеновской дифракции (XRD), рентгеновской фотоэлектронной спектроскопии (XPS), инфракрасной спектроскопии с преобразованием Фурье (FTIR), энергодисперсионной рентгеновской спектроскопии (EDS). ), сканирующая электронная микроскопия (SEM) и просвечивающая электронная микроскопия (TEM). Синтез наночастиц был подтвержден методами XRD и УФ-видимой области с сильным поглощением при 350 нм с размером в диапазоне от 16 до 52 нм для имбиря и 11-59 нм для чеснока. Сканирующая и просвечивающая электронная микроскопия подтвердила плеоморфизм с НЧ кубической и более сферической формы. Более того, точное количество экстрактов чеснока и имбиря (1:3,6 мл), включенных для синтеза NiO-NP, было успешно подтверждено методом FTIR. Фитохимически восстановленные НЧ чесноком проявляли повышенную бактерицидную активность против нескольких устойчивых к лекарствам Staphylococcus aureus при возрастающих концентрациях (0,5, 1,0 мг / 50 мкл), а также эффективно разрушал краситель метиленовый синий (МБ). Безусловно, синтезированные в зеленом виде NiO-NP являются приближающимися активистами для решения проблемы лекарственной устойчивости, а также являются экологически безопасным каталитическим агентом, который можно использовать в промышленных масштабах.
Введение
Влияние нанотехнологий на материю, по крайней мере, с одним размером 1–100 нм, что дает возможность конструировать материалы, контролируя их размер [17]. НЧ из-за их уникальных химических, физических и биологических свойств в различных областях, включая медицину, привлекли большое внимание. Их свойства можно легко изменить, изменив размер в нанометровом масштабе [47].
НЧ никеля (Ni) и оксида никеля (NiO) имеют большое значение из-за их особых магнитных, каталитических и электронных свойств в энергетической технологии, магнетизме, биомедицине и электронике [9, 26, 35]. NiO с широкой запрещенной зоной от 3,6 до 4,0 эВ и кубической структурой решетки имеет потенциал, связанный с полупроводником p-типа. Эти НЧ, обладающие высокой химической стабильностью, сверхемкостными свойствами, способностью к переносу электронов и электрокатализом, используются в биомедицине и имеют фотокаталитическую, противовоспалительную и антибактериальную активность [8, 10, 11, 45]. Возникновение инфекционных заболеваний, особенно устойчивых к антибиотикам (МЛУ), нанесло серьезный ущерб общественному здравоохранению во всем мире. Как правило, как патогенные грамположительные (G + ve), так и грамотрицательные (G − ve) штаммы бактерий относятся к числу основных угроз общественному здоровью.
В молочной промышленности мастит крупного рогатого скота является серьезным проблемным заболеванием, имеющим большое экономическое влияние, которое характеризуется химическими, микробиологическими и физическими изменениями в молоке, а также патологическими изменениями в железистых тканях вымени [6, 19]. Этиология мастита включает инфекционных агентов, то есть бактерий, вирусов и грибков, и наиболее важными из них являются бактерии, разделенные на две группы:основные ( Streptococci, Staphylococcus aureus , Corynebacterium pyogenes и колиформ ) и второстепенных патогенов ( Corynebacterium bovis и коагулазонегативные стафилококки ) [25]. Появление множественных лекарственно-устойчивых грамположительных и грамотрицательных штаммов бактерий представляет значительную угрозу для здоровья населения [23, 32].
Zingiber officinale (имбирь) является важным ингредиентом в аюрведии и унани, а китайская фитотерапия лечит различные недуги, такие как тошнота, помощь пищеварению, ревматизм и нарушения свертываемости крови, благодаря широкому разнообразию эфирных масел, таких как зингиберол, монотерпен, сесквитерпен и сесквитерпеновые углеводороды [12, 13, 43]. Однако Allium sativum (чеснок) содержат сероорганические компоненты, т.е. аллилсульфидные группы, аллиин, аджоен, аллилцистеин и аллицин, и другие, такие как витамины, фосфолипиды, флавоноиды, аминокислоты и жирные кислоты, которые определяют его лечебные свойства [14, 24] . Мы стремились оценить бактерицидное действие фитохимически восстановленных НЧ оксида металла Ni против МЛУ ( S. aureus ), изолята мастита крупного рогатого скота, и это будет первый отчет из Пакистана в области ветеринарных исследований по вышеупомянутому агенту.
Методы
Настоящее исследование было направлено на изучение бактерицидного действия фитохимически восстановленных NiO-NP против МЛУ ( S. aureus ), изолят мастита крупного рогатого скота.
Материалы
Нитрат никеля [Ni (NO 3 ) 2 ], гидроксид натрия (NaOH), метиленовый синий (МБ) и боргидрид натрия (NaBH 4 ) аналитической чистоты были приобретены у Sigma-Aldrich®, а свежие корни имбиря и чеснока были собраны на местном рынке. Корни сушили в тени для достижения постоянного веса для дальнейшей обработки. Диски с антибиотиками были приобретены в компании Bioanalyse® (Турция). Используемые среды для выращивания бактерий были аналитической степени чистоты от TM Media (Titan Biotech Ltd, Индия).
Приготовление водных экстрактов
Корни имбиря и чеснока измельчали до мелкой пыли с помощью электрической мельницы и хранили в пластиковых контейнерах. Порошок измельченного корня смешивали с контролируемым количеством дистиллированной воды-DIW (1:10) при интенсивном перемешивании при 70 ° C в течение 30 минут. Экстракты охлаждали, фильтровали через фильтровальную бумагу Whatman № 1 и хранили при 4 ° C (рис. 1) до дальнейшего использования.
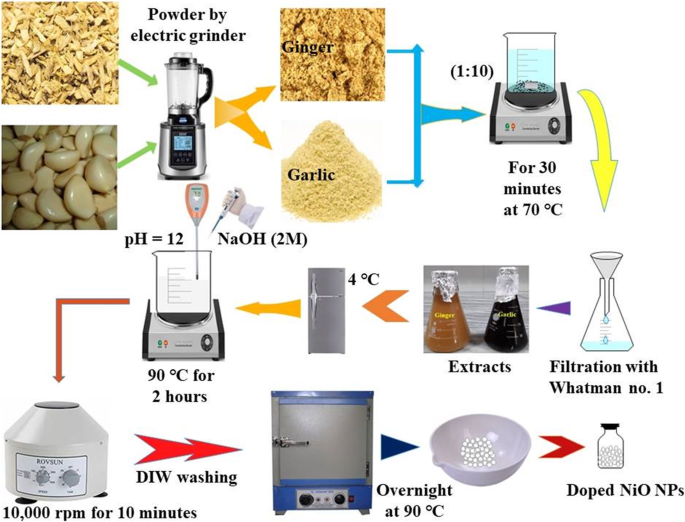
Схема синтеза экстракции имбиря и чеснока и фитохимически восстановленных NiO-NP
Экологичный синтез NiO-NP
Водные экстракты имбиря и чеснока различных соотношений (1,2, 1,8, 2,4, 3,0, 3,6 и 4,2 мл) добавляли к нитрату никеля (0,1 М) при непрерывном перемешивании. PH перемешиваемого раствора 12 поддерживали с помощью NaOH (2 M) при 90 ° C в течение 2 часов. Образовавшиеся осадки центрифугировали при 10000 об / мин в течение 10 минут, промывали DIW и сушили в течение ночи в сушильном шкафу с горячим воздухом при 90 ° C, как показано на рис. 1.
Характеристика
Максимумы поглощения ( ƛ макс ) синтезированных НЧ сканировали на спектрофотометре UV-Vis (Genesys 10 S) в диапазоне длин волн 200–800 нм. Фазовый состав и структурная информация были проанализированы с помощью дифракции рентгеновских лучей (XRD) фазера BUNKER D2 с диапазоном 2θ (10–80 °), снабженного излучением Cu Kα1 λ =1,540 Å. Функциональные группы NiO-NP, синтезированные зеленым цветом, регистрировали с помощью инфракрасной спектроскопии с преобразованием Фурье (ATR-FTIR). Размер, форма и элементный анализ НЧ анализировали с помощью автоэмиссионного электронного микроскопа (FESEM) и просвечивающей электронной микроскопии Hitachi H7100FA (ТЕМ). Состав образцов с соответствующей шириной запрещенной зоны исследовали методом рентгеновской фотоэлектронной спектроскопии (XPS).
Выделение и идентификация MDR S. золотистый
Изоляция S. золотистый
Клинически положительные образцы коровьего молока, собранные в частных и государственных ветеринарных больницах и на фермах в Пенджабе, Пакистан, культивировали на 5% агаре с овечьей кровью и инкубировали при 37 ° C в течение 24–48 часов. Полученные характерные колонии дополнительно наносили штрихами на маннитоловый агар (MSA) TM Media (Titan Biotech Ltd, Индия) в триплетах для выделения очищенного S. золотистый .
Идентификация MDR S. золотистый
Идентификация бактериальных колоний проводилась с помощью морфологических характеристик, окрашивания по Граму и биохимических процедур (тест на коагулазу и каталазу) в соответствии с описанием в руководстве Берджи по детерминативной бактериологии.
Чувствительность характерных колоний к антибиотикам оценивали с помощью диско-диффузионного теста на основе рекомендаций Национального комитета по клиническим лабораторным стандартам (NCCLS) для выделения MDR S. золотистый . Диски с антибиотиками, содержащие окситетрациклин (30 мкг), тилозин (30 мкг), гентамицин (10 мкг), ципрофлоксацин (5 мкг) и триметоприм + сульфаметоксазол (1,25 мкг + 23,75 мкг), нанесенные в асептических условиях на агаре Мюллера-Хинтона TM (MHA) (Titan Biotech Ltd, Индия) 1 × 10 8 КОЕ / мл хранили при 37 ° С в течение 24 ч [7]. Бактерия, устойчивая как минимум к трем антибиотикам, была объявлена МЛУ [28].
Противомикробное действие
Потенциал антимикробного действия in vitro фитохимически восстановленных NiO-NP оценивался методом диффузии в лунках агара на десяти репрезентативных изолятах MDR S. золотистый собирают из маститного молока. Чашки Петри протирали 1,5 × 10 8 КОЕ / мл (0,5 стандарта МакФарланда) MDR S. золотистый на MSA. Лунки диаметром 6 мм формировали с использованием стерильного пробкового бурава. Применяли различные концентрации индивидуальных водных экстрактов имбиря, чеснока и зелени, синтезированных (фитохимически восстановленных) NiO-NP. Водные экстракты использовали при концентрациях (10 мг / 100 мкл) и (50 мг / 100 мкл) и NiO (0,5 мг / 50 мкл) и (1,0 мг / 50 мкл). Ципрофлоксацин (0,005 мг / 50 мкл) использовали в качестве положительного контроля, а DIW - в качестве отрицательного контроля (50 мкл).
Статистический анализ
Противомикробная эффективность рассчитывалась по размеру зоны ингибирования (мм), а диаметры зоны ингибирования анализировались статистически с помощью однофакторного дисперсионного анализа (ANOVA) с использованием SPSS 20.
Катализ
Для каталитической оценки синтезированного экстракта NiO свежеприготовленный водный борогидрид натрия (300 мкл) смешивали с 3 мл метиленового синего (0 . 03 × 10 −3 М) раствор. Затем к растворам добавляли 300 мкл коллоидного образца желаемой концентрации. Голубой цвет красителя метиленового синего (МБ) исчез, что свидетельствует о разложении красителя до лейкометиленового синего, как показано на рис. 2. Поглощение было отмечено в диапазоне 200–800 нм с использованием спектрофотометра в УФ-видимой области.
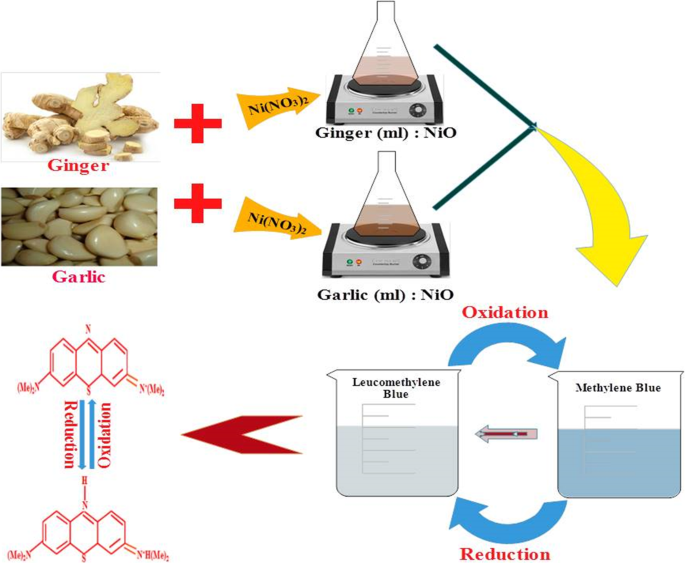
Принципиальная схема каталитического восстановления МБ до LMB синтезированными зелеными НЧ
Результаты и обсуждение
Оптические свойства фитохимически восстановленного NiO водными экстрактами имбиря и чеснока в диапазоне 200–600 нм представлены на рис. 3a, b. Максимальное поглощение ( λ макс ) в NiO-NP наблюдалась около 350 нм (1:3,6 мл), которая увеличивалась с увеличением концентрации экстрактов, сопровождаемой синим сдвигом. Пики поглощения экстрактов имбиря и чеснока появлялись около 275 и 280 нм соответственно. Резкое изменение цвета реакционных смесей от винно-красного до светло-зеленого после включения экстрактов корней. Ширина пика указывает на агломерацию частиц и электронный переход от валентной зоны к зоне проводимости с концентрацией экстракта в NiO, о чем свидетельствуют сильные полосы поглощения [20]. Следовательно, на фиг. 3a, b результаты показали снижение абсорбции синтезированных НЧ с увеличением или уменьшением объема экстракта сверх оптимизированного значения (1:3,6 мл). Ширина запрещенной зоны рассчитывалась с использованием графика Таука (уравнение 1).
$$ \ left (\ alpha hv \ right) =B {\ left (hv- {E} _g \ right)} ^ {\ raisebox {1ex} {$ 1 $} \! \ left / \! \ raisebox {-1ex } {$ 2 $} \ right.} $$ (1)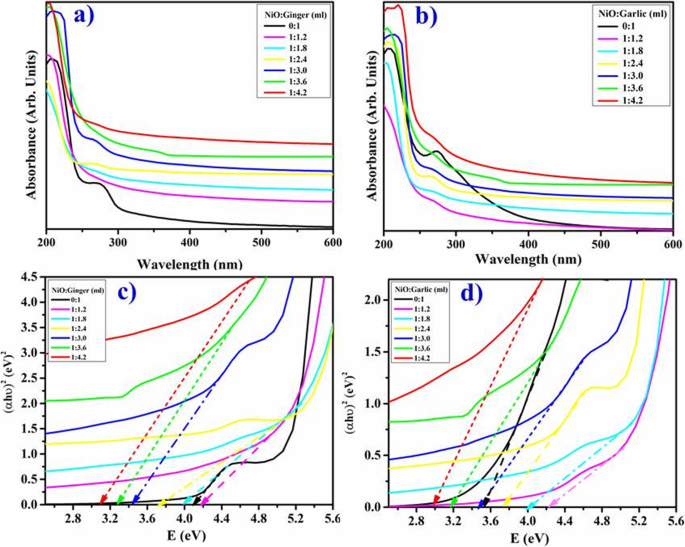
а - г Спектры поглощения синтезированных зеленым NiO-NP с имбирем ( a ) и экстракт чеснока ( b ). Ширина запрещенной зоны фитохимически восстановленного NiO имбирем ( c ) и чеснок ( d ) соответственно
Где α - коэффициент поглощения, h постоянная Планка, B постоянная, υ называется частотой фотона, а E g - ширина запрещенной зоны. Расчетная запрещенная зона фитохимически восстановленного NiO имбирем и чесноком по графику ( αhʋ ) 1/2 против энергии фотона ( hʋ ). Пересечение касательной к x -ось, которая обеспечивает значения энергии запрещенной зоны образцов, как показано на рис. 3c, d. Изменения в энергии запрещенной зоны были определены при добавлении имбиря в NiO от 4,15 до 3,1 эВ и чеснока от 3,5 до 3,0 эВ соответственно (рис. 3c, d).
Кристалличность, размер и фазовый состав NiO-NP были подтверждены методом XRD, как показано на рис. 4 a, b. Пики при значениях 2θ 37,10 °, 43,32 °, 62,81 ° и 76,51 ° соответствуют (111), (200), (220) и (311) (номер карты JCPDS:00-047-1049) (рис. 4a. , б) упоминается в [30]. Интенсивность пика указывает на гексагональный и гранецентрированный кубический (ГЦК) NiO со средним размером 32,9 нм, рассчитанным с помощью D =0,9λ / βcosθ для имбиря и 29,92 нм для фитохимически восстановленных NiO-НЧ чеснока. Широкие пики указывают на наличие кислородных пространств и локального беспорядка решетки в образце [38]. Различные фитохимические вещества имбиря (флавоноиды, алкалоиды, дубильные вещества и сапонины) и водные экстракты чеснока (аллицин, аллилсульфид, аллиин, жирные кислоты, гликолипиды, фенольные соединения, аминокислоты и флавоноиды), действующие как покрывающие агенты, ответственны за средний размер кристаллитов НЧ оксидов металлов [14, 46].
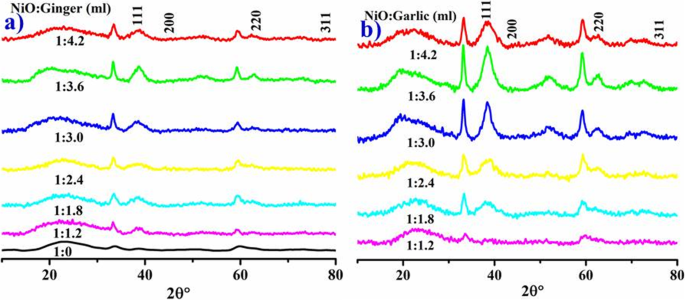
Рентгенограмма различных концентраций фитохимически восстановленного NiO имбирем ( a ) и чеснок ( b ) и стандартный NiO ( c )
Зарегистрированные FTIR-спектры NiO, биосинтезированного из корней имбиря и чеснока, показаны на рис. 5 а, б. Разработайте широкое поглощение при 3380 см −1 соответствуют ОН, а ширина пика указывает на карбонильную группу с частотой растяжения (N-H) амина [50]. Резкое поглощение на 2313 см −1 указывает на валентные колебания CO 2 либо антенна, либо CO 2 внутри зерен НП. Быстрое поглощение атмосферного CO 2 указывает на большую площадь поверхности материала [18]. Широкое поглощение на 1629 см −1 соответствуют растяжению ароматического кольца C =C и острым пикам при 1392 и 1064 см -1 соответствуют валентным колебаниям C – N алифатических аминов [48]. Интенсивные пики на 978 см −1 подтвердили частоту растяжения металлического кислорода NiO [44].
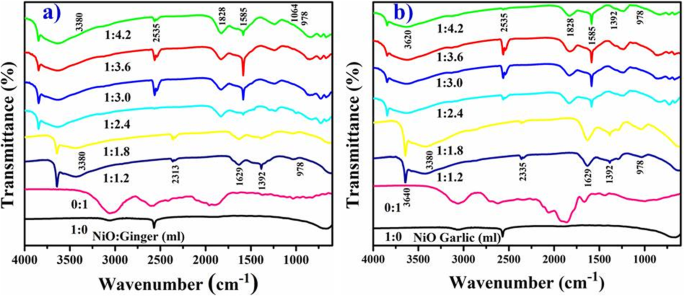
Спектры FTIR с экстрактом имбиря до NiO ( a ) и чеснок ( b )
Сдвиги пиков, наблюдаемые после биовосстановления NiO, составляют 2535–2313, 1828–1629 и 1585–1392 см −1 указывают на фитохимические вещества, терпеноиды, флавоноиды, полиолы и белки, содержащие кетоны, спирты, карбоновые кислоты и функциональные группы аминов, ответственные за хелатирование и блокирование при биовосстановлении [42].
Морфология поверхности и размер фитохимически восстановленных NiO-NP были определены с использованием автоэмиссионной сканирующей и просвечивающей электронной микроскопии, как показано на рис. 6a-f. NiO-NPs показали плеоморфизм кубической и более сферической формы (<50 нм) с небольшой агломерацией [40]. Агломерация наночастиц может быть очевидна по прилипанию полимера и магнитному взаимодействию между частицами [49].
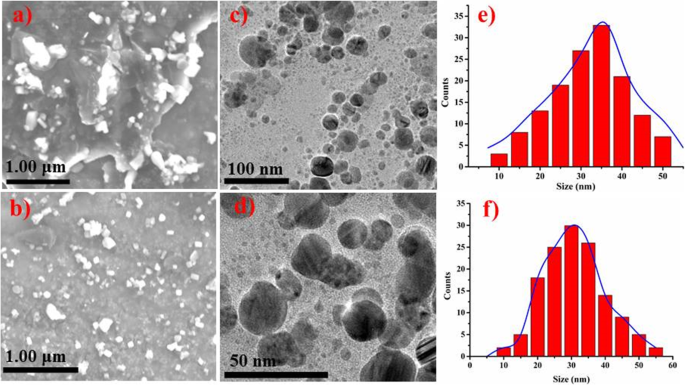
а - е СЭМ-изображение фитохимически восстановленного NiO имбирем ( a ) и чеснок ( b ). ПЭМ-изображение фитохимически восстановленного NiO с имбирем ( c ) и чеснок ( d ) и гранулометрический состав NiO, восстановленного фитохимически имбирем ( e ) и чеснок ( f )
Элементный анализ и другие особенности синтезированных NiO-NP были описаны с помощью энергодисперсионной рентгеновской спектроскопии (EDS), которая подтвердила наличие чистых фаз NiO, как показано на рис. 7a, b. Спектры EDS подтвердили три пика, напрямую связанных с высокой чистотой Ni, присутствующим в испытанных образцах между 1 и 10 кВ. Атомные массовые проценты, наблюдаемые в спектрах для Ni, O, C и Zn, составляют 54,69, 27,81, 18,06 и -0,55 соответственно.
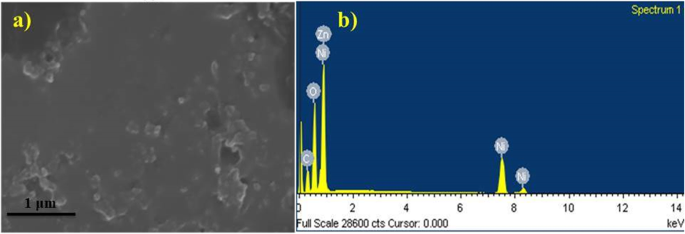
а , b Спектр ЭДС зеленых синтезированных NiO-НЧ
XPS показывает C1 s , O1 s , и Ni2 p спектры фитохимически восстановленных NiO-НЧ на рис. 8a – d, что свидетельствует о химической природе и связующих состояниях синтезированных образцов. Наиболее интенсивные пики при 284,8 и 286,2 эВ демонстрируют C1 s спектр (рис. 8б), соответствующий C – C и C – OH / C – O – C [21]. O1 s пик при 530,8 эВ (рис. 8в) может быть отнесен к гидроксильным группам атомов кислорода, атомам кислорода, примыкающим к вакансиям никеля, или связанным с кислородом атомам углерода C =O [1, 15, 37]. Вклад 532,2 эВ принадлежит атомам кислорода в поглощенных молекулах воды (NiOH) [31, 41]. Ni2 p спектр, содержащий Ni2 p 3/2 и Ni2 p Пики 1/2 можно разделить с помощью функции Гаусса – Лоренца на пять компонентов (рис. 8d). Наиболее интенсивные пики при 872,72 и 855,82 эВ принадлежат Ni2 p 1/2 и Ni2 p 3/2 с соответствующими сателлитными пиками 879,36 и 861,57 эВ соответственно [16]. Спин-орбитальное расщепление между Ni (2 p 1/2) и Ni (2 p 3/2), а уровень в ядре NiO-NP составляет 17,28 эВ, что хорошо согласуется с более ранними сообщениями [33, 34].
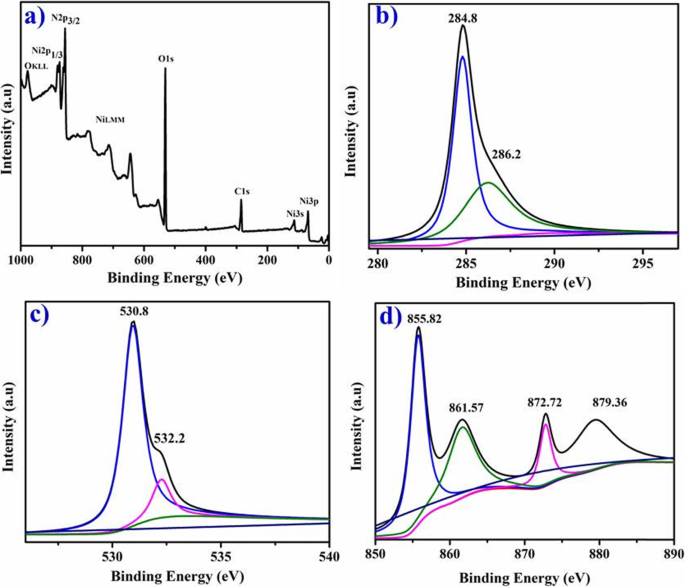
а - г XPS-исследование фитохимически восстановленных частиц ( a ), C1 s орбитали ( b ), O1 s спектры NiO ( c ) и Ni2 p ( д )
Антимикробное / бактерицидное действие экстрактов корня имбиря и чеснока и зеленых / фитохимически восстановленных NiO-NP оценивали с помощью анализа диффузии в лунках агара путем измерения зоны ингибирования (мм), как показано на рис. 9a – d и в таблице 1. Результаты демонстрируют сильную взаимосвязь между концентрацией НЧ и зонами ингибирования (мм). Зоны значительного ингибирования (мм) ( P <0,05) были зарегистрированы для образцов 1 (1,2 мл:1), 2 (1,8 мл:1), 3 (2,4 мл:1), 4 (3 мл:1), 5 (3,6 мл:1) и 6 ( 4,2 мл:1) в диапазоне (3–4,9 мм) и (3,05–5,2 мм) при низких и высоких концентрациях фитохимически восстановленных NiO-NP имбирем (рис. 9c, d), в то время как (3,15–5,3 мм) и (3,75–3,5 мм) 5,9 мм) фитохимически восстановленные НЧ с чесноком против MDR S. золотистый (Рис. 9e, f) . Водные экстракты корня имбиря показали нулевую эффективность (рис. 9a), а корни чеснока показали зоны ингибирования 2,65 и 5 мм при низких и высоких концентрациях, соответственно (рис. 9b). Все результаты сравнивали с отрицательным контролем DIW (0 мм) и положительным контролем ципрофлоксацином (12,55 мм). В целом, фитохимически восстановленные NiO-NP с чесноком показали значительную ( P <0,05) усиленное бактерицидное действие против MDR S. aureus.
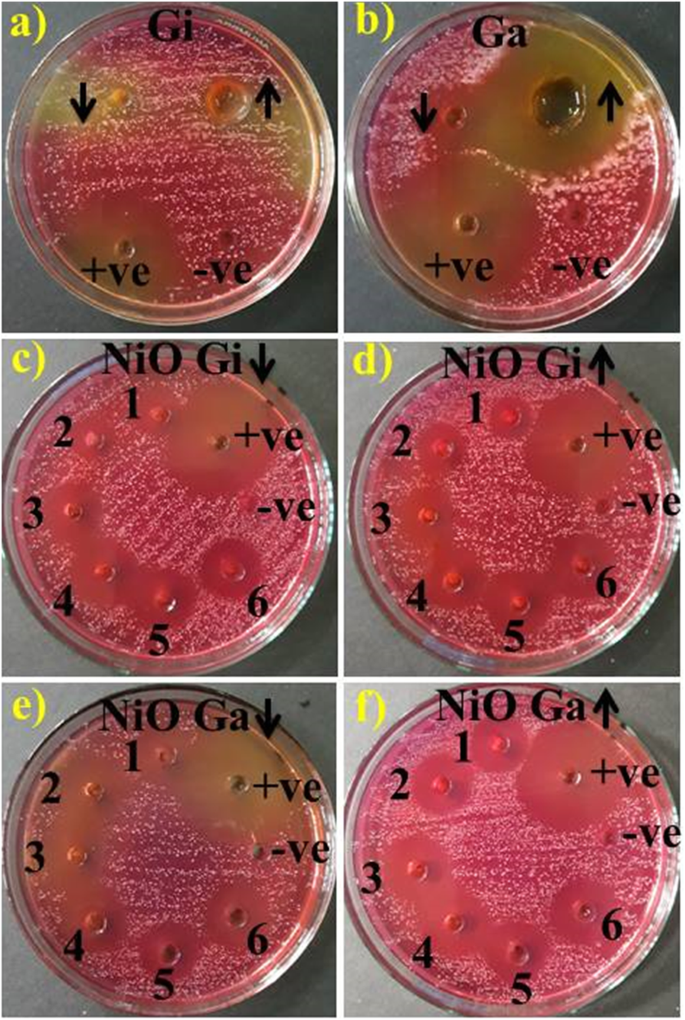
а - е Противомикробная активность водного экстракта имбиря in vitro ( a ), чеснок ( б ), и NiO-NP, фитохимически синтезируемые экстрактом имбиря в низких и высоких дозах ( c , d ) и чеснок ( e , f )
Различие в устойчивости к окислительному стрессу зависит от различных факторов, таких как площадь поверхности, морфология и размер частиц синтезированного наноматериала, играющих важную роль в потенциале антибактериального действия [29, 36]. Электростатическое взаимодействие между бактериальными штаммами и наноразмерными материалами приводит к образованию активных форм кислорода, ответственных за гибель бактериальных клеток [2,3,4,5, 22]. Было обнаружено, что для реакции наноматериала со штаммами бактерий возможны две реакции, включая сильное взаимодействие катионов Ni 2+ с отрицательно заряженными частями бактериальной клетки, что приводит к коллапсу, в то время как вторая реакция приводит к электронному возбуждению из зоны проводимости в зону проводимости при облучении поверхности NiO светом. Дальнейшая электронная реакция с O 2 генерирует O - 2 радикалы, приводящие к H 2 О 2 производство. Образование · OH происходило в результате реакции h + с водой. Таким образом, в результате получается O - 2 · Виды · и · OH сыграли значительную роль в разрушении липидной или белковой молекулы, присутствующей на внешней поверхности бактериальной клетки [39].
Каталитическая активность
Рис. 10 a – e демонстрирует каталитическое восстановление МБ в присутствии экстрактов корней и зеленых / фитохимически восстановленных NiO-NP при комнатной температуре. На рис. 10а показан каталитический потенциал NiO-НЧ, синтезированных обычным способом, а на рис. 10б, с) представлен каталитический потенциал водных экстрактов корня имбиря и корня чеснока. Каталитическая емкость фитохимически восстановленных NiO-NP представлена на рис. 10d, e. Очевидно, что NiO и экстракты корней растений не являются эффективными нанокатализаторами, так как на восстановление метиленового синего им потребовалось 15, 21 и 38 минут (рис. 10a – c). Фитохимически восстановленные НЧ с имбирем быстро разлагаются ( λ макс =8 мин) с эффективным превращением МБ в лейкометиленовый синий (рис. 10d). NiO-NP, опосредованные чесноком, показали аналогичную картину 100% -ного уменьшения количества красителей за 5 минут (рис. 10e).
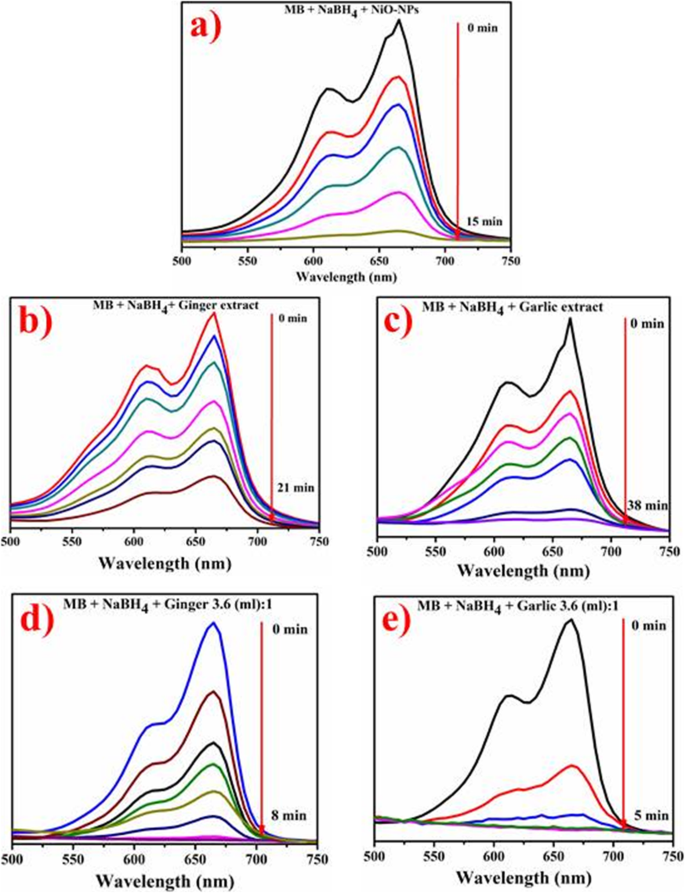
а - е Каталитическая активность NiO ( a ), экстракт имбиря ( b ), экстракт чеснока ( c ), фитохимически восстановленный NiO имбирем ( d ), а также НЧ с пониженным содержанием чеснока ( e )
Зеленые / фитохимически восстановленные НЧ осуществляют значительную каталитическую деградацию красителя путем переноса электронов от донорных частиц (BH 4 ) для акцептора (МБ) и стабилизации системы за счет снижения энергии активации [27]. Данные показали, что зеленые НЧ являются более эффективным нанокатализатором по сравнению с обычными НЧ и индивидуальным экстрактом.
Заключение
NiO-NP, содержащие экстракты корня имбиря и чеснока, служили отличным бактерицидным, а также каталитическим агентом. Включение экстракта корня, содержащего фитохимические группы, привело к успешному синтезу NiO-NP, выявленному с помощью FTIR. Пики XRD подтвердили гексагональную и гранецентрированную кубическую (ГЦК) решетку NiO, а сканирующий электронный микроскоп подтвердил плеоморфизм с кубической и более сферической морфологией НЧ, имеющих средний размер 16–52 (легирование имбирем) и 11–59 нм (легирование чесноком). Однако элементный анализ выявил химическую природу и состояния связывания, проанализированные с помощью EDS и XPS, и представил фактическое процентное содержание никеля и кислорода, в то время как УФ-анализ подтвердил разницу пиков поглощения в диапазоне 350 нм и привел к синему сдвигу при более высоком количестве примесей. Было обнаружено, что фитохимически восстановленный в чесноке NiO в высокой концентрации более эффективен по сравнению с НЧ имбиря против MDR S. золотистый а также эффективно уменьшил МБ. Таким образом, зеленый / восстановленный фитохимически NiO из экстрактов корня чеснока может быть принят в современной медицине в качестве заменителя устойчивости к антибиотикам, а в текстильной промышленности в качестве катализатора, не опасного для окружающей среды.
Доступность данных и материалов
Все данные полностью доступны без ограничений.
Сокращения
- EDS:
-
Энергодисперсионная рентгеновская спектроскопия
- fcc:
-
Гранецентрированный кубический
- FTIR:
-
Инфракрасная спектроскопия с преобразованием Фурье
- G + ve:
-
Грамположительный
- G –ve:
-
Грамотрицательный
- JCPDS:
-
Объединенный комитет по стандартам порошковой дифракции
- МБ:
-
Метиленовый синий
- Ни:
-
Никель
- NiO:
-
Оксид никеля
- нм:
-
Нанометр
- НП:
-
Наночастицы
- SEM:
-
Сканирующая электронная микроскопия
- ТЕМ:
-
Просвечивающая электронная микроскопия
- УФ-видимый:
-
Ультрафиолетовая видимая спектроскопия
- XPS:
-
Рентгеновская фотоэлектронная спектроскопия
- XRD:
-
Рентгеновская дифракция
Наноматериалы
- Биосовместимые наночастицы FePO4:доставка лекарств, стабилизация РНК и функциональная активность
- Биогенный синтез, характеристика и оценка антибактериального потенциала наночастиц оксида меди против Escheric…
- Получение и повышенная активность каталитического гидрирования наночастиц Sb / палигорскита (PAL)
- Наночастицы как насос оттока и ингибитор биопленки для омоложения бактерицидного действия обычных антибиот…
- Синтез зеленого цвета в одной емкости микросферы SnO2, украшенной серебром:эффективный и многоразовый катализ…
- Потенциальная токсичность наночастиц диоксида титана для печени, мозга и эмбрионов у мышей
- Модифицированный гиперразветвленный полиглицерин как диспергатор для контроля размера и стабилизации нано…
- Определение каталитической активности наночастиц TiO2, легированных переходными металлами, с помощью спектро…
- Синтез и эффективность in vitro покрытых полипирролом железо-платиновых наночастиц для фототермической терапии…
- Зеленая способность к синтезу и стабилизации наночастиц меди:каталитическая, антибактериальная, цитотоксич…



