Определение каталитической активности наночастиц TiO2, легированных переходными металлами, с помощью спектроскопического анализа поверхности
Аннотация
Модифицированный TiO 2 наночастицы (НЧ) для повышения их каталитической активности путем легирования их пятью переходными металлами (Cr, Mn, Fe, Co и Ni) были исследованы с использованием различных методов анализа поверхности, таких как сканирующая электронная микроскопия (SEM), рамановская спектроскопия, сканирование просвечивающая рентгеновская микроскопия (STXM) и фотоэмиссионная спектроскопия высокого разрешения (HRPES). Чтобы сравнить каталитическую активность этих легированных переходными металлами TiO 2 наночастицы (TM-TiO 2 ) с TiO 2 НЧ мы контролировали их характеристики при каталитическом окислении 2-аминотиофенола (2-АТФ) с использованием HRPES и при окислении 2-АТФ в водном растворе с помощью электрохимических (ЕС) измерений. В результате мы четко исследовали, что усиление дефектных структур, вызванное легированным переходным металлом, тесно коррелирует с усилением каталитической активности TiO 2 Наночастиц и подтверждают, что TiO, легированный Fe и Co 2 НЧ могут действовать как эффективные катализаторы.
Фон
В течение нескольких десятилетий было хорошо известно, что оксид титана (TiO 2 ) имеет эффективную каталитическую активность, а также низкую стоимость, поэтому TiO 2 привлек значительное внимание из-за его различных применений в солнечных элементах, фотокатализе и электрохимическом катализах [1,2,3,4,5,6,7]. Хотя TiO 2 перспективный материал, TiO 2 (структуры рутила или анатаза) имеет относительно широкую запрещенную зону (E g =3,0 ~ 3,2 эВ), и такая ширина позволяет ему поглощать только УФ-свет. Поэтому значительные усилия были приложены для уменьшения ширины запрещенной зоны и повышения каталитической активности. По этой причине для уменьшения ширины запрещенной зоны широко применяется введение посторонних элементов в качестве примесей, поскольку примесный элемент в TiO 2 может изменять состояния краев полосы.
Следовательно, наша стратегия состоит в том, чтобы ввести переходные металлы в качестве легирующих добавок в TiO 2 . НЧ для улучшения каталитических характеристик TiO 2 НЧ значительно, потому что они могут увеличивать дефектную структуру TiO 2 НЧ, что тесно связано с усилением каталитической активности [8,9,10,11,12,13,14,15,16,17,18]. Для дальнейшего изучения предыдущих исследований [19, 20] мы выполнили внедрение различных ионов переходных металлов (TM + ) в TiO 2 а затем сравнили каталитическую активность TiO 2 НЧ, содержащие различные легирующие примеси переходных металлов с TiO 2 НП. Исходя из этого, мы можем оценить эффективность легирующих примесей переходных металлов для TiO 2 НЧ и сравнить фотокаталитическую активность различных переходных металлов вместе.
В нашем исследовании мы успешно изготовили пять легированных переходными металлами TiO 2 НП (TM-TiO 2 ; TM =Cr, Mn, Fe, Co и Ni) с помощью процесса термосинтеза (см. Раздел «Методы»). Сначала мы сравнили морфологию и электронные свойства пяти TM-TiO 2 с TiO 2 НЧ с помощью сканирующей электронной микроскопии (SEM), рамановской спектроскопии и сканирующей просвечивающей рентгеновской микроскопии (STXM). Затем мы оценили их каталитическую способность путем окисления 2-аминотиофенола (2-АТФ) в условиях сверхвысокого вакуума (UHV) (базовое давление ниже 9,5 × 10 −11 Торр) с 365 нм УФ-освещением с использованием фотоэмиссионной спектроскопии высокого разрешения (HRPES) и циклической вольтамперограммы (CV) изменений в фазе раствора с помощью электрохимии. Эти реакции и анализы также проводились для определения механизма реакции каталитического окисления.
Методы
Подготовка растворов-предшественников
Мы приготовили каждый раствор прекурсора с помощью синтеза в одном сосуде. Желаемые количества легирующих примесей переходных металлов (TM) добавляли в форме TM (NO 3 ) x ∙ н H 2 O (нитрат металла n -гидрат; TM =Cr, Mn, Fe, Co или Ni) в мольных долях по отношению к TiO 2 (TM / (TM + TiO 2 )), которые использовались в качестве легирующих примесей. Все вещества были приобретены у Sigma-Aldrich. Растворы предшественников перемешивают 10 мин. 2-Аминотиофенол (2-АТФ, Sigma Aldrich, чистота 97%) и Nafion (Sigma Aldrich, 5 мас.% В низкомолекулярном алифатическом спирте и воде) были приобретены у Sigma-Aldrich. Таблетки с фосфатно-солевым буфером (PBS) приобретаются у Gibco.
Приготовление диспергированного TM-TiO 2 Решения
Гидроксид тетраметиламмония (TMAOH) (1,2 г) разбавляли бидистиллированной водой (DDW, 22,25 г). Изопропоксид титана (TTIP, 3,52 г) разбавляли изопропанолом (3,5 г). Оба раствора перемешивали отдельно в течение 10 мин. Белый TiO 2 появлялся при добавлении по каплям раствора TTIP к раствору TMAOH при комнатной температуре. Затем к каждому раствору синтетического геля на масляной бане при 80 ° C при перемешивании добавляли желаемые количества (5 мол.%) Примесей переходных металлов. Примерно через 10 мин раствор синтетического геля превратился в прозрачный раствор. Растворы переносили в автоклавы с тефлоновым покрытием и затем нагревали при 220 ° C в течение 7 часов в конвекционной печи. Полученный TM-TiO 2 (Cr-TiO 2 , Mn-TiO 2 , Fe-TiO 2 , Co-TiO 2 , и Ni-TiO 2 ) были отфильтрованы и промыты DDW для удаления любых остатков.
Изготовление TM-TiO 2 -Модифицированный нафион GCE и электрохимические измерения окисления 2-АТФ
Электрохимическое окисление 2-АТФ исследовали с использованием стеклоуглеродных электродов (ГЭЭ), модифицированных TM-TiO 2 . . Для каждой ТМ масса 4,0 мг TM-TiO 2 был диспергирован в 2,0 мл дистиллированной воды, содержащей 50 мкл нафиона, а затем смешан с использованием ультразвукового процессора в течение 5 минут для получения гомогенного TM-TiO 2 -Нафион смесь. После этого 20 мкл смеси помещали на GCE и сушили при 80 ° C в предварительно нагретой печи в течение 30 мин. Циклическая вольтамперограмма (CV) 0,01 M 2-АТФ в PBS была получена для каждого TM-TiO 2 -Нафион доработал GCE.
Характеристики
Морфология и распределение по размерам изготовленных наночастиц были проанализированы с помощью автоэмиссионной сканирующей электронной микроскопии (FE-SEM, FEI Inspect F50, работающая при 10 кВ). Рамановские спектры были получены с использованием спектрометра (Horiba, ARAMIS) с Ar + ионный непрерывный (514,5 нм) лазер. Результаты сканирующей просвечивающей рентгеновской микроскопии (STXM) с разрешением 25 нм были получены на канале 10A ускорительной лаборатории Pohang Accelerator Laboratory (PAL). STXM использовался для получения стопок изображений с помощью рентгеновской абсорбционной спектроскопии (XAS) для выявления легированного переходного металла L -кромка, Ti L -ребень и O K -краевые спектры. Эксперименты по фотоэмиссионной спектроскопии высокого разрешения (HRPES) были выполнены на электронном анализаторе (SES-100, Gamma-Data Scienta) на канале 8A2 PAL для идентификации электронной структуры. S 2 p Спектры остовного уровня регистрировались с помощью анализатора энергии электронов. В качестве рабочего электрода использовался GCE диаметром 2 мм, а в качестве противоэлектрода - платиновая проволока диаметром 1 мм, а электродом сравнения - Ag / AgCl (3 M KCl).
Результаты и обсуждение
Чтобы получить более подробные характеристики электронной структуры, мы сначала получили Ti L -ребень и O K рентгеновские адсорбционные спектры (XAS) для TiO 2 НП и пять TM-TiO 2 (Рис. 1) с помощью STXM. Черные области изображений-вставок, показанных на рис. 1a – f, происходят из TiO 2 НЧ и TM-TiO 2 . Во-первых, форма e g орбиталь расположена на ~ 460 эВ для Ti L 2,3 Спектры XAS по краю указывают на присутствие типичного анатаза TiO 2 структура во всем TiO 2 НП и пять TM-TiO 2 [21]. Однако когда TiO 2 НЧ легированы Fe 3+ (Рис. 1d) и Co 3+ ion (рис. 1д) отношение интенсивностей пиков t 2 г (457,4 эВ) и e g (459 ~ 460 эВ) ниже, чем у анатаза TiO 2 и другие TM-TiO 2 (Cr-TiO 2 , Mn-TiO 2 , и Ni-TiO 2 ), что свидетельствует о наличии слабого кристаллического поля или об увеличении количества недокоординированных атомов Ti. Другими словами, эти различия связаны с разными легирующими добавками, которые создают разные дефектные структуры в наночастицах. Небольшие дублеты при 456,0 и 456,6 эВ на этих рисунках соответствуют Ti 3+ государство; Хорошо известно, что легирование металлов усиливает дефектную структуру поверхности [22, 23]. О K рентгеновские спектры TiO 2 по краю НП и пять TM-TiO 2 содержат четыре пика при 529.9, 532.3, 537.9 и 543.7 эВ [24, 25]. Как упоминалось во введении, основная цель этого исследования - изучить электронные состояния TM-TiO 2 и влияние на их каталитическую активность. Интересно, что O K -кратные спектры показывают совершенно различную электронную структуру в зависимости от примесей переходных металлов. Как показано на O K -ребра, пики обусловлены переходом с O 1 s состояние незанятому p состояние, а из O 2 p состояние к O 2 p –Ti 3 d гибридное орбитальное состояние соответственно. Формы и интенсивность O K -краевые пики для Cr-TiO 2 , Mn-TiO 2 , и Ni-TiO 2 очень похожи на таковые для анатаза TiO 2 НП. Однако O K -ребра из Fe-TiO 2 и Co-TiO 2 указывают меньше на гибридную орбиталь (538 и 543 эВ), чем на чистый O 2 p переход (532,6 эВ). Другими словами, орбитали примесей Fe и Co менее гибридизованы с O 2 p орбитальный, включая TiO 2 по спектрам, что связано с каталитической активностью и будет обсуждаться снова.
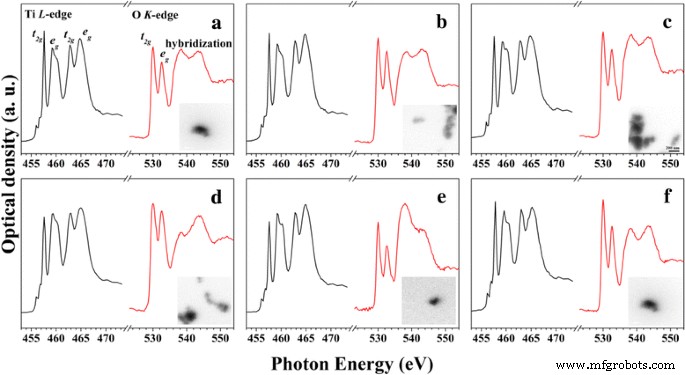
Спектры XAS (Ti L 2,3 -ребень и O K -edge) и соответствующие изображения в стопке для a анатаз TiO 2 , b Cr-TiO 2 , c Mn-TiO 2 , d Fe-TiO 2 , e Co-TiO 2 , и f Ni-TiO 2 (5 мол.% TM-TiO 2 НП). Размер наложенного изображения составляет 1 мкм × 1 мкм (шкала 200 нм)
Мы также измерили рамановские спектры TiO 2 НП и пять TM-TiO 2 . Как показано на рис. 2, электронные структуры TM-TiO 2 также обнаружены отличия по сравнению с анатазом TiO 2 скромно, по результатам спектроскопии комбинационного рассеяния света. Шесть образцов дают рамановский сдвиг около 395 (B 1g ), 514 (A 1 г ) и 636 см −1 (E g ), и они указывают на типичный анатаз TiO 2 пики [26]. Кроме того, мы обнаружили, что на каждом образце наблюдаются пики, вызванные легированными переходными металлами (Cr 2 О 3 :675,3 см −1 , MnO:644,5 см −1 , Fe 2 О 3 :614,2 см −1 , Co 2 О 3 :657,1 см −1 и NiO:564,8 см −1 ). Интересно, что мы выяснили, что легированные ионы переходных металлов превратились в стабильные формы оксидов металлов, и интенсивность E g пик TiO 2 NPs было немного ниже для TM-TiO 2 чем для анатаза TiO 2 НП. Мы также получили СЭМ (рис. 2) изображения TiO 2 НП и пять TM-TiO 2 для определения морфологии их поверхности. Изображения, полученные с помощью SEM, показывают, что они имеют разные структурные особенности и размеры. Cr-TiO 2 , Mn-TiO 2 , Fe-TiO 2 , Co-TiO 2 , и Ni-TiO 2 имеют однородную круглую или прямоугольную форму с размерами ~ 26, ~ 10, ~ 15, ~ 18 и ~ 16 нм соответственно. Эти пять TM-TiO 2 (TM =Cr, Mn, Fe, Co и Ni) значительно меньше, чем TiO 2 анатаза. НЧ (~ 40 нм:рис. 2а). Следовательно, возможно, что ионы Cr, Mn, Fe, Co и Ni могут изменить структуру TiO 2 НЧ, а затем могут действовать как центры зародышеобразования, которые способствуют образованию мелких частиц.
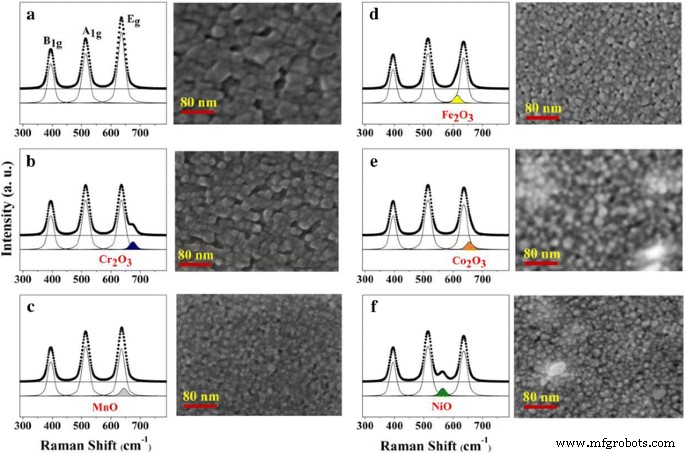
Рамановские спектры монодисперсного 5 мол.% TM-TiO 2 : а анатаз TiO 2 , b Cr-TiO 2 , c Mn-TiO 2 , d Fe-TiO 2 , e Co-TiO 2 , и f Ni-TiO 2 и соответствующие изображения SEM, соответственно
Чтобы более подробно изучить измененные электронные состояния, индуцированные легирующими добавками переходных металлов, мы зарегистрировали переходный металл L спектры XAS. На рис. 3a – e четко показаны электронные структуры пяти легирующих примесей переходных металлов, входящих в состав анатаза TiO 2 НП. Спектр на рис. 3а с пиками при 576,0 и 577,0 эВ с плечом 578,4 эВ соответствует типичному Cr 3+ L 3 -рочные результаты для Cr-TiO 2 [27]. Острый пик на рис. 3b при 639,2 эВ с небольшой особенностью при 640,7 эВ соответствует другим Mn 2+ L 3 -рёберные результаты [28]. Острый пик на рис. 3c при 708,5 эВ с небольшим пиком при 706,6 эВ соответствует другим Fe 3+ L 3 -рёберные результаты [29, 30]. Дублет на рис. 3d при 776,8 и 777,6 эВ - дублет Co 3+ L 3 -ребень [27]. Наконец, резкий пик при 850,3 эВ на рис. 3e с небольшим пиком при 852,2 эВ является типичным Ni 2+ L 3 -реберный спектр [30]. Эти результаты устанавливают электронные состояния легированных переходных металлов:Cr 2 О 3 , MnO, Fe 2 О 3 , Co 2 О 3 , и NiO соответственно.
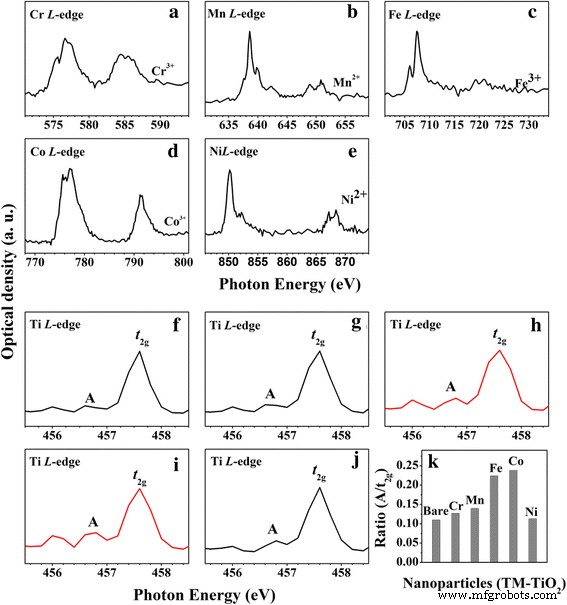
Легированный переходный металл L -крат и Ti L XAS-спектры 5 мол.% TM-TiO 2 : а и е Cr-TiO 2 , b и g Mn-TiO 2 , c и h Fe-TiO 2 , d и я Co-TiO 2 и e и j Ni-TiO 2 . к График соотношения предкраевого пика а и t 2 г пик для чистого TiO 2 и пять TM-TiO 2
Одна из наших задач - прояснить дефектные структуры, вызванные добавками переходных металлов в TM-TiO 2 в этом исследовании. Как показано на рис. 3f – j, можно заметить, что интенсивности для Fe-TiO 2 и Co-TiO 2 из двух предкраевых пиков при 456,7 и 457,4 эВ выше, чем у Cr-TiO 2 , Mn-TiO 2 , и Ni-TiO 2 (помечены a), что указывает на то, что эти пики обусловлены дефектными структурами поверхности (Ti 3+ состояние) [31]. Соотношения интенсивностей предкраевого пика (а) и t 2 г пик составляет 0,11, 0,127, 0,140, 0,224, 0,238 и 0,113 для TiO 2 , Cr-TiO 2 , Mn-TiO 2 , Fe-TiO 2 , Co-TiO 2 , и Ni-TiO 2 соответственно (см. рис. 3к). Этот результат означает, что Ti 3+ состояние присутствует в большем количестве в Fe-TiO 2 и Co-TiO 2 .
После подтверждения легирования переходным металлом анализом поверхности мы исследовали модуляцию запрещенной зоны, взяв спектры валентной зоны, как показано на рис. 4. Анатаз TiO 2 сообщалось, что ширина запрещенной зоны составляет ~ 3,2 эВ [32]. Как показано в спектрах валентной зоны на рис. 4a, максимум валентной зоны TM-TiO 2 сдвигается ниже по уровню Ферми (E F ) от 3,10 до 1,81 эВ (2,56 эВ, Cr-TiO 2 ; 2,52 эВ, Mn-TiO 2 ; 2,07 эВ, Fe-TiO 2 ; 1,81 эВ, Co-TiO 2 ; и 2,61 эВ, Ni-TiO 2 ). Исходя из этого, мы можем оценить, что легирование переходным металлом приводит к сужению запрещенной зоны, поскольку TiO 2 является полупроводниковым материалом n-типа, а E F в полупроводнике n-типа лежит близко к зоне проводимости. Сужение запрещенной зоны TM-TiO 2 возник в результате улучшения дефектных структур.
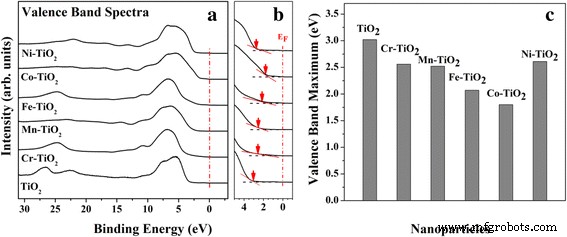
а Спектры валентности и b увеличенный вид края валентной зоны анатаза TiO 2 и пять TM-TiO 2 . c График максимальных значений валентной полосы TiO 2 и пять TM-TiO 2
В результате можно сделать вывод, что легированные переходные металлы образуют дефектные структуры TiO 2 НЧ, а затем способствуют уменьшению ширины запрещенной зоны в TM-TiO 2 (в специальном Fe-TiO 2 и Co-TiO 2 ). С таким пониманием вариаций структур и электронных свойств пяти TM-TiO 2 , теперь мы сравним эффекты легирования переходных металлов как точку их каталитической активности.
Электрохимическая окислительно-восстановительная реакция в водной фазе
CV были получены в растворе PBS, содержащем 0,01 М 2-АТФ, при различных типах GCE, облученных УФ-светом с длиной волны 365 нм. Как показано на рис. 5g, на чистом GCE наблюдается вялый ток окисления из-за медленного окисления 2-АТФ. Чтобы увеличить ток, связанный с окислением 2-АТФ, GCE, модифицированные TiO 2 и TM-TiO 2 Катализаторы-нафион изготовлены и испытаны, результаты показаны на рис. 5. Токи, связанные с окислением 2-АТФ, составляют 6,9 (± 1,4) мкА и 7,1 (± 1,6) мкА при использовании GCE, модифицированных Fe- TiO 2 и Co-TiO 2 соответственно - значительно больше (т.е. в 4,6 и 4,7 раза больше), чем значение 2,0 мкА, наблюдаемое при использовании только чистого GCE (рис. 5h). Напротив, токи, генерируемые при использовании анатаза TiO 2 НЧ, Cr-TiO 2 , Mn-TiO 2 , и Ni-TiO 2 составляют всего 2,7 (± 0,4) мкА, 4,4 (± 1,1) мкА, 2,8 (± 0,5) мкА и 2,9 (± 0,7) мкА соответственно, что незначительно (в 1,8, 2,9, 1,86 и 1,93 раза), но незначительно больше, чем для неизолированного электрода. Эти результаты показывают важность типа TM-TiO 2 для катализа реакций окисления, даже при использовании небольших количеств (5 мол.%) легированного переходного металла, и конкретно указать Fe-TiO 2 и Co-TiO 2 быть хорошими катализаторами окисления 2-АТФ.
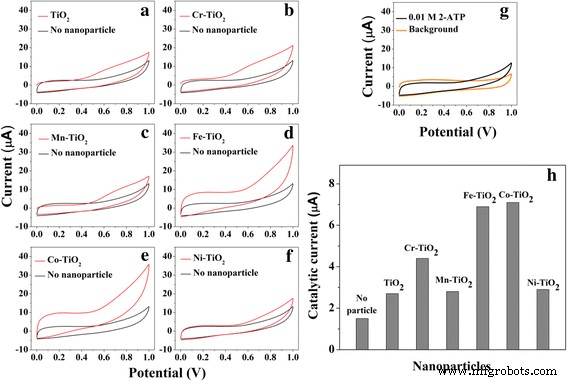
а - е CV (при скорости сканирования 50 мВ / с) в PBS, содержащем 0,01 M 2-ATP, на чистом GCE (черные линии) или GCE, модифицированных (красные линии) с 5 мол.% a анатаз TiO 2 , b Cr-TiO 2 , c Mn-TiO 2 , d Fe-TiO 2 , e Co-TiO 2 , и f Ni-TiO 2 . г Вялый ток окисления наблюдается на чистом GCE из-за медленного окисления 2-АТФ. ч Каталитические токи в результате электрохимического окисления 2-АТФ для различных типов анатаза TiO 2 и пять TM-TiO 2
Фотокаталитическое окисление 2-АТФ
Мы также определили прямую каталитическую активность TM-TiO 2 в окислении молекул 2-АТФ. S 2 p спектры ядра анатаза TiO 2 и 5 мол.% TM-TiO 2 были получены с HRPES после 180 мкл воздействия 2-АТФ в присутствии кислорода при УФ-освещении 365 нм (см. рис. 6a – f). Эти спектры содержат три различных 2 p 3/2 пики при 161,5, 162,9 и 168,6 эВ, которые относятся к S1, неограниченному состоянию C-SH, S2, связанному состоянию и S3, сульфоновой кислоте (SO 3 H) соответственно. Хорошо известно, что сульфоновая кислота является продуктом окисления тиоловых групп [33, 34]. Следовательно, мы можем контролировать окисление 2-АТФ, измеряя соотношение интенсивностей пиков S3 и S1. Рис. 6a – f подтверждает, что Fe-TiO 2 и Co-TiO 2 действуют как эффективные фотокатализаторы. Соотношения интенсивностей составляют 0,07, 0,12, 0,10, 0,27, 0,29 и 0,08 для анатаза TiO 2 . НЧ, Cr-TiO 2 , Mn-TiO 2 , Fe-TiO 2 , Co-TiO 2 , и Ni-TiO 2 соответственно, т.е. отношения Fe-TiO 2 и Co-TiO 2 также выше, чем у других наночастиц (см. рис. 6g). Этот результат тесно коррелирует с количеством дефектных структур в TM-TiO 2 показано на рис. 3. Измерения СТРМ подтверждают, что Fe-TiO 2 и Co-TiO 2 содержат больше Ti 3+ дефектные состояния (т.е. поверхностные дефектные структуры). Таким образом, эти результаты показывают, что увеличение количества Ti 3+ Дефектные структуры тесно коррелируют с усилением каталитической активности [7]. В результате Fe-TiO 2 и Co-TiO 2 , которые содержат много Ti 3+ состояния дефекта, имеют более высокую каталитическую активность.
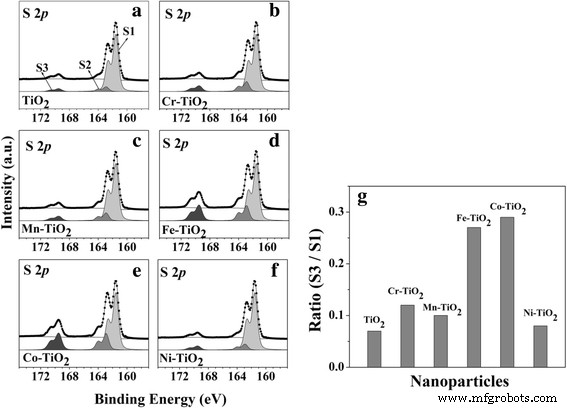
(Левая панель) HRPES S 2 p Спектры на уровне ядра, полученные после каталитического окисления 180 л 2-АТФ (насыщающее воздействие в нашей системе) на анатазе TiO 2 и 5 мол.% TM-TiO 2 ( а TiO 2 , b Cr-TiO 2 , c Mn-TiO 2 , d Fe-TiO 2 , e Co-TiO 2 , и f Ni-TiO 2 ). (Правая панель) g График отношения интенсивностей между S3 (- SO 3 H) и S1 (- SH) анатаза TiO 2 и пять TM-TiO 2 , что указывает на их каталитическую активность в окислении 2-АТФ, для экспозиции 180 л в УФ-свете 365 нм
По этой причине мы можем учитывать три фактора (зависимость от зарядового состояния, зависимость от дефектной структуры поверхности и гибридизацию между легированными переходными металлами и TiO 2 ), что может вызвать усиление каталитической активности TM-TiO 2 . Сначала влияние электронного зарядового состояния также было исследовано с помощью измерения СТРМ. Как показано на рис. 3a – e, мы подтверждаем, что ионы переходных металлов Cr, Fe и Co имеют TM 3+ зарядовые состояния, в то время как Mn и Ni имеют TM 2+ состояния заряда. Таким образом, можно сделать вывод об отсутствии корреляции между электронными зарядовыми состояниями допантов и каталитической активностью TM-TiO 2 . . Во-вторых, мы проверили зависимость дефектной структуры поверхности. Сравнение отношения интенсивностей предкраевого пика (A) и t 2 г пик, показанный на рис. 3, мы подтверждаем, что количество поверхностных дефектных структур составляет порядок Co-TiO 2 > Fe-TiO 2 > Mn-TiO 2 > Cr-TiO 2 > Ni-TiO 2 > TiO 2 . Как указывалось ранее, Fe-TiO 2 и Co-TiO 2 проявляют явное усиление каталитической активности. С увеличением поверхностных дефектных структур каталитическая активность TM-TiO 2 увеличивать. Контролируя соотношение перед краями, мы наблюдали четкую зависимость структуры поверхностных дефектов от повышения каталитической активности. Следовательно, дефектная структура поверхности влияет только на усиление каталитической активности TM-TiO 2 .
Наконец, еще одно разумное объяснение состоит в том, что согласно O K -ребро XAS, показанное на рис. 2, более высокая доля менее гибридизированных состояний кислорода (538 и 543 эВ) появляется в Fe-TiO 2 и Co-TiO 2 чем в другом TM-TiO 2 . Те переходы легированного переходного металла 3 d к O 2 p незанятое состояние может способствовать удалению атомов кислорода из TiO 2 наночастиц и усиливают каталитическое окисление 2-АТФ, поскольку сайт кислородной вакансии TiO 2 это активный сайт. Наконец, легирование TiO 2 Наночастица с Fe или Co дает более высокое увеличение каталитической активности для окисления 2-АТФ, чем легирование Cr, Mn или Ni.
Выводы
TM-TiO 2 синтезированные методом термосинтеза, были исследованы с помощью различных методов анализа поверхности. Чтобы сравнить каталитическую активность пяти TM-TiO 2 с анатазом TiO 2 НЧ мы контролировали их влияние на фотокаталитическое окисление молекул 2-АТФ с помощью HRPES и окисление 2-АТФ с помощью измерений EC. В зависимости от легированных переходных металлов мы четко исследовали, что увеличенная дефектная структура и меньшая гибридизация, вызванная легированными переходными металлами, влияют на повышенную каталитическую активность. В частности, Fe 3+ и Co 3+ ионы создают более эффективные различия в степени окисления, т. е. больше Ti 3+ дефектные структуры и поверхностные трансформации, чем ионы других металлов (Cr 3+ , Mn 2+ , и Ni 2+ ). В результате мы выяснили, что каталитические свойства Fe-TiO 2 и Co-TiO 2 превосходят анатаз TiO 2 НП и другие TM-TiO 2 (TM =Cr, Mn и Ni).
Сокращения
- HRPES:
-
Фотоэмиссионная спектроскопия высокого разрешения
- SEM:
-
Сканирующая электронная микроскопия
Наноматериалы
- Анализ первопричин с использованием метода 5 почему
- Биосовместимые наночастицы FePO4:доставка лекарств, стабилизация РНК и функциональная активность
- Получение и повышенная активность каталитического гидрирования наночастиц Sb / палигорскита (PAL)
- Влияние распределения наночастиц золота в TiO2 на оптические и электрические характеристики сенсибилизирован…
- Формирование и люминесцентные свойства нанокомпозитов Al2O3:SiOC на основе наночастиц оксида алюминия, модифици…
- Фотокаталитическая активность, усиленная Au-плазмонными наночастицами на фотоэлектроде нанотрубки TiO2, покры…
- Массивы нанотрубок TiO2:изготовлены с помощью мягко-твердого шаблона и зависимости характеристик эмиссии поля…
- Зеленая способность к синтезу и стабилизации наночастиц меди:каталитическая, антибактериальная, цитотоксич…
- Антибактериальная активность приготовленного in situ раствора наночастиц хитозана / серебра против метициллин…
- Влияние кислотного пептизирующего агента на соотношение анатаз-рутил и фотокаталитические характеристики н…



