CdS-модифицированный наночастицами α-Fe2O3 / TiO2 матричный фотоанод с наностержнями для эффективного фотоэлектрохимического окисления воды
Аннотация
В этой работе мы демонстрируем простой последовательный процесс адсорбции ионного слоя и реакции, сопровождаемый гидротермальным методом для синтеза модифицированного наночастицами CdS α-Fe 2 О 3 / TiO 2 массив наностержней для эффективного фотоэлектрохимического (ФЭП) окисления воды. Интегрируя CdS / α-Fe 2 О 3 / TiO 2 В тройной системе светопоглощающая способность фотоанода может быть эффективно улучшена с явно расширенным оптическим откликом на область видимого света, что значительно облегчает разделение фотогенерированных носителей, что приводит к повышению эффективности окисления воды PEC. Важно отметить, что для разработанной аномальной гетероструктуры II типа между Fe 2 О 3 / TiO 2 , положение зоны проводимости Fe 2 О 3 выше, чем у TiO 2 , фотогенерированные электроны из Fe 2 О 3 будет быстро рекомбинировать с фотогенерированными дырками из TiO 2 , таким образом, приводит к эффективному отделению фотогенерированных электронов от Fe 2 О 3 / дырки из TiO 2 на Fe 2 О 3 / TiO 2 интерфейс, значительно повышающий эффективность разделения фотогенерированных дырок в Fe 2 О 3 и увеличивает эффективность инжекции фотогенерированных электронов в TiO 2 . Работая как фотоанод ПЭК водного окисления, CdS / α-Fe 2 О 3 / TiO 2 гетероструктурный электрод демонстрирует улучшенную плотность фототока до 0,62 мА · см - 2 при 1,23 В по сравнению с обратимым водородным электродом (RHE) в щелочном электролите, с явно отрицательно смещенным начальным потенциалом 80 мВ. В этой работе представлены многообещающие методы повышения эффективности водного окисления ПЭК TiO 2 фотоаноды на основе гетероструктур.
Фон
Для решения серьезной проблемы загрязнения и ограниченных ресурсов ископаемых, фотоэлектрохимическое расщепление воды для производства водорода рассматривается как одна из наиболее многообещающих стратегий преобразования солнечной энергии. С момента первого отчета по окислению воды ПЭК на основе TiO 2 [1], TiO 2 привлек большое внимание как материалы фотоанодов для окисления воды ПЭК, благодаря своим стабильным свойствам ПЭК, сильному оптическому отклику и подходящему положению энергетической полосы [2, 3]. Тем не менее, эффективность ПЭК чистого TiO 2 photoanode в значительной степени ограничен кинетикой медленного окисления воды, происходящей из-за плохой способности к разделению фотогенерируемых носителей и недостаточной способности поглощения света [4, 5].
Поэтому были предприняты различные стратегии для улучшения характеристик водного окисления PEC чистого TiO 2, такие как модификация поверхности [6], сенсибилизация квантовых точек и построение гетеропереходов [7, 8]. Одним из эффективных методов повышения эффективности разделения фотогенерированных носителей является создание гетероструктурированного фотоанода. Например, построение гетероперехода между TiO 2 и другие металлооксидные полупроводники с согласованной структурой энергетических зон (например, Co 3 О 4 / TiO 2 [9] и ZnIn 2 S 4 / TiO 2 [10, 11]) может эффективно способствовать разделению фотогенерированных электронов и дырок; следовательно, эффективность водоразделения PEC чистого TiO 2 очевидно, может быть усилен. Среди различных полупроводников оксидов металлов гематит (α-Fe 2 О 3 ) считается перспективным материалом для фотоанодов из-за подходящей ширины запрещенной зоны (~ 2,0 эВ) для сбора солнечного света, отличной стабильности и низкой стоимости [12]. Кроме того, теоретическая эффективность преобразования энергии (PCE) α-Fe 2 О 3 может достигать 15,3%, при плотности фототока 12,6 мА · см - 2 при 1,23 В относительно обратимого водородного электрода (РВЭ) при стандартном солнечном облучении [13]. Следовательно, построение α-Fe 2 О 3 / TiO 2 гетероструктурированный фотоанод не только улучшает характеристики разделения носителей в TiO 2 но также эффективно расширяет диапазон поглощения света TiO 2 . Между тем, согласно некоторым последним исследованиям, α-Fe 2 О 3 фотоаноды страдают от короткого времени жизни электронно-дырочной пары и длины диффузии дырок (2–4 нм), что приводит к высокой скорости рекомбинации фотогенерированных носителей, что препятствует улучшению характеристик ФЭП [12]. В этом случае для дальнейшего улучшения характеристик водоотделения PEC Fe 2 О 3 / TiO 2 фотоаноды, некоторые полупроводники с узкой запрещенной зоной, такие как CdS [14, 15] и PbS [16], могут быть объединены для облегчения разделения фотогенерированных носителей. Среди них CdS / Fe 2 О 3 / TiO 2 Гетероструктурированный фотоанод считается перспективным выбором с согласованной шириной запрещенной зоны и расширенным диапазоном поглощения света. Кроме того, процесс транспортировки носителей может быть эффективно улучшен, поскольку фотогенерированные носители могут быть быстро разделены на границе раздела CdS / Fe 2 О 3 / TiO 2 , тем самым значительно снижая скорость рекомбинации носителей.
Более того, для создания усовершенствованного электрода для системы разделения воды PEC материалы электродов должны обладать такими характеристиками, как достаточная способность захвата падающего света и наличие туннелей для переноса заряда. По сравнению с обычными планарными фотоанодами, фотоаноды с массивом одномерных (1D) наностержней (NR) демонстрируют хорошие характеристики сбора падающего света из-за улучшенных процессов множественного рассеяния [17], что может привести к улучшенным характеристикам PEC-окисления воды. Кроме того, сообщается, что 1D матрица NR также демонстрирует отличные характеристики транспортировки носителей, поскольку фотогенерированные носители могут напрямую перемещаться по NR, таким образом, можно эффективно избежать прямой рекомбинации носителей на границе кристалла [18]. Кроме того, для дальнейшего увеличения площади поверхности таких массивов 1D NR, которые могут принести больше реакционных центров PEC и улучшить характеристики PEC, ожидается, что 1D NR с разветвленными наноструктурами [19]. Такая интегрированная архитектура предлагает длинный оптический путь для эффективного сбора света, короткое расстояние рассеивания для отличного переноса заряда и большую площадь поверхности для быстрого сбора межфазных зарядов, что имеет большое преимущество для улучшения характеристик PEC. Следовательно, было бы особенно интересно разработать модифицированный CdS Fe 2 О 3 / TiO 2 гетероструктурный массив NR для окисления воды PEC.
Здесь мы описали простой метод последовательной адсорбции и реакции в ионном слое (SILAR) -гидротермальный синтез CdS-модифицированного Fe 2 О 3 / TiO 2 Массив NR для эффективного окисления воды PEC. УФ-видимое исследование подтверждает соотношение CdS / Fe 2 О 3 / TiO 2 Массив NR демонстрирует превосходные оптические характеристики с очевидным расширенным диапазоном поглощения света. Об улучшении процесса переноса заряда и снижении скорости рекомбинации заряда можно судить по спектрам ФЛ и графикам EIS. Применяется как фотоанод для окисления воды ПЭК, CdS / Fe 2 О 3 / TiO 2 Массив NR демонстрирует значительно увеличенную плотность фототока 0,62 мА см - 2 (1,23 В относительно RHE) в щелочном электролите по сравнению с чистым TiO 2 (0,32 мА см - 2 при 1,23 В относительно RHE). Считается, что путь синтеза и применение CdS / Fe 2 О 3 / TiO 2 Представленные в настоящее время массивы NR имеют большое значение и могут применяться в других фотоэлектрических и фотоэлектронных устройствах.
Методы
Приготовление CdS / Fe 2 О 3 / TiO 2 Гетероструктурированный фотоанод NR
Синтез TiO 2 Массив NR
Для синтеза TiO 2 Массив NR на стекле FTO, FTO был разрезан на прямоугольник и подвергнут ультразвуковой очистке последовательно деионизированной водой, ацетоном и этанолом. Затем FTO помещали в автоклав, содержащий смешанный раствор деионизированной воды (20 мл), соляной кислоты (20 мл) и изопропоксида титана (1,1 мл), и прокаливали при 160 ° C в течение 6 часов. После реакции FTO несколько раз промывали деионизированной водой и этанолом, а затем отжигали на воздухе при 450 ° C в течение 0,5 ч.
Синтез Fe 2 О 3 / TiO 2 Массив NR
Для выращивания α-Fe 2 О 3 на TiO 2 NR, полученный TiO 2 Массив NR помещали в смешанный раствор FeCl 3 (15 мл, 0,1 М) и NaNO 3 (15 мл, 0,5 М), а затем перенесли в автоклав. Нагревая при 100 ° C в течение 2 ч, автоклав охлаждали до комнатной температуры и несколько раз промывали подложку FTO деионизированной водой и этанолом. Наконец, подложка FTO была отожжена на воздухе при 450 ° C в течение 1 часа.
Синтез CdS / Fe 2 О 3 / TiO 2 NR
Полученный α-Fe 2 О 3 / TiO 2 Массив NR предварительно обрабатывали этанольным раствором меркаптопропиновой кислоты (MPA, 0,3 M) в течение ночи при 50 ° C, а затем промывали этанолом для удаления избытка MPA. Для нанесения слоя CdS применяется простой метод последовательной адсорбции и реакции ионного слоя (SILAR). Предварительно обработанный массив NR был последовательно погружен в четыре различных раствора на 30 с, включая Cd (NO 3 ) 2 · 4H 2 О (этанол, 0,1 М), чистый этанол, Na 2 S · 9H 2 О (метанол, 0,2 М) и чистый метанол соответственно. Процесс SILAR повторяли пять раз, а затем субстрат промывали метанолом для удаления лишнего CdS.
Характеристики материалов
Фазовые структуры были охарактеризованы на порошковом рентгеновском дифрактометре (XRD) в диапазоне 2θ от 20 до 80 °. Морфологию продуктов изучали с помощью автоэмиссионной сканирующей электронной микроскопии (FE-SEM), прикрепленной к энергодисперсионной рентгеновской спектроскопии (EDS). Изображения просвечивающей электронной микроскопии (ПЭМ) получали с помощью оборудования Tecnai 20 U-Twin. Спектры поглощения и фотолюминесценции (ФЛ) были протестированы на TU-1900 и Hitachi U-4100 соответственно.
Характеристика фотоэлектрохимических характеристик
Характеристики водного окисления ПЭК характеризовали на электрохимической станции CHI660E с трехэлектродным режимом. Применяемый электролит состоял из 1M NaOH. Перед испытанием систему барботировали аргоном в течение 30 мин для удаления растворенного газа электролита. Вольтамперограммы с линейной разверткой (LSV) и хроноамперометрические I- t кривые были записаны при стандартном солнечном освещении (100 мВт / см - 2 ). Графики Мотта-Шоттки были измерены в темноте при частоте переменного тока 1,0 кГц.
В дальнейшем потенциал электрода был преобразован в потенциал RHE с помощью уравнения Нернста:
$$ {E} _ {\ mathrm {RHE}} ={E} _ {\ mathrm {Ag} / \ mathrm {AgCl}} + 0,059 \ \ mathrm {pH} + {E ^ o} _ {\ mathrm { Ag} / \ mathrm {AgCl}} $$ (1)где E RHE был преобразованный потенциал по сравнению с RHE, E Ag / AgCl был измеренный потенциал относительно Ag / AgCl электрода, и E о Ag / AgCl =0,1976 В при 25 ° C.
Результат и обсуждение
Характеристика структуры и морфологии
Фазовые структуры синтезированных продуктов характеризуются дифрактограммами на рис. 1. Как показано на рис. 1а, рутил TiO 2 Успешно синтезированы массивы наностержней (NR). Пики дифракции при 36,0 °, 44,1 °, 54,3 °, 62,7 °, 64,0 °, 65,4 ° и 69,8 ° хорошо соответствуют (101), (210), (211), (002), (310), (221). ) и (112) плоскости рутила TiO 2 (JCPDS. 21-1276). После осаждения Fe 2 О 3 дополнительные пики дифракции XRD при 32,9 ° и 45,2 ° могут быть отнесены к плоскостям (222) и (332) Fe 2 О 3 (JCPDS. 39-0238). Процесс SILAR применяется для выращивания наночастиц CdS, дифракционные пики при 26,4 °, 28,2 °, хорошо соответствующие плоскостям (002) и (101) CdS (JCPDS. 65-3414), подтверждают успешный рост наночастиц CdS на Fe 2 О 3 / TiO 2 . СЭМ-изображение на рис. 1b показывает, что TiO 2 НК равномерно выращиваются на подложке FTO диаметром 50 нм. Поверхность NR относительно гладкая. После роста Fe 2 О 3 на поверхности TiO 2 , диаметр Fe 2 О 3 / TiO 2 имеет больший размер и увеличивается до 60 нм. Кроме того, поверхность NR становится более шероховатой. Дальнейшее осаждение наночастиц CdS может вызвать увеличение диаметра Fe 2 О 3 / TiO 2 композитный NR. Для дальнейшего подтверждения элементного распределения полученного CdS / Fe 2 О 3 / TiO 2 NR, изображения сопоставления EDS в поперечном разрезе записываются и отображаются в Дополнительном файле 1:Рисунок S1, Дополнительный файл 2:Рисунок S2. Видно, что элементы Ti, Fe, Cd и S равномерно распределены по образцам.
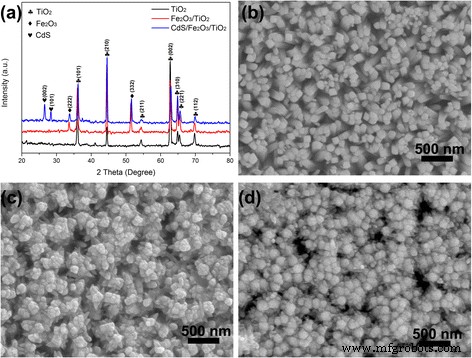
а Диаграммы XRD и b СЭМ изображения TiO 2 NR, Fe 2 О 3 / TiO 2 NR и CdS / Fe 2 О 3
Изображение HRTEM и выбранная область электронограммы (SAED) CdS / Fe 2 О 3 / TiO 2 NR показаны на рис. 2. Видно, что оба TiO 2 и Fe 2 О 3 хорошо кристаллизуются, а наночастицы CdS растут на поверхности Fe 2 О 3 . Шаг решетки 0,31, 0,27 и 0,21 нм может хорошо соответствовать плоскости (101), (222) и (210) CdS, Fe 2 О 3 , и TiO 2 соответственно (рис. 2а). Видны дифракционные кольца от записанной картины SAED на рис. 2b, которые могут быть хорошо проиндексированы по плоскостям (101), (210) рутилового TiO 2 , (222), (332) плоскости Fe 2 О 3 , и (002), (101) плоскости CdS соответственно. Результаты ПЭМ хорошо согласуются с результатами исследования XRD.

а ВРЭМ изображение CdS / Fe 2 О 3 / TiO 2 NR. Отмеченный d-интервал 0,31 нм хорошо соответствует плоскости (101) CdS, d-интервал 0,27 нм хорошо соответствует плоскости (222) Fe 2 О 3 и d-интервал 0,21 нм хорошо соответствуют плоскости (210) TiO 2 . б Электронограмма с выбранной областью CdS / Fe 2 О 3 / TiO 2 NR дифракционные кольца соответствуют плоскостям (002), (101) CdS, (222), (332) плоскостям Fe 2 О 3 и (101), (210) плоскости TiO 2
Химический состав и валентные состояния CdS / Fe 2 О 3 / TiO 2 гибридные NR изучены с помощью XPS-спектров. На рис. 3а представлены обзорные спектры, продемонстрировано наличие элементов Ti, Fe, O, Cd, S. Внешний вид элемента C соответствует защитной оболочке на основе углерода. Для XPS-спектра Ti 2p на рис. 3b эти разделенные два отдельных пика при 458,2 и 464,2 эВ могут быть отнесены к Ti 2 p 3/2 и 2 п 1/2 из TiO 2 [20]. Спектр РФЭС Fe 2p показан на рис. 3в. Видны два отчетливых пика при 710,6 и 724,10 эВ, которые хорошо соответствуют Fe 2 p 3/2 и 2 п 1/2 пики α-Fe 2 О 3 [21]. XPS-спектр остовного уровня O 1s показан на рис. 3d, где пик при 531,2 эВ отнесен к связи Ti – O между титаном и кислородом, а пик при 531,9 эВ может быть отнесен к связи Fe – O между железо и кислород [20, 21]. На рис. 3д показан XPS-спектр Cd, относящегося к Cd 3d 5/2 при 405,2 эВ. Спектр РФЭС S 2P показан на рис. 3е [22]. Центральный пик разделен на два пика S 2p 1/2 и 2р 3/2 при 161,5 и 162,6 эВ [22].
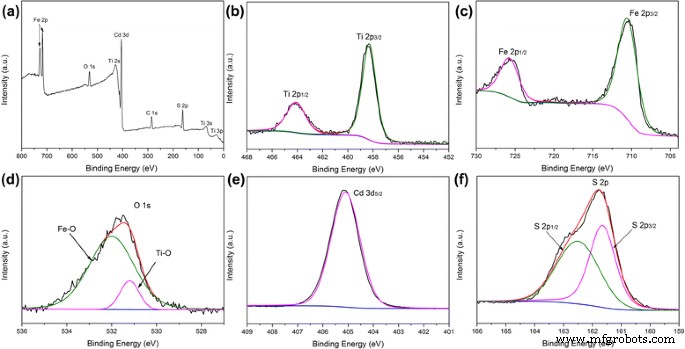
а XPS-спектры CdS / Fe 2 О 3 / TiO 2 Пример NR, b XPS-спектры Ti 2p, включая Ti 2p 1/2 и Ti 2p 3/2 , c XPS-спектры Fe 2p, включая Fe 2p 1/2 и Fe 2p 3/2 , d XPS-спектры O 1, включая связь Fe – O и связь Ti – O, e XPS-спектры Cd 3d 5/2 , и f XPS-спектры S 2p, включая S 2p 1/2 и S 2p 3/2
На рис. 4а показаны спектры поглощения различных фотоэлектродов. TiO 2 показывает типичный край полосы поглощения при 400 нм, который может быть отнесен к собственной запрещенной зоне поглощения TiO 2 (3,2 эВ). После связывания с Fe 2 О 3 , Fe 2 О 3 / TiO 2 показывает повышенное поглощение в области видимого света примерно при 540 нм. Расширение края полосы поглощения связано с видимой составляющей Fe 2 О 3 (2,0–2,2 эВ). После дальнейшей модификации наночастиц CdS край поглощения света может быть увеличен до 580 нм. Это подтверждает, что соединение TiO 2 с Fe 2 О 3 и CdS может эффективно настраивать свойство поглощения света на область видимого света. Спектр фотолюминесценции (ФЛ) применяется для изучения влияния включения CdS и Fe 2 О 3 в CdS / Fe 2 О 3 / TiO 2 гибрид на транспорт и рекомбинационное поведение фотогенерированных носителей. Чем меньше интенсивность пика ФЛ, тем выше эффективность разделения пар фотогенерированных носителей в образцах. На рис. 4б представлены спектры ФЛ TiO 2 . , Fe 2 О 3 / TiO 2 , и CdS / Fe 2 О 3 / TiO 2 образцы. Очевидно, что Fe 2 О 3 / TiO 2 NR обеспечивает более низкую скорость рекомбинации носителей, чем чистый TiO 2 , и CdS / Fe 2 О 3 / TiO 2 NR обеспечивает лучшую транспортную производительность.
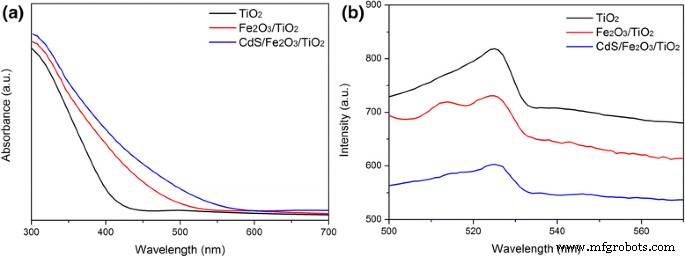
а Спектры поглощения в УФ-видимой области и b Спектры ФЛ TiO 2 NR, Fe 2 О 3 / TiO 2 NR и CdS / Fe 2 О 3 / TiO 2 Примеры NR
Чтобы дополнительно подтвердить этот вывод, графики переходных процессов флуоресценции с пикосекундным разрешением были протестированы и показаны как Дополнительный файл 3:Рисунок S3. Средний срок службы τ рассчитывается согласно τ =(В 1 τ 1 [2] + B 2 τ 2 [2]) / (B 1 τ 1 + B 2 τ 2 ), а постоянная времени переходных процессов флуоресценции на длине волны 511 нм указана в Дополнительном файле 4:Таблица S1 [23]. Видно, что после модификации чистого TiO 2 с Fe 2 О 3 время жизни фотогенерированных носителей увеличивается. В сочетании с CdS срок службы носителей может быть увеличен. Этот результат, очевидно, демонстрирует, что эффективность разделения зарядов может быть эффективно улучшена за счет образования CdS / Fe 2 О 3 / TiO 2 многопереходный.
Возможный процесс транспортировки носителей показан на рис. 5. В CdS / Fe 2 О 3 / TiO 2 тройная система, поскольку положение зоны проводимости и валентной зоны CdS выше, чем у Fe 2 О 3 , фотоиндуцированные электроны в CdS будут перенесены в зону проводимости Fe 2 О 3 , а фотоиндуцированные дыры в валентной зоне в Fe 2 О 3 будет перенесен на CDS. Для разработанной аномальной гетероструктуры II типа между Fe 2 О 3 / TiO 2 , положение зоны проводимости Fe 2 О 3 выше, чем у TiO 2 . При освещении солнечным светом фотовозбужденные электронно-дырочные пары будут генерировать оба в TiO 2 и Fe 2 О 3 . Фотогенерированные электроны в зоне проводимости Fe 2 О 3 немедленно переместится в валентную зону TiO 2 для рекомбинации с фотогенерированными дырками, тем самым значительно улучшая эффективность разделения фотогенерированных дырок в Fe 2 О 3 и увеличивает эффективность инжекции фотогенерированных электронов в TiO 2 [24, 25]. Это означает, что связывание TiO 2 с Fe 2 О 3 и CdS может эффективно снижать скорость рекомбинации пар фотогенерированных носителей. Между тем фотогенерированные электроны в TiO 2 перейти к противоэлектроду, где происходит реакция восстановления. Итак, аномальная гетероструктура II типа между Fe 2 О 3 / TiO 2 играет важную роль в улучшении характеристик окисления воды PEC.
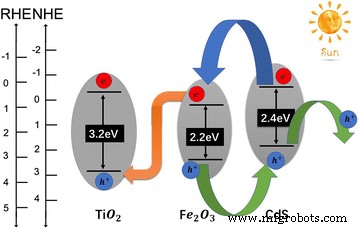
Относительное положение полос CdS / Fe 2 О 3 / TiO 2 тройная система
На рисунке 6 показаны вольтамперограммы с линейной разверткой (LSV) и хроноамперометрические I- t . кривые CdS / Fe 2 О 3 / TiO 2 , Fe 2 О 3 / TiO 2 , и TiO 2 образцы. Как показано на рис. 6а, плотность фототока фотоанодов при освещении постепенно увеличивается после взаимодействия с α-Fe 2 О 3 и наночастицы CdS, а также CdS / Fe 2 О 3 / TiO 2 Образец NR показывает самую большую плотность фототока 0,61 мА · см - 2 при 1,2 В по сравнению с RHE, что почти вдвое больше, чем у чистого TiO 2 образец. Я- т кривые при потенциале смещения 1,2 В в зависимости от RHE при прерывистом освещении показаны на рис. 6b, можно видеть, что образцы остаются превосходной стабильностью и хорошими характеристиками оптического отклика при прерывистом освещении. CdS / Fe 2 О 3 / TiO 2 Образец NR поддерживает плотность фототока около 0,6 мА см - 2 , что соответствует кривым LSV.
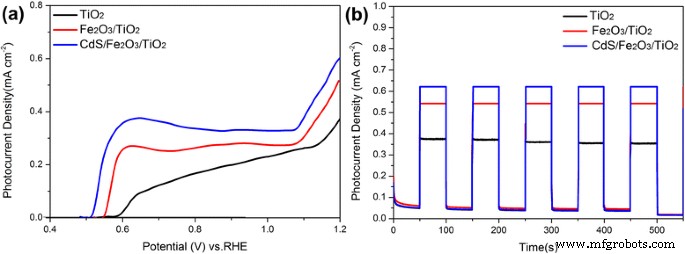
а Кривые LSV TiO 2 NR, Fe 2 О 3 / TiO 2 NR и CdS / Fe 2 О 3 / TiO 2 Освещение образцов NR в 1M NaOH, b хроноамперометрический I- t кривые при потенциале смещения 1,2 В при прерывистом освещении
Измерение EIS выполняется при освещении, и графики Найквиста показаны на рис. 7a и в дополнительном файле 5:на рис. S4. Они демонстрируют, что графики Найквиста имеют два полукруга с последовательным контактным сопротивлением ( R s ) на подложке FTO. Маленький полукруг на графиках Найквиста объясняется сопротивлением переносу заряда на границе электрод / электролит, а большой полукруг представляет сопротивление переносу заряда, связанное с переносом / рекомбинацией электронов в материалах фотоанода. Листовое сопротивление ( R s ) подложки сопротивление переносу заряда противоэлектрода ( R ct1 ) и сопротивление переносу заряда ( R ct2 ) были смоделированы с помощью программного обеспечения Zview, и соответствующие данные показаны в Дополнительном файле 6:Таблица S2. Приспособленный R s и R ct1 значения для всех образцов аналогичны из-за одинаковой конфигурации и использования растущих субстратов, в то время как R ct2 значения явно показывают вариации 1079,5, 880,6 и 679,5 Ом для TiO 2 , Fe 2 О 3 / TiO 2 , и CdS / Fe 2 О 3 / TiO 2 , соответственно. Видно, что после модификации TiO 2 с Fe 2 О 3 и CdS, кинетика межфазного переноса заряда значительно улучшена.
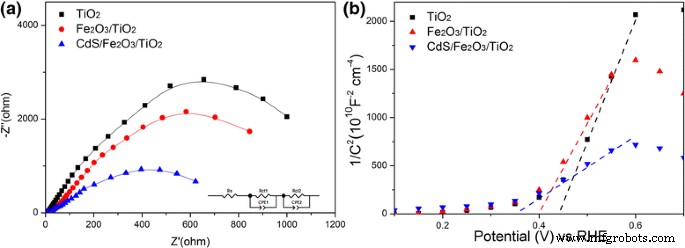
а Спектры EIS, измеренные при потенциале смещения 1,2 В при освещении и b Графики Мотта-Шоттки, полученные с частотой 1 кГц в темноте для TiO 2 NR, Fe 2 О 3 / TiO 2 NR и CdS / Fe 2 О 3 / TiO 2 Примеры NR
Графики Мотта-Шоттки для полученных образцов приведены на рис. 7b. Наклоны, определенные из графиков Мотта-Шоттки, используются для оценки плотности носителей в соответствии со следующим уравнением [26]:
Nd =\ (\ frac {2} {e_0 {\ varepsilon \ varepsilon} _0} \ times \ left [\ frac {dV} {d \ left (1, /, {C} ^ 2 \ right)} \ right] \)
где e 0 - заряд электрона, ε диэлектрическая проницаемость образца, ε 0 - диэлектрическая проницаемость вакуума, Nd - донорная плотность, а V приложенное напряжение. Как правило, относительно меньший наклон означает более высокую плотность носителей.
Потенциал плоской зоны можно оценить по следующему уравнению:
$$ \ frac {1} {C ^ 2} =\ frac {2} {e_0 {\ varepsilon \ varepsilon} _0 \ mathrm {Nd}} \ times \ left [E- {E} _ {\ mathrm {fb} } - \ frac {kT} {e} \ right] $$Потенциал плоской зоны ( E fb ) определяется взятием x пересечение линейной аппроксимации графика Мотта-Шоттки, 1 / C 2 , как функция приложенного потенциала ( E ). Кроме того, замечательный катодный сдвиг плоского потенциала с 0,44 В для TiO 2 образец до 0,36 В для CdS / Fe 2 О 3 / TiO 2 Образец NR не наблюдался. Это говорит о большем скоплении электронов в гетеропереходе и отражает уменьшение рекомбинации заряда.
Следует отметить, что характеристики PEC-водного окисления синтезированного образца CdS / Fe2O3 / TiO2 сопоставимы с некоторыми аналогичными работами. Например, Sharma et al. сообщил Fe-TiO 2 / Zn-Fe 2 О 3 тонкие пленки с производительностью 0,262 мА · см - 2 при 0,95 В (относительно SCE) [27], а FTO / Fe 2 О 3 / ZnFe 2 О 4 фотоанод обеспечивает плотность фототока 0,4 мА см - 2 [28]. Кроме того, для сообщенного Fe 2 О 3 / TiO 2 фотоаноды с нанотрубками, плотность фототока 0,5 мА см - 2 достигается [29, 30]. Сравнивая с родственными работами, видно, что полученный CdS / Fe 2 О 3 / TiO 2 фотоанод действительно обеспечивает выдающиеся и надежные характеристики водоразделения PEC.
Выводы
В заключение, простой метод последовательной адсорбции и реакции ионного слоя (SILAR) -гидротермальный разработан для производства CdS-модифицированного Fe 2 О 3 / TiO 2 Массив NR для эффективного окисления воды PEC. УФ-видимое исследование подтверждает соотношение CdS / Fe 2 О 3 / TiO 2 Массив NR демонстрирует превосходные оптические характеристики с очевидным расширенным диапазоном поглощения света. Применяется как фотоанод для окисления воды ПЭК, CdS / Fe 2 О 3 / TiO 2 Фотоанод с матрицей NR демонстрирует значительно увеличенную плотность фототока - 0,62 мА · см - 2 (1,23 В относительно RHE) в щелочном электролите по сравнению с чистым TiO 2 (0,32 мА см - 2 при 1,23 В по сравнению с RHE).
Наноматериалы
- Композиты с квантовыми точками на S, N-графене / TiO2 для эффективного фотокаталитического производства водород…
- Замещающее легирование для алюмосиликатного минерала и превосходное расщепление воды
- Исследование каркаса Zr – металл – органика как эффективного фотокатализатора для производства водорода
- Иерархическая гетероструктура полых сфер ZnO @ TiO2 для высокоэффективного фотокаталитического выделения водор…
- Нанокристалл Sb2O3, легированный S:эффективный катализатор в видимом свете для разложения органических веществ
- Простой синтез углеродных точек полидофамина в одной емкости для фототермической терапии
- Хорошо выровненные массивы нанотрубок TiO2 с наночастицами Ag для высокоэффективного обнаружения ионов Fe3 +
- Эффективная обработка поверхности TiO2 с использованием Cs2CO3 для солнечных батарей планарного типа Sb2S3, обрабат…
- Повышение производительности солнечных элементов, сенсибилизированных квантовыми точками CdS / CdSe, с помощью …
- Использование системы мониторинга уровня реки на основе IoT для эффективного управления водными ресурсами



