Фотокаталитические свойства порошков TiO2 с покрытием Co3O4, полученных методом плазменного осаждения атомного слоя
Аннотация
Со 3 О 4 коммерческий TiO с покрытием 2 порошковые (P25) фотокатализаторы p-n-перехода были приготовлены методом плазменного осаждения атомных слоев (PEALD). Систематически исследовались структура, морфология, ширина запрещенной зоны и фотокаталитические свойства в ультрафиолетовом свете. Хотя отложение Co 3 О 4 не изменяет структуру анатаза и размер кристаллитов порошков Р25, заметно улучшается ультрафиолетовая фотокаталитическая активность. Для Co 3 О 4 -покрытые порошки P25, следовые ионы Co существуют в виде Co 3 О 4 наночастицы, прикрепленные к TiO 2 поверхность порошка вместо заполнения Ti 4+ положение в TiO 2 решетка. Ко 3 О 4 Порошки P25 с покрытием демонстрируют повышенную эффективность фотокаталитического разложения метиленового синего почти на 100% за 1,5 часа в ультрафиолетовом свете по сравнению с P25, равным 80%. Графики Мотта-Шоттки порошков фотокатализаторов подтверждают образование p-n-гетероперехода в Co 3 О 4 –TiO 2 нанокомпозитные материалы, что способствует повышению эффективности разделения фотогенерируемых электронов и дырок. Кроме того, Co 3 О 4 покрытие также способствует адсорбции органических красителей метиленового синего на порошках P25.
Фон
С быстрым развитием современной промышленности загрязнение воды стало серьезной проблемой [1, 2]. Органические красители обладают токсическим действием и уменьшают проникновение света в загрязненную воду [3]. Более того, большинство красителей для текстиля устойчиво к химическому окислению и другим традиционным методам очистки сточных вод. К счастью, TiO 2 фотокатализаторы на основе демонстрируют отличную деградацию до органических красителей [4]. TiO 2 был широко и интенсивно изучен как один из популярных фотокаталитических материалов из-за его низкой токсичности, высокой химической стабильности и каталитической активности в устранении большого количества органических загрязнителей [5,6,7]. Однако его общая квантовая эффективность относительно невысока из-за высокой скорости рекомбинации фотогенерированных электронно-дырочных пар [8]. Кроме того, собственная большая запрещенная зона TiO 2 ограничивает свое оптическое поглощение УФ-областью, на которую приходится менее 4% всего солнечного излучения [9, 10]. Эти недостатки препятствуют его практическому применению. Следовательно, были исследованы различные подходы для улучшения его фотокаталитической активности, включая легирование металл / неметалл [11, 12], сенсибилизацию красителем [13] и образование гетеропереходов [14, 15].
Было продемонстрировано, что построение p-n гетероперехода между TiO 2 n-типа и полупроводник p-типа, такой как NiO или Ag 2 O полезен для снижения скорости рекомбинации фотогенерированных электронов и дырок [16,17,18]. Во-первых, p-n-переход может создавать встроенный потенциал на границе раздела полупроводников. При освещении внутреннее электрическое поле будет способствовать разделению и транспортировке фотогенерированных электронно-дырочных пар [19]. Во-вторых, полупроводники с меньшей шириной запрещенной зоны могут увеличивать поглощение света катализатором с большей шириной запрещенной зоны [20]. Более того, некоторые полупроводники также могут быть использованы для повышения стабильности катализатора и облегчения поверхностных электрохимических реакций [21]. В результате фотокаталитическая активность может быть значительно улучшена за счет образования гетероперехода полупроводник / полупроводник. Chen et al. сообщили, что p-n переход NiO / TiO 2 фотокатализатор показал улучшенную фотоактивность при разложении метиленового синего (МБ) [22].
Со 3 О 4 , один из наиболее универсальных оксидов переходных металлов, широко применяется во многих областях, таких как деградация красителей [23, 24], газовые сенсоры [25], литий-ионные батареи [26], окисление CO при низкой температуре [27] , и H 2 поколение [28]. Со 3 О 4 , как NiO и Ag 2 O, относится к полупроводникам p-типа. Его запрещенная зона (2,1 эВ) относительно уже по сравнению с шириной запрещенной зоны NiO (3,5 эВ). Более того, он показывает лучшую химическую стабильность, чем Ag 2 . О, потому что Ag 2 O склонен поглощать CO 2 в воздухе с образованием Ag 2 CO 3 или разлагается на Ag при сравнительно высокой температуре [28]. Сообщалось, что p-n Co 3 О 4 / BiVO 4 или Co 3 О 4 / TiO 2 переход проявлял более высокую фотокаталитическую активность, чем отдельный полупроводник из BiVO 4 или TiO 2 в удалении органических красителей [29, 30].
Для синтеза Co 3 было использовано довольно много методов. О 4 наносистемы на основе, такие как химическое осаждение из паровой фазы (CVD) [31,32,33], плазменное напыление [34] и процессы CVD с использованием плазмы (PECVD) [35,36,37]. Ко 3 О 4 / TiO 2 p-n переход был также изготовлен методом пропитки-осаждения-разложения [30]. Требовалось последующее прокаливание и возбуждение, что могло привести к выбросу выхлопных газов.
Осаждение атомных слоев (ALD) - это новый метод нанесения тонких пленок, основанный на последовательных самоограниченных и дополнительных реакциях поверхностной хемосорбции с использованием пара прекурсора. По сравнению с методами CVD, PECVD и химического раствора, он обладает уникальными преимуществами, включая однородность большой площади, превосходную трехмерную конформность, точное и простое управление толщиной пленки, гибкую модификацию поверхности и низкую температуру обработки [38]. Плазменно-усиленное осаждение атомных слоев (PEALD), когда плазменные частицы используются в качестве реактивного газа на одном этапе процесса циклического осаждения, демонстрирует некоторые преимущества по сравнению с термическим ALD, такие как большая свобода от температуры подложки и прекурсоров. В последнее время ALD продемонстрировал растущие перспективы и широкое применение в различных областях, таких как полупроводники [39], новая энергия [40] и фотокатализ [41], особенно в модификации поверхности наноматериалов [42].
Здесь проследите Co 3 О 4 TiO с покрытием 2 Фотокатализатор на p-n переходе был изготовлен методом ALD. По сравнению с методом пропитки-осаждения-разложения с многоступенчатыми процедурами [30], метод ALD имеет только одноэтапное осаждение и низкую температуру обработки 200 ° C без последующего отжига. Кристаллическая структура, морфология, состав и запрещенная зона Co 3 О 4 порошки P25 с покрытием были охарактеризованы различными аналитическими методами. Фотокаталитическая активность Co 3 О 4 порошки P25 с покрытием со 100 и 200 циклами разложения метиленового синего (МБ) красителя под воздействием ультрафиолетового (УФ) излучения были глубоко исследованы. Можно обнаружить, что, в отличие от чистых порошков P25, 100-цикловый Co 3 О 4 Образец p-n-перехода P25 с покрытием демонстрирует заметно увеличенную УФ-фотокаталитическую эффективность. Возможный фотокаталитический механизм Co 3 О 4 TiO с покрытием 2 порошки также предлагаются.
Методы
Коммерческий TiO 2 порошки (P25) использовались в качестве вспомогательных веществ для Co 3 О 4 осаждение. Порошки P25 равномерно загружали в пористый контейнер и помещали в камеру PEALD (SUNALE R-200, Picosun). Дикарбонилциклопентадиенилкобальт (CoCp (CO) 2 , Strem Chemicals, 96%) выдерживали при 45 ° C, а кислородную плазму при комнатной температуре использовали в качестве прекурсора кобальта и источника кислорода для Co 3 О 4 осаждения соответственно. Кислород высокой чистоты (99,999%) использовался в качестве источника кислородной плазмы с аргоном (99,999%) в качестве газа-носителя, а мощность плазмы и O 2 расход газа составлял 2500 Вт и 160 см3 соответственно. Затем 100- и 200-тактный Co 3 О 4 были нанесены на порошки P25 при 200 ° C с помощью PEALD, где один цикл состоял из 0,2 с CoCp (CO) 2 дозирование, 6 с N 2 продувка, 21,5 с O 2 дозирование плазмы и 6 с N 2 продувка. Для 600-тактного Co 3 О 4 Образец P25 с покрытием, в качестве источника кислорода использовался поток кислорода (130 см3 / см3) вместо кислородной плазмы. Температура прекурсора Со и реактора не изменилась. Следовательно, 600-тактный Co 3 О 4 были нанесены на порошки P25 методом термической ALD, где один цикл состоял из 2 с CoCp (CO) 2 дозирование, 8 с N 2 продувка, 5 с O 2 дозирования, и 10 с N 2 продувка. В нашей предыдущей работе было продемонстрировано, что PEALD Co 3 О 4 на углеродных нанотрубках показали низкую скорость осаждения и режим роста островков [43]. Толщина 800- и 2400-тактного Co 3 О 4 составляла 5 и 20 нм соответственно. Шероховатая поверхность осаждения была покрыта Co 3 О 4 наночастицы. Следовательно, 100- и 200-тактный Co 3 О 4 осаждение на P25 может все еще находиться на стадии зародышеобразования, что может привести к образованию Co 3 О 4 наночастицы TiO с покрытием 2 Структура p-n перехода.
Кристаллическая структура Co 3 О 4 порошки P25 с покрытием были охарактеризованы дифракцией рентгеновских лучей (XRD, Rigaku-D / max 2000) с излучением Cu Kα (λ =0,15418 нм). Угол сканирования составлял от 10 ° до 80 ° при 40 кВ и 40 мА. Химические свойства поверхности анализировали с помощью рентгеновской фотоэлектронной спектроскопии (XPS, Thermo ESCALAB-Thermo fisher K-alpha) с использованием излучения Al Kα (1486,6 эВ) в качестве источника возбуждения. Все энергии связи относятся к пику C 1s при 284,6 эВ. Для измерения содержания элементов Co в порошках фотокатализаторов была проведена масс-спектрометрия с индуктивно связанной плазмой (ICP-MS, Thermo X Series 2 ICP-MS).
Микроструктура и морфология поверхности порошков были охарактеризованы с помощью автоэмиссионной сканирующей электронной микроскопии (FESEM, Ultra 55, ZRISS) и просвечивающей электронной микроскопии (TEM, FEI Tecnai G 2 F20 S-Twin). Порошки катализатора полностью диспергировали в этаноле с помощью 20-минутной ультразвуковой вибрации перед тем, как капать на медную сетку с ультратонкой углеродной фольгой для наблюдения с помощью ПЭМ. Удельные площади поверхности Брунауэра-Эммета-Теллера (БЭТ) определяли с использованием аппарата для адсорбции азота (Micromeritics Tristar-3000).
Фотокаталитическая активность Co 3 О 4 TiO с покрытием 2 порошков при разложении метиленового синего (МБ) оценивали при облучении 100-ваттной УФ светодиодной лампой (UVEC-411). Циркуляционная охлаждающая вода использовалась для поддержания температуры системы на уровне ~ 25 ° C. Лампа располагалась на расстоянии 15 см от реакционного раствора. Пятьдесят миллиграммов катализатора добавляли в 50 мл водного раствора МБ (37,4 мг / л). Перед освещением смешанный раствор перемешивали в течение 3 ч в отсутствие света для достижения адсорбционного равновесия. После каждого заданного времени облучения отбирали около 4 мл смеси и разделяли центрифугированием для удаления суспендированного твердого катализатора. Процесс разложения контролировали по спектру поглощения в УФ-видимой области (UV-3600, Shimadzu, Япония), а концентрацию остаточного МБ анализировали количественно, измеряя максимальное поглощение при 664 нм.
Фотокаталитическая активность Co 3 в видимом свете О 4 TiO с покрытием 2 порошков также оценивали по разложению метилового оранжевого (МО) в водном растворе. Имитатор солнечного света (лампа Xe 300 Вт, MircoSolar300, PerfectLight) с фильтром отсечки 420 нм обеспечивает облучение видимым светом. Концентрация остаточной МО определялась путем измерения максимального поглощения МО при 464 нм.
Графики Мотта-Шоттки измеряли на электрохимической станции (CHI Instruments CHI760E) на частотах 1 и 2 кГц в темноте. Пятьдесят два миллиграмма P25 или 200-цикл Co 3 О 4 порошки P25 с покрытием вместе с 18 мг йода диспергировали в 50 мл ацетона с помощью ультразвуковой вибрации. Затем смешанную суспензию наносили гальваническим способом на проводящее стекло из оксида олова, легированного фтором (FTO), при напряжении 15 В в течение 2 мин. Электрохимические измерения проводили в 1 М электролите NaOH при комнатной температуре с использованием трехэлектродной конфигурации. Свежеприготовленное стекло FTO с фотокатализатором было принято в качестве рабочего электрода. Платиновая сетка (1 см × 2 см) и Ag / AgCl использовались в качестве противоэлектрода и электрода сравнения соответственно. Изоэлектрическая точка (IEP) MB, P25 и 200-цикла Co 3 О 4 P25 с покрытием в водных растворах определяли с использованием измерения дзета-потенциала (Malvern Zetasizer, Nano ZS 90 zeta).
Результаты и обсуждение
XRD использовался для определения фазовой структуры образцов. На рисунке 1 представлены дифрактограммы чистого P25 и 200-циклового Co 3 . О 4 порошки P25 с покрытием. Оба образца демонстрируют аналогичные характеристические пики стандартного анатаза TiO 2 . (Карточка JCPDS №:21–1272), предполагая, что нет очевидных изменений в кристаллической структуре после Co 3 О 4 покрытие. Кроме того, размер кристаллитов обоих образцов можно оценить в 20 ± 2 нм по формуле Шеррера.
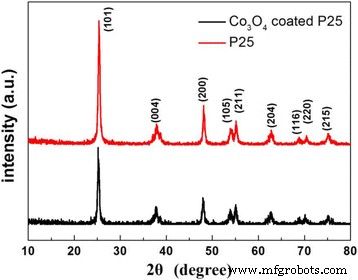
Рентгенограммы чистого P25 и 200-циклового Co 3 О 4 порошки P25 с покрытием
СЭМ и ПЭМ использовались для наблюдения морфологии и микроструктуры чистого P25 и 200-циклового Co 3 О 4 порошков P25 с покрытием, как показано на рис. 2a – d. Чистый P25 и 200-цикл Co 3 О 4 Образцы P25 с покрытием имеют аналогичную морфологию и размер кристаллитов 15–30 нм (рис. 2а, б). Распределение наночастиц по размерам также было рассчитано, как показано на рис. 2e, f, которое может быть подогнано к гауссовым кривым. Расчетное среднее значение размеров кристаллитов чистого P25 и 200-тактного Co 3 О 4 -покрытых порошков P25 составляет ~ 25,8 и ~ 26,2 нм, соответственно, что немного больше, чем результат XRD из-за того, что меньшие наночастицы легко пренебречь при наблюдениях SEM. Эти наночастицы агломерируются вместе, образуя более крупные кластеры размером 50–100 нм. На изображении ПЭМ высокого разрешения (ПЭМВР) на рис. 2с хорошо кристаллизованный TiO 2 с локальным увеличением нанокристалл с четкими каймами решетки можно увидеть в чистых порошках P25. После 200 циклов PEALD Co 3 О 4 , мы можем заметно различить небольшие аморфные наночастицы, расположенные на более крупном кристаллическом TiO 2 поверхность диаметром 2–3 нм, как показано стрелками на рис. 2г. Основываясь на нашей предыдущей работе [43], эти маленькие наночастицы должны быть производным PEALD Co 3 О 4 с режимом островного роста. В сочетании с результатами ПЭМ и XRD можно сделать вывод, что ионы Co существуют в виде Co 3 О 4 аморфные наночастицы, прикрепленные к TiO 2 поверхность порошка вместо заполнения Ti 4+ положение в TiO 2 решетка.
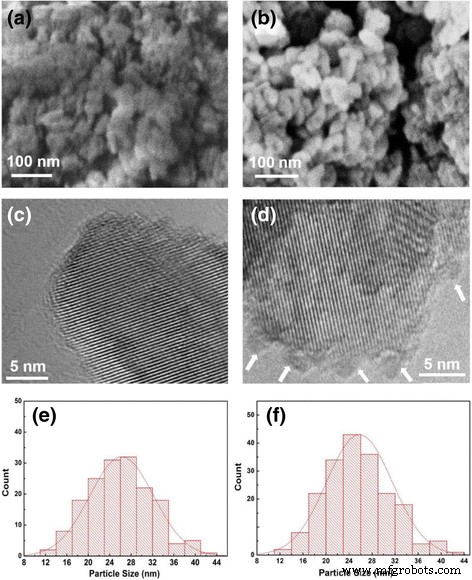
SEM ( a , b ) и HRTEM ( c , d ) изображения чистого P25 и 200-цикла Co 3 О 4 -покрытые порошки P25 вместе с гранулометрическим составом ( e , f ). а , c , e Чистые порошки P25. б , d , f 200-тактный Co 3 О 4 порошки P25 с покрытием
Кроме того, влияние PEALD Co 3 О 4 на удельную поверхность P25. Площадь поверхности по БЭТ составляет 112,6 и 104,0 м 2 / г для чистого P25 и Co 3 О 4 порошки P25 с покрытием соответственно, поэтому Co 3 О 4 осаждение на порошки P25 незначительно влияет на удельную поверхность P25.
XPS был выполнен для исследования химического состава образцов с 100-цикловым Co 3 PEALD и без него. О 4 покрытие. Оба образца показывают почти одинаковые сигналы для спектров Ti 2p и O 1s. На рис. 3а дублет 464,6 и 458,9 эВ может быть отнесен к Ti 4+ . 2р 1/2 и Ti 4+ 2р 3/2 пики связей Ti – O с энергией спин-орбитального расщепления 5,7 эВ, согласующиеся со значениями TiO 2 . Спектры O 1s можно разложить на два пика, как показано на рис. 3b. Сильный пик при 529.9 эВ можно отнести к связи O – Ti. Слабый пик с более высокой энергией связи при 532,2 эВ приписывается поглощенным частицам ОН на поверхности образцов [44]. Пик O1s Co 3 О 4 должна располагаться при ~ 529,8 эВ [43], что трудно отличить от связи O – Ti. Расчетное атомное соотношение Ti:O составляет примерно 1,00:2,13, что в основном соответствует составу TiO 2 . . Однако сигнал Co 100-периодного Co 3 О 4 порошки P25 с покрытием слишком слабы, чтобы их можно было обнаружить. Это может быть связано с тем, что содержание Co может быть ниже предела обнаружения XPS. Поэтому для определения содержания Co в чистом P25 и 100-цикловом Co 3 использовали ИСП-МС. О 4 порошки P25 с покрытием. Установлено, что содержание Co в чистом P25 и 100-цикловом Co 3 О 4 P25 с покрытием составляет 0,13 и 3,63 частей на миллион соответственно. Следовательно, трассировка Co 3 О 4 действительно наносится на порошки P25 компанией PEALD. Кроме того, XPS также использовался для анализа 600-циклового Co 3 О 4 -покрытые образцы P25, полученные методом термического ALD. Слабые спектры Co 2p можно распознать по атомному процентному содержанию Co ~ 0,6%.
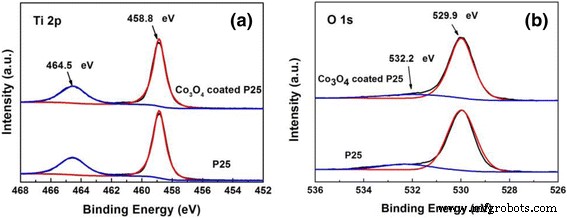
XPS-спектры Co 3 за 100 циклов О 4 порошки P25 с покрытием и чистые порошки P25. а Ti 2p. б O 1 с
На рис. 4а записаны спектры диффузного отражения чистого P25 и Co 3 при комнатной температуре в УФ-видимом диапазоне. О 4 -покрытые образцы P25 с 200 и 600 циклами. Чистый P25 и 200-цикл Co 3 О 4 образцы P25 с покрытием показывают почти такие же спектры оптического поглощения, однако, 600-периодный Co 3 О 4 Образцы P25 с покрытием, полученные с помощью термической ALD, демонстрируют относительно более сильное поглощение в видимом диапазоне от 400 до 700 нм, особенно в области 400–500 нм, которое возникает из-за перехода d-d для Co 3+ или Co 2+ ионы.
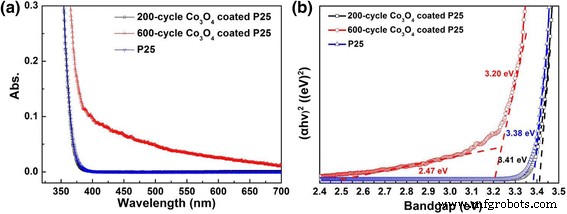
а УФ-видимые спектры диффузного отражения и ( b ) соответствующие графики определения ширины запрещенной зоны чистого P25, 200-циклового и 600-циклического Co 3 О 4 порошки P25 с покрытием
Для полупроводника с прямой запрещенной зоной соотношение между краем поглощения и энергией фотона ( hν ) можно записать следующим образом [45]:
( αhν ) 2 = А ( hν - E г ) где A - константа поглощения полупроводника с прямой запрещенной зоной. Коэффициент поглощения (α) определяется из спектров рассеяния и отражения согласно теории Кубелки-Мунка. Энергии прямой запрещенной зоны можно оценить по пересечению касательных к графикам, как показано на рис. 4b. Ширина запрещенной зоны 200-тактного Co 3 О 4 порошков P25 с покрытием составляет около 3,41 ± 0,02 эВ, почти так же, как чистый TiO 2 порошки (3,38 ± 0,02 эВ) из-за чрезвычайно низкого содержания Co (~ ppm по данным ICP-MS). Шестьсот циклов Co 3 О 4 Образцы P25 с покрытием имеют две запрещенные зоны из-за относительно более высокого содержания Co (~ 0,6 атомных% по данным XPS). Большая ширина запрещенной зоны 3,20 ± 0,03 эВ обеспечивается TiO 2 порошков, тогда как гораздо меньшая ширина запрещенной зоны 2,47 ± 0,03 эВ может быть связана с Co 3 О 4 покрытие. Производный от ALD Co 3 О 4 покрытие имеет немного более широкую запрещенную зону, чем литературное значение 2,3 эВ для Co 3 О 4 наносферы (~ 20 нм) методом растворного синтеза [46].
МБ обычно используется в качестве зонда для оценки фотокатализаторов, и механизм его разложения хорошо изучен. На рис. 5a – c показано фотокаталитическое разложение МБ в УФ-свете в присутствии чистого P25, 100- и 200-циклический Co 3 О 4 фотокатализаторы P25 с покрытием соответственно. Максимальное поглощение МБ находится при 664 нм. Интенсивность поглощения уменьшается со временем при облучении УФ-светом для всех образцов, что соответствует разложению МБ. На рис. 5г представлены кривые фотокаталитического разложения для всех образцов. И чистый P25, и Co 3 О 4 порошки P25 с покрытием могут разрушать МБ под воздействием УФ-излучения. Между тем, в УФ-свете без катализатора разложения МБ почти не наблюдается, что свидетельствует о том, что МБ устойчив в УФ-свете. Однако 100- или 200-цикловый Co 3 О 4 порошки P25 с покрытием показывают гораздо более высокую фотокаталитическую активность по сравнению с чистыми порошками P25. Эффективность разложения Co 3 О 4 P25 с покрытием может достигать почти 100% за 1,5 часа, в то время как чистый P25 составляет всего около 80%.
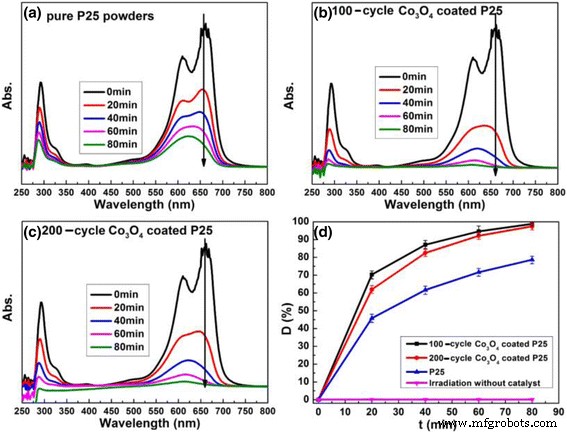
Кривые поглощения и разложения раствора МБ в УФ-видимой области с различными катализаторами. а Чистый P25. б 100-тактный Co 3 О 4 . c 200-тактный Co 3 О 4 -покрытый катализатор Р25. г Кривые разложения МБ
Также были проведены испытания рециклинга для определения стабильности композитных катализаторов Co 3 О 4 порошки P25 с покрытием. В 200-циклическом Co 3 падения фотокаталитической эффективности не наблюдается. О 4 -покрытые образцы P25 после трехкратного использования в фотодеградации МБ.
Повышенная фотокаталитическая активность Co 3 О 4 порошков P25 с покрытием можно отнести к образованию p-n-перехода между Co 3 О 4 и TiO 2 . На рисунке 6 показаны графики Мотта-Шоттки для P25 с 200-циклическим Co 3 или без него. О 4 покрытие. Чистые образцы P25 демонстрируют график Мотта-Шоттки с положительным наклоном, что указывает на полупроводник n-типа с электронными носителями. График Мотта-Шоттки с отрицательным наклоном подразумевает полупроводник p-типа с дырочными носителями. Для 200-циклового Co 3 О 4 -покрытый катализатор P25, сосуществование положительных и отрицательных наклонов с аналогичными значениями на графике Мотта-Шоттки может наблюдаться одновременно, что указывает на образование p-n-перехода в наших образцах. Это поможет разделить фотогенерированные электронно-дырочные пары [18, 22, 47].
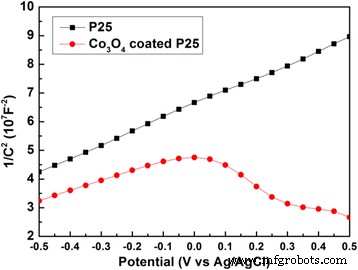
Графики Мотта-Шоттки для чистого P25 и Co 3 О 4 -покрытый P25 в 1 М водном растворе NaOH с частотами 1 и 2 кГц в темноте
На рисунке 7 показана схема уровня энергии и движения электрон-дырка в Co 3 . О 4 –TiO 2 структура p-n перехода. Со 3 О 4 имеет гораздо меньшую ширину запрещенной зоны (~ 2,4 эВ), чем TiO 2 (~ 3,4 эВ). При облучении ультрафиолетовым светом электронно-дырочные пары могут образовываться как в Co 3 О 4 и TiO 2 . Согласно структуре энергетических уровней на рис. 7 фотогенерированные электроны будут перемещаться из зоны проводимости Co 3 О 4 к TiO 2 . Напротив, дырки вводятся из валентной зоны TiO 2 к тому из Co 3 О 4 . В результате в зоне проводимости TiO 2 образуется высокая концентрация электронов и дырок. и валентная зона Co 3 О 4 , соответственно. Рекомбинация электронно-дырочной пары эффективно затрудняется из-за разделения фотогенерированных электронов и дырок. Затем отделенные электроны и дырки могут свободно вступать в реакции с реагентами, адсорбированными на поверхности фотокатализатора, и повышать фотокаталитическую активность. Следовательно, Co 3 О 4 –TiO 2 Структура p-n-перехода демонстрирует лучшие фотокаталитические свойства, чем чистый TiO 2 .
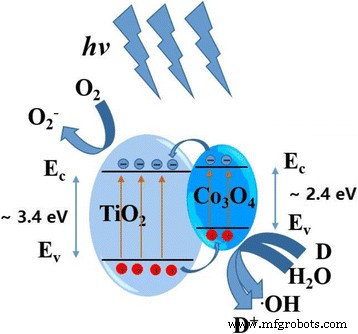
Схема энергетического уровня и движения электрон-дырки в Co 3 О 4 –TiO 2 Структура p-n перехода под воздействием УФ-излучения
Кроме того, чтобы оценить влияние изоэлектрической точки (IEP) на абсорбцию MB, IEP была обнаружена с использованием измерения дзета-потенциала, как показано на рис. 8. IEP MB, чистого P25 и 200- цикл Co 3 О 4 P25 с покрытием в водных растворах составляют 5,37, 6,74 и 7,42 соответственно. Значение pH красителя МБ и P25 или Co 3 О 4 водная суспензия P25 с покрытием составляет 6,68. Согласно результатам IEP, краситель МБ несет отрицательный заряд, в то время как оба катализатора несут положительный заряд. Кроме того, Co 3 О 4 порошки P25 с покрытием имеют больше положительных зарядов, чем чистый P25. Следовательно, Co 3 О 4 покрытие может способствовать адсорбции МБ на P25, что способствует усилению фотокаталитической активности.
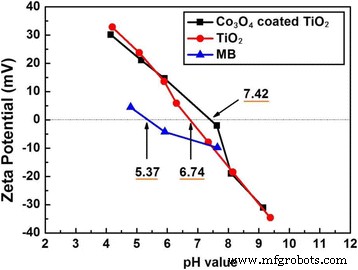
Дзета-потенциал MB, P25 и Co 3 О 4 P25 с покрытием в водных растворах в зависимости от значений pH
Наконец, тест фотодеградации метилового оранжевого (МО) с использованием Co 3 О 4 порошков P25 с покрытием также проводили при освещении видимым светом. 200-тактный Co 3 О 4 Образец P25 с покрытием не проявляет фотокаталитической активности в отношении разложения МО. Это можно объяснить тем, что существует только след Co 3 О 4 на поверхности P25. След Co 3 О 4 не может поглощать достаточно видимого света, чтобы стимулировать каталитические реакции. Поэтому мы приготовили 600-цикл Co 3 О 4 -покрытие образца P25 с помощью термического ALD для введения большего количества Co 3 О 4 наночастиц на порошки P25. Фотокаталитическая активность при разложении красителя МО была исследована при облучении видимым светом ( λ ≥ 420 нм), как показано на рис. 9. Шестьсот циклов Co 3 О 4 P25 с покрытием демонстрирует видимую фотокаталитическую активность с разложением ~ 26% MO за 120 мин. Это можно объяснить, рассматривая Co 3 О 4 активность наночастиц в видимом свете из-за узкой запрещенной зоны (~ 2,4 эВ), что подтверждается рис. 4d [28].
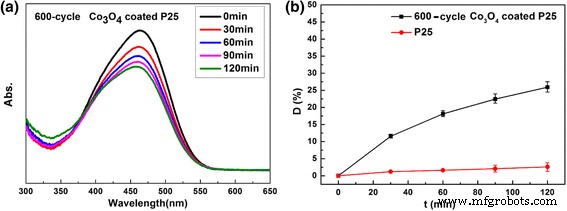
Видимая фотокаталитическая активность 600-цикла Co 3 О 4 порошки P25 с покрытием. а УФ-видимое поглощение и b кривые разложения раствора МО при облучении видимым светом
Выводы
Таким образом, Co 3 О 4 Порошковые фотокатализаторы p-n-перехода P25 с покрытием были успешно изготовлены компанией PEALD. Структура, морфология, состав и ширина запрещенной зоны этих модифицированных порошков P25 были систематически охарактеризованы. Фотокаталитическая активность разложения МБ в УФ-свете была глубоко изучена. Структура анатаза и размер кристаллитов порошков P25 не изменяются после 100 и 200 циклов Co 3 О 4 осаждение. Однако в УФ-свете Co 3 О 4 порошки P25 с покрытием демонстрируют скорость разложения почти 100% за 1,5 часа. Ультрафиолетовая фотокаталитическая активность явно увеличена по сравнению с чистыми порошками P25. Графики Мотта-Шоттки порошков фотокатализаторов подтверждают образование p-n гетероперехода в Co 3 О 4 –TiO 2 нанокомпозитные материалы, что способствует разделению фотогенерированных электронно-дырочных пар. Кроме того, результаты IEP также показывают, что Co 3 О 4 покрытие может способствовать адсорбции органических красителей метиленового синего на порошках P25. Прежде всего, ALD - это многообещающая и мощная технология для создания эффективного фотокатализатора на p-n-переходе путем модификации поверхности.
Наноматериалы
- Усовершенствованные технологии осаждения атомного слоя для микро-светодиодов и VCSEL
- Наножидкости TiO2 - Часть 1:Приготовление и свойства
- Композиты с квантовыми точками на S, N-графене / TiO2 для эффективного фотокаталитического производства водород…
- Характеристики биполярного резистивного переключения устройств RRAM с трехслойной структурой HfO2 / TiO2 / HfO2 на по…
- Межфазные, электрические характеристики и характеристики совмещения полос стопок HfO2 / Ge с прослойкой SiO2, сфор…
- Высокие фотокаталитические характеристики двух типов композитных фотокатализаторов TiO2, модифицированных г…
- Оптические и электрические характеристики кремниевых нанопроволок, полученных методом химического травлен…
- Иерархические антибактериальные полиамидные 6-ZnO нановолокна, полученные путем осаждения атомных слоев и гид…
- Настройка морфологии поверхности и свойств пленок ZnO путем создания межфазного слоя
- Настройка уровня Ферми пленок ZnO посредством суперциклического осаждения атомного слоя



