Синтез сферического покрытого серебром анодного материала Li4Ti5O12 с помощью золь-гелевого гидротермального метода
Аннотация
ᅟ
Сферический Li 4 с серебряным покрытием Ti 5 О 12 Композит был успешно синтезирован золь-гель-гидротермальным методом с использованием смеси этиленгликоля и нитрата серебра в качестве прекурсора, а влияние содержания Ag в покрытии на его электрохимические свойства было тщательно исследовано. Рентгеноструктурный анализ (XRD) показал, что покрытие Ag не изменяет структуру шпинели Li 4 Ti 5 О 12 . Анализ спектроскопии электрохимического импеданса (EIS) показал, что отличная электропроводность Li 4 Ti 5 О 12 / Ag является результатом наличия высокопроводящего слоя серебряного покрытия. Кроме того, наноразмерный слой серебра, который был равномерно нанесен на частицы, значительно улучшил способность этого материала к скорости обработки. Как следствие, покрытый серебром сферический кристалл Li 4 микронного размера Ti 5 О 12 показал отличные электрохимические характеристики. Таким образом, при соответствующем содержании серебра 5 мас.% Li 4 Ti 5 О 12 / Ag показал максимальную емкость 186,34 мАч г −1 при 0,5 ° C, что выше, чем у других образцов, и сохранял 92,69% своей начальной емкости при 5 ° C после 100 циклов. Даже при 10 ° C после 100 циклов у него все еще сохранялась емкость 89,17%, демонстрируя замечательную стабильность при циклических нагрузках.
Регистрация пробной версии
ISRCTN NARL-D-17-00568
Основные моменты
- 1.
Сферический Li 4 Ti 5 О 12 Композиты / Ag были синтезированы золь-гель-гидротермальным методом с использованием этиленгликоля и смеси нитрата серебра в качестве прекурсора для слоя покрытия, что значительно улучшило электронную проводимость и электрохимические характеристики Li 4 Ti 5 О 12 .
- 2.
Сферическая морфология может вызвать большую удельную плотность и, как следствие, увеличить объемную плотность энергии.
Фон
За последнее десятилетие литий-ионные аккумуляторные батареи (LIB) продемонстрировали множество преимуществ. Они легкие; имеют небольшие размеры, высокое напряжение и высокую удельную энергию; и вызывают большой интерес в качестве электрохимического накопителя энергии для уменьшения выбросов выхлопных газов и экономии топлива [1, 2]. Однако цена на прекурсоры лития, вопросы безопасности и срока службы, а также низкая плотность мощности являются препятствиями для применения LIB для крупномасштабного хранения энергии в будущем [3]. Поэтому для разработки материалов-заменителей, отвечающих требованиям безопасности крупномасштабных хранилищ, были приложены большие усилия [4].
Кубическая шпинель титанат лития (Li 4 Ti 5 О 12 ) материалы, анодные материалы литий-ионных аккумуляторов, стали многообещающим материалом из-за их структурных характеристик при нулевой деформации во время процесса интеркаляции и деинтеркаляции Li 4 Ti 5 О 12 [5,6,7,8,9]. Этот материал имеет платформенное напряжение ввода и вывода лития ~ 1,55 В (по сравнению с Li / Li + ), предотвращая образование литий-потребляющих пленок на границе раздела твердого электролита (SEI), что должно быть полезно для повышения безопасности и хорошей цикличности LIB. Следовательно, Ли 4 Ti 5 О 12 стал одним из потенциальных материалов для коммерческого применения и научных исследований. Ли 4 Ti 5 О 12 был получен различными методами, например твердотельным, химическим осаждением, микроволновым и золь-гель методом. Что касается твердотельного метода, некоторые исследования показали, что он имеет простой путь синтеза и низкую стоимость синтеза из-за более короткого расстояния для Li + диффузия и перенос электрона, Li 4 Ti 5 О 12 демонстрирует отличную скорость реакции, но реакция в твердом состоянии не может обеспечить однородную морфологию с узким размером. Однако процесс химического осаждения имеет сложный путь синтеза. Для золь-гель синтеза Li 4 Ti 5 О 12 , несколько исследователей сообщили, что с его помощью можно получать продукты с однородным однородным распределением и узкими частицами с хорошим стехиометрическим контролем.
Несмотря на эти многочисленные преимущества, основные недостатки Li 4 Ti 5 О 12 являются его плохая электронная и ионная проводимость и низкий коэффициент диффузии литий-ионных ионов, что приводит к низкой пропускной способности. Для улучшения переноса разряда / заряда были приняты многочисленные стратегии, включая уменьшение размера кристаллитов [10], легирование ионами металлов с высокой валентностью [11,12,13] и покрытие проводящими фазами [14,15,16,17]. свойства электродов. Кроме того, еще одним способом повышения электронной проводимости является синтез наноструктурированного Li 4 Ti 5 О 12 . Наноструктуры обеспечивают большую площадь контакта электрода с электролитом для увеличения кинетики интеркаляции и уменьшения путей диффузии для ускорения Li + и электронный транспорт [18]. Среди этих подходов наиболее эффективный способ улучшения электрохимических свойств Li 4 Ti 5 О 12 модификация проводящей поверхности. Aslihan et al. [2] синтезировал Li 4 Ti 5 О 12 золь-гель методом, а затем синтезированный Li 4 Ti 5 О 12 была покрыта серебром методом химического осаждения. Результаты показали, что серебряное покрытие (покрытие Ag) обеспечивает матрицу Li + с высокой проводимостью. вставка, улучшающая электронную проводимость. Zhu et al. [19] приготовили наноразмерный Li 4 с углеродным покрытием. Ti 5 О 12 нанопористые микросферы с замечательной скоростной способностью за счет процесса предварительного покрытия углеродом в сочетании с методом распылительной сушки, и показали, что сферические частицы микронного размера вызывают большую плотность утряски, что приводит к увеличению объемной плотности энергии. Однако как синтезировать Li 4 микронного размера с серебряным покрытием Ti 5 О 12 о сферических частицах, полученных золь-гель-гидротермальным методом, не сообщалось.
Здесь мы сообщаем о золь-гель гидротермальном методе синтеза сферического Li 4 микронного размера. Ti 5 О 12 / Ag с использованием смеси этиленгликоля и нитрата серебра в качестве предшественника, а содержание покрытия Ag регулировали, контролируя количество элемента серебра в предшественнике. Электрохимические свойства Li 4 Ti 5 О 12 / Ag со сферической морфологией подробно исследованы.
Экспериментальный
Синтез безупречного Li 4 Ti 5 О 12 и модификация его поверхности с помощью Ag
Синтез сферического предшественника с помощью золь-гелевого метода
Сферический предшественник гликолят титана (ТГ) был синтезирован золь-гель методом. Сначала к раствору, который содержал AgNO 3 , медленно добавляли 2 мл тетрабутилтитаната. (в соответствующем количестве, чтобы раствориться в 50 мл гликоля) при интенсивном перемешивании с образованием раствора предшественника. Во-вторых, раствор предшественника добавляли к 150 мл смеси ацетона, содержащей 0,1 мл Tween 80, и перемешивание продолжали в течение 1 ч при комнатной температуре с образованием осадка. Затем осадки выдерживали 8 ч, отделяли фильтрованием и дважды промывали безводным спиртом. Наконец, порошки прекурсора были получены путем термообработки при 80 ° C в течение 6 часов в печи с последующим измельчением.
Синтез сферического Li 4 Ti 5 О 12 / Ag
Сферический Li 4 Ti 5 О 12 / Ag получали гидротермальным методом. Во-первых, LiOH · H 2 О и предшественник в молярном соотношении 3,9:1 гомогенно смешивали путем перемешивания с 40 мл спирта в качестве среды в течение 1 часа с образованием смеси, которую затем нагревали при 180 ° C в течение 12 часов в герметичных тефлоновых изделиях до выпадения осадка. были получены. Во-вторых, осадки собирали центрифугированием (5000 об / мин, 5 мин) и затем несколько раз промывали безводным этанолом. Затем их сушили в сушильном шкафу при 80 ° C в течение 2 ч. Наконец, осадки нагревали в муфельной печи при 700 ° C в течение 2 часов (скорость нагрева 5 ° C · мин -1 ) на воздухе после измельчения и затем естественным охлаждением до комнатной температуры для получения сферического Li 4 Ti 5 О 12 / Ag порошок.
Характеристика материала
Структура Ли 4 Ti 5 О 12 образцы были идентифицированы с помощью дифракции рентгеновских лучей (XRD, Rigaku D / max-PC2200) с использованием источника излучения Cu Kα (λ =0,15405 нм) со скоростью сканирования 4 ° мин -1 от 10 ° до 80 ° и работал при 40 кВ и 20 мА. Морфология и размер частиц материалов были исследованы с помощью SEM (сканирующая электронная микроскопия, Supra 55 Zeiss) и TEM (просвечивающая электронная микроскопия, JEOL-2100).
Электрохимические измерения
Электрохимические характеристики продуктов были протестированы с использованием монетного элемента CR2025. Рабочие электроды были приготовлены путем смешивания 80 мас.% Li 4 Ti 5 О 12 / Ag, 10 мас.% Проводящего Super-P и 10 мас.% Связующего из поливинилиденфторида (ПВДФ) в растворителе N-метил-2-пирролидон (NMP) для образования однородной суспензии. Затем суспензию выливали на алюминиевую фольгу и сушили в вакууме при 80 ° C в течение 12 ч для удаления остаточного растворителя. Затем фольгу прессовали и разрезали на диски. Полипропиленовая микропористая мембрана Celgard 2400 и литиевая фольга использовались в качестве разделителя и отрицательного электрода соответственно. Раствор электролита - 1 М LiPF 6 . в этиленкарбонате (EC), диметилкарбонате (DMC) и этиленметилкарбонате (EMC) в объемном соотношении 1:1:1. Ячейки были собраны в наполненном аргоном перчаточном боксе, где уровни влажности и кислорода поддерживались ниже 1 ppm. Электрохимические испытания продуктов оценивали на тест-системе LAND CT2001A (Ухань, Китай). Испытания циклической вольтамперометрии (CV) были записаны на электрохимической рабочей станции CHI600A при 0,1 мВ с -1 скорость сканирования от 1,0 до 2,5 В (по сравнению с Li / Li + ). Измерения EIS проводились в диапазоне частот от 100 кГц до 10 мГц с возмущением 5 мВ.
Результаты и обсуждение
Структурные и морфологические свойства
Влияние количества добавки Ag на Li 4 Ti 5 О 12 / Исследованы порошки Ag. Рентгенограммы сферического Li 4 с серебряным покрытием Ti 5 О 12 композиты представлены на рис. 1. Легко видеть, что основные дифракционные пики всех образцов появляются при 18,4 °, 35,54 °, 43,2 °, 57,2 °, 62,8 ° и 66,1 ° и имеют индекс (111), (311), (400), (333), (440) и (531) соответственно. Эти пики хорошо согласуются с Li 4 Ti 5 О 12 стандартная дифракционная картина [20], за исключением характерных картин металла Ag (2θ =38,1 °, 44,3 °, 64,4 °). Пиков примесной дифракции не обнаружено ни в одном из образцов. Более того, пиковая интенсивность серебра соответственно возрастала с увеличением количества Ag.
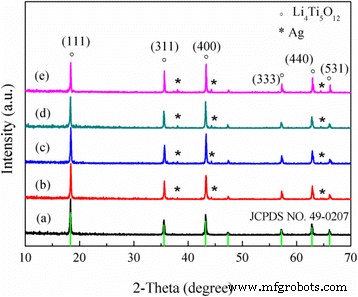
Картины XRD Li 4 Ti 5 О 12 / Ag. ( а ) 0 мас.%, ( b ) 1 мас.%, ( c ) 3 мас.%, ( d ) 5 мас.% И ( e ) 7 мас.%
Параметры решетки Li 4 Ti 5 О 12 / Образцы Ag с различными покрытиями Ag представлены в таблице 1. Существенных изменений с увеличением содержания Ag не наблюдалось. Таким образом, было высказано предположение, что серебро в основном покрывает поверхность Li 4 в виде элементарного Ag. Ti 5 О 12 частицы, но не проникающие в решетку шпинели Li 4 Ti 5 О 12 . Поскольку ионный радиус Ag + (0,126 нм) значительно больше, чем у Ti 4+ (0,068 нм), синтезированный Li 4 Ti 5 О 12 / Образец Ag представлял собой смесь металла Ag и Li 4 Ti 5 О 12 фаза.
На рисунке 2 показаны изображения предварительно полученного прекурсора, полученные с помощью СЭМ (a 1 -e 1 ) и Ли 4 Ti 5 О 12 / Ag (a 2 -e 2 ). Как показано на рис. 2, все образцы имеют однородную сферическую структуру с узким распределением по размерам 5–10 мкм, что благоприятно сказывается на контакте между активными материалами и электродом. На изображениях SEM сферический предшественник, частицы гликолата титана (TG), показывает плавную линию, тогда как Li 4 Ti 5 О 12 / Частицы серебра представляют собой грубую линию. Более того, хорошее диспергирование может увеличить площадь контакта электрода с электролитом и значительно ускорить транспортировку Li + и электрон. Однако поверхность Li 4 Ti 5 О 12 / Образцы Ag не очевидно более гладкие, чем образцы исходного прекурсора и гликолата титана, и они существуют до определенной степени в виде агломерации. Причем размеры частиц разных Li 4 Ti 5 О 12 / Композиты Ag намного крупнее, чем у Li 4 без Ag Ti 5 О 12 ; однако явление агломерации становится более очевидным с увеличением содержания серебра.

СЭМ-изображения предшественника и Li 4 Ti 5 О 12 / Ag. ( а ) 0 мас.%, ( b ) 1 мас.%, ( c ) 3 мас.%, ( d ) 5 мас.%, ( e ) 7 мас.%
Распределение серебра внутри частиц микронного размера было дополнительно исследовано, и анализы ПЭМ и ВРЭМ были представлены на рис. 3. Изображения ПЭМ (рис. 3а) показывают, что покрытые 5 мас.% Ag частицы микронного размера -сферический Li 4 Ti 5 О 12 частицы равномерно покрыты слоем серебра толщиной 3 ~ 4 нм, что указывает на то, что слой серебра создает проводящую сеть на поверхности всего материала, что облегчает перенос ионов лития и электронов. Как показано на рис. 3b, поверхность Li 4 микронного размера Ti 5 О 12 / Частицы Ag не гладкие, и d - расстояние между 5 мас.% покрытого Ag Li 4 Ti 5 О 12 частиц составляет 0,484 нм, что хорошо согласуется с таковой для плоскости LTO (111). Это говорит о том, что на поверхности частиц LTO не образовалась новая фаза, но на частицах был тонкий слой покрытия.

( а ) ТЕА и ( b ) HRTEM изображения Li 4 , покрытого 5 мас.% Серебра. Ti 5 О 12 , в котором «линия» обозначает слой серебра с покрытием
Электрохимические свойства
На рисунке 4 показаны первые кривые заряда-разряда сферического Li 4 микронного размера. Ti 5 О 12 / Электроды из серебра, покрытые разным содержанием серебра с разной скоростью. Как видно из рис. 4, все профили демонстрируют чрезвычайно плоское плато напряжения 1,55 В (по сравнению с Li / Li + ), что указывает на двухфазный переход между Li 4 Ti 5 О 12 и Ли 7 Ti 5 О 12 для литиевой вставки [21]. Платформа напряжения Li 4 Ti 5 О 12 / Композиты Ag длиннее, чем у Li 4 без Ag Ti 5 О 12 . При увеличении содержания Ag для более длинной платформы разгрузки Li 4 Ti 5 О 12 / Ag композиты, способность поддерживать платформу сильнее, что свидетельствует о том, что хорошая электронная проводимость может эффективно снизить поляризацию материала во время процесса электродной реакции и улучшить использование материала.
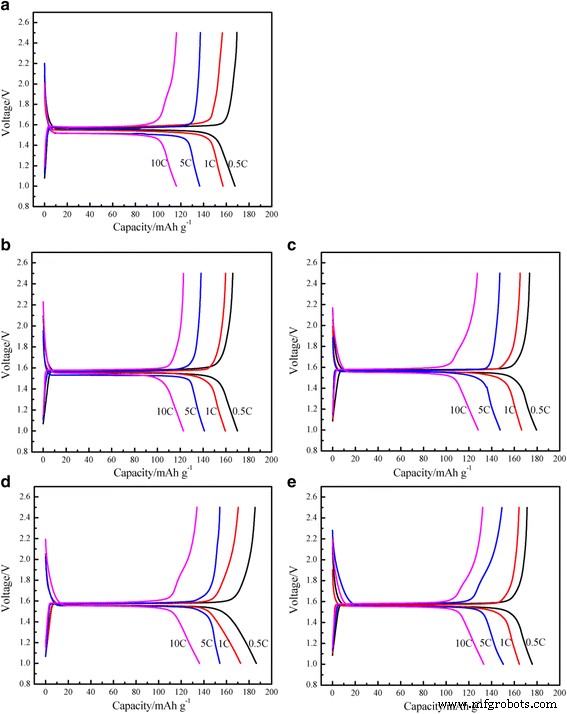
Кривые начального заряда-разряда при различной плотности тока Li 4 Ti 5 О 12 / Ag. ( а ) 0 мас.%, ( b ) 1 мас.%, ( c ) 3 мас.%, ( d ) 5 мас.%, ( e ) 7 мас.%
Как показано на рис. 4, Li 4 без Ag Ti 5 О 12 обеспечивает начальную удельную емкость разряда 167,62 мАч г -1 при скорости 0,5 ° C, тогда как доставляемая емкость сферического Li 4 микронного размера с серебряным покрытием Ti 5 О 12 композиты увеличивались с увеличением количества серебра:170,10, 179,54 и 186,34 мАч г −1 на 1, 3 и 5 мас.% соответственно. Но 7 мас.% Li 4 с покрытием из Ag Ti 5 О 12 проявлял несколько иное поведение. Доставляемая удельная емкость разряда уменьшалась с увеличением количества серебра:175,86 мАч г −1 на 7 мас.%. Li 4 , покрытый 5 мас.% Ag Ti 5 О 12 получили максимальную начальную разрядную емкость, а начальные удельные емкости при разрядке достигли 186,34, 172,47, 154,12 и 136,06 мАч г −1 при удельных токах 0,5, 1, 5 и 10C соответственно. Из-за плохой электронной проводимости и вялого Li + диффузии материал демонстрирует большую поляризацию при высоких скоростях заряда / разряда. Добавка Ag с высокой проводимостью может значительно усилить реакцию интеркаляции поверхности и уменьшить поляризацию [20, 22]. Даже самое высокое содержание Ag (7 мас.%) Может обеспечить наиболее продолжительное плато напряжения, а само металлическое серебро не может быть полностью интеркалировано в литий. Вместо этого высокое содержание Ag приведет к снижению удельной емкости Li 4 Ti 5 О 12 / Ag. Следовательно, соответствующее содержание серебра может не только эффективно улучшить проводимость Li 4 . Ti 5 О 12 и уменьшить поляризацию Li 4 Ti 5 О 12 в процессе реакции, но также может снизить потерю обратимой емкости из-за покрытия Ag.
Скоростные возможности Li 4 , не содержащего Ag Ti 5 О 12 и 5 мас.% Li 4 с покрытием из серебра Ti 5 О 12 композит был проанализирован при плотностях тока 0,5, 1, 5 и 10 ° C, и результаты показаны на рис. 5. Как показано, начальная емкость Li 4 , покрытого 5 мас.% Ag, Ti 5 О 12 композит при 5C составил 154,12 мАч г -1 . После 30 циклов емкость все еще сохранялась на уровне 150,50 мАч г -1 . , сохранив более 97,65% первоначальной мощности. Когда она была увеличена до 10 ° C, разрядная емкость, по-видимому, упала с 136,06 мАч г −1 . до 130,81 мАч г −1 после 30 циклов. При этом эффективность удержания емкости все же удалось сохранить на уровне 96,14%. Более того, характеристики Li 4 при езде на велосипеде Ti 5 О 12 Композит / Ag был значительно лучше, чем композит Li 4 , не содержащий Ag. Ti 5 О 12 при различных скоростях заряда-разряда. Как показано на рис. 6а, при соответствующем содержании серебра 5 мас.% Покрытый серебром Li 4 Ti 5 О 12 доставил максимальную емкость 186,34 мАч g −1 при 0,5 ° C, что выше, чем у других образцов, и сохранял 92,69% своей начальной емкости при 5 ° C после 100 циклов. Даже при 10 ° C после 100 циклов (рис. 6b) у него все еще сохранялась емкость 89,17%, демонстрируя замечательную стабильность при циклировании. Результаты показали, что при благоприятных условиях эксперимента Li 4 Ti 5 О 12 Поверхностное покрытие Ag не только улучшило электронную и ионную проводимость, но также, очевидно, увеличило перенос электронов во время реакции внедрения / извлечения лития и значительно улучшило стабильность цикла Li 4 Ti 5 О 12 .
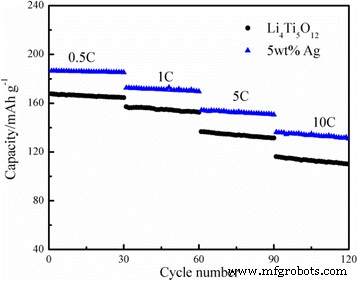
Расчетная способность Li 4 без Ag и с 5 мас.% Ag с покрытием Ti 5 О 12 по разным текущим ставкам
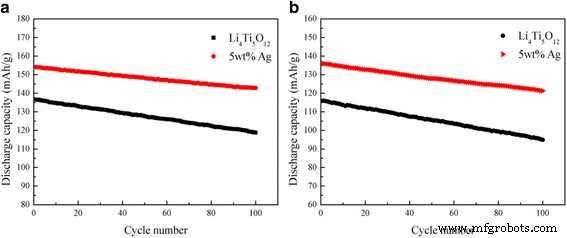
Циклические характеристики Li 4 , не содержащего Ag, и Li 4 , покрытого 5 мас.% Ag. Ti 5 О 12 при 5 ° C ( a ) и 10 ° C ( b )
На рисунке 7 представлены циклические вольтамперограммы (ВА) Li 4 , не содержащего Ag. Ti 5 О 12 и 5 мас.% Li 4 с покрытием из серебра Ti 5 О 12 композит, полученный при медленной скорости 0,1 мВ с −1 . Очевидно, были получены обратимые окислительно-восстановительные пики между 1,0 и 2,5 В, которые приписываются введению и извлечению ионов лития, что свидетельствует об отсутствии образования промежуточной фазы во время введения и удаления лития. Между тем, площади окислительно-восстановительных пиков этих двух кривых практически равны, что свидетельствует о высокой кулоновской эффективности [23]. Разница потенциалов между пиками окисления и восстановления Li 4 , покрытого 5 мас.% Ag Ti 5 О 12 составляет 0,244 В, что немного ниже, чем у Li 4 без Ag. Ti 5 О 12 (0,24 В). Это говорит о том, что надлежащее покрытие поверхности высокопроводящей добавкой Ag значительно уменьшило поляризацию Li 4 Ti 5 О 12 образец и эффективно улучшил его электрохимические характеристики. Кроме того, окислительно-восстановительные пики Li 4 , покрытого 5 мас.% Ag, Ti 5 О 12 острее и крупнее, чем у Li без Ag 4 Ti 5 О 12 , что указывает на то, что подходящее покрытие из серебра может улучшить динамические характеристики электрода.
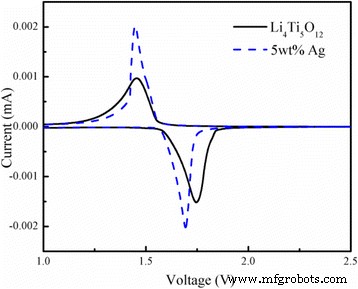
Кривые CV для Li 4 , не содержащего Ag, и Li 4 , покрытого 5 мас.% Ag Ti 5 О 12 составной
Измерения методом спектроскопии электрохимического импеданса (EIS) Li 4 , не содержащего Ag Ti 5 О 12 и 5 мас.% Li 4 с покрытием из серебра Ti 5 О 12 проводились в диапазоне частот 10 5 до 0,01 Гц перед гальваностатическими циклами. Кроме того, эквивалентная схема (вставка) и соответствующие данные по импедансу показаны на рис. 8. В эквивалентной схеме Rs представляет собой сопротивление раствору электролита, которое отражает электрическую проводимость электролита, сепаратора и электродов. (пересечение с Z ′ ось на высокой частоте), R ct показывает сопротивление переносу заряда в материалах, CPE - емкость двойного слоя и пассивирующей пленки, а Вт - импеданс Варбурга, связанный с диффузией ионов лития в области низких частот. Параметры, полученные при подгонке, перечислены в таблице 2. Как показано на рис. 8, обе кривые EIS состояли из вдавленного полукруга в высокочастотной области и наклонной прямой линии в низкочастотной области. Диаметр полукруга обозначает сопротивление переносу заряда, а наклонная прямая связана с импедансом Варбурга [24]. Импеданс полукругов в высокочастотной области соответствует процессу переноса заряда на границе раздела электрода и жидкого электролита, а прямая линия в низкочастотной области может быть выражена как поведение диффузии ионов лития в структуре оксида [25,26, 27,28]. Как показано на фиг. 8, диаметр полукруга Li 4 , покрытого 5 мас.% Ag Ti 5 О 12 короче, чем у голого Li 4 Ti 5 О 12 , что указывает на то, что надлежащее количество покрытия Ag может улучшить электронную проводимость Li 4 Ti 5 О 12 , и это связано с процессом переноса заряда, где Li + и электроны достигают поверхности электрода одновременно, чтобы завершить реакцию. Это в основном зависит от окислительно-восстановительной реакции на поверхности активных материалов. Меньшее сопротивление переносу заряда у Li 4 , покрытого 5 мас.% Ag Ti 5 О 12 отражают более быстрые реакции переноса заряда на границе раздела электрод / электролит.
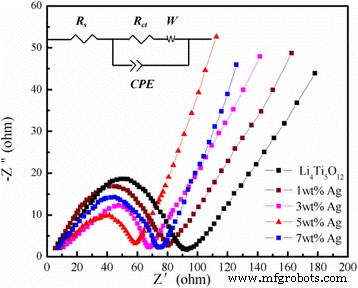
Паттерны EIS чистого Li 4 Ti 5 О 12 и Ли 4 Ti 5 О 12 покрытие с различным содержанием серебра
Коэффициент химической диффузии иона лития можно рассчитать по графику в низкочастотной области, используя следующую формулу. (1) [29,30,31,32,33].
$$ {D} _ {{\ mathrm {Li}} ^ {+}} =\ frac {R ^ 2 {T} ^ 2} {2 {A} ^ 2 {n} ^ 4 {F} ^ 4 { C} _ {Li} ^ 2 {\ sigma_w} ^ 2} $$ (1)Здесь \ ({D} _ {{\ mathrm {Li}} ^ {+}} \) - коэффициент диффузии ионов лития, R - газовая постоянная (8,314 Дж · К · моль −1 ), Т - абсолютная температура (298 K), A площадь поверхности электрода, n - количество электронов на молекулу, участвующих в реакции электронного переноса, F - постоянная Фарадея (96 500 C моль −1 ), C Ли - концентрация ионов лития в Li 4 Ti 5 О 12 электрод и σ w фактор Варбурга, имеющий следующие отношения с Ζ re :
$$ {Z} _ {\ mathrm {re}} ={R} _S + {R} _ {\ mathrm {ct}} + {\ sigma} _w \ cdot {\ omega} ^ {- 0.5} $$ (2 )Кроме того, связь между Z re а обратный квадратный корень из частоты для низкой частоты показан на рис. 9. Все параметры, полученные и вычисленные с помощью EIS, приведены в таблице 2. Как показано в таблице 2, \ ({D} _ {\ mathrm { L} {\ mathrm {i}} ^ {+}} \) из Li 4 , покрытого 5 мас.% Ag, Ti 5 О 12 равно 6,73 × 10 −11 , что на порядок больше, чем у Li 4 Ti 5 О 12 (8,69 × 10 −12 ). Li 4 , покрытый 5 мас.% Ag Ti 5 О 12 имеет самый большой коэффициент диффузии лития по сравнению с Li 4 без Ag Ti 5 О 12 и 1, 3 и 7 мас.% Li 4 с покрытием из серебра Ti 5 О 12 композиты, что указывает на то, что покрытие Ag является эффективным способом улучшения электронной проводимости. Следовательно, пропускная способность Li 4 , покрытого 5 мас.% Ag Ti 5 О 12 можно существенно улучшить.
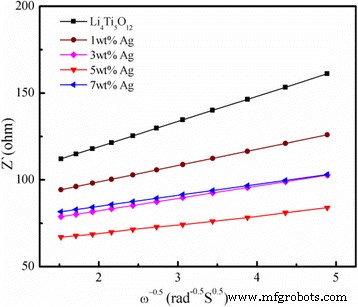
График Z re заговор против ω −0,5 в области низких частот для Li 4 Ti 5 О 12 и Ли 4 Ti 5 О 12 покрытие с различным содержанием серебра
Выводы
Анодные материалы сферические Li 4 Ti 5 О 12 / Ag композиты с высокой плотностью утряски были приготовлены золь-гель гидротермальным методом. Электрохимические испытания показывают, что соответствующее количество покрытия Ag может значительно улучшить электронную проводимость Li 4 Ti 5 О 12 и повысить стабильность цикла. Оптимальное содержание серебра составляет 5 мас.%, Что позволяет получить отличные электрохимические характеристики. Однако чрезмерное содержание серебра ухудшает электрохимические свойства материала. Поэтому подходящий сферический Li 4 с серебряным покрытием Ti 5 О 12 композит представляет собой превосходный литиевый накопительный материал, обладающий большой емкостью и превосходной безопасностью, и он имеет реальный потенциал в качестве многообещающего материала для литий-ионных аккумуляторов.
Наноматериалы
- Метод подготовки медно-вольфрамового контактного материала
- Метод С#
- Стратегия гидротермального спекания для анодного материала LiNb3O8 с пористой и полой структурой
- Простой синтез наночастиц SiO2 @ C, закрепленных на MWNT, в качестве высокоэффективных анодных материалов для лити…
- Гидротермальный синтез наночастиц In2O3, гибридные двойники, гексагональные дисковые гетероструктуры ZnO для по…
- Многослойный композит MoS2 / ацетиленовый черный как эффективный анодный материал для литий-ионных батарей
- Метод последующей обработки для синтеза монодисперсных бинарных наночастиц FePt-Fe3O4
- Влияние метода синтеза наночастиц манганита La1 - xSr x MnO3 на их свойства
- Встроенный композит Si / графен, изготовленный методом термического восстановления магнием в качестве анодно…
- Новый метод изготовления компьютерной памяти из оксида титана



