Продольный биосенсор осажденной емкости цеолит-оксид железа нанокомпозит для определения интерлейкина-3 при обнаружении сепсиса
Аннотация
Сепсис - это крайнее состояние, связанное с физической реакцией на тяжелую микробную инфекцию, которое вызывает смертельные и опасные для жизни проблемы. Сепсис возникает во время выброса химикатов с иммунной системой в кровоток для борьбы с инфекцией, которая вызывает воспаление и приводит к неотложной медицинской помощи. Комплексный нанокомпозит продольного цеолита и оксида железа был извлечен из летучей золы угольных шахт и использован для улучшения характеристик поверхности емкостного биосенсора для выявления приступов сепсиса. Антитело против интерлейкина-3 (анти-IL-3) прикрепляли к поверхности емкостного электрода, связанного с цеолитом и оксидом железа, через аминный линкер для взаимодействия с биомаркером сепсиса IL-3. Морфологические и химические компоненты нанокомплекса исследованы методами FESEM, FETEM и EDX. Приблизительно при 30 нм продольный нанокомпозит цеолита и оксида железа помог достичь предела обнаружения IL-3 3 пг / мл на линейной кривой с коэффициентом регрессии ( R 2 ) 0,9673 [ y =1,638 x - 1.1847]. Более низкий предел обнаружения был достигнут в дозозависимом диапазоне (3–100 пг / мл) из-за большего количества иммобилизации антител на чувствительной поверхности из-за наноматериалов и улучшенного поверхностного тока. Кроме того, контрольные эксперименты с соответствующими биомолекулами не показали изменений емкости, а повышенный уровень IL-3 в сыворотке крови человека увеличил емкость, что указывает на специфическое и избирательное обнаружение IL-3. Это исследование идентифицирует и количественно определяет IL-3 с помощью потенциально полезных методов и помогает в диагностике приступа сепсиса.
Введение
Сепсис - это смертельное состояние, которое возникает, когда организм серьезно реагирует на инфекцию [1]. Из-за атаки сепсиса организм производит более высокий уровень сигнальных биомолекул, называемых «цитокинами», которые привлекают иммунные клетки. Увеличивающееся количество этих клеток секретирует больше цитокинов, и цитокиновый шторм привлекает больше иммунных клеток. Вместо того, чтобы контролировать первоначальную инфекцию, иммунные факторы атакуют органы и ткани тела. Кроме того, эта инфекция запускает цепную реакцию во всем организме и вызывает органную недостаточность и повреждение тканей [2]. В частности, сепсис начинается в легких, коже, мочевыводящих путях и желудочно-кишечном тракте и широко распространяется.
к другим органам, что приводит к повреждению органа. Поэтому необходимо раньше останавливать процесс, чтобы не допустить нападения на другие органы. Выявление сепсиса на ранних стадиях с помощью подходящего биомаркера помогает обеспечить быстрое лечение пациентов и спасти жизни. Исследователи обнаружили, что воспалительный фактор интерлейкина-3 (IL-3) является независимым предиктором атаки и смерти сепсиса, вызванных B-клетками активатора врожденного ответа (IRA) после активации Toll-подобного рецептора. Кроме того, было обнаружено, что более высокий уровень IL-3 был связан с более высоким уровнем смертности у пациентов с сепсисом, и было подтверждено, что IL-3 играет важную роль в иммунной регуляции и более высоких ответах на кортикостероиды во время сепсиса. Это исследование было направлено на количественное определение уровня IL-3 с использованием емкостного электрохимического датчика, модифицированного нанокомпозитом цеолит-оксид железа (цеолит-железо).
Обнаружение биомолекул с помощью биосенсоров сильно зависит от иммобилизации молекулы-мишени или детектирующей молекулы на поверхности электрода преобразователя [3]. Большее количество иммобилизованных зондов захвата с правильной ориентацией приводит к более низким пределам обнаружения цели [4]. В большинстве случаев иммобилизация зонда захвата осуществляется посредством физической адсорбции, электростатического взаимодействия, ковалентного связывания и захвата биомолекул полимерами [5, 6]. Может быть трудно добиться воспроизводимости и биосовместимости иммобилизованных биомолекул с помощью вышеуказанных методов иммобилизации. В частности, усложняется прикрепление меньших молекул захвата, таких как РНК, ДНК, аптамеры и пептиды, к сенсорным поверхностям [7, 8]. Различные исследователи использовали разные техники для эффективной иммобилизации. В последнее время наноматериалы стали очень привлекательными для использования в процессе иммобилизации биомолекул на чувствительных поверхностях [9,10,11]. Наночастицы золота были эффективно иммобилизованы на различных сенсорных поверхностях, таких как полистирольные подложки для ELISA и алюминиевые электроды, и захватили потенциальные молекулы, включая антитела, белки, ДНК и аптамеры. Помимо кремнезема, для иммобилизации биомолекул обычно используются алюминий и графен. Эти наноматериалы увеличивают количество молекул захвата и обеспечивают биосовместимость и стабильность биомолекул на чувствительных поверхностях, что помогает улучшить стратегию обнаружения. В последнее время неорганические материалы, такие как цеолит, глина и золь-гель, привлекают внимание исследователей для решения этих проблем. Более того, синтез наноматериалов с использованием более экологичных подходов очень поощряется из-за значительных связанных с этим преимуществ, таких как отсутствие использования опасных материалов и меньшая стоимость [12,13,14,15]. Кроме того, можно использовать индивидуальные подходы для достижения желаемых размеров и форм наноматериалов. Текущее исследование соответствовало этому подходу и позволило получить цеолитный наноматериал в сочетании с изолированным железом для создания нанокомпозита.
Цеолит представляет собой кристаллический микропористый алюмосиликат, состоящий из TO 4 тетраэдры и атомы O [16]. Это многообещающий материал для биомолекулярной иммобилизации из-за его большей площади поверхности, способности к ионному обмену, контролируемой гидрофобности / гидрофильности, а также высокой механической и теплопроводности. Таким образом, различные исследования в области биосенсоров были проведены с использованием цеолитного материала для процесса биомолекулярной иммобилизации и достигли более низких пределов обнаружения для разработки биосенсоров, таких как сенсоры глюкозы и сенсоры мочевины [17,18,19]. Точно так же наноматериалы железа улучшают эффект катионообменных свойств и быстро реагируют на изменения тока при взаимодействии с биомолекулами. Нанокомпозит цеолит-оксид железа с уникальным составом, использованный в этом исследовании, улучшает высокие характеристики датчика, дополнительно обеспечивая улучшенную чувствительность за счет улучшения проводимости. В этом исследовании основное внимание уделялось наноматериалам цеолит-железо, извлеченным из летучей золы угольных шахт, и их использованию в качестве подложек для емкостных электродов для иммобилизации улавливающего зонда, представляющего собой антитело против IL-3. По сравнению с предыдущими случаями обнаружения различных интерлейкинов с помощью наноматериалов [20,21,22], текущая сенсорная система обеспечивает улучшения по нескольким направлениям. Например, его более высокая пригодность для электрохимических датчиков требует меньшего количества экспериментальных этапов, и он демонстрирует пригодность для химической функционализации поверхности и высокую способность не загрязнять.
Емкостный биосенсор - это электрохимический датчик, созданный путем регистрации притяжения между зондом и мишенью, взаимодействующими на поверхности электрода. Емкостной биосенсор помогает измерять изменения в диэлектрическом слое на границе раздела электродов, когда целевая биомолекула связывается с иммобилизованным зондом на чувствительной поверхности [23]. Емкость между электродом и электролитом описывается как C =(2 nε 0 εA ) / d , где ε :диэлектрическая проницаемость, А :площадь поверхности пластины, ε 0 :диэлектрическая проницаемость свободного пространства, n :количество повторяющихся пальцев и d :толщина изоляционного слоя [24, 25]. Емкостной нефарадеевский биосенсор помогает избежать денатурации белков, вызванной металлизацией, и улучшает взаимодействие мишени и связывания зонда [26, 27]. В различных исследованиях использовались емкостные биосенсоры для идентификации различных молекул-мишеней, включая нуклеотиды, тяжелые металлы, белки и органические молекулы [23, 28, 29, 30, 31]. В этом исследовании эксперимент с нефарадеевским емкостным биосенсором проводился на поверхности электрода, модифицированного цеолитом и железом. Цеолит-железо был прикреплен к емкостному электроду через (3-аминопропил) -триметоксисилан в качестве аминного линкера, а затем анти-IL-3 был прикреплен к поверхности за счет притяжения между поверхностью амина и карбоксильной (COOH) группой антитело. Электрод, модифицированный антителами против ИЛ-3, использовался для количественного определения ИЛ-3 и диагностики приступа сепсиса.
Материалы и методы
Аппаратура и реагенты
Летучая зола была получена с тепловой электростанции в Индии. Гидроксид натрия и серная кислота были приобретены у Sigma Aldrich (Миссури, США). (3-Аминопропил) триметоксисилан (APTMS) был получен от Merck (Нью-Джерси, США). Фильтровальная бумага Whatman была получена от Thermo Fisher Scientific (Массачусетс, США). Антитела к IL-3 и анти-IL-3 были получены от Santa Cruz Biotechnology (Техас, США). Для анализа наноматериала цеолит-железо методами, описанными ранее [ 32].
Синтез наноматериала цеолит-железо
Наноматериалы цеолит-железо были синтезированы с использованием железа, кремнезема и оксида алюминия, извлеченных из летучей золы. В этой процедуре были задействованы следующие три основных этапа:(1) разделение частиц железа; (2) экстракция алюмосиликата натрия; и (3) получение наночастиц цеолит-железо методом золь-гель-синтеза.
Отделение железа от летучей золы
Аликвоту золы-уноса объемом 25 г смешивали с 500 мкл дистиллированной воды и перемешивали в течение 30 мин с использованием магнитной мешалки. Частицы железа, прилипшие к магнитной мешалке, отделяли, а затем 1 г отделенных частиц смешивали с 25% серной кислотой и перемешивали в течение 1 ч при 50 ° C. Затем железосодержащий раствор и частицы железа были разделены фильтровальной бумагой Whatman и использованы в качестве основы для оксида железа для синтеза наноматериала цеолит-железо.
Извлечение алюмосиликата натрия из летучей золы
Метод щелочной экстракции был использован для извлечения алюмосиликата натрия из летучей золы методом щелочной экстракции [33]. Сначала 25 г золы-уноса, отделенной от железа, смешивали с 500 мкл 2 М гидроксида натрия и нагревали при 100 ° C при перемешивании в течение 6 часов. После охлаждения раствора алюмосиликат натрия (раствор в смеси) отделяли фильтровальной бумагой Whatman. Отфильтрованный раствор использовали в качестве основы для синтеза цеолита.
Наноматериал цеолит-железо, синтезированный золь-гелевым методом
Извлеченное железо и алюмосиликат натрия были использованы в качестве основы для синтеза наноматериалов цеолит-железо золь-гель методом. На первом этапе стакан, содержащий 200 мл алюмосиликата натрия при pH 12, был помещен на электрическую плиту при перемешивании. Затем раствор титровали раствором железа при pH 1, добавляя по каплям количество раствора железа до достижения pH 7. При pH 7 образовывался белый гель, и этот гель непрерывно перемешивали в течение ночи для получения однородно распределенных наночастиц цеолита-железа. . На следующий день гель отделяли центрифугированием (10,000 × g в течение 10 мин), а затем промывали 25% этанолом и дистиллированной водой. Конечный продукт сушили при 100 ° C в течение 1 ч с получением порошка, состоящего из наноматериалов цеолит-железо. Поверхность наноматериала цеолит-железо была охарактеризована методами FETEM и FESEM. Энергодисперсионный рентгеновский анализ (EDX) также был проведен для идентификации элементов в цеолите-железе.
Аминовая модификация цеолита и железа и функционализация поверхности емкостного электрода
Амин наносили на поверхность цеолита-железа с помощью силанового связующего агента APTMS. Для этого 1 г цеолита-железа смешивали с 1% КОН в течение 10 мин, а затем избыток КОН удаляли дистиллированной водой. После этого обработанный КОН цеолит-железо смешивали с 1% APTMS, и смесь помещали на нагретую мешалку на ночь. На следующий день наноматериал промывали этанолом и отделяли центрифугированием (10,000 × g в течение 10 мин). Этот APTMS-цеолит-железо прикрепляли к поверхности емкостного электрода для идентификации IL-3. Для этой иммобилизации APTMS-цеолит-железо наносили по каплям на гидроксилированный электрод и выдерживали при комнатной температуре в течение 3 часов. Связь между нанокомпозитом цеолит-оксид железа, APTMS и чувствительной поверхностью была обусловлена взаимодействием силана с образовавшимися оксидными группами. В общем, силановое связывание происходит с множественными ответвлениями, доступными оксидным группам, что дает связи между нанокомпозитом цеолит-оксид железа, APTMS и чувствительной поверхностью. Благодаря этим множественным связям формируется пространственное расположение на чувствительной поверхности. После промывания поверхности этанолом, а затем водой, был проведен процесс иммобилизации антител против ИЛ-3 для взаимодействия с ИЛ-3.
Определение IL-3 на поверхности емкостного электрода, модифицированного анти-IL-3
Описанная выше поверхность была образована путем связывания с амином, что позволяет взаимодействовать с доступными группами COOH при присоединении антитела. ИЛ-3 был идентифицирован на поверхности емкостного электрода, иммобилизованного против ИЛ-3. Для этого IL-3 в концентрации 100 пг / мл разбавляли в буфере PBS и капали на поверхность электрода, модифицированного антителами. После иммобилизации антитела оставшаяся несвязанная поверхность блокировалась PEG-COOH (1 мг / мл). Аналогичная реакция на антитело-APTMS происходит при присоединении PEG-COOH. Величина емкости регистрировалась до и после взаимодействия с Ил-3. Учитывались различия в величине связывания IL-3 с его антителом. Кроме того, для расчета предела обнаружения IL-3 титровали от 3 до 50 пг / мл и независимо капали на поверхности, модифицированные антителами. Другая экспериментальная процедура была выполнена, как описано ранее. Разница в значениях емкости для каждой концентрации IL-3 была рассчитана и нанесена на график для расчета обнаружения IL-3 с помощью R 2 ценность. Когда IL-3 прикрепляется к иммобилизованной поверхности антитела, происходит подлинное взаимодействие.
Биообрастание и выборочное определение IL-3 на поверхности электрода с модифицированной емкостью цеолита и железа
Эксперимент по биообрастанию проводили при трех различных условиях биомолекул, включая присутствие неиммунного антитела или контрольного белка и отсутствие антитела к IL-3. В первом случае вместо антитела к IL-3 использовали неиммунное антитело; во втором эксперименте вместо ИЛ-3 использовали контрольный белок; и последний эксперимент проводился без антитела к IL-3. Значения емкости сравнивали для специфического взаимодействия антитела IL-3 с IL-3. Селективный эксперимент проводили путем добавления IL-3 в разведение 1:100 сыворотки человека и добавления его по каплям на поверхность электрода, модифицированного анти-IL-3. Изменения емкости регистрировали для каждой концентрации IL-3, чтобы идентифицировать селективную идентификацию IL-3. Воспроизводимость была подтверждена повторением экспериментов три раза (в трех экземплярах) с аналогичными устройствами, изготовленными из одной партии. Также были определены срок хранения и стабильность поверхности с иммобилизованным зондом.
Результаты и обсуждение
Сепсис - это состояние, при котором в иммунной системе выделяется большое количество химических веществ, которое вызывает широко распространенное воспаление с серьезным повреждением органов. На рис. 1а схематически показана идентификация ИЛ-3 на поверхности емкостного электрода, модифицированного анти-ИЛ-3, для определения состояния, связанного с сепсисом. Цеолит-железо, модифицированный APTMS, использовали для прикрепления улавливающих антител к поверхности чувствительного электрода. APTMS на поверхности цеолита-железа был иммобилизован на поверхности электрода за счет взаимодействия между амином на наноматериале и группами ОН на поверхности электрода. Рисунок 1b подтверждает целостность поверхностного электрода на емкостном датчике, зафиксированную под мощным микроскопом. Антитело было связано с поверхностью через COOH и амин цеолита-железа. Цеолит-железо помогает прикрепить большее количество APTMS к чувствительному электроду, что помогает захватить больше антител на поверхности емкостного электрода. Различные исследования показали, что иммобилизация зонда захвата на чувствительной поверхности играет решающую роль в снижении предела обнаружения целевой молекулы. В этом исследовании наноматериал цеолит-железо использовался для прикрепления антитела против IL-3 к поверхности чувствительного электрода. Более высокая иммобилизация антител против ИЛ-3 при правильной ориентации помогает достичь более низких пределов обнаружения ИЛ-3.
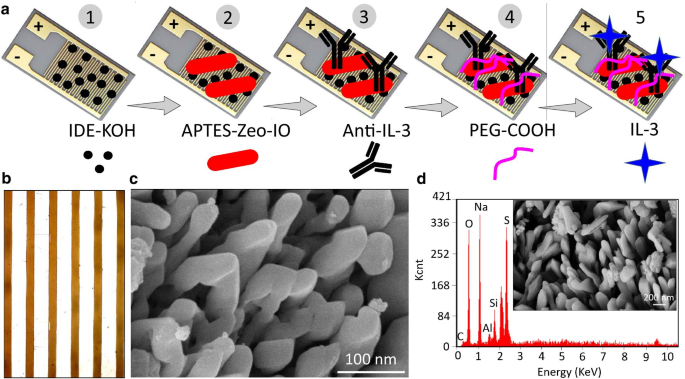
а Схематическое изображение идентификации IL-3 на поверхности измерения емкости, модифицированной против IL-3. APTMS-модифицированный цеолит-железо использовали для присоединения захватывающего антитела, а затем взаимодействовали с IL-3. PEG-COOH использовали в качестве блокирующего агента. б Морфологический анализ емкостной чувствительной поверхности с помощью мощной микроскопии. c Морфологический анализ цеолита-железа методом FESEM. Наноматериалы формировались с равномерным распределением и в продольном размере. г EDX-анализ. Обнаружено присутствие основных элементов Si, Al, Fe и O. Вставка рисунка получена FESEM при малом увеличении
Морфологический анализ наноматериала цеолит-железо с помощью FESEM и FETEM
На рис. 1c, d (вставка) показано морфологическое изображение наноматериала цеолит-железо, полученное с помощью FESEM при разном увеличении и элементного анализа EDX. Полученный наноматериал цеолит-железо был гладким и равномерно распределенным с плотно уложенной продольной наноструктурой. Размер этой наноструктуры составлял ~ 30 нм, и полученное изображение показывает, что нанокомпозит был расположен однородной формы и хорошо распределен на надлежащем расстоянии. Изображение FETEM также подтвердило форму, аналогичную полученной с помощью FESEM для сформированных нанокомпозитов цеолит-железо (рис. 2a, b). Результат EDX подтвердил присутствие Fe, Al, Si и O в синтезированном нанокомпозите цеолит-железо (рис. 2c, d). Было обнаружено, что содержание основных элементарных атомов Si, Al, Fe и O составляет 3,46, 0,78, 2,13 и 24,39% соответственно. Этот результат FESEM и EDX подтверждает образование наноматериалов цеолит-железо.
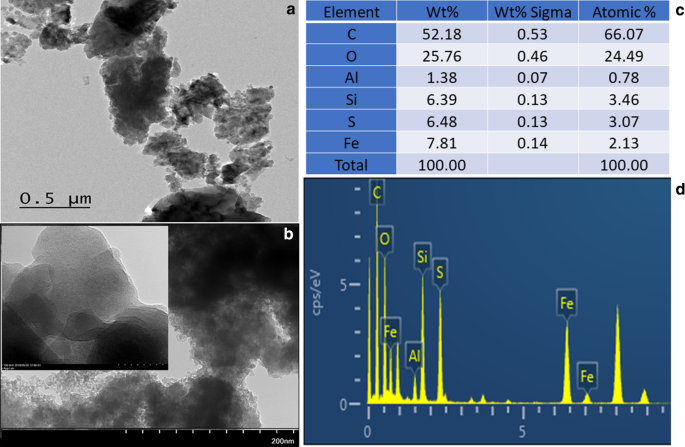
Изображения FETEM цеолита-железа на a Масштаб 50 нм и b Масштаб 200 нм. Наноматериал был сформирован с равномерным распределением. c EDX-анализ, подтверждающий наличие основных элементов Si, Al, Fe, C и O
Подготовка чувствительного электрода для определения IL-3
Иммобилизация антител против ИЛ-3 на емкостном биосенсоре подтверждается изменением уровня емкости после каждой биомолекулярной иммобилизации. На рис. 3а показаны изменения емкости в процессе прикрепления антител к поверхности, модифицированной цеолитом и железом. Как показано на рис. 3а, поверхность емкостного электрода, связанного с КОН, имеет значение емкости 1,74 × 10 09 . nF, а после добавления по каплям APTMS-цеолита-железа оно увеличивалось до 2,02 × 10 09 нФ. Это увеличение емкости подтвердило прикрепление наноматериалов к чувствительному электроду. Кроме того, после добавления антитела против ИЛ-3 значение емкости резко увеличилось до 3,42 × 10 09 нФ. Этот более высокий прирост был отмечен из-за большего количества иммобилизации антител на цеолите-железе, модифицированном APTMS. Кроме того, наноматериалы показали правильное расположение с большим количеством APTMS на поверхности чувствительного электрода, что в конечном итоге привело к привлечению большего количества антител. Наконец, для блокировки был добавлен PEG-COOH, и было обнаружено, что емкость увеличилась до 3,64 × 10 09 . нФ. Датчик работает на основе изменений поверхностного заряда и, в конечном итоге, изменения емкости. Изменения поверхностного заряда зависят от присоединения / взаимодействия молекул. Каждая молекула несет разные заряды и влияет на емкость датчика. Поэтому при измерениях учитывалась разница в емкости. Отмечены более высокие изменения емкости из-за большей занятости антител к IL-3 на поверхности чувствительного электрода (рис. 3b). PEG-COOH помогает уменьшить неспецифическое связывание IL-3 на поверхности чувствительного электрода и устраняет ложноположительные результаты. Различные исследования доказали, что полимеры на основе ПЭГ на чувствительных поверхностях улучшают биосовместимость, снижают отношение сигнал / шум и обеспечивают правильную ориентацию иммобилизованных биомолекул на чувствительных поверхностях, что приводит к более низкому пределу обнаружения датчика [34,35, 36,37]. Поскольку поверхность APTMS электростатически притягивает другие биомолекулы, PEG-COOH использовался для покрытия избыточной поверхности APTMS на наноматериале цеолит-железо, что помогает уменьшить биообрастание. Поверхность, модифицированная анти-ИЛ-3, была использована для идентификации ИЛ-3.
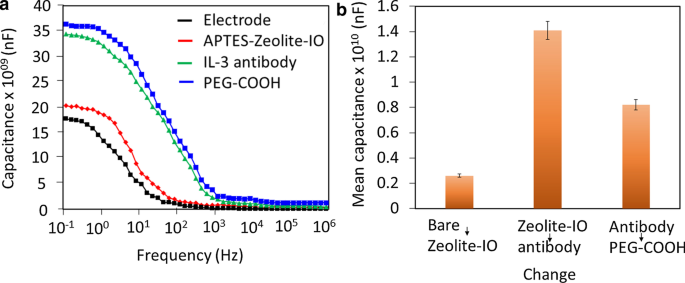
а Процесс прикрепления антител к поверхности, модифицированной цеолитом и железом. значения емкости увеличивались после каждой иммобилизации молекул. б Разница в емкости. Иммобилизация антител против ИЛ-3 показала более высокое изменение значения емкости. Значения были усреднены с использованием трех измерений в трех повторностях. [Цеолит-IO - Цеолит-оксид железа]
Определение и количественная оценка IL-3 на поверхности антитела против IL-3
Количество IL-3 определяли на чувствительной поверхности емкостного электрода, модифицированного анти-IL-3. Первоначально более высокая концентрация IL-3 (100 пг / мл) была протестирована на поверхности, модифицированной антителами, и значение емкости увеличилось с 3,74 × 10 10 нФ до 13 × 10 10 нФ. Это увеличение подтверждает взаимодействие IL-3 с антителом против IL-3 (фиг. 4a). Аналогичный эксперимент был проведен с концентрацией IL-3 от 3 до 50 пг / мл. Как показано на рис. 4b, значения емкости увеличились до 4,56 × 10 10 . нФ, 5,84 × 10 10 нФ, 6,64 × 10 10 нФ, 8,39 × 10 10 нФ и 12 × 10 10 нФ. Было отмечено, что с увеличением концентрации Ил-3 значения емкости постепенно увеличивались (рис. 5а). Разница в значениях емкости была рассчитана и нанесена на график в таблице Excel, а обнаружение IL-3 было рассчитано как 3 пг / мл со значением R2, равным 0,9673 (рис. 5b). Был обнаружен линейный дозозависимый ответ с различными концентрациями ИЛ-3 (3–100 пг / мл) при взаимодействии с анти-ИЛ-3. Однако при титровании при других концентрациях образцы были насыщенными.
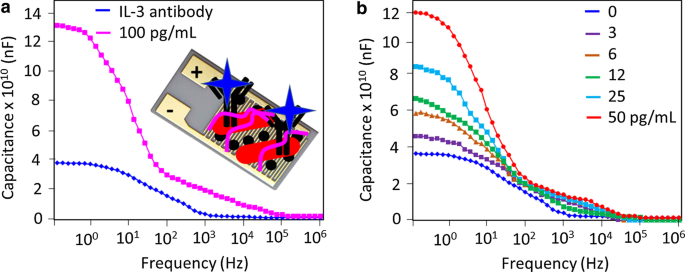
Определение IL-3 на поверхности, модифицированной анти-IL-3. а Идентификация 100 пг / мл ИЛ-3. Явные изменения емкости были отмечены после добавления ИЛ-3 по каплям. На вставке к рисунку показана схема. б Титрование различных концентраций IL-3 на антитело против IL-3. При всех концентрациях ИЛ-3 были отмечены изменения емкости
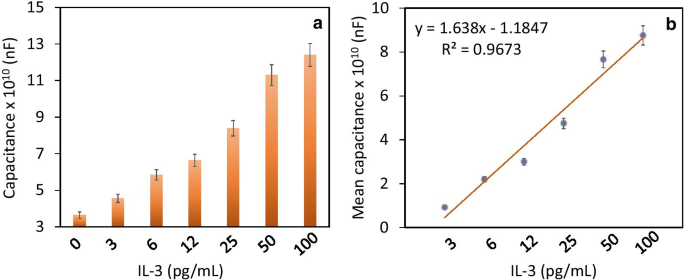
а Значение емкости для каждой концентрации IL-3. Увеличение концентрации ИЛ-3 приводит к постепенному увеличению величины емкости. б Разница в величине емкости для каждой концентрации ИЛ-3. Значения были нанесены в таблицу Excel, и предел обнаружения IL-3 был рассчитан как 3 пг / мл. Значения были усреднены с использованием трех измерений в трех повторностях
Биообрастание / необрастание на емкостном электроде APTES-цеолит-модифицированный железом
Биологическое обрастание - самая большая проблема в любом виде биосенсора, которая приводит к ложноположительной идентификации цели на сенсорной поверхности. Блокирующие агенты, такие как БСА, этаноламин и полимеры на основе ПЭГ, представляют собой распространенные молекулы, которые уменьшают биообрастание на чувствительных поверхностях. В данном случае PEG-COOH использовали в качестве блокирующего агента, и эффект биообрастания был подтвержден в трех различных контрольных экспериментах, а именно без антитела к IL-3, с неиммунным антителом и с контрольным белком (IL-8). Как показано на рис. 6а, во всех трех контрольных экспериментах не удалось повысить значение емкости, что указывает на конкретную идентификацию IL-3 без какого-либо биообрастания.
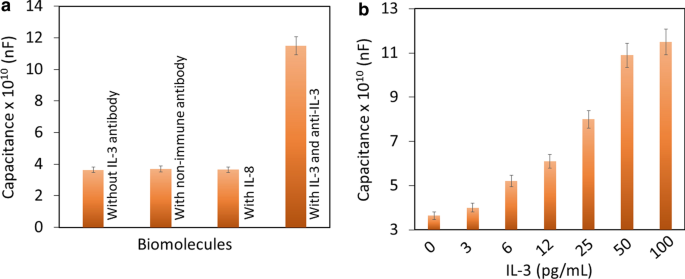
а Специфическое обнаружение ИЛ-3. Контрольные молекулы не показали увеличения значения емкости, что указывает на специфическое обнаружение IL-3. б Повышение уровня IL-3 в сыворотке крови человека. Пик в сыворотке человека увеличивал емкость с увеличением концентрации IL-3. Этот результат подтверждает избирательное обнаружение IL-3. Значения были усреднены с использованием трех измерений в трех повторностях
Повышение уровня IL-3 в сыворотке крови человека и стабильность
Различные концентрации IL-3 были увеличены в сыворотке крови человека и подвергнуты той же экспериментальной процедуре для идентификации IL-3 в реальных жизненных ситуациях. Как показано на фиг. 6b, повышенный уровень IL-3 в сыворотке крови человека явно вызывал повышенные значения емкости с повышенными концентрациями IL-3. Этот результат подтверждает избирательную идентификацию IL-3 с помощью емкостного электрода, модифицированного против IL-3.
Что касается воспроизводимости, чувствительная поверхность ведет себя хорошо с минимальными значениями погрешности. Срок службы изготовленного сенсорного наноматериала с прикрепленной поверхностью может быть продлен на три месяца при надлежащем хранении в эксикаторе. Однако после прикрепления зонда поверхность была стабильной в течение 2 недель и имела тенденцию к потере 19% стабильности, а потеря стабильности стала резкой, начиная с 3-й недели. Чтобы доказать высокую производительность текущего датчика, было проведено сравнительное исследование с доступными в настоящее время датчиками, и результаты показывают, что он сопоставим и ведет себя лучше в нескольких случаях (таблица 1).
Заключение
Сепсис опасен для жизни, вызывает подавляющую иммунную реакцию, чрезвычайно опасен и поражает все тело. Это исследование продемонстрировало идентификацию биомаркера сепсиса (IL-3) на емкостном электроде. Наноматериал цеолит-железо был извлечен из модифицированного углем емкостного электрода, чтобы увеличить ток при связывании биомолекул с чувствительным электродом. Аминовую модификацию проводили для присоединения антитела против IL-3 к цеолиту-железу. Обнаружение IL-3 проводилось на электроде, модифицированном антителами, и предел обнаружения IL-3 достигал 3 пг / мл. Дальнейшие контрольные эксперименты не показали увеличения значения емкости, подтверждающего специфическое обнаружение IL-3, а выборочные эксперименты с добавлением IL-3 в сыворотке крови человека показали явное увеличение емкости. Этот экспериментальный метод определяет уровни IL-3 и помогает диагностировать приступы сепсиса.
Доступность данных и материалов
Все данные полностью доступны без ограничений.
Сокращения
- IL-3:
-
Интерлейкин-3
- pg:
-
Пикограмма
- mL:
-
Миллилитр
- мкл:
-
Микролитр
- M:
-
Молярный
- FESEM:
-
Автоэмиссионный просвечивающий электронный микроскоп
- FETEM:
-
Автоэмиссионный растровый электронный микроскоп
- EDX:
-
Энергодисперсионный рентгеновский снимок
- IRA:
-
Активатор врожденной реакции
- COOH:
-
Карбоновые
- ДНК:
-
Нуклеиновая кислота дезоксирибозы
- РНК:
-
Нуклеиновая кислота рибозы
- ELISA:
-
Иммуноферментный анализ
- APTMS:
-
(3-аминопропил) триметоксисилан
- КОН:
-
Гидроксид калия
- PEG:
-
Полиэтиленгликоль
Наноматериалы
- Демонстрация гибкого биосенсора на основе графена для чувствительного и быстрого обнаружения клеток рака яи…
- Углеродные наноточки как двухрежимные нанодатчики для селективного обнаружения перекиси водорода
- Сверхчувствительный биосенсор для обнаружения ДНК холерного вибриона с помощью композитных наносфер полист…
- Нанопетали из мезопористого оксида никеля (NiO) для сверхчувствительного определения уровня глюкозы
- Атомное осаждение нанопленок оксида индия для тонкопленочных транзисторов
- Фотокаталитическая активность тройного нанокомпозита аттапульгит – TiO2 – Ag3PO4 для разложения родамина B при мод…
- Разработка электропряденого биокомпозита хитозан-полиэтиленоксид / фибриноген для потенциального заживлен…
- Флуоресцентный аптасенсор на основе оксида графена для обнаружения включения CCRF-CEM
- Двумерные мезопористые микрочипы VO2 для высокопроизводительного суперконденсатора
- Жерновое отшелушивание:отшелушивание с истинным сдвигом для многослойного оксида графена большого размера



