Разработка и оценка системы полуколичественного определения физических свойств кожи после воздействия наночастиц серебра
Аннотация
Чтобы гарантировать безопасное использование наночастиц серебра (нАг) в косметике, необходимо выявить физические свойства нАг внутри кожи, так как эти свойства могут изменяться в процессе чрескожного всасывания. В этом исследовании мы стремились создать аналитическую систему, основанную на масс-спектрометрии с индуктивно связанной плазмой с единичными частицами (sp-ICP-MS), для определения физических свойств nAg в коже. Во-первых, мы оптимизировали метод предварительной обработки для солюбилизации образцов кожи, а затем показали, что большая часть nAg была восстановлена обработкой гидроксидом натрия, оставаясь при этом в форме частиц. Для разделения кожи на эпидермис и дерму мы проверили несколько условий микроволнового излучения. Анализ sp-ICP-MS показал, что применение 200 Вт в течение 30 с было оптимальным, так как это условие обеспечивало полное разделение слоев кожи без изменения физических свойств большинства нАг. Наконец, мы оценили применение in vivo, проанализировав количество, а также физические свойства Ag в эпидермисе, дерме и периферической крови мышей после воздействия на кожу nAgs или Ag + . Последующий анализ sp-ICP-MS показал, что нАг может абсорбироваться и распределяться в более глубокие слои в ионизированной форме, тогда как Ag + абсорбируется и распределяется без изменения физических свойств. Это исследование показывает, что для того, чтобы получить полное представление о реакции кожи на воздействие нАг, важно учитывать распределение и размер частиц не только нАг, но и серебра + высвобождается из nAg в кожу.
Введение
Последние технологические достижения в области нанотехнологий ускорили разработку инженерных наночастиц (ENP), которые представляют собой частицы размером менее 100 нм. Благодаря своим полезным свойствам, таким как улучшенное проникновение в ткани и поверхностная реакция, по сравнению с материалами микро- или большего размера, ENP широко используются в различных продуктах, включая косметику, продукты питания и медицину [1,2,3]. Например, наночастицы серебра (nAgs), один из наиболее распространенных типов ENP, включаются в косметику из-за их антибактериальных свойств, возникающих в результате постоянного высвобождения ионов серебра (Ag + ) [4, 5]. Однако уникальные физико-химические свойства, связанные с малым размером частиц нАг, могут быть опасными. Известно, что эти частицы могут разрушать непреодолимые барьеры, такие как гематоэнцефалический барьер, и вызывать воспаление [6]. Кроме того, в некоторых исследованиях сообщается, что ENP могут проникать через кожный барьер [7,8,9]. Следовательно, для определения безопасности непрерывного использования этих частиц важно понимать токсические эффекты, связанные с ENP, содержащими нАГ, путем исследования динамики этих частиц в тканях, таких как кожа.
Для обеспечения безопасности необходимо понимать возможные риски, связанные с использованием ENP, что включает в себя комплексные концепции «опасностей» (потенциальная токсичность) и «условий воздействия». Несмотря на то, что риски ENP были проанализированы во всем мире, лишь в нескольких исследованиях изучались условия, связанные с воздействием ENP [10]. В частности, сообщалось, что nAgs и Ag + могут изменять свои физические свойства в теле. Например, ионизация nAgs приводит к образованию nAgs с меньшим размером частиц и высвобождению Ag + [11]. Напротив, nAg, имеющие малый размер частиц, могут быть обнаружены в кишечном эпителии крыс после перорального введения ацетата серебра [12]. Кроме того, мы недавно сообщили, что по сравнению с меньшими nAgs и Ag + , более крупные nAg легче обнаруживаются в грудном молоке кормящих мышей, подвергшихся воздействию этих nAg [13]. Следовательно, nAgs может изменять свои физические свойства в организме, что, в свою очередь, приводит к изменению кинетики. Таким образом, чтобы понять связанные с этим риски, необходимо оценить физические свойства, такие как размер частиц, этих частиц, и различать эти частицы и ионы в организме.
В этом отношении мы применили масс-спектрометрию с индуктивно связанной плазмой с единичными частицами (sp-ICP-MS), которая вводит максимум одну частицу в анализатор за время пребывания. Это эффективный метод, который можно использовать для определения размера частиц путем анализа пиковой интенсивности и концентрации частиц с помощью пиковых скоростей. Частицы и ионы можно различить, анализируя как пиковые, так и фоновые сигналы [14]. Ранее мы оптимизировали метод предварительной обработки биологических образцов для sp-ICP-MS для полуколичественного определения физических свойств ENP в различных органах, таких как печень, сердце, легкие, почки и селезенка [15]. P>
Кожа состоит из эпидермиса, включая роговой слой (SC), и дермы, содержащей кровеносные сосуды, лимфатические сосуды и нервы [16]. Следовательно, попадание ENP в каждый слой кожи может вызывать токсичность в той или иной степени. Например, распределение наночастиц диоксида титана в кератиноцитах кожи человека в клетках эпидермиса может стимулировать производство активных форм кислорода [17]. Более того, у безволосых мышей воздействие на кожу наночастиц диоксида титана в течение 60 дней привело не только к патологическим изменениям, таким как истончение дермы из-за местной токсичности, но и к патологическим изменениям в печени, таким как некроз разжижения из-за системной токсичности, которая распространяется через кровеносные сосуды в дерме [18]. Кроме того, биологические ответы в каждом слое также могут варьироваться в зависимости от физических свойств, таких как размер частиц, и различий между частицами и ионами [19]. Чтобы понять безопасность использования nAg, необходимо понимать физические свойства и биораспределение nAgs после контакта с кожей.
Чтобы решить эту конкретную проблему, необходим подход, который может предварительно обработать кожу и разделить ее слои без каких-либо потерь во время восстановления или изменения физических свойств ENP. Однако такой оптимальный подход для кожи так и не разработан.
В этом исследовании мы оптимизировали подход к предварительной обработке, который полуколичественно определяет физические свойства nAgs, модели ENP, в каждом слое кожи с помощью sp-ICP-MS, а затем оценили его эффективность in vivo.
Методы
Мыши
Slc:мышей ICR (самки, возраст 8 недель) были приобретены в Japan SLC (Сидзуока, Япония). Мышей помещали в комнату со следующим циклом свет-темнота:свет включается в 8 часов утра и выключается в 8 часов вечера. Пища и вода были доступны в виде кормовых гранул и системы водоснабжения, расположенной наверху клетки. Все протоколы экспериментов были выполнены в условиях, одобренных комитетом по исследованиям на животных Университета Осаки, Япония.
nAgs и Ag +
Суспензии нАг с блокировкой цитрат-лигандом диаметром 100 нм (nAg100) были приобретены в компании nanoComposix (Сан-Диего, Калифорния, США) в виде исходных дисперсий (1 мг / мл). Нитрат серебра (AgNO 3 ) был приобретен у Wako Pure Chemical Industries (Осака, Япония), также в виде исходных дисперсий (1 мг / мл). RM8013, используемый в качестве стандарта для расчета эффективности транспортировки, был приобретен в Национальном институте стандартов и технологий (Гейтерсбург, Мэриленд, США). Каждый тип наночастиц перед использованием обрабатывали ультразвуком в течение 10 мин. Наночастицы и ионы также встряхивали в течение 10 с перед использованием.
Реагенты
Гидроксид натрия (NaOH, 0,1 моль / л) был приобретен у Nacalai Tesque Company (Осака, Япония) и азотная кислота (HNO 3 , 70%) была приобретена у Kanto Kagaku Chemical Industries (Токио, Япония). Был приготовлен фосфатно-солевой буфер (PBS), pH 7.
Оптимизация методов предварительной обработки
Эпидермис и дерма каждой мыши были разделены, смешаны с PBS ( w / v соотношение 1:10) и гомогенизировали. Гомогенат смешивали с раствором nAg100 100 нг / мл. Затем смесь обрабатывали одним из следующих реагентов при об. / Об. соотношение 1:1; 0,1 моль / л NaOH, 70% HNO 3 , или PBS. Образцы инкубировали в течение 3 часов при 37 ° C и подвергали sp-ICP-MS.
Отделение кожи с помощью микроволнового излучения
Каждую мышь подвергали эвтаназии изофлураном (Wako), после чего 2 см 2 Образец кожи спины (2 см × 1 см) иссекали с помощью хирургических ножниц и пинцета. Особое внимание было уделено предотвращению повреждения тканей во время процедуры иссечения. Для облучения кожи использовали микроволновую печь (RE-SW-20-H, Sharp, Япония) с частотой 2450 МГц. Образцы кожи помещали на тарелку и помещали в центр микроволновой печи. В соответствии с требованиями испытаний образцы кожи облучали в течение 10, 30 и 60 с при мощности 200, 600 и 900 Вт соответственно. После облучения образцы были быстро удалены, и каждый эпидермис и дерма были быстро отделены осторожным соскабливанием хирургическим пинцетом. Раствор nAg100 100 нг / мл использовали для анализа скорости восстановления и среднего диаметра nAg после облучения (200 Вт, 30 с).
Трансдермальное введение nAg100 и Ag +
Девятинедельные самки мышей Slc:ICR были разделены на 6 групп по 3 мыши в группе в соответствии с их массой тела. Мышей анестезировали изофлураном. Волосы на спине сбривали машинкой для стрижки (Panasonic®, Осака, Япония) и ручной бритвой (Gillette®, Германия). Затем nAg100 и Ag + (20 мкг / см 2 ) наносили непосредственно на поверхность площадью 2,25 см 2 (1,5 см × 1,5 см) дорсальной кожи и плотно покрытой неабсорбирующей пластиковой пленкой. На полиэтиленовую пленку помещали кусок марли такого же размера. С помощью самоклеящейся эластичной повязки покрыли марлю, обернув ее вокруг кожи, и кожа оставалась закрытой на 5 дней.
Предварительная обработка образцов кожи и крови
Через пять дней после лечения для анализа собирали периферическую кровь из ретроорбитального венозного сплетения и дорсальной кожи. Далее 2,25 см 2 Образцы кожи спины (1,5 см × 1,5 см) иссекали с помощью хирургических ножниц и пинцета. Особое внимание уделялось предотвращению повреждения тканей во время иссечения. SC-слои были последовательно удалены с помощью 2-сантиметровых кусочков липкой ленты (Scotch®, 3M) перед отделением эпидермиса от дермы. Кусочки тейпа прижимали к обработанному участку кожи спины, после чего прикладывали постоянное давление в течение 10 с. Двадцать кусочков ленты потребовалось для полного удаления SC каждой мыши. Затем дерму и эпидермис разделяли с помощью микроволнового излучения и гомогенизировали с помощью PBS ( w / v соотношение 1:10). Собранную кровь, а также гомогенаты дермы и эпидермиса обрабатывали 0,1 моль / л NaOH при об. / Об. соотношение 1:1 и инкубируют отдельно 3 ч при 37 ° C. После инкубации общую массу серебра в смесях крови, эпидермиса и дермы анализировали с помощью масс-спектрометрии с индуктивно связанной плазмой (ICP-MS). Количественная оценка и оценка физических свойств nAgs и Ag + были проведены с использованием sp-ICP-MS.
Измерение общей массы серебра
Для измерения общей концентрации серебра в образцах крови, SC, эпидермиса и дермы использовалась система Agilent 7700x ICP-MS (Agilent Technologies, Санта-Клара, Калифорния, США). Условия, при которых проводился анализ, были следующими:мощность ВЧ 1550 Вт; газ-носитель 1,05 л / мин Ar; и время задержки 100 мс. Измерения повторяли трижды в режиме МС. В качестве внутреннего стандарта для Ag использовали родий. Целевыми элементами анализа ICP-MS были 103 Rh и 107 Ag. Стандартные растворы серебра и родия были получены от Wako.
Анализ и расчет sp-ICP-MS
Для анализа sp-ICP-MS использовали Agilent 7700x ICP-MS (Agilent Technologies). Условия анализа были следующими:мощность ВЧ 1550 Вт; газ-носитель 1,05 л / мин Ar; время задержки 10 мс; и время анализа 30 с. Для расчета размера частиц использовались инструменты расчета отдельных частиц - RIKILT, опубликованный Wagenen Food Safety Research (Университет Вагенингена, Вагенинген, Нидерланды) [20].
Статистический анализ
Все статистические анализы проводились с использованием программного обеспечения GraphPad Prism версии 5.0 для Macintosh (GraphPad Software, La Jolla, CA, USA). Статистическая значимость была установлена на уровне P . <0,05.
Результаты и обсуждение
Стратегии создания метода для определения количества и физических свойств nAg на каждом слое оболочки
Чтобы определить количество и физические свойства nAg в каждом слое кожи, необходимо полностью растворить образцы кожи и подготовить образцы, пригодные для анализа sp-ICP-MS. Также важно разделить эпидермис и дерму без потерь во время восстановления или изменения физических свойств nAg, потому что нАг, не абсорбированный трансдермально, иногда может быть удален во время удаления SC с помощью ленты [21]. / P>
Что касается солюбилизации образцов кожи, мы ранее сообщали, что предварительная обработка NaOH является методом, оптимальным для количественной оценки, а также анализа физических свойств nAg в тканях животных, таких как печень, сердце, легкие, почки и селезенка [16]. Поэтому образцы кожи, использованные в этом исследовании, подверглись предварительной обработке NaOH.
Гидротермальная обработка, которая приводит к размягчению коллагеновых волокон и усиленному перевариванию ферментов, что способствует разделению на эпидермально-дермальном соединении (EDJ), широко используется для разделения кожи на эпидермальный и дермальный слои [22]. Хотя эти процедуры эффективно разделяют слои кожи, nAg в этих слоях может быть ионизирован в водном растворе, что приведет к изменению его физических свойств. Сообщается, что короткий импульс микроволнового излучения позволяет разделить кожу на эпидермальный и дермальный слои за счет тепловыделения, которое разрушает EDJ [23, 24]. Поэтому мы короткое время подвергали раствор микроволновому облучению без инкубации.
В совокупности мы предложили стратегию (проиллюстрирована на рис. 1), которая была подтверждена путем анализа скорости восстановления и изменений физических свойств nAg в каждом слое кожи.
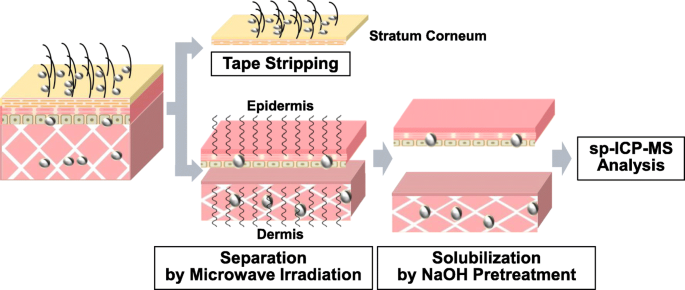
Стратегия определения количества и физических свойств nAg100 в каждом слое кожной ткани. Чтобы определить количество и физические свойства nAg100 в каждом слое кожной ткани, необходимо (1) полностью растворить кожные ткани и (2) разделить кожу на эпидермальные и дермальные ткани без потери ткани во время восстановления или изменений в тканях. физические свойства nAg100. В этом отношении мы сосредоточились на (1) предварительной обработке NaOH и (2) микроволновом облучении
Оптимизация методов предварительной обработки для обнаружения nAg100 в эпидермисе и дерме
Мы обратились к нашему предыдущему исследованию, чтобы оптимизировать метод предварительной обработки для солюбилизации образцов кожи. Ishizaka et al. [15] сообщили, что среди различных видов солюбилизирующих реагентов, таких как NaOH и HNO 3, Предварительная обработка NaOH была оптимальной. Таким образом, мы протестировали HNO 3 и NaOH в качестве кислотных и щелочных солюбилизирующих реагентов соответственно. Гомогенаты эпидермиса и дермы, выделенные из образцов кожи мыши, смешивали с nAg100 для получения конечной концентрации Ag 100 нг / мл с последующей обработкой каждым солюбилизирующим реагентом при 37 ° C. Сначала мы оценили скорость восстановления Ag после обработки этими реагентами. Анализ ICP-MS показал, что почти 100% степень извлечения была достигнута с помощью NaOH и HNO 3 только лечение (рис. 2а). Затем, чтобы оценить изменения физических свойств в результате каждой обработки, мы проанализировали восстановленные концентрации каждой частицы и иона. Анализ sp-ICP-MS показал, что nAg100 почти полностью ионизирован HNO 3 . Это предполагает, что HNO 3, в качестве кислотного реагента растворял частицы и превращал их в ионы, как также сообщалось в предыдущем исследовании [15]. Напротив, большая часть nAg100, обработанного NaOH, оставалась в виде частиц, а не ионов (рис. 2b). Таким образом, NaOH позволял большей части nAg100 оставаться в форме частиц. Наконец, было оценено распределение диаметров частиц, чтобы детально проанализировать физические свойства. HNO 3 обработка изменила средний диаметр частиц со 100 нм до 40 нм, что соответствовало ионизации nAg100. Напротив, средний диаметр частиц после обработки NaOH составлял приблизительно 100 нм, что соответствует начальному размеру частиц (рис. 2с). Это свидетельствует о том, что предварительная обработка NaOH была оптимальной для обнаружения nAg100 в коже мыши.
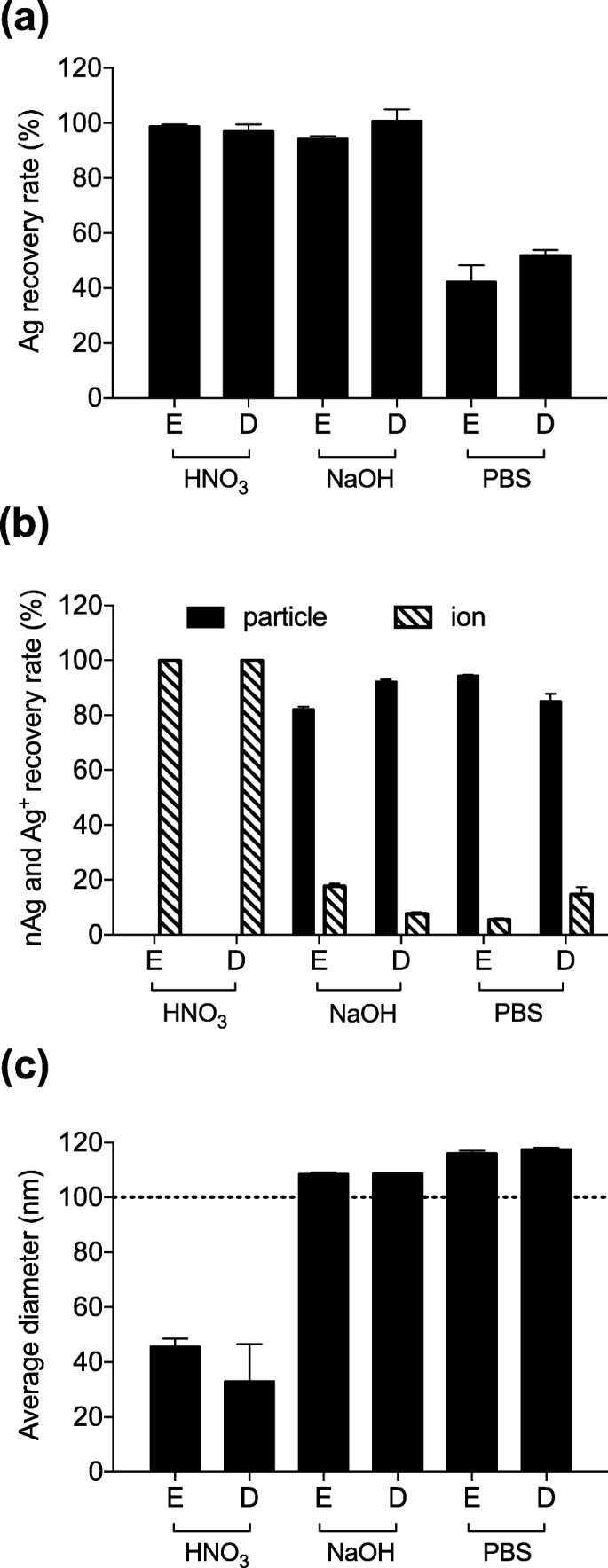
Предварительная обработка NaOH - оптимальный метод обнаружения nAg100 в дерме и эпидермисе. Два солюбилизирующих реагента (HNO 3 и NaOH) были проверены как растворители для предварительной обработки для лизирования тканей. Гомогенаты эпидермиса (E) и дермы (D) смешивали с nAg100 для получения конечной концентрации Ag 100 нг / мл и обрабатывали каждым солюбилизирующим реагентом при 37 ° C. Через 3 часа все образцы анализировали с помощью ICP-MS и sp-ICP-MS. а скорость извлечения Ag, b nAg (черные полосы) и Ag + (заштрихованные столбцы) скорость восстановления и c представлены средние диаметры частиц. Пунктирная линия представляет начальный размер частиц. Данные были выражены как среднее ± стандартное отклонение. ( нет =3)
Разделение образцов кожи на эпидермис и дерму с помощью микроволнового облучения и оценка скорости восстановления и изменений физических свойств нАГ
Чтобы разделить образцы кожи на эпидермальный и дермальный слои, мы применили различные условия микроволнового облучения, которые имели отношение к нашему исследованию и ранее сообщалось об успехе [24], и сравнили их эффективность в отношении разделяемости кожи и изменений в ней. физические свойства. Было замечено, что в условиях 200 Вт в течение 10 с, 600 Вт в течение 30 с, 600 Вт в течение 60 с, 950 Вт в течение 30 с и 950 Вт в течение 60 с, кожа не разделялась на эпидермальный и дермальный слои ( Рис. 3а). Более того, кожа была лишь частично разделена на эпидермальный и дермальный слои в условиях 200 Вт в течение 60 с, 600 Вт в течение 10 с и 950 Вт в течение 10 с. Напротив, кожа была полностью разделена на эпидермальный и дермальный слои только после облучения при 200 Вт в течение 30 с. Эти результаты показывают, что облучение мощностью 200 Вт в течение 30 с является оптимальным для разделения скин-слоя.
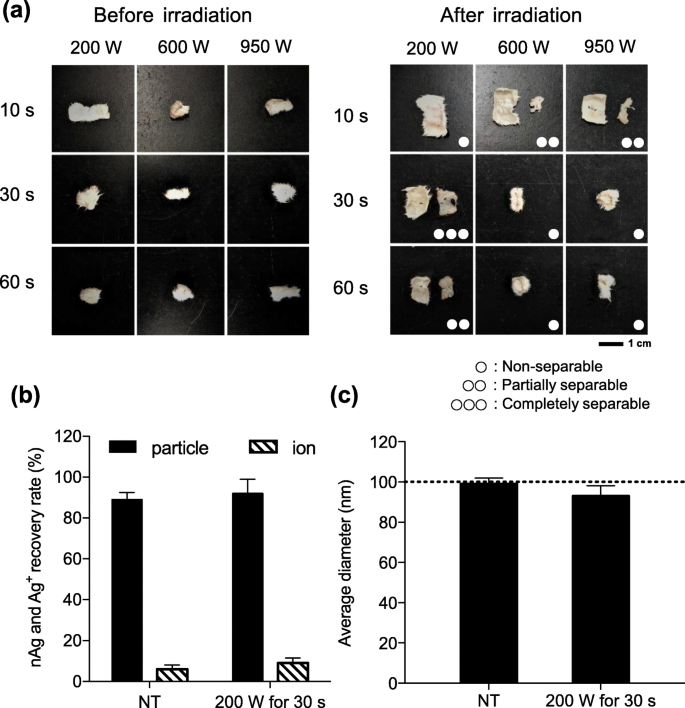
Скрининг и оценка условий разделения кожи на эпидермис и дерму с помощью микроволнового излучения. а Кожную ткань облучали микроволнами в девяти условиях и разделяли на эпидермальную и дермальную ткани. На левой и правой панелях показаны образцы кожи до и после облучения соответственно. На правой панели одиночные, двойные и тройные белые кружки показывают неразрывные, частично разделимые и полностью разделимые условия соответственно. Масштабные линейки:1 см. Гомогенаты кожи смешивали с nAg100 для получения конечной концентрации Ag 100 нг / мл, облучали при 200 Вт в течение 30 с и анализировали с помощью sp-ICP-MS. б NAg (черные полосы) и Ag + (заштрихованные столбцы) коэффициенты восстановления и c представлены средние диаметры частиц. Пунктирная линия представляет начальный размер частиц. Данные были выражены как среднее ± стандартное отклонение. ( нет =3)
Чтобы проверить, влияет ли это микроволновое облучение при 200 Вт в течение 30 с на физические свойства nAg100, мы определили физические свойства Ag в эпидермальном и дермальном слоях. Гомогенаты эпидермиса и дермы, каждый из которых был смешан с 100 нг / мл nAg100, соответственно, лизировали с использованием NaOH и облучали при 200 Вт в течение 30 с. Анализ Sp-ICP-MS показал, что большая часть nAg100, обработанного микроволновым излучением, оставалась в виде частиц, как и частицы в необработанной группе (рис. 3b). Для детального анализа физических свойств также оценивали распределения частиц по диаметру. Средняя частица имела диаметр почти 100 нм, что соответствовало исходному размеру частицы (рис. 3в). Эти результаты показывают, что микроволновое облучение образцов кожи при 200 Вт в течение 30 с является многообещающим подходом для эффективного разделения кожи на эпидермальный и дермальный слои без изменения физических свойств nAg100.
В совокупности эти результаты показывают, что мы успешно разработали систему для полуколичественного определения физических свойств nAg100 в каждом слое кожи. В частности, метод включает в себя следующее:(i) удаление не абсорбированного трансдермально nAg100 путем удаления SC с помощью метода удаления ленты [21]; (ii) разделение кожи на эпидермальный и дермальный слои с помощью микроволнового излучения; (iii) солюбилизация эпидермиса и дермы обработкой NaOH; и (iv) полуколичественное определение физических свойств Ag в каждом слое кожи с помощью sp-ICP-MS.
Практическая оценка путем определения количества и физических свойств nAg100 и Ag + в слоях кожи мыши In Vivo
Чтобы оценить практическое применение этого подхода, мы проанализировали количество и физические свойства Ag в эпидермисе и дерме, а также в периферической крови после воздействия на кожу мыши nAg100 и Ag + in vivo. Через пять дней после воздействия мы разделили кожу на эпидермис и дерму в условиях, оптимизированных для микроволнового излучения, и солюбилизировали их с помощью NaOH, как описано в предыдущем разделе. Анализ ICP-MS показал, что Ag присутствовал во всех тканях (таких как эпидермис, дерма и кровь) всех групп. В дерме и крови Ag в Ag + -экспозиции в группе имела тенденцию к увеличению по сравнению с группой, подвергнутой воздействию nAg100 (рис. 4а). Данные свидетельствуют о том, что, хотя и ионная форма, и форма частиц абсорбировались и распределялись через кожу, как сообщалось ранее [8, 9], ионным формам было легче проникнуть в глубокие слои ткани, чем формам частиц.
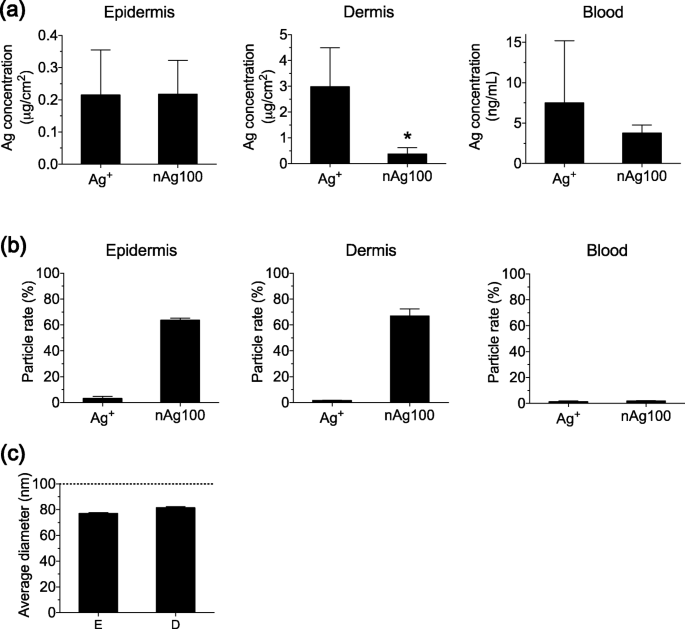
Полуколичественный анализ физических свойств nAg100 и Ag + наносится на кожу мыши in vivo. Сначала кожа мыши подвергалась воздействию nAg100 и Ag + (20 мкг Ag / см 2 ). Через пять дней после воздействия были проведены количественный анализ и оценка физических свойств Ag в эпидермисе, дерме и крови с помощью ICP-MS и sp-ICP-MS соответственно. а Концентрации Ag и b уровни частиц обнаруживаются в эпидермисе, дерме и крови. c Средний диаметр обнаруживаемых частиц в эпидермисе и дерме. Пунктирная линия представляет начальный размер частиц. Все данные были выражены как среднее ± стандартная ошибка. ( нет =3). * p <0,05 ( t студента тест)
Затем мы оценили соотношение nAg и Ag + в каждом образце. В Ag + -экспонированной группе, почти весь Ag был обнаружен в ионной форме в эпидермисе, дерме и крови, что указывает на то, что Ag + всасывается и распределяется чрескожно без изменения физических свойств. Напротив, в группе, подвергшейся воздействию nAg100, приблизительно 70% Ag в эпидермисе и дерме присутствовало в форме частиц, в то время как оставшийся Ag был ионизирован. Кроме того, Ag, обнаруженный в периферической крови, был почти полностью ионизирован, и форма частиц практически не определялась (рис. 4b). Наконец, мы оценили размер частиц в эпидермальном и дермальном слоях, где были обнаружены в основном формы частиц. Анализ sp-ICP-MS показал, что размеры частиц, обнаруженные в обоих слоях, составляли приблизительно 70–80 нм, что соответствует скорости ионизации nAg100 (рис. 4c). Эти данные предполагают, что когда кожа подвергается воздействию nAg100, он может абсорбироваться и распределяться при ионизации.
Как сообщалось ранее, поверхностные лиганды наночастиц влияют на их абсорбцию кожей [25, 26]. Например, наночастицы золота, модифицированные аминогруппой, абсорбировались кожей мыши и человека в большей степени, чем наночастицы золота, модифицированные карбоксильной группой, в экспериментах ex vivo [25]. Более того, молекулярно-динамический анализ показал, что проникающая способность наночастиц золота снижалась от нейтрально-гидрофобных до катионных и анионных наночастиц золота в этом порядке [26]. В этом отношении в этом исследовании был сделан вывод, что nAg100 с меньшей вероятностью проникает через SC в эпидермисе, начальный кожный барьер, потому что nAg100 был модифицирован цитратом и имел отрицательный заряд. Следовательно, причиной того, что частицы наблюдаются в дерме и крови, может быть то, что частицы проникают как через поры, так и через эпидермис.
Также сообщалось, что проницаемость наночастиц золота была улучшена путем модификации проникающими в клетки пептидами, такими как Tat и R7 [25]. Следовательно, в будущем могут быть рассмотрены аналогичные модификации для nAgs, чтобы доставлять их глубже в кожу. Кроме того, может потребоваться уменьшить размер nAgs, поскольку эффект модификации поверхности тем больше, чем больше удельная площадь поверхности.
Выводы
В этом исследовании мы разработали подход к предварительной обработке для полуколичественного определения физических свойств nAg100 в каждом слое кожи с помощью sp-ICP-MS. Используя этот подход, мы показали, что воздействие на кожу nAg100 может привести к ионизации, абсорбции и распределению nAg100 в более глубокие слои. Следовательно, чтобы понять биологические реакции или токсичность, связанные с воздействием на кожу nAg100, может потребоваться рассмотреть не только распределение nAg100 и размер его частиц, но и распределение Ag + из nAg100, который растворяется в тканях кожи. Таким образом, этот подход перспективен как фундаментальный метод, который можно использовать для анализа рисков.
Доступность данных и материалов
Совместное использование данных не применимо к этой статье, так как в ходе текущего исследования наборы данных не создавались и не анализировались.
Сокращения
- ENPs:
-
Разработанные наночастицы
- nAg ::
-
Серебряная наночастица
- Ag + :
-
Ионы серебра
- sp-ICP-MS:
-
Масс-спектрометрия одиночных частиц с индуктивно связанной плазмой
- SC:
-
Роговой слой
- nAg100:
-
Наночастица серебра диаметром 100 нм
- AgNO 3 :
-
Нитрат серебра
- NaOH:
-
Гидроксид натрия
- HNO 3 :
-
Азотная кислота
- PBS:
-
Физиологический раствор с фосфатным буфером
- ICP-MS:
-
Масс-спектрометрия с индуктивно связанной плазмой
- EDJ:
-
Эпидермально-дермальный переход
Наноматериалы
- Антимикробные свойства серебра
- Наночастицы для терапии рака:текущий прогресс и проблемы
- Получение и магнитные свойства легированных кобальтом наночастиц шпинели FeMn2O4
- Потенциальная токсичность наночастиц диоксида титана для печени, мозга и эмбрионов у мышей
- Формирование и люминесцентные свойства нанокомпозитов Al2O3:SiOC на основе наночастиц оксида алюминия, модифици…
- Новые биосовместимые наночастицы Au Nanostars @ PEG для КТ-визуализации in vivo и свойства очищения почек
- Получение наноструктуры Au @ TiO2 - оболочка и ее применение для разложения и обнаружения метиленового синего
- Исследование структурных, электронных и магнитных свойств кластеров Ag n V (n =1–12)
- Последние достижения в синтетических методах и применении серебряных наноструктур
- Технология психосенсорной электронной кожи для искусственного интеллекта и развития гуманоидов



