Высоконанопористое углеродное микроволокно, легированное азотом, полученное из биоресурсов, как новый вид электрокатализатора ORR
Аннотация
Синтез безметалловых электрокатализаторов на основе углерода для реакции восстановления кислорода (ORR) для замены традиционных катализаторов на основе платины в настоящее время стал горячей темой исследований. В этой работе предлагается стратегия карбонизации с помощью активации для производства легированных азотом нанопористых углеродных микроволокон (Me-CFZ-900) с высокой площадью поверхности по БЭТ (~ 929,4 м 2 г −1 ) за счет использования меламина в качестве промотора / источника азота и биологических отходов бамбукового углерода в качестве источника углерода с помощью активатора хлорида цинка. Электрохимические испытания показали, что материал Me-CFZ-900 продемонстрировал превосходную электрокаталитическую активность ORR и долгосрочную стабильность, а также продемонстрировал квазитрехэлектронный путь ORR в щелочном электролите. Мы также обнаружили, что графитовый N может быть каталитически активным центром для ORR, но образование планарного N может дополнительно способствовать повышению активности ORR для наших катализаторов. Результаты открывают новое пространство и дают новую идею получения ценных пористых наноуглеродных материалов на основе углеродсодержащих твердых отходов для катализа широкого спектра электрохимических реакций в будущем.
Фон
Современные электрохимические энергетические системы, такие как топливные элементы и металл-воздушные батареи, рассматриваются как многообещающие альтернативы традиционным ископаемым видам топлива [1, 2]. Реакция восстановления кислорода (ORR) является важной реакцией в этих энергетических технологиях, но она страдает несколькими недостатками, такими как высокий избыточный потенциал, медленная кинетика ORR и разнообразие путей, что ограничивает улучшение общих характеристик и эффективности преобразования [3, 4 ]. В настоящее время катализаторы на основе Pt широко используются для повышения ORR в практических приложениях, но высокая стоимость и ограниченные ресурсы металл-Pt препятствуют его коммерциализации [5,6,7]. Таким образом, поиск дешевых, активных и стабильных катализаторов ORR, не содержащих платины, имеет большое значение для быстрого развития экологически чистых энергетических технологий.
Чтобы найти некоторые ценные заменители катализаторов металл-Pt, легирование гетероатомов в углеродные аллотропы, такие как графен [8], графдин [9] и углеродные нанотрубки [10], широко изучается из-за их отличительных физических и электронных структур. Хотя огромное улучшение было проведено в контролируемом производстве катализаторов на основе активированного угля, происхождение каталитической активности ORR все еще неясно, что становится техническим узким местом в этой области [11, 12]. Обычно повышение активности ORR катализаторов с активированным углеродом можно объяснить модуляцией заряда и нарушенной электронейтральностью, вызванной легированием гетероатомом углеродного каркаса [13, 14]. Другие исследования также продемонстрировали, что активность ORR углеродных катализаторов обусловлена соответствующим местоположением и конфигурацией легирования [15,16,17]. Кроме того, легирование гетероатомов, таких как азот, может вызвать поляризацию поверхности углерода, что помогает формировать новые азотсодержащие активные центры, тем самым способствуя адсорбции атомов и ионов [18]. Таким образом, понимание вклада углеродных структур, богатых азотом, важно для выяснения каталитически активных центров ORR, что также может проложить путь к направленной разработке ORR-активных и стабильных катализаторов на основе легированного углерода.
Использование природной биомассы (например, сои [19], фиброина шелка [20], фасоли [21] и гемоглобина [22]) и биологических отходов животных (например, чешуи [23] и крови животных [24]) в качестве прямой предшественник или источник азота каталитически активных центров ORR считался эффективным способом изготовления катализаторов на основе легированного углерода. Совсем недавно Ли и др. также синтезировал катализатор ORR на основе легированного углерода с трехмерной пористой сеткой, используя геминовый биоматериал в качестве единственного источника и используя самоорганизующиеся кристаллы хлорида натрия в качестве шаблона [25]. Jiang et al. [26] преобразовали биологический фермент центров крови в Fe – N x каталитически активные центры электрокатализа ЧОО за счет многоступенчатого пиролиза биологических отходов крови. Полученный электрокатализатор демонстрирует превосходную каталитическую активность ORR, что указывает на то, что Fe – N x структура гема в клетках крови благоприятна для образования активных центров ORR и, следовательно, может способствовать работе катализаторов. Эти исследования могут быть стремлением к созданию нового типа высокоэффективных катализаторов на основе активированного угля путем надлежащего управления процессами пиролиза и выбора недорогих материалов биомассы в качестве прекурсоров.
В этой статье, вдохновленные дешевым и легкодоступным углеродом, легированным гетероатомом из биологических отходов для обеспечения превосходных характеристик ORR, мы разрабатываем стратегию синтеза нанопористого углеродного микроволокна, легированного азотом, в качестве нового типа электрокатализатора ORR (Me-CFZ-900) путем пиролиза потраченные впустую ткани из бамбука и углерода с активацией хлорида цинка в сочетании с использованием меламина в качестве промотора / источника азота. Насколько нам известно, до сих пор нет сообщений о создании пористых углеродных микроволокон в качестве катализатора ORR посредством легкого преобразования бамбуковых углеродных биоотходов. Мы обнаружили, что приготовленный катализатор Me-CFZ-900 имеет большое количество однородных мезопор со средним диаметром пор 2,23 нм и большой площадью поверхности (~ 929,4 м 2 г −1 ), что может быть полезно для массовой перевозки O 2 электрокаталитическое восстановление. Это исследование открывает новые возможности и предлагает новую идею для получения ценных пористых наноуглеродных материалов, которые могут функционировать как многообещающие электрокатализаторы ORR за счет дальнейшего улучшения характеристик пор и содержания активных частиц азота.
Методы
Синтез углеродных катализаторов ORR
Легированные азотом нанопористые углеродные микроволокна были приготовлены путем простого и легкого двухступенчатого пиролиза отработанных бамбуковых углеродных тканей (приобретенных у Fujian Hengan Group Co. Ltd., Китай) с помощью активации хлоридом цинка. Обычно использованные ткани измельчали в измельчителе, а затем карбонизировали при 350 ° C в течение 1 часа в трубчатой печи со скоростью нагрева 20 ° C мин -1 . в атмосфере азота для удаления некоторых остаточных органических веществ. Полученные углеродные микроволокна маркируются как CF350. Затем 0,5 г CF350, 1,0 г меламина и 1,0 г хлорида цинка были равномерно смешаны путем простого твердофазного измельчения в течение 0,5 ч в агатовой ступке для получения нового углеродистого предшественника (Me-CFZ). Предшественник Me-CFZ был дополнительно подвергнут термообработке в трубчатой печи при 900 ° C в течение 2 часов со скоростью нагрева 10 ° C мин -1 под N 2 атмосфере, в результате чего был успешно синтезирован Me-CFZ-900. Схематическая иллюстрация синтеза Me-CFZ-900 с помощью метода карбонизации с активацией показана на рис. 1. Чтобы проверить влияние температур пиролиза на производительность ORR углеродных катализаторов, мы также изготовили другие Me-CFZ. катализаторы при разных температурах, которые могут быть обозначены как Me-CFZ-700, Me-CFZ-800 и Me-CFZ-1000 соответственно. В качестве контроля аналогичным образом получали CF-900 и CFZ-900 без добавления меламина. Все образцы были дополнительно обработаны погружением в 0,5 моль л -1 Раствор HCl в течение 2 часов, прежде чем их можно будет использовать в качестве электрокатализатора ORR. Для обеспечения воспроизводимости мы подготовили все катализаторы ORR трижды, и их ошибки можно контролировать в диапазоне 5,0%.

Схематическое изображение синтеза мезопористых углеродных микроволокон, легированных азотом, для электрокатализа ORR посредством карбонизации с помощью активации бамбуковых углеродных биоотходов
Физическая характеристика
Сканирующая электронная микроскопия высокого разрешения (SEM) и просвечивающая электронная микроскопия (TEM) были проведены на приборах Hitachi UHR S4800 (Япония) и FEI Tecnai-G2 F30 с ускоряющим напряжением 300 кВ соответственно. Рентгеновскую фотоэлектронную спектроскопию (XPS) проводили на спектрометре Kratos XSAM800. Анализатор Micromeritics (ASAP 2010) был применен к тесту N 2 Изотермы адсорбции / десорбции при 77 К. Рентгеноструктурный анализ (XRD) проводили с использованием рентгеновского дифрактометра Shimadzu XRD-6000 (Япония) с Cu Ka 1 излучение ( λ =1,54178 Ǻ) при 4 ° мин
- 1
. Данные рамановской спектроскопии были записаны с помощью рамановской системы Horiba HR800 с длиной волны лазерного возбуждения 514,5 нм. XR-рентген был выполнен с использованием Shimadzu XRD-6000 ( λ =Рентгеновский дифрактометр (Япония) с Cu Ka 1 радиация  ).
).
Электрохимические измерения
Электрокаталитическое поведение катализатора ORR на основе углерода оценивали на бипотенциостате CHI760E (Shanghai Chenhua Instruments Co. Ltd., Китай). Стеклоуглеродный вращающийся кольцевой дисковый электрод (GC-RRDE, Φ =5 мм, Pine Instrument Co.), насыщенный каломельный электрод (SCE) и графитовый стержень ( Φ =0,5 см) использовались в качестве рабочего электрода (WE), электрода сравнения (RE) и вспомогательного электрода (AE) соответственно. Изготовление WE относится к нашим предыдущим отчетам [12]. Обычно 10 мкл 10 мг / мл -1 Дисперсию наносили пипеткой на поверхность GC-RRDE и сушили естественным образом на воздухе. Массовая загрузка катализаторов на основе углерода и коммерческого катализатора Pt / C (20 мас.% Pt, Aladdin Industrial Co. Ltd.) контролировалась на уровне ~ 600 мкг см -2 . . Все потенциалы (относительно SCE) были преобразованы в потенциалы относительно обратимого водородного электрода (RHE). Кроме того, спектры электрохимического импеданса (EIS) были получены в присутствии 1 ммоль / л -1 К 3 [Fe (CN) 6 ] / K 4 [Fe (CN) 6 ] (мольное соотношение =1:1) смесь в качестве окислительно-восстановительного зонда в 0,1 М растворе KCl. Чтобы в достаточной степени вызвать полное разложение пероксида, образовавшееся во время испытания, потенциал кольца был установлен на уровне 0,5 В (относительно SCE), как описано в другом месте. % HO 2 - выход и число переноса электрона ( n ) во время ORR были рассчитаны с использованием следующих уравнений [25]:
$$ \% {HO} _2 ^ {-} =100 \ times \ frac {2 {I} _ {\ mathrm {r}} / N} {I _ {\ mathrm {d}} + \ left ({I} _ {\ mathrm {r}} / N \ right)} $$ (1) $$ n =4 \ times \ frac {I _ {\ mathrm {d}}} {I _ {\ mathrm {d}} + {I } _ {\ mathrm {r}} / N} $$ (2)где I d фарадеев ток на диске, I r - фарадеев ток на кольце, а N - эффективность улавливания кольцевого электрода (0,38). нет рассчитывалась по уравнению Коутецкого-Левича [27]:
$$ 1 / {j} _d =1 / {j} _k + 1 / B {\ omega} ^ {1/2} $$ (3) $$ B =0,62 {nFC} _ {\ mathrm {O}} {D} _ {\ mathrm {O}} ^ {2/3} {\ nu} ^ {- 1/6} {\ omega} ^ {1/2} $$ (4)где F постоянная Фарадея, C O это O 2 концентрация насыщения в электролите, D O это O 2 коэффициент диффузии в электролите, ν - кинетическая вязкость электролита, а ω - скорость вращения электрода, 0,62 - постоянная величина, если скорость вращения выражена в об / мин.
Результаты и обсуждение
На рис. 2 показаны изображения катализатора Me-CFZ-900, полученные с помощью СЭМ и ПЭМ. Как видно на этих изображениях SEM, катализатор Me-CFZ-900 состоит из нерегулярных углеродных микроволокон, легированных азотом (рис. 2a, b). Кроме того, ПЭМ-изображения Me-CFZ-900 (рис. 2c, d) дополнительно подтверждают результаты анализа SEM. Образование мезопор внутри катализатора Me-CFZ-900 объясняется ролью активации хлорида цинка во время высокотемпературного пиролиза, который вызывает быстрое обезвоживание и каталитическое дегидроксилирование, что приводит к высвобождению водорода и кислорода в форме H 2 О пар. Этот процесс активации может способствовать образованию большего количества мезопор во время процесса легирования азотом внутри катализатора Me-CFZ-900. Кроме того, некоторые открытые краевые дефекты также могут наблюдаться благодаря легированию азотом, которое способствует каталитической активности ORR.

SEM ( a , b ) и ТЕА ( c , d ) изображения Me-CFZ-900
Изотермы адсорбции / десорбции азота использовались для изучения удельной поверхности Брунауэра-Эмметта-Теллера (БЭТ) и характеристик распределения пор, как показано на рис. 3а и в дополнительном файле 1:рис. S1. Установлено, что большая площадь поверхности по БЭТ (~ 929,4 м 2 г −1 ) Me-CFZ-900 можно объяснить его шероховатой, богатой дефектами поверхностью и мезопористыми характеристиками, что хорошо согласуется с результатами ПЭМ-измерений. Распределение пор BJH по размерам катализатора Me-CFZ-900 показано на вставке на фиг. 3a. Общий объем пор Me-CFZ-900 со средним диаметром пор 2,3 нм составляет ~ 0,53 см 3 . г −1 , но мезопоры в основном сосредоточены на диаметре пор 3,88 нм. Эти превосходные характеристики могут быть тесно связаны с повышением активности ORR. Углеродные структуры различных катализаторов ORR на основе углерода были исследованы с помощью дифрактограмм на рис. 3b. Никаких кристаллических пиков не наблюдается, за исключением двух углеродных плоскостей ((002) и (101)), расположенных под углом ~ 24 ° и ~ 43 ° соответственно, что свидетельствует об аморфной углеродной структуре [19, 20]. Сильный дифракционный пик (002) можно в основном отнести к плоскостям решетки типичного турбостратного углерода [28]. Однако более высокий 2-тета пика (002) и более низкий 2-тета пика (101) для Me-CFZ-900 по сравнению с таковыми для CF-900 и CFZ-900 могут быть получены из-за небольшого искажения кристаллической регулярность вдоль а или b направление легированием атомов азота в sp 2 углеродная решетка. Кроме того, все спектры комбинационного рассеяния CF-900, CFZ-900 и Me-CFZ-900 (рис. 3c) показали две полосы на плате, расположенные на ~ 1345 и ~ 1590 см −1 , которые приписываются неупорядоченным sp 3 углерод (полоса D) и графит sp 2 углерода (полоса G) соответственно. Соотношение интенсивностей ( I D / Я G ) полосы «D» на полосу «G» использовали для характеристики степени неупорядоченности и графита. Соответствующий I D / Я G для CF-900, CFZ-900 и Me-CFZ-900 составляют примерно 0,91, 0,91 и 0,92 соответственно. Высшее Я D / Я G Соотношение Me-CFZ-900 представляет более высокую эффективность легирования азотом и более дефектную структуру, способствуя увеличению плотности активного центра и усилению электрокаталитической активности ORR. В предыдущем отчете также предполагалось, что электропроводность катализаторов на основе легированного углерода может быть улучшена за счет добавления большего количества атомов азота [25]. По этой причине мы дополнительно проверили электропроводность (ЕС) всех катализаторов на основе легированного угля с помощью спектроскопии электрохимического импеданса (EIS) в 1 ммоль л -1 К 3 [Fe (CN) 6 ] / K 4 [Fe (CN) 6 ] (мольное соотношение =1:1) раствор зонда, как показано на рис. 3d. Результаты Боде доказывают, что Me-CFZ-900 предлагает гораздо более низкое сопротивление для массового транспорта, предполагая лучшую общую проводимость по сравнению с CF-900 и CFZ-900. Кроме того, более высокая электропроводность Me-CFZ-900 может способствовать повышению способности переносить электроны, что приводит к его лучшей активности ORR в щелочной среде.
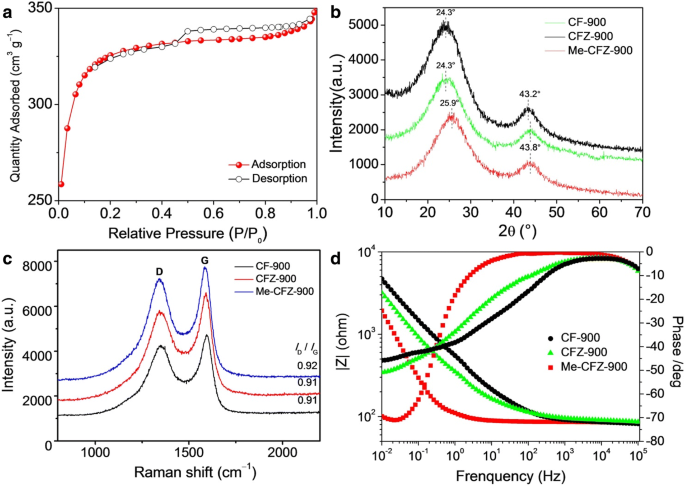
а N 2 -изотермы поглощения Me-CFZ-900. б Рентгенограммы CF-900, CFZ-900 и Me-CFZ-900. c Рамановские спектры CF-900, CFZ-900 и Me-CFZ-900. г Спектры Боде CF-900, CFZ-900 и Me-CFZ-900 под синусоидальной волной амплитудой 5,0 мВ в диапазоне частот от 100 кГц до 10 МГц
Данные обзора XPS (см. Дополнительный файл 1:Рисунок S2) показывают, что Me-CFZ-900 в основном состоит из азота, углерода и кислорода соответственно. Появление пика XPS N1s свидетельствует об успешном введении азота в углеродную структуру, что убедительно подтверждается анализом пика C1s Me-CFZ-900. Однако пик N1s CF-900 и CFZ-900 невозможно наблюдать из-за низкого содержания азота внутри бамбуковых углеродных биоотходов, как показано в Дополнительном файле 1:Рисунок S1 и Таблица S1. Кроме того, общее содержание N в трех катализаторах с добавками N определяли с помощью анализа поверхности XPS. Общее содержание N в Me-CFZ-900 составляет 2,71 ат.%, Но общее содержание N составляет только 0,91 ат.% Для CF-900 и 0,94 ат.% Для CFZ-900, соответственно. Мы дополнительно проверили XPS-спектры N1s высокого разрешения для CF-900, CFZ-900 и Me-CFZ-900, как показано на рис. 4 (a – c). Спектры XPS N1s CF-900 и CFZ-900 могут быть деконволютированы в один пик с энергией связи (BE) ~ 401,5 эВ, что соответствует типу графита-N. Однако XPS-спектр N1s высокого разрешения Me-CFZ-900 указывает на существование четырех типов азотных групп:пиридиновый-N при 398,3 эВ, пирроловый-N при 398,8 эВ, графитовый-N при 401,2 эВ и окисленный-N при 403,4 эВ [29,30,31]. Образование пиридинового N и пирролинового N происходит в результате термического разложения меламина во время процесса активации-карбонизации при высоких температурах. Кроме того, C1s-спектры высокого разрешения (рис. 4d и дополнительный файл 1:рис. S3) CF-900, CFZ-900 и Me-CFZ-900 можно деконволютировать на четыре пика при 284,5, 285,9, 287,0 и 293,0 эВ, которые отнесены к графитовой sp 2 углерод (C =C), аморфный углерод (C – C), sp 2 атомы углерода, связанные с азотом (C – N), и sp 2 атомы углерода, связанные с кислородом (C – O) [32], отдельно. Доля структуры C – N увеличивается с 7,8 ат.% Для CF-900 до 12,2 ат.%. % в Me-CFZ-900, что еще раз доказывает, что большее количество атомов азота было успешно включено в углеродный каркас Me-CFZ-900. Кроме того, эти результаты показывают, что добавление меламина в качестве промотора и источника азота во время пиролиза при 900 ° C может повлиять на содержание общего и легированного N, а затем способствовать образованию более активных центров внутри Me-CFZ-900, облегчая для повышения каталитической активности ORR во время электрохимических испытаний.
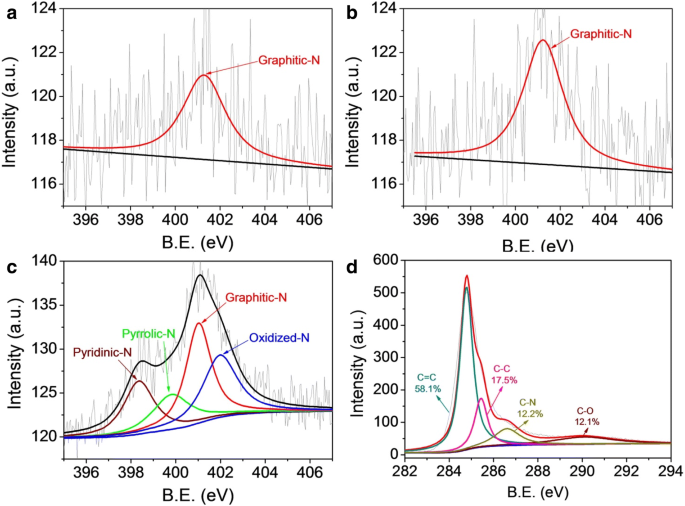
XPS-спектры высокого разрешения N1s CF-900 ( a ), CFZ-900 ( б ) и Me-CFZ-900 ( c ). (d ) XPS-спектры высокого разрешения C1s Me-CFZ-900 ( d )
Чтобы оценить электрокаталитическую активность ORR, три катализатора ORR на основе углерода были соответственно нанесены на поверхность GC-RRDE и дополнительно протестированы с помощью циклической вольтамперометрии (CV) и линейной вольтамперометрии (LSV) в O 2 -насыщенный 0,1 моль л -1 Раствор КОН. Электрохимические результаты по активности ORR показаны на рис. 5а. Можно обнаружить, что все CV-кривые CF-900, CFZ-900 и Me-CFZ-900 в O 2 -насыщенный электролит показывает четкие пики ORR с пиковыми потенциалами 0,69, 0,84 и 0,91 В относительно RHE, соответственно. Установлено, что активность ORR для трех углеродных катализаторов соответствует порядку Me-CFZ-900> CFZ-900> CF-900. Кроме того, кривые LSV (рис. 5b), записанные в O 2 -насыщенный раствор КОН получали при скорости вращения 1600 об / мин для дальнейшего понимания каталитической активности CF-900, CFZ-900 и Me-CFZ-900. Электрод с катализатором CFZ-900 демонстрирует лучшую активность ORR с полуволновым потенциалом ( E 1/2 ) 0,78 В по сравнению с электродом с катализатором CF-900 с E 1/2 0,65 В по сравнению с RHE. Кроме того, более высокое значение E 1/2 ~ 0,86 В и более ограниченная плотность тока при заданных потенциалах может быть получена на электроде, катализируемом Me-CFZ-900, что сопоставимо с таковыми для коммерческого катализатора Pt / C (20 мас.%) (см. Дополнительный файл 1:Рисунок S4) и другие углеродные катализаторы, о которых сообщается в литературе (см. Дополнительный файл 1:Таблица S2). Эти результаты хорошо согласуются с результатами измерений CV, дополнительно демонстрируя превосходную активность ORR Me-CFZ-900. Предполагается, что активация хлоридом цинка и добавление источника азота могут улучшить каталитическую активность ORR за счет образования мезопористых структур и повышения эффективности легирования азотом в процессе пиролиза.
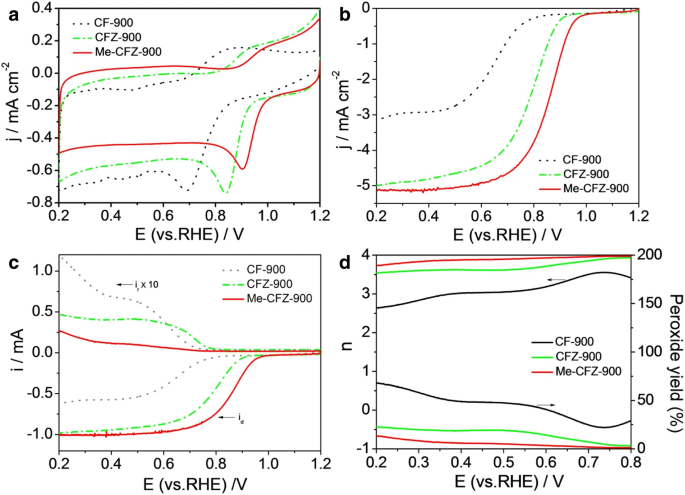
а Кривые CV CF-900, CFZ-900 и Me-CFZ-900 в O 2 -насыщенный 0,1 моль л -1 Раствор КОН. б Кривые LSV для ORR CF-900, CFZ-900 и Me-CFZ-900 и 20 мас.% Pt / C в O 2 -насыщенный 0,1 М раствор КОН при скорости вращения 1600 об / мин. c Дисковые и кольцевые токи, полученные с LSV на RRDE для CF-900, CFZ-900 и Me-CFZ-900 в O 2 -насыщенный 0,1 моль л -1 Раствор КОН. г Соответствующее число электронного переноса и H 2 О 2 доход от c
Измерения RRDE были проведены, чтобы получить представление о кинетике ORR углеродных катализаторов, как показано на рис. 5c. Кроме того, на основании данных RRDE передан соответствующий номер электрона ( n ) и пероксидные соединения (H 2 О 2 %), произведенные во время ORR, рассчитываются с использованием формул. (1) и (2) соответственно. Результаты расчета представлены на рис. 5г. H 2 О 2 выход (<14,0%) и число переноса электрона (3,45–3,95) на Me-CFZ-900 могут быть найдены в диапазоне потенциалов 0,2–0,8 В по отношению к RHE, что указывает на то, что квазитрехэлектронный путь для процесса ORR аналогичен к кинетике ORR коммерческого катализатора Pt / C (дополнительный файл 1:рисунок S3). По сравнению с Me-CFZ-900, более высокий H 2 О 2 Выход и меньшее число переноса электрона можно наблюдать как на CF-900, так и на CFZ-900 в одном и том же диапазоне потенциалов. Однако H 2 О 2 выход на CFZ-900 выше, чем на Me-CFZ-900, но число переноса электронов на CFZ-900 аналогично таковому на Me-CFZ-900, что также предполагает квазитрехэлектронный путь для процесса ORR. К сожалению, CF-900 показал самое низкое число переноса электрона (2,64–3,56) и самое высокое H 2 . О 2 выход (22,2–68,2%), подразумевая, что ORR, катализируемый CF-900, в основном следует смешанным путем, состоящим из двух- и четырехэлектронных процессов. Эти результаты доказывают, что углеродные катализаторы, полученные активацией хлоридом цинка, показали более высокую каталитическую эффективность ORR и электрокаталитические характеристики с добавлением меламина или без него. В сочетании с XPS-анализом и данными активности ORR мы обнаружили, что только разновидности графитового N могут существовать в CF-900 и CFZ-900, но проявляют каталитическую активность ORR, что доказывает, что графитовый N может быть одним из электрокаталитически активных центров, способствующих образованию Электрокатализ ORR. Примечательно, что добавление меламина в предшественник может способствовать образованию соединений пиридинового N и пирролового N с планарной структурой, которые могут быть ответственны за усиление активности ORR, что подтверждается ранее опубликованными результатами [29]. Кроме того, отличные показатели ORR Me-CFZ-900 можно также отнести к другим аспектам:(1) высокая площадь поверхности по БЭТ и мезопористая структура Me-CFZ-900 могут способствовать адсорбции и транспортировке молекулы кислорода и воздействию большего количества активные сайты; (2) более высокая электропроводность Me-CFZ-900 может эффективно повысить перенос электронов в процессе ORR; и (3) больше атомов N включается в углеродную структуру Me-CFZ-900, что может привести к образованию более богатых азотом дефектных структур и активных центров. Следовательно, контролируемый синтез с высоким содержанием плоских и графитных форм азота необходим для производства катализаторов на основе активного углерода для ORR, но дальнейшее улучшение электропроводности, эффективности легирования азотом и мезопористых характеристик является ключевым вопросом для улучшения каталитического восстановления ORR. активность.
Чтобы лучше понять влияние температур пиролиза на активность ORR, мы также приготовили еще три катализатора, такие как Me-CFZ-700, Me-CFZ-800 и Me-CFZ-1000, с помощью той же процедуры пиролиза. На фиг. 6а все приготовленные катализаторы показали очевидный пик ORR, но Me-CFZ-900 имеет наибольший пиковый ток и наиболее положительный пиковый потенциал. Кривые LSV, записанные при скорости вращения 1600 об / мин, дополнительно предполагают, что Me-CFZ-900 продемонстрировал более положительные потенциалы начала и полуволны для ORR по сравнению с другими катализаторами (фиг. 6b). Очевидно, что каталитическая активность полученных катализаторов ORR сильно зависит от температуры пиролиза. Оптимальная температура для нашей системы составляет 900 ° C, так как более высокая или более низкая по-прежнему будет давать низкую электрокаталитическую активность ORR. Это может быть связано с плотностью активных центров и характеристиками пористости внутри катализаторов, которые регулируются температурой пиролиза. Чтобы лучше понять поведение кинетики ORR различных углеродных катализаторов, мы также проводим тесты RRDE для мониторинга H 2 О 2 выход и число переноса электрона (рис. 6в, г). Видно, что кольцевой ток ( i r ) Me-CFZ-900, очевидно, ниже, чем у других катализаторов в диапазоне потенциалов 0,2–0,8 В, что приводит к наибольшему числу переноса электрона и наименьшему H 2 О 2 доходность Me-CFZ-900 по данным RRDE. Эти результаты дополнительно подтверждают, что наилучшая активность ORR приготовленных катализаторов может быть получена при 900 ° C.
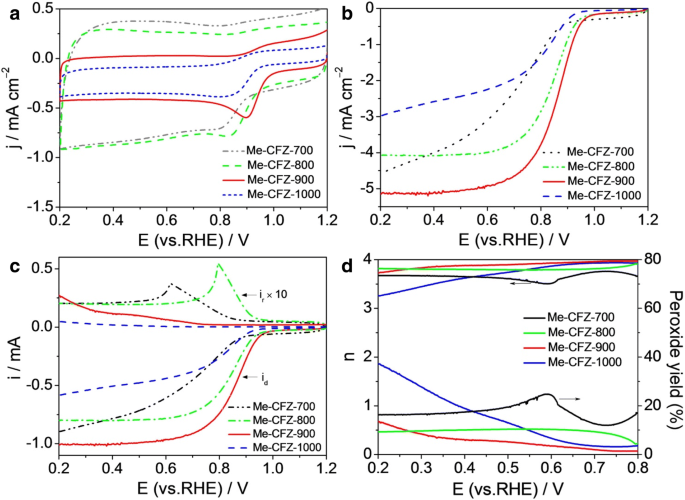
а CV и b Кривые LSV для Me-CFZ-700, Me-CFZ-800, Me-CFZ-900 и Me-CFZ-1000 в O 2 -насыщенный 0,1 моль л -1 Раствор КОН. c Дисковые и кольцевые токи, полученные с LSV на RRDE для Me-CFZ-700, Me-CFZ-800, Me-CFZ-900 и Me-CFZ-1000 в O 2 -насыщенный 0,1 моль л -1 Раствор КОН. г Соответствующее число электронного переноса и H 2 О 2 доход от c
Поведение Me-CFZ-900 в катализе ORR дополнительно оценивали по кривым CV и кривым LSV в N 2 против O 2 -насыщенный 0,1 моль л -1 Растворы КОН (рис.7). В N 2 -насыщенный электролит, за исключением четкого емкостного CV, на рис. 7а не наблюдается видимого пика, что указывает на его отсутствие характерных черт. Напротив, когда тест CV выполняется за O 2 -насыщенный электролит, получается хорошо выраженный пик ORR при ~ 0,90 В. Приведенные выше результаты качественно предполагают электрокаталитическую активность ORR Me-CFZ-900 с потенциалом начала ORR ~ 1,0 В, приближающимся к коммерческому катализатору Pt / C (дополнительный файл 1:Рисунок S4). Кроме того, чтобы лучше выявить процесс ORR Me-CFZ-900, измерения RDE были выполнены при скорости сканирования 5 мВ с -1 с разными скоростями вращения (400–2500 об / мин), как показано на рис. 7b. Предельная плотность диффузионного тока увеличивается с увеличением скорости вращения, демонстрируя, что ток регулируется кинетически. Сюжеты Коутецкого-Левича ( j -1 по сравнению с ω −1/2 ), полученные при 0,2–0,6 В, показывают хорошую линейность и близкую параллельность (или перекрытие) (рис. 7a), что указывает на аналогичные числа переноса электрона для ORR при пяти потенциалах (0,2–0,6 В). Среднее число переноса электрона рассчитано равным ~ 3,84 из наклона графиков Коутецкого-Левича с использованием формул. (3) и (4), дополнительно подтверждая, что ORR на Me-CFZ-900 следует по пути реакции с четырьмя электронами, подобно катализатору Pt / C [33]. Этот результат хорошо согласуется с результатами тестирования RRDE. Кроме того, стабильность электрокатализа ORR является одной из основных проблем в современной технологии щелочных топливных элементов. Для этого была измерена долговременная стабильность Me-CFZ-900 с помощью испытания на ускоренное старение (AAT) в O 2 -насыщенный 0,1 М раствор КОН. Перед повторными испытаниями LSV для катализа ORR катализатор Me-CFZ-900 подвергается непрерывным измерениям CV от 0,2 до 1,2 В относительно RHE в течение 5000 циклов при скорости сканирования 200 мВ с -1 . Как показано на рис. 7d, LSV-кривые Me-CFZ-900 демонстрируют только отрицательный сдвиг полуволнового потенциала на ~ 21 мВ и снижение ограниченной плотности диффузионного тока примерно на 2,0%, но заметного снижения потенциала начала ORR не наблюдается. . Наши предыдущие отчеты показывают, что коммерческий катализатор Pt / C обычно показывает отрицательный сдвиг на ~ 50 мВ в потенциале полуволны ORR после испытания CV в течение 5000 циклов. Эти электрохимические результаты предполагают многообещающую долгосрочную стабильность Me-CFZ-900, который, очевидно, превосходит коммерческий катализатор Pt / C (дополнительный файл 1:Рисунок S5). Таким образом, мы можем обнаружить, что катализатор Me-CFZ-900, приготовленный в этой работе, является весьма многообещающим кандидатом в качестве катализаторов ORR на основе Pt в щелочной среде.
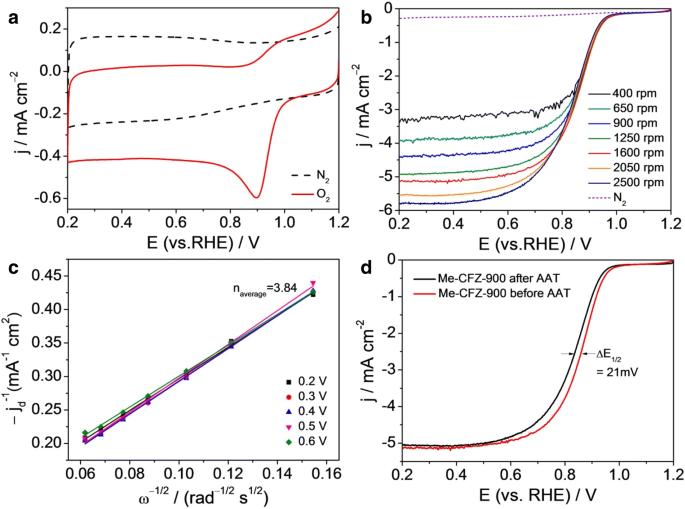
а ЦВА-кривые Me-CFZ-900 в 0,1 моль л -1 Раствор КОН, насыщенный N 2 против O 2 . б Кривые LSV Me-CFZ-900 в O 2 -насыщенный 0,1 моль л -1 Раствор КОН при разных скоростях вращения (400–3600 об / мин). c Графики Коутецкого-Левича j d -1 по сравнению с ω −1/2 получено из b при заданных потенциалах. г Кривые LSV Me-CFZ-900 в O 2 -насыщенный 0,1 моль л -1 Электролиты КОН до и после теста ААТ
Выводы
In summary, we develop a new method to prepare nanoporous N-doped carbon microfibers (Me-CFZ-900) derived from bamboo-carbon biowastes for the electrocatalysis of oxygen reduction reaction in alkaline media. The as-prepared Me-CFZ-900 catalyst exhibits the ORR electrocatalytic activity with a half-wave potential of ~ 0.86 V and a peak potential of ~ 0.91 V. The peroxide yield less than 14% and the average electron transfer number of 3.84 are obtained on Me-CFZ-900, further showing a quasi-four-electron reaction pathway. An only 21 mV negative shift in half-wave potential and 2.0% decline in the limited current density are observed on Me-CFZ-900 after doing the accelerated aging test. Furthermore, high BET surface area (929.4 m 2 г −1 ) and mesoporous structure of Me-CFZ-900 can facilitate the adsorption and transportation of oxygen molecule. This work can help the researchers to build the high-performance carbon-based ORR electrocatalyst derived from biomass wastes and to understand the origin of the ORR electrocatalytic activity.
Сокращения
- AAT:
-
Accelerated aging test
- AE:
-
Auxiliary electrode
- BET:
-
Brunauer-Emmett-Teller
- CF:
-
Carbon microfibers
- CV:
-
Cyclic voltammetry
- E 1/2 :
-
Half-wave potential
- E ORR :
-
Onset potential
- E p :
-
Peak potential
- FE-SEM:
-
Field-emission scanning electron microscopy
- GC:
-
Glassy carbon
- HR-TEM:
-
Просвечивающая электронная микроскопия высокого разрешения
- LSV:
-
Linear sweep voltammetry
- Me-CFZ-900:
-
Nitrogen-doped porous carbon microfibers
- ORR:
-
Oxygen reduction reaction
- Pt/C:
-
Platinum/carbon catalyst
- RDE:
-
Rotation disk electrode
- RE:
-
Reference electrode
- RHE:
-
Reversible hydrogen electrode
- RRDE:
-
Rotation ring-disk electrode
- SCE:
-
Saturated calomel electrode
- WE:
-
Working electrode
- XPS:
-
Рентгеновская фотоэлектронная спектроскопия
Наноматериалы
- Новая брошюра по кормлению и дозированию от Gericke
- Новые достижения в FDM от Stratasys
- Новая книга Домина Кардона
- Волокна из активированного угля с иерархической наноструктурой, полученные из отработанных хлопчатобумажны…
- Магнитные углеродные микросферы как многоразовый адсорбент для удаления сульфонамида из воды
- Простой подход к синтезу флуоресцентных квантовых точек углерода из сточных вод тофу
- Самолегированный высокопористый углерод графитового азота для электрокатализа реакции восстановления кисл…
- Синтез и характеристики суперконденсатора упорядоченных мезопористых углеродных композитов, легированных …
- Высокоактивные и стабильные электрокатализаторы восстановления кислорода Fe-N-C, полученные в результате элек…
- Простой синтез легированных азотом микропористых углеродных сфер для высокоэффективных симметричных супер…



