Изготовление полых микросфер TiO2, промотированных CdTe / BiOI, с превосходными фотокаталитическими характеристиками под искусственным солнечным светом
Аннотация
Полые и гетероструктурные архитектуры признаны эффективным подходом к улучшению фотокаталитических характеристик. В этой работе тройной TiO 2 / CdTe / BiOI с полой структурой был построен пошаговым методом. Кроме того, эффект TiO 2 структурное регулирование и выравнивание энергетических зон квантовых точек BiOI и CdTe (КТ CdTe) с TiO 2 в TiO 2 / CdTe / BiOI по фотокаталитическому удалению красителей. Результаты показывают, что TiO 2 Гетероструктуры / CdTe / BiOI с полыми подложками проявляют гораздо более высокую фотокаталитическую активность, чем чистый TiO 2 , P25, TiO 2 / CdTe и TiO 2 / BiOI и тройной TiO 2 / CdTe / BiOI с твердыми подложками. Для TiO 2 (H) / CdTe / BiOI, несколько синергетических факторов могут быть ответственны за замечательные характеристики фотодеградации в видимом свете, такие как сильное поглощение видимого света BiOI и большая удельная площадь поверхности.
Фон
Благодаря своим достоинствам в области энергосбережения и безвредности для окружающей среды фотокатализ полупроводников привлекает все больший интерес к охране окружающей среды. Фотокатализаторы могут использоваться в различных аспектах, таких как самоочищение, очистка воды, очистка воздуха и антибактериальная обработка [1, 2]. Среди них, благодаря преимуществам низкой стоимости, превосходной стабильности и нетоксичности [3], диоксид титана (TiO 2 ) был тщательно исследован. Однако он может использовать только небольшую часть солнечного спектра из-за его широкой запрещенной зоны и относительно быстрой рекомбинации зарядов, что ограничивает эффективность фотопреобразования [4].
Чтобы улучшить фотокаталитическую эффективность диоксида титана в видимом свете, были приняты различные стратегии, включая ионное легирование, загрузку благородных металлов, конструирование гетеропереходов и сенсибилизацию [5,6,7,8]. Среди этих стратегий гетеропереход, образованный за счет взаимодействия с полупроводником с узкой запрещенной зоной, считается одним из наиболее эффективных методов одновременного улучшения отклика в видимом свете и уменьшения рекомбинации зарядов [9].
Оксигалогениды висмута привлекли значительное внимание из-за низкой стоимости, хорошей стабильности и широкого диапазона светового отклика [10, 11], которые имеют изотропно-слоистую структуру с [Bi 2 О 2 ] 2+ слои, интеркалированные X - ионы (X =F, Cl, Br, I) [12]. Среди оксигалогенидов висмута BiOI с наименьшей шириной запрещенной зоны (1,72–1,9 эВ) [13] оказался эффективным фотокатализатором в видимом свете для разложения RhB [14] и MO [15]. Внутреннее электрическое поле между [Bi 2 О 2 ] 2+ и я - слои могут способствовать разделению фотоиндуцированных зарядов и повышать фотокаталитическую активность [16]. Хотя потенциалы зоны проводимости и валентной зоны лежат между потенциалами TiO 2 гетеропереход II типа может быть сформирован путем связывания BiOI p-типа и TiO n-типа 2 вместе, когда уровни Ферми достигают равновесия, что заставляет электроны зоны проводимости BiOI мигрировать в TiO 2 [17]. До сих пор, хотя много усилий было направлено на разработку бинарных гетероструктурных фотокатализаторов, ограниченный отклик на видимый свет и относительно низкая эффективность разделения зарядов все еще остаются камнем преткновения.
Для решения указанных выше проблем были разработаны многокомпонентные гетеропереходные системы. Теллурид кадмия (CdTe), как важный полупроводник p-типа II-VI, привлек большое внимание из-за его прямой запрещенной зоны 1,44 эВ [18] и большого коэффициента оптического поглощения в солнечном спектре [19]. Квантовые точки CdTe (КТ CdTe) широко используются для модификации различных полупроводников:Feng et al. [20] синтезировали TiO 2 , декорированный CdTe. массивы нанотрубок с помощью метода импульсного электроосаждения, и результаты показали CdTe / TiO 2 массивы нанотрубок (CdTe / TiO 2 NTA) продемонстрировали выдающиеся фотокаталитические свойства, чем чистый TiO 2 НТА; Лю и др. [21] сообщили о синтезе нанокомпозитов CdTe / ZnO методом горячей ванны, и результаты показали, что CdTe / ZnO обладает лучшей фотокаталитической активностью для родамина B, чем чистый ZnO. Однако, помимо бинарных гетероструктурных фотокатализаторов, тройной гетероструктурированный TiO 2 / BiOI, модифицированный квантовыми точками CdTe, может обладать удивительными фотокаталитическими характеристиками и заслуживает дальнейшего изучения.
В настоящей работе КТ CdTe / BiOI-модифицированный TiO 2 был подготовлен для фотокаталитического применения двухэтапным методом, а твердый и полый TiO 2 микросферы применялись в качестве прекурсоров. Кроме того, структурная эволюция TiO 2 Композиты / CdTe / BiOI и синергетический эффект CdTe и BiOI в фотокаталитическом процессе также были подробно изучены.
Методы
Материалы
Изопропоксид титана (TTIP, 97%) и пентагидрат нитрата висмута (AR, 99,0%) были приобретены у Macklin Inc. Полупентагидрат хлорида кадмия (CdCl 2 · 2,5 ч 2 O 99,0%), теллурит натрия (Na 2 ТеО 3 , 98,0%), N -ацетил- L -цистеин (98,0%), борогидрид калия (KBH 4 , 97%), гидроксид натрия (NaOH, 96,0%), нитрат калия (KNO 3 , 99%), бромид калия (KBr, 99%), соляная кислота (HCl, 36–38%), пероксид водорода (H 2 О 2 30%), этиленгликоль и абсолютный этанол были аналитической чистоты и приобретены у Sinopharm Chemical Reagent Co., Ltd.
Синтез TiO 2 Твердые микросферы и полые микросферы
В типичной процедуре 0,8 мл KNO 3 раствор (0,1 моль / л) растворяли в 200 мл этанола. Затем к вышеуказанному раствору добавляли 4,4 мл TTIP и перемешивали до образования белого осадка. Выдержав 12 ч, полученную белую суспензию центрифугировали и несколько раз промывали деионизированной водой и этанолом, а аморфный TiO 2 (TiO 2 · NH 2 O) можно было получить. После дополнительной сушки при 60 ° C в течение 12 часов и прокаливания при 450 ° C в течение 2 часов TiO 2 твердые микросферы (TiO 2 (S)) можно было получить.
Что касается TiO 2 полые микросферы, они были изготовлены с помощью гидротермального процесса. Обычно TiO 2 · NH 2 O (200 мг) диспергировали в 40 мл 0,05 мас.% H 2 О 2 и перемешивали 10 мин. Затем 480 мг порошка NaOH растворяли в указанной выше суспензии, смесь переносили в автоклав с тефлоновым покрытием и выдерживали при 180 ° C в течение 4 часов. Осадки собирали и затем погружали в хлористоводородную кислоту (0,1 моль / л). После многократной промывки деионизированной водой полученные продукты сушили и прокаливали, как и в предыдущей процедуре, и, таким образом, TiO 2 полые микросферы, обозначенные как TiO 2 (H), были получены.
Синтез TiO 2 Сферы, модифицированные с помощью квантовых точек CdTe
TiO 2 порошки (2,0 г) диспергировали в 40 мл деионизированной воды, а затем 97,9 мг N -ацетил- L -цистеин, 114,2 мг CdCl 2 · 2,5 ч 2 O и 178 мг KBH 4 затем добавляли в смесь с 30-минутными интервалами. После этого 10 мл Na 2 ТеО 3 (0,01 моль / л) водный раствор добавляли к указанной выше смеси со скоростью 5 мл / мин. Затем температуру системы повышали до 100 ° C за 30 мин и кипятили с обратным холодильником в течение 6 ч. Наконец, продукты были промыты водой и этиловым спиртом несколько раз и высушены при 60 ° C в течение 12 часов, и продукты были помечены как TiO 2 / CdTe .
Изготовление TiO 2 / CdTe / BiOI Тройные композиты
Вкратце, TiO 2 Порошки / CdTe (258 мг), полученные выше, диспергировали в 10 мл EG, образуя белую суспензию. После этого Би (NO 3 ) 3 раствор, приготовленный растворением 627,6 мг Bi (NO 3 ) 3 в 28 мл ЭГ закапывали в указанную выше суспензию за 15 мин. Затем в предыдущую смесь по каплям добавляли раствор, содержащий 214,8 мг KI и 24 мл EG. После перемешивания в течение 1 часа желтый раствор переносили в автоклав с тефлоновым покрытием и выдерживали при 80 ° C в течение 3 часов. Полученные в результате осадки собирали, достаточно промывали этанолом и деионизированной водой и сушили, которые были обозначены как TiO 2 . / CdTe / BiOI.
Двоичный TiO 2 / Гетероструктуры BiOI были получены аналогичным способом путем добавления однокомпонентного TiO 2 в решении выше.
Характеристика
Картины дифракции рентгеновских лучей (XRD) получали на рентгеновском дифрактометре Rigaku D-MAX2500, снабженном излучением Cu Kα. Сканирующую электронную микроскопию (СЭМ) получали с использованием автоэмиссионного сканирующего электронного микроскопа JSM-6700F (JEOL, Япония). Изображения образцов, полученные с помощью просвечивающей электронной микроскопии (ПЭМ), получали на микроскопе JEM-2100 (JEOL, Япония) при ускоряющем напряжении 200 кВ. Изотермы адсорбции / десорбции азота измеряли при 77 К с использованием анализатора площади поверхности и размера пор (NOVA 1000e, Quantachrome Instruments), а для оценки удельной площади поверхности применяли метод Брунауэра-Эммета-Теллера (БЭТ). Анализ рентгеновской фотоэлектронной спектроскопии (XPS) проводили на приборе XSAM800 (Kratos Corporation, UK) с источником ахроматического рентгеновского излучения Al Kα (1486,6 эВ). Спектры оптического поглощения и спектры диффузного отражения (DRS) были получены с использованием спектрофотометра в ультрафиолетовой и видимой областях (CARY500UV, Varian). Спектры фотолюминесценции регистрировали с помощью Shimadzu RF-5301 с длиной волны возбуждения 365 нм. Переходный фототок анализировали с помощью электрохимической рабочей станции (CHI760E, Шанхай, Ченхуа, Китай) со стандартной трехэлектродной системой, в которой использовалось стекло FTO с нанесенным катализатором в качестве рабочего электрода, Pt в качестве противоэлектрода и SCE в качестве электрода сравнения в электролите 0,5 М Na 2 SO 4 .
Фотокаталитическая производительность
Фотокаталитическая активность синтезированных композитов была протестирована на основе деградации метилового оранжевого (МО) с использованием Xe-дуговой лампы мощностью 500 Вт в качестве источника света. Здесь 140 мг фотокатализаторов добавляли к 50 мл раствора МО (5 мг / л), взятого в кварцевый стакан. Перед освещением суспензию перемешивали в течение 30 мин в темной камере для достижения адсорбционно-десорбционного равновесия между фотокатализаторами и раствором МО. Затем смесь облучали в течение 180 минут, и каждые 45 минут отбирали аликвоту раствора. Смесь центрифугировали при 8000 об / мин в течение 3 мин для удаления катализаторов из надосадочной жидкости. В тесте на стабильность фотокатализатора образцы промывали деионизированной водой после каждого цикла, а затем добавляли к свежему раствору MO для следующего цикла. Остаточную концентрацию МО контролировали с помощью УФ-видимого спектрофотометра (CARY500UV, Varian), а процент разложения количественно анализировали, сравнивая максимальное поглощение при 465 нм.
Обычно отверстия (h + ), электроны (e - ), супероксидные радикалы (• O - 2 ), а гидроксильные радикалы (• OH) могут образовываться в полупроводниковой фотокаталитической системе при облучении. Был проведен тест улавливания радикалов для фотоиндуцированных активных частиц. Эксперимент по улавливанию был аналогичен тестам на фотокаталитическое разложение, где динатриевая соль этилендиаминтетрауксусной кислоты (EDTA-2Na, 2 ммоль / л), бромат калия (KBrO 3 , 10 ммоль / л), бензохинон (BQ, 1 ммоль / л) и изопропиловый спирт (IPA, 10 ммоль / л) были использованы для удаления h + , e - , • O - 2 и • ОН реактивные частицы соответственно.
Результаты и обсуждения
На рис. 1 представлены порошковые дифрактограммы TiO 2 . , TiO 2 / CdTe, TiO 2 / BiOI и TiO 2 / CdTe / BiOI. Отмечено, что TiO 2 характерные пики можно выделить во всех образцах, а пики со значениями 2θ при 25,5 °, 37,8 °, 48,8 °, 53,5 ° и 55,6 ° можно индексировать как (101), (004), (200) и ( 105), (211) фасеты анатаза (JCPDS № 84-1285) [22]. Из диаграмм, показанных на рис. 1c, d, дифракционные пики при 2θ 29,7 °, 31,7 °, 45,5 ° и 51,3 ° показаны помимо пиков TiO 2 , что согласуется с тетрагональным BiOI (JCPDS № 73-2062) [23]. Однако пики BiOI гораздо более очевидны в TiO 2 . / BiOI, чем у TiO 2 / CdTe / BiOI. Что касается TiO 2 / CdTe (рис. 1b), кроме TiO 2 на рентгенограмме четко не обнаружено никаких других пиков. из-за небольшого размера кристаллитов или небольшого количества квантовых точек CdTe.
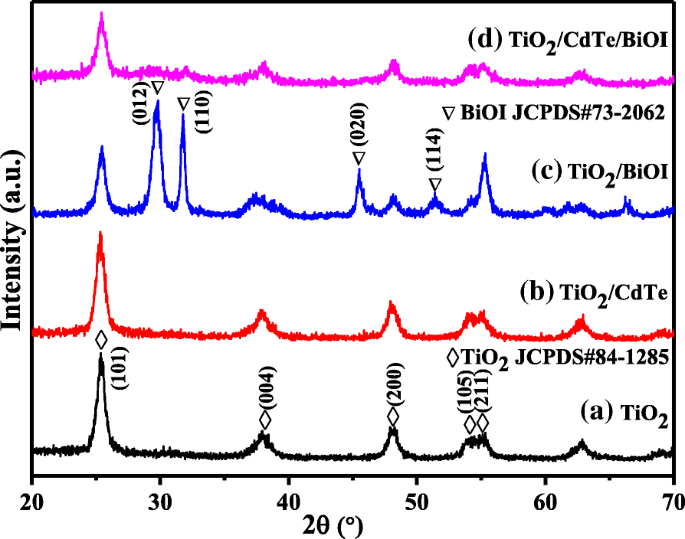
Диаграммы XRD a чистый TiO 2 , b TiO 2 / CdTe, c TiO 2 / BiOI и d TiO 2 / CdTe / BiOI
Внешняя морфология двойного TiO 2 / CdTe и тройной TiO 2 / CdTe / BiOI характеризуется с помощью SEM, как показано на рис. 2. Общее наблюдение за всеми TiO 2 композиты на основе имеют сферическую морфологию с диаметром около 200-400 нм и чешуйчатый BiOI, нанесенный на поверхность TiO 2 сферы, кроме TiO 2 / CdTe показан на рис. 2а. СЭМ изображение TiO 2 (S) / CdTe / BiOI, показанный на рис. 2b, показывает ситуацию, аналогичную TiO 2 . (S) / CdTe и TiO 2 (S) сферы покрыты множеством хлопьев BiOI с относительно правильной морфологией. Однако для TiO 2 дело обстоит иначе. (H) / CdTe / BiOI, в котором частицы обладают неоднородной морфологией с различным размером и поверхностью, подобной цветной капусте, как показано на рис. 2c, d. Более того, хлопья BiOI, кажется, легче прикрепить к TiO 2 (H) / CdTe, вызванный шероховатой поверхностью из TiO 2 (H), и первозданная полая структура TiO 2 (H) матрица может быть идентифицирована в увеличенном виде.

SEM-изображения a TiO 2 (S) / CdTe, b TiO 2 (S) / CdTe / BiOI и c - г TiO 2 (H) / CdTe / BiOI
ПЭМ-изображения дают дополнительное представление о структурной эволюции тройного TiO 2 / CdTe / BiOI, как показано на рис. 3. Однородный и хорошо диспергированный твердый сферический TiO 2 можно отчетливо наблюдать на рис. 3а, и некоторые крошечные частицы также обнаружены в этой области. Шаг решетки 0,238 нм и 0,33 нм, соответствующий плоскости (004) TiO 2 а плоскость (111) CdTe может быть идентифицирована на рис. 3b, демонстрируя образование гетеропереходов между TiO 2 сферы и КТ CdTe. Из рис. 3в видно, что к поверхности твердого сферического TiO 2 прикреплены многочисленные чешуйки. , а граница решетки составила 0,282 нм на рис. 3г, что соответствует направлению [110] кристалла BiOI. Более того, увеличение границы раздела также свидетельствует о существовании КТ CdTe и чешуек BiOI в TiO 2 (S) / CdTe / BiOI. Напротив, на рис. 3д показан TiO 2 (H) / CdTe / BiOI, который проявляется в морфологии агрегированных полых сфер без видимых прикрепленных чешуек. Это явление подразумевает, что компоненты BiOI, вероятно, состоят из гораздо более мелких частиц, чем огромная поверхность TiO 2 (H) сферы, состоящие из большого количества первичного TiO 2 наночастиц, децентрализует центры зародышеобразования. Точно так же увеличенное изображение границы раздела подтверждает присутствие гетероструктурированного тройного TiO 2 Композиты (H) / CdTe / BiOI, как показано на рис. 3f, и кристаллическая плоскость (111) CdTe и (002) BiOI могут быть четко видны.

TEM-изображения a - б TiO 2 (S) / CdTe, c - г TiO 2 (S) / CdTe / BiOI и e - е TiO 2 (H) / CdTe / BiOI
На рисунке 4 показаны изотермы адсорбции / десорбции азота тройного TiO 2 . (S) / CdTe / BiOI и TiO 2 Гетероструктуры (H) / CdTe / BiOI. Обе изотермы обладают схожими характеристиками изотермы типа IV согласно классификации IUPAC [24]. Однако TiO 2 (S) / CdTe / BiOI обладает петлей гистерезиса H2 типа в диапазоне 0,4-0,8 [25], что указывает на накопление однородного TiO 2 зерна прямым прокаливанием, а TiO 2 (H) / CdTe / BiOI с петлей гистерезиса типа H3 из-за закрепления пор является производным от гидротермальных нанолистов или предшественников нанотрубок [10], и результаты согласуются с изображениями SEM и TEM. Кроме того, удельная поверхность TiO 2 (S) / CdTe / BiOI и TiO 2 (H) / CdTe / BiOI было рассчитано как 77,7 и 91,6 м 2 г −1 с использованием метода Брунауэра-Эммета-Теллера (BET). Относительно большая площадь поверхности TiO 2 Микросферы (H) / CdTe / BiOI могут предоставить больше активных центров для адсорбции молекул реагентов, что приведет к более эффективным фотокаталитическим характеристикам.
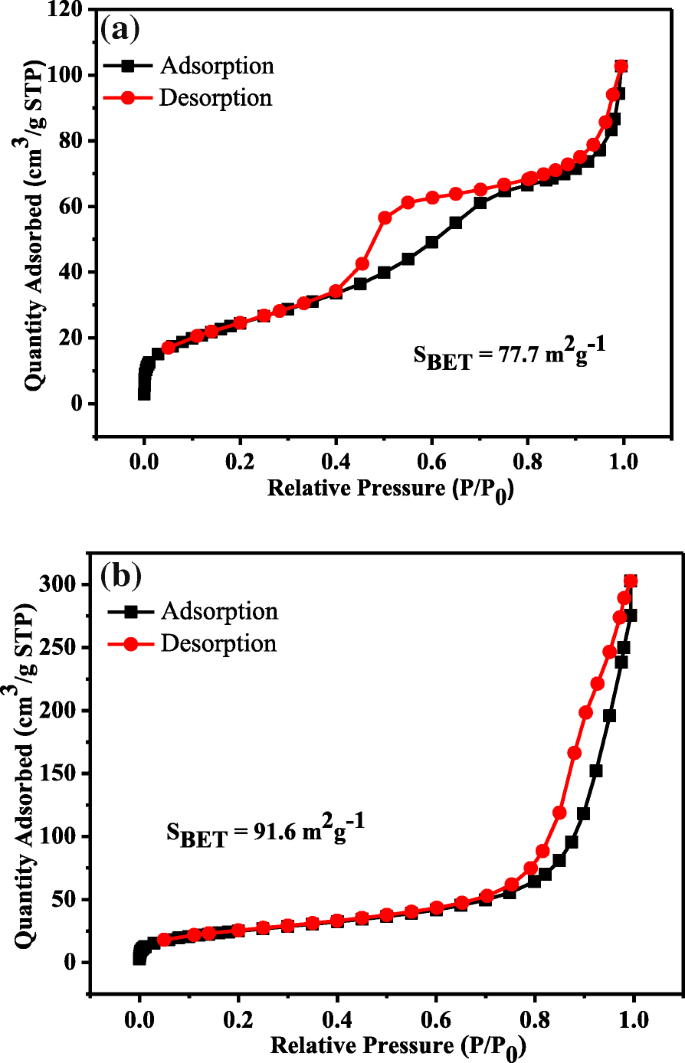
Изотермы абсорбции-десорбции азота а TiO 2 (S) / CdTe / BiOI и b TiO 2 (H) / CdTe / BiOI
Согласно обсуждению выше, эволюция TiO 2 Гетероструктуры / CdTe / BiOI можно проиллюстрировать схемой 1. В качестве альтернативы аморфный TiO 2 микросферы также могут превращаться в TiO 2 твердые микросферы непосредственно с помощью простой процедуры прокаливания. Во время следующего гидротермального процесса ранее существовавший TiO 2 Микросферы / CdTe QD могут действовать как центры зародышеобразования для кристаллизации BiOI, и, таким образом, тройной TiO 2 Гетероструктуры / CdTe / BiOI образуются одновременно. Хорошо известно, что BiOI обладает высокой скоростью зародышеобразования и роста; в результате частицы BiOI относительно большого размера и небольшого количества образуются на TiO 2 (S) в форме чешуек, растущих в направлении [110]. Однако в случае TiO 2 (H) микросферы, которые обладают большей поверхностью для кристаллизации BiOI, частицы BiOI имеют тенденцию существовать в форме, которая имеет относительно небольшой размер и большое количество. Следовательно, морфология поверхности TiO 2 микросферы определяют форму и форму частиц BiOI, как показали результаты SEM и TEM.
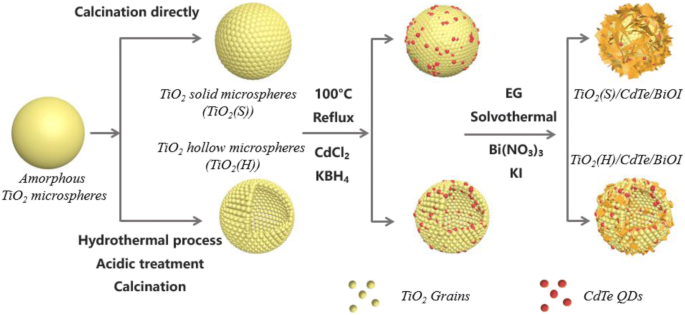
Структурная эволюция аморфного TiO 2 в TiO 2 / CdTe / Гетероструктуры BiOI
XPS используется для исследования поверхностных электронных состояний и химического состава образцов в исходном состоянии, и результаты показаны на рис. 5. Из обзорного спектра XPS видно, что TiO 2 / CdTe / BiOI содержит элементы Ti, O, Bi, I, Cd и Te. На рисунке 5b показано, что пики в XPS-спектре высокого разрешения Ti 2p, соответствующие энергии связи 458,5 эВ и 464,2 эВ, приписываются Ti 2p 3/2 и Ti 2p 1/2 , что указывает на степень окисления Ti (IV) [26], а измеренная энергия связи (BE) разделения 5,7 эВ согласуется с TiO 2 [27]. Однако энергии связи Ti 2p 1/2 и Ti 2p 3/2 для TiO 2 / CdTe и TiO 2 / CdTe / BiOI составляют 457,5 и 463,3 эВ, соответственно, оба из которых имеют сдвиг примерно на 0,8 эВ в область более низких энергий по сравнению с чистым TiO 2 , что еще раз доказывает сильное взаимодействие между CdTe и TiO 2 . Спектр остовного уровня O 1 s (рис. 5c) около 529,5 эВ связан с решеткой O в голом TiO 2 образцов, что связано со связями Ti-O [28]. Следует отметить, что сдвиг в сторону более низкой энергии связи пика O 1 с в TiO 2 / CdTe и TiO 2 Образцы / CdTe / BiOI указывают на потерю ионов кислорода [27], что может быть связано с частичным окислением CdTe на TiO 2 . Этот результат хорошо согласуется со сдвигом Ti 2p и подразумевает образование границы раздела между TiO 2 , BiOI и CdTe в гетеропереходе. Те 3d 5/2 Спектры (рис. 5д) показывают два состояния теллура при BE 564,1 и 577,1 эВ соответственно, которые характерны для CdTe.
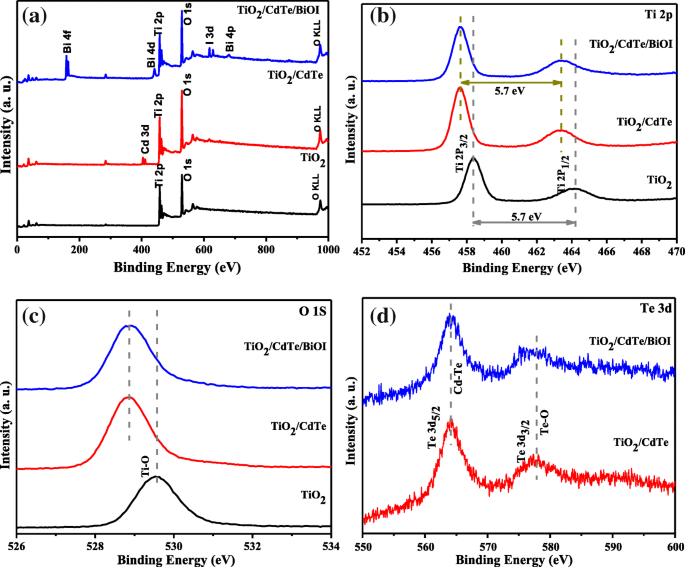
а Спектр сканирования XPS образцов TiO 2 , TiO 2 / CdTe, TiO 2 / CdTe / BiOI. б - г XPS-спектры Ti, O и Te с высоким разрешением
Поскольку оптические адсорбционные свойства считаются критическими для многокомпонентных полупроводников, спектры оптического поглощения TiO 2 (S), TiO 2 (S) / CdTe, TiO 2 (S) / BiOI, TiO 2 (S) / CdTe / BiOI и TiO 2 (H) / CdTe / BiOI показаны на рис. 6а. Свежеприготовленный TiO 2 показывает аналогичную тенденцию, как коммерческий P25, предполагая типичную характеристику ультрафиолетового ответа. Что касается бинарных и тройных композитов, TiO 2 (S) / CdTe / BiOI обладает гораздо более очевидным поглощением в видимой области, чем TiO 2 . (S) / CdTe и TiO 2 (S) / BiOI, что отражает усиление связи между компонентами за счет загрузки КТ CdTe. И поглощение TiO 2 (S) / CdTe / BiOI в видимом диапазоне немного слабее, чем у TiO 2 (H) / CdTe / BiOI; мы связываем это явление с эффектом дисперсии полой структурой TiO 2 микросферы, как описано выше. На вставленном изображении показаны графики Таука (Ahv) 1/2 по сравнению с hv образцов. Ширина запрещенной зоны TiO 2 (S), TiO 2 (S) / CdTe / BiOI и TiO 2 (H) / CdTe / BiOI оцениваются путем экстраполяции прямой линии на ось абсцисс и оцениваются как 3,02 эВ, 2,57 эВ и 2,45 эВ, соответственно. Стоит отметить, что TiO 2 (S) / CdTe / BiOI показывает небольшую выпуклость, отличную от TiO 2 (H) / CdTe / BiOI, независимо от синего сдвига на 0,12 эВ, что предполагает неравномерное распределение крупных частиц BiOI, как следует из результатов СЭМ, приведенных выше.
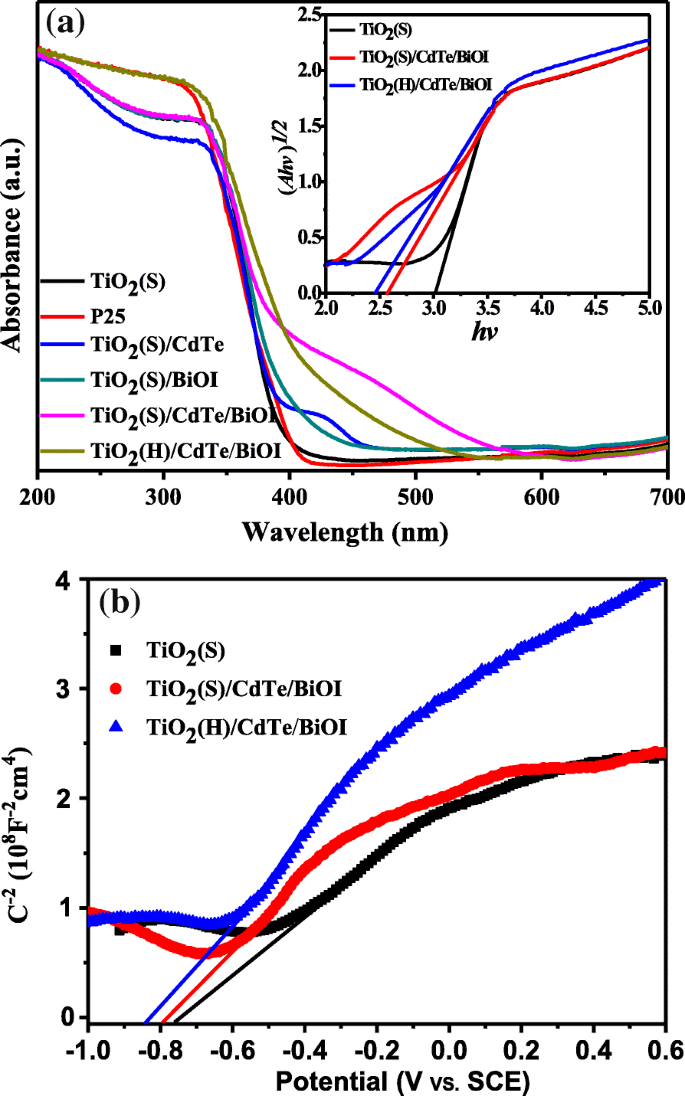
а УФ-видимые спектры диффузного отражения всех образцов и соответствующие графики Tauc TiO 2 (S), TiO 2 (S) / CdTe / BiOI и TiO 2 (H) / CdTe / BiOI образцы. б Графики Мотта-Шоттки в 0,5 M Na 2 SO 4 на частоте 1 кГц TiO 2 (S), TiO 2 (S) / CdTe / BiOI и TiO 2 (H) / CdTe / образцы BiOI
Чтобы лучше понять электронные свойства и структуру обоих фотокатализаторов, электрохимический эксперимент Мотта-Шоттки проводится в 0,5 M Na 2 SO 4 , как показано на рис. 6b. На рис. 6b все образцы показывают положительный наклон на графиках Мотта-Шоттки, что указывает на то, что полученные композиты явно являются полупроводниками n-типа [29, 30]. А энергия положения зоны проводимости (CB) образцов может быть приблизительно равна потенциалу плоской зоны ( E fb ) путем экстраполяции X пересечения линейного участка на графиках Мотта-Шоттки. Значение E fb TiO 2 (S), TiO 2 (S) / CdTe / BiOI и TiO 2 (H) / CdTe / BiOI составляет -0,76 В (против SCE), -0,80 В (против SCE) и -0,85 В (против SCE), соответственно. Поскольку SCE, который мы использовали в измерениях Мотта-Шоттки, имеет значение - 0,24 В по сравнению с NHE [31], CBM TiO 2 (S), TiO 2 (S) / CdTe / BiOI и TiO 2 Образцы (H) / CdTe / BiOI могут быть рассчитаны как -0,52 В (по сравнению с NHE), -0,56 В (по сравнению с NHE) и -0,6 В (по сравнению с NHE), соответственно, что более отрицательно, чем потенциал восстановления O 2 / • O - 2 (E 0 (O 2 / • O - 2 ) =- 0,33 В по сравнению с NHE). Кроме того, в сочетании со значением запрещенной зоны на рис. 6 максимум валентной полосы (VBM) находится при 2,5 В (против NHE), 2,01 В (против NHE) и 1,85 В (против NHE), соответственно.
На рис. 7а показана фотокаталитическая деструкция МО в растворах без катализатора и на различных фотокатализаторах. Хорошо видно, что TiO 2 твердые микросферы и P25 обладают относительно плохой фотокаталитической активностью при моделировании солнечного света, а деградация вызвана небольшой ультрафиолетовой частью от источника света. Напротив, фотокаталитические характеристики TiO 2 (S) / BiOI и TiO 2 (S) / CdTe немного увеличивается, и процент удаления МО достиг 46,3% и 57,5% после 180 мин облучения, соответственно. Стоит отметить, что фотокаталитическое разложение МО может достигать 88,4% за 180 минут и 99,7% за 90 минут для TiO 2 (S) / CdTe / BiOI и TiO 2 (H) / CdTe / BiOI, соответственно, из-за синергетического бинарного реагирующего на видимый свет компонента BiOI и квантовых точек CdTe. Кроме того, более эффективный TiO 2 (H) / CdTe / BiOI над TiO 2 (S) / CdTe / BiOI, вероятно, вызвано немного большей удельной поверхностью (91,6 м 2 г −1 более 77,7 м 2 г −1 ) как указано выше. На рисунке 7b показан эксперимент по циклической деградации TiO 2 . (S) / CdTe / BiOI и TiO 2 Композиты (H) / CdTe / BiOI. После трех циклов эффективность фотодеградации несколько снижается.
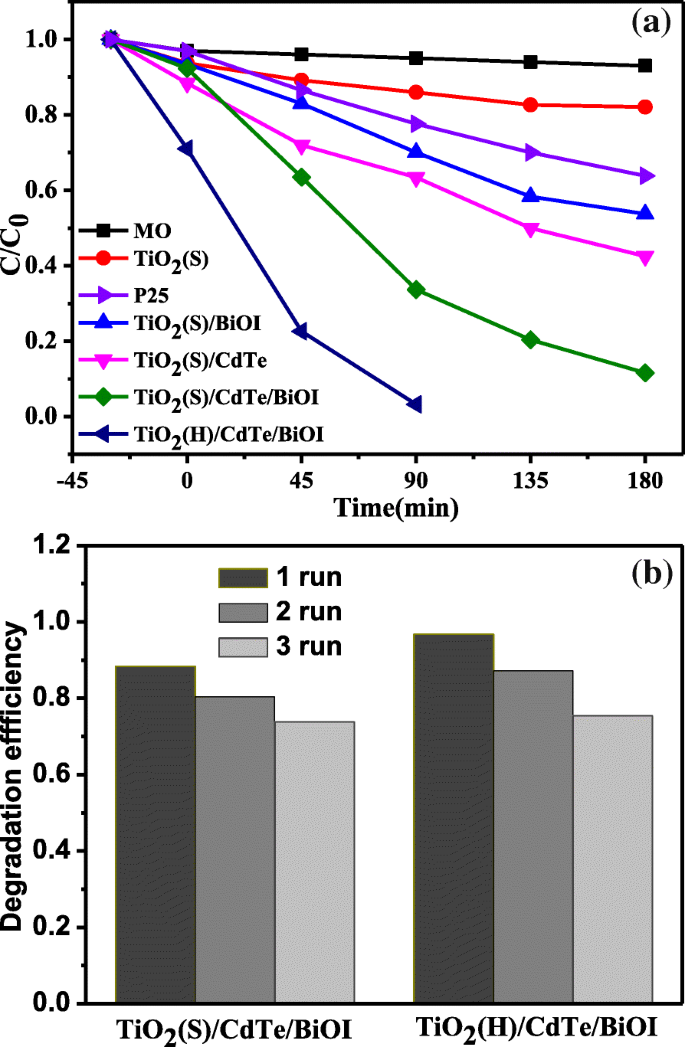
а Фотокаталитические характеристики образцов для удаления МО. б Эксперименты по фотокаталитическому рециркуляции TiO 2 (S) / CdTe / BiOI и TiO 2 (H) / CdTe / образцы BiOI
Чтобы оценить путь фотокаталитического разложения МО под действием TiO 2 / CdTe / BiOI, эффект h + , e - , • OH и • O - 2 был исследован путем улавливания эксперимента с использованием EDTA-2Na (h + ), KBrO 3 (е - ), BQ (• O - 2 ) и IPA (• OH). На рисунке 8 показана эффективность разложения МО во время этих фотокаталитических экспериментов в присутствии выбранных поглотителей. Можно обнаружить, что фотокаталитический процесс подавляется без какого-либо поглотителя, а эффективность разложения практически отсутствует в присутствии EDTA-2Na. Однако e - мусорщик мог ускорить деградацию, что продемонстрировало, что дыры (h + ) являются основными активными формами деградации МО. BQ как • O - 2 мусорщик просто повлиял на деградацию в небольшой степени, предполагая, что • O - 2 частично ответственны за процесс фотокаталитического окисления. Кроме того, влияние IPA на TiO 2 Удаление МО образца / CdTe / BiOI практически не наблюдается, что указывает на то, что • радикалы ОН вряд ли применимы в текущей фотокаталитической системе.
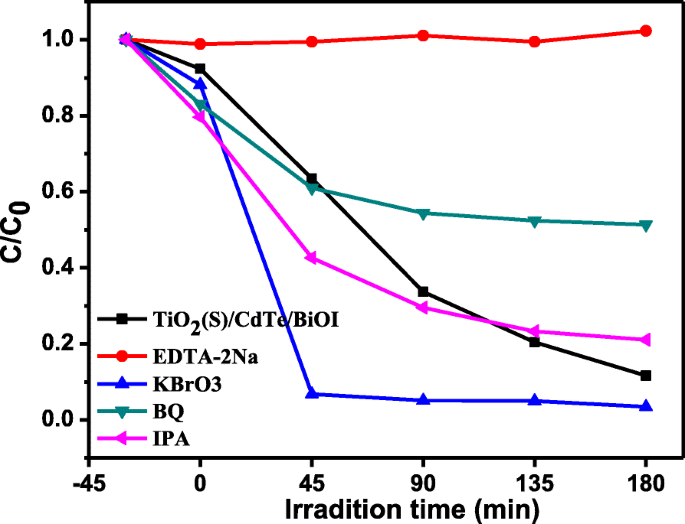
Графики фотодеградации МО при улавливании различных фотогенерированных активных частиц TiO 2 (S) / образец CdTe / BiOI
Спектроскопия излучения фотолюминесценции (ФЛ) проводится для дальнейшего изучения поведения переноса фотогенерированных носителей заряда. Как показано на рис. 9, все образцы демонстрируют широкий пик излучения ФЛ в области 450–500 нм с возбуждением на 365 нм. Голый TiO 2 (S) имеет сильный пик эмиссии, а TiO 2 (S) / CdTe / BiOI образец показывает более низкую интенсивность, чем TiO 2 (S). Это явление указывает на то, что скорость рекомбинации фотогенерированных носителей заряда была эффективно ограничена после декорирования CdTe и BiOI на поверхности TiO 2 . Кроме того, TiO 2 (H) / CdTe / BiOI демонстрирует значительно меньшую интенсивность ФЛ по сравнению с другими образцами, что вызвано более быстрым переносом электронов и дырок от КТ CdTe или нанолистов BiOI на поверхность TiO 2 . Результаты PL согласуются с результатом эксперимента по фотодеградации.
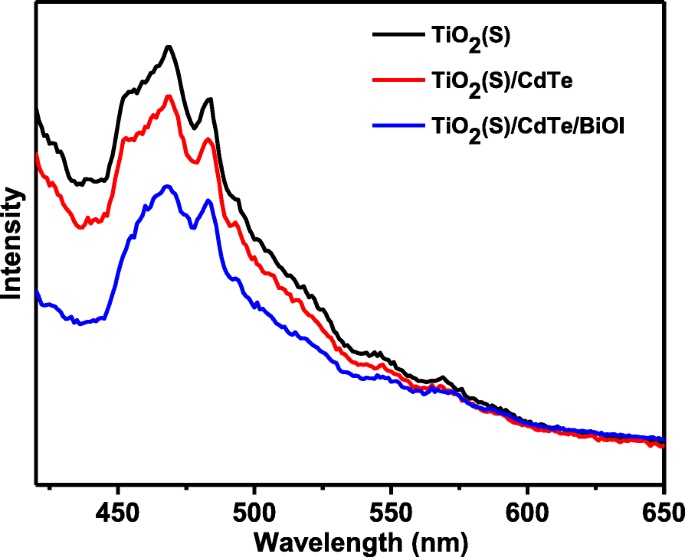
Спектры фотолюминесценции чистого TiO 2 (S), TiO 2 (S) / CdTe / BiOI и TiO 2 (H) / CdTe / образцы BiOI ( λ возбуждение =365 нм)
Фототок образцов показан на рис. 10. Стоит отметить, что TiO 2 Композиты (S) / CdTe показали более высокий отклик фототока, чем у чистого TiO 2 (S) и TiO 2 Композиты (S) / CdTe / BiOI. Следовательно, повышенный фототок можно в основном отнести к эффективному разделению и миграции фотогенераторов, что улучшает фотокаталитические характеристики.
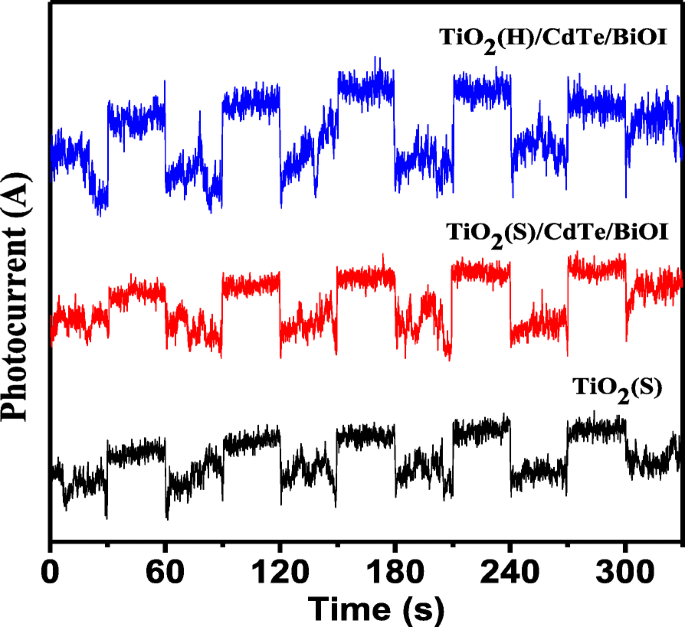
Переходный отклик фототока TiO 2 (S), TiO 2 (S) / CdTe / BiOI и TiO 2 (H)/CdTe/BiOI
Based on the results and discussions above, we propose a synergistic CdTe QDs/BiOI sensitization mechanism of the exciton transfer in TiO2 /CdTe/BiOI to explain the enhanced photo activity, as illustrated in Scheme 2. It is well known that TiO2 with a wide bandgap (3.02 eV) could only utilize the UV region in solar light, while the narrow bandgap CdTe QDs (~ 1.5 eV) [32] and BiOI nanostructures (~ 1.8 eV) [33] can be excited by photons in the visible range. In addition, a p-n junction is formed between p-type BiOI and n-type TiO2 when Fermi levels reached equilibrium, which facilitate photo-induced electrons to migrate from CB of BiOI to that of TiO2 [17, 34]. Similarly, a type II heterojunction is formed between p-type CdTe [18] and TiO2 microspheres; thus, electrons in the CB of CdTe QDs can transfer to TiO2 [35]. Therefore, the lifetime of the photogenerated electron and hole is prolonged, which is beneficial for the degradation towards MO.
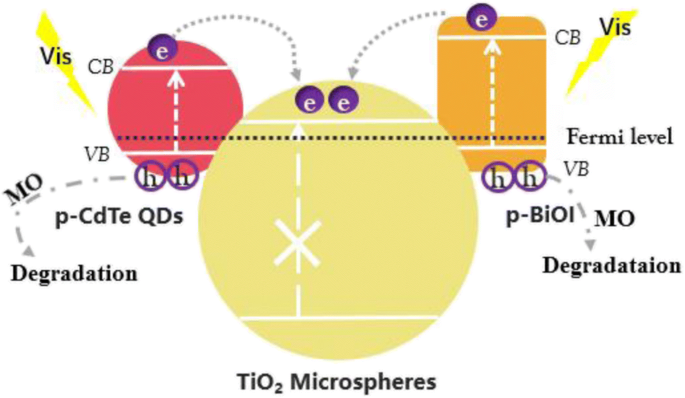
Illustration of photo-induced charge transfer in ternary TiO2 /CdTe/BiOI photocatalytic system
Выводы
In summary, a series of TiO2 -based photocatalysts were synthesized by a facile hydrothermal method. Modifications by BiOI and CdTe QDs were carried out to fabricate binary and ternary heterostructures, and the narrow bandgap semiconductors extended light response for the hybrid photocatalysts. In the case of ternary TiO2 /CdTe/BiOI heterostructured photocatalyst, the BiOI flakes and CdTe QDs act as sensitizers on one hand, which are excited by simulated solar light and transfer electrons to TiO2 . Meanwhile, the TiO2 microspheres serve as separation centers for the photo-induced charges on the other hand; thus, the synergistic effect among TiO2 , CdTe, and BiOI enhances the photocatalytic removal of MO. In addition, hollow TiO2 precursors were also employed to fabricate TiO2 /CdTe/BiOI heterostructures, and the improved photocatalytic performance towards MO degradation is attributed to a higher surface area and dispersion of BiOI components. The strategy of material regulation and incorporation will provide possibilities for the design of the multi-component semiconductor photocatalysts.
Сокращения
- TiO2 (H):
-
TiO 2 hollow microspheres
- TiO 2 (S):
-
TiO 2 solid microspheres
- TiO 2 /BiOI:
-
TiO 2 spheres modified with BiOI
- TiO 2 /CdTe:
-
TiO 2 spheres modified with CdTe QDs
- TiO 2 /CdTe/BiOI:
-
TiO 2 , CdTe, and BiOI ternary composites
Наноматериалы
- Высокие фотокаталитические характеристики двух типов композитных фотокатализаторов TiO2, модифицированных г…
- На пути к наножидкости TiO2 - Часть 2:Приложения и проблемы
- Фотокаталитическая активность, усиленная Au-плазмонными наночастицами на фотоэлектроде нанотрубки TiO2, покры…
- Иерархическая гетероструктура полых сфер ZnO @ TiO2 для высокоэффективного фотокаталитического выделения водор…
- Подготовка и фотокаталитические характеристики фотокатализаторов LiNb3O8 с полой структурой
- Новый фотокатализатор на гетеропереходе Bi4Ti3O12 / Ag3PO4 с улучшенными фотокаталитическими характеристиками
- Массивы нанотрубок TiO2:изготовлены с помощью мягко-твердого шаблона и зависимости характеристик эмиссии поля…
- Влияние кислотного пептизирующего агента на соотношение анатаз-рутил и фотокаталитические характеристики н…
- Фотокаталитическая активность тройного нанокомпозита аттапульгит – TiO2 – Ag3PO4 для разложения родамина B при мод…
- Повышенная эффективность преобразования мощности перовскитных солнечных элементов с использованием матери…



