Легкий синтез в одной емкости биомиметических фотокатализаторов Zn (II) -Porphyrin-Sensitized 3D TiO2 полых нанобоксов и синергетически усиленная деградация в видимом свете
Аннотация
Серия биомиметических фотокатализаторов цинка (II) мезо -тетра (4-карбоксифенил) порфиринато (ZnTCP) -сенсибилизированный трехмерный иерархический TiO 2 полые нанобоксы (TiO 2 -HNBs), собранный из шести упорядоченных нанолистов с доминирующей экспозицией {001} граней (ZnTCP @ TiO 2 -HNB) были успешно синтезированы простым однореакторным сольвотермическим методом через процесс топологического преобразования с TiOF 2 как шаблон. Инфракрасные спектры (ИК), УФ-видимая спектроскопия и рентгеновская фотоэлектронная спектроскопия (XPS) подтвердили, что ZnTCP играет решающую роль в создании трехмерных полых нанобоксов за счет образования сложноэфирной связи, объединенной с TiO 2 -HNB, которые также обеспечивают перенос фото возбужденных электронов мостиком для сенсибилизации TiO 2 -HNB для улучшения отклика в видимом свете. Из-за превосходной сенсибилизации и биомиметической активности ZnTCP скорость фотодеградации родамина B (RhB) в свежеприготовленном ZnTCP @ TiO 2 -HNB с ZnTCP / TiOF 2 массовая доля 2% (T-2p) улучшается в 3,6 раза по сравнению с TiO 2 -HNB с выходом разложения 99% в течение 2 часов при моделировании солнечного излучения (> 420 нм). Повышенная способность к фотодеградации была приписана синергическому видимому фотокаталитическому механизму биомиметического катализатора, который может не только производить гидроксильный радикал (• OH) и супероксидный радикал (• O 2 - ) в результате процесса возбуждения сенсибилизированного ZnTCP TiO 2 -HNBs, но также генерируют синглетный кислород ( 1 О 2 ), который был обеспечен только биомиметическим ферментом порфирином. Кроме того, фотокатализатор показал хорошую стабильность при переработке и диспергируемость после пяти циклов, что объясняется сильной химической связью ZnTCP с носителем TiO 2 -HNBs. С помощью электрохимического анализа циклической вольтамперометрии было изучено влияние центральных ионов цинка и исходных порфириновых колец на окислительно-восстановительные свойства биомиметического катализатора.
Фон
Все виды органических красителей играют незаменимую роль в различных областях промышленного применения, включая крашение тканей, кожи или бумаги [1]. Однако их токсичность, разнообразие и стойкость напрямую влияют на здоровье экосистем и представляют прямую угрозу для людей из-за загрязненных источников питьевой воды [2]. Как найти простой способ удалить синтетические красители, загрязняющие промышленные сточные воды, является неотложной задачей.
Были разработаны многочисленные методы удаления органических красителей из сточных вод, включая физические, биологические и химические методы [3,4,5]. Физические способы, такие как адсорбция, коагуляция, ионный обмен и мембранная фильтрация, используются для удаления органических загрязнителей [6, 7], тогда как физические методы только переносят органические молекулы из водной фазы, и это принципиально не решает проблему. Кроме того, биологические процессы обычно происходят в относительно мягких условиях из-за присущих им длительных процедур и их непереносимости к органическим загрязнителям, что затрудняет крупномасштабные промышленные применения. Поскольку он использовал солнечную энергию для разложения загрязняющих красителей, образовавшийся AuAgCuBi 2 О 4 композит проявляет превосходную фотокаталитическую активность в отношении разложения RhB под воздействием искусственного солнечного излучения. А композиты проявляют значительно повышенную фотокаталитическую активность [8,9,10,11]. Исходя из вышеизложенных соображений, эффективное удаление органических загрязнителей из сточных вод далеко от удовлетворительного результата, и по-прежнему существует острая необходимость в разработке экономически эффективных и экологически безопасных стратегий. Усовершенствованные процессы окисления (АОП), основанные на производстве активных веществ, таких как свободные гидроксильные радикалы, которые могут решить проблему разрушения красителей в водных системах, были использованы для отказа от селективного окисления широкого спектра органических загрязнителей [12] . Некоторые типичные методы АОП были успешно разработаны для обработки органических загрязнителей, включая схемы Фентона, озоновые системы, полупроводниковые фотокатализаторы и электрохимический катализ. В последние годы, благодаря простоте эксплуатации и экологической совместимости, значительное внимание было уделено разложению органических загрязнителей, катализируемому биомиметическим катализом, который объединяет преимущества распознавания ферментов и химического катализа [13].
По сравнению с химическим катализом высокая селективность является одним из самых больших преимуществ биомиметического катализа, и он может работать в мягких и экологически чистых условиях, что может значительно снизить энергозатраты и образование отходов. В последнее время металлопорфирин и его производные, которые могут имитировать процесс окисления, характерный для ферментов пероксидазы или железосодержащей оксигеназы, привлекли большое внимание к использованию в качестве окислительного разложения стойких органических загрязнителей из-за хорошей химической стабильности и их высокого коэффициента поглощения в солнечной среде. спектр. Чжао сообщил, что бипиридин железа (II), нанесенный на ионообменную смолу, может эффективно активировать O 2 разлагать органические красители в воде при облучении видимым светом [14]. Коллинз синтезировал серию железоцентрированных тетраамидо-макроциклических лигандных комплексов, которые были способны активировать как H 2 О 2 и O 2 разлагать органические загрязнители в гетерогенных водных системах, чтобы имитировать процессы, подобные пероксидазе, с ферментативной скоростью. Наши группы сообщили, что тетра (1,4-дитиин) порфиразин железа, нанесенный на анионообменную смолу (амберлит CG-400), показал отличную окислительную деструкцию органических красителей. Принимая во внимание опубликованные данные, установлено, что все эти металлопорфирины и их производные основаны на центральном ионе железа из-за переменной валентности иона железа. Однако поскольку Fe 2+ гораздо труднее хелатировать в порфириновое кольцо и при атмосферной нестабильности, этот процесс обычно выполняется в суровых условиях и при длительном времени реакции.
Как все мы знаем, порфирины цинка и его металлопорфирин обладают привлекательными свойствами, такими как высокая стабильность, хорошая светочувствительность, нетоксичность и легкий синтез, которые одобряются все большим количеством ученых. В частности, фоточувствительность порфиринов цинка может индуцировать квантовый выход синглетного кислорода, который можно использовать для фотодинамической терапии и фотокаталитического окислительного разложения органических загрязнителей [15]. Эти превосходные свойства вдохновляют нас на поиск лучших способов разработки композитов цинк-порфирина для легкого синтеза для изучения его фотокаталитического окисления органических загрязнителей. В то же время, учитывая гидрофильность порфирина цинка, в его периферическое большое кольцо были введены четыре карбоксильные группы.
Еще одна актуальная задача - решить подложки из цинк-порфириновых композитов. В соответствии с предыдущими отчетами нашей группы, металлопорфирины и металлопорфиразины проявляют отличную гетерогенную фотокаталитическую активность только тогда, когда они нанесены на анионообменную смолу (Amberlite CG-400) или ионообменную смолу. Однако все виды смол не могут генерировать пары электронов и дырок и быстро переносить заряды при облучении видимым светом. Поэтому мы сфокусируемся на типичном полупроводниковом фотокатализаторе TiO 2 .
До сих пор анатаз TiO 2 стал одним из самых важных фотокатализов из-за его потенциального применения в решении проблемы загрязнения окружающей среды и энергетического кризиса, такого как фотокаталитическое разложение органических загрязнителей в сточных водах, из-за его нетоксичности, более высокой химической стабильности и фотостабильности. Однако он может поглощать только очень небольшую часть ультрафиолета (около 4,5%) солнечного света из-за относительно широкой запрещенной зоны анатаза TiO 2 (3,2 эВ), что сильно ограничивает его практическое применение [16,17,18]. Следовательно, это очень важный вопрос для повышения фотореакционной активности TiO 2 в видимом свете. фотокатализаторов, позволяющих в полной мере использовать большой объем солнечного спектра, но остается сложной задачей. На сегодняшний день было проведено значительное количество исследований, посвященных улучшению использования TiO 2 в видимом свете. за счет взаимодействия полупроводников [19,20,21], легирования ионами металлов и неметаллов [22, 23] и модификации поверхности [24,25,26]. Это можно объяснить тем фактом, что поверхностные кислородные вакансии действуют как акцепторы фотоиндуцированных зарядов, а места адсорбции подавляют рекомбинацию фотогенерированных зарядов, что приводит к увеличению доступности фотогенерированных электронов и дырок для фотокаталитической реакции [27,28,29]. Что касается полупроводниковой связи, хотя она может эффективно увеличивать скорость разделения фотогенерированных электронно-дырочных пар, их эффективность фотореакции сильно зависит от их структур переходов и достигается только слишком низкая эффективность преобразования энергии для промышленного применения [30,31,32]. Легирующая модификация TiO 2 обычно довольно сложно приготовить с заменой решетки при высокой температуре и многоступенчатыми процедурами. Подход к поверхностной сенсибилизации может значительно расширить светочувствительную область TiO 2 от УФ до видимого света. Как хороший сенсибилизатор, металлопорфирин и TiO, сенсибилизированный его производными, 2 привлекли большое внимание из-за их высокого коэффициента поглощения в солнечных спектрах, небольшого синглет-триплетного расщепления, высокого квантового выхода для межсистемного пересечения, больших времен жизни триплетных состояний и хорошей химической стабильности [33, 34]. Что еще более важно, сенсибилизация порфирином может увеличить запрещенную зону TiO 2 оптическое поглощение в области видимого света, которое может эффективно катализировать разложение органических загрязнителей. Функциональные группы вокруг порфиринового кольца представляют собой канал, по которому электроны возбужденного состояния красителя переносятся на TiO 2 зона проводимости [35, 36].
В последнее время большое количество 3D TiO 2 полые наноструктуры были синтезированы всевозможными методами, такими как полые трехмерные нанотрубки или микросферы, построенные из нанопроволок, нанолистов, наностержней или наночастиц. Однако эти полые конструкции, состоящие из случайно собранных строительных блоков, в основном имеют сферическую структуру. Погоня за несферическим 3D TiO 2 полые наноматериалы, такие как структура в форме коробки или куба, состоящая из упорядоченной иерархической структуры, все еще остаются проблемой. На сегодняшний день как экспериментальный, так и теоретический анализ продемонстрировал, что высокоэнергетические грани {001} анатаза TiO 2 может эффективно разделять фотогенерированные электронно-дырочные пары и сужать запрещенную зону TiO 2 , который вызвал взрыв исследовательского интереса [37]. На основании вышеизложенного рассмотрения морфологии и модификации фасетов, как построить трехмерный иерархический TiO 2 полые коробчатые конструкции, собранные из шести упорядоченно расположенных листов, с преобладающим экспонированием граней {001} для увеличения поглощения видимого света, все еще остаются сложной проблемой. Таким образом, существует острая потребность в разработке простой и простой топологической синтетической стратегии для синтеза сенсибилизированного порфирином трехмерного полого TiO 2 структуры для получения отклика в видимом свете. Насколько нам известно, кубический TiOF 2 с индуцированным фторидом самотрансформацией изготовлению полых нанобоксов из цинк-порфиринового сенсибилизированного TiO 2 о композитном фотокатализаторе путем сольвотермической обработки не сообщалось.
Здесь мы предложили мезо -тетра (4-карбоксифенил) порфиринато-цинк (II) (ZnTCP) с карбоксильной группой на периферии порфирина в качестве сенсибилизатора и использовал простой топологический сольвотермический метод в одном сосуде для получения ZnTCP-сенсибилизированного TiO 2 полые нанобоксы (ZnTCP @ TiO 2 -HNB) с доминирующим обнажением граней {001} за счет образования устойчивых ковалентных связей между TiO 2 -ГНБ и порфирины цинка. Мы систематически изучали влияние массового содержания порфирина цинка на структуру и видимую фотокаталитическую активность TiO 2 , модифицированного порфирином цинка. полые нанобоксы (ZnTCP @ TiO 2 -HNBs).
Методы
Материалы
Все реагенты и растворители были качества реагентов, полученные от коммерческих поставщиков (Wuhan Guoyao Chemical Reagent Co. Ltd.), и использовались напрямую без дополнительной очистки. Все растворы готовили на дистиллированной воде.
Синтез ZnTCP-сенсибилизированного TiO 2 -HNB (ZnTCP @ TiO 2 -HNBs)
TiOF 2 Первоначально был подготовлен прекурсор в виде нанокубического шаблона
В типичной процедуре 30 мл ацетата, 5 мл фтористоводородной кислоты и 15 мл тетрабутилтитаната добавляли по каплям в стакан из поливинилфторида на 100 мл и непрерывно перемешивали в течение 25 минут. Затем смесь переносили в высушенный автоклав с тефлоновым покрытием объемом 100 мл и выдерживали при 200 ° C в течение 12 часов. После охлаждения до комнатной температуры белый порошок несколько раз промывали этанолом и сушили при 60 ° C в вакууме в течение ночи, затем получали TiOF 2 нанокубический прекурсор.
Получение порфиринов цинка (ZnTCP)
Процедура подготовки состояла из двух этапов. Первым этапом является синтез порфирина (TCP):обычно 100 мл пропионовой кислоты и 4,341 г (28,8 ммоль) 4-карбоксибензальдегида добавляли в трехгорлую колбу на 500 мл, которую нагревали на масляной бане и перемешивали в течение 30 мин. для обеспечения полного распыления. В указанную выше систему медленно по каплям добавляли раствор 10 мл пропионовой кислоты и 2 мл пиррола и кипятили с обратным холодильником при 140 ° C в течение 2 часов. Смесь охлаждали до комнатной температуры и дважды промывали 150 мл горячей воды. Затем с помощью карбоната натрия и серной кислоты для удаления смолы и корректировки значения pH от 5 до 7 соответственно. Продукт трижды экстрагировали бутанолом; наконец, продукт концентрировали и сушили на роторном испарителе. 1 Спектр ЯМР 1Н TCP показал ожидаемые сигналы, такие как протоны -ОН, Ar-H (фенил) и -CH (пиррол) при 4,12, 6,98-7,02 и 7,46-7,57 м.д., соответственно. Протоны NH во внутреннем ядре проявляются как широкий химический сдвиг при =-3,34 ppm, способный обмениваться дейтерием, как следствие 18 π-электронных систем планарной структуры. ИК (KBr, см −1 ) спектры, 3363 для -OH, 2927, 2852 для C-H, 1712 (C =O), 1623, 1488 и 1376 для C =C, 1053 для COOH, подтверждают структуру TCP. В масс-спектре обнаружен пик молекулярного иона при m / z =614,14 [M + 1] + . УФ-видимая [ДМФА, макс / нм] B-полоса при 419 нм и Q-полоса при 553 и 598 нм.
Во-вторых, синтез ZnTCP был следующим:0,544 г порфиринов и 0,20 г ацетата цинка растворяли в растворителе ДМФ. Смесь раствор нагревали и кипятили с обратным холодильником при 150 ° C в течение 2 ч на масляной бане при непрерывном перемешивании. Затем охлаждая его до комнатной температуры, продукт концентрировали и добавляли 100 мл деионизированной воды после того, как пурпурный полностью выпал в осадок. Наконец, воду удалили роторным испарителем и мезо Был получен -тетра (4-карбоксифенил) порфирин цинка (II) (ZnTCP). В 1 Спектры ЯМР 1Н ZnTCP, протоны NH внутреннего ядра исчезли; другие протоны показали аналогичный химический сдвиг при 4,12, 6,98–7,02 и 7,46–7,57 м.д. Из ИК-спектра резкий пик колебания связи C =O около 1720 см −1 был увеличен после реакции циклотетрамеризации, 3352 см -1 для -OH, 2928, 2853 см -1 для C-H, 1619, 1504 см −1 и 1378 см - 1 для C =C, 1231 и 1017 см −1 для C =O подтвердил структуру ZnTCP. Данные масс-спектра ZnTCP содержат сильный пик при m / z =678,11 [M + 1] + для иона родительского кольца. Спектр РФЭС подтвердил наличие пиков 2p1 / 2 Zn (II) с энергией связи 1021,5 эВ и 2p3 / 2 с энергией связи 1045,6 эВ. УФ-видимая [ДМФА, макс. / Нм] B-полоса при 432 нм и Q-полоса при 561 и 600 нм. Процедура синтеза ZnTCP проиллюстрирована на схеме 1.
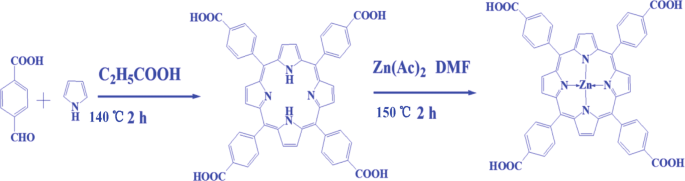
Схематическое изображение синтеза комплекса ZnTCP
Простой однокомпонентный синтезатор TiO, сенсибилизированного ZnTCP 2 -HNB (ZnTCP @ TiO 2 -HNB)
Использование TiOF 2 в качестве шаблона, этанол в качестве растворителя и порфирины цинка в качестве сенсибилизатора и TiO 2 полые нанобоксы в качестве опор, сенсибилизированные порфиринами трехмерные иерархические полые нанобоксы из диоксида титана с открытыми высокоэнергетическими гранями {001} были приготовлены посредством процесса топологического преобразования. В типичной процедуре 300 мг TiOF 2 70 мл этанола и 3 мг ZnTCP помещали в автоклав с тефлоновым покрытием и подвергали реакции в течение 48 часов при 200 ° C, затем охлаждали его до комнатной температуры; продукт концентрировали на роторном испарителе и сушили при 60 ° C под вакуумом в течение ночи. Затем полученный продукт обозначили как T-1p, где 1 представляет ZnTCP / TiOF 2 соотношение масс. Для сравнения, разные образцы были также синтезированы в других идентичных условиях, за исключением количества порфиринов цинка. Они обозначаются как T-0p, T-1p, T-2p, T-3p и T-5p соответственно. Однореакторный процесс синтеза ZnTCP @ TiO 2 -HNB показаны на схеме 2.
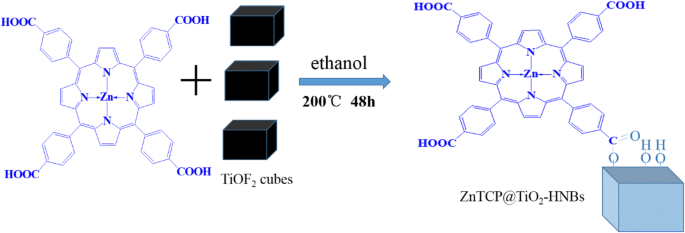
Схематическое изображение приготовления ZnTCP @ TiO 2 -HNBs
Характеристика
Инфракрасную спектроскопию с преобразованием Фурье (FT-IR) измеряли на спектрометре NeXUS 470 с использованием метода таблеток KBr. Кристаллическая структура этих катализаторов была охарактеризована порошковой дифракцией рентгеновских лучей (XRD) с использованием скорости сканирования 0,05 ° с -1 . в 2 θ диапазон от 10 до 80 ° в Bruker D8 Advance с использованием монохроматизированного излучения Cu-Ka. Рентгеновскую фотоэлектронную спектроскопию (XPS) регистрировали на фотоэлектронном спектрометре VG Multilab 2000 с использованием монохроматического Mg K a излучение в вакууме при 2 × 10 −6 Па. Все энергии связи относятся к пику C1s при 284,8 эВ поверхностного добавочного углерода. Морфология и микроструктура полученных образцов были проанализированы с помощью автоэмиссионного сканирующего электронного микроскопа (SEM) (Hitachi, Япония) и просвечивающего электронного микроскопа (TEM) (Tecnai G 2 20, США). Данные УФ-видимой спектроскопии диффузного отражения (DRS) были получены с использованием спектрофотометра Shimadzu UV-2600 от 240 до 800 нм с использованием BaSO 4 в качестве фона. Спектры фотолюминесценции (ФЛ) получали на флуоресцентном спектрофотометре Hitachi F-7000. Измерения циклической вольтамперометрии (ЦВА) проводились на рабочей станции электрохимии, управляемой внешним ПК и с использованием трехэлектродной конфигурации при комнатной температуре.
Фотокаталитические измерения
Все эксперименты по фотореакции проводились в самодельной системе фотокаталитического реактора, фотокаталитическая активность образцов после приготовления оценивалась с помощью органических красителей RhB (1 × 10 −5 моль / л) в качестве целевого загрязнителя при облучении видимым светом. Конкретный процесс выглядит следующим образом:50 мг фотокатализатора и 50 мл начальной концентрации 5 × 10 −4 Раствор RhB моль / л добавляли в цилиндрический реакционный сосуд с помощью ультразвукового диспергирования с диаметром 14 см 2 . плоской стороной и высотой 7 см, а затем перемешанный раствор перемешивали в темноте в течение ночи. После достижения адсорбционного равновесия фотокаталитическая реакция была инициирована путем облучения системы ксеноновой лампой 210 Вт со светофильтром ( λ > 420 нм), чтобы обеспечить освещение только видимым светом, система непрерывно охлаждалась водой, которая использовалась для поддержания системы при комнатной температуре. Через заданные интервалы времени собирали аликвоты по 3,5 мл и центрифугировали, а затем удаляли частицы катализатора для анализа. Концентрацию RhB через различные интервалы времени контролировали с помощью УФ-видимой спектроскопии. Все измерения проводились при комнатной температуре.
Метод фотолюминесценции (ФЛ) был использован для изучения активных частиц, образующихся во время разложения катализатора. Согласно драгоценному сообщению [38], кумарин, 4-хлор-7-нитробенз-2-окса-1, 3-диазол (NBD-Cl) и 1,3-дифенилизобензофуран (DPBF) использовались в качестве флуоресцентного зонда для обнаружения гидроксильный радикал (• OH), супероксидный радикал (• O 2 - ) и синглетный кислород ( 1 О 2 ), соответственно. ZnTCP @ TiO 2 Катализатор -HNB и вода реагируют с образованием гидроксильных радикалов активных частиц (• OH), а затем быстро захватываются кумарином с образованием 7-гидроксикумарина, который имеет сильную флуоресцентную способность. Обычно детектируемая процедура выглядит следующим образом:суспензии катализаторов (1,0 г / л), содержащие кумарин (0,1 ммоль / л), перемешивают при магнитной мешалке, а затем встряхивают в течение ночи. Смесь облучали ксеноновой лампой мощностью 210 Вт и отбирали образец с заданными интервалами 2 мин (или 4 мин, или 15 с). Флуоресцентный спектрофотометр использовался для анализа фильтрата при возбуждении соответствующей длиной волны.
Результаты и обсуждение
Изображения TEM и SEM
Морфология и кристаллические плоскости TiOF 2 , TiO 2 -HNBs и ZnTCP @ TiO 2 Образцы -HNB наблюдались с помощью просвечивающей электронной микроскопии, показанной на рис. 1. На рис. 1а показано, что TiOF 2 проявляет однородную твердую кубическую форму и гладкую поверхность со средним размером 250 нм. Как показано на рис. 1b, можно видеть, что морфология TiO 2 -HNB преобразованы в однородную полую коробчатую форму, состоящую из шести упорядоченных граней со средней длиной стороны 260 нм, что соответствует кубическому TiOF 2 шаблон. Внимательно посмотрев на рис. 1c – f, можно обнаружить, что трехмерные полые структуры ZnTCP @ TiO 2 -HNBs по-прежнему демонстрируют четко выраженную коробчатую морфологию во время индуцированного фтором самотрансформации кубического TiOF 2 к ZnTCP-сенсибилизированному TiO 2 процесс полых нанобоксов, которые имели правильную форму с некоторыми волосатыми щупальцами ZnTCP, покрытыми на поверхности полых коробок [39]. Изображения HRTEM (см. Вставку на рис. 1g) были получены, чтобы подтвердить, что полосы решетки составляют около 0,235 нм, что хорошо согласуется с высокоэнергетической гранью кристаллита {001} анатаза TiO 2 . Поверхность ZnTCP @ TiO 2 -На диаграмме решетки HNB представлены трехмерные иерархические полые нанобоксы, состоящие из шести упорядоченных нанолистов с доминирующими выступающими гранями {001}.

ПЭМ-изображения синтезированных катализаторов: a TiOF 2 , b TiO 2 -HNBs, c Т-1п, д Т-2п, э Т-3п и ф , г Т-5П
Морфология поверхности TiOF 2 , TiO 2 -HNBs и ZnTCP @ TiO 2 -HNBs были идентифицированы по изображениям SEM, показанным на рис. 2. Рисунок 2a состоит из однородного и полностью кубического TiOF 2 в соответствии с изображениями ПЭМ. Как показано на рис. 2b, изображения TiO 2 -HNBs показали морфологию полых коробок правильной формы, полученную из шаблона TiOF 2 кубы в процедуре топологического преобразования и окружены шестью упорядоченными TiO 2 массивы нанолистов. Как показано на рис. 2c – f, все ZnTCP @ TiO 2 Образцы -HNBs также показали полностью полые коробчатые структуры с волосатыми щупальцами из порфирина Zn (II), покрывающими поверхность нанобоксов, что хорошо согласуется с результатами ПЭМ, предполагая успешный процесс топологического преобразования с одним горшком из кубического TiOF 2 в TiO 2 полые нанобоксы с участием ZnTCP in situ.

СЭМ-изображения готовых катализаторов: а TiOF 2 , b TiO 2 -HNBs, c Т-1п, д Т-2п, э Т-3п и ф Т-5П
Как показано на рис. 3, вероятный механизм образования сенсибилизированного Zn (II) -порфирином 3D TiO 2 полые нанобоксы (ZnTCP @ TiO 2 -HNBs) был предложен в процессе топологического преобразования с участием шаблона. Этанол обеспечивает мягкие условия реакции за счет использования растворителя, реакция дегидратации которого (уравнение 1, основное) и сложноэфирная реакция между ZnTCP и этанолом (уравнение 2) дает H 2 O и способствовал гидролизу кубического TiOF 2 , который может топологически трансформироваться в анатаз TiO 2 полые коробчатые нанокристаллы во время сольвотермической реакции (уравнение 3). Поскольку адсорбция F - ион на поверхности TiO 2 нанокристаллы могут резко снизить поверхностную энергию граней (001), фторид-ионы способствуют образованию высокоэнергетического анатаза TiO 2 нанолистов, и понятно, что предшественник TiOF 2 может превращаться в TiO 2 сборка полых нанобоксов шестью упорядоченными нанолистами с обнаженными высокоэнергетическими гранями (001). Периферическая тетракарбоксильная группа ZnTCP образует сильную сложноэфирную связь, объединенную с носителем TiO 2 -HNBs (уравнение 4).
$$ {\ displaystyle \ begin {array} {l} {\ mathrm {TiO} \ mathrm {F}} _ 2 + 2 {\ mathrm {CH}} _ 3 {\ mathrm {CH}} _ 2 \ mathrm {O} \ mathrm {H} \ circledR {\ mathrm {TiO}} _ 2 + 2 \ mathrm {HF} +2 \ mathrm {CH} ={\ mathrm {CH}} _ 2 \ left ({\ mathrm {CH}} _ 3 {\ mathrm {CH}} _ 2 {\ mathrm {OCH}} _ 2 {\ mathrm {CH}} _ 3 \ right) \\ {} \ mathrm {cohol} \; \ overset {\ mathrm {dehydration}} {\ to} \; \ mathrm {alkene} \ \ left (\ mathrm {ester} \ right) + {\ mathrm {H}} _ 2 \ mathrm {O} \ end {array}} $$ (1) $$ \ mathrm {Zn} \ left (\ mathrm {II} \ right) \ hbox {-} \ mathrm {порфирин} \ hbox {-} \ mathrm {COOH} + {\ mathrm {CH}} _ 3 {\ mathrm {CH}} _ 2 \ mathrm {O} \ mathrm {H} \ circledR \ mathrm {Zn} \ left (\ mathrm {II} \ right) \ hbox {-} \ mathrm {порфирин} \ hbox {-} {\ mathrm {COOCH}} _ 2 { \ mathrm {CH}} _ 3 + {\ mathrm {H}} _ 2 \ mathrm {O} $$ (2) $$ {\ mathrm {TiO} \ mathrm {F}} _ 2 + {\ mathrm {H}} _ 2 \ mathrm {O} ={\ mathrm {TiO}} _ 2 \ left (\ mathrm {anatase} \ \ mathrm {crystal} \ right) +2 \ mathrm {HF} \ left (\ mathrm {in} \ \ mathrm {situtransformation} \ right) $$ (3) $$ \ mathrm {Zn} \ lef t (\ mathrm {II} \ right) \ hbox {-} \ mathrm {porphyrin} \ hbox {-} \ mathrm {CO} \ mathrm {OH} + {\ mathrm {TiO}} _ 2 \ hbox {-} \ mathrm {O} \ mathrm {H} =\ mathrm {Zn} \ left (\ mathrm {II} \ right) \ hbox {-} \ mathrm {порфирин} \ hbox {-} \ mathrm {CO} \ hbox {- } \ mathrm {O} \ hbox {-} {\ mathrm {TiO}} _ 2 $$ (4)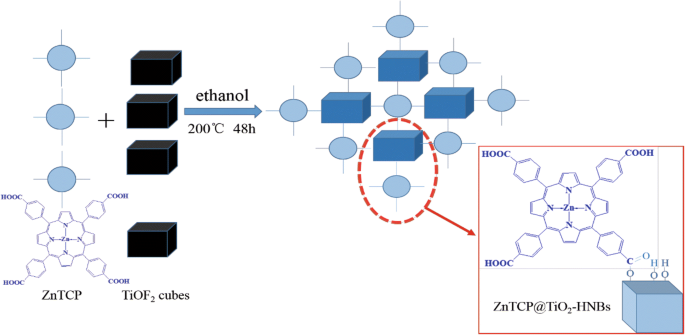
Предлагаемый процесс образования TiO 2 , сенсибилизированного порфирином Zn (II) -HNB (ZnTCP @ TiO 2 -HNBs)
XRD-анализ
Хорошо известно, что кристаллические плоскости TiO 2 катализаторы на основе катализаторов играют очень важную роль в их фотокаталитических свойствах. На рис. 4 показан анализ рентгенограмм всех образцов, как только они были приготовлены. Глядя на кривую относительно TiOF 2 предшественник, {100}, {200} и {210} кристаллические плоскости TiOF 2 соответствует 2 θ =24,05 °, 48,34 ° и 54,45 ° четко наблюдались. Для всех TiO 2 образцов, широкий пик при 2 θ =25,37 °, что соответствует {101} плоской дифракции анатаза TiO 2 (JCPDS № 21–1272), отличная от 24,05 °, что связано с дифракционным пиком TiOF 2 , указывает, что все образцы успешно завершили процесс топотактического преобразования с TiOF 2 как шаблон [40]. Из-за F - ионов в качестве агента контроля формы, рутила TiO 2 не было паттерны, сформированные в процессе синтеза. По сравнению с TiO 2 -HNB (T0p), дифракционные пики около {101} и {200} кристаллической поверхности TiO 2 , сенсибилизированного порфирином Zn (II) - образцы ГНБ становятся более острыми, что подразумевает более высокую степень кристаллизации, что объясняется тем фактом, что увеличение количества порфирина Zn (II) привело к увеличению концентрации сложноэфирных химических связей между TiO 2 поверхностная гидроксильная группа и периферическая тетракарбоксильная группа ZnTCP. Другие характерные дифракционные пики TiO 2 образцы на рентгенограммах не демонстрировали каких-либо сдвигов или изменений формы пиков, что указывает на то, что модификация и сенсибилизация ZnTCP не меняют кристаллическую структуру TiO 2 -HNBs.
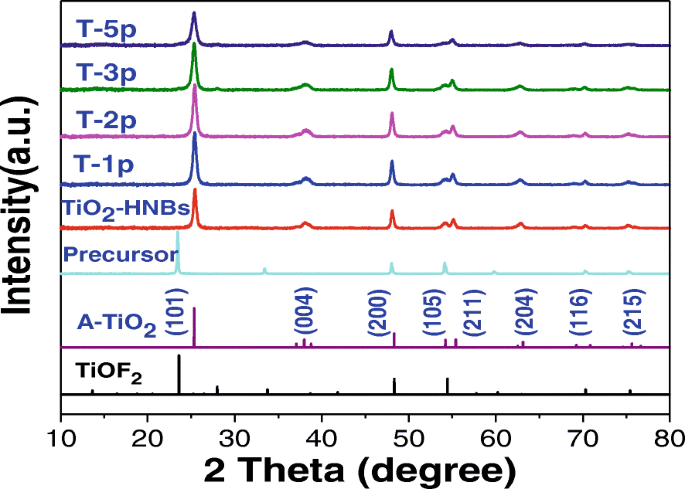
Рентгенограммы образцов в свежеприготовленном виде
Для дальнейшего исследования размеров кристаллитов ZnTCP @ TiO 2 -HNBs, уравнение Шеррера использовалось на основе их дифракционного пика {101} [41, 42]. Как описано в таблице 1, все образцы показали средний размер частиц около 260 нм согласно структурному анализу, что хорошо согласуется с измерениями SEM и TEM. Однако « d ”Пробел ZnTCP @ TiO 2 Образцы HNB не увеличились по сравнению с TiO 2 -HNBs, подразумевая размер элементарной ячейки свежеприготовленного ZnTCP @ TiO 2 -HNBs катализатор вряд ли изменится во время процедуры, сенсибилизированной порфирином Zn (II).
УФ-видимая спектроскопия
На рис. 5 показан УФ-видимый спектр раствора ZnTCP в 5 × 10 −4 раствор ДМФА (моль / л) (а) и спектроскопия диффузного отражения в УФ-видимой области (DRS) ZnTCP @ TiO 2 -HNBs образцы и BaSO 4 использовался как эталонный образец (б). As Fig. 5a displayed, the strong 432 nm absorption peak was ascribed to the characteristic B-band absorption of porphyrin rings, whereas weaker 561 nm and 600 nm peaks in the visible region were attributed to the characteristic Q-band absorption of ZnTCP, implying the successful synthesis of porphyrin ring. Compared to Fig. 5a, the Q-band absorption peaks of ZnTCP was red-shifted to 660 nm into the longer wavelength visible region after sensitization to TiO2 . Because there is a presented strong interaction force between zinc porphyrins and TiO2 -HNBs after hydrothermal reaction, which provides favorable prerequisites for the degradation of organic dyes under the visible-light irradiation. It can be found that TiO2 -HNBs displayed less absorption above its fundamental absorption edge (> 400 nm), while Zn(II) porphyrin-sensitized TiO2 samples displayed an obvious broad visible-light absorbance, as described in Fig. 5b, and the absorption intensities of ZnTCP@TiO2 -HNBs samples were gradually enhancing much stronger as Zn(II) porphyrin amount increased. In addition, the color of as-prepared samples become deepened gradually from white to blue purple with the increasing of mass ratio of ZnTCP/TiO2 -HNBs, and it was widely accepted that the purple coloration cause Zn(II) porphyrin-sensitized samples resulted into enhanced visible-light absorption. To further investigate the bandgap in each sample, the energy gap (eV) threshold was obtained using the transversal method, and the graph of the transformed Kubelka-Munk function against the photon energy for samples T-2p and TiO2 -HNBs are displayed in Fig. 5c. According to the transformed Kubelka-Munk function plot, the energy gaps of E г (T-2p) и E г (TiO2-HNBs) are 2.83 and 3.08 eV, respectively. The reduced bandgap arises because ZnTCP can form a local energy state between the valence and conduction bands as ZnTCP concentration increases, which reduce the forbidden band width and the electron transition energy. Meanwhile, we find that the ZnTCP self-doped samples also exhibit very strong UV absorption, which indicates ZnTCP self-doping not only enhances the visible-light response of the catalysts, but also improves their UV light absorption. Thus, it can be predicted that more photo-generated electrons and holes can be excited and can participate in photocatalytic reactions, which is attributed to the increased probabilities of activation by UV and visible light.
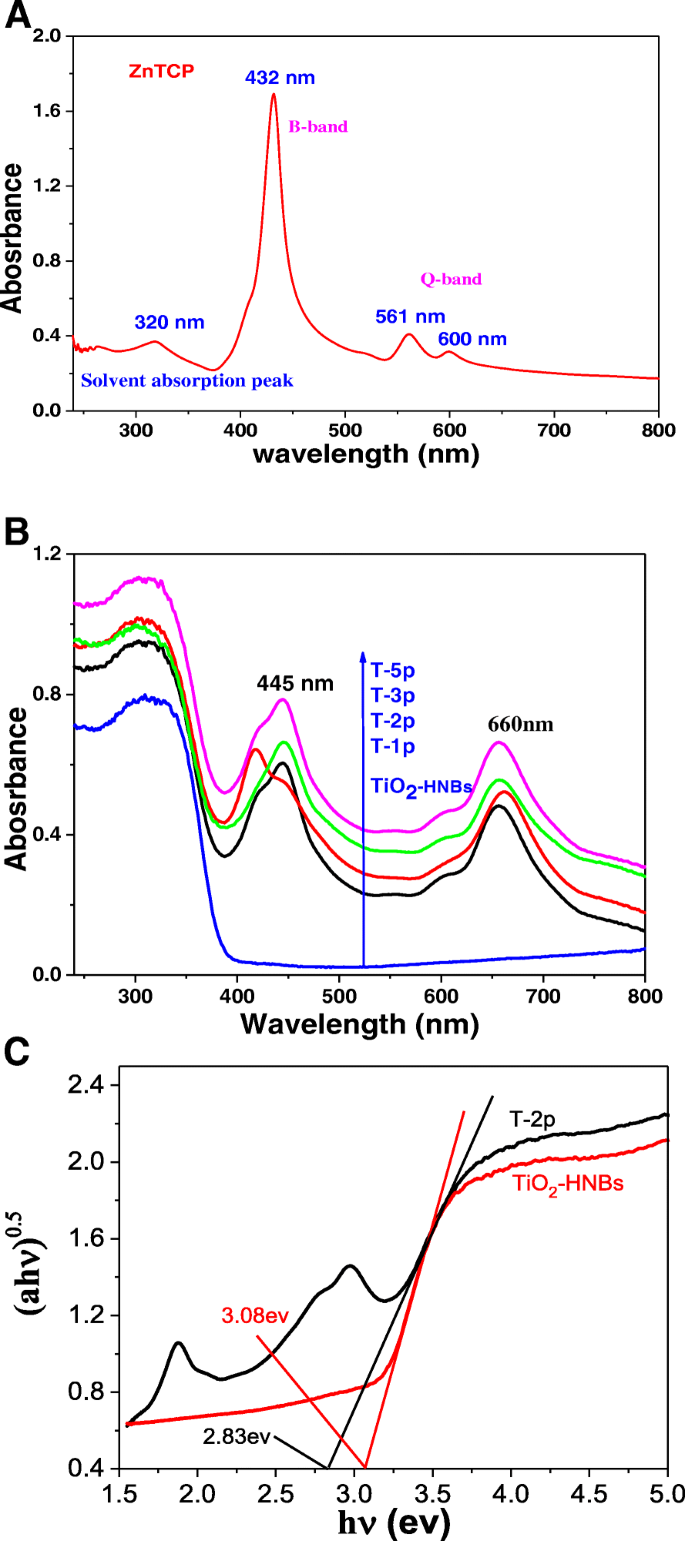
а UV-Vis spectra of ZnTCP in 5×10 −4 mol/L DMF solution. б UV-vis diffuse reflectance spectra (DRS) of all the samples. ( c ) Estimated optical absorption edges for the T-2p and TiO2-HNBs
FT-IR Spectra Analysis
FT-IR spectra analysis is a powerful tool to identify characteristic functional groups [43]. Figure 6 displays the FT-IR spectra of ZnTCP, TiO2 -HNBs, and T-2p. Looking at the spectra relative to ZnTCP, the broad band at 3443 cm −1 is assigned to the stretching vibration of the -OH in the peripheral t carboxyl groups, the characteristic absorption peak of C=O at 1720 cm −1 . The stretching vibration of Ar-H bond is clearly observed at 2995 cm −1 . Furthermore, the spectra of ZnTCP show the characteristic absorption peak of benzene ring at 1620 and 1469 cm −1 relative to ZnTCP [44].
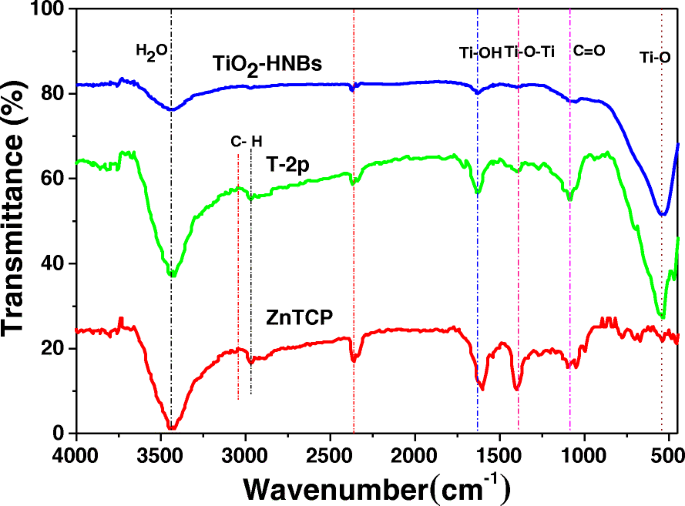
FT-IR spectra of TiO2 -HNBs, ZnTCP, and T-2p sample
Seeing from the spectra relative to TiO2 -HNBs, the stretching vibration and bending vibration of the absorption H2 O and Ti–OH group on the surface of samples were found about 3446 cm −1 and 1627 cm −1 , соответственно. The stretching vibration of Ti-O-Ti is observed at 1388 cm −1 , and the adsorption peaks around 521 cm −1 is assigned to the bending vibrations of Ti-O bond.
Compared to ZnTCP and TiO2 -HNBs, the T-2p spectra features the characteristic stretching/bending vibration of the Ar-H bond at 2996 cm −1 and 1386 cm −1 attributed to Ti-O-Ti bond. Furthermore, the spectra of T-2p shows the characteristic absorption peak of phenyl ring at 1621 and 1468 cm − 1 corresponding to ZnTCP, indicating the existence of ZnTCP on the surface of sensitized TiO2 [44]. However, the signal corresponding to -OH vibration peak disappeared, which demonstrates the formation of ester chemical bond between ZnTCP and TiO2 . The stretching vibration of the C=O bond of ester group is clearly observed at 1713 cm −1 [45], further confirmed ZnTCP combined to TiO2 -HNBs composites. The above information indicates that the TiO2 -HNBs surface has been successfully functionalized with ZnTCP molecules. After sensitization, the spectra of T-2p show an increased intensity of the stretching vibration peak at 520 cm −1 and the characteristic absorption bands in the region of 1200~1060 cm −1 attributed to the CO-O-Ti bond resulting from the esterification between COOH of ZnTCP and OH of TiO2 [46]. This reveals that the strong interaction (conjugated chemical bonds) between ZnTCP and TiO2 -HNBs was established rather than simple physical adsorption. The results displayed on FT-IR spectra were in accordance with the photocatalytic performance of these catalysts, suggesting that the strong conjugated chemical bonds between ZnTCP and TiO2 greatly contribute to the improvement of the photocatalytic activity as a transferring electrons bridge.
XPS Analysis
To further investigate chemical environments of as-prepared catalysts, the X-ray photoelectron spectra (XPS) measurements of TiO2 -HNBs and T-2p were carried out [43]. As shown in full spectra of Fig. 7a, two elements including Ti and O were both observed at the corresponding positions, respectively. Figure 7b–f displayed the high-resolution XPS spectra of the corresponding element of two samples.
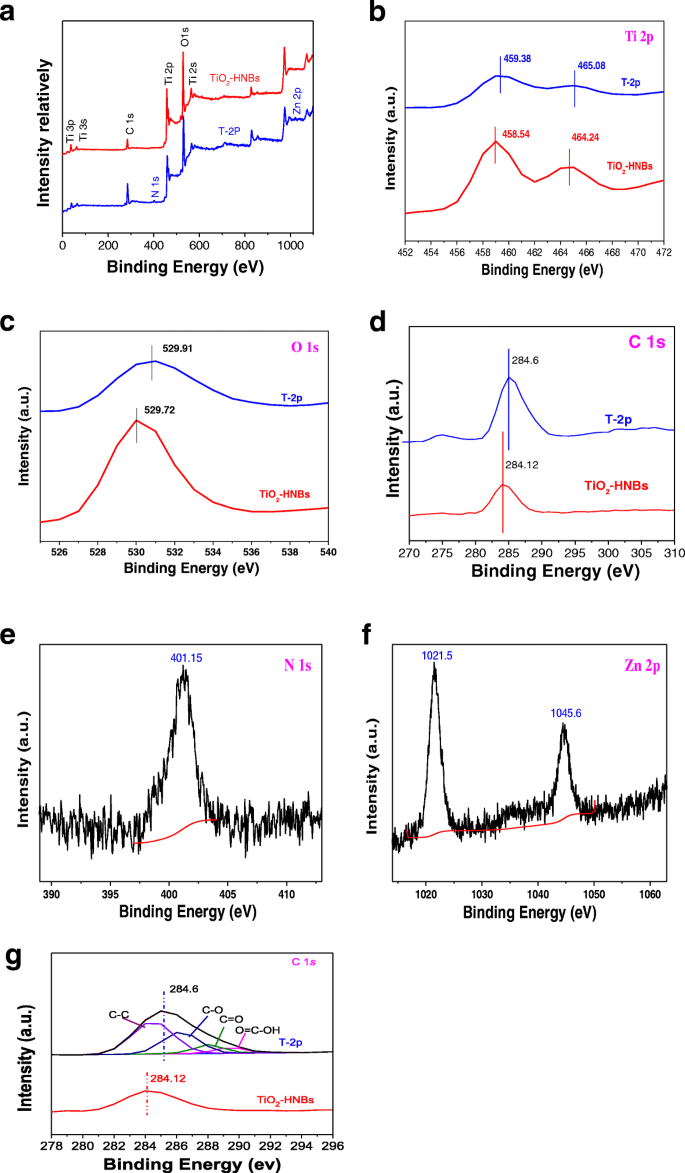
а The full spectra of all kinds of elements in sample TiO2 -HNBs and T-2p; б the high-resolution Ti 2p XPS signals of TiO2 -HNBs and T-2p; c the O1s XPS signals of TiO2 -HNBs and T-2p; г the C1s O1s XPS signals of TiO2 -HNBs and T-2p; е the N1s XPS signals of T-2p; е the Zn 2p XPS signals of T-2p; г the C XPS-peak-differentation-imitating analysis
The high-resolution Ti 2p XPS signals of TiO2 -HNBs in Fig. 7b consisted of two binding energy levels of Ti 2p1/2 и 2р 3/2 at 464.24 and 458.54 eV with a separation energy of about 5.70 eV. However, the binding energy levels of Ti 2p1/2 и 2р 3/2 XPS peaks of T-2p exhibited at 465.08 and 459.38 eV, which shift 0.84 eV toward the lower energy region compared to TiO2 , indicative of a partial charge transferred from the surface C=O ester moiety to Ti 4+ centers, which was probably due to the strong interactions between ZnTCP molecules and TiO2 .
As shown in Fig. 7c, the O1s XPS signals of TiO2 -HNBs and T-2p displayed at 529.72 and 529.91 eV respectively, with a deviation energy of nearly 0.19 eV. The shifting of lattice oxygen peaks in T-2p toward lower energy, compared to TiO2 standard, further verified the different chemical environment due to ZnTCP sensitization. As displayed in Fig. 7d, the C 1s of T-2p appeared the distinct peaks at 284.6 eV, which were ascribed to C=O (and COO) bonds in the peripheral tetracarboxyl group, further confirmed that ZnTCP was well bonded on the surface of TiO2 . It was found that the weak peak at 401.15 eV of T-2p in Fig. 7e was attributed to N1s of the N=N- bond in the porphyrin ring. The Zn 2p binding energy signals of T-2p appeared at 1021.5 eV and 1044.46 eV in Fig. 7f, which are basically consistent with the complex molecular structure of ZnTCP, further implying it well impregnated onto the surface of TiO2 . Figure 7g shows the XPS spectra of C 1s region for samples. In Fig. 7g, the peak with a binding energy of 284.6 eV can be attributed to the C–C bonds, while the deconvoluted peaks centered at the binding energies of 286.5, 288.3, and 289.6 eV can be assigned to the C–O, C=O, and O=C–OH functional groups, respectively. C 1s spectra for the ZnTCP@TiO2 -HNBs composite are shown in Fig. 7. In the spectrum of ZnTCP@TiO2 -HNBs, all peaks from oxygen-containing functional groups decreased dramatically in intensity or even disappeared entirely, indicating a significant reduction of GO by solvothermal treatment. In addition, an additional shoulder peak was found, which was usually assigned to the formation of a chemical bond between a carbon atom and a titanium atom in the lattice of TiO2 -HNBs, which resulted information of Ti–O–C bonds.
Photocatalytic Activity of ZnTCP@TiO2 -HNBs Catalysts
The photocatalytic activity of ZnTCP@TiO2 -HNBs was evaluated by measuring the degradation with RhB as a probe molecule. Figure 8a exhibits the degradation curve of RhB under simulated sun light conditions with as-prepared ZnTCP@TiO2 -HNBs catalysts. It is clearly observed that, after the adsorption-desorption equilibrium process, the self-degradation of probe molecule RhB can be negligible and the visible-light degradation activities of ZnTCP-sensitized TiO2 -HNBs samples indicates much higher photocatalytic efficiencies than TiO2 -HNBs and ZnTCP under visible-light irradiation (λ ≥ 420 nm), which depends on the concentration of RhB versus visible-light irradiation time. The T-2p sample shows highest photocatalytic activity with RhB degradation rate of 99% after 2 h under visible-light irradiation, resulting from its enhanced visible-light response. However, the TiO2 -HNBs (T-0p) shows little decomposition rate of RhB under the same reaction conditions. In this process, the order of degradation rate is T-2p> T-3p> T-1p> T-5p> ZnTCP>TiO2 -HNBs.
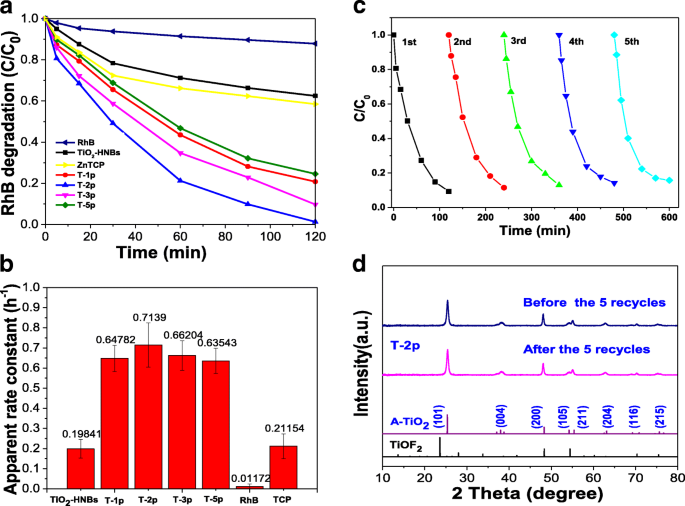
а The C t /C0 vs. time curves of RhB photodegradation under visible-light irradiation. б The apparent first-order rate constant of RhB photodegradation. c Cyclic degradation curve of T-2p. г The XRD before and after recycles of T-2p
It is well accepted that the slopes for the curve of RhB intensity versus illumination time (rate constant) represent the photodegradation activity of the samples. Therefore, the exponential curve of the degradation RhB under visible-light irradiation was fitted in Fig. 8b, and the degradation kinetics of RhB was described by the first-order kinetics curves. Degradation experiments followed the first-order kinetic equation ln(C0 -C) = − Kt + b (in which K is the apparent first-order rate constant and t is the reaction time). By comparing the rate constants (K values) of ZnTCP-sensitized TiO2 -HNBs catalysts, we can see that the rate constants of these catalysts increase first and then decrease with the ZnTCP/TiO2 -HNBs mass ratio increase. Observed from the rate constants histogram (Fig. 8b), we can find that T-2p reveals the highest visible-light photocatalytic activity (rate constant of 0.7139), which is 3.6 times higher than that of TiO2 -HNBs (T-0p) (rate constant of 0.19841); furthermore, the photocatalytic rate constants of other ZnTCP@TiO2 -HNBs samples are basically larger than that of TiO2 -HNBs.
The possible reasons is that may be because ZnTCP-sensitized TiO2 -HNBs can extend the absorption wavelength range of TiO2 -based catalysts, reducing the bandgap of TiO2 , and facilitate the effective separation of the electron-hole pairs generated by TiO2 -HNBs after absorbing visible light, thereby improving the utilization of electron-hole pairs. However, too much ZnTCP-sensitized parts may result in the increase of defects on the surface of TiO2 -based catalyst, resulting in a rapid recombination center of photogenerated electrons and holes, thereby decreasing the photocatalytic activity.
In order to investigate the long-term stability of as-prepared ZnTCP@TiO2 -HNBs, the photocatalysts were recycled after each photocatalytic degradation experiment and then were reused in the next run after washing treatment. Figure 8c shows sample T-2p were recycled to 5 rounds after bleaching RhB under visible-light irradiation; as the number of photodegradation cycles increased, the photocatalytic rate of RhB still maintained a high catalytic activity, indicating that the active site of ZnTCP@TiO2 -HNBs surface did not decrease, and the composite photocatalyst has good photocatalytic stability under visible-light irradiation. The strong bridging ester bond-linking leads to a slower decrease of the degradation efficiency for sample T-2p. These results further demonstrate that ZnTCP can establish a steady chemical bridging bond-linking interaction between ZnTCP and TiO2 -HNBs, thus enhancing the visible-light photocatalytic performance, stability, and recyclability of ZnTCP@TiO2 -HNBs. XRD shows that the T-2p is still anatase type and did not change the crystal type after many cycles, further verifying the stability of the catalyst (Fig. 8d).
PL Analysis
In order to study the active species generated during photocatalytic degradation, the coumarin, 4-chloro-7-nitrobenzo-2-oxa-1,3-diazole (NBD-Cl), and 1,3-diphenylisobenzofuran (DPBF) were used as the hydroxyl radical (•OH), superoxide radical (•O2 - ), and singlet oxygen ( 1 О 2 ) fluorescent probe molecules, respectively. Figure 9a displays the active species of hydroxyl radical detection map with T-2p as photocatalyst. As shown in Fig. 9a, the fluorescence emission wavelength was centered at 450 nm and the fluorescence intensity gradually increased, indicating the concentration of •OH group was increasing with the increase of illumination time. The reason is due to the fact that the continuously generated •OH active group and coumarin react to obtain 7-hydroxycoumarin, the amount of the reaction is gradually increased, and the fluorescence intensity is gradually increased [44, 45].
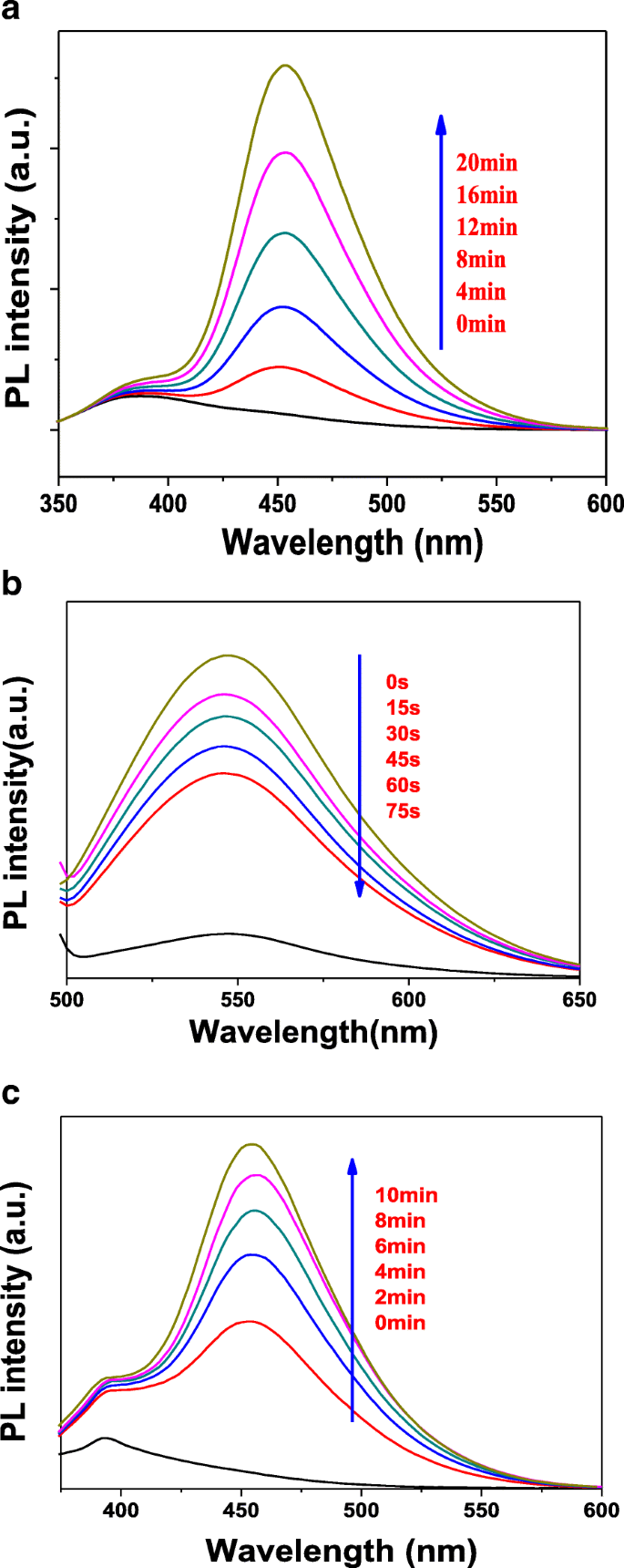
Fluorescent detection of active species •OH (a ), •O2 - ( б ), and 1 О 2 ( c ) with T-2p as photocatalyst
It is well accepted that quantification of superoxide ion concentration can be monitored its reaction with 4-chloro-7-nitrobenzo-2-oxa-1,3-diazole (NBD-Cl) by measuring its fluorescence emission intensity at 550 nm using an excitation wavelength of 470 nm. According to Fig. 9b, it can be found that the fluorescence emission wavelength was centered 550 nm and the fluorescence intensity gradually decreased with the increase of illumination time. In the presence of NBD-Cl, the degradation rate is not obviously increased. The results indicate that •OH radical is hardly generated, while •O2 - is the significant active species generated in the system. More e − can react with O2 to form superoxide radical •O2 - instead of the rapid recombination with h + , which further improves the photodegradation activity and testifies the catalyst can generate the active species •O2 - .
In addition, a typical fluorescence method for detecting singlet oxygen ( 1 О 2 ,) by using 1,3-diphenylisobenzofuran (DPBF) as a probe molecule is proposed, which exhibited a strong fluorescence spectrum with a maximum at 455 nm when excited at 410 nm. As shown in Fig. 9c, the fluorescence emission wavelength was centered 455 nm and the fluorescence intensity gradually increased with the increase of illumination time. Based on the above observation, it can be concluded that the photocatalyst produces a certain amount of singlet oxygen in the light condition. To sum up, the ZnTCP@TiO2 -HNBs catalyst can generate •OH, •O2 - , and 1 О 2 active species during the photodegradation process under visible-light irradiation.
Electrochemical Analysis
To attain more insights into photocatalytic transformation for oxidation degradation organic pollutants, the electrochemical properties of ZnTCP and ZnTCP@TiO2 -HNBs (T-2p) in DMF were investigated with cyclic voltammetry (CV) on a glassy carbon electrode using tetrabutylammonium perchlorate as supporting electrolyte. It can be clearly seen that two complete oxidation and reductions processes for ZnTCP observed from the potential window are shown with blue dashed lines in Fig. 10. Furthermore, ZnTCP@TiO2 -HNBs (T-2p) distinctly displayed similar two oxidation processes resulted from the ZnTCP center with red dashed lines [39]. The oxidation-reduction electrochemical behavior of ZnTCP complexes mainly occurred on the porphyrins ring and did not involve the change in the valence state of the central metal ions, which were good agreement with our previous reported [47]. However, the oxidation degradation reaction of ZnTCP@TiO2 -HNBs (T-2p) was very similar as that of ZnTCP, which indicated the photocatalytic transformation mainly happened on the porphyrin ring, not relative to the center zinc ion and TiO2 -HNBs. These results further confirm that the strong interaction, such as conjugated ester chemical bonds between TiO2 -HNBs and ZnTCP, was established rather than simple physical adsorption interaction.
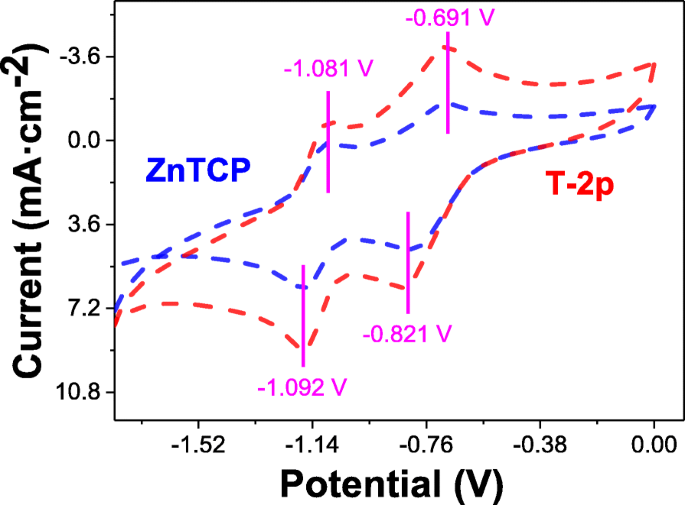
Cyclic voltammetry analysis of 1.0 × 10 −3 mol dm −3 of ZnTCP and T-2p on Pt in 0.1 mol dm −3 TBAP/DMF vs. SCE. Scan rate:0.1 V s −1
Proposed Probable Photocatalytic Mechanism
Much effort has been devoted to illustrate the photocatalytic mechanism for oxidation degradation organic pollutants. In order to speculate the photodegradation mechanism, the main oxidative species in the photocatalytic process was firstly detected through radical and hole trapping experiments by using EDTA (hole h + scavenger), p -benzoquinone (BZQ, superoxide radical •O2 - scavenger), iso -propyl alcohol (IPA, hydroxyl radical •OH scavenger) and 1,3-diphenylisobenzofuran (DPBF, singlet oxygen 1 О 2 scavenger). Figure 11 shows the Ct/C0 vs. time curves of different reactive species scavengers on the photodegradation of RhB under visible-light irradiation.
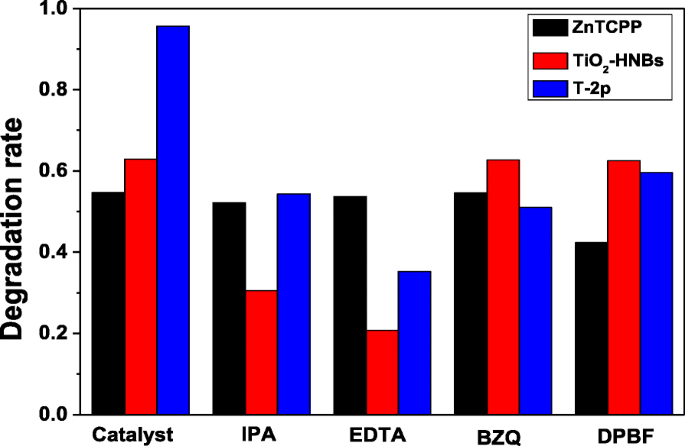
The C t /C0 vs. time curves of different reactive species scavengers on the photodegradation of RhB under visible-light irradiation
As displayed in Fig. 11, the photocatalytic degradation of RhB was apparently restrained after the injection of the active species scavenger. Taking the decreasing photodegradation rate into consideration, it can be found that RhB degradation rate with ZnTCP as a photocatalyst mainly depended on active species of 1 О 2 group according to the 1,3-diphenylisobenzofuran (DPBF) detection results. Furthermore, RhB photodegradation rate with TiO2 -HNBs as catalysts mostly depended on active species of h + and •OH group. However, it is very clear that RhB photodegradation rate with ZnTCP@TiO2 -HNBs (T-2p) as catalysts was influenced by all active species of hole (h + ), hydroxyl radical (•OH), superoxide radical (•O2 - ), and singlet oxygen ( 1 О 2 ), further confirming ZnTCP@TiO2 -HNBs (T-2p) can generate these active species during the photodegradation process.
The probable photodegradation mechanism of organic dyes with ZnTCP-sensitized TiO2 -HNBs as catalysts under visible-light irradiation is shown in Fig. 12. The degradation process generally consists of three moieties. The first part mainly involves the generation of singlet oxygen ( 1 О 2 ). When irradiated by simulated sunlight, the inspired electrons of ZnTCP are transferred from the ground state of porphyrin [Pp] to the excited singlet state 1 [Pp]* [47], and then, relaxation of the singlet excited state generates the triplet excited state 3 [Pp]* through a process of intersystem crossing. Electrons from 1 [Pp]* and 3 [Pp]* excited states are trapped by the adsorbed O2 to form singlet oxygen ( 1 О 2 ), which can cause RhB degradation into pieces of small organic molecule or mineralization to CO2 .
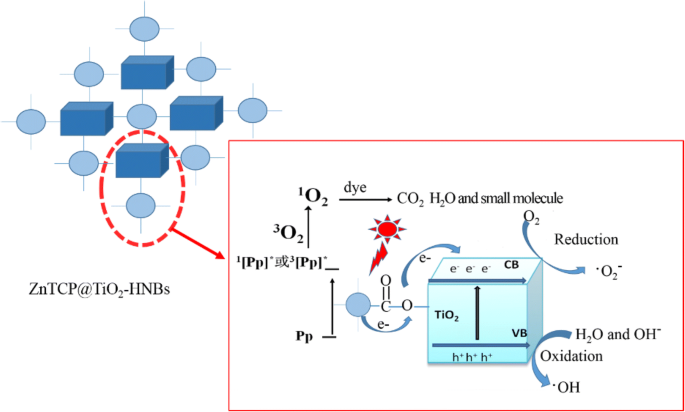
Proposed probable photocatalytic mechanism of ZnTCP@TiO2 -HNBs
In contract, superoxide radical (•O2 - ) can be generated in the second moiety. Biomimetic catalytic moiety of ZnTCP is not only responsible to generate singlet oxygen ( 1 О 2 ), but also acts as electron bridges from 1 [Pp]* and 3 [Pp]* excited states transferred to conduction band (CB) of TiO2 -HNBs, which can be trapped further by the adsorbed O2 , resulting in formation of an amount of •O2 - causing photodegradation of RhB present on the surface of TiO2 -HNBs.
On the other hand, in the sensitization of porphyrins, the electrons of TiO2 are excited from valence band (VB) to conduction band (CB) forming electron-hole pairs (e − -h + ) during the visible-light irradiation [48, 49]. The photogenerated holes transfer to the surface of TiO2 reacted with H2 O or OH − , resulting in formation of hydroxyl radical (•OH). The photogenerated electrons are transferred to the surface of TiO2 trapped by the adsorbed oxygen molecule, obtained an amount of superoxide radical (•O2 - ), and these active species (•O2 - , •OH) mainly implement the degradation of organic dyes by its successive formation of intermediaries participated.
Thus, overall, a cooperative mechanism is proposed for the degradation of organic dyes involving three components of photocatalytic system. The enhanced visible-light photodegradation activities of Zn(II)TCP@TiO2 -HNBs compared to ZnTCP and TiO2 -HNBs might be related to synergetic generation of three active species (•O2 - , •OH, and 1 О 2 ), resulting in more higher efficient photocatalytic activities.
Conclusions
A facile one-step solvothermal treatment via a topotactic transformation process was employed to synthesize a series of visible-light-driven biomimetic photocatalysts based on ZnTCP-sensitized TiO2 hollow nanoboxes assembled by six ordered nanosheets with high-energy {001} facets dominant exposure. ZnTCP played an important role in formation ester bonds to construct 3D hollow nanoboxes and transfer photogenerated electrons to sensitize TiO2 -HNBs for enhancing visible-light response. Due to synergistic visible photodegradation mechanism of biomimetic catalyst, which can produce not only hydroxyl radical (•OH) and hyperoxygen radical (•O2 - ) from TiO2 , but also singlet oxygen ( 1 О 2 ) generated by biomimetic enzyme porphyrin, the photocatalytic degradation RhB rate constants of ZnTCP@TiO2 -HNBs (T-2p) were greatly enhanced with a degradation yield of 99%, much larger (3.6 time) than TiO2 -HNBs under visible-light irradiation. This novel approach is expected to provide a perfect reference for perfect dye-sensitized method to synergistically fabricate other surface modification TiO2 -based composites, which is of great value with promising application for purifying domestic sewage.
Сокращения
- 3D:
-
Трехмерный
- Резюме:
-
Циклическая вольтамперометрия
- DRS:
-
UV-vis diffuse reflectance spectroscopy
- IR:
-
Infrared spectra
- PL:
-
Фотолюминесценция
- SEM:
-
Сканирующий электронный микроскоп
- ТЕМ:
-
Просвечивающий электронный микроскоп
- TiO2 -HNBs:
-
TiO 2 hollow nanoboxes
- UV-vis:
-
UV-vis spectroscopy
- XPS:
-
Рентгеновская фотоэлектронная спектроскопия
- XRD:
-
Рентгеновская дифракция
- ZnTCP:
-
Zinc(II) meso -tetra(4-carboxyphenyl)porphyrinato
- ZnTCP@TiO2 -HNBs:
-
Zinc(II) meso -tetra(4-carboxyphenyl)porphyrinato-sensitized TiO2 hollow nanoboxes
Наноматериалы
- Нановолокна и нити для улучшенной доставки лекарств
- Наножидкости TiO2 - Часть 1:Приготовление и свойства
- Легкий синтез и оптические свойства малых нанокристаллов и наностержней селена
- Синтез зеленого цвета в одной емкости микросферы SnO2, украшенной серебром:эффективный и многоразовый катализ…
- Простой синтез окрашенного и проводящего композита CuSCN, покрытого наночастицами CuS
- Простой синтез серебряных нанопроволок с разным соотношением сторон и используемых в качестве высокоэффект…
- Гидротермальный синтез наночастиц In2O3, гибридные двойники, гексагональные дисковые гетероструктуры ZnO для по…
- Легкий синтез червоточиноподобного мезопористого оксида олова за счет самосборки, вызванной испарением, и у…
- Синтез нанопластин Cu2ZnSnSe4 в одном резервуаре и их фотокаталитическая активность, управляемая видимым светом
- Экологичный и простой синтез нанопроволок Co3O4 и их перспективное применение с графеном в литий-ионных батаре…



