Простой синтез поверхностно-функционализированных магнитных нанокомпозитов для эффективной селективной адсорбции катионных красителей
Аннотация
Новый магнитный наноадсорбент, модифицированный поликатехином Fe 3 О 4 магнитные наночастицы (Fe 3 О 4 / PCC MNP) были получены простым методом химического соосаждения с использованием солей железа и раствора катехина в качестве предшественников. Fe 3 О 4 / PCC МНЧ обладают отрицательно заряженной поверхностью с кислородсодержащими группами и демонстрируют высокую адсорбционную способность и высокую скорость адсорбции для удаления катионных красителей в воде. Адсорбционная способность метиленового синего (MB), катионного бирюзового синего GB (GB), малахитового зеленого (MG), кристаллического фиолетового (CV) и катионного розового FG (FG) составляла 60,06 мг г - 1 , 70,97 мг г - 1 , 66,84 мг г - 1 , 66,01 мг г - 1 и 50,27 мг г - 1 , соответственно. Механизм адсорбции был предложен на основе анализа изотерм адсорбции и кинетики адсорбции катионных красителей на Fe 3 О 4 / ПКК МНП. Кроме того, были исследованы катионные красители, адсорбированные на МНЧ в зависимости от времени контакта, значения pH, температуры, сосуществующих катионных ионов и ионной силы. Эти результаты свидетельствуют о том, что Fe 3 О 4 / PCC MNPs перспективно использовать в качестве магнитного адсорбента для селективной адсорбции катионных красителей при очистке сточных вод.
Фон
Неорганические и органические отходы, образующиеся в результате деятельности человека, привели к образованию больших объемов загрязненных вод, которые угрожают здоровью людей и других живых организмов [1]. Загрязнение воды на сегодняшний день является одной из самых серьезных экологических проблем, тормозящих развитие человеческого общества [2, 3]. В частности, загрязняющие красители вызывают широкую озабоченность общественности из-за их высокой видимости и токсического воздействия на биологические организмы и экологию [4]. Органические красители широко используются в различных отраслях, таких как текстильная, бумажная, полиграфическая, цветная фотография, фармацевтическая промышленность, кожевенная, косметическая, пластиковая и другие отрасли промышленности, которые являются основными источниками промышленных сточных вод [5]. Количество сточных вод от красителей чрезвычайно велико, как правило, объем сточных вод, сбрасываемых на каждом этапе текстильной операции, составляет примерно от 40 до 65 л / кг продукта [6]. Кроме того, красители - это небиоразлагаемые вещества, которые остаются стабильными в различных условиях из-за своего синтетического происхождения и сложной ароматической структуры [7]. Поэтому необходимо выбрать подходящий метод удаления красителей из сточных вод перед сбросом в окружающую среду.
В последние годы для очистки сточных вод от красителей использовались различные методы, включая фотокаталитическую деградацию [8], коагуляцию [9], электрохимические процессы [10], химическое окисление [11], мембранную фильтрацию [12], биологическую очистку [13]. и адсорбция [14]. Среди этих методов очистки сточных вод от красителей широко используется адсорбция благодаря их простоте, высокой эффективности и экономичности [15, 16]. Сообщалось, что многие адсорбенты, такие как активированный уголь, каолин, монтмориллонитовая глина, отработанный красный шлам, земля для долбления и обожженная глина, обесцвечивают сточные воды [17, 18]. В частности, магнитные наночастицы (МНЧ) привлекли значительное внимание в качестве адсорбирующих материалов для органических красителей и тяжелых металлов из-за их уникальных магнитных свойств, низкой стоимости, биосовместимости, легко синтезируемых, легко перерабатываемых, особенно экономичных и экологически чистых [19]. Было разработано несколько методов синтеза магнитного Fe 3 . О 4 наночастицы, в том числе i) соосаждение водного раствора двухвалентного и трехвалентного железа в присутствии основания [20]; б) термическое разложение комплекса железа [21]; iii) сонохимический подход [22].
Из-за их высокой поверхностной энергии и собственных магнитных взаимодействий, легкое агрегирование Fe 3 О 4 МНЧ могут снизить соотношение поверхность / объем и стабильность дисперсии в водном растворе [23]. Стабилизаторы, такие как поверхностно-активные вещества, носители, оксиды или полимерные соединения, были использованы для модификации Fe 3 О 4 MNP для повышения их стабильности и улучшения их дисперсности. Zhang et al. синтезированный магнитный Fe 3 О 4 / C ядро и оболочка наночастиц и используются в качестве абсорбентов, обладающих хорошей адсорбционной способностью для удаления красителей [24]. Wang et al. подготовленный Fe 3 О 4 наночастицы с помощником цетилтриметиламмонийбромида (CTAB) для адсорбционного удаления конго красного (CR) и метиленового синего (MB) [25]. Кроме того, адсорбционная способность чистого Fe 3 О 4 МНП недостаточно сильны.
Для улучшения адсорбционных свойств поверхностная функционализация Fe 3 О 4 MNP были изучены. Zhang et al. модифицированный Fe 3 О 4 МНЧ с 3-глицидоксипропилтриметоксисиланом (GPTMS) и глицином (Gly), магнитные нанокомпозиты, могут превосходно удалять как анионные, так и катионные красители в суровых условиях (сильнокислой или сильнощелочной) [26]. Более того, избирательная адсорбция может быть значительно улучшена для обогащения загрязняющих веществ за счет введения большого количества активных центров. Пурджавади и др. сообщили о новом функционализированном магнитном нанокомпозите из полиметилакрилата для эффективного удаления анионных красителей из водных сред [27]. Поликатехол, образующийся в результате полимеризации катехола, катализируемой Fe (III) [28,29,30], был использован для модификации поверхности в качестве адгезивов и покрытий для широкого спектра как органических, так и неорганических материалов из-за их уникальных термических и структурных свойств. , а также способность образовывать стабильные комплексы с оксидами металлов [31, 32]. Это означает, что Fe 3 О 4 МНЧ, модифицированные поликатехолом, значительно увеличивают адсорбционную способность Fe 3 О 4 MNP. Однако сообщений о модифицированном поликатехолом Fe 3 нет. О 4 МНЧ, безусловно, являются абсорбентом для удаления красителей.
В этой работе поликатехол модифицировал Fe 3 О 4 МНЧ (Fe 3 О 4 / PCC MNP) были получены простым методом соосаждения и использовались в качестве адсорбентов для удаления красителя. Абсорбент охарактеризовали с использованием петель магнитного гистерезиса, термогравиметрического анализа и анализа дзета-потенциала. Пять видов катионных красителей, включая метиленовый синий (MB), катионный бирюзовый синий GB (GB), малахитовый зеленый (MG), кристаллический фиолетовый (CV) и катионный розовый FG (FG), были выбраны в качестве модельных соединений для выявления адсорбции. поведение Fe 3 О 4 / ПКК МНП. Также были исследованы кинетика адсорбции, изотермический анализ и влияние различных экспериментальных условий на удаление катионных красителей.
Методы
Материалы
Хлорид железа (FeCl 3 · 6H 2 O), сульфат железа (FeSO 4 · 7H 2 O), гидроксид аммония (NH 3 · H 2 O, 25%), MB, GB, MG, CV, FG, Orange ΙΙ, фуксин, метиловый оранжевый (MO) и катехол были получены от Chuandong Chemical Inc., Chengdu, Sichuan, China. Все химические вещества были аналитической чистоты и использовались без дополнительной очистки, а все растворы и суспензии были приготовлены на деионизированной воде. Структуры пяти катионных красителей, включая MB, GB, MG, CV и FG, показаны на рис. 1.
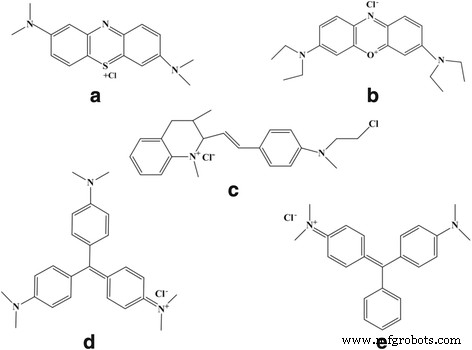
Молекулярные структуры ( a ) МБ ( b ) ГБ ( c ) MG ( d ) CV ( e ) FG. Как показано на рис. 1, описана структура пяти видов катионных красителей
Получение и характеристика Fe 3 О 4 / PCC MNPs
Fe 3 О 4 / PCC MNP были получены простым методом химического соосаждения с использованием солей железа и катехинов в качестве прекурсоров [23]. Весь процесс синтеза проводился при окружающей атмосфере. Вкратце, FeCl 3 · 6H 2 O (10 ммоль) и FeSO 4 · 7H 2 O (5 ммоль) растворяли в 75 мл деионизированной воды, затем достаточно смешивали с 75 мл катехола (20 мМ). Когда катехол был смешан с раствором железа (pH 2,87), полимеризация катехола, катализируемая Fe 3+ Произошло образование поликатехола, который представлял собой крупные крупные осадки черного цвета [30]. Одновременно Fe 3+ ионы химически адсорбируются на поликатехоле в результате комплексообразования и служат предшественниками зародышеобразования. Смесь выдерживали в течение 30 минут, а затем быстро добавляли к 100 мл гидроксида аммония (3,3 М), выдерживая в течение 120 минут при интенсивном перемешивании. Магнитные наночастицы in situ росли с образованием агрегатов на поверхности поликатехиновых цепочек. Пары Fe 3 О 4 Цепи / PCC плотно соединяются друг с другом с образованием Fe 3 О 4 / ПКК МНП. Все процессы синтеза проводились в окружающей атмосфере, без какой-либо защитной атмосферы. Черные магнитные наночастицы отделяли внешним магнитом, промывали деионизированной водой до нейтрального значения pH и сушили в вакуумной печи при 50 ° C в течение 24 часов. Fe 3 О 4 МНЧ были синтезированы теми же процедурами, что и упомянутые выше, без добавления катехола. Все продукты хранили в эксикаторе при температуре окружающей среды для дальнейших экспериментов.
Магнитные свойства измеряли при комнатной температуре в системе измерения магнитных свойств (MPMS XL-7, Quantum Design, America). Термогравиметрический анализ (ТГА) проводили для порошковых образцов с использованием термогравиметрического анализатора (ТГА) TGA / DSC 1 (Mettler-Toledo, Швейцария) под N 2 окружающей среды при скорости нагрева 5 ° C мин - 1 . Дзета-потенциалы суспензий катализаторов при различных значениях pH определяли с помощью Malvern 3000 Zetasizer.
Эксперименты по периодической адсорбции
Эксперименты по изотерме сорбции проводили встряхиванием 25 мг Fe 3 О 4 / PCC МНЧ в 25 мл раствора с различными адсорбатами, с начальной концентрацией адсорбата от 0,02 мМ до 0,4 мМ. Смесь непрерывно встряхивали на шейкере со скоростью 180 об / мин при контролируемой температуре 30 ° C до достижения равновесия. PH раствора регулировали, используя 1,0 M H 2 . SO 4 или 1,0 М растворы NaOH. После адсорбции адсорбент отделяли от раствора под действием магнетизма, а затем измеряли надосадочную жидкость при максимальном поглощении каждого красителя с помощью УФ-видимого спектрофотометра.
Кроме того, была изучена адсорбционная кинетика процессов. 100 мг Fe 3 О 4 / PCC МНЧ суспендировали в 100 мл 0,1 мМ растворов адсорбатов, а затем встряхивали при 180 об / мин при pH 6,0 и 30 ° C. Через разные интервалы времени отбирали 0,5 мл образца суспензии и сразу же разделяли с помощью внешнего магнетизма, а надосадочную жидкость собирали для анализа.
Также было изучено влияние значения pH и температуры на адсорбцию катионных красителей. Типичный эксперимент по периодической адсорбции проводили следующим образом:50,0 мг Fe 3 О 4 / PCC МНЧ диспергировали в 50,0 мл раствора катионных красителей, а затем встряхивали на шейкере со скоростью 180 об / мин.
Все эксперименты по адсорбции проводили в двух экземплярах. Адсорбционная способность каждого красителя в адсорбционной системе, q e , был рассчитан по формуле. (1):
$$ {q} _e =\ left ({C} _i- {C} _e \ right) \ V / {M} _s $$ (1)Где q e (мг г - 1 ) - адсорбционная способность, C e (мМ) - равновесная концентрация в водной фазе, Ci (мМ) - начальная концентрация водной фазы, V (L) - объем раствора, а M s (г) - масса твердого адсорбента.
Результаты и обсуждение
Характеристика Fe 3 О 4 / PCC MNPs
На рис. 2а показаны петли магнитного гистерезиса, определенные при комнатной температуре для Fe 3 . О 4 и Fe 3 О 4 / ПКК МНП. Значения намагниченности насыщения Fe 3 О 4 / PCC MNP были 53,5 emu g - 1 , выше, чем у Fe 3 О 4 (49,6 эму г - 1 ), предполагая, что они могут быть легко разделены внешним магнитным полем [33]. Размер частиц, явление спинового скоса, размерный эффект и другие факторы связаны с намагниченностью насыщения наночастиц феррита [34]. Модификация поликатехола делает Fe 3 О 4 / PCC МНЧ с более высокой степенью кристаллизации и меньшим размером частиц, чем Fe 3 О 4 МНЧ, которые могут привести к более высокой намагниченности насыщения Fe 3 О 4 / PCC МНЧ, чем Fe 3 О 4 MNP. Кроме того, более высокая намагниченность насыщения приготовленного Fe 3 О 4 / PCC MNP также можно отнести к поверхностному эффекту, который иногда называют «мертвой поверхностью». Мертвая поверхность связана с беспорядком поверхностного вращения [35].
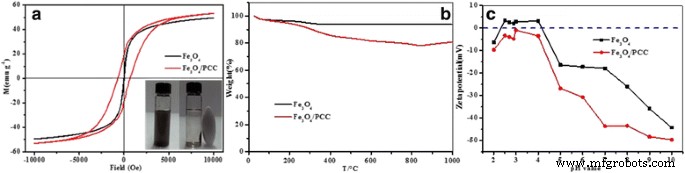
а Поведение намагничивания Fe 3 О 4 МНЧ и Fe 3 О 4 / ПКК МНЧ при комнатной температуре. б Кривые термогравиметрии (ТГА) Fe 3 О 4 МНЧ и Fe 3 О 4 / ПКК МНП. c дзета-потенциалы Fe 3 О 4 Магнитные наночастицы PCC. На рис. 2 пустые линии представляют природу Fe 3 . О 4 MNP, а красные линии - от имени собственности Fe 3 О 4 / PCC MNPs
Температурное поведение Fe 3 О 4 и Fe 3 О 4 / PCC МНЧ были дополнительно исследованы с помощью термогравиметрического анализа (ТГА) (рис. 2b). Для кривой ТГА Fe 3 О 4 У MNP потеря веса (6,5%) ниже 150 ° C была связана с потерей физически адсорбированной воды. Для кривой Fe 3 О 4 / PCC MNP, потеря веса (5,2%) ниже 150 ° C была связана с потерей физически адсорбированной воды, потеря веса (9,4%) от 150 ° C до 400 ° C была приписана потере кислородсодержащего функционального элемента. групп, потеря веса (6,8%) от 400 ° C до 800 ° C была в основном связана с сжиганием углерода, а небольшое увеличение веса (2,3%) при температуре выше 800 ° C было связано с окислением Fe 3 О 4 к γ-Fe 2 О 3 [36]. Fe 3 О 4 / PCC МНЧ показали более низкую термическую стабильность, чем Fe 3 . О 4 , за счет модификации поликатехола [37].
На рисунке 2c показаны дзета-потенциалы Fe 3 . О 4 и Fe 3 О 4 / Суспензии ПКК при различных значениях pH. Как показано на рис. 2c, изоэлектрическая точка Fe 3 О 4 составляла 4,2, а поверхность Fe 3 О 4 / PCC МНЧ обладают отрицательными зарядами в диапазоне pH 3,0–10,0, что может быть связано с электроотрицательностью фенольной гидроксильной группы в поликатехине. Кроме того, поверхностная плотность заряда Fe 3 О 4 / PCC МНЧ увеличивались при увеличении pH с 3,0 до 10,0. Отрицательные заряды Fe 3 О 4 / PCC MNPs также предотвращают агломерацию наночастиц.
Селективная адсорбция Fe 3 О 4 / PCC MNPs
Адсорбционные свойства Fe 3 О 4 / PCC МНЧ по отношению к катионным красителям, анионным красителям и фенолу из водного раствора были подробно исследованы. На рисунке 3 показаны эффективности удаления МБ как разновидности катионного красителя, МО как разновидности анионного красителя и фенола, адсорбированного на Fe 3 . О 4 / ПКК МНП. Было замечено, что эффективность удаления МБ составила 75,7%. Однако эффективность удаления MO составила только 10,9%, а эффективность удаления фенола - только 1,5%. Результаты показали, что Fe 3 О 4 / PCC МНЧ селективно адсорбируют катионный краситель из-за электростатического взаимодействия (рис. 2c).
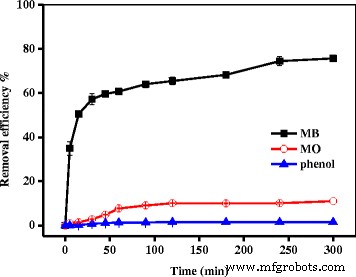
Эффективность удаления МБ, МО и телефона, адсорбированного Fe 3 О 4 / ПКК МНП. Как показано на рис. 3, пустая линия представляет эффективность удаления MB, красная линия представляет удаление MO, а синяя линия представляет удаление phonel
Кинетика адсорбции катионных красителей
Кинетика адсорбции пяти катионных красителей на Fe 3 О 4 / PCC МНЧ были исследованы с использованием двух кинетических моделей, а именно модели псевдопервого порядка и модели псевдовторого порядка (рис. 3). В кинетической модели псевдопервого порядка константа скорости адсорбции красителей выражается как [38]:
$$ Ln \ left ({q} _e- {q} _t \ right) =\ mathit {\ ln} \ left ({q} _e \ right) \ hbox {-} {k} _1 \ t $$ ( 2)где q e и q т - количество адсорбированных красителей (мг г - 1 ) в состоянии равновесия и в любой момент времени t (мин) соответственно и k 1 - константа скорости адсорбции псевдопервого порядка (мин - 1 ).
Кинетическая модель псевдо-второго порядка описывается формулой [39]:
$$ t / {q} _t =1 / {k} _ {ad} \ {q_e} ^ 2 + 1 / {q} _e $$ (3)Где q e и q т представляют собой, соответственно, количество красителей, адсорбированных в момент равновесия, и время t (мг г - 1 ); и k объявление - константа скорости псевдо-второго порядка для процесса адсорбции (мг г - 1 мин - 1 ). Значения параметров для каждой модели были рассчитаны методом линейных наименьших квадратов, а коэффициенты корреляции представлены в таблице 1. Результаты показали, что вся кинетика адсорбции этих пяти катионных красителей на Fe 3 О 4 / PCC MNPs могут быть хорошо описаны моделью кинетики псевдо-второго порядка с высоким коэффициентом корреляции (R 2 > 0,997) и константы скорости ( k объявление ) были рассчитаны до 0,043, 0,047, 0,051, 0,057, 0,052 г мг - 1 мл - 1 , соответствующие MB, GB, MG, CV и FG соответственно (рис. 4 и таблица 1). Кроме того, адсорбционная способность МБ по Fe 3 О 4 / PCC MNP были значительно улучшены по сравнению с Fe 3 О 4 MNP (дополнительный файл 1:рисунок S1). Основной причиной было электростатическое притяжение между положительным зарядом катионных красителей и отрицательным зарядом Fe 3 О 4 / PCC MNPs.
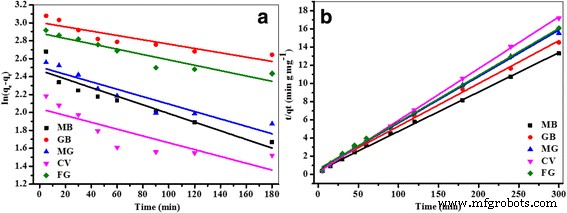
Адсорбция катионных красителей на Fe 3 О 4 / PCC MNP ( a ) кинетика псевдо-второго порядка ( b ) кинетика псевдопервого порядка. Как показано на рис. 4, пустая линия представляет адсорбцию MB, красная линия представляет адсорбцию GB, синяя линия представляет адсорбцию MG, пурпурная линия представляет адсорбцию CV, а оливковая линия представляет адсорбцию. ФГ
Изотермы адсорбции различных катионных красителей
Изотерма адсорбции сыграла значительную роль в оценке адсорбционных свойств Fe 3 О 4 / ПКК МНЧ [40]. Для подробного описания процесса адсорбции были применены два хорошо известных уравнения изотермы, уравнения Ленгмюра и Фрейндлиха (уравнения (4) и (5)) [41].
Уравнение Ленгмюра:
$$ {C} _e / {q} _e ={C} _e / {q} _m + 1 / {K} _L \ {q} _m $$ (4)где q e (мг г - 1 ) - равновесная адсорбционная способность красителя на адсорбенте; C e (мг л - 1 ) - равновесная концентрация красителя в растворе; q м (мг г - 1 ) максимальная емкость адсорбента; и K L (L мг - 1 ), постоянная Ленгмюра.
Уравнение Фрейндлиха:
$$ {q} _e ={K} _F \ {C_e} ^ {1 / n} $$ (5)Где q e и C e определены как такие же, как указано выше; К F (L мг - 1 ) - постоянная Фрейндлиха; а n - коэффициент неоднородности.
На рис. 5 показаны изотермы адсорбции катионных красителей на Fe 3 . О 4 / ПКК МНП. Результаты показали, что адсорбция пяти катионных красителей лучше соответствовала уравнению Ленгмюра, чем уравнению Фрейндлиха, в соответствии с коэффициентами корреляции. Максимальная адсорбционная способность ( q м ) для этих красителей были рассчитаны по уравнению Ленгмюра, которые перечислены в таблице 2. q м для катионных красителей:MB, GB, MG, CV и FG были 60,06, 70,97, 66,84, 66,01 и 50,27 мг г - 1 , соответственно. В подобранной модели Ленгмюра предполагается, что один загрязнитель связан с одним участком на адсорбенте и что все участки поверхности на адсорбенте имеют одинаковое сродство к загрязнителю и не взаимодействуют между собой [42].
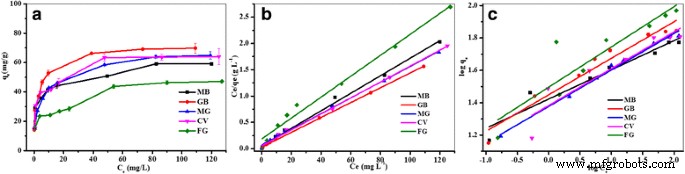
а Изотермы адсорбции катионных красителей на Fe 3 О 4 / PCC MNP ( b ) Ленгмюра и ( c ) Модели изотермы адсорбции Фрейндлиха органических красителей по Fe 3 О 4 / ПКК МНП. Как показано на рис. 5, пустая линия представляет адсорбцию MB, красная линия представляет адсорбцию GB, синяя линия представляет адсорбцию MG, пурпурная линия представляет адсорбцию CV, а оливковая линия отражает адсорбцию. адсорбция ФГ
Влияние температуры на адсорбцию катионных красителей
Влияние температуры на адсорбцию катионных красителей показано на рис. 6. Как видно, эффективность удаления МБ возрастает с повышением температуры (30–45 ° C) и достигает 84% при 45 ° C. , что предполагает, что адсорбция МБ на Fe 3 О 4 / PCC был эндотермическим процессом. В то время как эффективность удаления GB и CV снижалась с повышением температуры, что свидетельствует об экзотермической реакции адсорбции GB и CV, что указывает на то, что процессы сорбции были в основном физической адсорбцией. Кроме того, температура реакции мало влияла на адсорбцию WG и FG. Влияние температуры реакции на адсорбцию пяти катионных красителей было различным, в основном из-за разной структуры красителей и дырки МНЧ. Когда отверстия в МНЧ слишком малы, чтобы попасть в них, молекулам адсорбата приходится преодолевать высокий барьер, чтобы попасть в отверстие. Поскольку отверстия маленькие и диффузия заблокирована, процесс адсорбции более нестабилен, что приводит к более высокой энергии и эндотермическому процессу. В противном случае процесс будет экзотермическим.
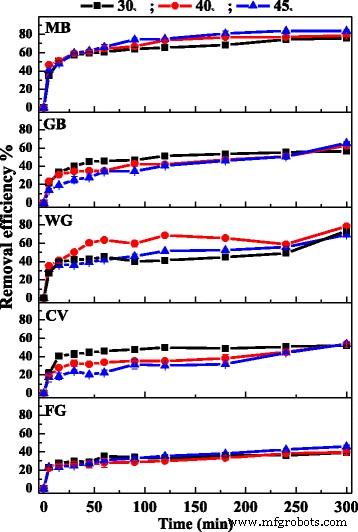
Влияние температуры на адсорбцию катионных красителей на Fe 3 О 4 / ПКК МНП. Как показано на рис. 6, пустая линия означает, что температура составляет 30 ° C, красная линия означает, что температура составляет 40 ° C, а синяя линия означает, что температура составляет 45 ° C.
Влияние pH на адсорбцию катионных красителей
PH водного раствора был важным фактором, влияющим на процесс адсорбции красителя, поскольку он влиял на поверхностный заряд адсорбента и поведение ионизации как адсорбента, так и красителя [43]. Влияние pH на удаление катионных красителей изучали при концентрации красителя 0,1 мМ при 30 ° C и значениях pH от 3,0 до 9,0. Как показано на рис. 7, эффективность удаления катионных красителей возрастает с увеличением значения pH. Поскольку Fe 3 О 4 / PCC МНЧ обладали отрицательным зарядом, и их поверхностная плотность заряда увеличивалась с увеличением pH (рис. 2c), катионные красители адсорбировались на Fe 3 О 4 / PCC МНЧ за счет электростатического притяжения между положительным зарядом молекул катионных красителей и отрицательным зарядом Fe 3 О 4 / ПКК МНП. По мере увеличения pH электростатическое притяжение между отрицательно заряженной поверхностью Fe 3 О 4 / Композит PCC и молекула катионных красителей увеличиваются, что приводит к увеличению адсорбционной способности катионных красителей. Следовательно, повышенный pH помог удалить катионные красители с помощью Fe 3 О 4 / PCC MNPs.
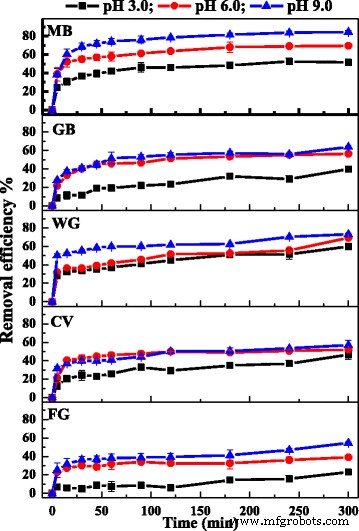
Влияние начального pH на удаление катионных красителей на Fe 3 О 4 / ПКК МНП температура 30 ° С. Как показано на рис. 7, пустая линия означает, что pH раствора равен 3,0, красная линия означает, что pH раствора равен 6,0, а синяя линия означает, что pH раствора равен 9,0
Влияние сосуществующих катионов на адсорбцию МБ
Стоки красителя всегда содержали большое количество сосуществующих ионов, которые могли повлиять на процесс адсорбции красителя [4]. В этом исследовании три обычно сосуществующие соли:NaCl, MgSO 4 и FeCl 3 были выбраны для изучения влияния сосуществующих катионов и их ионной силы на адсорбцию МБ на Fe 3 О 4 / PCC МНЧ с результатами, представленными на рис. 8. Как видно, Na + , Mg 2+ и Fe 3+ вся адсорбция МБ подавлена из-за конкуренции адсорбции между катионами и МБ на адсорбционных центрах Fe 3 О 4 / ПКК МНП. Более того, эффективность удаления МБ снизилась с 63% до 20% с Fe 3+ . концентрация увеличивается с 0,1 мМ до 0,5 мМ. О такой конкурентной адсорбции широко сообщалось в литературе [44]. Результаты дополнительно подтвердили электростатическую адсорбцию МБ на Fe 3 . О 4 / PCC MNPs.
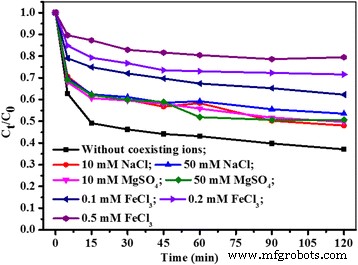
Влияние сосуществующих катионов и ионной силы на адсорбцию МБ на Fe 3 О 4 / ПКК МНП. Как показано на рис. 8, пустая линия представляет адсорбцию МБ без каких-либо сосуществующих ионов, красная линия отражает влияние на адсорбцию МБ с помощью 10 мМ NaCl, синяя линия отражает влияние на адсорбцию МБ с помощью 50 мМ NaCl, пурпурная линия отражает влияние на адсорбцию МБ с помощью 50 мМ NaCl. линия показывает влияние на адсорбцию МБ с 10 мМ MgSO 4 оливковая линия отражает влияние на адсорбцию МБ с помощью 50 мМ MgSO 4 , темно-синяя линия отражает влияние на адсорбцию МБ с 0,1 мМ FeCl 3 фиолетовой линией показано влияние на адсорбцию МБ 0,2 мМ FeCl 3 фиолетовая линия отражает влияние на адсорбцию МБ 0,1 мМ FeCl 3
Утилизация адсорбента
После адсорбции Fe 3 О 4 / PCC МНЧ можно регенерировать десорбцией этанолом при pH 4,0 в течение 12 ч и промыть деионизированной водой до нейтрального состояния. Fe 3 О 4 / PCC MNP можно было регенерировать и повторно использовать пять раз. На рисунке 9 показаны адсорбционные характеристики регенерированного Fe 3 . О 4 / ПКК МНЧ для катионных красителей. Эффективность удаления катионных красителей постепенно снижалась от первого цикла адсорбции-десорбции до пятого цикла. На шестом цикле эффективность удаления MB, GB, MG, CV и FG резко снизилась до 27%, 23%, 37%, 43% и 39% соответственно. Примечательно, что присутствие магнитных наночастиц способствовало разделению и извлечению адсорбента. Это указывает на то, что Fe 3 О 4 / PCC MNPs имеет определенную экономическую целесообразность.
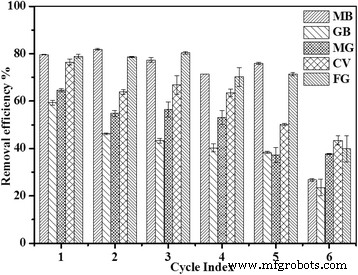
Гистограмма эффективности удаления катионных красителей Fe 3 О 4 / PCC МНЧ адсорбция ([Fe 3 О 4 / PCC] =1,0 г л - 1 , [красители] 0 =0,1 мМ, pH 6,0, t =300 мин)
Заключение
В заключение, новый магнитный наноадсорбент (Fe 3 О 4 / PCC MNPs) были успешно получены с активными адсорбционными центрами для удаления катионных красителей из водного раствора. Введение поликатехола в структуру Fe 3 О 4 / PCC MNP обладают удивительными преимуществами, включая предотвращение агломерации наночастиц и улучшение адсорбционных свойств MNP. Установлено, что электростатическое взаимодействие является основной силой адсорбционного поведения катионных красителей. Процесс адсорбции хорошо описывался кинетикой псевдо-второго порядка и моделями изотермы Ленгмюра соответственно. Результаты показали, что Fe 3 О 4 / МНЧ PCC продемонстрировали потенциальное применение для удаления катионных красителей из промышленных стоков.
Сокращения
- CR:
-
Конго красный
- CTAB:
-
Бромид цетилтриметиламмония
- Fe 3 О 4 / PCC:
-
Fe 3 О 4 / поликатехол
- Gly:
-
Глицин
- GPTMS:
-
3-глицидоксипропилтриметоксисилан
- МБ:
-
Метиленовый синий
- MNP:
-
Магнитные наночастицы
- PCC:
-
Поликатехол
- TGA:
-
Термогравиметрический анализ
Наноматериалы
- Красители для текстиля
- Наноалмазы для магнитных датчиков
- Достижения и проблемы флуоресцентных наноматериалов для синтеза и биомедицинских приложений
- Легкий синтез и оптические свойства малых нанокристаллов и наностержней селена
- Простой синтез гетероструктурированных WS2 / Bi2MoO6 как высокоэффективных фотокатализаторов, управляемых видим…
- Простой синтез наночастиц SiO2 @ C, закрепленных на MWNT, в качестве высокоэффективных анодных материалов для лити…
- Углеродные наноточки как двухрежимные нанодатчики для селективного обнаружения перекиси водорода
- Исследования сорбции ионов тяжелых металлов с использованием нанокомпозитов из модифицированного железом б…
- Метод последующей обработки для синтеза монодисперсных бинарных наночастиц FePt-Fe3O4
- Магнитные поли (N-изопропилакриламид) нанокомпозиты:влияние метода получения на антибактериальные свойства



