Сравнение функционализации магнитных наночастиц Fe3O4 на основе фолиевой кислоты и пептида gH625 для усиления интернализации клеток
Аннотация
Универсальный синтетический маршрут на основе магнитного Fe 3 О 4 Префункционализация наночастиц (MNP) монослоем фосфоновой кислоты была использована для ковалентного связывания пептида gH625 на поверхности наночастиц. gH625 представляет собой мембранотропный пептид, способный легко проходить через мембраны различных клеток, включая типичные компоненты гематоэнцефалического барьера человека. Аналогичный путь синтеза был использован для получения другого класса МНЧ, имеющих функциональное покрытие на основе PEG, родамина и фолиевой кислоты, хорошо известной молекулы-мишени, для сравнения эффективности двух систем, проникающих в клетки (например, gH625 и фолиевой кислоты). кислота). Наши результаты демонстрируют, что поглощение GH625-декорированных MNPs иммортализованными эндотелиальными клетками микрососудов человеческого мозга через 24 часа более очевидно по сравнению с MNPs, функционализированными фолиевой кислотой, что подтверждается конфокальной лазерной сканирующей микроскопией. С другой стороны, оказалось, что обе функционализированные системы способны интернализоваться в линии опухолевых клеток головного мозга (то есть в глиобластоме A-172). Эти результаты показывают, что функционализация MNP с gH625 улучшает интернализацию их эндотелиальных клеток, предлагая жизнеспособную стратегию создания функциональных наноструктур, способных сначала пересекать ГЭБ, а затем достигать определенных опухолевых клеток мозга.
Фон
Гематоэнцефалический барьер (ГЭБ) - это динамический интерфейс между кровью и мозгом, который играет решающую роль в поддержании гомеостаза центральной нервной системы (ЦНС). Основными компонентами ГЭБ являются эндотелиальные клетки (то есть астроциты и перициты), которые образуют непрерывный слой, покрывающий внутреннюю поверхность микрососудов головного мозга. Они связаны между собой плотными контактами, которые имеют решающее значение как для контроля проницаемости сосудов ГЭБ [1], так и для защиты мозга от различных циркулирующих токсинов и других вредных молекул [2, 3]. Нейроны и микроглия, которые являются другими компонентами сосудисто-нервных единиц, играют иную роль в ГЭБ [4, 5].
Из-за сплошного слоя эндотелиальных клеток 98% низкомолекулярных лекарств и 100% крупномолекулярных лекарств не проходят через ГЭБ, таким образом не доставляя лекарства в ткань мозга [6]. Таким образом, чтобы разработать эффективные системы доставки для лечения многих заболеваний головного мозга, крайне важно изучить способность носителей проникать через ГЭБ [7].
В последнее десятилетие системы на основе наночастиц широко изучались как эффективные терапевтические агенты для нацеливания и терапии рака. В этом контексте органические функционализированные магнитные наночастицы железа (МНЧ) вызвали большой интерес, поскольку они сочетают в себе универсальность функционализации поверхности с магнитными свойствами и нетоксичной биосовместимой природой их ядра. МНЧ широко используются для тераностических применений (диагностических и терапевтических), таких как сортировка и манипуляции с белками и клетками [8, 9], маркировка клеток [10, 11], магнитно-контролируемая доставка лекарств [12, 13], магнитно-резонансная томография (МРТ). [14, 15] и гипертермия [16,17,18,19]. Чтобы их можно было эффективно использовать в биомедицинских целях, МНЧ должны быть способны пересекать клеточные мембраны и, в частности, проходить через различные биологические барьеры. Модификация поверхности МНЧ функциональными молекулами часто используется для улучшения их интернализации в клетках, но во многих случаях пересечение ГЭБ остается проблемой.
В этом контексте можно увидеть использование проникающих в клетку пептидов (CPP), группы относительно коротких пептидов (5-40 аминокислот), происходящих либо из природных источников, либо из синтетически сконструированных конструкций, которые могут легко проходить через бислой мембраны. как перспективный подход. Среди множества доступных CPP пептид gH625, состоящий из 20 остатков, полученный из гликопротеина H (gH) вируса простого герпеса 1, был недавно разработан и использован для пересечения ГЭБ с целью увеличения поглощения различных грузов [20, 21] в цитозоль.
В настоящем исследовании МНЧ были функционализированы двумя различными классами нацеленных покрытий на основе связующего слоя 3-аминопропилфосфоновой кислоты (NH 2 -ПА). Два покрытия были получены путем подключения к NH 2 -PA-модифицированные МНЧ (NH 2 @MNPs) либо пептид, проникающий в клетки gH625 (gH625 @ MNPs), либо молекулы PEG и фолиевой кислоты (PEG, FA @ MNPs). В частности, введение фолиевой кислоты (FA) в ПЭГилированные наночастицы направлено на улучшение клеточного поглощения опухолевыми клетками посредством интернализации, опосредованной рецептором FA [22], и биосовместимости всей наносистемы [23]. Влияние двух поверхностных покрытий на внутриклеточное поглощение МНЧ первичными эндотелиальными клетками микрососудов головного мозга человека (HBMEC) оценивали с помощью конфокальной лазерной сканирующей микроскопии. С этой целью в обе системы были включены люминесцентные зонды. В частности, gH625 был помечен зондом 4-хлор-7-нитробенз-2-окса-1,3-диазола (NBD), в то время как карбокси- X -родамин (род) зонд был добавлен к оболочке PEG, FA @ MNPs.
Изучение внутриклеточного поглощения МНЧ, модифицированных gH625, эндотелиальными клетками и их сравнение с МНЧ, модифицированными FA, насколько нам известно, никогда раньше не проводилось.
Помимо способности пересекать ГЭБ, нацеливание на опухолевые клетки головного мозга является еще одним важным требованием для терапевтических агентов против опухолей головного мозга. Следовательно, также оценивалась клеточная интернализация двух МНЧ с различным покрытием в одной из наиболее распространенных злокачественных глиом человека, глиобластоме A-172.
Обратите внимание, что хотя наночастицы железа с функционализированным gH625 были недавно получены Perillo et al. [24], в настоящей работе мы сообщаем о другой стратегии синтеза, основанной на универсальной платформе фосфоновой кислоты. В частности, химия фосфоновой кислоты позволяет образовывать прочные связи между МНЧ и фосфоновыми монослоями, стабильность которых сопоставима со стабильностью силанизированных МНЧ. Более того, поскольку самоконденсация P-O-P незначительна, использование фосфоновых линкеров преодолевает недостатки образования олигомеров, которые часто встречаются при использовании силанов [25].
Методы
Материалы
Все реагенты, используемые для синтеза и функционализации МНЧ, FeCl 2 · 4H 2 O, FeCl 3 · 6H 2 О, 3-аминопропилфосфоновая кислота, метоксиполиэтиленгликоль уксусная кислота N -сукцинимидиловый эфир (PEG-NHS) с молекулярной массой 5000 Да, фолиевая кислота, N -гидроксисукцинимид (NHS) и карбокси- X -родамин N -сукцинимидиловый эфир (Rhod-NHS) был приобретен у Sigma-Aldrich и использован без дополнительной очистки. Аминокислоты, защищенные 9-флуоренилметоксикарбонилом (Fmoc), используемые для синтеза пептидов, были приобретены Romil Del Chimica, Chemicals, и использовались без дополнительной очистки. Вода была марки Milli-Q (18,2 МО см) и фильтровалась через фильтр 0,22 мкм.
Синтез MNP
МНЧ из чистого оксида железа были синтезированы щелочным соосаждением Fe 3+ и Fe 2+ , согласно протоколу, описанному в литературе [26]. Вкратце, FeCl 2 · 4H 2 O и FeCl 3 · 6H 2 O (молярное соотношение 1:2) растворяли в воде (50 мл) в атмосфере N 2 атмосфера при энергичном перемешивании. NH 3 25% в H 2 О (5 мл) добавляли к раствору при 80 ° C, и реакцию продолжали в течение 30 минут. Полученную суспензию охлаждали до комнатной температуры и промывали сверхчистой водой. Полученные незащищенные магнитные наночастицы (голые МНЧ) были изолированы от растворителя с помощью магнитной декантации.
Синтез gH625
Пептид получали, как сообщалось ранее [27], с использованием стандартного твердофазного метода 9-флуоренилметоксикарбонила (Fmoc). Вкратце, 50 мкмоль пептида синтезировали на смоле Ванга (0,75 ммоль / г) последовательными циклами снятия защиты и связывания. Связанный со смолой пептид затем подвергали взаимодействию с 4-хлор-7-нитробензофуразаном (NBD-Cl); реакцию проводили в течение ночи в присутствии DIPEA. Пептид отщепляли от смолы и снимали защиту обработкой смесью трифторуксусной кислоты (TFA) и поглотителями и после осаждения в ледяном этиловом эфире. Пептид растворяли в воде и сушили вымораживанием. Характеристику неочищенного пептида проводили методом ЖХ-МС с ионизацией электрораспылением (ESI), используя линейный градиент ацетонитрила (0,1% TFA) в воде (0,1% TFA) от 20 до 80% за 15 минут. Затем он был очищен препаративной обращенно-фазовой высокоэффективной жидкостной хроматографией (ОФ-ВЭЖХ).
Синтез N -Гидроксисукцинимидный эфир фолиевой кислоты (FA-NHS)
FA-NHS получали по следующей опубликованной методике [28]. Пятьсот миллиграммов фолиевой кислоты (FA) растворяли в 10 мл диметилсульфоксида (ДМСО) с 240 мл триэтиламина. NHS (260 мг) и N , N Добавляли -дициклогексилкарбодиимид (470 мг), и смесь оставляла реагировать в течение ночи при комнатной температуре в темноте. Побочный продукт, дициклогексилмочевина, удаляли фильтрацией. Затем раствор в ДМСО концентрировали при пониженном давлении и FA-NHS осаждали диэтиловым эфиром. Продукт несколько раз промывали безводным эфиром и сушили на воздухе.
Синтез функционализированных MNP
Синтез NH 2 @MNPs
МНЧ (200 мг) диспергировали в H 2 O (25 мл) с помощью ультразвуковой ванны в течение 30 мин. NH 2 Добавляли -PA (100 мг) и суспензию перемешивали в течение 2 часов при комнатной температуре. Частицы отделяли магнитным способом и четыре раза промывали H 2 . O, а затем этанолом и сушили на воздухе.
Синтез gH625 @ MNP
NH 2 @MNP (300 мг) и gH625 (1,2 мг) диспергировали в ДМСО (20 мл). Раствор перемешивали в течение ночи при 25 ° C. Полученные частицы разделяли магнитным способом; промывают ДМСО, H 2 О и этанол; и сушат на воздухе.
Синтез PEG, FA @ MNP
NH 2 @MNPs (300 мг), PEG-NHS (30 мг), FA-NHS (3 мг) и Rhod-NHS (3 мг) диспергировали в ДМСО (15 мл), и раствор перемешивали в течение ночи при 25 ° C. . Полученные частицы разделяли магнитным способом; промывают ДМСО, H 2 О и этанол; и сушат на воздухе.
Примеры характеристик
Измерения дифракции рентгеновских лучей на порошке (XRD) были выполнены с θ - θ Дифрактометр 5005 Bruker-AXS (Zeiss, Оберкохен, Германия) с использованием излучения Cu Kα, работающего при 40 кВ и 30 мА. Рентгеновская фотоэлектронная спектроскопия (XPS) была выполнена с помощью многофункционального спектрометра ESCA-Auger PHI 5600 со стандартным источником рентгеновского излучения Al-Kα. Анализы проводились под углом фотоэлектрона 45 ° (относительно поверхности образца) с углом приема ± 7 °. Шкала энергии связи XPS (B.E.) была откалибрована путем центрирования пика C 1s, обусловленного углеводородными фрагментами и дополнительным углеродом, при 285,0 эВ. УФ / видимые измерения проводились с помощью спектрофотометра JASCO V-560 UV / Vis, и спектры регистрировались с разрешением ± 0,2 нм. Измерения динамического рассеяния света (DLS) и дзета-потенциала МНЧ проводили при 25 ° C с помощью Zetasizer Nano-ZS (Malvern Instruments, Малверн, Великобритания), оснащенного гелий-неоновым лазером (633 нм) и детектором обратного рассеяния (173 °). ). Измерения пропускающей способности FT-IR регистрировались с помощью спектрометра JASCO FTIR 430 с использованием метода таблеток KBr, с получением 100 сканирований на спектр (диапазон сканирования 560–4000 см - 1 , разрешение 4 см - 1 ).
Культура клеток
Эндотелиальные клетки микрососудов головного мозга человека (HBMEC) и линия клеток глиобластомы человека A-172 выращивали до слияния в колбах для культур ткани, покрытых коллагеном типа I, покрытых крысиным хвостом, в соответствии с описанным методом [29]. Вкратце, HBMEC выращивали в среде эндотелиальных клеток с добавлением 5% фетальной бычьей сыворотки (FBS) и 1% добавки для роста эндотелиальных клеток. Клеточную линию A-172 выращивали в среде DMEM, содержащей 2 мМ глутамина и 10% FBS, как описано ранее [30]. В обоих случаях к культурам также добавляли 100 Ед / мл пенициллина и 100 мкг / мл стрептомицина.
Анализ жизнеспособности клеток
Жизнеспособность клеток определяли с помощью [3- (4,5-диметил-2-тиазолил) -2,5-дифенил-2 H -тетразолий бромид] (МТТ) тест [31]. Во всех экспериментальных условиях концентрация FBS была снижена до 1% (голодная среда). Клетки высевали в 96-луночные планшеты по 7000 клеток / лунку для получения оптимальной плотности клеток на протяжении всего эксперимента. Во всех анализах клетки сначала инкубировали при 37 ° C с МТТ в течение 3 часов; затем добавляли изопропанол с 0,04 M HCl и оптическую плотность измеряли через 1 час в планшет-ридере (Synergy 2-BioTek) с длиной волны 570 нм [32].
Конфокальная микроскопия
Конфокальную микроскопию проводили на клетках глиобластомы HBMEC и A-172, выращенных на покровных стеклах микроскопа, помещенных в 24-луночный планшет. После инкубации с МНЧ или без них клетки фиксировали добавлением 4% параформальдегида в PBS и обрабатывали для иммуноцитохимии, как описано ранее [33]. Анализы с конфокальной микроскопией выполнялись с помощью конфокального лазерного сканирующего микроскопа (LSM) Olympus FV1000, оснащенного следующими источниками возбуждения:диодным лазером (405 нм), многолинейным Ar-лазером (457, 488 и 515 нм), гелий-неоновым (G) лазером ( 543 нм) и гелий-неоновый (R) лазер (633 нм). Использовался масляный иммерсионный объектив (60xO PLAPO), и излучаемый свет регистрировался в последовательном режиме через систему спектральной фильтрации. Коэффициент усиления детектора был зафиксирован на постоянном значении, и были сделаны изображения для всех образцов в случайных местах по всей площади скважины. Были использованы следующие параметры сбора данных: λ ex / em =405/425 - 475 нм (синий канал, ядерное окрашивание с помощью DAPI); λ ex / em =488/500 - 530 нм (зеленый канал, маркировка gH625 @ MNP NBD); и λ ex / em =633/650 - 700 нм (красный канал, маркировка PEG, FA @ MNP с помощью rhod). Количественный анализ флуоресценции был выполнен с использованием программного обеспечения ImageJ (версия 1.50i, NIH).
Результаты и обсуждение
Синтез и характеристика MNP
Общая стратегия, реализованная для получения gH625 @ MNP и PEG, FA @ MNP из Fe 3 О 4 Наночастицы, полученные совместным осаждением, включают два этапа, как показано на рис. 1. Первый этап, который одинаков для обоих классов наночастиц, основан на функционализации МНЧ фосфоновой кислотой, несущей аминогруппу (NH 2 -ПА). На втором этапе NH 2 -PA-предварительно функционализированные MNP (NH 2 @MNPs) дополнительно конъюгированы со специфическими функциональными молекулами посредством реакций сочетания NHS. В частности, N -гидроксисукцинимид-активированная форма gH625, меченная NBD, была использована для получения gH625 @ MNPs, и N Активированные -гидроксисукцинимидом формы PEG, FA и Rhod использовали для получения PEG, FA @ MNP. Обратите внимание, что как gH625 @ MNP, так и PEG, FA @ MNP были помечены люминесцентными зондами (то есть NBD и Rhod соответственно) для проведения исследований конфокальной лазерной сканирующей микроскопии.
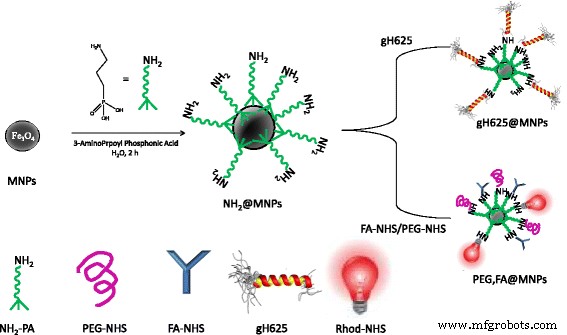
Схема реакции. Этапы реакции для получения функционализированных МНЧ
Рентгенодифрактометрическая (XRD) характеристика голых МНЧ, полученных после стадии соосаждения, аналогична описанной в наших предыдущих статьях [34, 35]. Вкратце, типичная картина (рис. 2а) показывает четыре дифракционных пика (2 θ =30,16 °, 35,48 °, 43,10 ° и 57,04 °), что согласуется с присутствием магнетита, маггемита или любого промежуточного состава между двумя фазами. Постоянная решетки, a , который оказался равным 8,389 (4) Å, что хорошо согласуется с параметром решетки объемного магнетита (8,396 Å), а также средний размер кристалла 11,2, определенный с помощью уравнения Дебая – Шеррера, сопоставимы со значениями ранее сообщил [34, 35].
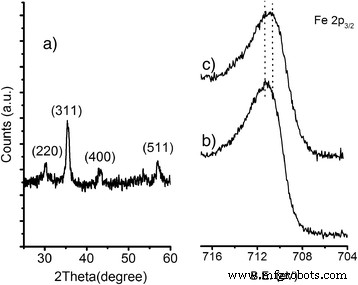
Типичные XRD- и XPS-спектры MNP. Рентгенограмма а) голых МНЧ и Fe 2p 3/2 высокого разрешения Спектральные области XPS б) голых МНЧ и в) NH 2 @MNPs
Обратите внимание, что поскольку кристаллическая структура Fe 3 О 4 магнетит очень похож на γ-Fe 2 О 3 маггемита, очень трудно различить две фазы с помощью XRD. По этой причине для дальнейшего анализа МНЧ использовалась рентгеновская фотоэлектронная спектроскопия (XPS). На рисунке 2b показано Fe 2p 3/2 . XPS-спектры высокого разрешения голых МНЧ. Центроид полосы, наблюдаемой при 710,9 эВ, соответствует Fe 2p 3/2 вершина горы. Это значение ниже, чем указано для Fe 3+ . либо в октаэдрических отверстиях α-Fe 2 О 3 (711,6 эВ) [36, 37] или в смешанных тетраэдрических и октаэдрических дырках γ-Fe 2 О 3 (711,4 эВ), и это согласуется со смешанной степенью окисления Fe в Fe 3 О 4 [37, 38].
Наконец, подробные магнитные характеристики подобных MNP представлены в наших предыдущих статьях [34, 35].
Процесс функционализации оценивали с помощью FT-IR и XPS. После функционализации фосфоновыми монослоями Fe 2p 3/2 полоса (рис. 2c) не показывает соответствующих модификаций, тем самым подтверждая, что Fe 3 О 4 фаза сохраняется. Однако небольшой сдвиг (0,4 эВ) Fe 2p 3/2 наблюдалась центроид в направлении более низкой энергии связи (B.E), что было связано с закреплением фосфонового монослоя. Подобные сдвиги действительно наблюдались при адсорбции фосфата различными оксидами железа [39] и могут быть приписаны некоторому переносу заряда от адсорбата к атомам Fe. Fe 2p 3/2 положение 710,5 эВ сохранялось после всех этапов функционализации для закрепления PEG и FA.
На рисунке 3 показано сравнение спектральных областей P2p, N1s и C 1s NH 2 . @MNPs, PEG, FA @ MNPs и gH625 @ MNPs соответственно. Положение пика P2p (133,2 эВ) NH 2 @MNPs обычно ассоциируется с присутствием фосфоновой кислоты, закрепленной на поверхности бидентатно [40,41,42,43]. Положение полосы P2p в спектрах gH625 @ MNPs и PEG, FA @ MNPs такое же, как наблюдаемое в NH 2 @MNPs спектра, таким образом показывая, что молекулы фосфоновой кислоты не удаляются во время реакций связывания пептида и иммобилизации фолиевой кислоты.
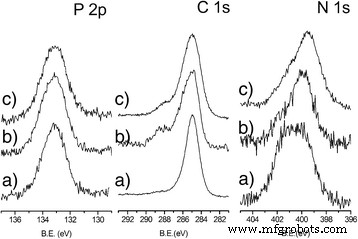
XPS-характеристика функционализированных MNP. Спектральные области XPS P 2p, C 1s и N 1s высокого разрешения:a) NH 2 @MNPs, b) PEG, FA @ MNPs, и c) gH625 @ MNPs
Форма и положение пика N1s-спектров NH 2 @MNP согласуются с наличием заякоренного NH 2 -ПА. Полоса состоит из двух различных компонентов:первая при 399,9 эВ связана с -NH-группами заякоренного аминопропилфосфата, а вторая компонента с центром при 401,5 эВ связана с аминогруппами, взаимодействующими с поверхностью Fe 3. О 4 через протонирование или образование связей –H.
После закрепления либо пептида gH625, либо FA, PEG и Rhod, компонент N1s при 399,8 эВ увеличивается по сравнению с компонентом при 401,8 эВ, относящимся к протонированным аминогруппам NH 2 @MNPs. Этот прирост обусловлен перекрывающимися сигналами атомов N, участвующих в амидной связи (400,2 эВ) между закрепленным аминопропилфосфатом и сопряженными молекулами (например, gh625, FA, PEG и Rhod), а также атомами N gh625. и FA (399,1 и 400,6 эВ).
Группа C 1s NH 2 Спектр @MNPs состоит из одного пика при 285,0 эВ, относящегося к алифатическим углеродам, как сообщалось ранее [40].
В C1s-спектрах gH625 @ MNPs и PEG, FA @ MNPs присутствие компонента C 1s при 288,3 эВ обусловлено карбоксильными и амидными группами молекул gh625, FA и Rhod.
ИК-Фурье спектры NH 2 @MNPs, gH625 @ MNPs и PEG, FA @ MNPs представлены на рис. 4. Во всех образцах спектры не показывают полосы при 1250 см - 1 из-за P =O и резких пиков в диапазоне 900–1050 см - 1 диапазоны из-за растяжения P – O – H [44,45,46], но широкая и сильная полоса при 1040 см - 1 , что связано с колебаниями ПО 3 2– группа, прикрепленная к поверхности железа. Эта полоса указывает, согласно результатам XPS, что фосфоновые кислоты депротонированы и прикреплены к поверхности через связи P – O – Fe, как сообщалось ранее [34, 40, 41]. ИК-область спектра от 1500 до 1700 см - 1 показывает полосы, принадлежащие амино и амидным группам gH625 и FA. В частности, спектр NH 2 @MNPs показывает острый пик около 1650 см - 1 связанный с NH 2 изгибание [47]. После фиксации PEG, Rhod и FA 1700–1500 см - 1 область PEG, FA @ MNPs показывает более широкие полосы из-за свертки колебаний непрореагировавшего NH 2 , амидные группы и бензольные кольца FA и Rhod (1630–1600 см - 1 ) [35]. Аналогичным образом, после заякоривания пептида широкие полосы примерно при 1650–1600 см - 1 может быть связано с вкладом нескольких колебаний из-за непрореагировавшего NH 2 и аминогруппы боковых цепей пептида и фрагмента С =О амидных связей пептида [48]. Кроме того, компонент размером около 1540 см - 1 из-за комбинированного δ Также присутствуют (N – H) / ν (C – N) колебания пептида [48].
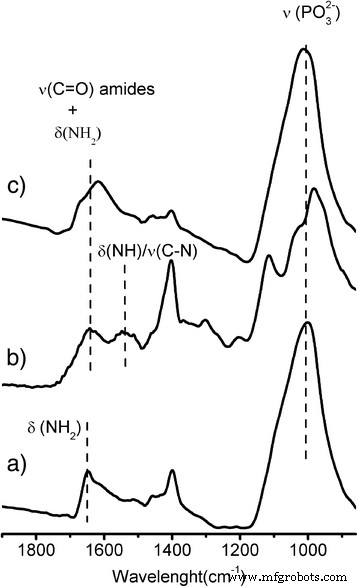
FT-IR характеристика функционализированных MNP. Спектральный диапазон FT-IR в диапазоне 850–1900 см −1 диапазон а) NH 2 @MNPs, b) gH625 @ MNPs, и c) PEG, FA @ MNPs
Заякоривание FA на MNPs было также подтверждено спектрами УФ / Vis коллоидного раствора PEG, FA @ MNPs. На рисунке 5 сравниваются спектры NH 2 . @ МНЧ и ПЭГ, ФА @ Коллоидные дисперсии МНЧ. Спектр раствора FA (5 мкМ) добавлен в качестве эталона. Явная полоса при 274 нм, типичная для FA, четко видна как в контрольном растворе, так и в коллоидном растворе PEG, FA @ MNPs, что подтверждает присутствие FA в MNP. Обратите внимание, что небольшой сдвиг от поглощения FA-NHS при 280 нм к значению 274 нм после закрепления, вероятно, связан с изменением окружающей среды от свободного FA-NHS и FA-заякоренного FA. Наличие переменных сдвигов полосы поглощения при 280 нм после закрепления на поверхности FA или конъюгации с другими молекулами уже наблюдалось в литературе [49,50,51].
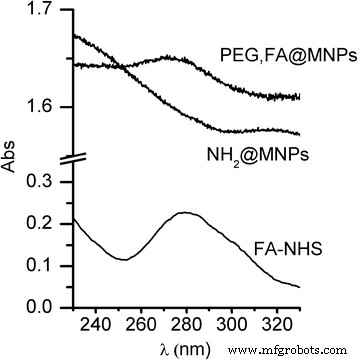
УФ / видимая характеристика функционализированных MNP. УФ / видимые спектры раствора 5 мкМ FA-NHS и NH 2 @MNPs и коллоидные дисперсии PEG, FA @ MNPs. Отметим, что высокий фон, наблюдаемый в спектрах NH 2 @MNPs и PEG, FA @ MNPs возникает из-за рассеяния коллоидной дисперсии наночастиц
Средний гидродинамический диаметр, индекс полидисперсности (PDI) и дзета-потенциал функционализированных MNP определяли с помощью DLS в буфере PBS при pH 7,4 на приготовленных дисперсиях MNP и после 72 ч старения (Таблица 1). Гидродинамические диаметры NH 2 -PA @ MNPs, gH625 @ MNPs и PEG, FA @ MNPs составляли 73,0 ± 3,0 нм, 104,0 ± 4,0 нм и 51 ± 2 нм, соответственно, и значения PDI указывают на достаточно узкое распределение частиц по размеру. Как и ожидалось, конъюгация с gH625 увеличивала размер наночастиц, в то время как уменьшение размера PEG, FA @ MNPs связано с лучшей дисперсией, чем NH 2 @MNP, связанные с наличием цепей PEG.
В любом случае обратите внимание, что сильно отрицательный дзета-потенциал (<- 30 мВ) наблюдался для всех систем. Такие отрицательные значения дзета-потенциала обеспечивают долгосрочную стабильность и предотвращают обширную агрегацию частиц [52, 53]. Действительно, отрицательный поверхностный заряд лишь незначительно зависел от покрытия, но в основном был результатом комбинации отрицательно заряженного ядра Fe 3 О 4 наночастиц [54] и эффект групп фосфоновой кислоты, наблюдаемый для аналогичных систем [52, 34]. Следовательно, по сравнению с другими синтетическими стратегиями, используемыми для функционализации MNP, использование монослоев фосфоновой кислоты в качестве линкеров не только позволяет формировать стабильную связь между поверхностью и функциональными группами, но также индуцирует сильно отрицательный дзета-потенциал. После 72 часов старения размер и дзета-потенциал NH 2 -PA @ MNP, gH625 @ MNP и PEG, FA @ MNP остаются примерно такими же, что позволяет предположить, что все декорированные поверхности стабильны во времени.
Жизнеспособность ячейки
Жизнеспособность клеток HBMEC и A-172, инкубированных с gH625 @ MNP и FA, PEG @ MNP, оценивали с помощью анализа MTT при разном времени инкубации и в присутствии различных концентраций наночастиц (10 и 20 мкг / мл). Как показано на рис. 6, не наблюдалось зависящего от концентрации и / или времени (24–48–72 ч) цитотоксического действия декорированных систем на клетки HBMEC и A-172.
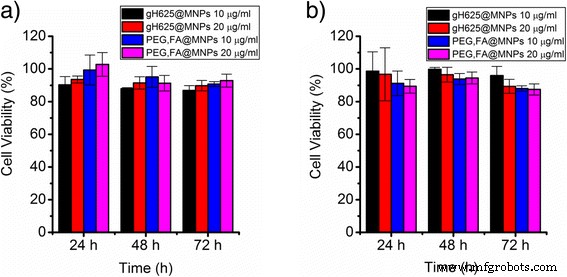
Жизнеспособность клеток. Жизнеспособность клеток а HBMEC и b Клетки A-172, инкубированные в течение 24, 48 и 72 ч с gH625 @ MNPs 10 мкг / мл (черная полоса), gH625 @ MNPs 20 мкг / мл (красная полоса), PEG, FA @ MNPs 10 мкг / мл (синяя полоса ) и ПЭГ, ФА @ МНЧ 20 мкг / мл (пурпурный столбик)
Внутриклеточное поглощение
Чтобы определить, сохраняется ли способность пептида gH625 проникать в клетки после его иммобилизации на поверхности наночастиц, и сравнить способность gH625 и FA пересекать ГЭБ, интернализация в эндотелиальные клетки мозга человека меченных NBD gH625 @ MNPs и меченные Rhod PEG, FA @ MNPs были исследованы с помощью конфокальной лазерной сканирующей микроскопии.
После 24 ч инкубации захват PEG-FA @ MNPs не очевиден, в то время как интернализация gH625 @ MNPs отчетливо видна (рис. 7). Конъюгация с gH625 приводит к более быстрому захвату и почти в два раза большей интенсивности внутриклеточной флуоресценции (рис. 8).
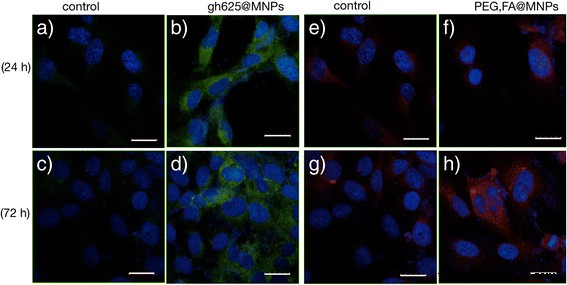
LSM флуоресцентные микрофотографии HBMEC. Микрофотографии флуоресценции LSM HBMEC, инкубированного в течение 24 ч ( b , f ) и 72 часа ( д , ч ) с меченным NBD gH625 @ МНЧ 15 мкг / мл ( b , d ) и их элементы управления ( a , c ) или меченный родом PEG, FA @ MNPs 15 мкг / мл ( f , ч ) и их элементы управления ( e , г ). Масштабная линейка =20 мкм
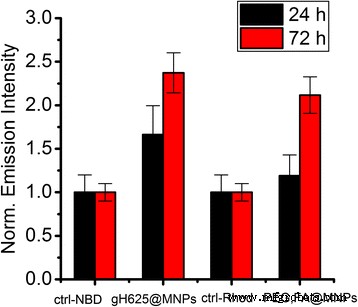
Нормированные интенсивности внутриклеточной флуоресценции. Количественный анализ внутриклеточной флуоресценции после инкубации HBMEC через 24 и 72 часа с NBD-меченными gH625 @ MNP и Rhod-меченными FA, PEG @ MNP
При более продолжительном времени инкубации (72 ч) различия между интернализацией двух систем уменьшаются. Такое поведение не является неожиданным, поскольку в течение длительного времени инкубации могут происходить неспецифические процессы интернализации FA, PEG @ MNP, и наши результаты дополнительно подтверждают то, что мы ранее сообщали о поглощении функционализированных и нефункционализированных наночастиц полистирола [55].
Для дальнейшего изучения возможности использования gH625 @ MNP в качестве терапевтического агента для опухолей головного мозга было исследовано клеточное поглощение gH625 @ MNP и FA, PEG @ MNP с использованием клеточной линии глиобластомы A-172. Глиобластома - одна из наиболее распространенных первичных опухолей головного мозга, а также одна из самых смертельных форм рака.
Поглощение клетками gH625 @ MNP и FA, PEG @ MNP через 24 часа инкубации сопоставимо, как показано на рис. 9.
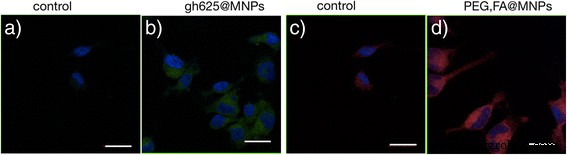
LSM флуоресцентные микрофотографии клеток глиобластомы. LSM флуоресцентные микрофотографии клеток глиобластомы. Объединенные сине-зеленые изображения:контрольные ячейки ( a ) и клетки, инкубированные с 15 мкг / мл меченных NBD gH625 @ MNP ( b ). Объединенные сине-красные изображения:контрольные ячейки ( c ) и клетки, инкубированные с 15 мкг / мл меченного родом PEG, FA @ MNP ( d ). Масштабная линейка =20 мкм
Такое поведение предполагает, что gH625 способен нацеливаться на опухоль головного мозга с такой же эффективностью, как и более часто применяемая единица нацеливания на FA.
Выводы
Fe 3 О 4 nanoparticles have been functionalized with the gH625 viral cell penetrating peptide adopting a versatile route based on MNP prefunctionalization with a monolayer consisting of a bifunctional phosphonic linker, 3-aminopropylphosphonic acid. The cell internalization capabilities of this system have been evaluated by comparing them with those of a reference system based on MNPs functionalized with PEG, rhodamine, and folic acid, obtained adopting the same NH2 -PA-based platform. The uptake of the two differently decorated MNPs was assessed in primary microvascular endothelial cells from human brain, which are the main components of the BBB and simulate an in vitro model of the BBB. These surface modifications influence the internalization of MNPs in HBMEC and, therefore, their capability to cross the BBB. In fact, conjugation with the gH625 peptide upgraded the delivery of nanoparticles across the in vitro BBB, leading to significant higher cell uptake in HBMEC after 24 h compared with that of FA bearing MNPs (FA,PEG@MNPs). Note that also other strategies have been used to enhance nanoparticle uptake across the BBB. A common approach is to attach targeting ligands in order to activate receptor-mediated endocytosis. As examples, transferrin-coupling nanoparticles can penetrate into the BBB through a transferrin receptor-mediated process [56]. Analogously, the linkage of the apolipoprotein E to the nanoparticles enhances the BBB penetration [57]. Besides, nanoparticles having a surface charges modified with polyethylenimine (PEI) has been reported to cross the BBB by absorptive-mediated transcytosis [58]. Finally, the ability of MNPs to pass through human brain microvascular endothelial cells, used as an in vitro BBB model, can be also facilitated by an external magnet [59]. In our work, we studied a different approach which use a cell penetrating peptide, the gh625, to improve internalization capabilities of Fe3 О 4 наночастицы. These results are in accordance with those previously obtained by D. Guarnieri et al. using different kinds of MNPs [55, 60] confirming that the gH625-decorated magnetic nanoparticle has a relevant role in crossing the BBB and could be used as a safe and effective drug delivery system.
Сокращения
- A-172:
-
Human glioblastoma cell line
- B.E.:
-
Binding energy
- BBB:
-
Blood-brain barrier
- CNS:
-
Central nervous system
- CPPs:
-
Cell-penetrating peptides
- DIPEA:
-
N , N -Diisopropylethylamine
- DLS:
-
Динамическое рассеяние света
- DMEM:
-
Dulbecco’s modified Eagle’s medium
- DAPI:
-
4′,6-Diamidino-2-phenylindole
- DMSO:
-
Dimethyl sulfoxide
- FA:
-
Folic acid
- FA-NHS:
-
Activated form of FA with NHS
- FBS:
-
Фетальная бычья сыворотка
- Fmoc:
-
9-Fluorenylmethoxycarbonyl
- FT-IR:
-
Инфракрасная спектроскопия с преобразованием Фурье
- gh625:
-
20-Residue peptide derived from the glycoprotein H (gH) of the Herpes simplex virus 1
- gH625@MNPs:
-
NH 2 @MNPs functionalized with gh625
- HBMECs:
-
Microvascular endothelial cells from human brain
- MNPs:
-
Magnetic iron nanoparticles
- MTT:
-
3-(4,5-Dimethyl-2-thiazolyl)-2,5-diphenyl-2H -tetrazolium bromide
- NBD:
-
4-Chloro-7-nitrobenz-2-oxa-1,3-diazole
- NH2 @MNPs:
-
MNPs modified with NH2 -PA
- NH2 -PA:
-
3-Aminopropylphosphonic acid
- NHS:
-
N -Hydroxysuccinimide
- PBS:
-
Phosphate-buffered saline
- PDI:
-
Индекс полидисперсности
- PEG:
-
Полиэтиленгликоль
- PEG,FA@MNPs:
-
NH 2 @MNPs functionalized with FA, Rhod and PEG
- PEG-NHS:
-
Methoxypolyethylene glycol acetic acid N -succinimidyl ester
- PEI:
-
Polyethylenimine
- Rhod:
-
Carboxy-X -rhodamine
- Rhod-NHS:
-
Carboxy-X -rhodamine N -succinimidyl ester
- TFA:
-
Trifluoroacetic acid
- XPS:
-
Рентгеновская фотоэлектронная спектроскопия
- XRD:
-
X-ray powder diffraction
Наноматериалы
- Нановолокна и нити для улучшенной доставки лекарств
- Наночастицы для терапии рака:текущий прогресс и проблемы
- Получение и магнитные свойства легированных кобальтом наночастиц шпинели FeMn2O4
- Получение и повышенная активность каталитического гидрирования наночастиц Sb / палигорскита (PAL)
- Улучшенное фотоэлектрохимическое определение мочевой кислоты на электроде из стеклоуглерода, модифицирова…
- Изучение in vitro влияния наночастиц Au на клеточные линии HT29 и SPEV
- Гидротермальный синтез наночастиц In2O3, гибридные двойники, гексагональные дисковые гетероструктуры ZnO для по…
- Повышенная стабильность магнитных наночастиц золота с помощью сополимера поли (4-стиролсульфоновой кислоты …
- Глубокие межфазные эффекты в наночастицах ядра / оболочки CoFe2O4 / Fe3O4 и Fe3O4 / CoFe2O4
- Синтез монодисперсных CoFe2O4 @ Ag наночастиц ядро-оболочка и их характеристика



