Экологичный и простой синтез нанопроволок Co3O4 и их перспективное применение с графеном в литий-ионных батареях
Аннотация
В этой работе мы разработали экологичную стратегию приготовления Co 3 О 4 нанопроволоки. Процесс состоял из двух этапов:контролируемый синтез нанопроволок металлического кобальта, за которым следовала стадия легкого окисления на воздухе. Одномерная нанопроволочная структура с высоким соотношением сторон была легко получена за счет самосборки комплексов ионов кобальта при помощи магнитного поля во время восстановления. После прокаливания на воздухе Co 3 О 4 нанопроволоки были изготовлены в больших масштабах и готовы к использованию в качестве анодного материала для литий-ионных аккумуляторов. Ко 3 О 4 нанопроволоки, которые имели длину от 3 до 8 мкм с соотношением сторон более 15, демонстрировали обратимую емкость литиевого накопления до ~ 790 мАч / г при использовании небольшого количества бездефектных графеновых чешуек в качестве проводящих добавок. Превосходные электрохимические характеристики были приписаны синергетическому эффекту «плоского наложения» между 1D нанопроволокой и 2D графеном. Следовательно, Co 3 О 4 Композит нанопроволока / графен имеет многообещающее применение для литий-ионных аккумуляторов.
Фон
В связи с быстро растущим спросом на стратегию экологически чистой и устойчивой энергетики устройства хранения электроэнергии остро нуждаются во многих приложениях, таких как электромобили и портативные электронные устройства. Литий-ионные батареи (LIB) могут обеспечивать относительно высокую плотность энергии и обеспечивать множество преимуществ, таких как длительный срок службы, низкая стоимость и хорошая обратимость. Оксиды переходных металлов рассматривались как перспективные аноды для LIB из-за их большого количества, низкой стоимости и высокой теоретической емкости [1, 2], среди которых оксид кобальта (Co 3 О 4 ) привлек большое внимание из-за своей высокой теоретической емкости (890 мАч / г) [2,3,4]. Однако изначально низкая проводимость, большой объем и изменение во время циклирования, а также низкий коэффициент использования Co 3 О 4 , приводят к плохим электрохимическим характеристикам, что затрудняет его практическое применение [5, 6].
В последние годы развитие нанонауки и нанотехнологий открывают революционные возможности для дальнейшего улучшения характеристик LIB, особенно одномерных наноструктур (например, нанопроволок, нанолент, нановолокон). Они привлекли большое внимание благодаря своим исключительным электрохимическим свойствам, включая большую площадь поверхности, короткий путь ионного / электротранспорта и хорошую способность выдерживать объемное расширение во время заряда / разряда [5, 7, 8, 9, 10].>
Хотя эти одномерные наноматериалы, такие как Co 3 О 4 нанопроволоки (Co 3 О 4 ННК), привлекательны в качестве электродных материалов, синтез таких наноструктур вызвал широкий интерес, но все еще оставался довольно сложной задачей. Многие методы получения нанопроволок, включая гидротермальные и сольвотермические методы [11,12,13], электроосаждение на основе темплатов [14] и влажное химическое восстановление [15], хорошо разработаны в течение последних десятилетий. Эти подходы, однако, часто включают жесткие условия синтеза, такие как высокое давление / температура, дорогостоящий шаблон или сильная кислота (например, HF, широко используемая для растворения шаблона), что препятствует практическому применению таких наноматериалов. Например, Донг и др. подготовил Co 3 О 4 NW путем нагревания чистой кобальтовой фольги в атмосфере, но время реакции, температуру и влажность необходимо тщательно контролировать. Процесс приготовления был сложным и трудоемким [16]. Ji et al. использовали метод синтеза на основе шаблона для получения Co 3 О 4 ННК в узких порах шаблона AAO, тогда как сильная кислота и шаблон были незаменимы [14]. По результатам Xu et al. Co 3 О 4 НВ были синтезированы модифицированным гидротермальным методом при высоком давлении [11]. Как указывается во многих литературных источниках, существующие подходы страдают многими недостатками, такими как сложная работа, сложность очистки, высокая стоимость и сильное загрязнение окружающей среды. Для преодоления множества трудностей, которые долгое время препятствовали крупномасштабному применению таких наноструктур, крайне важно разработать новый метод синтеза структур на основе нанопроволоки с улучшенной масштабируемостью, осуществимостью и экологичностью.
Здесь мы сообщаем о новом, легком и экологически безопасном методе получения Co 3 О 4 NWs. В данном исследовании был принят двухэтапный метод:синтез нанопроволок Co (CoNWs) с помощью магнитного поля и окисление CoNWs. Обладая превосходной эффективностью и простотой, нынешний метод расширил бы электрохимическое применение Co 3 О 4 материалы, по сравнению с предыдущими подходами к синтезу. Насколько нам известно, нет соответствующего отчета об этой новой стратегии синтеза. В этом отчете Co 3 О 4 ННК демонстрируют относительно прочную структуру с отношением длины к диаметру ~ 15, что полезно для построения путей передачи электронов / ионов. С помощью небольшого количества графена (3 мас.%), Действующего в качестве проводящей подложки, такой Co 3 О 4 ННК / графеновые материалы обладают обратимой емкостью ~ 790 мАч / г и хорошими скоростными характеристиками по сравнению с обычным Co 3 О 4 наночастицы (Co 3 О 4 NPs), что делает его хорошим кандидатом для применения в литий-ионных аккумуляторах.
Экспериментальный
Материалы
Гексагидрат хлорида кобальта (II) (CoCl 2 · 6H 2 O, 99 мас.%), Динатриевая соль этилендиаминтетрауксусной кислоты (EDTA-2Na, 99 мас.%), Гидроксид натрия (NaOH, 98 мас.%), Хлорид натрия (NaCl, 99,5 мас.%), Хлорид калия (KCl, 99,5 мас.%). ), поливинилпирролидон K30 (ПВП (–CH (NCH 2 Канал 2 Канал 2 CO) CH 2 -) n , M w =29 000–35 000) и моногидрат гидразина (N 2 H 4 · H 2 O, 80 об.%) Были закуплены у Chengdu KeLong Reagent Co., Ltd. (Китай), а гексагидрат платинохлористоводородной кислоты (H 2 PtCl 6 · 6H 2 O, 38 мас.%) Был приобретен в Шэньянском научно-исследовательском институте цветных металлов (Китай). Все химические вещества были аналитической чистоты без дополнительной очистки. Все водные растворы готовили на деионизированной воде (D.I. water). Коммерчески доступный Co 3 О 4 НЧ, полученные от Shanghai Aladdin Bio-chem Technology Co., Ltd., использовали в качестве контрольной группы.
Синтез CoNW
В типичном синтезе 0,6 ммоль CoCl 2 · 6H 2 O и 0,6 ммоль EDTA-2Na помещали в стакан из ПТФЭ вместимостью 100 мл, растворяли в 60 мл D.I. вода. Значение pH раствора доводили до 14 титрованием разбавленного NaOH, и 0,15 г ПВП в качестве поверхностно-активного вещества растворяли в растворе при интенсивном перемешивании. После хорошего диспергирования химический стакан помещали между двумя магнитами (в водяной бане), прикладывая поле 35 мТл, измеренное тесла-метром HT20, и водяную баню устанавливали на 80 ° C. Когда температура реакционного раствора достигнет 80 ° C, 0,30 мл N 2 H 4 · H 2 O действовал как восстановитель и был добавлен к вышеуказанному раствору для восстановления Co 2+ и 0,12 мл 0,0253 моль / л H 2 PtCl 6 · 6H 2 O (работавший как инициатор) были смешаны с раствором. CoNW формировались постепенно в течение 10 мин. После реакции соединение вынимали из раствора с помощью магнита и несколько раз промывали ультразвуком, используя этанол и дистиллированную воду для удаления примесей. Наконец, образцы сушили в вакуумном сушильном шкафу с замораживанием в течение 12 часов.
Синтез Co 3 О 4 NW
0,01 г свежеприготовленного образца помещали в фарфоровую лодочку, однородно смешанную с 0,3 г KCl и 0,2 г NaCl. Затем смесь выдерживали в муфельной печи и нагревали при 650 ° C в течение 4 ч. После естественного остывания муфельной печи изделие вынимали и промывали Д.И. воды трижды и сушили в сушильном шкафу при 80 ° С в течение 4 ч. Процесс формирования Co 3 О 4 ННК показан на рис. 1.
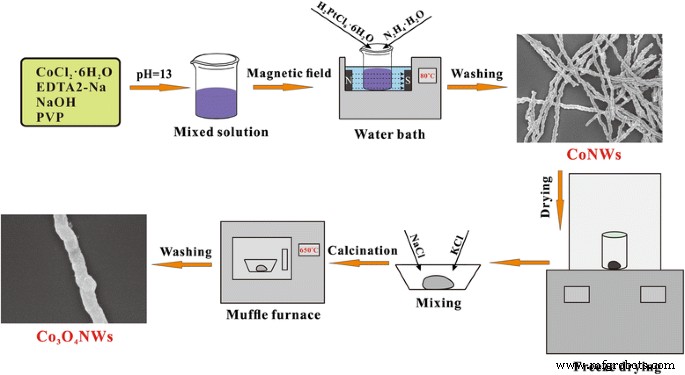
Схематическое изображение препарата Co 3 О 4 НБ
Характеристика
Характеристика материалов
Фазу состава полученных продуктов проверяли и сравнивали с помощью рентгеноструктурного анализа (XRD, Philips X’Pert Pro MPD) с использованием CuKα в качестве источника излучения (λ =0,154249 нм) при напряжении 40 кВ. Углы дифракции (2 θ ) были установлены между 20 ° и 90 ° с шагом 4 ° мин −1 . Фазовая идентификация была достигнута путем сравнения дифрактограммы образца со стандартными картами в базе данных ICDD-JCPDS.
Морфологию микроструктур образцов характеризовали с помощью автоэмиссионного сканирующего электронного микроскопа (SEM, JSM-6701F, JEOL, Япония) при ускоряющем напряжении 150 кВ. Перед наблюдением с помощью СЭМ все образцы были покрыты золотом.
Изображение просвечивающей электронной микроскопии (ПЭМ) и изображение ПЭМ высокого разрешения (ПЭМВР) были получены на ТЕМ Tecnai-G20 (FEI, США) для микроструктурной характеристики при ускоряющем напряжении 200 кВ. Электронная дифракция на выбранной площади (SAED) также была записана с использованием того же оборудования.
Электрохимические измерения
Электрохимические характеристики Co 3 О 4 Новички и партнеры 3 О 4 NP измеряли на основе полукруглых ячеек CR2025. Бездефектные графеновые нанолисты (df-GNS) были получены путем модифицированного жидкофазного расслоения [17], а затем использовались в качестве проводящего компонента в электроде. Бездефектный графен толщиной до ~ 0,5 нм и поперечным размером ~ 1 мкм был приготовлен и диспергирован в N -метил-пирролидон (NMP). Рабочий электрод без связующего был изготовлен путем покрытия суспензией смеси, которая состояла из активных материалов (Co 3 О 4 NW / Co 3 О 4 НЧ) и графеновых нанолистов (ГНС) в массовом соотношении 100:3 на токосъемник из медной фольги. Загрузка активного материала составляла 0,5 ~ 1 мг на ячейку.
Раствор электролита 1 моль / л LiPF 6 растворяется в смеси этиленкарбоната (EC), пропиленкарбоната (PC) и диэтилкарбоната (DEC) с объемным соотношением EC / PC / DEC =1:1:1. В качестве разделителя использовалась мембрана Celgard 2325. Монетные элементы были собраны в перчаточном боксе, заполненном аргоном, где содержание кислорода и влаги составляло менее 0,1 ppm.
Циклы гальваностатического заряда-разряда были протестированы с использованием системы тестирования батарей (LAND 2001A) в диапазоне напряжений 0,01 ~ 3 В. Циклические вольтамперограммы (CV) Co 3 О 4 Электрод NWs / df-GNS были выполнены на коммерческой электрохимической рабочей станции в диапазоне напряжений 0,01 ~ 3,0 В при скорости сканирования 0,5 мВ / с. Электрохимическая импедансная спектроскопия (EIS) проводилась при напряжении холостого хода в диапазоне частот от 0,1 Гц до 100 кГц с амплитудой напряжения 5,0 мВ.
Результаты и обсуждение
Фазы CoNW, Co 3 О 4 NW и Co 3 О 4 НЧ были впервые исследованы методом XRD. Их брэгговские дифракционные пики показаны на рис. 2а – в соответственно. Видно, что дифракционные пики CoNW хорошо проиндексированы с отражениями от гранецентрированного кубического (ГЦК) Co (JCPDS № 15-0806). Наблюдались два типичных характерных пика ГЦК Со при значении 2-тета 44 ° и 76 °, соответствующих индексам Миллера (111) и (220), соответственно. Ко 3 О 4 NW и Co 3 О 4 Пики дифракции НЧ хорошо проиндексированы отражениями гранецентрированного кубического (ГЦК) Co 3 О 4 (JCPDS № 15-0806). Зарегистрированные дифракционные пики Co 3 О 4 НП и Ко 3 О 4 СЗ при 2-тета =19 °, 31 °, 37 °, 39 °, 45 °, 56 °, 59 ° и 65 ° были хорошо отнесены к (111), (220), (311), (222), (400), (422), (511) и (440) плоскости ГПУ Co 3 О 4 , соответственно, с параметром ячейки a =8,084 Å, b =8,084 Å и c =8,084 Å. Между тем, резкие и высокие дифракционные пики предполагали, что приготовленный Co 3 О 4 ННК имели высокую степень кристаллизации. Затем средний размер кристаллических зерен был оценен по рентгенограммам в соответствии с формулой Шеррера D = λk / ( β cos θ ) (где D - средний размер кристаллитов, λ - длина волны рентгеновского излучения 0,1542 нм, k коэффициент формы частицы, β обозначает угловую ширину линии половинной максимальной интенсивности, а θ представляет собой угол Брэгга) со значениями 18,67 и 25,35 нм для CoNW и Co 3 О 4 NWs соответственно. Было очевидно, что эти значения были меньше, чем размеры одиночной частицы Co в нанопроволоке, как наблюдалось с помощью SEM, что предполагало, что каждая частица нанопроволок состояла из нескольких кристаллических зерен. Никаких характерных пиков из-за примесей обнаружено не было, что указывает на высокую чистоту Co 3 О 4 NWs. Также было удивительно иметь такое высокое CoNWs-to-Co 3 О 4 Выход конверсии ННК посредством простого окисления на воздухе, что можно отнести к более высокой реакционной способности ННК по отношению к кислороду из-за их высокой удельной поверхности.
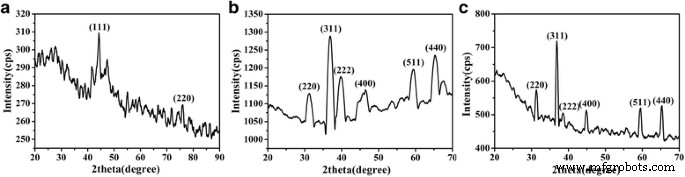
XRD-диаграмма CoNW ( a ), Co 3 О 4 NW ( b ) и Co 3 О 4 НП ( c )
Морфология полученных образцов была охарактеризована с помощью сканирующей электронной микроскопии (SEM). На SEM-изображении был показан Co 3 О 4 Образцы НЧ имели однородный диаметр 80 нм, и большинство образцов имело неповрежденную сферическую морфологию (см. Рис. 3а). Однородные CoNW диаметром ~ 150 нм и длиной 20 мкм наблюдались, как показано на рис. 3b. Можно было увидеть четкую морфологию поверхности, напоминающую ожерелье, состоящую из взаимосвязанных крошечных частиц, что подтверждает предложенный нами выше механизм реакции. Более того, CoNW имели прочную структурную целостность, которая сохраняла проволочную форму даже после шести раз ультразвуковой обработки (каждый раз по 1 мин). После многократной промывки CoNW водой и этанолом, CoNW легко трансформировались в Co 3 О 4 ННК простым окислением на воздухе. Изображения Co 3 О 4 ННК (рис. 3c, d) имели относительно гладкие нанопроволоки и оставались диаметром около 180 нм, что указывает на то, что нанопроволоки все еще сохраняли проволочную структуру после прокаливания. Таким образом, окисление на воздухе было простым и действенным способом получения Co 3 О 4 NWs.

СЭМ изображения Co 3 О 4 НП ( а ), CoNWs ( b ), а Co 3 О 4 NW ( c , d ) с разным увеличением
Микроструктура Co 3 О 4 НП, НС и Со 3 О 4 Образцы ННК были дополнительно исследованы с помощью просвечивающей электронной микроскопии (ПЭМ), дифракции на выбранной площади (SAED) и просвечивающей электронной микроскопии высокого разрешения (HRTEM), как показано на рис. 4a-f. Типичные изображения ПЭМ были показаны на рис. 4a – c, а морфология и структура образцов почти соответствовали тому, что наблюдалось на изображениях SEM. Кроме того, как показано на вставках на рис. 4a – c, узоры концентрических колец Co 3 О 4 НП и Ко 3 О 4 Наблюдаемые ННК (рис. 4а, в) можно отнести к плоскостям (200), (311), (440) и (511) Co 3 О 4 , и наблюдаемые концентрические кольцевые структуры CoNW (рис. 4b) могут быть отнесены к плоскостям (111) и (220) Co. SEAD был точно идентичен кубической решетке Co и Co 3 О 4 соответственно, что согласуется с результатами XRD. Ориентация решетки CoNW на изображениях HRTEM на рис. 4e, как предшественник Co 3 О 4 ННК имели межплоскостное расстояние 0,12 и 0,21 нм, что соответствовало плоскостям (111) и (211) структуры Co. Шаг решетки (рис. 4d, f) вдоль направлений (220), (311), (440) и (511) оценивается в 0,28, 0,25, 0,15 и 0,14 нм, что близко к стандартным данным. 0,29, 0,24, 0,15 и 0,14 нм.

ПЭМ-изображения Co 3 О 4 НП ( а ), CoNWs ( b ) и Co 3 О 4 NW ( c ). Вставки ( a , b , и c ) показаны выбранные области электронограммы (SAED) соответствующих образцов. ПЭМ-изображения Co 3 с высоким разрешением О 4 НП, НС и Со 3 О 4 NW в ( d , e , и f )
CoNW были приготовлены с использованием реакционного пути на основе раствора. На рис. 5 мы предложили возможный механизм образования. Вначале EDTA-2Na координировалась с Co 2+ ионы для образования комплексов в растворе. Затем молекулы ПВП самоорганизовались в сферические мицеллы в воде [18, 19], а ядра Со были обернуты и, возможно, абсорбированы на поверхности сферических мицелл, чтобы уменьшить поверхностную свободную энергию Гиббса. Впоследствии, с введением N 2 H 4 · H 2 O в раствор, часть N 2 H 4 беспрерывно заменял ЭДТА 2- анионы и координированный с Co 2+ катионы с образованием [Co (N 2 H 4 ) 3 ] 2+ комплексы, а остальные из них служили восстановителем, вводились в мини-реактор и превращали [Co (N 2 H 4 ) 3 ] 2+ к мелким наночастицам Co. Согласно предыдущей литературе, Со, а также его соединения были предпочтительны для образования микросфер [20, 21]. Из-за внутренней магнитной природы металлического Co дипольные магнитные моменты атомов Co выровнены относительно направления внешнего магнитного поля. В результате наночастицы Co будут выстраиваться вдоль линий магнитной индукции, образуя CoNWs.
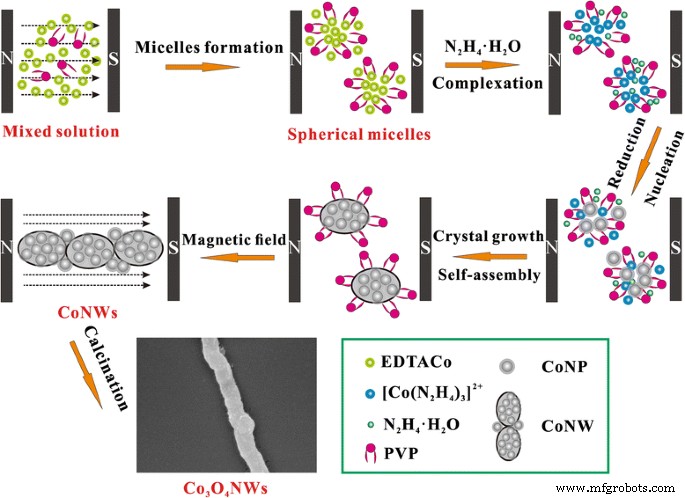
Схематические чертежи Co 3 О 4 Механизм образования ННК с помощью внешнего магнитного поля
Использование одномерных геометрических характеристик Co 3 О 4 ННК мы подготовили электроды, используя небольшое количество 2D-бездефектного графена (df-графен) в качестве проводящей основы для создания 1D-2D гибридной структуры (метод приготовления df-графена был описан в предыдущем исследовании [17]. ). На рисунке 6а показана морфология Co 3 . О 4 Электрод NWs / df-GNS. Для изготовления электродов Co 3 О 4 ННК в форме порошка добавляли к дисперсии df-GNS / NMP, а затем суспензию смеси обрабатывали ультразвуком в течение 10 мин перед литьем по медной фольге. Как видно на рис. 6b, из-за низкоразмерной природы нанопроволок и нанолистов Co 3 О 4 И NW, и df-GNS сформировали морфологию «плоской поверхности» на токосъемнике с нанопроволокой, встроенной между нанолистами. Эта структура может обеспечить множество преимуществ:(1) она может предотвратить самоагрегацию этих наноматериалов, особенно самоагрегацию и переупаковку Co 3 О 4 ННК, что является основным недостатком для практического применения таких наноструктур; (2) df-GNS может не только предлагать пути быстрых электронов, но также действовать как гибкая буферная подушка, чтобы приспособиться к изменению объема Co 3 О 4 NW во время заряда / разряда; (3) 1D-2D наноструктура предлагает множество пор и нанотуннелей для ускорения переноса ионов, поскольку площадь внешней поверхности, площадь микропор и средний размер пор Co 3 О 4 Было обнаружено, что сЗ составляет 28,554 м 2 . / г, 43,697 м 2 / г, 14,682 нм соответственно.
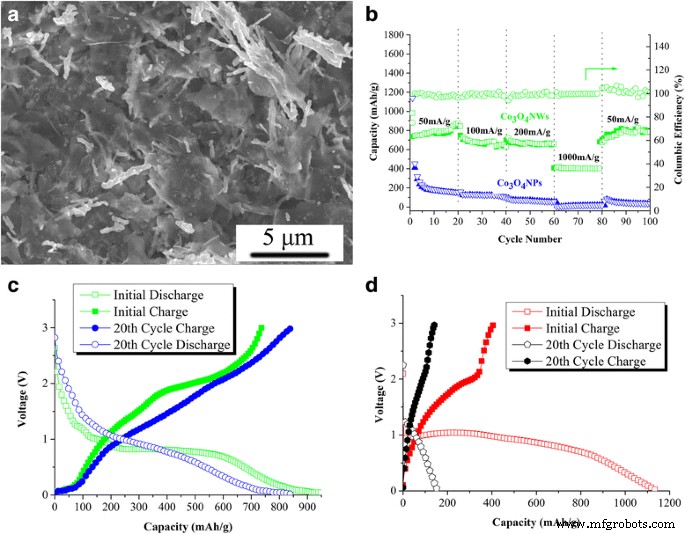
а СЭМ-изображения Co 3 О 4 Электрод NWs / df-GNS. б Оцените возможности Co 3 О 4 Новички и партнеры 3 О 4 НЧ при различных плотностях тока от 50 до 1000 мА / г. c , d Типичные кривые заряда и разряда Co 3 в начале / 20-м цикле О 4 NW ( c ) и Co 3 О 4 НП ( d )
Электрохимические характеристики электродов после их изготовления оценивали путем гальваностатического цикла заряда / разряда при различных плотностях тока в диапазоне от 50 до 1000 мА / г. Как видно, готовый Co 3 О 4 Электроды NWs / df-GNS обеспечивают обратимую емкость ~ 790 мАч / г после 20 циклов при плотности тока 50 мА / г, небольшое снижение емкости наблюдалось в течение первых 20 циклов заряда / разряда (как показано на рис. 6c). Между тем, Co 3 О 4 Электроды NPs / df-GNS, по-видимому, имели относительно высокую начальную емкость ~ 1130 мАч / г при первом разряде, даже выше, чем у Co 3 О 4 NWs / df-GNS (~ 980 мАч / г) и теоретическая емкость Co 3 О 4 (890 мАч / г). Мы считаем, что эта высокая начальная необратимая способность связана с образованием слоя поверхности раздела твердого электролита (SEI) в результате разложения электролита. Однако высокая начальная емкость Co 3 О 4 NPs / df-GNS казались крайне необратимыми и распадались до ~ 400 мАч / г во втором цикле. После 20 циклов при плотности тока 50 мА / г для Co 3 наблюдалось только ~ 150 мАч / г. О 4 Электрод NPs / df-GNS (как показано на рис. 6d). Когда плотность тока увеличилась до 100, 200 и 1000 мА / г, Co 3 О 4 Электрод NWs / df-GNS обеспечивал емкость ~ 680, ~ 650 и ~ 400 мАч / г соответственно, в то время как Co 3 О 4 Электрод NPs / df-GNS имеет очень низкую емкость (менее 150 мАч / г при 100–200 мА / г и менее 20 мАч / г при 1000 мА / г).
Когда плотность тока возвращается к 50 мА / г, в Co 3 была получена емкость, близкая к 800 мАч / г. О 4 NWs / df-GNS, а Co 3 О 4 Электрод NPs / df-GNS практически потерял способность накапливать литий-ионные аккумуляторы. Причина сильного снижения емкости Co 3 О 4 NPs / df-GNS можно отнести к следующим факторам:(1) большое изменение объема во время введения / извлечения лития, которое вызвало потерю контакта между активными материалами и проводящим наполнителем / токосъемником. Во время циклических процессов Co 3 О 4 Электрод из наночастиц постепенно утратил свой путь передачи электронов, что в конечном итоге привело к снижению емкости; (2) самоагрегированная конфигурация наночастиц привела к Li 2 Матрица O и / или слой гелеобразного полимера, оборачивающийся вокруг кластера наночастиц, который может препятствовать диффузии ионов и / или электронов в ядро кластера. Напротив, нанопроволока / графен 1D / 2D-гетероструктура в Co 3 О 4 Электрод NWs / df-GNS не только имеет плоскую конфигурацию, которая может выдерживать большое изменение объема, но также предлагает многочисленные пустоты и поры для усиления ионно-электронной передачи. В результате как циклические, так и скоростные характеристики Co3O4NWs / df-GNS были значительно улучшены по сравнению с Co3O4NPs / df-GNS, сохраняя высокую емкость после 100 циклов.
В дополнение к гальваностатическим испытаниям заряда-разряда, циклические вольтамперограммы (CV) изготовленного Co 3 О 4 NWs / df-GNS представлены на рис. 7а. В первом цикле наблюдались два катодных пика в диапазоне напряжений ~ 1,1 и ~ 0,4 В, что можно было соотнести с многоступенчатым электрохимическим восстановлением Co 3 О 4 Ли с образованием металлического Co (литиирование) [22]. Основной анодный пик при 2,2 В приписывается реакции окисления металлического Со с преобразованием Со 3 О 4 . Эту обратимую реакцию электрохимического превращения можно резюмировать следующим образом:
$$ {\ mathrm {Co}} _ 3 {\ mathrm {O}} _ 4 + 8 \ mathrm {Li} {\ displaystyle \ begin {array} {c} \ mathrm {разряд} \\ {} \ leftrightharpoons \\ { } \ mathrm {charge} \ end {array}} 3 \ mathrm {Co} +4 {\ mathrm {Li}} _ 2 \ mathrm {O} $$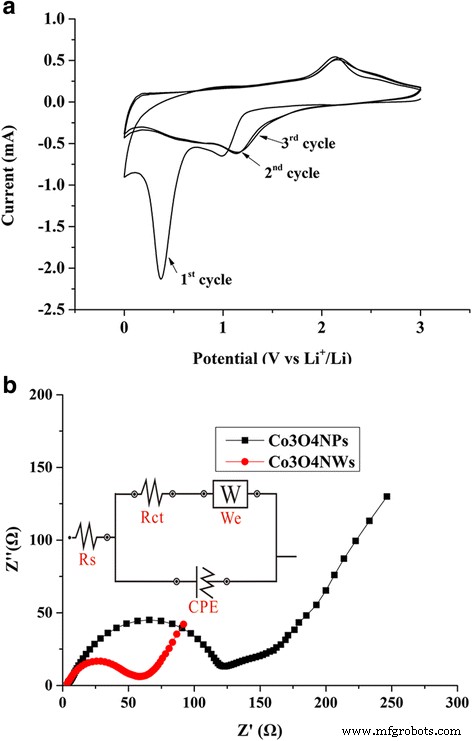
а Циклические вольтамперограммы Co 3 О 4 Электрод NWs / df-GNS со скоростью сканирования 0,5 мВ / с. б Спектры электрохимического импеданса Co 3 О 4 НПС / ДФ-ГНС и Ко 3 О 4 Электроды NWs / df-GNS, полученные путем наложения синусоидальной волны с амплитудой 5,0 мВ в диапазоне частот 100 кГц ~ 0,1 Гц
Наблюдался огромный сильный катодный пик при ~ 0,4 В в первом цикле; однако катодный пик во втором и третьем цикле в этой области напряжения проявился только как «выпуклость». Мы пришли к выводу, что во время первого процесса разряда образовывалась пленка на границе раздела твердый электролит (SEI), которая оставалась стабильной в последующих циклах. В результате CV-кривые второго и третьего циклов почти перекрывали друг друга, показывая катодные пики при 1,2 и 0,7 В и широкий анодный пик при 2,1 В. Такое поведение свидетельствует о стабилизированных слоях SEI и высокой электрохимической обратимости Co 3 О 4 Электроды NWs / df-GNS. Ко 3 О 4 NWs / df-GNS и Co 3 О 4 Электроды NPs / df-GNS также были охарактеризованы спектроскопией электрохимического импеданса (EIS). На графиках Найквиста двух электродов, показанных на рис. 7b, видны полукруг в высокочастотной области и наклонная линия в низкочастотной области. Данные импеданса могут быть помещены в эквивалентную электрическую схему, показанную на вставке к рис. 7b, в которой CPE - это элемент постоянной фазы, связанный с емкостью двойного слоя, We - импеданс Варбурга, а Rs и Rct - сопротивление электрохимической системы. и сопротивление переносу заряда соответственно. Сопротивление переноса заряда Rct Co 3 О 4 Расчетное сопротивление NWs / df-GNS составило 52,6 Ом; однако, что Co 3 О 4 NPs / df-GNS составляла 109 Ом. Мы предполагаем, что эта превосходная способность нанопроволок переносить заряд способствовала быстродействию электрода.
Выводы
Таким образом, мы предложили новую, легкую и безопасную для окружающей среды стратегию синтеза Co 3 О 4 NW с превосходной эффективностью и рентабельностью. В таких наноматериалах наблюдались отличные свойства аккумуляции лития. Результаты XRD и SAED показали, что полученный Co 3 О 4 Образцы ННК показали хорошее качество по химическому и фазовому составу. Ко 3 О 4 ННК со средним диаметром около 180 нм и длиной от 3 до 8 мкм наблюдались с помощью SEM и TEM. Эти нанопровода демонстрируют хорошие электрохимические характеристики, достигая емкости накопления лития выше 700 мАч / г в результате быстрого транспорта электронов и приспособляемости к изменению объема уникальной гибридной наноструктуры 1D-2D в сочетании с 2D-графеном.
Сокращения
- Co 3 О 4 :
-
Оксиды кобальта
- Co 3 О 4 НП:
-
Со 3 О 4 наночастицы
- Co 3 О 4 Новые версии:
-
Со 3 О 4 нанопроволоки
- Резюме:
-
Циклические вольтамперограммы
- DEC:
-
Диэтилкарбонат
- df-GNS:
-
Бездефектные графеновые нанолисты
- EC:
-
Этиленкарбонат
- EIS:
-
Электрохимическая импедансная спектроскопия
- GNS:
-
Нанолисты графена
- HRTEM:
-
ТЕМ высокого разрешения
- LIB:
-
Литий-ионные батареи
- NMP:
-
N -Метилпирролидон
- ПК:
-
Пропиленкарбонат
- SAED:
-
Электронная дифракция в выбранной области
- SEI:
-
Интерфейс твердого электролита
- SEM:
-
Эмиссионный растровый электронный микроскоп
- ТЕМ:
-
Просвечивающая электронная микроскопия
- XRD:
-
Рентгеноструктурный анализ
Наноматериалы
- Легкий синтез и оптические свойства малых нанокристаллов и наностержней селена
- Синтез квантовых точек ZnSe / CdS / ZnS Core / Shell с подавленной реабсорбцией и их применение для иммуносорбентного ана…
- СИНТЕЗ И ЭЛЕКТРОХИМИЧЕСКИЕ СВОЙСТВА КАТОДНЫХ МАТЕРИАЛОВ LiNi0.5Mn1.5O4 с легированием композитов Cr3 + и F− для литий-…
- Простой синтез окрашенного и проводящего композита CuSCN, покрытого наночастицами CuS
- Простой синтез серебряных нанопроволок с разным соотношением сторон и используемых в качестве высокоэффект…
- Синтез нанокристаллов ZnO и применение в инвертированных полимерных солнечных элементах
- Подготовка гибридных микроматериалов MnO2 с полипропиленовым покрытием и их улучшенные циклические характери…
- Синтез композита поли (3,4-этилендиокситиофен) / золото / графен в твердом состоянии и его применение для амперо…
- Синтез водорастворимых квантовых точек сульфида сурьмы и их фотоэлектрические свойства
- Синтез нанопластин Cu2ZnSnSe4 в одном резервуаре и их фотокаталитическая активность, управляемая видимым светом



