Наноносители на основе нуклеозидов и липидов для доставки сорафениба
Аннотация
Хотя применение сорафениба, небольшого ингибитора тирозиновых протеинкиназ, для лечения рака остается всемирным вариантом химиотерапии, необходимы новые стратегии для решения проблем с низкой растворимостью в воде (<5 мкМ), токсичностью и побочными эффектами этого препарата. В этом контексте в настоящее время исследуется использование наноносителей для преодоления этих недостатков. В этой статье мы сообщаем о новом типе наночастиц на основе сорафениба, стабилизированных гибридными нуклеозид-липидами. Твердые липидные наночастицы (SLN) показали отрицательные или положительные значения дзета-потенциала в зависимости от нуклеозидно-липидного заряда. Просвечивающая электронная микроскопия SLN, нагруженных сорафенибом, выявила наночастицы в форме параллелепипеда размером около 200 нм. Биологические исследования, проведенные на четырех различных клеточных линиях, включая рак печени и груди, выявили повышенную противоопухолевую активность SLN на основе сорафениба по сравнению со свободным лекарством. Важно отметить, что изображения микроскопии с контрастной фазой, записанные после инкубации раковых клеток в присутствии SLN при высокой концентрации в сорафенибе (> 80 мкМ), показали полную гибель раковых клеток во всех случаях. Эти результаты подчеркивают потенциал СЛУ на основе нуклеозидов и липидов в качестве систем доставки лекарств.
Фон
Сорафениб, выпускаемый на рынок под названием Нексавар ™, представляет собой гидрофобный лекарственный ингибитор киназы [1], одобренный для лечения различных видов рака человека, включая запущенную почечно-клеточную карциному (ПКР) [2], гепатоцеллюлярную карциному (ГЦК) [3] и позднюю стадию рака щитовидной железы. карцинома. Сорафениб имеет множество известных мишеней протеинкиназ, включая трансмембранные рецепторы и внутриклеточные тирозиновые и серин-треониновые киназы, а также было показано, что он вызывает апоптоз. Что касается механизма действия, сорафениб, как сообщается, подавляет рост опухоли с помощью нескольких мишеней, действуя непосредственно на опухоль и / или на ангиогенез опухоли (посредством ингибирования передачи сигналов VEGFR и PDGFR) [4, 5]. Его эффективность в подавлении роста злокачественных клеток была продемонстрирована при многих гистологических типах рака, таких как, например, меланома [6], щитовидная железа [7], поджелудочная железа [5], гепатоцеллюлярная карцинома и лейкемия [8]. Однако низкая растворимость в воде, токсичность и побочные эффекты ограничивают использование сорафениба во многих клинических применениях. Для решения этих проблем в настоящее время исследуются несколько составов сорафениба [9, 10], включая жидкокристаллические наночастицы [11], наноэмульсию [12], модифицированные циклодекстрином наночастицы пористого кремния [13], нанокомпозиты с лекарственным покрытием [14], полиэлектролит наночастицы на основе [15] или самоорганизующиеся наночастицы куркумина [16]. Однако липидные наночастицы (НЧ), содержащие сорафениб, мало изучены [17, 18].
Здесь мы сообщаем о первом примере твердых липидных наночастиц (SLN) на основе сорафениба [19], стабилизированных нуклеозид-липидами [20,21,22]. Хроматографические исследования положительно и отрицательно заряженных нуклеолипидов (DOTAU и diC 16 dT соответственно) указывают на то, что эти амфифилы обладают необходимой стабильностью и чистотой для их использования в рамках приложений доставки лекарств [23, 24]. Простая процедура нанопреципитации позволяет формировать SLN с положительными (SLN + ) или отрицательные заряды (SLN - ) (Рисунок 1). Стоит отметить, что все исследованные SLN усиливали цитотоксический эффект сорафениба на различные карциномы человека, демонстрируя, что SLN могут преодолевать ограничения сорафениба с точки зрения растворимости в воде и противораковой активности.
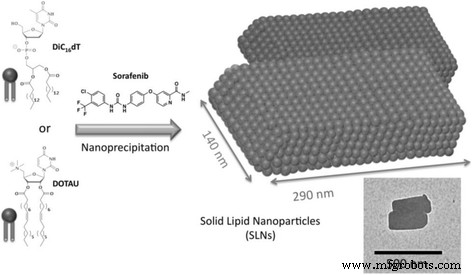
Схема получения СЛУ. Химические структуры анионного нуклеотид-липида тимидина 3 '- (1,2-дипальмитоил- sn -глицеро-3-фосфат) (diC 16 dT), катионно-нуклеозид-липид DOTAU (2 ', 3'-диолеил-5'-дезокси-5'-триметиламмоний-уридин) и сорафениб, использованный в этом исследовании (слева). Схематическое изображение SLN с формой параллелепипеда, полученное после нанопреципитации нуклеолипида (либо diC 16 dT или DOTAU, ведущие к SLN - и SLN + соответственно) с сорафенибом (справа). Схематическое изображение адаптировано из изображения просвечивающей электронной микроскопии (ТЕМ), на котором показаны наночастицы, содержащие сорафениб DOTAU (вставка, полоса 500 нм)
Методы
Химические вещества и реагенты
Метанол (MeOH), муравьиная кислота (FA) и формиат аммония (AFNH 4 ) были приобретены у VWR Chemicals (Франция), и все они были чистыми для ВЭЖХ (высокоэффективной жидкостной хроматографии). Вода для ВЭЖХ (минимальное удельное сопротивление 18,2 МОм) была произведена компанией ELGA Millipore system (Франция). DOTAU (номер CAS:868226-06-6) и diC 16 dT (номер CAS:1160002-70-9) были синтезированы в лаборатории в соответствии с протоколом, описанным в ссылках [23,24,25]. Сорафениб, 4- [4 - [[4-хлор-3- (трифторметил) фенил] карбамойламино] фенокси] - N -метилпиридин-2-карбоксамид (номер CAS:284461-73-0) был приобретен у SynVec http://synvec.fr (Ref # D114250414).
Хроматографические исследования
Метод обращенно-фазовой УВЭЖХ (сверхвысокопроизводительной жидкостной хроматографии) был разработан для нуклеолипидов (DOTAU и diC 16 dT) и количественное определение сорафениба в SLN. Перед введением методом ВЭЖХ водные растворы наночастиц разбавляли этанолом в 5 и 10 раз для количественного определения нуклеолипидов и сорафениба соответственно.
Использовали хроматографическую систему UHPLC UltiMate 3000 от Dionex-Thermo Scientific (США), состоящую из насоса с системой четвертичных клапанов для выбора колонки, термостатированного автоматического пробоотборника и термостатированного отсека для колонки. Разделение проводили на колонке Syncronis C18 50 × 2,1 мм, 1,7 мкм. Подвижная фаза состояла из 70/30 MeOH / 25 мМ ацетата аммония (pH =7,4) (A) и 26,5 мМ ацетата аммония в MeOH (pH =7,9) (B). Использовалась скорость потока 0,2 мл / мин, профиль градиента составлял 0–2 мин, 0–100% B; 2–20 мин, 100% Б. Температуру колонки устанавливали на уровне 25 ° C. Обнаружение сорафениба и diC 16 проводили при 267 нм. dT и 257 нм для DOTAU. Введенный объем составлял 1 мкл, что приводило к пределу количественного определения 0,6 нг для сорафениба и 15 нг для нуклеолипидов, а также DOTAU и diC 16 dT.
Стандартные кривые для сорафениба, DOTAU и diC 16 dT в этаноле показаны в дополнительном файле 1:рисунки SI1, SI2 и SI3 соответственно.
Приготовление наночастиц сорафениба
Десять миллиграммов сорафениба растворяли в 1 мл этанола и 10 мг NL (либо diC 16 dT или DOTAU) растворяли в 1 мл этанола. Сто микролитров NL, 100 мкл растворов сорафениба и 800 мкл этанола смешивали вместе при комнатной температуре и добавляли по каплям в 10 мл дистиллированной воды при магнитном перемешивании. Раствор помещали в ультразвуковую баню на 90 мин при 25 ° C. Этанол удаляли в вакууме при 30 ° C, и объем доводили до 1 мл. Этот раствор дважды обрабатывали ультразвуком с использованием ультразвукового зонда 6 мм (Vibracell 75186) в течение 10 минут при 100% амплитуде с импульсом 2 секунды каждые 5 секунд. Один миллилитр диализовали против 30 мл дистиллированной воды в течение 3 × 15 мин. Этот объем доводят до 2 мл и сохраняют для количественного определения характеристик и исследований стабильности. Кроме того, контрольные эксперименты были проведены по тому же протоколу в отсутствие нуклеолипидов.
Просвечивающая электронная микроскопия (TEM и EDX)
Наночастицы визуализировали с помощью микроскопии с отрицательным окрашиванием. Десять микролитров наночастиц переносили на покрытую углеродом медную сетку на 10 мин. Затем образец сушили и окрашивали 2,5% ( w / w ) уранилацетата в воде в течение 2 мин. Образцы наблюдали с помощью электронного микроскопа Hitachi H 7650. Энергодисперсионная рентгеновская спектроскопия была выполнена с использованием просвечивающего электронного микроскопа TECNAI в сочетании с Quantax-X-Flash SVE 6.
Размер частиц и определение дзета
Дзета и размер частиц определяли с использованием Zetasizer NanoZS, Malvern. Эксперименты проводились с 40 мкл наночастиц, разведенных в 400 мкл воды, а измерения проводились при 25 ° C.
Анализ цитотоксичности
HuH7 и HepG2 выращивали в монослое в среде DMEM-Glutamax с добавлением 10% фетальной телячьей сыворотки. MDA-MB-134 и T-47D выращивали в монослое в RPMI с добавлением 10% фетальной телячьей сыворотки (только для T-47D, заменитель AA 1X, глюкоза 0,45%, инсулин 10 мг / л -1 и пируват натрия 1X). Все реактивы для культивирования были от Invitrogen. 10 4 клеток на лунку в 90 мкл полной культуральной среды высевали в 96-луночный планшет и инкубировали в течение 24 часов при 37 ° C и 5% CO 2 перед добавлением 10 мкл SLN или сорафениба в культуральную среду. Сорафениб (номер CAS:284461-73-0) растворяли в культуральной среде с 0,1% ДМСО. Обратите внимание, что в этих условиях максимальная концентрация сорафениба без преципитации составляла 5 мкМ, тогда как для SLN, нагруженных сорафенибом, максимальная протестированная концентрация составляла 120 мкМ без ДМСО. После 4 дней инкубации жизнеспособность клеток оценивали с помощью анализа пролиферации на основе формазана (набор для анализа пролиферации клеток с одним водным раствором CellTiter 96®, Promega) путем добавления 20 мкл на лунку раствора реагента. После 30-минутной инкубации при 37 ° C, 5% CO 2 оптическую плотность каждой лунки измеряли при длине волны 492 нм с использованием спектрофотометра Бертольда. Результаты выражаются в процентах от \ (\ frac {{\ mathrm {OD}} _ {492} \ \ mathrm {of} \ \ mathrm {обращено} \ \ mathrm {cells} - {\ mathrm {OD}} _ {492} \ \ mathrm {of} \ \ mathrm {blank}} {\ {\ mathrm {OD}} _ {492} \ mathrm {of} \ \ mathrm {untreated} \ \ mathrm {cells} - {\ mathrm {OD}} _ {492} \ \ mathrm {of} \ \ mathrm {blank}} \).
Исследования жизнеспособности клеток
HuH7 выращивали, как описано ранее в разделе «Анализ цитотоксичности». Жизнеспособность клеток определяли через 4 дня инкубации с SLN + загружен сорафенибом в различных концентрациях (0, 1, 5, 10, 25, 50 и 100 мкМ) с использованием анализа жизнеспособности живых / мертвых клеток (Invitrogen). Вкратце, культуральную среду удаляли и прикрепленные клетки один раз промывали сбалансированным солевым раствором Хенкса (HBSS). Двести микролитров HBSS, содержащего 2 мкМ ацетоксиметилового эфира кальцеина и 4 мкМ гомодимера этидия-1, добавляли в каждую лунку и инкубировали в течение 45 мин при 37 ° C и 5% CO 2 . После окрашивания клетки один раз промывали HBSS и получали микроскопическое изображение на инвертированном флуоресцентном микроскопе. Процент мертвых клеток оценивали с помощью анализа сортировки клеток с активацией флуоресценции (FACS). После окрашивания 4 мкМ раствора гомодимера этидия-1 клетки обрабатывали трипсином и дважды промывали фосфатно-солевым буфером (PBS) центрифугированием при 1000 об / мин в течение 5 мин. Данные были получены на проточном цитометре LSRFortessa от Becton Dickinson, и результаты были проанализированы с использованием программного обеспечения DIVA. Образец мертвых клеток был приготовлен с использованием 70% метанола и использован в качестве контроля.
Результаты и обсуждение
Синтез и характеристика SLN
Нетоксичность и свойства самосборки нуклеолипидов делают их идеальными амфифильными адъювантами для инкапсулирования гидрофобных лекарственных средств, таких как сорафениб. В этом исследовании была разработана простая процедура нанопреципитации для решения проблемы низкой растворимости в воде сорафениба и повышения его противораковой активности, что во многих случаях ограничивает его клиническое использование. Что касается растворимости в воде, мы предположили, что гидрофобный характер, гетероциклы и функции водородных связей сорафениба будут способствовать взаимодействиям с нуклеолипидами и образованию нанообъектов. Также ожидалось, что SLN, загруженные сорафенибом, должны увеличить противоопухолевую активность за счет увеличения клеточного поглощения сорафениба. Действительно, в одном из наших предыдущих исследований, проведенных на наночастицах цисплатина, мы продемонстрировали, что усиление противоопухолевой активности цисплатина было связано с увеличением количества лекарственного средства, интернализированного в раковые клетки [23] [1]. Наш процесс нанопреципитации включает три этапа:(i) солюбилизация сорафениба в этаноле при 40 ° C (10 мг / мл сорафениба, 100 мкл) и добавление одного эквивалента нуклеолипида (либо анионного нуклеотид-липида, diC 16 -3′-dT [тимидин 3 ′ - (1,2-дипальмитоил- sn -глицеро-3-фосфат)] или катионный нуклеозид-липид DOTAU [23] [2 ', 3'-диолеил- 5' -деокси-5'-триметиламмоний-уридин], 100 мкл раствора с концентрацией 10 мг / мл в этаноле; (ii) 1 мл этанольного раствора добавляют по каплям при комнатной температуре к 10 мл дистиллированной воды; и (iii) полученную суспензию упаривали для удаления избытка этанола и обрабатывали ультразвуком.
Хроматографические исследования
Чтобы оценить способность новых препаратов к загрузке лекарственного средства, был разработан метод обращенно-фазовой УВЭЖХ. Используя этот метод ВЭЖХ, одновременное разделение сорафениба и нуклеолипидов было достигнуто за 12 минут, что позволило провести индивидуальное квантование соединений в SLN (дополнительный файл 1:Рисунок SI1–4).
Коэффициенты загрузки (массовые отношения сорафениб / нуклеолипиды в наночастицах) 50 и 80% и выходы инкапсуляции сорафениба около 55 и 75% были получены для составов, состоящих из сорафениба / DOTAU (SLN + ) и сорафениб / diC 16 dT (SLN - ), соответственно. Во время контрольного эксперимента, проведенного в отсутствие нуклеолипида, около 90% сорафениба было потеряно на различных этапах приготовления препарата, вероятно, из-за низкой растворимости сорафениба в воде. Этот результат демонстрирует, что нуклеолипиды необходимы для солюбилизации сорафениба и стабилизации SLN.
Физико-химические исследования
Для характеристики образования SLN были проведены эксперименты по динамическому рассеянию света (DLS). И отрицательные, и положительные нуклеолипиды (diC 16 dT и DOTAU) образуют аналогичные несферические наночастицы с формой параллелепипеда в водном растворе с монодисперсностью (индекс полидисперсности, PDI =0,202 и 0,289; размер =335,2 и 304,4 нм, соответственно, рис. 2 и дополнительный файл 1:рис. SI7). Как и ожидалось, дзета-потенциалы объектов на основе SLN зависят от полярных голов нуклеолипидов ( ζ =+ 59,1 и - 54,9 мВ для SLN + и SLN - , см. Дополнительный файл 1:Рисунок SI10). Присутствие сорафениба в NP было подтверждено с помощью ПЭМ-изображений, а получение EDX SLN- было выполнено с помощью EDX-снимков. На рис. 2д, е показаны пятна I и II. Пятно I на рис. 2f демонстрирует излучение атома хлора (пятно I, рис. 2e, f), указывающее на присутствие сорафениба (см. Химическую структуру на рис. 2f). Обратите внимание, что хлор присутствует только в пятне I, а не во втором пятне (рис. 2е).
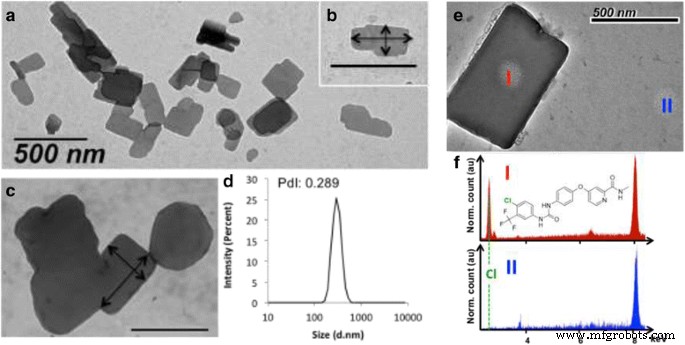
Характеристика SLN. Изображения просвечивающей электронной микроскопии (ПЭМ), показывающие морфологию наночастиц сорафениба с DOTAU ( a ) и вставка ( b ). Пример SLN на основе DOTAU с размером 327 на 172 нм (стрелки), что подтверждает средний размер 304 нм, измеренный DLS ( d ). c Пример изображения ПЭМ, показывающего diC 16 dT-SLN (стрелки 330 на 500 нм соответственно). ( е ) ТЕМ изображение SLN-. Точки I и II - это локализации, в которых было выполнено получение EDX. ( е ) EDX-спектры в положениях I и II. Пунктирной линией выделено излучение атома хлора, которое присутствует только в I. Также представлена химическая структура молекулы сорафениба. Оба спектра нормированы на излучение атома Cu при 8 кэВ (из-за сетки TEM Cu)
Важно отметить, что в контрольных экспериментах нанопреципитация сорафениба в отсутствие нуклеолипида не приводила к появлению каких-либо нанообъектов, демонстрируя, что нуклеолипиды позволяют формировать и стабилизировать SLN.
Исследования стабильности
Коллоидная стабильность SLN + и SLN - были измерены с помощью DLS и дзета-потенциала при двух температурах (рис. 3а и дополнительный файл 1:рис. SI10). В случае diC 16 Составы на основе dT, размер SLN - не был изменен через 30 дней как при 4, так и при 37 ° C, что указывает на высокую стабильность этих наночастиц (дополнительный файл 1:рисунок SI9). Такая стабильность может быть объяснена характером взаимодействий (с участием Н-связей, π - π накопление, взаимодействие заряда / заряда) между диС 16 dT и сорафениб. Однако для составов на основе DOTAU SLN + были стабильными только при 4 ° C в течение 30 дней, как показали исследования DLS (рис. 3a), тогда как при 37 ° C наблюдалось увеличение как размера, так и PDI (рис. 3a). Эта относительная нестабильность наблюдается при 37 ° C в случае SLN + можно объяснить отталкивающими кулоновскими взаимодействиями, происходящими между положительными зарядами как сорафениба, так и DOTAU. Интересно, что исследования коллоидной стабильности показывают, что можно регулировать стабильность, следовательно, доставку сорафениба из SLN в физиологическую среду, в зависимости от нуклеолипида, используемого для стабилизации SLN. Модуляция стабильности может быть привлекательной в зависимости от необходимой кинетики высвобождения.
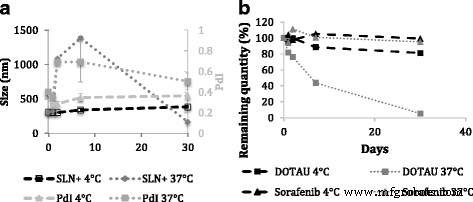
Исследования стабильности SLN. Коллоидная стабильность SLN + ( а ) и химическая стабильность сорафениба и DOTAU в SLN + от времени при 4 и 37 ° C ( b ). PDI, индекс полидисперсности
Наряду с коллоидной стабильностью, химическая стабильность сорафениба, DOTAU и diC 16 dT в составах на основе SLN исследовали как функцию времени при 4 и 37 ° C с использованием нового хроматографического метода (см. дополнительный файл 1:рисунок SI4). Кинетические исследования при обеих температурах показаны на рис. 3b и в дополнительном файле 1:SI5 для DOTAU-SLN и diC 16 dT-SLN соответственно. Результаты показывают, что сорафениб и diC 16 Молекулы dT в составах остаются стабильными в течение как минимум 1 месяца, что указывает на долгосрочную химическую стабильность при обеих температурах в случае SLN - . Однако снижение DOTAU со временем наблюдалось в SLN + составы. Во-первых, при 4 ° C были измерены потери около 12% за 7 дней и 20% за 30 дней. При повышении температуры стабильность DOTAU снижалась с потерей 55% за 7 дней и до 95% за 30 дней при 37 ° C. Такие различия в химической стабильности между нуклеолипидами уже были подтверждены в ходе предыдущих исследований стабильности (см. Дополнительный файл 1:Рисунок SI6).
Биологические исследования
Цитотоксичность SLN оценивали по активности метаболизма и морфологии клеток. Анализ МТТ позволил сравнить свободный сорафениб (в 0,1% ДМСО) и SLN, нагруженные лекарством (рис. 4), на четырех клеточных линиях, включая две гепатокарциномы (HuH7 и HepG2) и два рака просвета молочной железы (MDA-MB-134 и T- 47D). Во-первых, при концентрациях, близких к максимальной растворимости свободного сорафениба (5 мкМ сорафениба в 0,1% ДМСО, 2,8 мкМ для сорафениба / DOTAU и 4 мкМ для сорафениба / diC 16 dT), оба SLN подавляли жизнеспособность клеток лучше, чем свободный сорафениб. Как показано на рис. 4b, исследование жизнеспособности клеток, проведенное на клетках MDA-MB-134, показало, что активность свободного сорафениба ограничена его растворимостью в воде (100% жизнеспособности клеток при [сорафенибе] =5 мкМ), тогда как IC 50 значения 15 и 50 мкМ наблюдались для SLN + и SLN - соответственно (рис. 4б). В исследовании FACS, полученном на HuH7, IC 50 примерно 50 мкМ (дополнительный файл 1:рисунки SI12 и SI13). Изображения фазово-контрастной микроскопии действительно показывают пониженную плотность слоев клеток, обработанных либо SLN - и SLN + по сравнению с необработанными или обработанными сорафенибом клетками без изменения морфологии клеток (дополнительный файл 1:рисунок SI11). Во-вторых, аналогичные эксперименты были проведены при более высоких концентрациях SLN ([сорафениб] =120 и 84 мкМ для SLN - и SLN + соответственно) и по сравнению со свободным сорафенибом на пределе его растворимости (концентрация 5 мкМ). В этих условиях оба СЛУ проявляют сильное цитотоксическое действие на четыре линии раковых клеток, как показано на рис. 5. Как показано на изображениях фазово-контрастной микроскопии, для обоих СЛУ - наблюдались клеточные остатки. (Рис. 5C1–4) и SLN + (Рис. 5D1–4), что свидетельствует о гибели клеток, тогда как клетки остаются живыми в случае свободного сорафениба (Рис. 5B1–4). Стоит отметить, что сильные цитотоксические эффекты для обоих SLN наблюдались в случае клеток рака молочной железы в просвете B (рис. 5C1–2 и D1–2). Такой противоопухолевый эффект, о котором ранее не сообщалось, открывает новые возможности терапевтического применения сорафениба благодаря СЛУ.
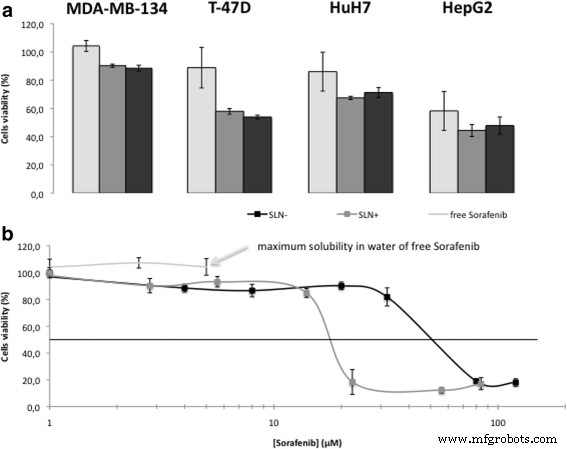
Цитотоксический эффект сорафениба или СЛУ. а ) Сравнение цитотоксичности со свободным сорафенибом или SLN сорафениба в 4 линиях клеток (2 просвета рака молочной железы B и 2 гепатокарциномы) после количественной оценки с помощью анализа MTS в 3 лунках при 5 мкМ свободного сорафениба, 2,8 мкМ NPs Sorafenib / DOTAU (SLN + ) и 4 мкМ НЧ Sorafenib / diC16dT (SLN-). б ) Анализ жизнеспособности клеток (клетки MDA-MB-134) в присутствии свободного сорафениба (ограниченная растворимость), SLN + (серый) или SLN- (черный)
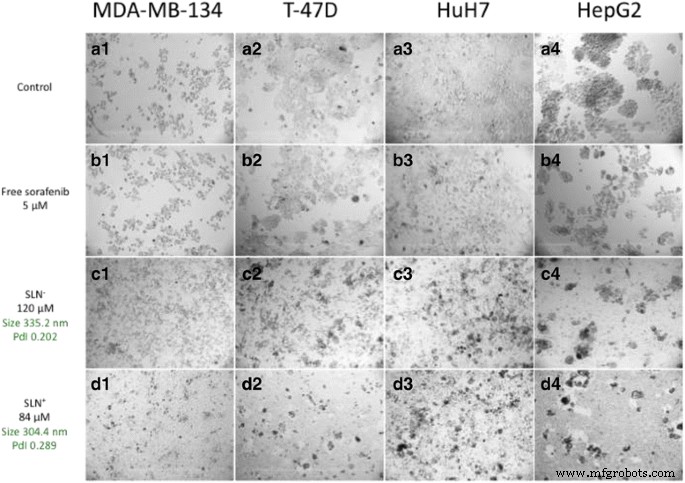
Сравнение морфологии клеток между контролем, свободным сорафенибом или SLN. Фазово-контрастные микроскопические изображения, показывающие цитотоксичность в различных условиях на четырех клеточных линиях карциномы человека (гепатокарциномы, HuH7, HepG2 и люминальная карцинома молочной железы MDA-MB-134, T-47D). A) В отсутствие сорафениба (контрольные эксперименты, A1 - A4 для MDA-MB-134, T-47D, HuH7, HepG2, клеточных линий соответственно). Б) Клетки инкубировали в течение 4 дней в присутствии 5 мкМ свободного сорафениба. C и D) клетки, инкубированные в присутствии SLN - и SLN + при концентрации сорафениба 84 и 120 мкМ соответственно
Заключение
Мы сообщаем о новом подходе, основанном на нуклеолипидах, который обеспечивает эффективную инкапсуляцию и доставку сорафениба. Наши исследования демонстрируют образование двух типов твердых липидных наночастиц (SLN), сильно загруженных сорафенибом. Эти SLN, которые показывают либо отрицательные, либо положительные значения дзета-потенциалов, имеют форму параллелепипеда. Как показали исследования DLS и HPLC, стабильность SLN можно регулировать в зависимости от используемого нуклеолипида. Важно отметить, что оба SLN + и SLN - составы способны резко повысить растворимость сорафениба в воде (концентрации выше 120 мкМ). Такие SLN проявляют лучшую противоопухолевую активность в отношении четырех линий раковых клеток (рака печени и молочной железы) по сравнению со свободным сорафенибом, действие которого ограничено из-за его недостаточной растворимости в воде. Контрастно-фазовые микроскопические изображения, записанные на четырех линиях раковых клеток, демонстрируют резкую гибель клеток при инкубации с 120 мкМ SLN - или 84 мкМ SLN + . Следовательно, этот препарат можно использовать в качестве новых терапевтических возможностей в случае рака печени (например, использование сорафениба во внутриартериальной химиотерапии) или рака груди. Насколько нам известно, этот отчет является первым примером исследования сорафениба против рака молочной железы B просвета, демонстрирующим полезность подхода SLN. В целом результаты, представленные в этой публикации, подчеркивают потенциал СЛУ на основе нуклеозидов и липидов в качестве систем доставки лекарств.
Сокращения
- AFNH 4 :
-
Формиат аммония
- DLS:
-
Динамическое рассеяние света
- FA:
-
Муравьиная кислота
- HCC:
-
Гепатоцеллюлярная карцинома
- ВЭЖХ:
-
Высокоэффективная жидкостная хроматография
- LN:
-
Липидные наночастицы
- MeOH:
-
Метанол
- PDI:
-
Индекс полидисперсности
- RCC:
-
Почечно-клеточный рак
- SLN:
-
Твердые липидные наночастицы
- УВЭЖХ:
-
Сверхвысокопроизводительная жидкостная хроматография
Наноматериалы
- Нановолокна и нити для улучшенной доставки лекарств
- Нано-гетеропереходы для солнечных элементов
- Металлоорганические каркасы, реагирующие на окружающую среду, как система доставки лекарств для терапии опу…
- Три основы планирования маршрутов для крупных розничных торговцев
- Как улучшить доставку на последнюю милю для небольших отправлений
- Шесть способов подготовиться к задержке крупных заказов
- Доставка из магазина в тот же день? Пять советов по ускорению доставки
- Будущее бесконтактной доставки
- Новая роль Интернета вещей в системе оказания медицинской помощи
- Микророботы, напечатанные на 3D-принтере, обещают доставку лекарств



