Фотокаталитически улучшенное удаление катионных красителей с помощью слоистых двойных гидроксидов Zn-Al
Аннотация
Прокаленные и органо-модифицированные слоистые двойные гидроксиды Zn-Al (СДГ) были изучены в качестве адсорбентов и фотокатализаторов для удаления катионных красителей, таких как метиленовый синий (МБ) . Zn-Al СДГ с катионным соотношением 2:4 были получены методом соосаждения. Образцы после синтеза прокаливали при различных температурах, а фазовые превращения исследовали методами XRD, TG / DTG и UV-vis-DR. Активность синтезированных и прокаленных СДГ Zn-Al в УФ-свете приписывалась присутствию фазы ZnO. Количество ZnO в СДГ можно регулировать, варьируя соотношение Zn / Al и температуру нагрева. Влияние соотношения Zn / Al на фотокаталитическую активность СДГ наблюдалось преобладающим образом. Прокаленные Zn-Al СДГ продемонстрировали низкую адсорбцию МБ. Модификацию СДГ ZnAl додецилсульфатом натрия проводили методом реконструкции. Наногибриды органо / СДГ продемонстрировали высокую адсорбционную способность к МБ. Удаление МБ из растворов с органо / Zn-Al СДГ было улучшено за счет использования ультрафиолетового света из-за фотодеструкции МБ.
Фон
Удаление опасных органических красителей из сточных вод и устранение загрязняющих веществ в поверхностных водах, грунтовых водах является серьезной проблемой в мире. Для обработки сточных вод, содержащих красители, известно несколько традиционных методов, включая адсорбцию, коагуляцию, флокуляцию, озонирование, мембранную фильтрацию, ионный обмен, окисление и химическое осаждение [1, 2]. Адсорбция - недорогой метод, не требующий специальной настройки. В последние годы было разработано множество видов адсорбентов с каталитической функцией, которые используются для удаления из воды нитратов, тяжелых металлов и органических загрязнителей [3,4,5].
Было исследовано использование слоистых двухслойных гидроксидов (СДГ) в качестве альтернативных материалов для удаления органических красителей из водных сред [6,7,8]. СДГ известны как анионные глины и гидроталькитоподобные материалы. Их основная структура напоминает структуру брусита, Mg (OH) 2 , когда дробь x двухвалентных катионов изоморфно замещается трехвалентными катионами, образуя положительно заряженные слои. Химический состав СДГ выражается общей формулой [M 2+ 1 − x M 3+ x (ОН) 2 ] [A n– ] x / n · ZH 2 O, где M 2+ может быть обычным явлением; Мг 2+ , Zn 2+ , или Ni 2+ , и M 3+ может быть обычным явлением; Аль 3+ , Га 3+ , Fe 3+ , или Mn 3+ . Безрамочный заряд, компенсирующий неорганический или органический анион (CO 3 2– , Cl - , SO 4 2– , RCO 2 - ) подписывается как A n− ; x обычно составляет 0,2-0,4. Слои LDH получают положительный заряд за счет изоморфного замещения M 3+ для M 2+ , что компенсируется межслоевыми анионами и водой [9].
Термическая обработка СДГ приводит к потерям физадсорбированных и межслоевых молекул воды, ОН - группы слоев и уравновешивающие заряд анионы. Слоистая структура разрушается и образуется смешанный твердый раствор оксидов металлов. Смешанные оксиды обычно обладают большой удельной поверхностью, термической стабильностью и синергическим взаимодействием между различными металлическими компонентами. Таким образом, продукты прокаливания СДГ нашли широкое применение в различных каталитических процессах [10,11,12].
Благодаря своей анионообменной способности СДГ подходят для интеркаляции и сорбции анионных красителей, но неприменимы для катионных красителей. Модификация поверхности СДГ анионными ПАВ позволяет получать композиты, способные адсорбировать различные типы органических молекул [13, 14]. ЛДГ, модифицированные додецилсульфатом (DS), продемонстрировали чрезвычайно высокую сорбцию катионных красителей, таких как сафранин [15], метиленовый синий [16] и основной синий [17].
В последнее время СДГ интенсивно исследуются как перспективные гетерогенные фотокатализаторы из-за их внутренних характеристик фотоотклика, низкой стоимости, а также простоты получения и модификации [18]. СДГ в качестве фотокатализаторов продемонстрировали высокую эффективность преобразования энергии в результате высокой дисперсии активных частиц в слоистой матрице, что облегчает разделение зарядов. Смешанные оксиды с полупроводниковыми свойствами получают прокаливанием соответствующих СДГ, содержащих переходные металлы. Катионы металлов, например Zn 2+ . и Ti 4+ , могут быть введены в слои [19, 20]. Их относительные пропорции можно варьировать в широких пределах, что дает возможность получать полупроводниковые оксиды с регулируемыми свойствами. Фотокаталитические приложения СДГ - интересная развивающаяся область. Было изучено несколько полупроводниковых смешанных оксидов, полученных из СДГ, таких как Zn-Al [20], Zn-Ce, ZnFe, Zn-Cr [21], Mg-Zn-Al [22] и Zn-Ga [23]. для фотокаталитического разложения загрязняющих веществ.
Помимо нежелательного цвета, продукты распада красителей также оказывают мутагенное или канцерогенное действие на человека, и их прием внутрь может вызвать серьезный ущерб организмам. Хлор и хлорноватистая кислота, образующиеся при разложении, являются сильными токсичными окислителями. Они могут окислять органические вещества и одновременно восстанавливаются до хлоридов [24]. Как важный базовый краситель, используемый для печати ситца, окрашивания хлопка и кожи, МБ может вызывать различные вредные эффекты, такие как ожоги глаз, раздражение желудочно-кишечного тракта и кожи. [25].
Продемонстрирована высокая адсорбционная способность прослоек Zn-Al, модифицированных ДС для метиленового синего (МБ) [26]. Присутствие фотоактивного компонента в адсорбенте может повысить эффективность материалов на основе Zn-Al LDH для удаления катионного красителя с помощью УФ-излучения. Таким образом, в настоящей работе были определены оптимальные условия приготовления Zn-Al СДГ для удаления катионного красителя, такого как МБ, путем адсорбции и фотодеструкции.
Методы
Синтез Zn-Al LDH
Все химические вещества были аналитической чистоты и использовались без дополнительной очистки. Zn-Al СДГ с карбонатом в качестве межслоевого аниона с [Zn]:[Al] =1:2 были синтезированы методом соосаждения при постоянном pH, аналогичном [9]. Первый раствор, содержащий Na 2 CO 3 (0,5 М) и NaOH (1,5 М). Второй раствор, содержащий смесь нитратов металлов Zn (NO 3 ) 2 ∙ 6H 2 O и Al (NO 3 ) 3 ∙ 9H 2 О (общая концентрация металла составляла 0,6 М, молярное соотношение Zn / Al 2:1, 3:1, 4:1) готовили и осторожно добавляли по каплям к первому раствору при перемешивании. PH доводили до 10 добавлением NaOH. После завершения добавления температуру повышали до 85 o . C, и суспензию выдерживали в течение 6 ч при этой температуре при непрерывном перемешивании. После этого суспензию охлаждали до комнатной температуры в течение нескольких часов. Продукт выделяли фильтрованием и несколько раз промывали деионизированной водой до pH 7. После этого твердое вещество сушили при 100 ° C. Образцы были обозначены как ZnAl 21 . ЛДГ, ZnAl 31 ЛДГ и ZnAl 41 LDH.
Синтезированные выше Zn-Al СДГ прокаливали при 450 ° C в течение 2 часов и при 600 ° C в течение 1, 2 и 5 часов на воздухе. Образцы были обозначены как ZnAl 21 . -450, ZnAl 31 -450, ZnAl 41 -450, ZnAl 21 -600-1, ZnAl 31 -600-1, ZnAl 41 -600-1, ZnAl 21 -600-2, ZnAl 31 -600-2, ZnAl 41 -600-2, ZnAl 21 -600-5, ZnAl 31 -600-5, ZnAl 41 -600-5.
Zn-Al СДГ были модифицированы додецилсульфатом натрия CH 3 . (Канал 2 ) 11 SO 4 Na методом реконструкции. Суспензии 1 г прокаленных СДГ и 50 мл 0,05 М водных растворов ДС перемешивали 24 ч при комнатной температуре. Полученные композиты были обозначены как ZnAl 21 . -450 / DS, ZnAl 31 -450 / DS, ZnAl 41 -450 / DS, ZnAl 21 -600-1 / DS ZnAl 31 -600-1 / DS ZnAl 41 -600-1 / DS.
Характеристика
Рентгенограммы образцов регистрировали на дифрактометре ДРОН-4-07 (ООО «Буревестник», Санкт-Петербург, Россия), (CuK α радиация). Термогравиметрический анализ (ТГА) и дифференциальный термический анализ (ДТА) проводили на аппарате Derivatograph Q-1500 D (MOM, Венгрия), работающем в потоке воздуха при скорости нагрева 10 ° мин -1 . Спектры диффузного отражения получали на спектрометре Lambda 35 UV-Vis (Perkin Elmer, Германия), оборудованном интегрирующим устройством Labsphere RSA-PR-20 в диапазоне длин волн 200-1000 нм. УФ-видимые спектры растворов регистрировали с помощью спектрометра Lambda 35 UV-Vis (Perkin Elmer, Германия).
Фотокаталитический эксперимент
0,020 г СДГ Zn-Al было диспергировано в 40 мл 9 × 10 -5 M (для кальцинированных СДГ) и 10 -4 М (для СДГ, модифицированных ДС) водный раствор МБ в кварцевом реакторе. Перед освещением суспензии перемешивали в течение 1 ч (прокаленные СДГ) и 24 ч (СДГ, модифицированные ДС) в темноте для достижения адсорбционно-десорбционного равновесия между фотокатализатором и молекулами МБ. Затем раствор облучали в течение 3 ч ртутной лампой (λ max =365 нм) при магнитном перемешивании. Через заданные интервалы времени раствор анализировали путем измерения спектров поглощения с использованием спектрометрии УФ-видимого диапазона.
Результаты и обсуждения
Характеристика
Рентгенограмма синтезированных СДГ Zn – Al с различными Zn 2+ / Аль 3+ катионные отношения представлены на рис. 1а. Структура, подобная гидротальциту, образовалась при всех соотношениях катионов. На рентгенограммах присутствуют характерные рефлексы, относящиеся к слоистым двойным гидроксидам. Дополнительная фаза ZnO присутствовала в ZnAl 41 ЛДГ, как показано на рентгенограммах. Пики 2θ при 31,9 °, 34 ° и 36,2 ° принадлежат фазе ZnO, образующейся на поверхности бруситоподобных листов. Все отражения резкие, что указывает на высококристаллический материал.
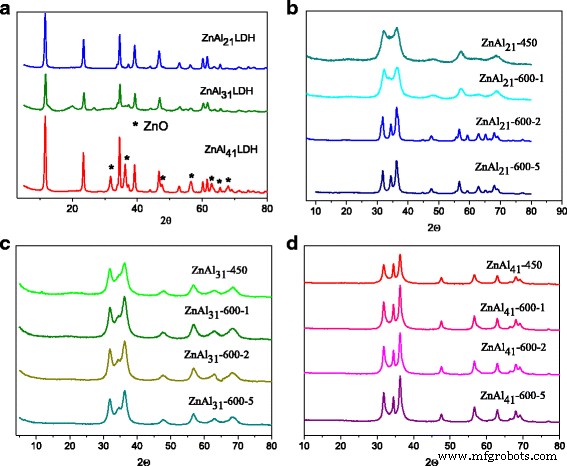
Рентгенограммы синтезированных Zn-Al СДГ ( a ) и прокаленный:ZnAl 21 ЛДГ ( b ), ZnAl 31 LDH ( c ), ZnAl 41 LDH ( d )
Анализ дифрактограмм прокаленных производных показал, что слоистая структура исходных СДГ была полностью разрушена, что свидетельствует о почти полном разложении исходных СДГ и удалении большей части межслоевых карбонатных анионов и воды (рис. 1b – d). Все отражения могут быть идеально проиндексированы как гексагональная структура вюрцита ZnO. Нет характерных отражений, соответствующих Al 2 . О 3 фазы наблюдались на рентгенограммах. Следует отметить, что более высокая степень кристалличности ZnO улучшалась с увеличением Zn 2+ / Аль 3+ катионное соотношение.
Известно, что гидратация прокаленных Zn-Al СДГ в водной суспензии приводит к реконструкции фазы гидроталькита [9]. Видно, что слоистая структура восстанавливалась при гидратации прокаленных Zn-Al СДГ в водных растворах ДС (рис. 2). Появление дифрактограмм под малыми углами свидетельствует о наличии ДС-интеркалированных СДГ. Все реконструированные Zn-Al СДГ, модифицированные DS, также содержали фазу, интеркалированную карбонатом. Следует отметить, что полная реконструкция слоистой структуры наблюдалась только для ZnAl 21 . -450 / DS LDH (рис. 2а). Диаграммы XRD ZnAl 31 -450 / DS и ZnAl 41 -450 / DS СДГ содержали рефлексы ZnO (рис. 2а). Согласно [27] гидратация смешанных оксидов Zn-Al с соотношением Zn / Al 1:5 привела к образованию структуры гидроталькита с Zn / Al =2 независимо от исходного соотношения Zn / Al. Итак, ZnAl 31 -450 / DS, ZnAl 41 -450 / DS LDH содержали меньшее количество DS-интеркалированной фазы. На рентгенограммах всех СДГ, модифицированных DS, полученных из смешанных оксидов Zn-Al, прокаленных при 600 ° C, присутствовали отражения фазы ZnO (рис. 2б). Очевидно, что непрерывное выделение Zn 2+ из фазы аморфного оксида приводило к образованию большего количества наночастиц ZnO при повышении температуры прокаливания.
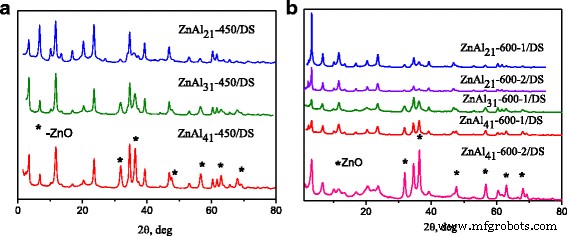
Рентгенограммы модифицированных DS СДГ Zn-Al, полученные реконструкцией СДГ, прокаленных при 450 ° C ( a ) и 600 ° C ( b )
Термогравиметрические следы, записанные для СДГ Zn-Al, были очень похожими для всех соотношений Zn / Al. Кривые ТГ, ДТА и ДТГ для образцов с Zn / Al =4:1 представлены на рис. 3. График ТГА для СДГ-карбоната (рис. 3а) показал потерю массы в интервале температур 60–190, 190–300 и 300–500 ° С. Потеря массы на первом этапе - обычная характеристика гидроталькита, связанная с высвобождением физадсорбированной и межслойной воды. Вторая потеря массы была приписана первой стадии дегидроксилирования и удаления карбонат-ионов из прослойки. В этом диапазоне температур гидроталькит подвергался реакциям декарбонатирования и дегидроксилирования, приводящим к образованию оксидов металлов. На третьем этапе потери массы, которая происходила при температуре выше 500 ° C, потеря массы была признана как полное дегидроксилирование и коллапс структуры из-за удаления оставшихся межслоевых анионов [28]. Незначительная потеря массы, наблюдаемая при 500–1000 ° C, может быть приписана потере некоторых карбонатных анионов, которые сильно адсорбируются на кристаллитах смешанных оксидов [29].
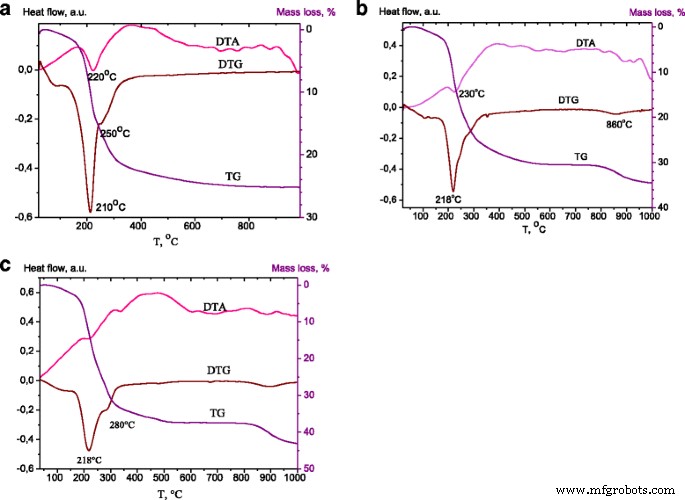
Кривые ТГ, ДТА и ДТГ ZnAl 41 LDH ( а ), ZnAl 41 -450 / DS ( b ), ZnAl 41 -600-1 / DS ( c )
Стадии термического разложения для всех изученных СДГ Zn-Al представлены в таблице 1. Полная потеря массы уменьшается с увеличением отношения Zn / Al в СДГ ZnAl, так как материалы с более низкой плотностью заряда содержат меньше карбонат-анионов. Кроме того, как ZnAl 31 ЛДГ и ZnAl 41 СДГ содержал фазу ZnO, в образцах присутствовало меньшее количество гидроксидов металлов и межслоевых карбонат-ионов. Итак, процессы дегидроксилирования и декарбоксилирования ZnAl 31 ЛДГ и ZnAl 41 LDH были не такими интенсивными, как ZnAl 21 LDH.
Термогравиметрические следы, записанные для ZnAl 41 -450 / DS представлены на рис. 3б. Первую стадию термического разложения связывали с потерей межслоевой воды. Вторая стадия разложения - дегидроксилирование бруситоподобных листов - сопровождалась разрушением ДС. Разложение ионов ДС происходило в интервале 210–250 ° C [30, 31], поэтому большая потеря наблюдалась ниже 200 ° C. Потеря массы СДГ, модифицированных ДС, при 300–500 ° C приписывалась полному дегидроксилированию и разрушению слоистой структуры. Увеличение потери массы на этой стадии связано с загрузкой ДС, разложение которой отражается потерей массы при 400–900 ° C. Потеря массы между 800–900 ° C может быть определена как SO 3 эволюция из-за разложения сульфата (Zn, Al), образовавшегося при разложении DS на второй стадии потери массы [32].
Суммарные потери массы ZnAl 31 -450 / DS и ZnAl 41 -450 / DS были меньше по сравнению с ZnAl 21 -450 / DS указывает на меньшее содержание интеркалированных DS-фаз в образцах с соотношением Zn / Al 3:1 и 4:1. Наличие рефлексов ZnO на картинах этих СДГ свидетельствует о неполной перестройке СДГ при регидратации смешанных двойных оксидов в водном растворе ДС (рис. 2а). Согласно [33], в СДГ сосуществуют экстра-фазы. Синтезированные и регидратированные Zn-Al СДГ (Zn:Al =2:1) содержали примерно 25 и 23 мас.% Аморфной фазы [33]. Авторы обнаружили, что регидратированные образцы содержат дополнительно около 3 мас. % фазы ZnO (цинкит) в результате выделения Zn из бруситоподобных слоев. Вероятно модификация ZnAl 21 СДГ с ДС вызывали дополнительное образование фазы аморфного гидроксида цинка. Как было предложено в [27], на ранней стадии реконструкции аморфной фазы гидроксида цинка была предварительная реакция регидратации, а затем регидратация оксидов Zn-Al во время процесса реконструкции. Возможно, регидратация аморфной фазы привела к образованию карбонатно-интеркалированной фазы. Регидратация оксидов Zn-Al в растворах ДС привела к образованию фазы, интеркалированной ДС. Потери массы для ZnAl 21 -600-1 / DS, ZnAl 31 -600-1 / DS, ZnAl 41 -600-1 / DS существенно отличались. Очевидно, что Zn-Al СДГ, прокаленные при 600 ° C, содержат меньше аморфной фазы.
Присутствие фотоактивного ZnO расширяет диапазон применения СДГ и композитов на основе СДГ, особенно в качестве фотокатализаторов, УФ-фильтров, сенсибилизированных красителями солнечных элементов. Было исследовано влияние фазовых превращений на способность Zn-Al СДГ поглощать УФ-свет. Спектры оптического поглощения синтезированных Zn-Al СДГ, кальцинированных Zn-Al СДГ и DS-модифицированных Zn-Al СДГ для образцов с Zn:Al =2:1 показаны на рис. 4a, b. Реконструкция смешанных оксидов, прокаленных при 450 и 600 ° C в течение 1 часа, способствовала образованию дополнительного количества кристаллического ZnO, что приводило к красному смещению полосы поглощения ZnAl 21 -450 / DS и ZnAl 21 -600-1 / DS (рис. 4а, б). Полоса поглощения ZnAl 21 -600-2 был сдвинут в видимый свет примерно на 35 нм. Не было изменений в абсорбции смешанных оксидов с Zn:Al =2:1, полученных прокаливанием СДГ в течение 5 часов (рис. 4b).
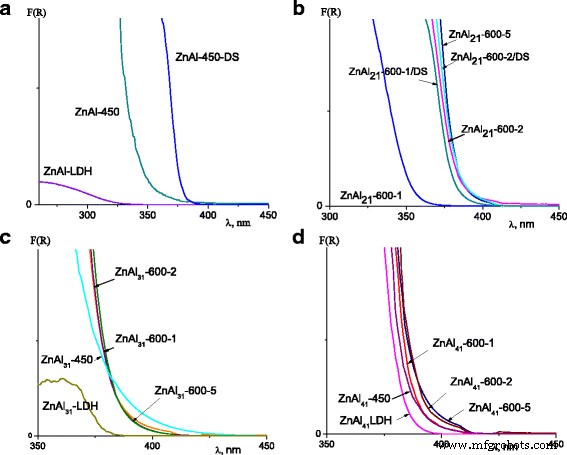
УФ-видимые спектры Zn-Al СДГ с соотношением Zn / Al:2:1 ( a , b ), 3:1 ( c ), 4:1 ( d )
Положение полосы поглощения смешанных оксидов с Zn:Al =3:1 было почти одинаковым для образцов, обработанных при 450 и 600 ° C, и не зависело от продолжительности термообработки (рис. 4c). Для Zn-Al СДГ и смешанных оксидов с Zn:Al =4:1 полосы поглощения располагались при 382–390 нм (рис. 4d).
Поскольку Al 2 О 3 представляет собой материал с широкой запрещенной зоной (5,55 эВ), поглощение света в УФ-диапазоне за счет присутствующего в образцах ZnO, ширина запрещенной зоны которого составляет 3,37 эВ [34]. Значения запрещенной энергии (E g ) образцов рассчитывали по пересечению спектров УФ – видимой области с использованием уравнения:E g =1240 / λ [35] (таблица 3). Среди прокаленных Zn-Al СДГ наименьшее значение энергии запрещенной зоны наблюдалось для образца с наибольшим содержанием Zn (Таблица 3).
Фотокаталитическое исследование
Чтобы оценить фотокаталитические характеристики Zn-Al СДГ, разложение водных 2 * 10 -5 Раствор М МБ в УФ-свете. Плохая светопоглощающая способность СДГ с соотношением Zn / Al 2:1 и 3:1 обусловила его низкую активность при облучении (таблица 2).
ZnO-содержащий ZnAl 41 ЛДГ среди других ЛДГ продемонстрировали более высокую фотокаталитическую активность в разрушении МБ. Фотокаталитическая активность была значительно улучшена при прокаливании образцов при 450 и 600 ° C из-за образования большего количества фазы ZnO. Кривые фотодеградации МБ для Zn-Al СДГ, прокаленных при 600 ° C, представлены на рис. 5а. Поскольку разница в фотокаталитических характеристиках прокаленных Zn-Al СДГ была вызвана фазой ZnO, СДГ с соотношением Zn / Al 4:1 продемонстрировали лучшие результаты при фотодеструкции МБ.
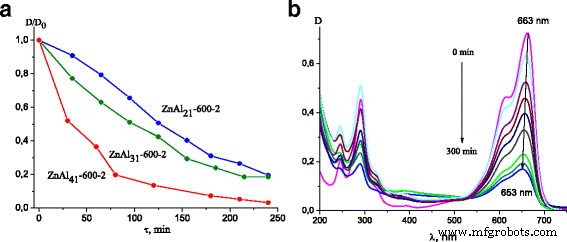
Кривые разложения МБ над кальцинированными СДГ Zn-Al под воздействием УФ-излучения ( a ); Изменения поглощения 2 * 10 -5 Раствор M MB в процессе фотодеградации ZnAl 31 -600-1 ( b )
Изменение спектров поглощения раствора МБ за разное время облучения в присутствии ZnAl 31 -600-1 можно увидеть на рис. 5b. Пики при 610 и 663 нм были отнесены к поглощению сопряженной π-системы, а пики около 300 нм - к поглощению ароматического кольца [36]. Видно, что интенсивность исходных пиков уменьшалась с увеличением времени облучения. Кроме того, можно было наблюдать параллельное уменьшение интенсивности и небольшой сдвиг в синий цвет полос, расположенных на длине волны 663 нм. Это было вызвано N-деметилированием фенотиазина и его сопутствующей деградацией [37]. Подобные изменения в спектрах оптического поглощения МБ наблюдались для фотокаталитических систем со всеми СДГ.
Модификация СД Zn-Al СДГ увеличивала его сродство к МБ за счет гидрофобных взаимодействий между поверхностно-активными веществами и молекулами красителя [26]. ZnAl 41 -600-1 / DS показал лучший результат по адсорбции МБ (таблица 3). Фотокаталитическая активность органо / Zn-Al СДГ была сопоставима с кальцинированными Zn-Al СДГ (таблица 3). Более высокий уровень деградации МБ наблюдался для ZnAl 41 -450 / ДС. Показатели удаления МБ с помощью СДГ Zn-Al, модифицированных ДС, путем адсорбции были выше, чем при фотодеструкции . Таким образом, адсорбционное удаление МБ с помощью органо / Zn-Al СДГ может быть улучшено за счет применения светового облучения.
Вероятно, фотодеструкция красителя произошла на поверхности СДГ Zn-Al, модифицированных ДС, которая не фиксировалась в условиях эксперимента. После достижения равновесия модифицированные DS Zn-Al СДГ с адсорбированным МБ имели интенсивный синий цвет.
Выводы
В данной работе были приготовлены синтезированные и прокаленные Zn – Al СДГ с различным соотношением катионов. Полученные материалы охарактеризованы и использованы для удаления МБ катионных красителей из водных растворов. Исследования фотодеструкции МБ в УФ-свете как на СДГ, так и на кальцинированных СДГ показывают, что:
Фотокаталитическая активность Zn – Al СДГ обусловлена присутствием фазы ZnO. Образование фазы ZnO в СДГ можно регулировать увеличением отношения Zn / Al в СДГ и температурной обработкой СДГ.
Влияние отношения Zn / Al на фотокаталитическую активность СДГ было преобладающим. Фотодеградация МБ в синтезированном ZnAl 41 ЛДГ и ZnAl 41 ЛДГ при 600 ° C составила 72 и 95% соответственно. Для прокаливания при 600 ° C ZnAl 31 ЛДГ и ZnAl 21 LDH, фотодеградация МБ составила 76 и 74% соответственно.
Органо / Zn-Al СДГ показали высокую адсорбционную способность по отношению к катионному красителю MB. Они также продемонстрировали фотокаталитическую активность при разрушении МБ. Следовательно, адсорбционное удаление МБ из растворов с СДГ Zn-Al, модифицированными DS, может быть улучшено с помощью УФ-облучения.
Наноматериалы
- Фотокаталитическая активность, усиленная Au-плазмонными наночастицами на фотоэлектроде нанотрубки TiO2, покры…
- Новый фотокатализатор на гетеропереходе Bi4Ti3O12 / Ag3PO4 с улучшенными фотокаталитическими характеристиками
- Синергетические эффекты наночастиц Ag / BiV1-xMoxO4 с повышенной фотокаталитической активностью
- Новые взгляды на адсорбцию CO2 наноматериалами на основе слоистого двойного гидроксида (LDH)
- Повышенная эффективность преобразования мощности перовскитных солнечных элементов с использованием матери…
- Удаление антибиотиков из воды с помощью полностью углеродной трехмерной нанофильтрационной мембраны
- Повышенные энергетические характеристики на основе интеграции с наноламинатами Al / PTFE
- Улучшенные фотоэлектрические свойства в солнечном элементе с плоским гетеропереходом Sb2S3 с подходом быстрог…
- Фотоэлектрические характеристики солнечных элементов с наноконусной решеткой с контактным переходом и улуч…
- Чрезвычайно улучшенный отклик фототока в нанолистах топологического изолятора с высокой проводимостью



