Нанокристаллы NiCo2S4 на углеродных нанотрубках, легированных азотом, в качестве высокоэффективного анода для литий-ионных батарей
Аннотация
В последние годы разработка литий-ионных аккумуляторов (LIB) с высокой плотностью энергии стала одним из важных направлений исследований для удовлетворения потребностей электромобилей и технологий интеллектуальных сетей. В настоящее время традиционные LIB достигли своих пределов с точки зрения емкости, срока службы и стабильности, что требует их дальнейшего совершенствования и разработки альтернативных материалов с значительно улучшенными свойствами. Азотсодержащая углеродная нанотрубка (N-CNT) для биметаллического сульфида (NiCo 2 S 4 ) предлагается в данном исследовании в качестве анода с привлекательными электрохимическими характеристиками для LIB. Подготовленный NiCo 2 S 4 Нанокомпозит / N-CNT продемонстрировал улучшенную циклическую стабильность, быстродействие и отличную обратимую емкость 623,0 мАч г –1 после 100 циклов при 0,1 А g –1 и поддерживал высокую емкость и стабильность при циклических нагрузках при 0,5 А изб. –1 . Превосходные электрохимические характеристики композита можно отнести к уникальной пористой структуре, которая может эффективно увеличивать коэффициент диффузии ионов Li, уменьшая объемное расширение во время процессов заряда-разряда.
Фон
Литий-ионный аккумулятор (LIB) - это ведущая аккумуляторная технология, используемая в портативных электронных устройствах, электромобилях и накопителях возобновляемой энергии [1, 2]. Таким образом, разработка LIB с высокой плотностью энергии стала важнейшим направлением исследований для устойчивого развития различных секторов экономики и промышленности [3,4,5]. Например, удельная энергоемкость промышленного графитового анодного материала достигла теоретической емкости 372 мАч г –1 . , что не оставляет много места для его дальнейшего совершенствования, чтобы удовлетворить требования к производительности появляющейся электроники и технологий электромобилей [6, 7]. В результате для удовлетворения потребностей современного общества крайне важно разработать альтернативные анодные материалы для LIB.
Сульфиды переходных металлов (ТМС) обладают значительно более высокой удельной емкостью, чем традиционные электродные материалы [8,9,10,11,12]. В последнее время сообщалось о TMS как об анодах с превосходной проводимостью и каталитической активностью. Среди них бинарный сульфид никель – кобальт (NiCo 2 S 4 ) имеет высокую теоретическую удельную емкость (703 мАч г –1 ), отличная электронная проводимость (1,26 × 10 6 S м –1 ) и большее количество сайтов окислительно-восстановительной реакции [13,14,15,16,17]. Сообщенный общий механизм заряда / разряда NiCo 2 S 4 с литием (Li) протекает следующие реакции:
$$ {\ text {NiCo}} _ {2} {\ text {S}} _ {4} + 8 {\ text {Li}} ^ {+} + 8 {\ text {e}} ^ {{- }} \ to {\ text {Ni}} + {\ text {Co}} + 4 {\ text {Li}} _ {2} {\ text {S}} $$ (1) $$ {\ text { Ni}} + x {\ text {Li}} _ {2} {\ text {S}} \ leftrightarrow {\ text {NiS}} _ {x} + 2x {\ text {Li}} ^ {+} + 2x {\ text {e}} ^ {{-}} $$ (2) $$ {\ text {Co}} + x {\ text {Li}} _ {2} {\ text {S}} \ leftrightarrow {\ text {CoS}} _ {x} + 2x {\ text {Li}} ^ {+} + 2x {\ text {e}} ^ {{-}} $$ (3)Однако, несмотря на большую емкость Li NiCo 2 S 4 , по-прежнему существуют проблемы, связанные с низкой обратимостью процессов заряда / разряда из-за сопутствующего изменения объема, что приводит к дезинтеграции материала и, как следствие, серьезному снижению емкости [18]. Другая серьезная проблема возникает из-за челночного эффекта полисульфидов, образующихся при растворении полисульфида лития (LPS) в электролите, что также приводит к низкому сохранению емкости [19, 20].
Чтобы преодолеть проблемы NiCo 2 S 4 анодов, связанных с изменением объема и растворением LPS, были разработаны различные подходы, включая наноструктурирование и использование углеродсодержащих добавок и углеродных хозяев с многообещающими результатами. Наноструктурирование и его комбинация с сетками углерод / графен может увеличить площадь контакта электрод-электролит и сократить пути литий-ионных путей, что приводит к более высокой удельной емкости [18]. Таким образом, в этом исследовании сообщается о росте NiCo 2 на месте. S 4 наночастиц на структуру углеродных нанотрубок (УНТ) с использованием гидротермального метода. Кроме того, для увеличения электроактивности материала электрода гетероатомы азота (N) были включены в матрицу УНТ. Такая обработка делает N-CNT более подходящими, что приводит к равномерному росту NiCo 2 S 4 и, таким образом, улучшая кристалличность NiCo 2 S 4 / N-CNT анод. В этой уникальной структуре УНТ образуют эластичную матрицу, которая увеличивает структурную стабильность, улучшает ионную проводимость композита и уменьшает изменение объема NiCo 2 S 4 частицы. NiCo 2 S 4 Материал / N-CNT сохраняет хорошую емкость во время цикла и значительно ограничивает падение напряжения. NiCo 2 S 4 Композитный анод / N-CNT демонстрирует начальную разрядную емкость 1412,1 мАч г –1 при 0,1 А г –1 , а разрядная емкость остается на уровне 623,0 мАч g –1 после 100 циклов.
Методы
Синтез NiCo 2 S 4
Сначала 0,074 г Co (AC) 2 · 4H 2 O и 0,037 г Ni (Ac) 2 · 4H 2 О растворяли в 40 мл этанола. Раствор перемешивали на водяной бане при 80 ° C в течение 2 часов и еще 2 часа при комнатной температуре. Затем к смеси добавляли 0,078 г тиомочевины, которую дополнительно непрерывно перемешивали в течение 20 часов перед переносом реакционной смеси в автоклав на 100 мл. Гидротермальную реакцию проводили при 170 ° C в течение 3 часов. После охлаждения до комнатной температуры продукт несколько раз промывали деионизированной водой и сушили вымораживанием при пониженном давлении.
Синтез NiCo 2 S 4 / N-CNT Нанокомпозиты
Сначала 68 мг слабо окисленных УНТ диспергировали ультразвуком в 40 мл этанола. Затем 0,074 г Co (AC) 2 · 4H 2 O и 0,037 г Ni (Ac) 2 · 4H 2 O, и смесь перемешивали на водяной бане при 80 ° C в течение 2 часов. Затем 2 мл NH 3 · H 2 К раствору добавляли О и 0,078 г тиомочевины, и реакционную смесь перемешивали в течение 2 часов. Реакционную смесь переносили в автоклав на 50 мл, после чего проводили гидротермальную реакцию при 170 ° C в течение 3 часов. Продукт охлаждали до комнатной температуры, несколько раз центрифугировали с деионизированной водой и сушили вымораживанием. NiCo 2 S 4 / CNT был синтезирован по тому же методу, но без добавления NH 3 · H 2 О.
Характеристика материалов
Кристаллическая структура синтезированных образцов была охарактеризована порошковой дифракцией рентгеновских лучей (XRD, D8 Discover Bruker). Рентгеновская фотоэлектронная спектрометрия (XPS) была проведена для анализа элементного состава образцов с использованием анализатора K-Alpha 1063. Морфологию образцов изучали с помощью растрового электронного микроскопа (SEM, JSM-7100F, JEOL) и просвечивающего электронного микроскопа (TEM, JEM-2100F). Удельную поверхность образцов рассчитывали методом Брунауэра – Эммета – Теллера (БЭТ) на основе N 2 Изотермы адсорбции – десорбции, полученные с помощью V-Sorb 2800P. Термогравиметрический анализ (ТГА) проводился на воздухе при скорости нагрева 10 ° C мин -1 . .
Электрохимические измерения
Электрохимические характеристики NiCo 2 S 4 Образцы / N-CNT оценивали в монетных ячейках CR 2032. Для приготовления электродной суспензии 70 мас.% NiCo 2 S 4 Композит / N-CNT, 15 мас.% Технического углерода (Super P) и 15 мас.% Связующего из поливинилиденфторида (ПВДФ) смешивали в 1-метил-2-пирролидиноне (NMP). Суспензию равномерно распределяли на медной фольге с помощью ракельного ножа, а затем сушили при 70 ° C в течение 8 часов на воздухе. Круглые дисковые электроды были вырезаны после сушки, и ячейки были собраны в перчаточном боксе, заполненном газом Ar высокой чистоты (99,9995%) (MBraun). Массовая загрузка NiCo 2 S 4 / N-УНТ в электродах составляло около 2 мг / см –2 . Фольга из чистого Li использовалась в качестве электрода сравнения и противоэлектрода, а микропористый полипропилен Celgard 2300 использовался в качестве сепаратора. Электролит - 1 моль л –1 . LiPF 6 (Aladdin, номер CAS:21324-40-3) в смеси этиленкарбоната (EC, Aladdin, номер CAS:96-49-1) и диметилкарбоната (DMC, номер CAS:616-38-6) с объемом соотношение 1:1. Измерения гальваностатического заряда / разряда проводились с использованием многоканальной системы тестирования батарей (Neware BTS4000) при потенциальном окне 0,01–3,00 В (по сравнению с Li + / Ли). Циклическую вольтамперометрию (CV) и спектроскопию электрохимического импеданса (EIS) проводили с использованием электрохимической рабочей станции (Princeton, VersaState4).
Результаты и обсуждение
На схеме 1 показан способ получения NiCo 2 . S 4 / N-CNT композит. Первоначально поверхность УНТ была предварительно обработана раствором Ni 2+ и Co 2+ . Затем атомы N были легированы в УНТ посредством гидротермальной реакции при 170 ° C, а NiCo 2 S 4 был выращен in situ на поверхности УНТ. Кристаллические структуры NiCo 2 S 4 , NiCo 2 S 4 / CNT и NiCo 2 S 4 Композиты / N-УНТ были охарактеризованы методом XRD (рис. 1а). Характерные дифракционные пики NiCo 2 S 4 (JCPDS 20-0728) наблюдались во всех трех образцах. Более того, пики NiCo 2 S 4 / N-CNT были более выраженными и резкими, чем в NiCo 2 S 4 / CNT [21]. Считается, что N-CNT можно использовать в качестве активных центров зародышеобразования для обеспечения равномерного и плотного роста NiCo 2 S 4 [22]. На рисунке 1b показаны результаты BET для NiCo 2 S 4 / Нанокомпозиты N-УНТ. Удельная поверхность NiCo 2 S 4 / Нанокомпозиты N-CNT - 62,67 м 2 г −1 . Как показано в данных анализа ТГА (рис. 1c), NiCo 2 S 4 Нанокомпозит / N-CNT показал потерю массы в интервале температур 400–600 ° C, которая была вызвана горением УНТ. Следовательно, содержание NiCo 2 S 4 в NiCo 2 S 4 Композит / N-CNT был определен как ~ 30 мас.%.
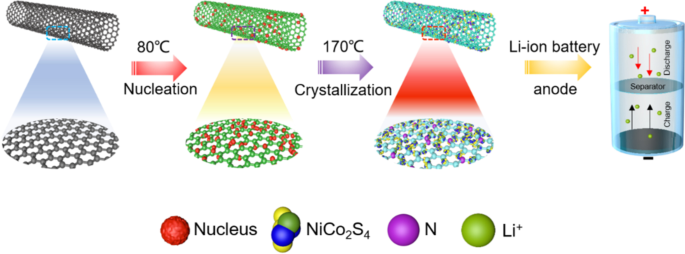
Схематическое изображение NiCo 2 S 4 / N-CNT композит
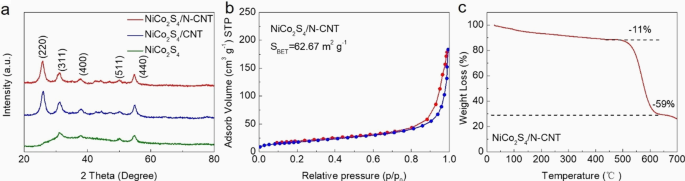
а Диаграммы XRD NiCo 2 S 4 , NiCo 2 S 4 / CNT и NiCo 2 S 4 / N-CNT; б N 2 изотермы адсорбции – десорбции NiCo 2 S 4 / N-CNT; c ТГА NiCo 2 S 4 / N-CNT
Результаты СЭМ образцов представлены на рис. 2а, б. Синтезированный NiCo 2 S 4 наночастицы кажутся более плотно упакованными и агломерированными. С другой стороны, благодаря введению CNT и N-CNT, NiCo 2 S 4 наночастицы были равномерно распределены и осаждались с образованием NiCo 2 S 4 Композит / УНТ (рис. 2в, г) и NiCo 2 S 4 / N-CNT (рис. 2д, е) соответственно. Однако плотность NiCo 2 S 4 наночастицы на поверхности N-CNT в NiCo 2 S 4 / N-CNT был значительно выше, чем в NiCo 2 S 4 / УНТ композит. Это подтверждает, что введение атомов N в УНТ способствует более плотному росту NiCo 2 S 4 наночастицы.

SEM-изображения a , b NiCo 2 S 4 ; c , d NiCo 2 S 4 / CNT; и е , f NiCo 2 S 4 / N-CNT
Изображения ПЭМ на рис. 3а показывают, что NiCo 2 S 4 частицы имеют средний диаметр ~ 5 нм и равномерно распределены по поверхности N-CNT. На изображении NiCo 2 , полученном методом просвечивающей электронной микроскопии (ПЭМВР) высокого разрешения S 4 / N-CNT, показанные на рис. 3b, наночастицы диаметром около 5 нм демонстрируют четкую полосу кристаллической решетки размером 0,35 нм, соответствующую плоскости (220) NiCo 2 S 4 . Кроме того, вокруг наночастиц наблюдалось множество кривых полос графитовой решетки. Профили быстрого преобразования Фурье (БПФ) и шага решетки на рис. 3b дополнительно подтвердили включение NiCo 2 S 4 наночастиц в структуру N-CNT.
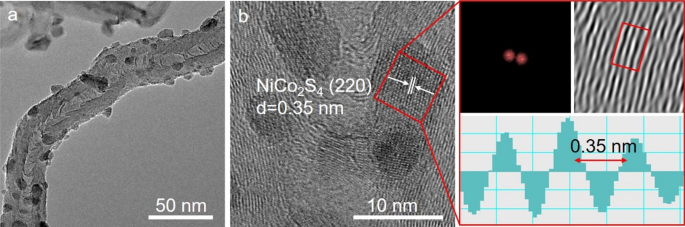
а ТЕМ изображение; б HRTEM изображение NiCo 2 S 4 / N-CNT
Кроме того, XPS был использован для определения характеристик сцепления и химического состава поверхности NiCo 2 S 4 / N-CNT. Co 2 p Спектры (рис. 4а) можно разделить на два пика при 778,8 эВ и 793,0 эВ, соответствующих Co 3+ и Co 2+ соответственно [23, 24]. В N 1 s В спектре (рис. 4б) пики при 398,3, 399,7 и 400,9 эВ могут быть отнесены к пиридиновому, пиррольному и графитному азоту соответственно [25, 26]. В XPS-спектре S 2 p (Рис. 4c), S 2 p 3/2 и S 2 p 1/2 хорошо видны при 161,2 и 163,1 эВ соответственно, а пик при 163,8 эВ соответствует связи металл-сера [27, 28]. Как показано на рис. 4d, помимо сателлитных пиков, энергии связи Ni 2 p с центром при 854,6 и 856,9 эВ соответствуют Ni 2 p 3/2 , а при 871,1 и 875,5 эВ - Ni 2 p 1/2 . Это указывает на присутствие как Ni 3+ и Ni 2+ в выборке [29, 30]. Как показано на рис. 4e, на профиле C1s присутствуют три подгоночных пика при 284,9, 285,7 и 290,4 эВ, которые можно отнести к связям C – C, C – N и –C =O соответственно. Таким образом, XPS NiCo 2 S 4 / N-CNT указывает на образование высокоупорядоченной кристаллической структуры NiCo 2 S 4 и продемонстрировали успешное введение элемента N в структуру соединений.
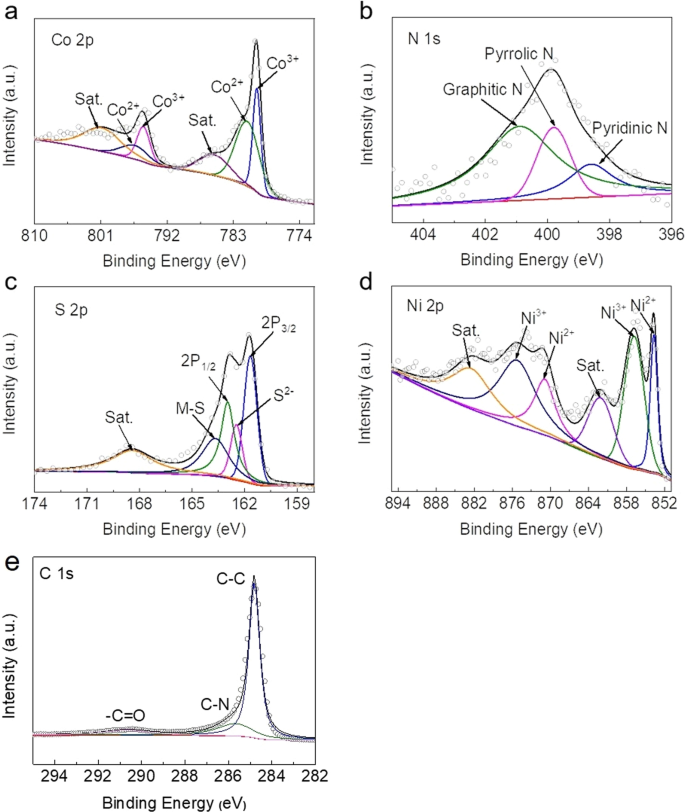
XPS-спектры a Co 2 p , b N 1 s , c S 2 p , d Ni 2 p и e C 1 s в NiCo 2 S 4 / N-CNT
Электрохимические характеристики NiCo 2 S 4 / N-CNT для хранения Li были оценены с помощью CV и циклического заряда-разряда, как показано на рис. 5, в диапазоне потенциалов 0,01–3,00 В (по сравнению с Li + / Ли). Катодный процесс состоял из трех пиков восстановления (рис. 5а), расположенных при 1,71 В, 1,33 В и 0,70 В. Самый сильный пик расположен при 1,33 В, а два более слабых пика соответствуют восстановлению NiCo 2 S 4 для Ni и Co. Для сравнения, пики при 1,71 В и 0,70 В соответствуют образованию Li 2 S и пленка SEI соответственно. В анодном процессе пики окисления при 1,33 В и 2,05 В можно отнести к окислению металлического Co до CoS x . Кроме того, имеется интенсивный пик при 2,32 В в результате реакций окисления металлических Ni и Co до NiS x и CoS x , соответственно. Форма кривой, положение пика и интенсивность пиков относительно стабильны в следующих циклах, что указывает на то, что NiCo 2 S 4 / N-CNT обладает хорошей стабильностью и обратимостью.
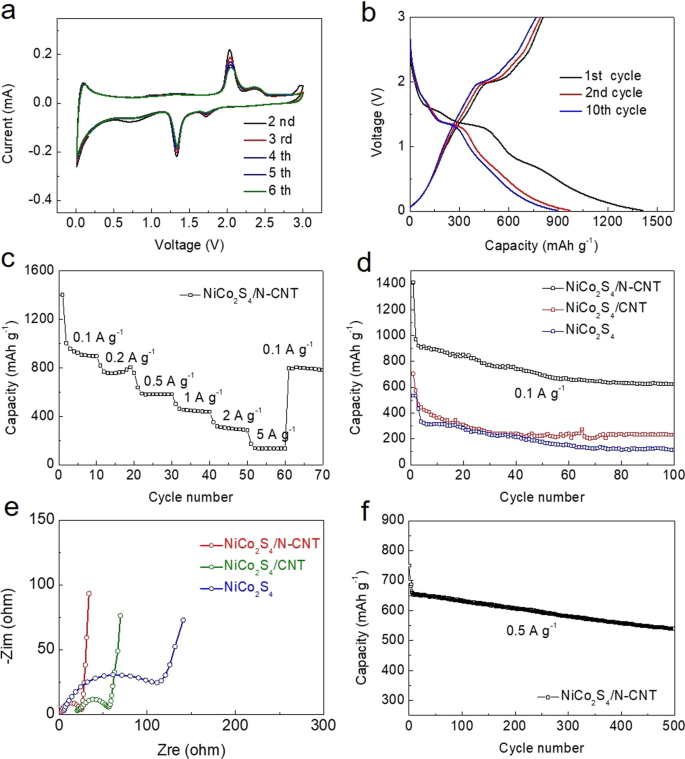
а Резюме NiCo 2 S 4 / N-CNT при скорости сканирования 0,1 мВ с -1 от 0,01 до 3,0 В по сравнению с Li + / Ли; б Кривые заряда / разряда NiCo 2 S 4 / N-CNT при 0,1 А изб. −1 ; c скоростная способность NiCo 2 S 4 / Электроды из N-УНТ при различных токах; г езда на велосипеде NiCo 2 S 4 / N-CNT, NiCo 2 S 4 / CNT и NiCo 2 S 4 при 0,1 А г –1 ; е Графики EIS для NiCo 2 S 4 / N-CNT, NiCo 2 S 4 / CNT и NiCo 2 S 4 ; е производительность при езде на велосипеде при плотности тока 0,5 А изб. −1
На рисунке 5b показаны кривые заряда-разряда NiCo 2 . S 4 / N-CNT при 0,1 А изб. –1 для 1-го, 2-го и 10-го циклов. Первая зарядка и разрядка NiCo 2 S 4 / N-CNT электрод достиг 807,6 и 1412,1 мАч г –1 соответственно с начальной кулоновской эффективностью 57,2%. Разрядная емкость 2-го и 10-го циклов составляет 970,7 мАч г –1 и 891,1 мАч г –1 , соответственно. Обратимость процесса заряда / разряда улучшилась с увеличением числа циклов, что сопровождалось увеличением кулоновской эффективности. Полученные CV-профили соответствуют кривым заряда / разряда NiCo 2 S 4 / N-CNT.
Для дальнейшего изучения электрохимических характеристик NiCo 2 S 4 / N-CNT, производительность оценивалась при плотностях тока от 0,1 до 5 А · г –1 (Рис. 5c). Результаты показывают, что емкость NiCo 2 S 4 / N-CNT уменьшалась с увеличением плотности тока. Когда плотность тока вернулась к 0,1 А изб. −1 , емкость NiCo 2 S 4 / N-CNT вернулся к значению 796,1 мАч г –1 , демонстрируя сохранение около 84% емкости и демонстрируя, что NiCo 2 S 4 / N-CNT демонстрирует отличные скоростные характеристики. Данные о производительности при езде на велосипеде NiCo 2 S 4 / N-CNT, NiCo 2 S 4 / CNT и NiCo 2 S 4 на 100 циклов при 0,1 А g –1 показаны на рис. 5г. В течение первых 50 циклов анод претерпевает небольшое снижение емкости. Затем NiCo 2 S 4 Анод / N-CNT стабилизировал свою емкость для остальных циклов и показал значение 623,0 мАч г –1 после 100 циклов. Эти результаты показывают, что по сравнению с NiCo 2 S 4 / CNT и NiCo 2 S 4 электроды, NiCo 2 S 4 Электрод / N-CNT показал значительно более высокую удельную разрядную емкость и лучшую стабильность цикла. На рисунке 5e показаны данные EIS. Высокочастотные полукруги на графиках Найквиста соответствуют сопротивлению переносу заряда ( R ct ) электродов. NiCo 2 S 4 Электрод / N-CNT явно показывает самое низкое R ct значения, предполагающие заметно улучшенную кинетику переноса заряда / массы. На рис. 5f показаны циклические характеристики NiCo 2 . S 4 / Электрод из N-УНТ при 0,5 А изб. −1 более 500 циклов. NiCo 2 S 4 Электрод / N-CNT обеспечивает начальную удельную разрядную емкость 750,2 мАч г −1 и поддерживает обратимую емкость 539,3 мАч г −1 после 500 циклов, что еще раз подтверждает отличную циклическую и скоростную способность этого анода большой емкости для литиевых батарей.
Выводы
Таким образом, NiCo 2 S 4 Композит / N-CNT был получен с использованием простого способа гидротермального синтеза в одном реакторе. За счет введения атомов N в структуру УНТ равномерно распределенный NiCo 2 S 4 Были получены наночастицы с уменьшенным размером частиц. Собранные ячейки с NiCo 2 S 4 Анод / N-CNT продемонстрировал высокую удельную емкость около 623,0 мАч г –1 и отличная устойчивость к циклическим нагрузкам при 0,1 А g –1 после 100 циклов. Кроме того, этот электрод показал отличные циклические характеристики при 0,5 А · г -1 . более 500 циклов, что подтверждает его способность поддерживать высокие характеристики при повышенной плотности тока. Наше исследование показывает, что этот метод синтеза является реальным способом выращивания NiCo 2 S 4 наночастицы с равномерным распределением на поверхности подложки УНТ в качестве высокоэффективного анода для LIB.
Доступность данных и материалов
Все данные, полученные или проанализированные в ходе этого исследования, включены в эту опубликованную статью.
Сокращения
- LIB:
-
Литий-ионные батареи
- CNT:
-
Углеродные нанотрубки
- NiCo 2 S 4 :
-
Бинарный сульфид никель – кобальт
- PVDF:
-
Поливинилиденфторид
- NMP:
-
N -Метил-2-пирролидон
- XRD:
-
Рентгеновская порошковая дифракция
- SEM:
-
Сканирующая электронная микроскопия
- Резюме:
-
Циклическая вольтамперометрия
- EIS:
-
Электрохимическая импедансная спектроскопия
- N-CNT:
-
Азотсодержащие углеродные нанотрубки
- TMS:
-
Сульфиды переходных металлов
- LPS:
-
Полисульфид лития
- XPS:
-
Рентгеновская фотоэлектронная спектрометрия
- ТЕМ:
-
Просвечивающий электронный микроскоп
- HRTEM:
-
Просвечивающий электронный микроскоп высокого разрешения
- СТАВКА:
-
Брунауэр – Эммет – Теллер
- TGA:
-
Термогравиметрический анализ
- EC:
-
Этиленкарбонат
- DMC:
-
Диметилкарбонат
- БПФ:
-
Быстрое преобразование Фурье
- N:
-
Азот
- Ли:
-
Литий
Наноматериалы
- Нанокристаллы олова для будущей батареи
- Возобновляемые марки PVDF для литий-ионных батарей
- Механический композит LiNi0.8Co0.15Al0.05O2 / углеродных нанотрубок с улучшенными электрохимическими характеристикам…
- Простой синтез наночастиц SiO2 @ C, закрепленных на MWNT, в качестве высокоэффективных анодных материалов для лити…
- Многослойный композит MoS2 / ацетиленовый черный как эффективный анодный материал для литий-ионных батарей
- Подготовка гибридных микроматериалов MnO2 с полипропиленовым покрытием и их улучшенные циклические характери…
- Влияние различных связующих на электрохимические характеристики металлооксидного анода для литий-ионных ба…
- Композит Na4Mn9O18 / углеродных нанотрубок как материал с высокими электрохимическими характеристиками для водн…
- Встроенный композит Si / графен, изготовленный методом термического восстановления магнием в качестве анодно…
- Аэрогель / серный композит с активированным углем с полианилиновым покрытием для высокопроизводительных лит…



