Эффективный бифункциональный электрокатализатор MOF, допированных фосфорным углеродом
Аннотация
Компания стремится разработать высокоэффективные и дешевые бифункциональные электрохимические катализаторы как для реакции восстановления кислорода (ORR), так и для реакции выделения кислорода (OER) для решения энергетического кризиса и экологических проблем. Здесь мы сообщаем о серии ZIF-производных Co-P-C со-легированных полиэдрических материалов с четко определенной морфологией. Оптимизированный катализатор Co / P / MOFs-CNTs-700 проявил благоприятную электрохимическую активность с наименьшим перенапряжением 420 мВ для достижения плотности тока 10 мА см -2 для OER и полупотенциал 0,8 В для ORR в 0,1 М NaOH. Рабочие характеристики могут быть хорошо улучшены за счет легирования фосфорного ресурса, который сильно изменил его морфологию. Между тем, ресурсы легированного углерода также улучшают проводимость, что делает его многообещающим бифункциональным электрохимическим катализатором и может быть сопоставимым с коммерческими электрокатализаторами.
Введение
В последние годы быстрорастущий спрос на устойчивое развитие энергетики вызвал большой интерес у исследователей в области электрохимического преобразования энергии и технологий хранения энергии [1,2,3]. Чтобы удовлетворить потребность в преобразовании и распределении энергии, постоянным стремлением будет исследование альтернативного электродного материала из неблагородных металлов с хорошо продуманной структурой, контролируемыми химическими веществами и превосходными электрохимическими характеристиками [4,5,6,7]. Реакция выделения кислорода (OER) и реакция восстановления кислорода (ORR) являются важными реакциями, которые играют важную роль в применении в солнечных элементах, электролизерах, перезаряжаемых элементах металл-воздух, топливных элементах и т. Д. [8,9 , 10,11]. Тем не менее, унылая кинетика OER и ORR серьезно ограничивала крупномасштабное использование эффективности преобразования энергии [8, 12,13,14,15].
Поэтому в последние десятилетия были приложены большие усилия для исследования эффективного и стабильного электрохимического катализатора для улучшения тяжелой кислородной реакции. Известно, что катализаторы из благородных металлов являются эталоном кислородной реакции. Однако эти перспективные материалы страдали от дефицита, высокой стоимости и низкой стабильности. Например, диоксид иридия и диоксид рутения, наиболее многообещающие катализаторы OER, демонстрируют превосходную электрокаталитическую активность OER как в кислотных, так и в щелочных условиях при низком перенапряжении, но все же не обладают долговременной стабильностью. Коммерческий платиноуглеродный катализатор в качестве катодного электрокатализатора с блестящей электрохимической активностью ORR все еще подвергается перекрестному влиянию электролита, легко отравляется и не обладает определенной долговечностью. Следовательно, из-за вышеупомянутых недостатков драгоценных катализаторов, все больше и больше исследователей посвящают себя разработке электрохимических катализаторов на основе богатых на Земле элементов для устойчивого развития. Интересно, что металлоорганические каркасные материалы (MOF) привлекли огромный интерес из-за их низкой стоимости, большого количества источников и способности служить в качестве шаблонов для синтеза нанопористых материалов на основе углерода. Кристаллические пористые материалы MOF обычно легко спроектировать, формируя их самосборкой из ионов металлов и органических групп [16, 17]. Комплексы углерод-металл, полученные из них, могут иметь различную морфологию, показывать чрезвычайно большую площадь поверхности и иерархическую структуру пор, которые вносят большой вклад в электрохимическую активность ORR и OER [18, 19]. Тем не менее, степень графитизации этих материалов относительно низкая, что снижает проводимость материалов.
Между тем углеродные наноматериалы из-за их высокой проводимости и контролируемой морфологии чрезвычайно привлекательны и используются во многих электрохимических устройствах, таких как полимерные топливные элементы [2, 20]. Более того, было доказано, что углеродные наноматериалы, легированные гетерогенными элементами, могут значительно повысить каталитическую активность и химический состав поверхности [4, 13, 20, 21, 22, 23, 24, 25, 26]. Гетеролегированные углеродные материалы также обладают синергетическим эффектом при прямом катализе ORR [27, 28]. Следовательно, чтобы повысить проводимость и каталитическую активность материалов, целесообразно синтезировать эффективные гетерогенные легированные атомами материалы из недорогих MOF материалов с богатым источником, которые могут быть хорошо применены в топливных элементах, металл-воздушных батареях и т. Д. вкл.
Таким образом, мы сообщаем об эффективном бифункциональном электрохимическом катализаторе металлоорганического каркаса с фосфором и углеродом, совместно легированными методом легирования in situ. Мы обнаружили, что легирование гетерогенного атома может изменить его морфологию и улучшить проводимость, подтвержденную методами SEM и XPS, что позволило ему обработать благоприятно низкое перенапряжение 420 мВ для достижения плотности тока 10 мА см −2 для OER и полупотенциал 0,8 В для ORR в 0,1 М NaOH. Этот многообещающий бифункциональный электрохимический катализатор может быть сопоставим с коммерческими электрокатализаторами.
Методы
Синтез углеродных наноматериалов Co-MOF
Чтобы синтезировать углеродные наноматериалы Co-MOF, типичный и простой метод был выполнен следующим образом. Сначала 1,28 г 2-метилимидазола диспергировали с помощью ультразвука в 20 мл метанола с образованием раствора A. 1,0 г ацетилацетоната кобальта (II) диспергировали с помощью ультразвука в 60 мл метанола с образованием раствора B. в течение 5 мин с последующим интенсивным перемешиванием еще 10 мин при комнатной температуре. Затем смесь герметично закрывали в политрафторэтиленовом реакторе, который переносили в сушильный шкаф, нагревали от комнатной температуры до 160 ° C и выдерживали при 160 ° C в течение 24 часов с последующим естественным охлаждением до комнатной температуры. Полученный пурпурный твердый порошок центрифугировали, несколько раз промывали метанолом и сушили при 70 ° C в течение ночи. Полученные нанокристаллы подвергали пиролизу в атмосфере аргона в проточной кварцевой трубке, установленной в центре трубчатой печи, следующим образом. Сначала производство нагревали от комнатной температуры до 350 ° C со скоростью 5 ° C / мин и выдерживали при 350 ° C в течение 1 часа. Затем мы увеличили его до желаемой температуры (500, 600, 700, 800 и 900 ° C) в течение 2 часов с той же скоростью нагрева, чтобы получить Co-MOFs-x, где «x» представляет температуру карбонизации.
Синтез углеродных наноматериалов Co / P-MOF
Чтобы выяснить влияние легирования P на электрохимическую активность, во время синтеза были приняты различные источники фосфина. 1,28 г 2-метилимидазола диспергировали с помощью ультразвука в 20 мл метанола с образованием раствора A. 1,0 г ацетилацетоната кобальта (II) и 0,25 г источника фосфора диспергировали с помощью ультразвука в 60 мл метанола с образованием раствора B. Источниками фосфора были гипофосфит натрия, трифенилфосфин и др. и O -триметилфенилфосфин. Следующие шаги были такими же, как и выше; мы только изменили наиболее подходящую температуру карбонизации на 700 ° C. Наконец, мы получили продукты, названные Co / P0-MOF, CoP1-MOF и Co / P2-MOF, где P0, P1 и P2 представляют собой гипофосфит натрия, трифенилфосфин и O -триметилфенилфосфин соответственно.
Мы выбрали трифенилфосфин в качестве источника фосфора и изменили массу источника фосфора на этапе 1 на 0,5, 0,75 и 1,0 г соответственно. И остальные экспериментальные шаги остались без изменений. Конечный продукт получил названия Co / P / MOFs-700-0.25, Co / P / MOFs-700-0.5, Co / P / MOFs-700-0.75 и Co / P / MOFs-700-1.0 соответственно.
Синтез углеродных наноматериалов Co-MOFs-C
Чтобы улучшить проводимость материала, были добавлены дополнительные источники углерода. 1,28 г 2-метилимидазола диспергировали с помощью ультразвука в 20 мл метанола с образованием раствора A. 1,0 г ацетилацетоната кобальта (II) и 0,125 г источников углерода диспергировали с помощью ультразвука в 60 мл метанола с образованием раствора B. Источниками углерода служили углеродные нанотрубки (УНТ). , ацетиленовая сажа (CB) и A-OMCS, которые были получены в нашей официальной статье [25], которые были обработаны кислотой. Следующие шаги были такими же, как шаг 2.2 (1). Наконец, мы получили продукцию, названную Co / MOFs-CNTs-700, Co / MOFs-CB-700 и Co / MOFs-A-OMCS-700 соответственно.
Синтез углеродных наноматериалов Co / P-MOFs-CNTs-700
Чтобы улучшить проводимость и электрокаталитические характеристики, источники углерода и углеродные материалы использовались одновременно. 1,28 г 2-метилимидазола диспергировали с помощью ультразвука в 20 мл метанола с образованием раствора A. 1,0 г ацетилацетоната кобальта (II), 0,25 г трифенилфосфина и 0,125 г УНТ, обработанных кислотой, диспергировали с помощью ультразвука в 60 мл метанола с образованием раствора B. шаги были такими же, как и выше. Наконец, мы получили продукцию под названием Co / P / MOFs-CNTs-700.
Характеристика синтезированных углеродных наноматериалов
Рентгеновскую дифракцию (XRD) проводили на дифрактометре TD-3500 (Tongda, Китай). Рентгеновскую фотоэлектронную спектроскопию (XPS) проводили с использованием фотоэлектронного спектрометра K-Alpha + (Thermo Fisher Scientific). Изображения, полученные с помощью сканирующей электронной микроскопии (СЭМ), получали на растровом электронном микроскопе SU8220 (Hitachi, Япония). Получение изображений с помощью высокоуглового кольцевого темного поля (HAADF) и анализ элементарного картирования энергодисперсионного спектрометра (EDS) выполняли в режиме сканирующей просвечивающей электронной микроскопии (STEM) на полевом излучении FEI Tecnai f20 с коррекцией аберраций; электронный микроскоп работал при 200 кВ.
Электрохимические тесты
Все данные по электрохимической активности собирали на электрохимической рабочей станции (Ivium, Нидерланды) при комнатной температуре, соединенной с системой вращающегося дискового электрода (RDE) (Pine, США) в стандартной трехэлектродной системе. Трехэлектродная система состояла из Pt-проволочного противоэлектрода, электрода сравнения Hg / HgO (0,1 M раствор NaOH) для щелочной среды и рабочего электрода на основе стеклоуглерода (GC, 0,196 см 2 ). Электроды с катализатором получали следующим образом. Во-первых, каталитические чернила были приготовлены путем обработки ультразвуком смеси 1 мл 0,25 мас.% Раствора этанола нафиона и 5 мг соответствующего катализатора в течение 30 мин. Затем 20 мкл каталитических чернил наносили на рабочий электрод на основе стеклоуглерода в тестах RDE. Наконец, рабочий электрод сушили под инфракрасной лампой в течение 1–2 мин. Загрузка катализатора составляла приблизительно 0,5 мг / см -2 . . В качестве электролита использовали 0,1 М раствор NaOH, который продували высокочистым N 2 . или O 2 газ примерно за 30 мин перед тестированием. Тесты линейной вольтамперометрии (LSV) проводились при скорости вращения 1600 об / мин и скорости развертки потенциала 10 мВ с -1 . Тест стабильности проводился на рабочей станции Autolab Electrochemical Instrumentation (Metrohm) в стандартной трехэлектродной системе, в которой OER определялся хронопотенциометрией при постоянной плотности тока 10 мА см −2 в 0,1 М NaOH с загрузкой 0,2 мг / см -2 и ORR было выполнено с помощью хроноамперометрического теста отклика, выполненного при постоянном потенциале 0,8 В при тех же условиях. Все потенциалы откалиброваны относительно обратимого водородного электрода (RHE).
Результаты и обсуждение
Как показано на рис. 1a, дифракция рентгеновских лучей (XRD) показала, что мы успешно синтезировали многогранники органических каркасных материалов с переходными металлами. При повышении температуры карбонизации дифракционные пики при 44,216 °, 51,522 ° и 75,853 ° становятся более отчетливыми, что хорошо согласуется с плоскостями (111), (200) и (220) кубического кобальта (PDF № 15- 0806). Как всем известно, температура отжига оказывает существенное влияние на физико-химические и электрохимические характеристики образцов [29, 30]. Таким образом, на полученных образцах с серией температурных градиентов были проведены электрохимические измерения для исследования оптимизированной температуры. На рис. 1б показана электрохимическая активность материалов, обработанных при различных температурах. Очевидно, что полученный катализатор, карбонизированный при 700 ° C (Co / MOFs-700), демонстрирует наилучшие характеристики OER. Перенапряжение составляет около 480 мВ для достижения плотности тока 10 мА см −2 . в 0,1 М NaOH.
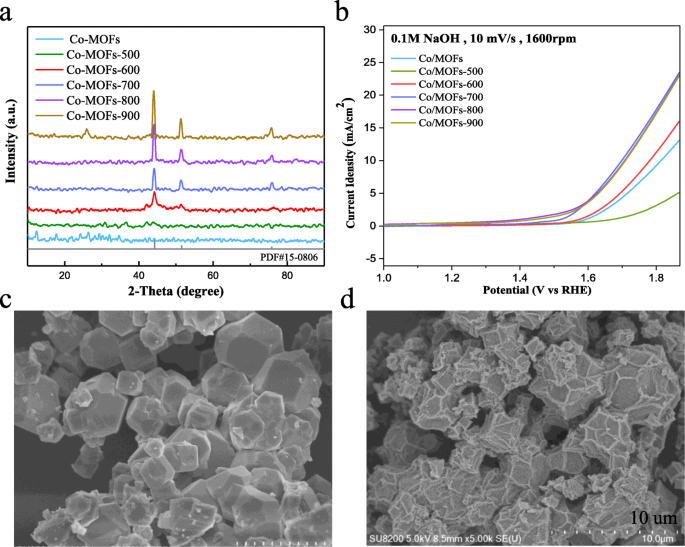
а Рентгенограммы образцов Co / MOF перед карбонизацией и карбонизацией при разных температурах. б Кривые LSV для OER Co / MOF, Co / MOF-500, Co / MOF-600, Co / MOF-700, Co / MOF-800 и Co / MOF-900. c , d СЭМ-изображения образца Co / MOFs-700 до и после карбонизации
Затем были выбраны Co / MOF перед карбонизацией и наиболее эффективные Co / MOF-700 для проведения измерений на сканирующем электронном микроскопе. Как показано на рис. 1c, d, морфология полученного Co / MOF-700 сильно изменилась после карбонизации при 700 ° C. На его поверхности появляется множество складок, которые не более гладкие, чем исходные материалы без карбонизации. Но он по-прежнему обрабатывает морфологию многогранника с регулярной дисперсией частиц и без знака коллапса.
Как сообщалось в предыдущих статьях, добавление люминофора в органический каркасный полиэдр переходных металлов может повысить стабильность образца в кислотном или щелочном растворе, а также может эффективно улучшить электрохимическую каталитическую активность за счет нарушения электронейтральности и облегчения O 2 адсорбция [31,32,33]. Поэтому образцы, легированные фосфором, были синтезированы методом легирования in situ и исследованы электрохимические характеристики. Полученные продукты были названы Co / P0 / MOFs-700, Co / P1 / MOFs-700 и Co / P2 / MOFs-700, в то время как P0, P1 и P2 представляют собой источники фосфора гипофосфита натрия, трифенилфосфина и О -триметилфенилфосфин соответственно.
Согласно рис. 2а, дифракционные пики легированных фосфором образцов все еще имеют структуру кубического кобальта (PDF № 15-0806), что указывает на то, что легирование небольшим количеством люминофора не изменит структуру MOF. Затем были проведены электрохимические измерения для изучения влияния различных источников фосфора на электрохимическую каталитическую активность. Как показано на рис. 2c, открытый потенциал (0,87 В) и потенциал полуволны (0,78 В) показывают, что Co / P1 / MOFs-700 обладает наилучшей активностью ORR. Однако он немного слабее, чем у исходного продукта Co / MOFs-700, карбонизированного при той же температуре. На рисунке 2d представлены характеристики OER для различных продуктов, легированных фосфором. Когда ограниченная плотность тока составляет 10 мА см −2 , только Co / P1 / MOFs-700 обладает самым низким перенапряжением 430 мВ, демонстрируя, что включение фосфора в образцы может увеличить активность OER, что совпадает с опубликованной статьей о том, что включение фосфора может регулировать электрическую проводимость и в то же время облегчать быстрый перенос электронов [34]. Кроме того, на рис. 2b показано сравнение между образцом с трифенилфосфином в качестве источника фосфора и исходным образцом (рис. 1с) без включения элементов. Можно обнаружить, что включение фосфора сильно повлияло на морфологию материала по сравнению с Co / MOFs-700. Поэтому легирующий люминофор может не только повысить электрохимическую активность, но и изменить морфологию образца.
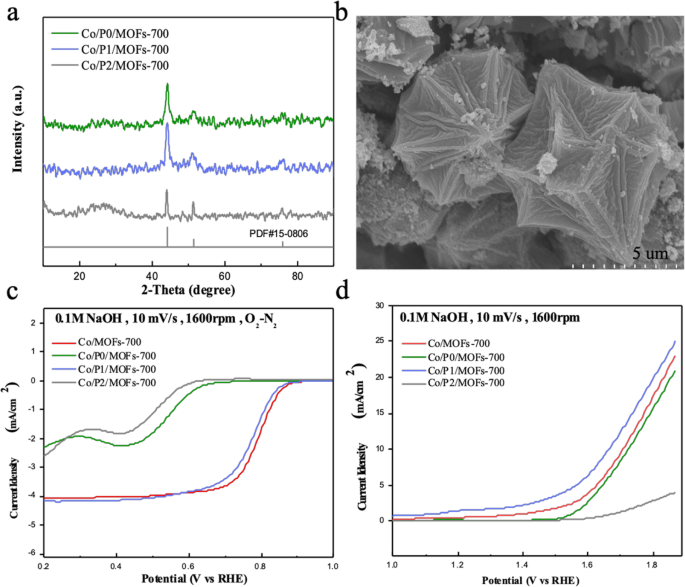
а Рентгенограмма Co / P0 / MOFs-700, Co / P1 / MOFs-700 и Co / P2 / MOFs-700. б СЭМ изображения Co / P1 / MOFs-700. c Поляризационные кривые ORR образцов, легированных фосфором. г Поляризационные кривые ООР образцов, легированных фосфором
Впоследствии, чтобы выяснить причину, по которой легирование фосфором может усилить электрохимическую активность, был проведен анализ XPS для исследования состава и химического состояния образцов Co / MOFs-700 и Co / P1 / MOFs-700. Согласно рис. 3а, обзор XPS-спектров Co / MOFs-700 и Co / P1 / MOFs-700 показывает присутствие Co 2p, O 1s, N 1 и C 1s. Следует отметить, что пик P 2p появляется в обзоре спектров XPS в Co / P1 / MOFs-700, но показывает довольно слабый сигнал по сравнению с сильными пиками C 1s. Кроме того, на рис. 3b показаны Co 2p-спектры Co / MOF-700 и Co / P1 / MOF-700. Было обнаружено, что Co 2p 3/2 можно уместить в два пика. Пики, расположенные под 778,2 ° и 780,7 °, можно отнести к Co (0) и Co (2 + ), в то время как Co 2p 1/2 может также отображаться в виде двух пиков, расположенных под 793,3 ° и 796,7 °, которые можно отнести к Co (0) и Co (2 + ). Пики спутников располагались под 786,2 ° и 802,7 ° [35,36,37]. При сравнении с образцом Co / P1 / MOFs-700, легированным фосфором, мы можем обнаружить, что Co (0) значительно увеличился, в то время как Co (2 + ) уменьшилось, что указывает на то, что легирование источника фосфора в процессе синтеза может увеличить содержание Co (0) в полученных образцах. Как всем нам известно, Co (0) может значительно повысить проводимость, тем самым улучшая электрохимические характеристики, что также соответствует предыдущему отчету [38].
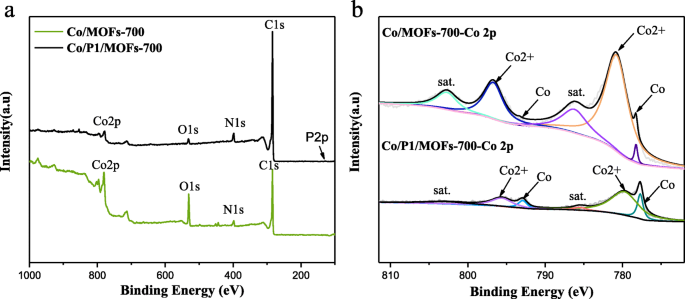
а Обзор РФЭС спектров Co / MOFs-700 и Co / P1 / MOFs-700. б Co 2p-спектры Co / MOF-700 и Co / P1 / MOF-700
После этого мы продолжили исследование влияния на качество источника легированного фосфора. Полученные продукты с различным молярным соотношением P были названы Co / P / MOFs-700-x ( x =0,25, 0,5, 0,75, 1,0), в то время как P представляет собой трифенилфосфин, а x представляет качество источника фосфора. Рисунок 4a показывает, что при увеличении содержания источников фосфора дифрактограмма показывает, что основные дифракционные пики в этих образцах по-прежнему принадлежат кобальту (PDF № 15-0806). Как показано на рис. 4b, Co / P / MOFs-700-0.5 обладает лучшей активностью ORR, чей полуволновой потенциал составлял около 0,8 В среди этих продуктов, допированных фосфором, но активность ORR Co / P / MOFs-700-0,5 составляет существенно не увеличился по сравнению с исходным образцом Co / MOFs-700. Из рис. 4с видно, что активность ООР образцов значительно увеличивалась при добавлении трифенилфосфиновых соединений и снижалась с увеличением массы источника фосфора. Когда ограниченная плотность тока составляет 10 мА см −2 , Co / P / MOFs-700-0,25 и Co / P / MOFs-700-0,5 оба обладают минимальным перенапряжением 450 мВ, что указывает на то, что только надлежащее количество источников фосфора может улучшить активность OER, в то время как количество 0,25 и 0,5 показывает наилучшие результаты. . Однако по сравнению с коммерческим платиновым углеродом (потенциал полуволны 0,81 В, предельная плотность тока 5,43 мА · см −2 ) и превосходный оксид иридия электрокатализатора OER (1,61 В @ 10 мА см −2 ), Co / P / MOFs-700-0,5 по-прежнему остается значительной разницей среди ограниченной плотности тока в производительности ORR. Как сообщается в статье, когда проводимость материала мала, то ограничивается и плотность тока [39].
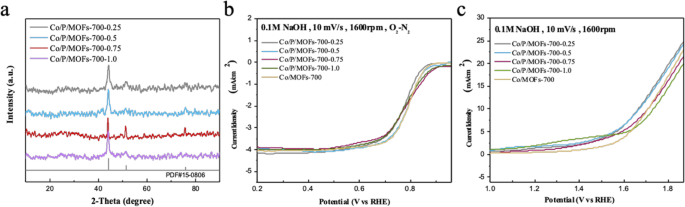
а Рентгенограммы легирования различных источников фосфора в Co-MOF. б , c Поляризационные кривые ORR и OER Co / MOFs-700, Co / P / MOFs-700-0,25, Co / P / MOFs-700-0,5, Co / P / MOFs-700-0,75 и Co / P / MOFs-700 -1.0 соответственно
Чтобы повысить проводимость, мы сначала измерили текущее содержание углерода в синтезированном Co / P / MOFs-700-0,5, проанализированном с помощью изображений EDS. Согласно рис. 5 очевидно, что качество кобальта составляет большую часть, что составляет почти 52,38%, в то время как качество углерода относительно меньше - 29,13%.
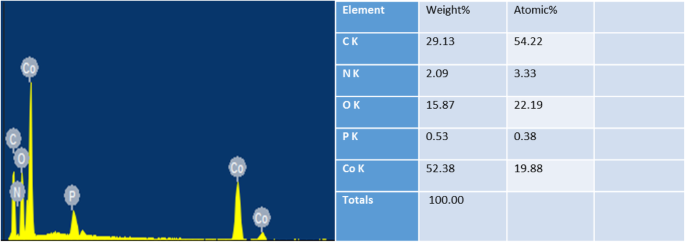
ЭЦП Co / P / MOFs-700-0,5
Поэтому, чтобы улучшить проводимость материала, мы дополнительно легировали образцы углеродом без каких-либо источников фосфора. Полученные продукты были названы Co / MOFs-CNTs-700, Co / MOFs-CB-700 и Co / MOFs-A-OMCS-700 соответственно. На рис. 6а показано, что легирование углеродом не повлияет на структуру образцов, которая по-прежнему сохраняет те же дифракционные пики кобальта (PDF № 15-0806). Как показано на рис. 6b, можно видеть, что ограниченная плотность тока продуктов значительно увеличивается с включением источника углерода в ORR, в то время как рис. 6c показывает, что включение источника углерода не имеет смысла для улучшения свойств OER. катализаторов.
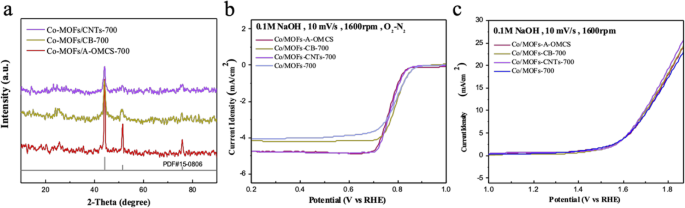
а Рентгенограммы легирования различных источников углерода в Co-MOF. б , c Поляризационные кривые ORR и OER Co / MOFs-700, Co / MOFs-CNTs-700, Co / MOFs-A-OMCS-700 и Co / MOFs-CB-700 соответственно
В сочетании с предыдущими экспериментальными данными и выводами мы легировали исходный образец фосфором и углеродными элементами, добавив 0,5 г трифенилфосфина и подходящее количество различных источников углерода (УНТ, CB и A-OMCS) в материал для сравнения. Полученные образцы были названы Co / P / MOFs-CNTs-700, Co / P / MOFs-CB-700 и Co / P / MOFs-A-OMCS-700 соответственно. Согласно рис. 7а, картина рентгеновской дифракции не изменилась, поскольку все образцы хорошо согласуются с кубическим кобальтом (PDF № 15-0806). Как показано на рис. 7b, совместное легирование фосфором и углеродом значительно увеличило ограниченную плотность тока и характеристики ORR продуктов. Образец Co / P / MOFs-CNTs-700 показывает лучшую активность ORR, в которой потенциал полуволны и предельная плотность тока составляют 0,8 В и 4,81 мА см −2 и на 10 мВ ниже, чем у коммерческого платинового углерода. Кроме того, как ясно видно на рис. 7c, показатели OER продуктов также значительно улучшились. Образец Co / P / MOFs-CNTs-700 показывает самое низкое перенапряжение 420 мВ (Таблица 1). По сравнению с напряжением, соответствующим диоксиду иридия, Co / P / MOFs-CNTs-700 только примерно на 40 мВ выше, чем диоксид иридия. Таким образом, Co / P / MOFs-CNTs-700 является подходящим бифункциональным электрокатализатором.
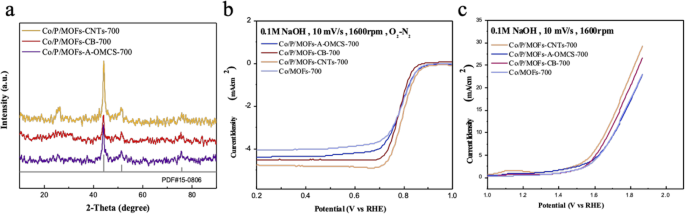
а Рентгенограммы Co / P / MOFs-CNTs-700, Co / P / MOFs-A-OMCS-700 и Co / P / MOFs-CB-700. б , c Кривые ORR и OER LSV для указанных выше образцов, соответственно
Между тем, чтобы оценить стабильность наиболее эффективных Co / P / MOFs-CNTs-700, были проведены тесты хронопотенциометрии и хроноамперометрии. Как видно на рис. 8a, b, перенапряжение увеличилось только на 1,5 мВ, а производительность ORR снизилась на 79,5% после 18 часов непрерывных испытаний, что доказывает, что как OER, так и ORR активности Co / P / MOFs-CNTs-700 являются довольно стабильна в 0,1 М NaOH.
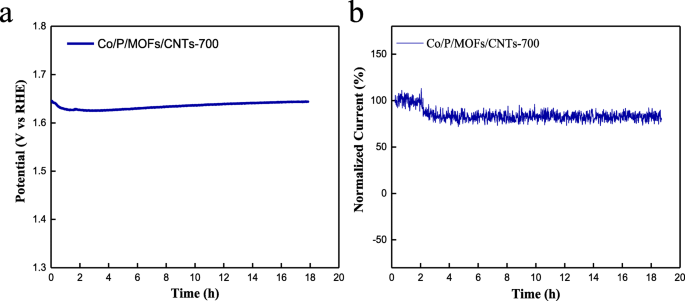
а Измерение хронопотенциометрии Co / P / MOFs-CNTs-700. б Хроноамперометрический отклик Co / P / MOFs-CNTs-700
Также были выполнены сканирующая электронная микроскопия, EDS и картирование на образце Co / P / MOFs-CNTs-700. Как видно из рис. 9a – c, Co / P / MOFs-CNTs-700 сохранил морфологию многогранника с множеством складчатых линий на поверхности. Кроме того, углеродные нанотрубки внедряются в каркас продукта, что может увеличить удельную поверхность продукта и обеспечить больше участков адсорбции для электрохимической реакции. Рисунки 9 d – g представляют собой анализ карты образца. Видно, что источники углерода и фосфора равномерно диспергированы в скелете образца и становятся целыми.

СЭМ изображения Co / P / MOFs-CNTs-700 ( a - c ) и соответствующее элементарное отображение Co ( d ), P ( e ), C ( f ) и N ( g ) соответственно
Как показывает EDS, содержание фосфора и углерода в материале увеличено по сравнению с исходным образцом Co / MOFs-700 за счет легирования in situ, что приводит к увеличению активности ORR и OER (рис. 10). Попутно продемонстрировано, что включение двух видов фосфора и углеродных элементов может быть полезным для увеличения электрохимической активности металлоорганических каркасных материалов, содержащих кобальт [40], поскольку электроотрицательность P (2.19) отличается от электроотрицательности атомов углерода ( С 2,55). Совместное допирование нарушит электронейтральность, что может способствовать O 2 адсорбция и повышение активности ORR [41]. Между тем, большее количество активных центров может возникнуть из-за совместного легирования фосфором и углеродом за счет изменения асимметричной спиновой плотности гетероатомов и эффективного ослабления связи O-O, что приводит к усилению активности ORR [42].
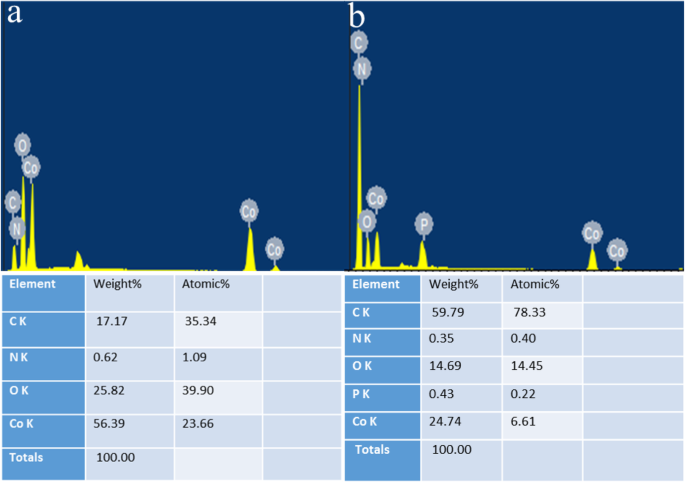
а , b EDS-анализ Co / MOF-700 и Co / P / MOF-CNT-700, соответственно
Выдающуюся электрохимическую активность можно объяснить следующими причинами. Во-первых, легирование гетероатомов приведет к перераспределению плотности заряда на поверхности катализатора, что способствует адсорбции кислорода и повышению активности ORR [43]. Во-вторых, совместное допирование различных атомов в MOF привело бы к синергетическому эффекту, который также способствует улучшенным электрохимическим характеристикам [44]. В-третьих, было доказано, что механизм OER катализатора на основе Co представляет собой динамический процесс самовосстановления поверхности. Атомы Co на поверхности могут образовывать самоорганизующийся активный слой оксида (гидроксида) металла CoOOH, который работает как реальный активный центр [45]. Помимо состава, уникальная гибридная структура в сочетании с высокой проводимостью может обеспечить большую площадь поверхности для быстрой передачи заряда.
Заключение
В заключение, был успешно синтезирован эффективный и экономичный многогранный углеродный наноматериал с органическим каркасом переходного металла (Co / P / MOFs-CNTs-700), совместно легированный фосфором и источниками углерода, который может служить эффективным и дешевым бифункциональным электрохимическим продуктом. катализатор. Наименьшее перенапряжение Co / P / MOFs-CNTs-700 составляет 420 мВ для достижения плотности тока 10 мА · см −2 . для OER, а полупотенциал составляет 0,8 В для ORR в 0,1 М NaOH, что очень близко к таковым для коммерческих электрохимических катализаторов. Он может быть использован в качестве многообещающего электрохимического бифункционального электрокатализатора в области накопления энергии, а также может дать многообещающее представление о разработке электрохимического бифункционального электрокатализатора.
Доступность данных и материалов
Данные, использованные для подтверждения результатов этого исследования, включены в статью.
Сокращения
- ORR:
-
Реакция восстановления кислорода
- OER:
-
Реакция выделения кислорода
- SEM:
-
Сканирующая электронная микроскопия
- HAADF:
-
Круговое темное поле под большим углом
- EDS:
-
Энергодисперсионный спектрометр
- STEM:
-
Сканирующая просвечивающая электронная микроскопия
- XPS:
-
Рентгеновская фотоэлектронная спектроскопия
- XRD:
-
Рентгеновская дифракция
- RDE:
-
Вращающийся дисковый электрод
- Co-MOFs-x:
-
Металлоорганические каркасы кобальта-x представляет температуру
- Co / P-MOFs:
-
Кобальт / фосфор-металлорганические каркасы
- Co / P / MOFs-700-0.25:
-
Кобальт / фосфор-металлоорганические каркасы-700 ° C-масса источника фосфора 0,25
- Co-MOFs-C:
-
Кобальт-металлоорганические каркасы-углерод
- Co / P-MOFs-CNTs-700:
-
Кобальт / фосфор-металлорганические каркасы-углеродные нанотрубки-700 ° C
- GC:
-
Стеклоуглерод
- LSV:
-
Вольтамперометрия с линейной разверткой
- RHE:
-
Реверсивный водородный электрод
- Pt / C:
-
Платиновый / угольный катализатор
Наноматериалы
- Роль углеродного волокна в аэрокосмических материалах
- Производство композитных материалов:почему углеродное волокно лучше
- Материалы:полипропилен, армированный стеклом и углеродным волокном, для автомобилей
- Раскрытие атомной и электронной структуры углеродных нановолокон с набором чашек
- Композиты с квантовыми точками на S, N-графене / TiO2 для эффективного фотокаталитического производства водород…
- Синтез обогащенных пиридином N, S-углеродных квантовых точек как эффективных имитаторов ферментов
- Исследование каркаса Zr – металл – органика как эффективного фотокатализатора для производства водорода
- Проектирование чистых и композитных углеродных нанотрубок с помощью порозиметрических характеристик
- Композит Na4Mn9O18 / углеродных нанотрубок как материал с высокими электрохимическими характеристиками для водн…
- Сравнительное исследование электрохимических, биомедицинских и тепловых свойств природных и синтетических…



