Углеродные точки как материалы нового поколения для нанотермометра:обзор
Аннотация
Высокочувствительное бесконтактное измерение температуры важно для изучения фундаментальных химических реакций, биологических процессов и приложений в медицинской диагностике. Термометры на основе наномасштаба гарантируют неинвазивные датчики для чувствительного и точного измерения температуры с субклеточным разрешением. Датчики температуры на основе флуоресценции продемонстрировали большую производительность, поскольку они работают в «бесконтактном» режиме и предлагают двойные функции - визуализацию клеток и определение температуры на молекулярном уровне. Достижения в области наноматериалов и нанотехнологий привели к разработке новых сенсоров, таких как нанотермометры (новые термочувствительные материалы с высоким пространственным разрешением на наномасштабе). Такие нанотермометры были разработаны с использованием различных платформ, таких как флуоресцентные белки, органические соединения, металлические наночастицы, наночастицы, легированные редкоземельными элементами, и полупроводниковые квантовые точки. Углеродные точки (CD) привлекли интерес во многих областях исследований из-за выдающихся свойств, таких как сильная флуоресценция, устойчивость к фотообесцвечиванию, химическая стабильность, недорогие прекурсоры, низкая токсичность и биосовместимость. Недавние отчеты показали, что некоторые компакт-диски обладают термочувствительностью, что делает их альтернативой другим термометрам на основе наноматериалов. Этот вид термометра на люминесцентной основе перспективен для измерения температуры в нанополости и теплового картографирования, чтобы лучше понять биологические процессы. Поскольку компакт-диски все еще находятся на начальной стадии в качестве материала на основе нанометров для измерения температуры, в этом обзоре мы даем исчерпывающее представление об этом новом нанотермометре, методах функционализации для повышения термочувствительности и разрешающей способности, а также о механизме поведения датчика температуры. P>
Температура - это фундаментальная термодинамическая переменная, которая оказывает заметное влияние на биологические и химические системы. Точное определение температуры имеет большое значение в связи с широким спектром его применения почти во всех областях естествознания, инженерии, сельского хозяйства и медицины [1, 2]. В медицине термометрия используется для раннего выявления различных заболеваний, таких как инсульт, рак или воспаления, одним из первых симптомов которых является появление локальных температурных особенностей.
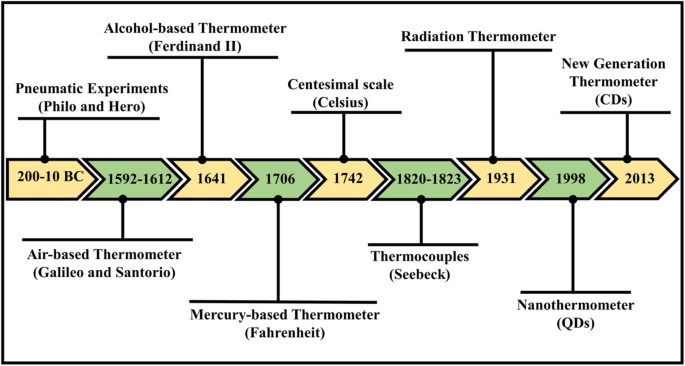
В истории самые ранние оценки температуры основывались на ощущениях или наблюдениях. В древние времена, 200–10 гг. До н.э., пневматические эксперименты (расширение воздуха за счет тепла) считались старейшими признанными образцами аппаратов, используемых для количественного измерения тепла. Среди наиболее примитивных работ, связанных с тепловым расширением воздуха, приписывают работы Филона Византийского и Героя (или Герона) Александрийского относительно пневматических экспериментов [3]. Позже, между 1592 и 1603 годами, Галилео Галилей изобрел термоскоп, поставив эксперименты с расширением воздуха за счет тепла, построив простой прибор с использованием трубки, содержащей воздух, захваченный над водяным столбом. Вслед за Галилео, итальянский Санторио получил аккредитацию первым за внедрение этого простого аппарата в медицинские обследования лихорадки. Первый полностью герметичный жидкостный стеклянный термометр, стеклянная трубка, заполненная спиртом, был собран Фердинандом II в 1641 году. Он мог измерять температуру без помощи атмосферного давления, в отличие от открытого термоскопа Галилео и Санторио. Практическая работа Фаренгейта по термометрии началась в 1706 году; он начал с алкоголя, но впоследствии стал легендарным благодаря своим ртутным термометрам. Признание сотенной шкалы температур получил Андерс Цельсий, который в 1742 году спроектировал шкалу с нулем при температуре кипения воды и 100 при температуре замерзания воды. Электронные эксперименты проводились в девятнадцатом веке, когда Томас Иоганн Зеебек рассматривал концепцию термоэлектричества. В серии экспериментов, проведенных между 1820 и 1823 годами, он проверил электрический потенциал в точках соединения двух разных металлов, когда между соединениями существует разница в температуре. Позже это было известно как эффект Зеебека, и он служит источником термопары, которая считается наиболее точным средством измерения температуры [3,4,5,6,7]. Схематическая временная шкала термометра показана на рис. 1.
Схема временной шкалы развития термометров
Обычные термометры можно разделить на:
Стеклянные термометры с жидким наполнением на основе теплового расширения материалов
Термопары на основе эффекта Зеебека
Оптические датчики [8]
Кроме того, их можно разделить на контактные и бесконтактные термометры. Контактный режим, включая классическое заполненное жидкостью стекло, термопары, термисторы и резистивные датчики температуры (RTD), все требует подключения электрических кабелей и прямого контакта между термометром и подложкой. Этот режим не подходит для приложений, в которых электромагнитный шум сильный, искры могут быть опасными, окружающая среда разрушительна или детали быстро перемещаются. Кроме того, традиционные термометры не способны проводить измерения при понижении пространственного разрешения до субмикронного масштаба, например, при изменении внутриклеточной температуры и отображении температуры микросхем и микрофлюидики [9]. Точно так же инженерные приложения требуют передовых стратегий термочувствительности для миниатюрных регионов и сложных условий [10]. Таким образом, для наноразмерных доменов следует подумать о других подходах и материалах.
Новая бесконтактная термометрия может решить вышеупомянутые проблемы. Например, оптические термодатчики (молекулярные термометры) являются более поздним поколением аналитических инструментов, которые состоят из классов молекул, которые используют измерение излучаемого света для определения температуры [11, 12]. Флуоресцентные термочувствительные датчики представляют собой многообещающую область термометрии в приложениях наносистем. Информация о температуре может быть извлечена на основе их интенсивности флуоресценции, формы полос, стоксова сдвига или времени распада, может относиться к температуре, если правильно откалибрована [13, 14].
Молекулярные термометры обладают большим потенциалом в диагностике больных или канцерогенных клеток, физиологические температуры которых отличаются от температуры обычных клеток. В медицинских приложениях возможности варьируются от температурно-индуцированного контроля экспрессии генов [15] и клеточного метаболизма [16] до избирательного проникновения в клетки и лечения заболеваний [17], а также улучшения отвода тепла от интегрированных источников тепла [18] . В последнее время в качестве термодатчика (нанотермометра) использовались такие наноматериалы, как полупроводники [19], полимерные [10] и металлические наночастицы [20], которые показали субмикронное тепловое разрешение.
Термометры, которые могут определять субградусную температуру в широком диапазоне температур, которые также могут быть интегрированы в живые системы, могут предложить новый важный инструмент в бесчисленных областях биологических, физических и химических исследований. Поэтому в этом обзоре мы сосредоточимся на «новом поколении» или «новом классе» нанотермометров, основанных на углеродных наноматериалах (углеродистых материалах). Насколько нам известно, об углеродных точках в качестве нанотермометра не сообщалось. Недавно углеродные точки (углеродные квантовые точки, графеновые квантовые точки) вместе с их уникальными характеристиками продемонстрировали чувствительные термические свойства, которые делают их отличными кандидатами для термометрического поведения в наноразмерной области. Здесь рассматриваются определения, преимущества и механизмы термочувствительного поведения углеродных точек. Наконец, представлены будущие перспективы этого нового класса термоматериалов.
Под «нанотермометрией» подразумевается использование термочувствительных материалов нанометрового размера для получения температурной информации о локальной среде нано- или микромасштабной области [21, 22]. Тепловые зонды на основе наночастиц обладают большой производительностью в широком спектре приложений измерения, и в последнее время появились сообщения о многочисленных прогрессивных так называемых «нанотермометрах». Кроме того, сообщалось, что различные виды обычных наноматериалов обладают термочувствительными люминесцентными свойствами, такие как полимеры [23, 24], нанокристаллы [25], наночастицы, легированные редкоземельными элементами [26, 27] и металлические наночастицы [28]. / P>
Таким образом, нанотермодатчики представляют собой неинвазивные, бесконтактные, точные термометры, работающие в наномасштабе с высоким разрешением [9]. Температурное зондирование с использованием наноматериалов может быть достигнуто путем изменения их оптических свойств. Флуоресцентную нанотермометрию можно разделить на несколько классов в зависимости от точного параметра, на основе которого производятся тепловые измерения, включая интенсивность сигнала, форму полосы, время жизни флуоресценции, сдвиг полосы, поляризацию длины волны возбуждения и спектральный сдвиг. В первом случае флуоресценция изменяется при изменении температуры и может быть обнаружена как абсолютное увеличение (или уменьшение) сигнала [9, 29,30,31].
Бесконтактная люминесцентная нанотермометрия, в которой используются люминесцентные наноматериалы с температурно-зависимым излучением, в основном подходит для биологических приложений [32, 33]. Эти люминесцентные наноматериалы включают флуоресцентные полимеры [24], металлические наночастицы [34], наночастицы, легированные редкоземельными элементами [35] и наноалмазы [36], которые обладают термочувствительными свойствами в физиологическом диапазоне. Эти новаторские работы были способны обеспечить среднюю температуру для отдельных ячеек. Температурно-зависимые люминесцентные зонды на основе органических красителей (например, родамин 6G) и полимеров (например, поли ( N -изопропилакриламид)) обычно демонстрируют плохую фотостабильность и выраженную перекрестную чувствительность к кислороду, что нежелательно для работы с живыми клетками [8]. Кроме того, существует сильная зависимость pH от срока службы флуорофора, что затрудняет его использование без точного контроля pH окружающей среды [37].
Сообщалось о другом классе нанотермометров, основанных как на чистых, так и на легированных полупроводниковых нанокристаллах, с наиболее известными кандидатами, такими как CdSe, ZnS, InP или PbSe [19, 38, 39, 40]. Полупроводниковые квантовые точки (ПКТ) являются кандидатом на роль наноразмерных термометров, учитывая, что они имеют высокий квантовый выход, длительный срок службы до фотообесцвечивания и адекватную биосовместимость после надлежащей модификации поверхности. Кроме того, они могут быть легко конъюгированы с белками и ДНК для зондирования и визуализации [41]. Исключительная проблема, с которой сталкиваются люминесцентные термометры этого типа, - связанное с ними распознавание яркости, фотостабильности, чувствительности и точности при T =20–40 ° C при зондировании субклеточной микросреды. SQD были подробно рассмотрены с точки зрения синтеза, физико-химических свойств, люминесценции, а также их потенциальных применений. Здесь мы обращаем внимание читателя на эти многочисленные замечательные обзоры [42,43,44,45,46]. По сравнению с органическими красителями SQD демонстрируют превосходную яркость для обнаружения, более широкий профиль возбуждения для мультиплексирования и лучшую фотостабильность для долгосрочных исследований. Кроме того, SQD в качестве датчиков температуры устойчивы к pH и другим изменениям окружающей среды, которые, как ожидается, будут преобладать внутри клетки [47].
Как правило, в SQD из-за комбинации различных процессов повышение температуры вызывает уменьшение интенсивности флуоресценции (тушение), которое сопровождается спектральным сдвигом. Этот сдвиг можно считать линейным в биофизическом диапазоне. Величина обоих эффектов (тушение люминесценции и спектральный сдвиг) сильно зависит от материала, из которого состоят квантовые точки, и от их размера [48].
Каждая группа люминесцентных наноматериалов имеет ограничения в использовании, а также свои преимущества. Как описано выше, SQD предпочтительнее флуоресцентных полимеров и органических красителей. SQD хороши с точки зрения фотостабильности, квантовой эффективности и настраиваемой флуоресценции, но QD не могут использоваться для отслеживания отдельной молекулы для долгосрочного мониторинга из-за их внутреннего мерцания [49]. Более того, основная проблема КТ - их токсичность, которая связана с содержанием в них тяжелых металлов, включая такие металлы, как кадмий; это ограничивает их биологические и экологические применения. Кроме того, наличие элементов-прекурсоров в природе относительно невелико, и поэтому SQD считаются дорогостоящими [50].
Чтобы преодолеть проблемы, возникающие при использовании неуглеродных нанотермометров (как мы объясняли в предыдущем разделе), были приготовлены углеродные наноматериалы, обладающие уникальными свойствами, такими как низкая токсичность, простота приготовления, недорогой прекурсор, фотостабильность. , и биосовместимость. Эти углеродные наноматериалы показали чувствительные термочувствительные свойства. Кроме того, улучшение безметалловых наночастиц является важным и неотложным из-за опасности для окружающей среды при биологических применениях таких токсичных материалов [51, 52]. Среди семейства углеродных наноматериалов о флуоресцентных наноалмазах впервые было сообщено как о нанотермометрах [53]. Флуоресцентные наноалмазы обладают внутренней биосовместимостью, обусловленной их химически устойчивой и инертной поверхностью [54]. Другие наноалмазы недавно были использованы для внутриклеточного термодатчика с точностью до степени ниже [55, 56]. Термическая чувствительность этих наноалмазов основана на так называемых азотно-вакансионных центрах окраски, которые представляют собой точечные дефекты, состоящие из атома азота, замещающего атом углерода решетки, и ближайшего вакантного узла решетки [48, 57]. Азот-вакансионный центр флуоресцентных наноалмазов широко изучается и хорошо охарактеризован с точки зрения фотофизики, а также использования в биологических приложениях [58]. Принцип работы термометрии на основе вакансий азота зависит от точного измерения этого центра окраски, который может быть оптически обнаружен с высоким пространственным разрешением [30, 59]. Однако низкая эффективность флуоресценции и плохая управляемость сильно затрудняют применение флуоресцентных наноалмазов [36].
Один из новейших классов семейства углеродных наноматериалов - это высоколюминесцентные углеродные точки (CD), которые обладают исключительной яркой фотолюминесценцией, фотохимической стабильностью, растворимостью в воде, большой биосовместимостью и нетоксичностью [60,61,62]. КД представляют собой нульмерные наночастицы сферической формы с диаметром менее 10 нм [63, 64]. Для приготовления различных типов КД применялись различные подходы, например, лазерная абляция [65], сольвотермический [66], гидротермальный синтез [67], с помощью микроволнового излучения [68], дуговый разряд [69], кислотное окисление [70], и другие химические и физические подходы [71, 72]. Кроме того, компакт-диски демонстрируют желаемую перспективу для различных приложений, таких как биологическая визуализация [73], химическая и биосенсорная [74,75,76,77], адресная доставка лекарств [78], фармацевтический анализ [79] и катализ [80, 81]. Углеродные точки были подробно рассмотрены с точки зрения синтеза, физико-химических свойств, а также их потенциального применения. Здесь мы отсылаем читателя к многочисленным хорошим обзорам углеродных точек [72, 82,83,84,85,86,87,88].
В последние годы флуоресцентные компакт-диски в качестве датчиков температуры привлекают большое внимание исследователей. В принципе, для эффективного измерения температуры необходимы некоторые требования, например, углеродные наноточки должны демонстрировать заметное изменение своей фотолюминесценции в диапазоне соответствующих температур [89]. Фотостабильность, стабильность pH и срок хранения - это другие требования, которые следует учитывать при практическом применении.
Компакт-диски являются многообещающей альтернативой обычным полупроводниковым квантовым точкам (SQD). По сравнению с квантовыми точками компакт-диски демонстрируют множество выдающихся преимуществ, таких как низкая стоимость, низкая токсичность и уникальные прочные оптические / химические свойства [90]. Кроме того, компакт-диски демонстрируют гораздо меньшее фотообесцвечивание. По сравнению с другим флуоресцентным сырьем, компакт-диски производятся из недорогих источников углерода, которые широко распространены в природе [91]. Кроме того, существует несколько простых методов модификации и функционализации состояния поверхности ЦД, которые позволяют адаптировать растворимость, стабильность, физико-химические свойства и квантовые выходы ЦД в соответствии с их экспериментальными требованиями [49, 92, 93].
В литературе очень мало статей об углеродных точках с температурно-зависимой флуоресценцией, которые показаны в таблице 1.
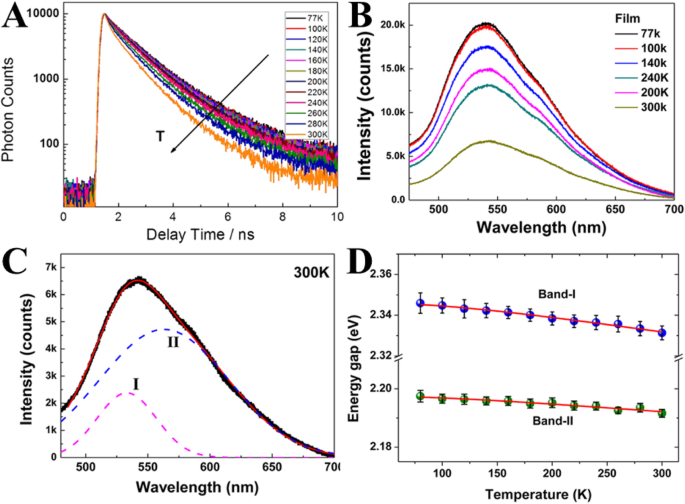
Yu et al. [51] в 2012 году первыми исследовали температурно-зависимую флуоресценцию углеродных наноточек и сравнили их с полупроводниками и наночастицами на основе металлов. Они зависели от измерения времени жизни фотолюминесценции в зависимости от температуры с помощью метода коррелированного по времени однофотонного счета (TCSPC). Динамика релаксации фотолюминесценции ускоряется при повышении температуры (рис. 2а), что можно объяснить процессами безызлучательного распада. Было проведено измерение спектров флуоресценции пленки КД в зависимости от температуры от криогенной до комнатной температуры (рис. 2б). С повышением температуры интенсивность флуоресценции периодически уменьшается.
а Измерения фотолюминесценции с временным разрешением как функция температуры. б Спектры флуоресценции CD-пленки в зависимости от температуры. c Спектры флуоресценции при 300 К, аппроксимированные двухгауссовой функцией. г Ширина полосы флуоресценции как функция температуры. (Воспроизведено с разрешения из ссылки [51])
Спектр ФЛ демонстрирует асимметричные пики, поэтому спектры ФЛ при каждой температуре могут быть хорошо аппроксимированы двухгауссовой функцией, показанной на рис. 2в. Полоса высоких энергий, полоса I; полоса низких энергий, полоса II (рис. 2г).
Кроме того, энергетическая щель (ширина полосы) флуоресценции была проверена как функция температуры (рис. 2d). Полная ширина полосы проявляется в зависимости от температуры (электрон-электронное рассеяние) и от температуры (электрон-фононное и поверхностное / дефектное рассеяние). Ширина полосы I и полосы II не зависит от температуры, что указывает на преобладание электрон-электронного рассеяния в компакт-дисках.
Таким образом, слабый температурный эффект в КД согласуется с тем фактом, что основной механизм взаимодействия связан с электрон-электронным взаимодействием, а не с электрон-фононным взаимодействием. Кроме того, широкая полоса фотолюминесценции (> 100 нм), обычно наблюдаемая даже при очень низкой температуре (77 К), связана с сильным электрон-электронным взаимодействием (рис. 2в). Этот результат аналогичен металлическим нанокластерам и отличается от полупроводниковых квантовых точек. Поэтому Ю и его коллеги предположили, что π-электроны в компакт-дисках могут действовать аналогично свободным электронам в металлических нанокластерах.
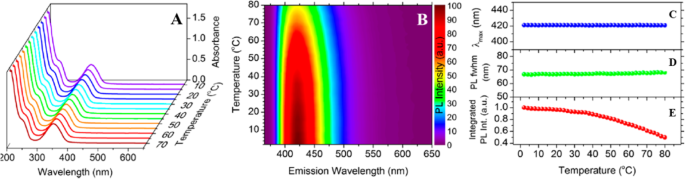
Каличук и др. [89] синтезировали высоколюминесцентные водорастворимые N, S-CD путем одностадийной гидротермальной обработки лимонной кислотой и l-цистеином. Они собрали стационарные спектры поглощения в широком диапазоне температур, чтобы охарактеризовать свойства фотолюминесценции компакт-дисков в зависимости от температуры. Спектры поглощения N, S-CD, диспергированных в воде при температурах от 10 до 70 ° C (увеличиваясь на 5 ° C за шаг), показаны на рис. 3a. В отличие от полупроводниковых нанокристаллов, положение и интенсивность полосы поглощения не менялись с температурой. Подобные результаты ранее были получены для CD, синтезированных гидротермальной обработкой глюкозы в присутствии глутатиона [1].
а Поглощение в зависимости от температуры в диапазоне температур от 10 до 70 ° C. б Нормализованный цветовой график температурно-зависимого излучения ФЛ при температурах от 2 до 80 ° C с размером шага 2 ° C и возбуждением при 355 нм. Соответствующие температурно-зависимые изменения максимума пика ФЛ λmax ( c ), PL fwhm ( d ) и интегральной интенсивности ФЛ ( e ). (Воспроизведено из ссылки [89])
В своей работе они показали цветную диаграмму спектров ФЛ N, S-CD, полученных при температурах от 2 до 80 ° C с шагом 2 ° C (рис. 3б). Повышение температуры снижает интенсивность излучения ФЛ примерно в 2 раза без какого-либо заметного сдвига излучения ФЛ [89]. Положение максимума излучения ФЛ, полная ширина ФЛ на полувысоте (fwhm) и интегральная интенсивность ФЛ были количественно определены при исследуемой температуре, что обобщает результаты на рис. 3c – e соответственно.
Положение пика ФЛ N, S-CD показывает слабую температурную зависимость, в отличие от большинства полупроводниковых нанокристаллов, ширина запрещенной зоны которых изменяется с температурой, вызывая сдвиг излучения ФЛ. Более того, их ФЛ fwhm демонстрирует лишь незначительное уширение (1,4 ± 1 нм) в том же диапазоне температур (рис. 3d), что указывает на то, что пик ФЛ N, S-CD показывает незначительное тепловое уширение. Чтобы охарактеризовать процессы безызлучательной релаксации, происходящие в КД, они проанализировали тушение интегральной интенсивности ФЛ в зависимости от температуры. График температурно-зависимой интегральной интенсивности ФЛ для N, S-CD показан на рис. 3д, со значениями, нормированными на интенсивность при 2 ° C, показывая, что интенсивность монотонно уменьшается в исследуемом диапазоне температур, а при 80 ° C примерно вдвое меньше, чем при 2 ° C. Основываясь на этих результатах, энергия активации термического тушения для CD при температурах от 2 до 80 ° C была оценена в 17,0 ± 0,7 мэВ с использованием формулы Аррениуса для N, S-CD, что близко к значению, сообщенному Ю. и другие. [51].
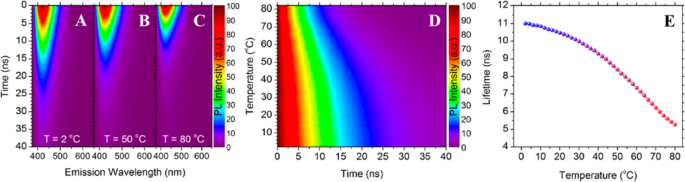
Кроме того, Каличук и др. [89] исследовали динамику излучения КД при различных температурах. На рис. 4a – c показана сильная температурная зависимость их излучения ФЛ с временным разрешением, где показаны данные эмиссионной спектроскопии с временным разрешением для трех различных температур. Карты транзиентного излучения ФЛ CD были получены в спектральной области между 375 и 650 нм при 2, 50 и 80 ° C, как показано на рис. 4a – c. Наблюдается явное уменьшение затухания ФЛ при повышении температуры, что позволяет предположить, что КД обладают удовлетворительными свойствами для измерения температуры на основе времени жизни ФЛ. Важно отметить, что спектрально однородное одноэкспоненциальное затухание наблюдалось по профилям излучения точек при всех исследованных температурах, что указывает на то, что рекомбинация происходит через очень похожие каналы с высокой эмиссией во всем ансамбле КД. Динамика PL компакт-дисков, возможно, является их наиболее многообещающим качеством в отношении приложений измерения температуры. В частности, температурная чувствительность компакт-дисков делает их нанотермометрами срока службы фотолюминесценции.
Температурно-зависимое излучение ФЛ компакт-дисков с временным разрешением. Нормализованные цветные графики, показывающие карты излучения PL с временным разрешением для компакт-дисков в a 2 ° С, b 50 ° C и c 80 ° С. г Нормализованный цветной график интенсивности ФЛ с временным разрешением в максимуме излучения ФЛ (λem =421 нм) при температурах от 2 до 80 ° C. е График зависимости времени жизни экстрагированной фотолюминесценции от температуры в диапазоне 2–80 ° C. (Воспроизведено из ссылки [89])
Изменение времени жизни фотолюминесценции компакт-дисков при температурах от 2 до 80 ° C было тщательно исследовано; На рис. 4d, e показаны данные ФЛ с временным разрешением, собранные в максимуме излучения ФЛ точек, как функция температуры. Цветовой график переходной ФЛ в исследованном диапазоне температур представлен на рис. 4г, показывающий, что повышение температуры приводит к монотонному сокращению видимого затухания ФЛ. Все записанные кривые затухания были аппроксимированы одноэкспоненциальной функцией. Данные по извлеченным временам жизни представлены на рис. 4д. При повышении температуры от 2 до 80 ° C время жизни ФЛ монотонно уменьшается с 11.0 до 5.3 нс. Температурный диапазон, в котором была продемонстрирована эта чувствительность к времени жизни фотолюминесценции (2–80 ° C), охватывает как физиологически значимый температурный диапазон, так и типичные рабочие температуры многих электронных устройств. Абсолютная псевдолинейная чувствительность этого тепловизионного зонда на основе компакт-диска со сроком службы ФЛ составляет 0,08 нс K
−1
. , а его максимальная относительная чувствительность составляет 1,79% K
−1
при 62 ° С. Одноэкспоненциальная аппроксимация затухания ФЛ люминесцентного нанозонда на основе КД в исследуемом диапазоне температур дает единственный параметр - время жизни ФЛ (τ), которое можно напрямую преобразовать в единицы температуры с помощью калибровочной кривой. Это важное преимущество перед типичными полупроводниковыми квантовыми точками, которые демонстрируют многоэкспоненциальное затухание, что ограничивает их полезность в приложениях, связанных с измерением времени жизни ФЛ.
Они также изучили температурную зависимость времени жизни ФЛ ЦД в фосфатно-солевом буфере (PBS) и среде Игла, модифицированной Дульбекко (DMEM), и показали аналогичное поведение.
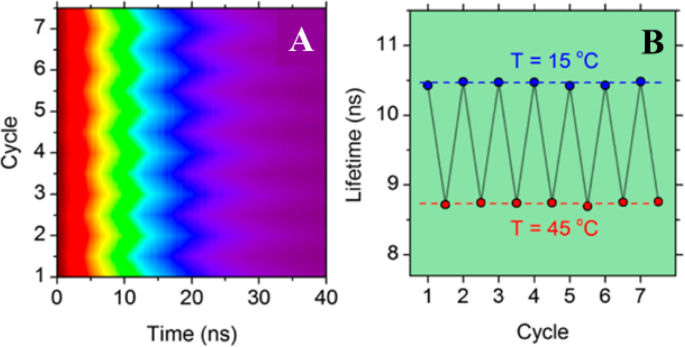
Чтобы продемонстрировать возможность повторного использования люминесцентных термометров на основе CD, кривые затухания ФЛ выбранных образцов были измерены в течение семи последовательных циклов нагрева и охлаждения при температурах от 15 до 45 ° C (рис. 5a).
а Нормализованный цветной график обратимости затухания ФЛ за семь последовательных циклов нагрева и охлаждения. б Соответствующая термическая стабильность срока службы фотолюминесценции в течение семи циклов нагрева и охлаждения от 15 до 40 ° C. (Воспроизведено из ссылки [89])
В каждом цикле измерений затухание ФЛ измерялось после 5-минутного теплового уравновешивания. Никакого теплового гистерезиса не наблюдалось во время циклов нагрева и охлаждения, и результирующее изменение времени жизни фотолюминесценции показано как функция времени на (рис. 5b), демонстрируя, что время жизни фотолюминесценции компакт-дисков демонстрирует превосходную термическую стабильность.
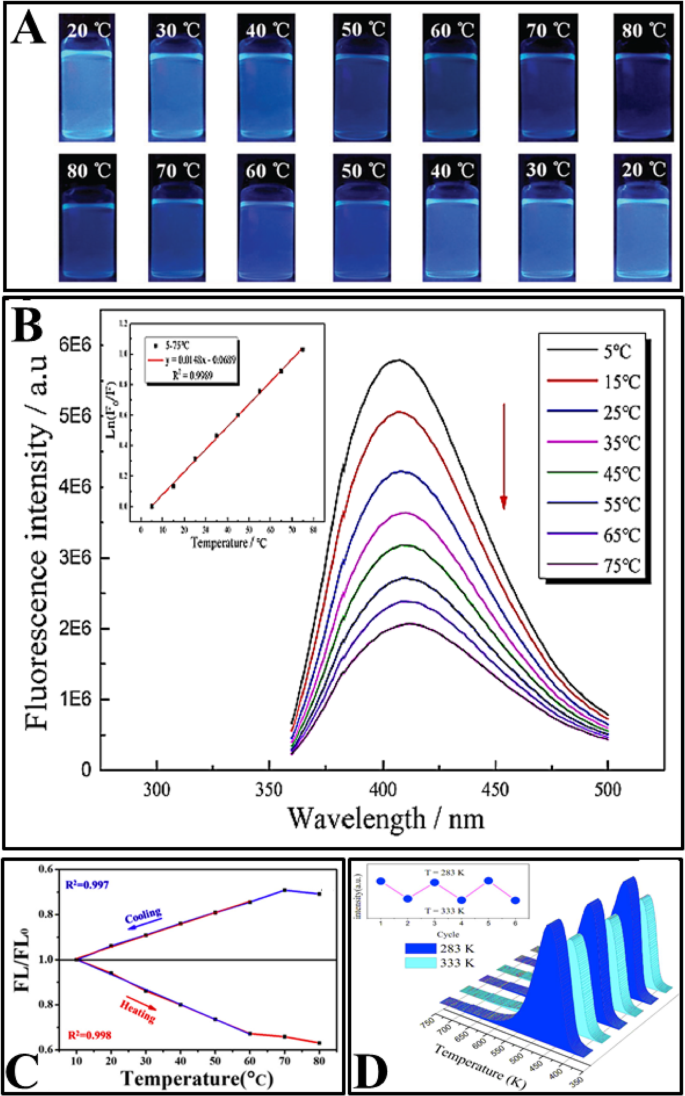
Позже были изготовлены несколько компакт-дисков с температурно-зависимым излучением с использованием различных методов синтеза, таких как гидротермальная и сольвотермическая обработка [2, 77, 92, 95, 97, 98, 99, 100, 101, 102, 103], нагревание с обратным холодильником [94, 96] и лазерная обработка. абляции [14], как показано в Таблице 1. Полученные CD показали линейную температурно-зависимую флуоресценцию в физиологических диапазонах (показанных в Таблице 1). Интенсивность флуоресценции компакт-дисков уменьшалась с повышением температуры. Кроме того, во всех статьях изучалась обратимость и возможность восстановления интенсивности флуоресценции. На рисунке 6 показаны некоторые общие свойства компакт-дисков, изученные в различных статьях.
а Цифровые фотографии N, S-CD при возбуждении УФ-светом (365 нм) при разных температурах в процессе нагрева (вверху) и охлаждения (внизу). (Воспроизведено из ссылки [96]). б Спектры флуоресцентного излучения CD, допированных N, S, измеренные в диапазоне 5–75 ° C (сверху вниз) при возбуждении на длине волны 340 нм, вставка:соответствующая линейная регрессия температуры в зависимости от Ln ( F / F 0 ). (Воспроизведено из ссылки [97]). c FL / FL 0 -температурные графики MnOx-CD в процессах охлаждения и нагрева. (Воспроизведено из ссылки [103]). г Обратимая температурная зависимость ФЛ раствора КД. (Воспроизведено из ссылки [102])
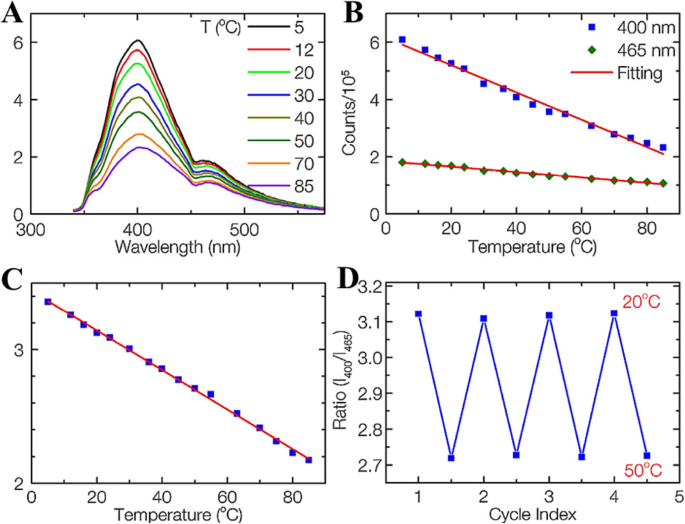
Nguyen et al. [14] синтезировали углеродные точки (КД) с помощью фемтосекундной лазерной абляции графитового порошка в этилендиамине. На поверхности были образованы многочисленные функциональные группы, которые формируют несколько поверхностных состояний на участке поверхности и приводят к множественной эмиссии CD. Они исследовали температурную чувствительность компакт-дисков, зависящую от флуоресценции, используя стационарные спектры флуоресценции. Температурно-зависимые спектры излучения компакт-дисков при возбуждении 320 нм показаны на рис. 7а. Обе интенсивности флуоресценции пиков 400 и 465 нм постепенно уменьшаются с повышением температуры из-за термической активации путей безызлучательного распада. Интенсивность пиков изменяется линейно с температурой в диапазоне от 5 до 85 ° C (рис. 7b). Температурно-чувствительные компакт-диски показали изменение интенсивности флуоресценции на 3,3 и 2,1% на ° C для пиков 400 и 465 нм соответственно. Это указывает на то, что компакт-диски можно использовать в качестве обычного датчика температуры на основе интенсивности с высокой чувствительностью.
а Спектры излучения компакт-дисков записаны при температуре от 5 до 85 ° C при возбуждении на длине волны 320 нм. б Интенсивность флуоресценции пиков 400 и 465 нм в зависимости от температуры. c Отношение пиков 400 нм к 465 нм в зависимости от температуры. г Исследование температурной обратимости компакт-дисков между 20 и 50 ° C. (Воспроизведено из ссылки [14])
Примечательно, что уникальное свойство мультиэмиссии делает компакт-диски перспективными флуорофорами для ратиометрических флуоресцентных датчиков температуры. Отношение двух интенсивностей флуоресценции при 400 и 465 нм (возбуждение 320 нм) в зависимости от температуры показано на рис. 5c. Между коэффициентом интенсивности и температурой существует очень хорошая линейная зависимость в широком диапазоне температур от 5 до 85 ° C ( R
2
=0,998). Thermal linearity is advantageous since it makes the correlation between the peak-intensity ratio and temperature straightforward and meanwhile provides a constant thermal sensitivity along with the entire dynamic range. The temperature-sensitivity of CDs is determined to be 1.48% °C
−1
, which is comparable with that of other materials. It should be noted that the temperature response range of CDs is much wider than those of other reports on dual-emission temperature sensors and covers both the physiological temperature for biology studies and the working temperature for many electronic devices. Besides 320 nm excitation, the CDs also work at other excitation wavelengths, such as 340 and 365 nm, with the same sensitivity. Thus, the CDs can be utilized for temperature sensing in many practical applications by selected different working wavelengths.
They have shown that the ratiometric temperature sensor was reversible between 20 and 50 °C, four cycles and photostable (when the intensity of the power source changed) as shown in Fig. 7d. This result suggests that the CDs sensing system is stable and robust with any changes in sample concentration, excitation, or detection efficiency.
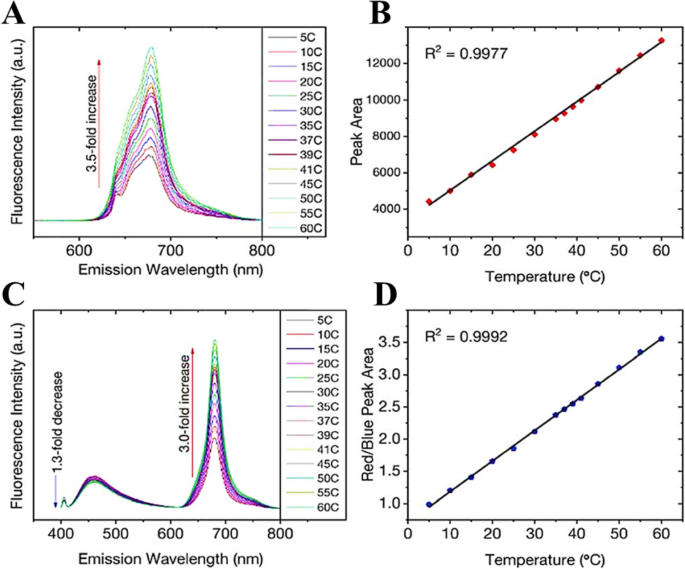
Increasing temperature is not always accompanied by PL quenching; however, it could show enhancement of the PL as well. Macairan et al. [29] showed the PL enhancement of dual-fluorescent carbon dots with increasing temperature. They prepared biocompatible dual-fluorescing carbon dots CDs in a one-step microwave assisted-reaction using formamide and glutathione. They found that following excitation at 640 nm, the fluorescence intensity and PL integrated area increase over the range of 5–60 C by a factor of 3.5 observed over the entire analysis range and the temperature (Fig. 8a). As shown in Fig. 8b, a linear response (R
2
=0.999) is observed over the entire analysis range and the temperature sensitivity was determined to be as high as 3.71% C
−1
.
а Excitation at 640 nm yields a 3.5-fold increase in fluorescence intensity and the corresponding integrated area is plotted in b showing a linear response over the range of 5–60 °C. c Changes in the fluorescence spectra of the CDs (λex =405 nm) as a function of temperature over the entire range. A 1.3-fold decrease is noted for the blue fluorescence in contrast to the 3-fold increase for the red counterpart. г The ratio of the integrated areas of the red and blue fluorescence components are plotted as a function of temperature showing a linear increase over the entire temperature range. (Reproduced from reference [29])
The temperature-dependent fluorescence was also studied following excitation at 405 nm. Interestingly, the blue and red fluorescence bands are not equally sensitive to the change in temperature. With increasing temperature, the fluorescence intensity (and the corresponding integrated area under the curve) of the blue component shows a very slight decrease in contrast to the red component, which significantly increases (Fig. 8c). These observations are noted over the range of 5–60 °C where the blue emission decreases by a factor of 1.3 in contrast to the red emission, which increases by a factor of 3.0.
As shown in Fig. 8d, the ratio of red to blue fluorescence increases with temperature, and a highly linear response is triplicate on 3 unique samples and the linear plot reflects the observed with an R
2
=0.998. These analyses were repeated in an average of these measurements, which have small deviations at each temperature. The thermal sensitivity of the CDs, over the entire temperature range, varied from 1.33 to 4.81% °C
−1
, which is an improvement over previously reported carbon dot nano-thermometry systems and other dual-emitting nanomaterials such as quantum dots and metal-organic frameworks-dye composites. The thermal resolution of the CDs was calculated to be 0.048 K
−1
indicating that it is indeed possible to measure small thermal changes.
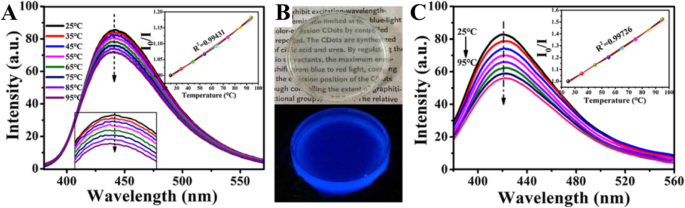
Zhang et al. [98] synthesized CDs that have temperature-responsive characteristics in the range of 25–95 °C, and they have excellent sensitivity and remarkable reversibility/recoverability (Fig. 9a). CD/epoxy composites were further prepared by uniformly doping CDs into an epoxy resin. First, 5 μg of the CDs were dissolved in 50 μL of triethylenetetramine (TETA). Then, 350 μL epoxy resin was added to the mixed solution and fully mixed by high-speed stirring. The resulting composite showed significantly enhanced temperature response.
а Temperature dependence of the CD emission. б CD/epoxy composites. c Temperature dependence of the emission of the CD/epoxy composites. (Reproduced from reference [98])
Epoxy resin is a common thermosetting resin and is widely used to package LED chips. Figure 9b shows optical micrographs of CD/epoxy composite discs of approximately 2 cm in diameter and 8–10 mm in thickness. The cured CD/epoxy composites are transparent, and their fluorescence emission spectra are shown in Fig. 9c. The emission peak of the CD/epoxy composite is blue-shifted by approximately 10 nm compared to that of the CDs’ solution. Notably, the temperature response of the composite is significantly improved. In the temperature range of 25–95 °C, the fluorescence intensity decreases by 35% with increasing temperature, which is more than twice that of the solution state, and the linear results are more stable. The linear equation satisfies I 0 / Я =0.0074 [°C] + 0.80454 (R
2
=0.99724), where I 0 и я are the fluorescence intensity of the CD/epoxy composite before and after the temperature rise, and the excitation wavelength is 360 nm. The blue shift of the emission peak and the enhancement of the temperature response characteristics may be due to changes in the dielectric constant of the environment in which the CDs are located. The composite has a wide temperature detection range, and its excellent sensitivity and stability make it suitable for use as a temperature sensor based on a fluorescent nanomaterial in a variety of environments.
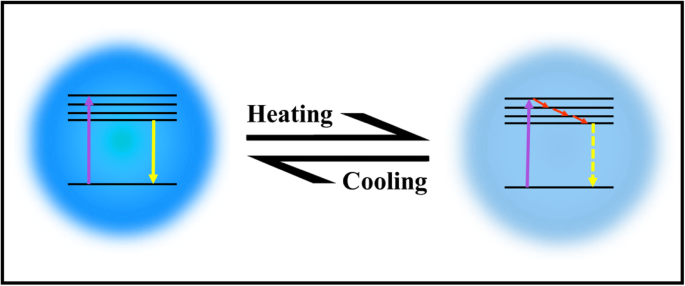
Up to now, there is no well-established mechanism for explaining the thermo-sensing behavior of carbon dots. Some reports attribute the mechanism to the thermal activation of non-radiative channels of surface (trap/defect) states. The general picture is that the non-radiative channels were not activated at low temperatures, so the excited electrons could emit photons radiatively. On the contrary, as the temperature increases, more non-radiative channels became activated, and excited electrons got back to the ground state by non-radiative processes, leading to the decreasing fluorescence intensity [2, 95, 99, 100, 103]. The mechanism of CDs emissions with heating/cooling is shown in Fig. 10.
Schematic illustration of CDs responding to temperature changes
To better understand the thermodynamics of the CD emission processes, Kalytchuk et al. [89] correlated the radiative (\( {\tau}_r^{-1} \)) and nonradiative ( \( {\tau}_{nr}^{-1} \)) recombination rates of a CD sample with its PL quantum yield. The radiative rate is determined from the PL quantum yield (QY) and the measured recombination rate τ
−1
as \( {\tau}_r^{-1} \) =QY × τ
−1
. The nonradiative relaxation rate \( {\tau}_{nr}^{-1} \) is expressed as \( {\tau}_{nr}^{-1} \) =τ
−1
- \( {\tau}_r^{-1} \). The PL QY of CDs at various temperatures was calculated from their temperature-dependent absorption and integrated PL intensity together with the PL QY determined at room temperature. Both radiative and nonradiative recombination rates derived from time-resolved PL measurement data are plotted as functions of temperature in Fig. 11. The radiative recombination rate is greater than the correspondent nonradiative rate up to 70 °C and does not vary appreciably at temperatures between 2 and 80 °C, remaining in the range of (0.74–0.82) × 10
6
s
−1
. In contrast, there is a pronounced (almost 7-fold, from 0.16 × 10
6
to 1.12 × 10
6
s
−1
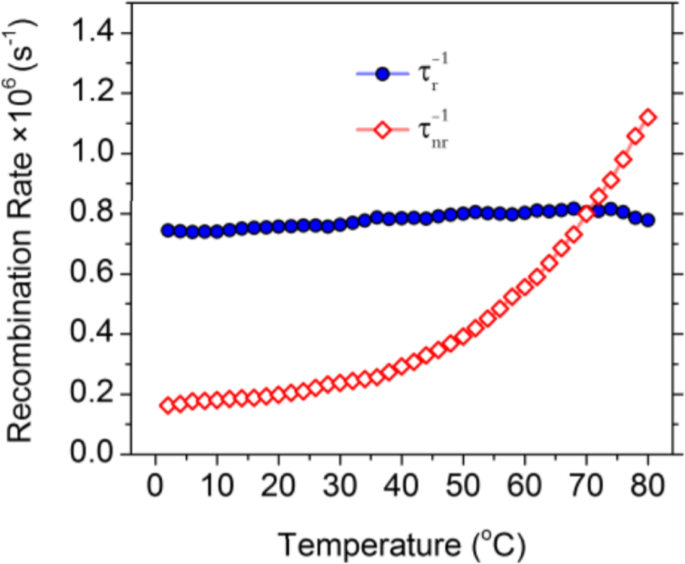
) monotonic increase in the rate of nonradiative recombination by increasing the temperature from 2 to 80 °C. Temperature-dependent crossover of the radiative and nonradiative rates occurs at 70 °C, at which temperature the PL QY is 50%. These results suggest that the temperature activation of PL quenching in their CDs is primarily caused by the activation of nonradiative relaxation channels [89].
Radiative (solid symbols, blue color) and nonradiative (hollow symbols, red color) recombination rates for CDs plotted against the temperature for temperatures of 2–80 °C. (Reproduced from supporting information of reference [89])
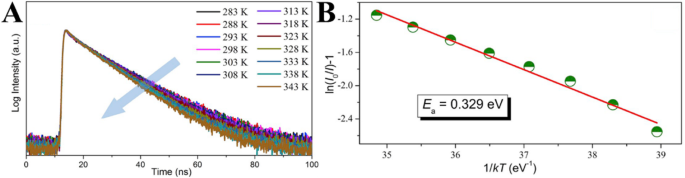
Guo et al. [102] ascribed the thermal-quenching of their prepared carbon dots not just to activation of the nonradiative decay process, but also to the occurrence of nonradiative trapping with increasing temperature. They measured the temperature-dependent decay lifetimes of the CDs and shown in Fig. 12a. The data were collected by monitoring emission maximum as a function of the temperature under the 320 nm laser excitation. The result shows that the PL lifetime drops from 15.03 to 11.70 ns with the temperature increasing from 283 to 343 K, which could be ascribed to the occurrence of nonradiative decay processes. Besides, the PL relaxation dynamics of the CDs reveal multi-exponential decay with temperature increasing, which suggests the photoexcited carriers following the complicated relaxation processes. The occurrence of non-radiative trapping will be increased with rising temperature, and this could be quantitatively analyzed by the Arrhenius plot of the integrated PL intensities as:
Temperature-dependent decay curves of CDs solution (a , λex =350 nm, λem =450 nm); the dependence of ln[(I 0 / Я T )-1] on 1/kT CDs solution (b ). (Reproduced from reference [102])
где E а is the activation energy, k is the Boltzmann constant, and a является константой. Figure 12a displays the plotting of the emission intensity with respect to 1/T , where the value of activation energy (E а ) is calculated to be 0.329 ± 0.02 eV. In order to probe the reason for thermal quenching of CDs emission process, the radiative (V r ) and nonradiative (V nr ) recombination rates of CDs were determined from the lifetime (τ*) and quantum yield (QY) as:
The QY of CDs at various temperatures was calculated from their temperature-dependent absorption and integrated PL intensity with the QY determined at room temperature. They have noticed that the radiative rates have a slight decline when the temperature rises from 283 to 343 K; at the same time, the nonradiative recombination rates have gradually increased by about 2-fold. These results further indicate that the temperature-activated PL quenching in CDs is mainly due to the activation of nonradiative relaxation channels [102].
Other groups used microscopic and spectroscopic techniques to understand the mechanism of thermos-sensing of carbon dots.
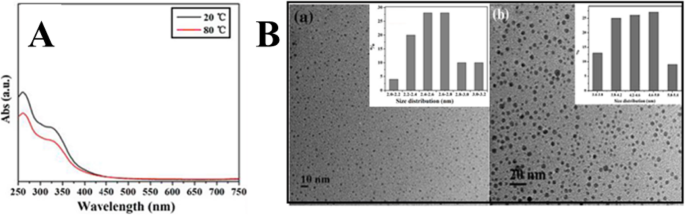
Wang at el. used TEM and UV–Vis spectra to study the temperature-responsive PL behavior of prepared CDs. As shown in Fig. 13a, the CDs display no change in the UV–Vis spectra upon increasing the temperature from 20 to 80 °C. However, it was found that the average diameter of CDs increased from 2.6 ± 0.2 nm at room temperature to 4.4 ± 0.2 nm at 80 °C (Fig. 13b). Thus, increasing the temperature, the aggregation of as-prepared CDs occurred which caused the obvious fluorescence quenching [1].
а UV–Vis absorption spectra of CDs in aqueous solution under 20 and 80 °C. б the TEM image of CDs in aqueous solution (a ) at room temperature, the average size was 2.6 ± 0.2 nm (b ) at 80 °C, and the size increased up to 4.4 ± 0.2 nm. (Reproduced from reference [1])
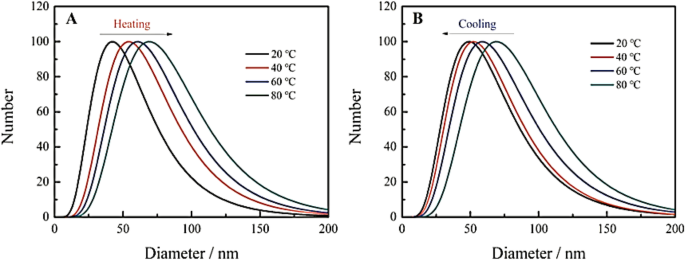
He et al. [101] reported that the hydration particle size of their CDs emerges as larger with the increase in the temperature (Fig. 14a), which indicates that the temperature rise gives rise to the aggregation of the CDs, eventually results in the fluorescence quenching. Nonetheless, with the decline in the temperature, the hydration particle size of CDs starts declining (Fig. 14b), which indicates that the cooling has the potential of causing CDs to depolymerize [101].
Change of hydrated particle size of carbon dots during heating (a ) and cooling (b ). (Reproduced from reference [101])
Another group such as Cui et al. also attributed the fluorescence quenching to the aggregation of CDs. They also tried to apply the undoped CDs synthesized using only acrylic acid as a precursor in temperature sensors. Unfortunately, undoped CDs possessed weaker quenching effects under the same temperature elevation than doped CDs [92].
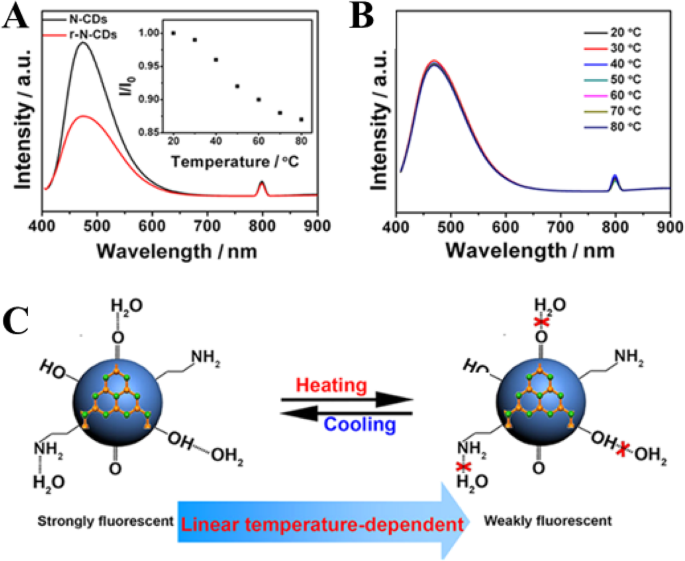
Ян и др. [94] in their work proposed two key factors concerning the temperature-dependent PL property of the N-CDs, including (i) surface functional groups and (ii) hydrogen-bonding interaction. To examine the effect of the first factor, the surface O-containing groups, another control experiment was conducted by treating N-CDs (4.0 mL) with a strong reducing agent NaBH4 (1.0 mL, 0.1 mol L
−1
) to remove C=O species on carbon dots surface. The obtained reduced N-CDs are denoted as r-N-CDs for brevity. Compared with N-CDs, the r-N-CDs exhibit weaker fluorescence intensity (Fig. 15a). Besides, the fluorescence intensity of r-N-CDs only decreases by 13% with temperature increasing from 20 to 80 °C (the inset in Fig. 15a) that gives a much lower temperature sensitivity, which is ascribed to the decreased O-containing groups [94].
а PL spectra (excitation wavelength, 400 nm) of N-CDs (black trace) and r-N-CDs (red trace). The inset shows I / Я 0 −T of reduced N-CDs. б PL spectra (excitation wavelength, 400 nm) of N-CDs dispersed in C2 H 5 OH at various temperatures. c A schematic mechanism for the temperature-dependent fluorescence intensity of N-CDs. (Reproduced from reference [94])
The second factor, the effect of hydrogen bonding with the solvent on fluorescent behavior of N-CDs was explored. N-CDs solution (1.0 mL) was dropped on a filter paper and left to dry in the air to obtain a solid sample, which still emits bright fluorescence. However, no obvious change of fluorescence intensity of the solid N-CDs with temperature increase was observed. They also measured the fluorescence of N-CDs dispersed in ethanol. The fluorescence intensity of N-CDs in C2 H 5 OH is lower than that in water and little variation of the PL intensity is observed with temperature increasing from 20 to 80 °C (Fig. 15b). Hence, the strong hydrogen bonds play a key role in the temperature-dependent PL property of the N-CDs. Figure 15c is a schematic mechanism for the temperature-dependent fluorescence intensity of N-CDs [94].
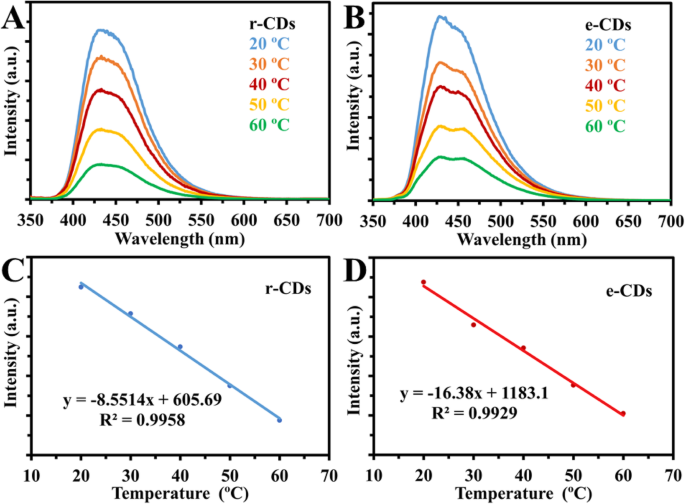
However, our group used the same experimental strategy as Yang group; in both cases, the r-CDs and e-CDs emissions were quenched linearly with increasing temperature, in the same way as the original results of their CDs (Fig. 16). Thus, our results ruled out the synergistic effects of abundant oxygen-containing functional groups and hydrogen bonds [77].
а , b Fluorescence spectra of reduced CDs (r-CDs) and CDs in ethanol (e-CDs) at temperatures (20 to 60 °C). c , d Linear correlation between fluorescence intensity and temperature (°C) for r-CDs and e-CDs respectively. (Reproduced from the supplementary information of reference [77])
In literature, only a few articles explored the temperature-responsive fluorescent properties of CDs in biological imaging. Prior to such experimentations, in vitro cytotoxicity analysis is crucial for CDs because they make it possible to estimate the CD’s toxicity in living subjects. In vitro cytotoxicity analysis evaluates the effect or influence of the nanomaterial on cultured cells [89].
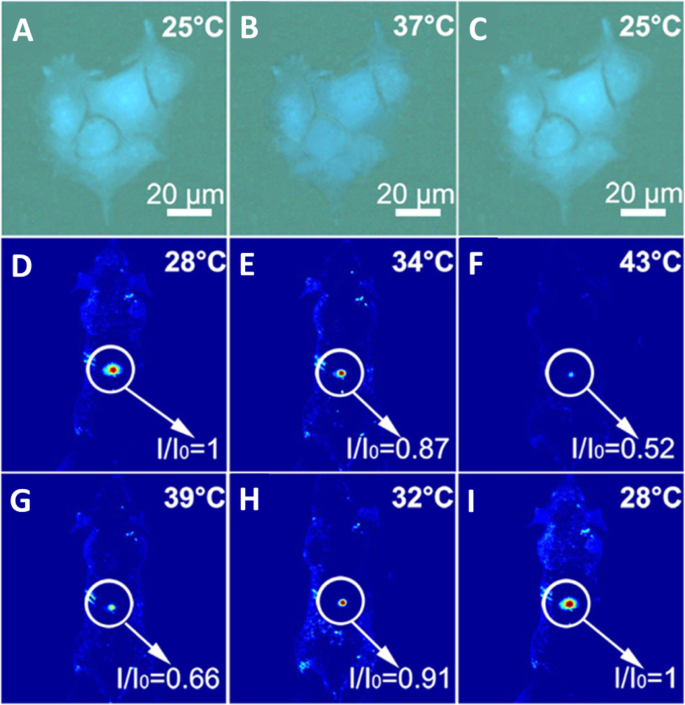
Ян и др. [94] verified that the CDs could be used as an effective thermometer in living cells; HeLa cells were washed with PBS after treatment with CDs for 6 h. Bright-blue fluorescence of the CDs in HeLa cells is observed when the temperature is 25 °C as shown in Fig. 17a. With the temperature increasing to 37 °C, the blue fluorescence becomes weaker (Fig. 17b), the fluorescence of N-CDs is recovered when the temperature was decreased to 25 °C (Fig. 17c). As a thermos-imaging in vivo, the fluorescent images of mice were collected immediately after being injected with N-CDs at different temperatures. By setting the fluorescence intensity at 28 °C as the reference (I o ), Я / Я o of the area where CDs were injected varies from 1.0 to 0.87 with the increase of temperature from 28 to 34 °C (Fig. 17d, e). With temperature further increasing to 43 °C, I / Я o declines to 0.52 and the fluorescence becomes nearly undetectable (Fig. 17f). And I / Я o can be reversibly enhanced back from 0.66 to 1.0 with the temperature decreases from 39 to 28 °C (Fig. 17g–i). All of these results indicated that N-CD could be used as an effective in vitro and in vivo nanothermometer [94].
a–c Fluorescent images of a single Hela cell at 25, 37, and 25 °C after treatment with N-CDs, respectively. г - е Fluorescent photographs of a mouse given an injection of N-CDs at increasing temperatures. г - я Fluorescent photographs of a mouse given an injection of N-CDs at decreasing temperatures. ( Reproduced from reference [94])
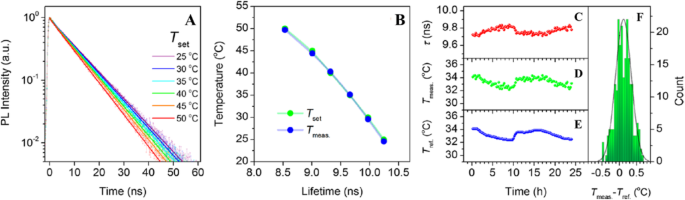
In an exploratory experiment, Kalytchuk et al. tested the capacity of CDs for intracellular temperature monitoring in human cervical cancer HeLa cells. Figure 18 shows the measured intracellular temperatures of HeLa cells incubated with CDs (500 μg/mL). The CDs’ PL decay curves at each temperature were highly reproducible and could be fitted with a single-exponential function at all recorded temperatures. In Fig. 18a, the recorded PL decay curves for temperatures between 25 and 50 °C (with a step size of 5 °C) are indicated by symbols, while the corresponding single-exponential fits are represented by solid lines. They were able to confirm that the PL signal in these PL lifetime measurements was derived exclusively from the CDs for the CD concentration of ≥ 100 μg/mL. The intracellular temperature in each measurement was determined from the calibration curve between PL lifetimes as the temperature increases from 2 to 80 °C. The temperatures determined in this way (T meas ) are plotted as functions of the PL lifetime in Fig. 18b. Independently, the temperature of the cell solution was determined using a calibrated reference thermometer (shown in Fig. 18b as Tset ). The temperatures reported by the luminescent CD probe and the reference detector are in good agreement. These results show that the PL lifetime of nanoprobes based on CDs can be reliably used to measure intracellular temperatures [89].
In vitro intracellular PL lifetime thermal sensing using CDs. а PL emission decays of HeLa cells incubated with CDs (500 μg/mL) at different temperatures (T set ). б Temperatures determined using the calibration (T meas ) and set temperatures (T set ) plotted against the PL lifetime. c - е Applicability of CDs for long-term remote intracellular temperature monitoring. c PL lifetimes extracted from PL transients recorded every 15 min for 24 h of HeLa cells incubated with CDs (500 μg/mL). г Temperatures determined using the calibration curve. е Temperatures measured with a reference thermometer (T ref ). е Histogram showing the distribution of temperature differences between the obtained and reference temperatures; the solid line is the distribution curve. (Reproduced from reference [89])
To further evaluate the potential of luminescent CD nanoprobes for long-term real-time temperature monitoring, PL decay profiles of HeLa cells incubated with CDs (500 μg/mL) every 15 min for 24 h were recorded. The PL lifetimes extracted from the measured PL decay values during this period were then plotted as functions of time, as shown in Fig. 18c. Using these results, the temperature variation over time was calculated using the calibration curve, as shown in Fig. 18d. In addition, the sample’s temperature at each measurement point was determined using a reference thermometer with a temperature reproducibility of 60 mK. The temperature determined with the reference thermometer is plotted in Fig. 18e, which shows that there was excellent agreement between the measured and reference temperatures. The high accuracy of the PL-based temperature measurements is further demonstrated by statistical analysis of the differences between the measured and real (reference) temperatures (Fig. 18f). Using these data, the absolute average accuracy of temperature detection by the presented method was calculated to be 0.27 °C. This experiment confirms the potential of CD-based thermal probes in biological systems [89].
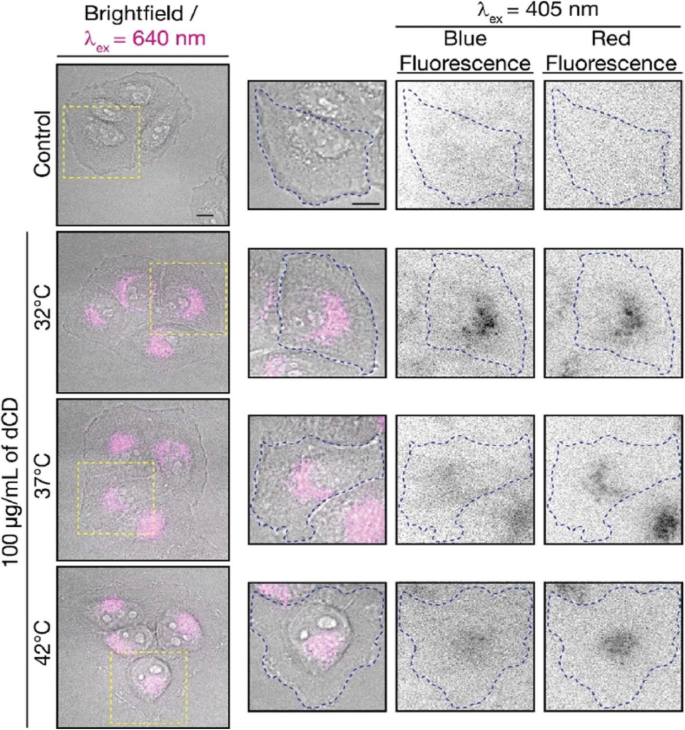
Macairan et al. [29] displayed that the prepared CDs can be used for thermal sensing inside cells using intensity and ratiometric approaches. HeLa cells treated with CDs were allowed to equilibrate at 32, 37, and 42 °C (Fig. 19). Excitation at 640 nm was used to selectively monitor the red fluorescence of the CDs in the cells. The thermal changes could be due to changes in intracellular concentration or not correlate with a change in intensity (λex + 640 nm). This could be due to changes in intracellular concentration or localization of the CDs at higher temperatures. Thus, simply relying on changes in fluorescence intensity leads to accurate intracellular thermal sensing.
Fluorescence microscopy images of CD-treated HeLa cells. Fluorescence signals from the CDs (λex =640 nm; left and 405 nm; right) fluorescence ratios are 1.8 at 32 °C, 2.0 at 37 °C, and 2.3 at 42 °C. The control shows untreated HeLa cells at 42 °C with no fluorescence signal as expected. (Reproduced from reference [29])
In contrast, these limitations are excluded using the ratiometric approach. The CDs maintain dual blue and red fluorescence in cells following excitation at 405 nm, as previously observed for the colloidal dispersions (Fig. 19). The red-to-blue ratio increases with increasing temperature, with values of 1.8 at 32 °C, 2.0 at 37 °C, and 2.3 at 42 °C. The ratiometric relationship of the red-to-blue fluorescence of the CDs highlights the advantage of ratiometric temperature sensing in the development of fluorescent nano-thermometry probes. The relative red-to-blue emission ratio remains unaffected, regardless of the amount of CDs taken up by the cells, which can be affected by various factors such as confluency and is not concentration-dependent. Lastly, the CDs have shown fluorescence reversibility with respect to changes in intracellular temperature. Following incubation in HeLa cells, they were subjected to a heating/cooling cycle from 32/42/32 °C. This emphasizes the robustness of the proposed CD-nanothermometer and these findings further demonstrate the fluorescence reversibility [29].
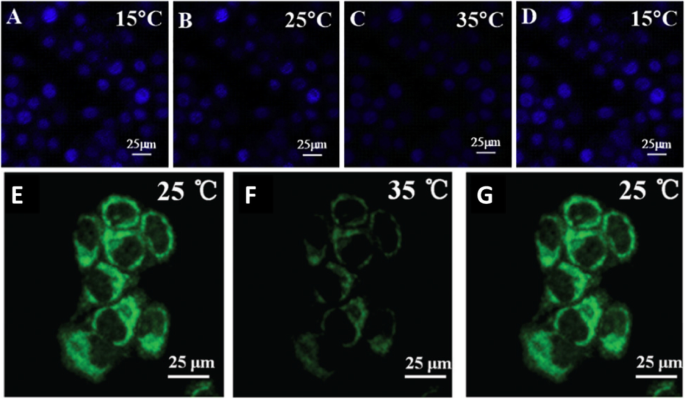
Confocal laser scanning microscopy was used to thermal image colon cancer cell HT-29 using N, S, and I-doped CDs, as shown in Fig. 20 [100]. The fluorescent spots were temperature-dependent as shown in Fig. 20g–i, as the most intense is at 15 °C, while the weakest point was at 35 °C. Interestingly, the fluorescence spots were reversible, and the spots were very photostable after 20 min of continuous excitation [100]. Shin et al. [96] also used confocal laser scanning microscopy for Hela cells, shown in Fig. 20e–g.
a–d Are confocal microscopy images of N, S, I-CDs-colon cancer cell HT-29 with corresponding fluorescence field at 15, 25, 35, and 15 °C, respectively. (Reproduced from reference [100]). е - г Confocal microscopy images of N, S-CDs-stained cells with corresponding fluorescence field at 25, 35, and 25 1C, respectively. (Reproduced from reference [96])
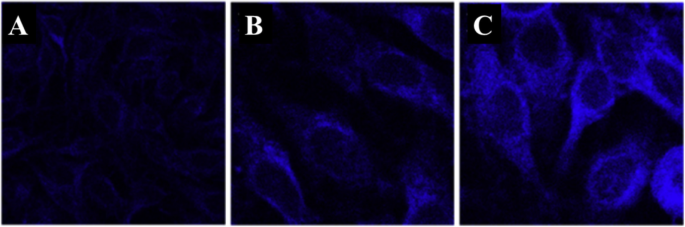
Ли и др. 103 prepared a nanocomposite composed of MnOx-CDs to be used as a nano thermos responsive fluorophore for biological environments. HepG2 cells were incubated with MnOx-CDs at different culture temperatures. As illustrated by confocal laser scanning microscopy (excited at 405 nm), the blue luminescence of the MnOx-CDs in the HepG2 cells is weak when the environmental temperature was 40 °C (Fig. 21a), and the blue luminescence of the MnOx-CDs in HepG2 cells enhances as the temperature decreased to 30 °C (Fig. 21b) even to 20 °C (Fig. 21c). Due to the temperature-responsive properties, the as-synthesized MnOx-CDs can be readily applied in the biomedical fields like bioimaging and photothermal therapy in cancer treatment [103].
Confocal laser scanning microscopy images (excited at 405 nm) of MnOx-CDs in HepG2 cells at 40 °C (a ), at 30 °C (b ), and 20 °C (c ). (Reproduced from reference [103])
Carbon nanodots exhibit unique properties to be exploited for nanothermometry, such as thermal-sensitivity, low-cost, and photostability. Flexible surface modification and facile preparation will pave the way to establish an enormous number of thermal sensitive nanomaterials for a variety of applications. The overall trends in thermo-sensing nanomaterials are aimed at enhancing photostability and thermal-resolution with using low-cost and safe materials. CDs can be classified as a new generation of thermometer that can fulfill these requirements and can be used for biomedical thermometry applications, such as temperature monitoring during hyperthermia treatment. Facile-preparation protocols, biocompatibility, and easy functionalization of CDs are promising criteria which make the CDs alternative next-generation nanothermometer materials. More efforts are required to promote basic research in this field. Limitations should be overcome to produce carbon dot-based nanothermometers comprising enhancing thermal sensitivity, and working in a broader range of temperature. A better understanding of the fluorescence thermal-sensing mechanism is another key issue to be able to design and manipulate the structure of CDs and enhance thermal resolution. More experiments and theoretical modeling are necessary to understand the correlation between the methods of fabrication of CDs with their thermal behavior. Введение
Нанотермометрия
Углеродные точки как нанотермометры
Mechanism of Thermo-sensing
Bioimaging in Living Cells (Thermal Imaging)
Conclusions and Future Perspective
Наноматериалы
- Исследование Массачусетского технологического института для установления нового стандарта оценки жизненно…
- Новый диапазон противовирусных технологий для различных материалов
- Материалы:новый самосклеивающийся LSR для литья под давлением на ПК, PBT
- Материалы:советы по отжигу аморфных полимеров, часть 2
- Материалы части 3:советы по отжигу полукристаллических полимеров
- Материалы:полипропилен, армированный стеклом и углеродным волокном, для автомобилей
- DARPA работает над материалами следующего поколения для гиперзвуковых транспортных средств
- Новые кристаллы для технологий отображения следующего поколения
- Trelleborg объявляет о новом дистрибьюторе инструментальных материалов
- Новые материалы Solvay, процессы, разработанные для индустриализации



