Целевой ген, подавляющий синергетический фототермический эффект BRAF, подавляет рост клеток гепатомы с использованием новой наносистемы GAL-GNR-siBRAF
Аннотация
Рак печени - одно из самых распространенных злокачественных новообразований во всем мире. Ингибиторы киназы RAF эффективны при лечении гепатоцеллюлярной карциномы (HCC); следовательно, ингибирование пути BRAF / MEK / ERK стало новой терапевтической стратегией для новой терапии HCC. Однако системы адресной специфической доставки для опухолей по-прежнему являются серьезным препятствием для клинического применения. Галактоза (GAL) может нацеливаться на рецептор асиалогликопротеина (ASGPR), который высоко экспрессируется на раковых клетках печени. В этом исследовании мы разработали новый многофункциональный наноматериал GAL-GNR-siBRAF, который состоит из трех частей:GAL как нацеленный на рак печени фрагмент, золотые наностержни (GNR), обеспечивающие фототермические свойства в ближнем инфракрасном свете, и siRNA, специфически подавляющие BRAF (siBRAF). ). Наноноситель GAL-GNR-siBRAF показал высокую нагрузочную способность миРНК и ингибировал деградацию миРНК в сыворотке. По сравнению с голыми золотыми наностержнями GAL-GNR-siBRAF обладал более низкой биотоксичностью и более высокой эффективностью подавления генов. Обработка GAL-GNR-siBRAF значительно подавляла экспрессию BRAF и нарушала пролиферацию, миграцию и инвазию клеток рака печени. Более того, комбинаторные фототермические эффекты и нокдаун BRAF под действием GAL-GNR-siBRAF эффективно вызывают гибель опухолевых клеток. Поэтому в нашем исследовании был разработан новый тип целевого многофункционального наноматериала GAL-GNR-siBRAF для лечения рака печени, который дает идеи для разработки новых клинических методов лечения.
Введение
Гепатоцеллюлярная карцинома (ГЦК) - серьезная глобальная проблема здравоохранения [1]. Это шестой по распространенности рак в мире и третье место среди причин смерти от рака [2, 3]. Большинство случаев ГЦК происходит в Восточной Азии и странах Африки к югу от Сахары. Однако заболеваемость растет в некоторых развитых странах, включая Францию, Великобританию, Японию и США [4]. Стандартным лечением раннего ГЦК является хирургическое удаление опухоли. После операции 5-летняя выживаемость может составлять от 89 до 93% [5]. К сожалению, лишь небольшой процент пациентов с ГЦК (около 20–30%) диагностируется на ранней стадии; большинство пациентов с ГЦК (> 70%) обнаруживаются на поздних стадиях и не могут подвергнуться хирургической резекции. Другие варианты лечения включают трансплантацию печени, транскатетерную химиоэмболизацию артерий (ТАХЭ) и системную химиотерапию [6]. Однако трансплантация печени ограничена поставками, а неполная эмболизация ТАСЕ может привести к неэффективности лечения со значительными побочными эффектами системной химиотерапии и плохим общим прогнозом. Поэтому новые методы лечения гепатоцеллюлярной карциномы крайне требовательны с клинической точки зрения [7].
Путь передачи сигналов RAS / RAF играет важную роль в развитии рака печени, а BRAF является одним из основных генов, связанных с раком, в этом пути. Генетические изменения в этих генах часто приводят к двум каскадным нарушениям. Аномальная активация сигнального пути RAS / RAF связана с плохим прогнозом у онкологических больных [8]. BRAF является наиболее часто мутируемым геном в семействе RAF, и нацеливание на путь RAS / RAF является новой терапевтической стратегией для лечения HCC [8,9,10]. Поскольку было показано, что ингибитор киназы RAF сорафениб полезен при лечении HCC, мутации BRAF стали предпочтительной мишенью для терапии HCC [8]. Более конкретно, мутации BRAF стали желательной мишенью для лечения запущенной HCC, поскольку клиническая разработка сорафениба, ингибитора киназы RAF, была обнаружена для лечения HCC в Азии, Европе и США [11]. По сравнению с плацебо сорафениб увеличивал общую выживаемость, продлевая медианную общую выживаемость пациентов с распространенным ГЦК [12,13,14]. Однако сорафениб обладает плохой способностью воздействовать на опухоли, что может приводить к побочным эффектам, таким как высокое кровяное давление, выпадение волос и тошнота [15]. Лекарства, которые нацелены на рак печени с высокой специфичностью и блокируют RAF, требуют дальнейшего изучения.
Рецептор асиалогликопротеина (ASGPR), также известный как рецептор галактозы печени, представляет собой лектин С-типа, экспрессируемый на синусоидальной поверхности гепатоцитов [16]. ASGPR считается важной мишенью для наноструктур печени, поскольку он играет важную роль в связывании, интернализации и удалении веществ с концевыми остатками галактозы [17]. Сообщалось, что некоторые моносахариды (галактоза, манноза, лактоза, N-ацетилгалактозамин и сиаловая кислота) в разной степени взаимодействуют с ASGPR, а галактоза проявляет более высокое сродство к ASGPR [18]. Поскольку ASGPR сильно экспонируется на поверхности паренхимных клеток печени [19], рецептор имеет сильное сродство к галактозе и галактозилированным пролекарствам или системам доставки, нацеленным на печень. Наночастицы галактозы [20], мицеллы галактозы [21] и липосомы галактозы [22] были идентифицированы как системы лекарственных препаратов, нацеленных на печень, которые нацелены конкретно на гепатоцеллюлярные карциноидные клетки.
Золотые наностержни (ЗНП) представляют собой стержневые наночастицы золота, которые обладают значительными преимуществами в качестве наноносителей [23]. Золотые наностержни (GNR) обладают превосходной биосовместимостью и могут использоваться для стабильной доставки миРНК [24]; они имеют большую удельную поверхность, что позволяет гибко модифицировать специфические адаптеры, нацеленные на опухоль [25]; Локализованный поверхностный плазмонный резонанс (LSPR) имеет высокую эффективность фототермического преобразования при облучении светом в ближней инфракрасной области и стал отличным фототермическим противоопухолевым материалом [26]. Максимальная фототермическая эффективность может быть достигнута путем регулировки соотношения сторон золотых наностержней (GNR). Токсичность наночастиц золота in vitro и in vivo зависит от их размера, поверхностного заряда и покрытия поверхности [27]. Однако бромид цетилтриметиламмония (CTAB) является важным активным агентом в синтезе золотых наностержней, который обладает очевидной цитотоксичностью и ограничивает биологические применения [28].
РНК-интерференция (РНКи) стала многообещающим подходом к лечению рака, поскольку она эффективно нокаутирует или заглушает гены-мишени с помощью малой интерферирующей РНК (миРНК) [29]. Недавно молекулы миРНК вошли в фазу испытаний на людях и считаются многообещающими способами лечения рака и опухолей с множественными мутантными генами [30]. Однако применение siRNA по-прежнему сталкивается с огромными проблемами, такими как нестабильность сыворотки (деградация под действием нуклеаз во внеклеточной среде) и нецелевые эффекты [31]. Более того, миРНК заряжены отрицательно, что не позволяет им связываться с отрицательно заряженными клеточными мембранами [32]. Из-за этих характеристик маловероятно, что сама миРНК будет доставлена непосредственно в клетки. Стабильность миРНК может быть улучшена химической модификацией миРНК или вставкой загрузчиков миРНК в материалы защитного носителя [33].
В этом исследовании мы недавно сконструировали многофункциональный наноноситель GAL-GNR-siBRAF. В системе используются золотые наностержни с оптической способностью генерировать тепло в качестве внутреннего ядра и внешне модифицированный GAL (d-галактоза) со специфической нацеленностью на опухоли печени. Эта система снижает биологическую токсичность CTAB на поверхности золотых наностержней и демонстрирует высокую нагрузочную способность siRNA и может быть использована для эффективного подавления гена BRAF при раке печени. Применение GAL-GNR-siBRAF значительно ослабило пролиферацию, инвазию и миграцию раковых клеток печени. Кроме того, GAL-GNR-siBRAF одновременно индуцировал сайленсинг генов BRAF и фототермические эффекты, которые обеспечивали синергетический эффект в отношении способности уничтожать опухолевые клетки, обеспечивая новый образ мышления для разработки клинического лечения рака печени.
Материалы и методы
Мобильная линия
Клеточная линия гепатоцеллюлярной карциномы мыши Hepa1-6 была приобретена в Банке стволовых клеток Китайской академии наук. Клетки культивировали в среде DMEM (Life Technologies, Карлсбад, Калифорния), содержащей 10% FBS при 37 ° C с 5% CO 2 .
Синтез миРНК BRAF
Последовательность siRNA, нацеленная на ген BRAF, представляет собой 5'-GCUUACUGGAGAGGAGUUACA-3 'и была синтезирована Dharmacon, Inc. (Лафайет, Колорадо, США). Коммерчески доступный целевой ген люциферазы siGL2 использовали в качестве миРНК отрицательного контроля.
Синтез CTAB-GNR
Водорастворимые золотые наностержни были синтезированы с использованием опосредованного семенами пути роста [34]. Затравочный раствор был приготовлен следующим образом:1 мл цетилтриметиламмонийбромида (ЦТАБ) (0,2 М) (Sinopharm) осторожно смешивали с 1 мл HAuCl 4 (0,5 мМ) (Sinopharm). Перемешивали раствор при 28 ° C, тщательно перемешивали и добавляли 0,12 мл холодного NaBH 4 . (0,01 М) (Sinopharm) до тех пор, пока полученный посевной раствор не станет коричневым и не останется в резерве. Затем раствор для роста был синтезирован следующим образом:50 мл CTAB (0,2 M) и 50 мл HAuCl 4 (1 мМ), 2,5 мл AgNO 3 (4 мМ) (Sinopharm) слегка перемешивали при 28 ° C. После тщательного мягкого перемешивания добавляли 670 мкл аскорбиновой кислоты (0,079 М), когда цвет раствора изменится с темно-желтого на бесцветный. Сто двадцать микролитров затравочного раствора добавляли при осторожном перемешивании при 28 ° C, и цвет постепенно становился прозрачным от пурпурного до пурпурно-черного. После 24 часов перемешивания при постоянной температуре раствор центрифугировали при 12000 об / мин в течение 10 минут для удаления дополнительного количества ЦТАБ и лиофилизировали в вакууме до порошка GNR для дальнейшего использования.
Синтез MUA-PEI и GAL-PEI-MUA
Меркаптоундекановую кислоту (MUA; 654 мг) растворяли в 30 мл хлороформа (CHCl 3 ), а затем инкубировали со 100 ммоль гидрохлорида 1-этил-3- [3-диметиламинопропил] карбодиимида (EDC) и 100 ммоль N-гидроксисукцинимида (NHS) в течение 15 минут при комнатной температуре. Затем к вышеуказанному раствору добавляли 100 ммоль полиэтиленимина (PEI). Через 24 часа реакции при комнатной температуре равный объем деионизированной воды использовали для экстракции водорастворимого PEI-MUA. Тот же метод был использован для завершения активации d-галактозы в водном растворе. Затем к вышеуказанному водорастворимому раствору PEI-MUA добавляли избыток активированной d-галактозы (500 ммоль), и реакцию достаточно проводили при комнатной температуре в течение 24 часов для получения водорастворимого раствора GAL-PEI-MUA. сложный.
Синтез GAL-PEI-MUA-GNR (GAL-GNR) и PEI-MUA-GNR (PEI-GNR)
Лиофилизированный порошок CTAB-GNR (10 мг) суспендировали в 10 мл водорастворимых комплексов PEI-MUA или GAL-PEI-MUA. CTAB заменяли связью Au – S при перемешивании при комнатной температуре в течение 24 ч. Раствор центрифугировали при 12000 об / мин в течение 15 мин для удаления избыточного супернатанта, а осадок промывали трижды дистиллированной водой. Порошки PEI-GNR или GAL-GNR получали путем сублимационной сушки, взвешивали и растворяли в воде, не содержащей рибозимов, а затем наблюдали эффект плазменного резонанса с помощью многофункционального ферментного анализатора (Spectra Max M5e, Мэриленд, США).
Просвечивающая электронная микроскопия
GNR или GAL-GNR суспендировали в дистиллированной воде, а ресуспензию помещали на медную сетку. После того как образцы на медной сетке были тщательно высушены на воздухе в течение 30 минут, медная сетка была визуализирована с помощью просвечивающего электронного микроскопа (LIBRA 120, Carl Zeiss, Германия).
Анализ в ультрафиолетовой видимой области
GNR, PEI-GNR или GAL-GNR суспендировали в дистиллированной воде. Эффект поверхностного плазмонного резонанса наноматериалов в диапазоне длин волн от 600 до 900 нм был исследован с помощью многофункционального микропланшетного ридера (SpectraMax M5e, Мэриленд, США).
Анализ дзета-потенциала и гидродинамического диаметра
GNR, PEI-GNR или GAL-GNR суспендировали в дистиллированной воде, а затем измеряли дзета-потенциал и гидродинамический диаметр наноматериала на Zetasizer Nano ZS.
Анализ ядерного магнитного резонанса
Лиофилизированный порошок GAL-GNR растворяли в тяжелой воде (99%, Sigma), чтобы получить гомогенную суспензию, и затем суспензию переносили в пробирку для образца ЯМР. Состав GAL-GNR был определен методом ядерного магнитного резонанса (ЯМР) (Bruker, 600 МГц, Германия).
Анализ гелевого сдвига
GAL-GNR и siBRAF смешивали в соответствии с массовым соотношением (0:1, 1:1, 2:1, 3:1, 4:1, 5:1, 6:1, 7:1). После инкубации при комнатной температуре в течение 30 мин в смесь добавляли буфер для загрузки ДНК. Все образцы добавляли в 2% агарозный гель, содержащий 0,01% Goldview (Bioshop, США), а затем подвергали электрофорезу при 90 В в течение 30 мин. Степень обертывания siBRAF визуализировалась на гелевой системе визуализации.
Стабильность миРНК в сыворотке
Смесь GAL-GNR-siBRAF (6:1) инкубировали в свежей мышиной сыворотке при 37 ° C в течение 0 часов, 3 часов, 6 часов, 12 часов, 24 часов и 48 часов соответственно. Группу голого siBRAF плюс свежей мышиной сыворотки обрабатывали в тех же условиях. К раствору GAL-GNR-siBRAF добавляли равный объем 2% додецилсульфата натрия (SDS). После инкубации в течение 30 минут при комнатной температуре добавляли буфер для загрузки ДНК, и все образцы загружали в 2% агарозный гель (содержащий 0,02% Goldview (Bioshop, США)) и подвергали электрофорезу при 90 В в течение 30 минут. Яркость полосок siBRAF визуализировали на гелевой системе визуализации.
Анализ конкурентного ингибирования GAL-GNR-siBRAF
2 × 10 5 Клетки Hepa1-6 культивировали в 12-луночных микропланшетах в течение ночи. Затем клетки предварительно обрабатывали лактобионовой кислотой в течение 12 часов, а затем трансфицировали GAL-GNR - siBRAF (меченый Cy3) в течение 30 минут. Интенсивность внутриклеточной флуоресценции определяли с помощью флуоресцентного микроскопа (шкала =200 мкм).
Возможность доставки GAL-GNR-siBRAF, направленная на рак печени
Один микрограмм cy3-меченного siBRAF инкубировали с PEI-GNR (30 мкг / мл), GAL-GNR (30 мкг / мл) в течение 20 минут при комнатной температуре, а затем добавляли в среду клеток Hepa1-6. После 30 мин инкубации клетки трижды промывали 50% FBS и измеряли интенсивность флуоресценции в клетках под флуоресцентным микроскопом.
Фототермические эффекты
Двадцать, 40, 60, 80 и 100 мкг GAL-GNR и 100 мкг лиофилизированного порошка GNR были тщательно растворены в 1 мл дистиллированной воды. Раствор добавляли в 24-луночный планшет и непрерывно облучали источником лазера ближнего инфракрасного диапазона с длиной волны 803 нм (2 Вт / см 2 ) в течение 15 мин. Температуру каждой группы регистрировали с помощью инфракрасного термометра каждые 0,5 мин в течение первых 5 мин, а затем температуру отмечали каждые 1 мин.
Анализ МТТ
Двести микролитров клеток (3,5 × 10 4 / мл) культивировали в 96-луночных микропланшетах в течение 24 ч, а затем культивировали с различными концентрациями GNR или GAL-GNR (0, 15, 30, 45, 60, 75, 90, 105, 120 мкг / мл). Через 24 или 48 часов инкубации в культуральную систему добавляли 20 мкл МТТ и инкубировали еще 4 часа. Пурпурные кристаллы растворяли в 150 мкл ДМСО с последующим спектрофотометрическим анализом при 490 нм с использованием эталона 650 нм в считывающем устройстве для микропланшетов (SpectraMax M5e, Мэриленд, США).
Тест на окрашивание Calcein-AM и PI
Hepa1-6 клеток (1,5 × 10 5 ) хранили в течение ночи в 12-луночном планшете и обрабатывали PBS, лазером, GAL-GNR-siBRAF (30 мкг / мл:1 мкг), GAL-GNR-siGL2 (30 мкг / мл:1 мкг) + лазером или GAL. -GNR-siBRAF (30 мкг / мл:1 мкг) + лазер в течение 4 ч, а затем облучение ближним инфракрасным светом (808 нм, 2 Вт / см 2 ) в течение 15 мин. Цитотоксичность GAL-GNR определяли с помощью экспериментов по окрашиванию кальцеином-AM (живые клетки) и PI (мертвые клетки). Зеленая флуоресценция кальцеина-AM и красная флуоресценция PI были сфотографированы под флуоресцентной микроскопией.
Количественная ПЦР в реальном времени
Полную клеточную РНК экстрагировали с помощью Trizol (реагент Trizol, Invitrogen) и использовали в качестве матрицы для синтеза кДНК. Q-ПЦР проводили с использованием ген-специфичных прямого и обратного праймеров (0,5 мкл × 10 мкМ каждый) в системе qRT-PCR Stratagene Mx3000P (Agilent Technologies, Lexington, MA, USA). SYBR green PCR MasterMix (Life Technologies) использовали по схеме производителя. Ген домашнего хозяйства β-актин был использован в качестве внутреннего эталона. Последовательности праймеров представляли собой β-актин:5'AGGGAAATCGTGCGTGACATCAAA-3 '(прямой) и 5'ACTCATCGTACTCCTGCTTGCTGA-3' (обратный); BRAF:5'-CAATTGGCTGGGACACGGACAT-3 '(прямой) и 5'-TTGACAACGGAAACCCTGGAAAAG-3' (обратный). Разница в экспрессии генов была рассчитана и отображена как 2 −∆∆Ct метод.
Вестерн-блот
Общий белок клеток Hepa1-6 получали с помощью буфера RIPA (Cell signaling, Pickering, Ontario, Canada) и количественно определяли с помощью бицинхониновой кислоты (BCA). Белок разделяли в 12% SDS-PAGE и переносили в поливинилиденфторид (PVDF). Ген домашнего бета-актина использовали в качестве внутреннего стандарта для определения экспрессии белка BRAF. Полоса белка и внутренний эталон целевого белка были обнаружены с помощью хемилюминесценции ECL.
Скретч-тест
Трансфицированный Hepa1-6 (1,7 × 10 5 / мл) клетки высевали в 12-луночные планшеты в течение ночи. Клетки, которые полностью прилипли к планшету, царапали кончиком пипетки на 10 мкл. Клетки дважды промывали PBS и заменяли средой, содержащей 2% FBS. Среднее значение линии раны наблюдали под микроскопом через 0, 24 и 48 часов. Каждый скретч-тест проводился в трех экземплярах.
Анализ Transwell для миграции и вторжения
Для оценки миграции и инвазии клеток использовали восьми микрометровые трансвелл-камеры (Corning Life Science). Hepa1-6, суспендированный в 200 мкл бессывороточной среды, добавляли в верхние камеры с плотностью 1,7 × 10 5 . мл клеток / лунку, а затем в нижнюю камеру добавляли 500 мкл среды, содержащей 12% FBS. После инкубации в течение 24–48 ч клетки фиксировали 4% -ным раствором параформальдегида в течение 30 мин, а затем клетки окрашивали 1% -ным раствором кристаллического фиолетового в течение 30 мин. Наконец, клетки фотографировали и подсчитывали под инвертированным микроскопом. Для анализа клеточной инвазии эксперименты с клеточной инвазией требуют покрытия гелем ECM, а остальные шаги являются последовательными.
Статистика
Все эксперименты проводили в трех повторностях. Данные были выражены как среднее ± стандартное отклонение и t Стьюдента. тест (двусторонний), чтобы определить разницу между двумя методами. Для сравнения нескольких групп использовали односторонний тест ANOVA. Данные считались статистически значимыми при p <0,05 (* p <0,05, ** p <0,01, *** p <0,001).
Результаты
Синтез и характеристика наноносителя GAL-GNR-siBRAF
Мы разработали новый наноноситель GAL-GNR, который способен доставлять малую интерферирующую РНК (миРНК) в клетки печени и одновременно поддерживать фототермический эффект золотых наностержней. Процедура синтеза GAL-GNR показана на схеме 1. Эта система, нацеленная на печень, содержит три функциональных компонента. Во-первых, основная часть GAL-GNR представляет собой каркас GNR, который имеет длину около 30 нм и диаметр 10 нм, как показано на изображении TEM (рис. 1a), и химически конъюгированный GNR (GAL-GNR) не показал значительных размер изменился и по-прежнему обладал хорошей диспергируемостью (рис. 1b). Данные о размере частиц показали, что средний размер GNR составлял 30,23 нм, что согласовывалось с результатами электронной микроскопии, а размер GAL-GNR (50 нм) и PEI-GNR (42,35 нм) был больше, чем размер GNR, поскольку конъюгация GAL и PEI увеличивала гидратацию между частицами (рис. 1c). Во-вторых, биологически токсичный CTAB на поверхности GNR был заменен положительно заряженным MUA-PEI, который может быть загружен отрицательно заряженной siRNA. Измерение дзета-потенциала показало, что поверхностный заряд GNR увеличился с 35,6 до 42,7 мВ или 41,8 мВ, когда GNR были модифицированы PEI или GAL-PEI соответственно, что указывает на то, что GAL-GNR обладает сильной способностью связывать миРНК (рис. 1d). В-третьих, мы применили GAL в качестве направляющей молекулы для конъюгирования наноносителей GNR, которые могут быть использованы для специфического самонаведения гепатоцеллюлярной карциномы. Спектроскопия поглощения UV-Vis использовалась для предварительного определения структуры модифицированного GNR. Начальная длина волны спектра поглощения немодифицированного GNR составляла 763 нм; сдвиг на 7 нм в длине волны наблюдался первоначально с модификацией MUA-PEI, а другой сдвиг на 8 нм наблюдался в конце синтеза, когда модификация GNR с помощью GAL была успешной (рис. 1e). Чтобы подтвердить GAL в наносистеме, для анализа химических групп использовалось изображение ЯМР. Результаты показали, что сигнал H галактозы был обнаружен только в спектре GAL-GNR в спектре водорода ЯМР, который был δ:3,60, 3,65, 3,70, 3,78, 3,90, 4,53. Спектры ЯМР подтвердили химическую структуру GAL, в которой GAL был успешно конъюгирован с поверхностью GNR (рис. 1f).
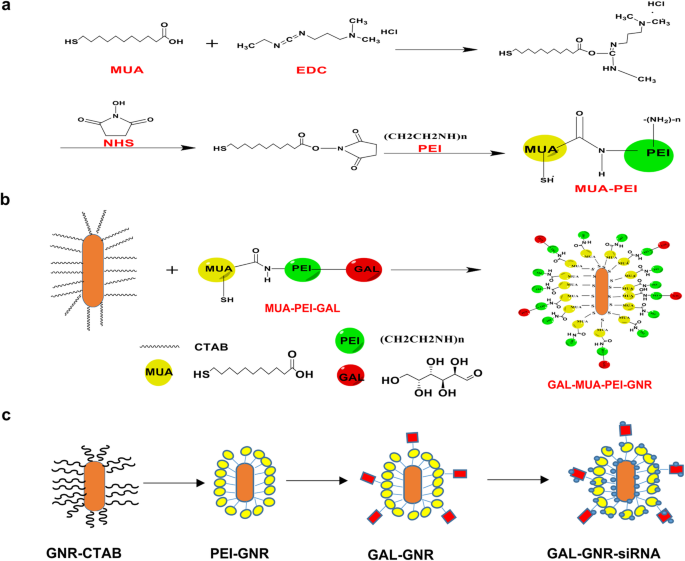
Синтетическая процедура GAL-GNR. а Синтетический процесс MUA-PEI. б Активация d-галактозы и химическая реакция с MUA-PEI. c Конечный синтетический продукт GAL-GNR
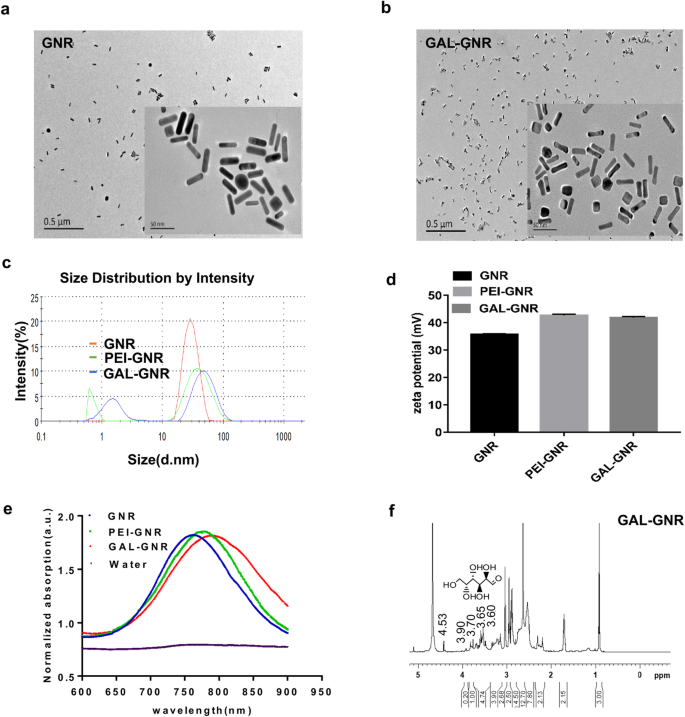
Характеристика GNR и GAL-GNR. а ПЭМ-микрофотография ГНР (масштаб 0,5 мкм / 50 нм). б ПЭМ-микрофотография GAL-GNR (масштаб =0,5 мкм / 50 нм). c Анализ размера частиц различных модифицированных ГНР. г Анализ дзета-потенциала различных модифицированных GNR (GAL-GNR). е Нормированные спектры поглощения различных модифицированных ГНЛ и воды в УФ – видимой области. е Спектры ЯМР поглощения GAL-GNR
Возможность инкапсуляции siRNA и стабильность GAL-GNR
Наноскелет GAL-GNR был модифицирован положительно заряженным PEI, который может быть объединен с отрицательно заряженной siRNA посредством электростатического взаимодействия. Мы использовали анализ сдвига геля для оценки способности GAL-GNR связывать миРНК. Свободная миРНК может перемещаться по проходу геля, в то время как связанная миРНК замедляется или полностью останавливается. Кроме того, связанная миРНК больше не будет эффективно связываться с бромидом, и, таким образом, интенсивность флуоресценции будет соответственно уменьшаться. Результат гель-электрофореза показал, что оптимальное соотношение для насыщения GAL-GNR siBRAF составляет 6:1 (мас. / Мас.) (Рис. 2а).
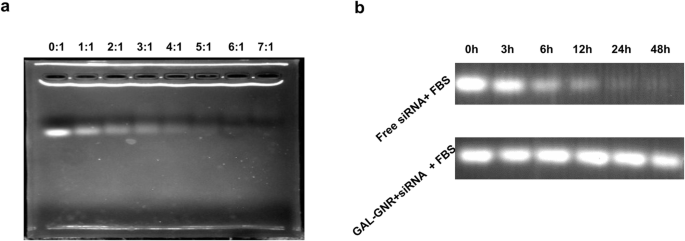
Анализ сдвига геля. а Емкость GAL-GNR по загрузке миРНК. Один микрограмм siRNA смешивали в равных объемах с различными массовыми соотношениями GAL-GNR. После инкубации в течение 30 мин использовали анализ миграции геля для оценки способности GAL-GNR к загрузке миРНК. б Стабильность миРНК в сыворотке крови мышей. Один микрограмм миРНК BARF инокулировали GAL-GNR в массовом соотношении 1:6 и затем добавляли к свежей мышиной сыворотке. После реакции в течение 0, 3, 6, 12, 24 и 48 часов при 37 ° C миРНК из GAL-GNR-siBARF экстрагировали 2% SDS и визуализировали с помощью бромистого этидия
Голая миРНК очень разлагается, особенно in vivo. Важной функцией системы доставки является защита миРНК от деградации. Таким образом, мы протестировали защитный эффект наноносителя GAL-GNR на siRNA в свежей сыворотке соответственно. По сравнению с голой миРНК, связанная миРНК хранилась в сыворотке в течение более длительных периодов времени. Как показано на рис. 2b, голая миРНК могла существовать в сыворотке до 12 часов, в то время как связанная миРНК все еще была в изобилии через 48 часов. Результат продемонстрировал, что GAL-GNR может эффективно предотвращать разложение siRNA в сыворотке, обеспечивая адресную доставку in vivo.
Цитотоксичность наноматериалов
Низкая биологическая токсичность - еще одно важное свойство наноматериалов, которое позволяет использовать их в лечении рака. Чтобы оценить биосовместимость этой новой наноструктуры GAL-GNR, мы проверили ее цитотоксичность. Как показано на фиг. 3, мертвые клетки Hepa1-6 в группе, обработанной немодифицированным GNR, первоначально наблюдались при низкой концентрации 30 мкг / мл. После инкубации с 75 мкг / мл GNR в течение 24 часов, уровень гибели клеток достиг 56,09%, а смертность увеличилась до 75,5% после инкубации в течение 48 часов. Напротив, модификация GAL значительно снижает цитотоксичность. После инкубации GAL-GNR в течение 48 часов более 80% клеток были все еще живы даже при высокой концентрации (105 мкг / мл). Эти данные свидетельствуют о том, что наноноситель GAL-GNR обладает высокой биосовместимостью по сравнению с GNR, обеспечивая безопасность применения.
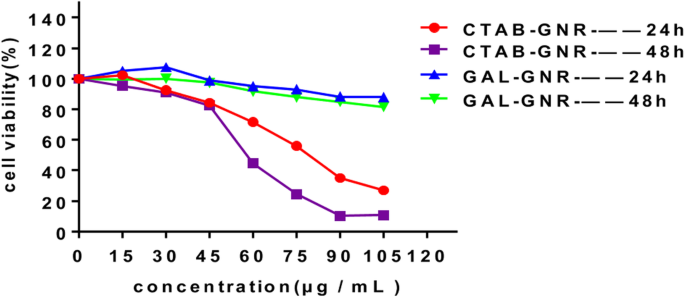
Токсичность GAL-GNR. Клетки Hepa1-6 обрабатывали GNR (CTAB-GNR) или GAL-GNR в течение 24 или 48 часов в указанных концентрациях. Жизнеспособность клеток измеряли с помощью анализа МТТ ( n =5)
Целевая доставка миРНК в клетки гепатомы и подавление генов BRAF in vitro
Способность доставлять миРНК в раковые клетки - одна из наиболее важных функций наноматериалов. Чтобы исследовать потенциал GAL-GNR в доставке siRNA, мы обнаружили эффективность подавления гена с использованием siBRAF, загруженного GAL-GNR в клетках Hepa1-6. По сравнению с пустой группой, экспрессия BRAF в клетках, трансфицированных GAL-GNR-siGL2 (отрицательный контроль), не изменилась, в то время как клетки, трансфицированные GAL-GNR-siBRAF, имели значительное снижение (фиг. 4a). Более того, эффект подавления был дозозависимым, что коррелировало с увеличением концентрации GAL-GNR. Результаты кПЦР продемонстрировали, что идеальная трансфицированная концентрация GAL-GNR-siBRAF составляла 30 мкг / мл, а эффективность подавления молчания может достигать 90,29%, что было аналогично группе липофектамина 2000 (положительный контроль). Результат вестерн-блоттинга соответствовал результатам количественной ПЦР, а экспрессия белка BRAF снижалась после 48 ч трансфекции (рис. 4b).
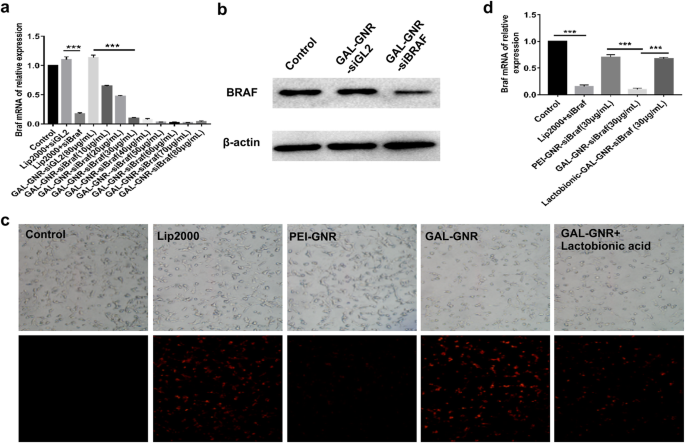
Нацеленная доставка миРНК в клетки гепатомы и подавление генов BRAF in vitro. а МРНК экспрессии BRAF после трансфекции GAL-GNR-siBRAF. Клетки Hepa1-6 трансфицировали различными концентрациями GA-GNR, несущими одинаковое количество миРНК BRAF (1 мкг), в течение 24 часов. Экспрессию мРНК BRAF определяли с помощью кПЦР. Полоса ошибок представляет собой стандартное отклонение трех экспериментов (*** p <0,001). б Экспрессия белка BRAF в Hepa1-6 после трансфекции GAL-GNR-siBRAF. Клетки Hepa1-6 трансфицировали GAL-GNR-siBRAF, GAL-GNR-siGL2 или PBS в течение 48 ч, уровни BRAF и β-актина определяли с помощью вестерн-блоттинга. c и d Способность GAL-GNR-siBRAF к доставке, направленной на рак печени. Один микрограмм cy3-меченного siBRAF инкубировали с lip2000, PEI-GNR (30 мкг / мл), GAL-GNR (30 мкг / мл) в течение 20 минут при комнатной температуре, а затем добавляли в среду клеток Hepa1-6. Для анализа конкурентного ингибирования клетки Hepa1-6 предварительно обрабатывали лактобионовой кислотой в течение ночи. Интенсивность внутриклеточной флуоресценции наблюдали под флуоресцентным микроскопом (шкала =200 мкм), а экспрессию мРНК BRAF количественно оценивали с помощью q-PCR. Полоса ошибок представляет собой стандартное отклонение трех экспериментов (* p <0,05)
Лактобионовая кислота похожа на GAL по структуре, которая может конкурировать с рецептором асиалогликопротеина (ASGPR), который экспрессируется на поверхности клеточной мембраны гепатоцеллюлярной карциномы [35]. Чтобы подтвердить специфическую эффективность нацеливания GAL-GNR, клетки Hepa1-6 предварительно инкубировали с лактобионовой кислотой, а затем трансфицировали GAL-GNR-siBRAF. Необработанные клетки использовали в качестве холостого контроля, а классический реагент для трансфекции липофектамин 2000 использовали в качестве положительного контроля. Как показано на фиг. 4c, интенсивность красной флуоресценции клеток, трансфицированных GAL-GNR, была аналогична группе положительного контроля, в то время как интенсивность флуоресценции клеток, трансфицированных PEI-GNR, значительно снижена. С другой стороны, клетки, трансфицированные только GAL-GNR-siBRAF, наблюдали более сильную красную флуоресценцию Cy3, чем клетки Hepa1-6, предварительно обработанные лактобионовой кислотой (рис. 4c), и результат qPCR соответствовал результатам красной флуоресценции ( Рис. 4г). Эти результаты дополнительно продемонстрировали, что GAL эффективно способствует эндоцитозу siRNA клетками Hepa1-6 и может применяться в качестве целевого фрагмента HCC.
Влияние GAL-GNR-siBRAF на пролиферацию, миграцию и вторжение клеток Hepa1-6
BRAF играет важную роль в пути MAPK, который отвечает за регулирование пролиферации, миграции и инвазии клеток [36]. Чтобы оценить влияние GAL-GNR-siBRAF на клетки гепатоцеллюлярной карциномы, мы сначала проанализировали пролиферацию клеток с помощью тестов MTT. Как показано на фиг. 5а, пролиферация клеток hepa1-6, трансфицированных GAL-GNR-siBRAF, была значительно снижена по сравнению с клетками, обработанными GAL-GNR-siGL2 (отрицательный контроль) или PBS. Затем мы исследовали влияние GAL-GNR-siBRAF на миграцию клеток методами царапин и трансвелл. Compared with negative control cells, the migration ability of Hepa1-6 cells that transfected with GAL-GNR-siBRAF was evidently reduced (Fig. 5b–d).
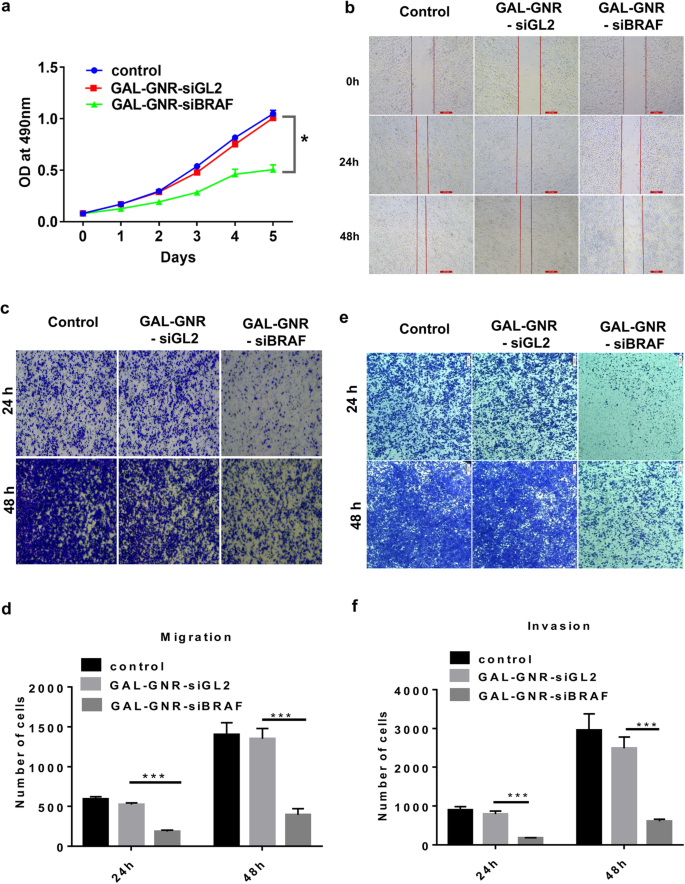
The impact of silencing BRAF gene on Hepa1-6 cells by GAL-GNR-siBRAF. а Proliferation of Hepa1-6 Cells. Hepa1-6 cells were transfected with GAL-GNR-siBRAF, GAL-GNR-siGL2, or PBS, and the cell proliferation was measured by MTT assay (n =5). The error bar represents the standard deviation of three experiments (*p <0,05). б Scratch test of Hepa1-6 cells. Hepa1-6 cells were transfected for 24 h as described above and then scraped with a 10 μL tip. The cell scratch images were taken at different time points (scale bar =200 μm). c и е Migration and invasion of Hepa1-6 cells. Hepa1-6 cells were transfected for 24 h as described above. Cell migration and invasion ability was determined by transwell assay, and imagines were taken at different time points (scale bar =200 μm). г и е Columnar statistical analysis of cell migration and invasive capacity (***p <0.001)
To further investigate the potential of GAL-GNR-siBRAF on the invasion, transwell assays were performed. The results showed that hepa1-6 cells transfected with GAL-GNR-siBRAF haven significantly decreased the invasion of Hepal-6, as compared with GAL-GNR-siGL2 or PBS (Fig. 5e and f). The above results implied that knockdown of BRAF gene using GAL-GNR-siBRAF complexes can effectively reduce migration and invasion of hepatocellular carcinoma cells.
Combination Treatment with Photothermal Effect and Gene Silencing of GAL-GNR-siBRAF
Our previous studies have demonstrated that gold nanomaterials can generate thermal energy under near infrared radiation [37]; this phenomenon is called photothermal effect due to LSPR properties of the GNR. Our results showed that, with the increase of GAL-GNR concentration, the heat production capacity of GAL-GNR was enhanced. When the concentration of GAL-GNR is 100 μg/mL, the temperature quickly rises from 24 to over 60 °C. In addition, there was no significant difference in heat production capacity between GNR and GAL-GNR (Fig. 6a).
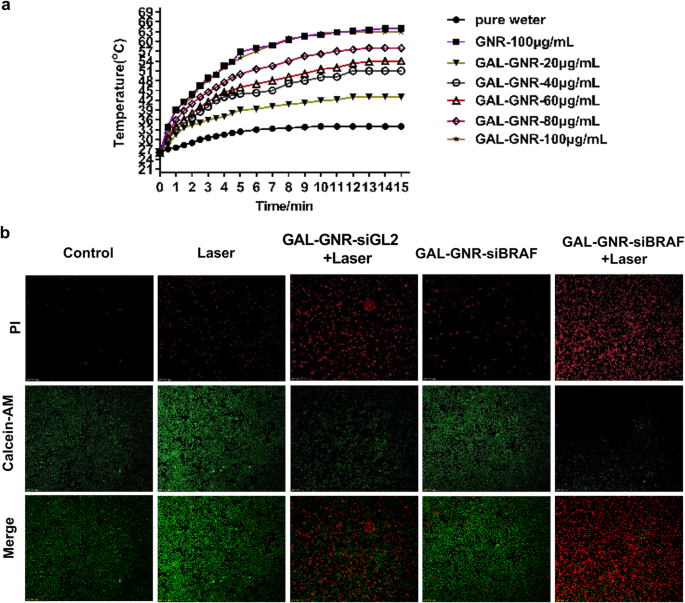
Photothermal effect induced by GAL-GNR and combination treatment of photothermal effect and gene silencing on liver cancer cells. а 803 nm near-infrared laser source (2 W/cm 2 ) was used to irradiate the solution of GNR, GAL-GNR, or distilled water (blank control) for 15 min. The temperature was detected by infrared thermometer at different time point. б Hepa1-6 cells were treated with PBS, laser, GAL-GNR-siBRAF, GAL-GNR-siGL2 + Laser, or GAL-GNR-siBRAF + Laser, respectively. Green fluorescence of calcein AM (live cells) and red fluorescence of PI (dead cells) were observed under fluorescence microscope
The novel nano-system GAL-GNR-siBRAF possesses three individual characteristics:specific targeting of liver cancer, siRNA-based gene silencing of BRAF, and GNR-offered photothermal effects. Thus, we further study the synergistic therapeutic effect of GAL-GNR-siBRAF in anti-tumor treatment. Hepa1-6 cells without GAL-GNR kept higher viability even under near infrared radiation, suggesting laser itself had no significant effect on tumor cells. Once the laser irradiation was carried out on the basis of GAL-GNR-siGL2 treatment, the photothermal effect showed powerful killing ability on Hepa1-6 cells. Although BRAF gene silencing alone induced cell death, the effect was not conclusive. The treatment of cells with the nano-material GAL-GNR-siGL2 plus laser irradiation resulted in much stronger cell-killing ability than BRAF gene silencing individual (Fig. 6b). These data indicates that the BRAF gene silencing and photothermal effect can synergistically increase the potential of killing tumor cells.
Discussion
Difficulties in tumor-targeted delivery are major obstacles in the clinical treatment of tumors. This study demonstrated for the first time that we have developed a novel multifunctional nanocarrier GAL-GNR-siBRAF, and it was provided with many advantages. The modified GAL-GNR not only possessed good biocompatibility but also maintained the LSPR phenomena of GNR skeleton and still has excellent photothermal conversion ability. GNR modified with GAL can home hepatocellular carcinoma cells through ASGPR, which has great potential in targeted molecular therapy of hepatocellular carcinoma. Further studies showed that BRAF gene silencing inhibited the proliferation, migration, and invasion of hepatoma cells. It is worth noting that GAL-GNR-siBRAF shows a stronger cell killing ability in the combination of photothermal effect and gene silencing of BRAF.
RNA interference (RNAi) has attracted much attention due to its crucial role in gene expression and regulation. Using siRNA to knock down sequence-specific genes in cancer cells for gene therapy is an effective and specific targeted gene therapy, and which has become a new therapeutic tool for many diseases including cancer [29, 31]. However, low stability in serum and poor cell uptake limit siRNA in clinical application [38]. On the other hand, siRNA possess negative charge that prevents it from binding negatively charged cell membranes, and siRNA itself is unlikely to be delivered directly into cells [32, 39]. In addition, there are problems associated with low transfection efficiency and poor cell internalization in siRNA therapy [40]. These barriers impede the delivery of siRNA to target cells. To enhance siRNA stability and to strengthen gene silencing efficacy, we synthesized a novel nanocarrier, GAL-GNR-siBRAF, which includes three components (Scheme 1). This nanocarrier has low molecular size (about 30-nm longitude and 10-nm diameter) and good dispersibility (Fig. 1). Additionally, GAL-GNR-siBRAF could effectively load large amount of siRNA at low concentration (Fig. 2a) and protect siRNA degradation from RNase in serum; the siRNA was evidenced by stability for at least two days at 37 °C in the presence of fresh murine serum (Fig. 2b).
Good biocompatibility is essential for nanomaterials used in the field of biotherapy. CTAB is an essential active reagent in the synthesis of gold nanorods although it has apparent cytotoxicity that limits its biological application [41]. In order to reduce the cytotoxicity of the material, we manipulated the GNR by external modification of positive charge PEI and targeting adaptor GAL (d-galactose). Our results showed that, compared with unfunctionalized GNR, GAL-modified GNR has a better biocompatibility. The cell viabilities maintained over 80% even at very high concentrations (105 μg/mL) of GAL-GNR for 48 h (Fig. 3). In addition, the small molecular size and cylindrical shape of the nanorod facilitate its penetration through the cell membrane into the cell [37, 38, 42]. This phenomenon is particularly evident in targeted therapy of cancer cells. Nano-construct modified with the galactose-targeting moieties resulted in high accumulation of GAL-GNR-siBRAF in tumor cells, inducing effective downregulation of BRAF gene expression (Fig. 4). Moreover, according to the competitive inhibition experiments, we found that GAL-GNR entered cells mainly through ASGPR surface receptors of Hepa1-6 cells (Fig. 4c).
It was reported that HCC with high expression of BRAF and RAF1 tends to have rapid proliferation and growth [41, 43, 44]. B-Raf and Raf1 mainly act on the downstream of ERK/MAPK pathway, regulating nuclear factors through cascade amplification. Activation of this pathway accelerates the proliferation and differentiation of HCC cells abnormally [41, 44, 45]. RAF gene can also promote the expression of matrix metalloproteinases (MMPs), which can change the adhesion of tumor cells, degrade extracellular matrix (ECM) and basement membrane, and promote the invasion and metastasis of tumors [44, 45]. BRAF kinase regulates the RAS-RAF-MEK-ERK pathway, which promotes tumor cell proliferation, invasion and metastasis, and allows cell death through apoptosis [5, 46, 47]. In previous work, we found that BRAF gene was highly expressed in Hepa1-6 cells (data were not shown). It is speculated that the knock down of BRAF expression in Hepa1-6 will block the RAS-RAF-MEK-ERK pathway and lead biological changes of Hepa1-6. To verify our hypothesis, we transfected hepatocellular carcinoma cells with GAL-GNR-siBRAF and found that it can restrain the cell proliferation, migration, and invasion significantly (Fig. 5), providing a new strategy for clinical treatment of hepatocellular carcinoma.
Another important advantage of GNR is that it possesses local surface plasmon resonance (LSPR), which can convert absorbed light energy into heat energy under near infrared light irradiation, thereby killing and destroying cells [42]. Then, we explored the light-to-heat conversion ability of GAL-GNR, and the results showed that the modified GAL-GNR can induce heat energy effectively under the irradiation of near infrared light (Fig. 6a). Next, we further investigated the synergistic effects of GAL-GNR-siBRAF. Whereas BRAF gene silencing showed limited cytotoxicity, the treatment of GAL-GNR-siGL2 + laser had a much stronger killing ability on tumor cells. At the same time, the combination of photothermal hyperthermia and BRAF gene silencing could cause more than 85% cell death (Fig. 6b) which indicates that the synergy of GAL-GNR-siBRAF and photothermal effects could be an ideal strategy to inhibit liver cancer.
Conclusion
This study showed that GAL-GNR-siBRAF overcome the obstacle of siRNA degradation, effectively increased the stability of siRNA in serum in vitro. In addition, GAL-GNR-siBRAF can target deliver siRNA to hepatocellular carcinoma cells and knockdown the expression of BRAF and inhibit the cell proliferation, invasion, and migration significantly. More importantly, GAL-GNR-siBRAF, as a new multifunctional nanocarrier, can greatly enhance the ability of killing tumor cells when combined with near-infrared light. In conclusion, GAL-GNR-siBRAF has great potential in treatment of hepatocellular carcinoma and provides new ideas for clinical application of liver cancer.
Доступность данных и материалов
All data generated and materials used in this study are included in the manuscript and corresponding additional files.
Сокращения
- GAL:
-
d-galactose
- GNR:
-
Golden nanorods
- siBRAF:
-
Small interfering RNA specific for BRAF
- HCC:
-
Гепатоцеллюлярная карцинома
- ASGPR:
-
Asialoglycoprotein receptor
- TACE:
-
Transcatheter arterial chemoembolization
- LSPR:
-
Локализованный поверхностный плазмонный резонанс
- CTAB:
-
cetyltrimethylammonium bromide
- MUA:
-
Mercaptoundecanoic acid
- EDC:
-
1-ethyl-3-[3-dimethylaminopropyl] carbodiimide hydrochloride
- NHS:
-
N-hydroxysuccinimide
- PEI:
-
Полиэтиленимин
- ТЕМ:
-
Просвечивающая электронная микроскопия
- NMR:
-
Nuclear magnetic resonance
- FBS:
-
Фетальная бычья сыворотка
- DMSO:
-
Dimethyl Sulfoxide
- BCA:
-
Bicinchoninic acid
- PVDF:
-
Поливинилиденфторид
Наноматериалы
- Получение наночастиц mPEG-ICA, нагруженных ICA, и их применение в лечении LPS-индуцированного повреждения клеток H9c2…
- PLGA-липидные наночастицы с отслеживанием 131I как носители доставки лекарств для целевого химиотерапевтическо…
- Новый метод целевого нанопрепарата без органического растворителя для повышения противоопухолевой эффекти…
- Влияние отжига in situ на подвижность и морфологию органических полевых транзисторов на основе TIPS-пентацена
- Эффект распыленного под косым углом электрода ITO в структурах перовскитных солнечных элементов MAPbI3
- Стимуляция роста клеток SH-SY5Y наночастицами золота, модифицированными 6-меркаптопурином и проникающим в нейро…
- Токсичность наночастиц CoFe2O4, покрытых ПЭГ, с лечебным эффектом куркумина
- Прямое выращивание желтого светодиода на основе нитрида III-нанопровода на аморфном кварце с использованием т…
- Золотые наночастицы круглой формы:влияние размера и концентрации частиц на рост корней Arabidopsis thaliana
- Эффективное поглощение света с использованием решеток двусторонней пирамиды для тонкопленочных кремниевых…



