Иерархический пористый углерод с взаимосвязанными упорядоченными порами из биологических отходов для электродов высокоэффективных суперконденсаторов
Аннотация
Использование биоотходов в качестве прекурсоров для получения наноматериалов с добавленной стоимостью имеет решающее значение для устойчивого развития устройств. Лигносульфонаты являются побочными продуктами целлюлозно-бумажной промышленности и обычно выбрасываются как отходы. В настоящем исследовании лигносульфонат используется в качестве прекурсора для получения иерархически упорядоченного пористого углерода со взаимосвязанными порами для применения в электрохимическом накоплении энергии. Уникальная молекулярная структура и свойства лигносульфоната обеспечивают получение высококачественного пористого углерода с контролируемой структурой пор и улучшенными физическими свойствами. В результате предварительно подготовленный пористый углерод иерархического порядка демонстрирует отличные характеристики накопления энергии при использовании для сборки симметричного суперконденсатора, который демонстрирует высокую удельную емкость 289 Ф · г -1 при плотности тока 0,5 А изб −1 , с плотностью энергии 40 Вт · ч кг −1 при удельной мощности 900 Вт кг −1 . Настоящее исследование предлагает многообещающую стратегию производства высокопроизводительных накопителей энергии по невысокой цене.
Введение
Суперконденсаторы являются многообещающими в качестве накопителей энергии для систем резервного копирования и различной электроники из-за их высокой плотности мощности, длительного срока службы, легкости по сравнению с батареями и обычными конденсаторами [1,2,3,4,5,6]. Наноматериалы на основе углерода известны своими превосходными характеристиками аккумулирования энергии в качестве материалов активных электродов в суперконденсаторах, которые накапливают электричество через двойной электрохимический слой. Их характеристики аккумулирования энергии определяются физическими свойствами активных материалов электродов, особенно пористой структурой [7,8,9]. Макропоры (более 50 нм) служат резервуарами для ионной буферизации, мезопоры (2–50 нм) - каналами транспорта ионов электролита, а микропоры - обычно местами накопления заряда [10]. Наша предыдущая работа, основанная на исследовании линейной корреляции, показывает, что удельная емкость и скоростная способность сильно зависят от объема как микропор, так и мезопор [11, 12], соответственно. Ожидается, что суперконденсаторы на основе углеродных наноматериалов будут иметь иерархическую пористую структуру со сбалансированным распределением макропор, мезопор и микропор, которые связаны между собой.
Были предприняты значительные усилия, чтобы подготовить иерархический пористый углерод для лучшего накопления энергии [13,14,15,16]. Исследователи разработали различные твердые шаблоны, включая цеолит, MCM-41, MCM-48, SBA-15, SBA-16 и KIT-6 для приготовления пористого углерода с упорядоченными мезопорами [17, 18]. Химическая и физическая активация также широко используются, что обычно приводит к беспорядочно распределенным закрытым порам [13] и, следовательно, плохо контролирует структуру пор.
Биомасса и биоотходы были химически и физически активированы при повышенных температурах для получения пористого углерода [19]. Немногие из них были использованы в темплатных методах синтеза пористого углерода с упорядоченной пористой структурой [11, 12, 20]. Многие пористые угли получают из дорогих и невозобновляемых поверхностно-активных веществ и блок-сополимеров. Лигнин является вторым по распространенности органическим материалом и самым распространенным ароматическим полимером, существующим в видах растений [21]. В бумажной промышленности лигнин превращается в лигносульфонаты в процессе варки целлюлозы и обычно выбрасывается как отходы, что приводит к серьезным экологическим проблемам [22]. Лигносульфонаты обычно представляют собой небольшие молекулы с ароматическим кольцом и кислородсодержащими группами. Как правило, они имеют гораздо меньшую молекулярную массу, чем лигнин, и демонстрируют отличную растворимость в воде за счет кислородсодержащих групп [23]. Эти достоинства делают лигносульфонаты идеальными предшественниками, которые можно использовать в темплатном методе для синтеза пористого углерода с упорядоченной структурой пор с добавленной стоимостью.
В настоящем исследовании мы использовали KIT-6 в качестве твердого шаблона из-за его хорошей взаимосвязанности упорядоченных пор и возможности контроля над размером пор для получения упорядоченного мезопористого углерода, объединившего постхимическую активацию для создания микропор в мезопористой структуре. Лигносульфонат натрия использовался в качестве прекурсора. Свежеприготовленный иерархически упорядоченный пористый углерод (HOPC) был использован для сборки симметричного суперконденсатора, который демонстрирует выдающиеся характеристики накопления энергии.
Методы
Подготовка KIT-6
Упорядоченный мезопористый темплат диоксида кремния (KIT-6) был синтезирован согласно [24]. В модифицированной методике 5,53 г Pluronic P123 (EO 20 ЗП 70 EO 20 , MW =5800, Aldrich) сначала растворяли в 200 г деионизированной воды, содержащей 10,9 г концентрированной HCl (35%), в стеклянной бутылке объемом 250 мл. Затем в бутыль добавили 5,53 г бутанола при перемешивании при 35 o . После перемешивания в течение 1 часа к вышеуказанному раствору добавляли 11,9 г TEOS (тетраэтилортосиликат, Aldrich), а затем смесь перемешивали в течение 24 часов при 35 ° C. C. Затем бутылку выдерживали еще 24 часа при 100 o . C в статических условиях. Твердый продукт собирали фильтрованием и сушили при 100 ° С. C без стирки. Органический остаток удаляли экстракцией смесью этанола и HCl с последующим прокаливанием при 550 o . C в течение 6 ч.
Приготовление упорядоченного мезопористого углерода
Упорядоченный мезопористый углерод (OMC) получали с использованием синтезированного KIT-6 в качестве твердой матрицы и лигносульфоната натрия в качестве источника углерода. Синтезированный выше темплат диоксида кремния KIT-6 использовали для загрузки лигносульфоната. Обычно 0,6 г лигносульфоната натрия, приобретенного в Lanyi Reagent (Пекин, Китай), растворяли в 15 мл деионизированной воды с последующим добавлением 0,6 г шаблона KIT-6. Смесь перемешивали в течение 24 ч при комнатной температуре с последующей сушкой при 70 ° С. Высушенный композит, содержащий диоксид кремния и лигносульфонат натрия, использовали в качестве прекурсора для карбонизации. Процесс карбонизации проводился при 900 o C в течение 2 часов в Ar при расходе газа 30 см3 / мин. После карбонизации шаблон из диоксида кремния удаляли, погружая композит в 2,5 М водный раствор NaOH на 12 ч при комнатной температуре. После промывки с использованием разбавленного раствора HCl и деионизированной воды был получен мезопористый упорядоченный углерод (сокращенно OMC), который был записан как OMC-900 (цифровое число относится к температуре карбонизации). OMC-700, OMC-800 и OMC-1000 относятся к полученным образцам, карбонизированным при 700 o . С, 800 o C и 1000 o C соответственно.
Подготовка иерархического упорядоченного пористого углерода
Для получения иерархически упорядоченного пористого углерода (сокращенно HOPC) был использован процесс постхимической активации. Вкратце, свежеприготовленный OMC-900 гомогенно смешивали с ZnCl 2 . раствор с массовым отношением углерода к ZnCl 2 1:1 и сушат при 110 o C в течение 6 ч. Активационная обработка проводилась путем нагревания композитов при 900 o C в течение 3 ч в Ar при расходе газа 30 см3 / мин. Чтобы исследовать влияние температуры карбонизации, шаблоны KIT-6, пропитанные лигносульфонатом натрия, также карбонизировали при 700 o C и 800 o C, обозначенный как OMC-700 и OMC-800. Для сравнения, чистый лигносульфонат натрия без какой-либо обработки был непосредственно карбонизирован в тех же условиях, и полученный углерод был записан как лигнин-углерод.
Характеристика
Морфология синтезированной матрицы KIT-6 и пористых углеродных образцов была охарактеризована с помощью сканирующей электронной микроскопии Hitachi SU8020 (SEM). Мелкопористая структура была дополнительно исследована с помощью просвечивающей электронной микроскопии (ПЭМ) JEOL 2100F. Картину дифракции рентгеновских лучей под низким углом записывали на порошковом рентгеновском дифрактометре XD-2 / XD-3. Химическая структура была исследована с помощью рентгеновской фотоэлектронной спектроскопии (XPS) ESCALAB250Xi. Рамановская характеристика была проведена с использованием рамановской спектроскопии HORIBA Science. Инфракрасные спектры с преобразованием Фурье (FTIR) регистрировали с использованием FTIR-спектроскопии NEXUS 670. Пористые характеристики шаблона КИТ-6 и пористого углерода были проанализированы с помощью N 2 эксперименты по адсорбции / десорбции при 77 К с использованием Micromeritic ASAP2020 V3.02 H. Удельную поверхность измеряли в соответствии с методом Брунауэра-Эмметта-Теллера (БЭТ), а распределение пор по размерам рассчитывали с использованием нелокальной плотности щелевых пор. модель функциональной теории (NLDFT).
Электрохимические измерения
Электрохимические характеристики свежеприготовленных образцов пористого углерода были исследованы с использованием трехэлектродной конфигурации. Наконец, оптимизированный HOPC был исследован с использованием двухэлектродной конфигурации. Рабочий электрод в трехэлектродной системе был изготовлен путем физического смешивания свежеприготовленного пористого углерода и ПВДФ, который был заранее растворен в растворителе НМП с массовым отношением углерода к ПВДФ 9:1. Гомогенная суспензия была нанесена на никелевую фольгу с площадью покрытия около 1 см 2 . с последующей сушкой при 80 o C в течение 12 ч для удаления остаточного растворителя. При испытании с тремя электродами платиновая пластина (1 см 2 ) и Ag / AgCl использовались в качестве противоэлектрода и электрода сравнения соответственно. Рабочий электрод в двухэлектродной системе был приготовлен по той же методике с заменой никелевой фольги на пеноникелевый. Пеноникелевый пенопласт с тем же количеством загружаемых материалов активных электродов был использован для сборки симметричного суперконденсатора, в котором фильтровальная бумага использовалась в качестве разделителя. Как в трехэлектродной, так и в двухэлектродной конфигурациях в качестве электролита использовались 6 М водные растворы КОН.
Циклическую вольтамперометрию (CV), спектроскопию электрохимического импеданса (EIS) и постоянный гальваностатический заряд / разряд проводили на приборе Gamry reference 3000. Измерение CV в трехэлектродной конфигурации проводилось при потенциальном окне от -1 до 0 В по сравнению с Ag / AgCl, в то время как потенциальное окно в симметричном суперконденсаторе составляло от 0 до 1 В. Определение характеристик EIS проводилось при амплитуде переменного тока 5 мВ в диапазоне частот от 1 МГц до 0,01 Гц. Удельная емкость из кривых CV, собранных при испытании с тремя электродами, была рассчитана по уравнению C =ʃ Я dt / мВ . Удельная емкость, полученная из кривой CV при испытании двух электродов и гальваностатическом испытании, была определена с помощью C =4ʃ I dt / MV и C =v4 Я т / МВ , соответственно, где I - ток разряда, t - время разряда, В - окно рабочего напряжения, м - масса активного материала на рабочем электроде в трехэлектродной конфигурации, а M - полная масса активного материала на двух электродах симметричного суперконденсатора. Плотность энергии ( E ) и удельной мощности ( P ) были рассчитаны на основе испытаний гальваностатического заряда / разряда с помощью E = CV 2 / 2 и P = E / t , соответственно, где C - удельная емкость при испытании двух электродов и t время разряда.
Результаты и обсуждение
Образец HOPC был синтезирован в пять этапов, как показано на рис. 1. (a) Шаблон из диоксида кремния KIT-6 был приготовлен модифицированным методом, описанным в литературе [24]; (b) лигносульфонатом натрия пропитывали шаблон KIT-6 путем погружения шаблона из диоксида кремния KIT-6 в водный раствор лигносульфоната натрия; (c) KIT-6, загруженный лигносульфонатом натрия, карбонизировали в течение 2 часов в газообразном аргоне. Чтобы оптимизировать процесс карбонизации, мы провели карбонизацию при 700 o С, 800 o С, 900 o C и 1000 o (D) после карбонизации шаблон из диоксида кремния KIT-6 затем удаляли в теплом 2,5 М растворе NaOH для получения упорядоченного мезопористого углерода (OMC); (e) образец углерода OMC был дополнительно химически активирован с использованием ZnCl 2 в 900 o C в течение 3 ч для приготовления HOPC.
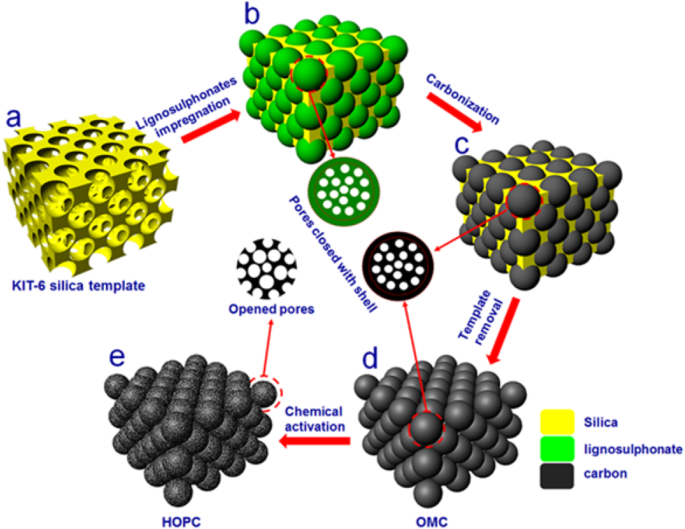
Иллюстрация процессов синтеза иерархически упорядоченного пористого углерода (HOPC) с использованием метода жесткого шаблона в сочетании с постхимической активацией
Свежеприготовленный шаблон из диоксида кремния KIT-6 был сначала проанализирован с использованием малоугловой порошковой дифрактограммы (XRD), как показано на фиг. 2a. Синтезированный кремнезем КИТ-6 относится к кубическому Ia3d с двумя характерными дифракционными пиками при 1 o и 1.2 o плоскостей (211) и (220) кубической упорядоченной мезопористой структуры [24]. Результаты N 2 Адсорбционный / десорбционный анализ показывает, что матрица диоксида кремния KIT-6 состоит из большинства мезопор и небольшого количества микропор с хорошей взаимосвязью (рис. 2b). Распределение пор по размерам сосредоточено на 2,5 нм и 7,5 нм (рис. 2c). Площадь поверхности БЭТ (Брунауэра-Эмметта-Теллера) составляет 1481 м 2 г −1 а общий объем пор - 2,62 см 3 г −1 . Мы дополнительно исследовали микроморфологию и структуру пор синтезированного шаблона KIT-6 с помощью просвечивающей электронной микроскопии (ПЭМ), как показано на рис. 2d. Яркие точки обозначают поры и темные участки стен (кремнезем). Толщина стенки и средний размер пор составляют 3,1 нм и 6,4 нм соответственно. Изображение вставки шаблона БПФ на рис. 2d подтверждает периодически упорядоченную структуру пор.
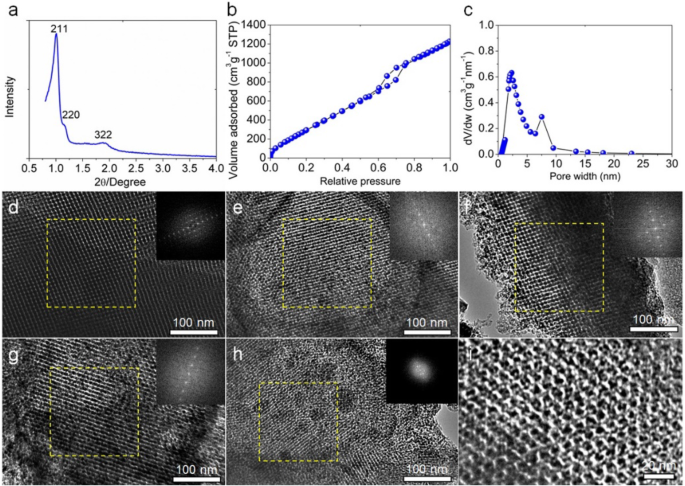
Характеристика подготовленного темплата из диоксида кремния КИТ-6, а Малоугловая дифрактограмма диоксида кремния КИТ-6. б N 2 изотерма адсорбции / десорбции темплата КИТ-6. c Соответствующее распределение пор по размерам для N 2 рассчитано с использованием модели NLDFT с щелевой порой. ПЭМ-изображения ( d ) Кремнезем КИТ-6, образцы углерода OMC, полученные на заводе ( e ) 700 o C, ( f ) 800 o C и ( g ) 900 o C и образец HOPC ( h - я ). Вставленные изображения представляют собой соответствующие шаблоны быстрого преобразования Фурье выбранных областей
Образцы углерода OMC были охарактеризованы методами СЭМ и ПЭМ. На рисунке S1 свежеприготовленные образцы углерода OMC при различных температурах карбонизации демонстрируют сотовую морфологию с упорядоченными порами. Далее мы использовали ПЭМ для исследования микропористой структуры, как показано на рис. 2e – g. На изображениях ПЭМ показаны упорядоченные нанодомены. Темные части представляют собой изолированный углерод, а светлые части - соединенные между собой поры. На изображениях БПФ видны четкие и яркие пятна для всех образцов углерода OMC, что еще раз подтверждает упорядоченную структуру пор. Размер пор составляет 2,9 нм, 2,1 нм и 2,4 нм для OMC-700, OMC-800 и OMC-900 соответственно, что очень близко к толщине стенки темплата из диоксида кремния. Напротив, образец, полученный карбонизацией лигносульфоната натрия без использования темплата из диоксида кремния, не показывает пористой структуры (рис. S2). Сделан вывод, что заказанный мезопористый углерод успешно получается с использованием лигносульфоната натрия и кремнеземного шаблона KIT-6 при выбранных температурах карбонизации.
Эксперименты по адсорбции / десорбции азота были проведены для исследования физических и химических свойств синтезированных образцов углерода OMC, как показано на рисунке S3. Все кривые изотермы имеют аналогичные промежуточные значения, и адсорбированный объем увеличивается при очень низком относительном давлении и быстро увеличивается с увеличением относительного давления, что свидетельствует о сосуществовании как микропор, так и мезопор с большим объемом пор для всех свежеприготовленных образцов OMC. Распределение пор по размерам для образцов OMC имеет центр при 0,6 нм и 2,3 нм. Мы дополнительно повысили температуру карбонизации до 1000 o . C и изотермическая кривая образца OMC-1000, показанного на рисунке S4, демонстрируют аналогичный профиль, что указывает на аналогичную структуру пор. На рис. 3а показаны зависимости удельной поверхности, общего объема пор, объема микропор и объема мезопор от температуры карбонизации. Увеличение удельной поверхности связано с увеличением общего объема пор. Дальнейшее повышение температуры карбонизации до 1000 o C удельная поверхность уменьшается до 1948 м 2 г −1 , с уменьшенным объемом микропор и увеличенным объемом мезопор. Предполагается, что оптимальная температура карбонизации составляет 900 o . C. Таблица S1 суммирует физические свойства полученных образцов углерода OMC. Установлено, что образец OMC-900 показывает самую высокую удельную поверхность 2201 м 2 . г −1 и общий объем пор 3,74 см 3 г −1 .
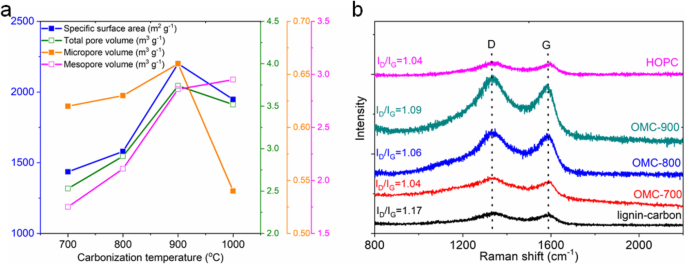
Характеристика свежеприготовленного углерода OMC и образцов HOPC. а Удельная поверхность, общий объем пор, объем микропор и объем мезопор как функция температуры карбонизации. б Рамановские спектры
Поэтому мы провели химическую активацию с использованием ZnCl 2 . в качестве реагента активации с использованием образца OMC-900 для дальнейшего создания иерархической пористой структуры. Как видно из SEM-изображения на рисунке S5, упорядоченная трехмерная сеть пор была частично разрушена после химической активации с образованием множества изолированных наночастиц. На изображении ПЭМ на рис. 2e четко видны упорядоченные поры, а соответствующая картина БПФ показывает яркие пятна, указывающие на существование упорядоченных нанодоменов. Изображение ВРЭМ на рис. 2е показывает, что микропоры образуются на стенках мезопор после химической активации. Результаты N 2 адсорбция / десорбция показывают, что после химической активации образец HOPC показывает значительно увеличенную удельную поверхность 2602 м 2 г −1 , с объемом микропор 1,03 см 3 г −1 и объем мезопор 3,49 см 3 г −1 (Таблица S1 и рисунки S6a и b).
Свойства лигносульфонатов способствуют образованию упорядоченного мезопористого углерода. На рисунке S7 показана типичная молекулярная структура лигносульфоната, а гидроксильные группы позволяют молекулам лигносульфоната протекать реакции сшивания [25]. В настоящем исследовании предполагается, что молекулы лигносульфоната адсорбируются на гидрофильных стенках диоксида кремния через гидроксильные группы и сшиваются друг с другом посредством водородных связей с образованием трехмерных сеток. Спектры FTIR матрицы KIT-6, лигносульфоната натрия и лигносульфонатов, импрегнированных шаблоном KIT-6, показаны на рисунке S8. Пики лигносульфоната натрия расположены при 3429 см −1 , 2950 см −1 , 1635 см −1 , 1514 см −1 , 1041 см −1 может быть отнесен к растяжению O – H, растяжению C – H, растяжению C =O, растяжению C – C и растяжению C – O [26] соответственно. Пики темплата из диоксида кремния КИТ-6, расположенные на 463 см −1 , 802 см −1 , и 1090 см −1 относятся к качанию Si – O – Si. Пик расположен на 967 см −1 обусловлено колебанием Si – O поверхностных силанолов [27]. В спектрах лигносульфонат-диоксид кремния сосуществуют характерные пики лигносульфоната и диоксида кремния, что подтверждает импрегнирование лигносульфоната в темплате диоксида кремния. Кроме того, пик расположен на 3429 см −1 в лигносульфонате-диоксид кремния расширен, что указывает на образование водородных связей между молекулами лигносульфоната посредством реакции сшивания. Адсорбированные и ориентированные молекулы лигносульфоната превращаются в твердые углеродные слои во время процесса карбонизации, что может вызвать появление множества закрытых пор, как показано на этапах b и c на рис. 1. Химическая активация помогает открыть эти закрытые поры для дальнейшего улучшения физических свойств. .
Рамановская характеристика использовалась для исследования степени графита в свежеприготовленных образцах углерода, и результаты показаны на рис. 3b. Все спектры комбинационного рассеяния показывают характеристическую полосу D и полосу G, расположенную при 1340 см -1 . и 1590 см −1 , соответственно. Отношение интенсивностей полосы D (неупорядоченный углерод) и полосы G (упорядоченный углерод) для образцов OMC и образца HOPC составляет около 1,06, что ниже 1,17 для образца углерода, полученного карбонизацией лигносульфоната без использования диоксида кремния. шаблон. Этот результат показывает, что образцы углерода OMC имеют более высокую степень графита, чем образец углерода, полученный в результате прямой карбонизации лигносульфоната. Причина, вероятно, связана с вышеупомянутой реакцией сшивания между молекулами лигносульфоната, которая помогает ориентации ароматических колец. Результат XPS-анализа на Рисунке S9 показывает, что все образцы в основном содержат углерод и кислород. Нет обнаруживаемого сигнала о примеси в конечных углеродных продуктах. Разложение лигносульфоната натрия может привести к образованию CO 2 и Na 2 CO 3 [28], которые могут быть полностью удалены при последующей промывке деионизированной водой. Уровень керна C1s может быть деконволюционирован на четыре компонента для всех образцов углерода, как только они были приготовлены. То есть C – O (286,7 эВ), C =O (288,0 эВ) [29], sp 2 углерод (284,8 эВ, упорядоченный углерод) и sp 3 углерод (285,4 эВ, неупорядоченный углерод) [30].
Электрохимические характеристики свежеприготовленных образцов углерода OMC и образца активированного HOPC оценивали с помощью трехэлектродной конфигурации в 6 M водном электролите KOH. Образец углерода, полученный в результате прямой карбонизации лигносульфоната, показывает незначительные характеристики накопления энергии (Рисунок S10). Образцы углерода OMC демонстрируют прямоугольные профили CV, указывающие на улучшенные электрохимические характеристики (рис. S11 и рис. 4a). При 2 мВ с −1 , удельная емкость составляет 59 Ф · г −1 , 93 Ф г −1 , 130 Ф г −1 , и 120 Ф г −1 для OMC-700, OMC-800, OMC-900 и OMC-1000 (рис. 4b). Электрод OMC-900 показывает лучшие электрохимические характеристики среди всех образцов углерода OMC. После химической активации удельная емкость дополнительно увеличивается до 243 Ф · г -1 . для образца HOPC почти вдвое выше, чем для образца OMC-900 до активации. Удельная емкость HOPC в этом исследовании намного выше, чем у углерода, полученного из грибов (196 Ф · г −1 при 5 мВ с −1 ) [31], а также выше, чем у мезопористого углерода на основе графенового аэрогеля, полученного из твердого темплата из диоксида кремния (226 F g −1 при 1 мВ с −1 ), которая уменьшается до 83 Ф г −1 при 100 мВ с −1 [32]. Для углерода, полученного из грибов, удельная емкость уменьшается до 90 Ф · г -1 . при 100 мВ с −1 . Однако удельная емкость HOPC по-прежнему составляет 128 Ф · г -1 . с той же скоростью сканирования.
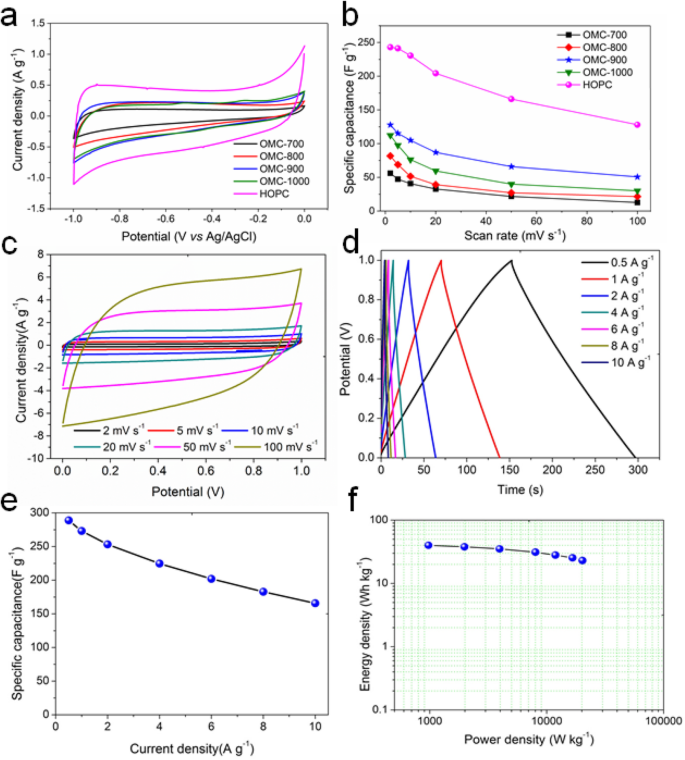
а Профили циклической вольтамперометрии (CV) электродов OMC-700, OMC-800, OMC-900, OMC-1000 и HOPC при скорости сканирования 2 мВ с −1 с использованием трехэлектродной конфигурации и b соответствующая удельная емкость. c CV-профили HOPC-электрода в симметричном двухэлектродном суперконденсаторе при скоростях сканирования от 2 мВ с −1 до 100 мВ с −1 в 6 М водном электролите КОН. г Кривые заряда-разряда при различной плотности тока от 0,5 А изб −1 до 10 А г −1 . е Удельная емкость рассчитана на основе кривых разряда при испытании заряда-разряда. е Графики Рагона, показывающие плотность энергии как функцию плотности мощности
Были проведены измерения импеданса для исследования проводимости образцов. На рисунке S12 показаны спектры сопротивления Найквиста в диапазоне частот от 1 МГц до 0,01 Гц и соответствующая эквивалентная схема, которая состоит из эквивалентного последовательного сопротивления ( R s ), сопротивление переносу заряда ( R ct ) и электрохимической емкости двойного слоя. Эквивалентное последовательное сопротивление R s составляет 0,7 Ом см −2 для всех электродов, что свидетельствует о высокой электропроводности образцов и высоком качестве электродов. Графики Найквиста показывают, что электрод HOPC показывает самое низкое сопротивление переносу заряда - 5 Ом.
Доставляемая энергия и плотность мощности во многом зависят от частотно-зависимой емкости [33, 34], которая может быть выражена следующим образом
$$ C =\ frac {1} {jwZ} =\ frac {- {Z} _ {\ mathrm {image}}} {W {\ left | Z \ right |} ^ 2} -j \ frac {- { Z} _ {\ mathrm {real}}} {W {\ left | Z \ right |} ^ 2} ={C} _ {\ mathrm {real}} - j {C} _ {\ mathrm {image}} $$где C и Z - емкость и сопротивление соответственно. Я реальный и Z изображение относятся к действительной и мнимой части Z . C реальный - действительная часть емкости, представляющая поставляемую емкость электродных материалов, а C изображение - мнимая емкость, связанная с необратимой потерей удельного сопротивления в устройстве. На рисунке S13a показано, что образец HOPC дал самый быстрый ответ. Частота ƒ частота символов, с которой C изображение достигает максимума, и t =1 / ƒ - постоянная времени суперконденсатора. Оба f и t - характеристическая способность к скорости. Суперконденсаторы с высокой плотностью мощности обычно имеют высокую частоту символов ƒ и маленькие t . На рисунке S13b показаны графики C изображение как функция частоты. Частота символов OMC-700, OMC-800, OMC-900, OMC-1000 и HOPC составляет 0,01 Гц, 0,1 Гц, 0,01 Гц, 0,01 Гц и 0,5 Гц, а соответствующая постоянная времени составляет 100 с, 10 с, 100 с, 100 с и 2 с. Образец HOPC показывает наивысшую частоту символов и наименьшую постоянную времени, что указывает на самый быстрый отклик на выходную мощность.
Было продемонстрировано, что HOPC демонстрирует высокие электрохимические характеристики. Однако для практических применений тестирование трехэлектродной конфигурации не может выявить фактическую способность накопления энергии [33, 35]. Поэтому мы использовали образец ВОПК для изготовления электродов для сборки симметричных суперконденсаторов. На рис. 4в показаны ВАХ электрода из ВОФК. CV-профили имеют почти прямоугольную форму с хорошей симметрией при всех скоростях сканирования от 2 мВ с −1 до 100 мВ с −1 , что свидетельствует о хороших электрохимических свойствах и скоростной стабильности HOPC-электрода. Гальваностатические измерения заряда-разряда при постоянной плотности тока были также выполнены на симметричном суперконденсаторе в собранном виде, и результаты показаны на рис. 4d. Линейные зависимости напряжения от времени во время процесса заряда и разряда показывают идеальную треугольную форму с хорошей симметрией, что свидетельствует о выдающейся способности HOPC-электрода накапливать энергию. При плотности тока 0,5 А изб. −1 время разряда составляет 150 с, что соответствует удельной емкости около 289 Ф · г -1 . Удельная емкость HOPC из лигносульфоната при 10 А · г −1 все еще достигает 166 F g −1 , как показано на рис. 4e. Показатели HOPC в этом исследовании лучше, чем значения образцов углерода в литературе [3, 36,37,38,39].
Высокая удельная емкость HOPC обусловлена низким омическим сопротивлением и сопротивлением переносу заряда, которое составляет около 0,6 Ом · см −1 . и 2,4 Ом · см −1 соответственно, как показано на Рисунке S14. Фазовый угол симметричного суперконденсатора на самой низкой частоте 0,01 Гц составляет около 81,7 o (Рисунок S15), что очень близко к значению идеального суперконденсатора (90 o ). Частота символов составляет около 0,2 Гц, что соответствует постоянной времени 5 с. Это означает, что электрод HOPC обладает хорошей способностью передавать энергию. Поставляемая емкость достигает 290 мФ (Рисунок S16). На рисунке 4f показан график Рагона для симметричного суперконденсатора. Плотность энергии находится в диапазоне 40 Вт · ч · кг -1 . до 23 Вт · ч кг −1 с удельной мощностью около 0,9 кВт кг −1 до 20 кВт кг −1 .
Высокая удельная емкость и плотность энергии HOPC могут способствовать оптимизации структуры пор. Образец HOPC содержит большой объем пор как микропор, так и мезопор. Как показано в предыдущей литературе с помощью корреляционного анализа [40, 41], микропоры сильно связаны с накоплением энергии, а мезопоры сильно связаны с удержанием емкости, поскольку мезопоры в основном отвечают за перенос ионов. Также сделан вывод о том, что мезопоры вносят вклад в накопление заряда. Помните приведенную выше инструкцию, мы специально использовали метод твердой матрицы и химическую активацию для подготовки образца HOPC. Настоящие результаты не только дополнительно демонстрируют приведенные выше выводы, но также демонстрируют дизайн для изготовления высокоэффективных аккумуляторов энергии. Чтобы измерить циклируемость, симметричный суперконденсатор, использующий HOPC в качестве материала электрода, повторно заряжается и разряжается при 2 A g −1 на 3000 циклов (рисунок S17). Установлено, что после 3000 циклов удельная емкость составляет 218 Ф · г -1 . с небольшим уменьшением по сравнению с исходными 253 F g −1 с сохранением емкости 86,2%. Удельная емкость нашего образца HOPC из двухэлектродной системы выше и сопоставима после 3000 циклов со значениями, указанными в таблице S2. Таким образом, настоящее исследование предлагает потенциальный путь для разработки высокоэффективных электродно-активных материалов суперконденсаторов из промышленных отходов.
Заключение
В этом исследовании мы успешно подготовили заказанные мезопористые углеродные материалы с использованием лигносульфоната биоотходов в качестве источника углерода с использованием технологии литья в формы на основе шаблона KIT-6. During the mold casting process, lignosulphonate can easily be cast into the pores of KIT-6. The crosslinking reaction of lignosulphonate molecules not only increases the pore volume, but also bridges the aromatic rings to promote the graphitization. The as-synthesized ordered mesoporous carbons exhibit high electrical conductivity, high-specific surface area, and pore volume, which are highly dependent on the carbonization temperature. The results of Raman analysis and N2 adsorption/desorption experiments show that the OMC-900 sample has the best physical properties. The pore structure of OMC-900 was further optimized through ZnCl2 chemical activation to prepare HOPC. The specific capacitance of HOPC in the symmetric supercapacitor was about 289 F g −1 with the energy density as high as 40 Wh kg −1 . The present study indicates lignosulphonate is very suitable to prepare hierarchical ordered porous carbon at low cost with high-performance supercapacitors.
Доступность данных и материалов
All data generated or analyzed in this study are included in the manuscript and the supplementary information files. All the materials are available from the corresponding author on request.
Сокращения
- HOPC:
-
Hierarchical ordered porous carbon
- KIT-6:
-
The ordered mesoporous silica template
- OMC:
-
The ordered mesoporous carbon
- NMP:
-
N-methyl pyrrolidone
- PVDF:
-
Поливинилиденфторид
- Резюме:
-
Циклическая вольтамперометрия
- EIS:
-
Электрохимическая импедансная спектроскопия
- AC:
-
Переменный ток
Наноматериалы
- Графен и полимерные композиты для суперконденсаторов:обзор
- Волокна из активированного угля с иерархической наноструктурой, полученные из отработанных хлопчатобумажны…
- Простой синтез серебряных нанопроволок с разным соотношением сторон и используемых в качестве высокоэффект…
- Монодисперсные углеродные наносферы с иерархической пористой структурой в качестве материала электродов дл…
- Магнитные углеродные микросферы как многоразовый адсорбент для удаления сульфонамида из воды
- Простой подход к синтезу флуоресцентных квантовых точек углерода из сточных вод тофу
- Оценка структур графен / WO3 и графен / CeO x как электродов для применения в суперконденсаторах
- Аэрогель / серный композит с активированным углем с полианилиновым покрытием для высокопроизводительных лит…
- Синтез и характеристики суперконденсатора упорядоченных мезопористых углеродных композитов, легированных …
- Двумерные мезопористые микрочипы VO2 для высокопроизводительного суперконденсатора



