Влияние CTAB-покрытых семян и их времени старения на морфологию наночастиц серебра
Аннотация
В отличие от полидисперсных наностержней, образованных обычным методом опосредованного семенами роста без присутствия бромида цетилтриметиламмония (CTAB) в затравочном растворе, мы успешно получили наночастицы серебра с разной морфологией в одной и той же реакционной системе путем добавления CTAB в затравочный раствор. В этой работе в раствор добавляли соответствующее количество CTAB для получения затравочных кристаллов серебра. Результаты показывают, что время старения серебряных затравок имеет большое влияние на размеры и морфологию наночастиц серебра, и, таким образом, наночастиц серебра с контролируемой формой можно легко получить, просто изменив время старения затравки. Результаты также подтверждают, что селективную адсорбционную способность или адсорбционные свойства TSC можно регулировать путем добавления CTAB в процедуру приготовления серебряных затравок. Мы предполагаем, что разное время старения по-разному влияет на конкурентную адсорбцию между ЦТАБ и цитратом, чтобы вызвать ориентационный рост серебряных зародышей. В результате серебряные наносферы, наностержни и треугольные нанопластинки можно легко приготовить в одной и той же системе. Кроме того, мы преодолеваем временные ограничения на использование затравок, добавляя CTAB в затравочный раствор, и делаем синтез наночастиц серебра или других металлов с различной морфологией более простым и эффективным.
Фон
Наночастицы серебра (AgNP), наноструктура благородных металлов, всегда были горячей темой исследований на протяжении многих лет. Благодаря их поверхностному эффекту [1], квантовому размерному эффекту [2], макроскопическому квантовому туннельному эффекту [3] и другим уникальным свойствам AgNP успешно используются во многих областях [4]. Например, AgNP могут применяться в качестве противомикробных материалов [5,6,7], противораковых материалов [8], каталитических материалов [9, 10], материалов для обнаружения ДНК [11] и носителей для доставки лекарств [12]. Результаты исследований показывают, что на физические и химические свойства анизотропных наночастиц, таких как наностержни, нанопроволоки и нанопластинки, сильно влияют их размер [13] и морфология [14, 15]. Таким образом, исследование синтеза AgNP с контролируемым размером и морфологией в настоящее время является важным и сложным.
Первоначально наночастицы серебра были синтезированы различными способами, включая литографические, биологические, физические и химические методы [16,17,18]. Среди них метод мокрого химического восстановления выделяется, поскольку с его помощью легко получать однородные частицы и он подходит для применения в крупномасштабном производстве. Что касается развития мокрого химического синтеза, многие исследователи посвятили себя этому делу. Xia et al. использовали поливинилпирролидон (ПВП) в качестве реакционной среды и приготовили высококачественные нанопроволоки [19]. Группа Миркина впервые представила синтез треугольных наночастиц в жидкой фазе с помощью оптического излучения, а их эксперименты выяснили оптические характеристики нанопризм и нанопластин [20].
Опосредованный семенами метод удобен для контроля размера и морфологии полученных наночастиц [21,22,23]. В настоящее время он быстро развивается, и изучение механизма роста продолжается. Однако остается еще много неясных факторов, требующих решения. Мерфи и др. впервые представил метод, опосредованный семенами, в 2001 году [24], который оказал глубокое влияние на последовавших за ним исследователей. Как правило, рост анизотропных наночастиц происходил в присутствии бромида цетилтриметиламмония (ЦТАБ), и размер образующихся наностержней контролировался в коллоидном растворе. Однако большое количество сферических частиц, смешанных в продуктах, потребовало нескольких разделений, что привело к низкому выходу. Кроме того, в первоначальном методе, предложенном Мерфи, отмечалось, что семена следует использовать в ограниченный промежуток времени. Не существует хорошего решения для постоянного решения ограниченной по времени проблемы, и прогресс исследований метода, опосредованного семенами, все еще ограничен. Исследования показали, что семена, покрытые ЦТАБ, были использованы вместо затравок с цитратами для приготовления золотых наностержней, что значительно улучшило регулярность полученных частиц [25]. Результат показал, что CTAB играет решающую роль в росте затравочных кристаллов. Молекулы CTAB обладают высоким сродством к грани (110) и вызывают анизотропный рост семян. Это может быть основным фактором улучшения регулярности наночастиц.
Из-за высокой поверхностной энергии отдельные наночастицы обычно легко образуют агрегаты. Добавление специального защитного агента может сделать поверхность неактивной и предотвратить образование скоплений наночастиц. CTAB, популярное поверхностно-активное вещество, может образовывать мицеллы, когда его концентрация превышает критическую концентрацию мицелл (CMC). Кроме того, избирательная адсорбция ЦТАБ на поверхности вызывает ориентационный рост затравочных кристаллов.
В этой статье мы использовали улучшенный затравочный метод для синтеза наночастиц серебра с различной морфологией. При приготовлении затравочных кристаллов серебра мы добавляли определенную концентрацию CTAB для регулирования селективной адсорбции на поверхности затравочных кристаллов и, таким образом, вызывали анизотропный рост затравочных кристаллов. На основе этого метода мы приготовили наносферы, наностержни и нанопластинки в одной и той же системе, и единственным отличием было время старения затравок серебра. Кроме того, наши семена можно использовать с начала до 52 часов и более. В результате мы преодолеваем ограничения, связанные с затравками, и упрощаем и повышаем эффективность синтеза наночастиц серебра или других металлов с различной морфологией.
Методы
Чтобы исследовать влияние затравочных кристаллов, покрытых CTAB, и их время старения на морфологию наночастиц серебра, соответствующее количество CTAB было добавлено в раствор для получения затравочных кристаллов серебра. Затем из этих семян, выдержанных в разное время, были приготовлены AgNP с разной морфологией.
Материалы
Нитрат серебра (AgNO 3 ), борогидрид калия (KBH 4 ), гидроксид натрия (NaOH), тринатрийцитрат (TSC) и аскорбиновая кислота (V c ) все были аналитически чистыми (AR) и использовались без дополнительной очистки. Бромид цетилтриметиламмония (CTAB) был приобретен у AMRESCO LLC. Вода, использованная в экспериментах, подвергалась двойной дистилляции.
Инструменты
Гранулометрический состав семян серебра определяли с помощью Zetasizer Nano ZS90 (Malvern Instruments, Malvern, UK) в режиме динамического светорассеяния (DLS) для распределения частиц по размерам, снабженного лавинным фотодиодом для обнаружения сигнала. При измерении концентрацию посевного раствора разбавляли бидистиллированной водой до одной десятой. УФ-видимый спектрофотометр U-3900 зарегистрировал резонансное поглощение сформированных наночастиц серебра. Изображения, полученные с помощью просвечивающего электронного микроскопа (ПЭМ), были получены на просвечивающем электронном микроскопе JEM-1400.
Подготовка серебряных семян
0,2 мл 0,1 M CTAB, 0,5 мл 0,01 M AgNO 3 , и 0,5 мл 0,01 M TSC были добавлены в 19,0 мл дистиллированной воды по порядку. Затем 0,6 мл 0,01 М свежеприготовленного ледяного KBH 4 сразу же быстро добавляли в реакционный раствор. Затем реакционный раствор осторожно перемешивали. Лучше поддерживать реакционную систему при 28 ° C. Раствор стал ярко-желтым, что свидетельствует об образовании нанокристаллов серебра. Примерно через 10 мин раствор стал желто-зеленым. Разновременные нанокристаллы в этом растворе использовались в качестве затравки от начала до 52 ч и даже дольше. Напротив, семена были приготовлены путем добавления CTAB, но без добавления TSC, и другие условия были такими же, как в предыдущем случае.
Подготовка наночастиц серебра
В чистой и сухой конической колбе на 50 мл помещают 15,0 мл 0,1 М CTAB и 0,5 мл 0,01 М AgNO 3 . были добавлены. Затем в раствор смеси добавляли 0,25 мл затравочного коллозола, приготовленного и выдержанного в течение разного времени. Затем 1,0 мл 0,1 M V c и 3,0 мл 0,1 М NaOH, и раствор быстро и быстро перемешивали в течение 3 мин. Раствор становился темно-желтым, коричневато-красным и сине-черным, что соответствует времени старения семян. Для сравнения, цвет коллоидного раствора AgNPs был желтым и не изменялся со временем старения серебряных затравок, полученных путем добавления CTAB, но без добавления TSC.
Результаты и обсуждение
Формирование наночастиц серебра семенами в разное время старения
Серебряные наностержни имеют два типичных пика поглощения:поперечную плазмонную полосу (с центром на ~ 400 нм) и продольную плазмонную полосу [26, 27]. Треугольные наночастицы серебра имеют три характерных пика поглощения, обусловленных их дипольным плазмонным резонансом в плоскости, квадрупольным резонансом в плоскости и квадрупольным резонансом вне плоскости [20].
УФ-видимые спектры на рис. 5а показывают спектральное поглощение наночастиц серебра, генерируемых затравками при разном времени старения. По тенденции изменения спектра видно, что семена, выдержанные в течение разного времени, оказывают большое влияние на морфологию образующихся AgNP. Полученные наночастицы, приготовленные из свежих зародышей, имеют только одну основную плазмонную полосу при ~ 412 нм, что указывает на то, что сформированные наночастицы почти представляют собой наносферы. В то время как нанокристаллы, выдержанные в течение 10 минут, используются в качестве затравок, появляется новый, но небольшой пик поглощения при 480 нм, что указывает на начало образования наностержней серебра. Однако пик поглощения при ~ 412 нм выше, чем при ~ 480 нм, что, вероятно, вызвано большим количеством сферических наночастиц, смешанных в продукте. Затем, при использовании семян, выдержанных в течение 15 мин, пик на длине волны ~ 345 нм становится все более очевидным. При использовании семян, выдержанных более 15 минут, пиковая интенсивность при ~ 412 нм становится ниже, а максимальная длина волны поглощения ( λ макс ) имеет красное смещение, а пиковая интенсивность на ~ 500 нм становится выше. В то время как семена выдерживаются около 30 минут, можно увидеть типичное резонансное поглощение треугольных наночастиц в УФ-видимом спектре. Судя по тенденции к изменению спектра, пик поглощения с центром на ~ 412 нм непрерывно уменьшается, а пик с центром на ~ 500 нм постепенно повышается с очевидным красным смещением. При ~ 350 нм это сначала плечевой пик, а затем, наконец, небольшой пик. Эти спектральные явления означают, что морфология образующихся наночастиц значительно изменяется при использовании семян, выдержанных в течение первых 30 минут.
ПЭМ-изображения на рис. 1b, c и e показали морфологию полученных наночастиц, полученных при разном времени старения семян. ПЭМ-изображения серебряных наностержней и треугольных нанопластинок с меньшим увеличением, соответствующие рис. 1c, e, были представлены в дополнительном файле 1:рис. S4. Обнаружено, что полученные AgNP соответствуют выводам из вышеуказанного резонансного поглощения. Гистограммы распределения формы, показанные на рис. 1d и f, показывают, что морфология основных наночастиц меняется от наносфер к наностержням и треугольным нанопластинам, в то время как AgNP готовятся нашими затравками, которые выдерживаются в течение разного времени от 0 до 30 мин. В то время как использовались свежие семена (то есть семена не были выдержаны), коллоидный раствор серебра имел темно-желтый цвет (вставка на рис. 1b). Сформированные наночастицы, показанные на рис. 1б, в основном представляли собой наносферы серебра и около наносфер с av. диаметр около 41,0 ± 14,3 нм. Некоторые усеченные нанотреугольники также перемешивались в наносферах и около наносфер (гистограммы распределения формы AgNP не представлены).
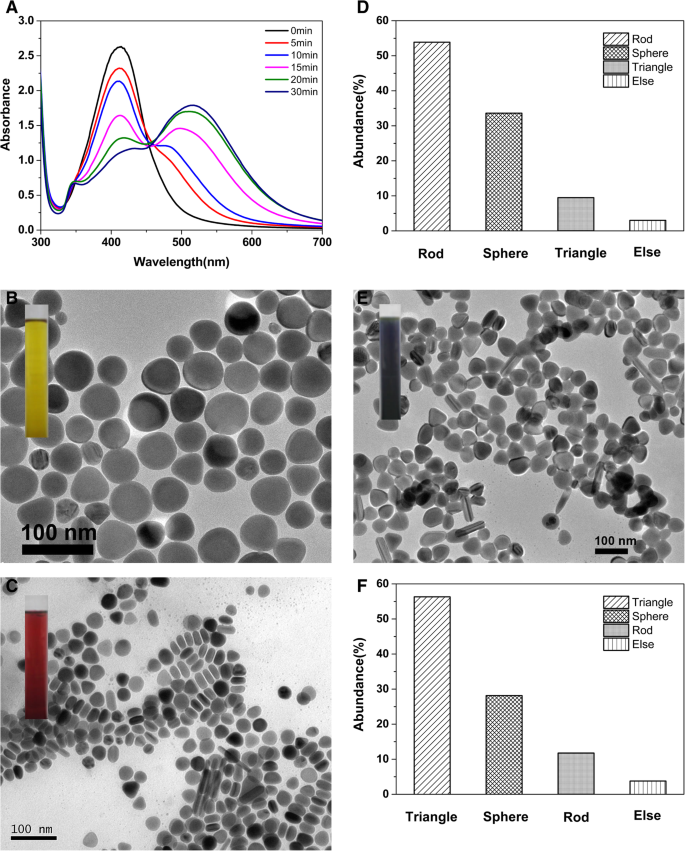
а УФ-видимые спектры наночастиц, полученные при разном времени старения затравки. б , c , e Электронно-микроскопические изображения наносфер серебра, приготовленных из семян, выдержанных в течение 0 мин, наностержней серебра, полученных из семян, выдержанных в течение 15 мин, и треугольных нанопластинок серебра, полученных из семян, выдержанных в течение 30 мин. г , f Гистограммы распределения формы AgNP, соответствующие изображениям ПЭМ c и е ; статистические числа частиц 279 и 308 соответственно
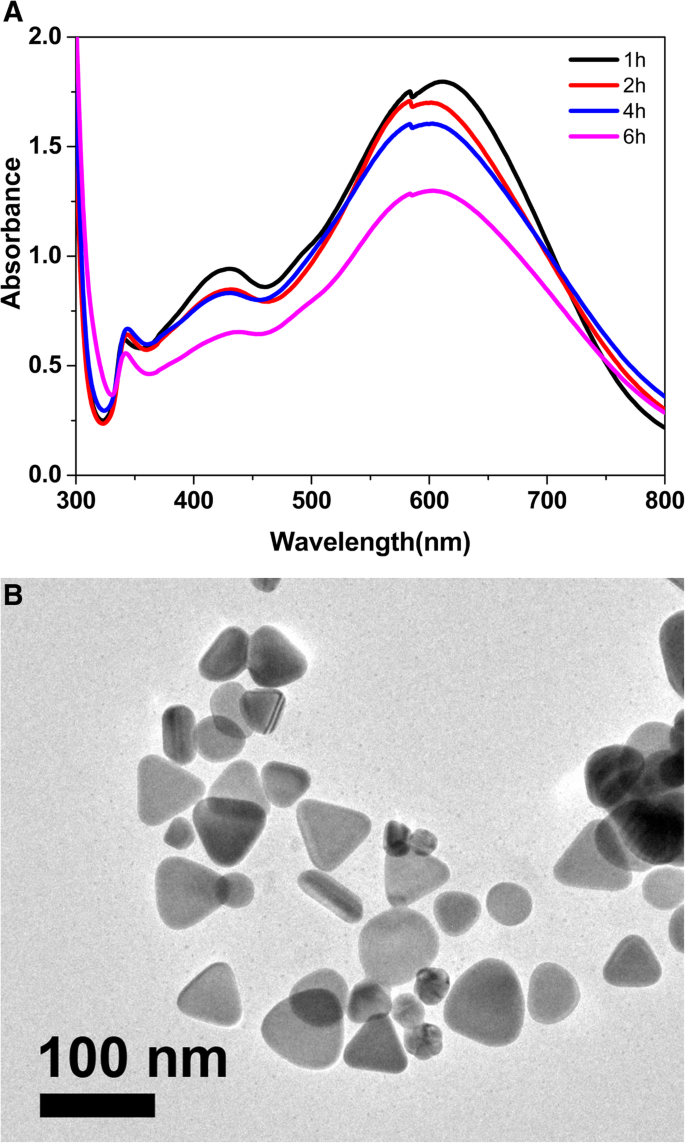
а УФ-видимые спектры полученных наночастиц, приготовленных из длительно выдержанных семян. б ПЭМ-изображение усеченных треугольных нанопластинок, приготовленных из семян, выдержанных в течение 6 ч
Когда семена были выдержаны в течение 15 минут, сформированные наночастицы, показанные на рис. 1c, были в основном серебряными наностержнями, а коллоидный раствор имел коричневато-красный цвет (изображение на вставке на рис. 1c). Кроме того, есть несколько сфероидальных и несколько треугольных наночастиц, которые появились как побочные продукты наностержней. Гистограммы распределения формы сформированных наночастиц Ag, показанные на рис. 1d, показывают, что количество наностержней серебра достигло примерно 53,9%, а количество основных ассоциированных наночастиц, то есть наносфер серебра, составляло примерно 33,6%. В то время как семена выдерживались в течение 30 минут, сформированные наночастицы, показанные на рис. 1e, в основном представляли собой треугольные нанопластинки, а коллоидный раствор серебра имел сине-черный цвет (вставленное изображение на рис. 1e). Полученные треугольные наночастицы имеют усеченную форму. На рис. 1f показано, что количество серебряных треугольных нанопластинок, наносфер и наностержней составляет примерно 56,3%, 28,2% и 11,8% соответственно.
Считалось, что семена должны выдерживаться в течение как минимум 2 часов после приготовления, а через 5 часов на поверхности затравочного раствора появлялась тонкая пленка наночастиц, указывающая на агрегацию нанокристаллов. Таким образом, семена можно было использовать через 2 часа, но нельзя было использовать через 5 часов после приготовления [24]. Что касается причины, по которой новые семена должны быть выдержаны в течение некоторого времени перед использованием, никаких дополнительных объяснений в их исследовании не приводится. Мы предполагаем, что затравочные кристаллы сформировались плохо, и сразу после приготовления затравок были дефекты кристаллов. Зародыши, выдержанные в течение подходящего времени (например, 2 ч), способствуют селективной адсорбции молекул поверхностно-активного вещества на специальной поверхности кристалла. Затравки, выдержанные в течение длительного времени (например, 5 часов), приводят к всесторонней адсорбции поверхностно-активных веществ на затравочных кристаллах и формированию полных кристаллических наночастиц, а также к агрегации затравочных нанокристаллов.
На рис. 2а представлены УФ-видимые спектры полученных наночастиц, полученных из семян, которые были выдержаны в течение длительного времени. Пики поглощения при ~ 600 нм, 420 нм и 350 нм явно не изменяются в длине волны максимального поглощения, но интенсивность поглощения уменьшается, что означает, что полученные нанопластинки уменьшаются с увеличением времени старения. На рис. 2б показано ПЭМ-изображение нанопластинок, приготовленных из семян, выдержанных 6 ч. Это указывает на то, что полученные наночастицы, приготовленные из затравок, которые долго состарены, представляют собой почти треугольные нанопластинки с av. длина стороны около 52,2 ± 10,3 нм. Полученные треугольные нанопластинки также имеют усеченную форму, и некоторые наносферы смешаны между собой из-за конкурентного роста между неадсорбированными и адсорбированными плоскостями решетки затравок серебра. В результате семена, полученные с помощью нашего улучшенного метода, опосредованного семенами, отличаются от опубликованных исследований, и наши семена можно использовать как в процессе подготовки, так и в течение довольно длительного времени путем добавления соответствующего CTAB в подготовку семян.
Как CTAB, добавленный в исходный раствор, влияет на формирование AgNP?
Цитрат тринатрия (TSC) является важным химическим веществом при приготовлении семян серебра для определения морфологии образующихся наночастиц [28]. Как ЦТАБ, добавленный в посевной раствор, влияет на образование AgNP? Что будет, если в процедуру посевов серебра добавить CTAB вместо TSC? Об этом не сообщалось в опубликованной литературе. Чтобы изучить влияние CTAB и TSC на процедуру приготовления серебряных семян, эксперименты по контрастированию были проведены с использованием серебряных семян с и без TSC в процедуре приготовления.
УФ-видимые спектры, показанные на фиг. 3, показали образование наночастиц серебра при использовании двух указанных выше затравок серебра (с добавлением или без добавления TSC) при разном времени старения. Очевидно, серебряные наносферы, наностержни и треугольные нанопластинки были сформированы затравками серебра, которые выдерживались в течение 0, 15, 30 мин в нашей реакционной системе (с добавлением как TSC, так и CTAB). Эти результаты хорошо согласуются с предыдущими экспериментальными исследованиями (раздел «Образование наночастиц серебра семенами при разном времени старения»). Напротив, цвет коллоидного раствора AgNPs был желтым и не изменялся с увеличением времени старения серебряных затравок (0 ~ 30 мин), когда TSC отсутствовали в процедуре приготовления. Кроме того, можно увидеть характерное поглощение (с центром на ~ 400 нм) серебряных наносфер в УФ-видимых спектрах, что указывает на то, что только серебряные наносферы были сформированы с использованием затравок серебра (с CTAB и без TSC), которые были состарены в течение 0, 15 и 30 мин. Приведенные выше экспериментальные результаты показали, что затравки, полученные простым добавлением CTAB, выросли до сферических наночастиц, что означает, что рост затравочных кристаллов был неселективным, то есть адсорбция молекул CTAB на кристаллических плоскостях затравочных кристаллов серебра не имеет селективности.
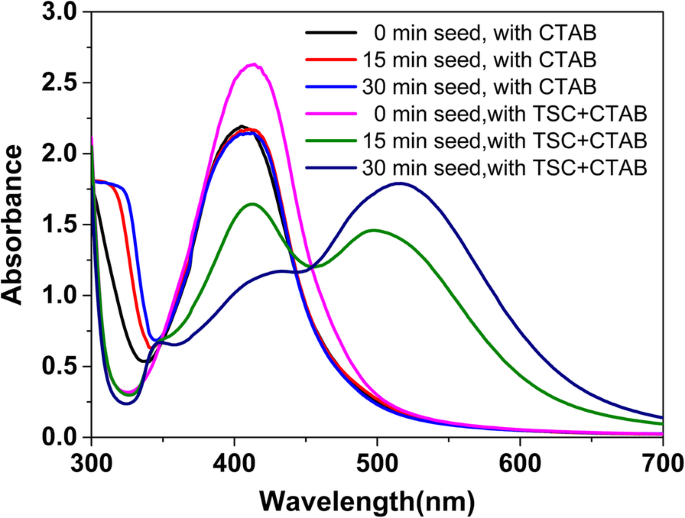
УФ-видимые спектры AgNP, полученных с использованием двух типов затравок серебра (с добавлением или без добавления TSC) при разном времени старения
Однако результаты подтверждают, что селективную адсорбционную способность или адсорбционные свойства TSC можно регулировать путем добавления CTAB в процедуру приготовления серебряных затравок (см. Наши экспериментальные результаты о добавлении TSC и CTAB на рис. 3). Кроме того, время старения коллозола семян имеет большое влияние на поведение селективной адсорбции, происходящее от новых семян в нашем случае. В результате морфологию и размер сформированных наночастиц можно контролировать следующими способами:(1) путем изменения времени старения серебряных затравок, полученных путем добавления как TSC, так и CTAB, и (2) путем регулирования добавления TSC и CTAB в процедуре посева семян серебра [29].
Очевидно, что влияние CTAB в затравочном растворе имеет большое значение для контроля морфологии и размера наночастиц. Здесь мы проводим теоретические расчеты и экспериментальные исследования, чтобы проверить влияние CTAB в затравочном растворе. При 30 ° C первая CMC CTAB составляет 0,72 мМ, а вторая CMC составляет 9,6 мМ. Если концентрация CTAB находится между первой и второй CMC, образующиеся мицеллы имеют сферическую форму. Хотя концентрация ЦТАБ выше, чем его вторая ККМ, мицеллы меняются от сферических до стержневидных [30]. В нашем эксперименте концентрация ЦТАБ в посевном растворе составляет 0,96 мМ. По-видимому, CTAB образует сферические мицеллы в затравочном растворе.
Теоретическим расчетом можно подтвердить, что реакция осаждения между Ag + и Br - доминирует в системе, что указывает на то, что большая часть Ag + реагирует с Br - вместо цитрата [29]. Это может замедлить процедуру восстановления и, таким образом, снизить концентрацию свободного Ag + . Образовавшийся AgBr быстро восстанавливается до Ag с добавлением KBH 4 . Затем большое количество атомов Ag поглощается сферическими мицеллами, избегая скопления среди миниатюрных наночастиц серебра. Однако осадки AgBr образуются в результате реакции между AgNO 3 и CTAB может разлагаться на свету. Образование затравок серебра или AgNP может происходить в результате конкуренции между разложением и восстановлением AgBr. Чтобы изучить конкуренцию разложения и восстановления, контрастная реакция для получения AgNP была проведена с добавлением и без добавления NaOH в систему (дополнительный файл 1:рисунок S1). Результаты показали, что реакционный раствор все еще представлял собой бесцветный прозрачный раствор, и в течение 60 минут не наблюдалось явных пиков поглощения, что означает, что осадок AgBr в этой системе не разлагался или скорость разложения AgBr была незначительной при свете.
Скорость восстановления ионов серебра в значительной степени контролируется кислотностью-основностью V c реакционный раствор [31]. Ионизация V c зависит от кислотности и основности раствора, а окислительно-восстановительный потенциал ионов серебра зависит от разницы в комплексообразующем действии между ионом серебра с моноанионом и дианионом V c . Для образования AgNPs путем добавления NaOH всего 3 мин потребовалось для проведения синтеза серебряных треугольных нанопластинок и наностержней или около наносфер. Напротив, ионы серебра не восстанавливаются на V c в растворе без NaOH. Для образования семян серебра путем добавления CTAB и TSC в нашу систему экспериментальные результаты аналогичны результатам, полученным в вышеупомянутых экспериментах (дополнительный файл 1:Рисунок S2). То есть осадок AgBr при получении как затравок серебра, так и AgNP не разлагается, или скорость разложения AgBr незначительна при естественном освещении в нашей системе. Стабильность фотодеградации AgBr должна происходить из осадка AgBr, закрытого мицеллами CTAB или адсорбированного CTAB и цитратом в нашей системе.
Для дальнейшего изучения решающей роли ЦТАБ мы приготовили два различных затравочных кристалла, используя 0,1 М NaBr и 0,1 М ЦТАБ, соответственно. Фиг.4 представляет собой УФ-видимые спектры наночастиц серебра, полученных из двух указанных выше затравок. Спектры AgNP (при использовании 0,1 М NaBr) явно не изменяются по длине волны максимального поглощения. Однако интенсивность его поглощения заметно снижается. Пик поглощения в направлении большей длины волны (с центром на ~ 600 нм) имеет меньшую оптическую интенсивность. Это означает, что образующиеся наночастицы полидисперсны в затравочном растворе. Связанные исследования показали, что Br - может прочно связываться с Ag + с образованием AgBr, подавляющего рост семян серебра [29, 32]. Согласно нашим экспериментальным результатам, это объясняет, что CTAB выполняет две основные функции в образовании затравок серебра, то есть связывание с серебром с образованием AgBr для уменьшения скорости восстановления Ag + и демонстрирует его избирательную адсорбцию в присутствии TSC, чтобы вызвать ориентационный рост серебряных затравок.
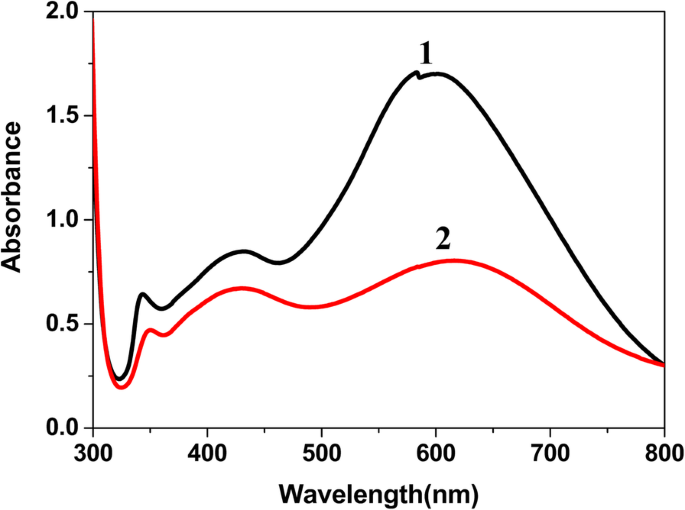
УФ-видимые спектры AgNP, полученных из двух разных семян, полученных с использованием 0,1 M CTAB (1) и 0,1 M NaBr (2) соответственно и выдержанных в течение того же времени (20 мин)
Что случилось с семенами в процессе их старения?
Некоторые исследователи предполагают, что старение влияет только на мелкие нанокристаллы [33]. Исследования, связанные со сроком выдержки семян, показали, что семена следует использовать в ограниченный промежуток времени после приготовления. В ходе исследования мы преодолеваем этот недостаток и можем производить различные наночастицы серебра в простой системе. Здесь мы пытаемся выяснить, что произошло с семенами в процессе их старения.
УФ-видимые спектры на рис. 5 показывают изменение поглощения затравочных кристаллов в период старения затравок от 0 до 6 часов. Только один главный плазмонный пик при ~ 400 нм указывает на то, что сформированные затравочные кристаллы представляют собой наносферы, которые имеют такую же морфологию, как и морфология затравок серебра, полученных только с помощью TSC [34]. Максимальные длины волн поглощения ( λ макс ) составляют 411, 410, 408, 409, 409, 408, 408 и 408 нм с соответствующим временем старения затравки 0, 10, 20, 30, 60, 120, 180 и 360 минут соответственно. От 0 до 20 минут λ макс имеет синий сдвиг 3 нм (как показано на рис. 5а). Через 20 минут λ макс почти не имеет изменений, но полная ширина на полувысоте (FWHM) резонансного поглощения затравочного коллозола постепенно уменьшается с возрастом (как показано на фиг. 5b). Полоса поглощения сужается с уменьшением FWHM, и мы можем предсказать увеличение размера частиц [35]. Из спектров на рис. 5b видно уменьшение интенсивности поглощения, которое может быть вызвано образованием тонкой пленки частиц, уменьшающей количество затравок серебра в коллоидном растворе. Результат согласуется с литературными данными [24]. Однако время выдержки не повлияло на использование посевного раствора в наших экспериментах, даже если посевной раствор выдерживался более 6 часов.
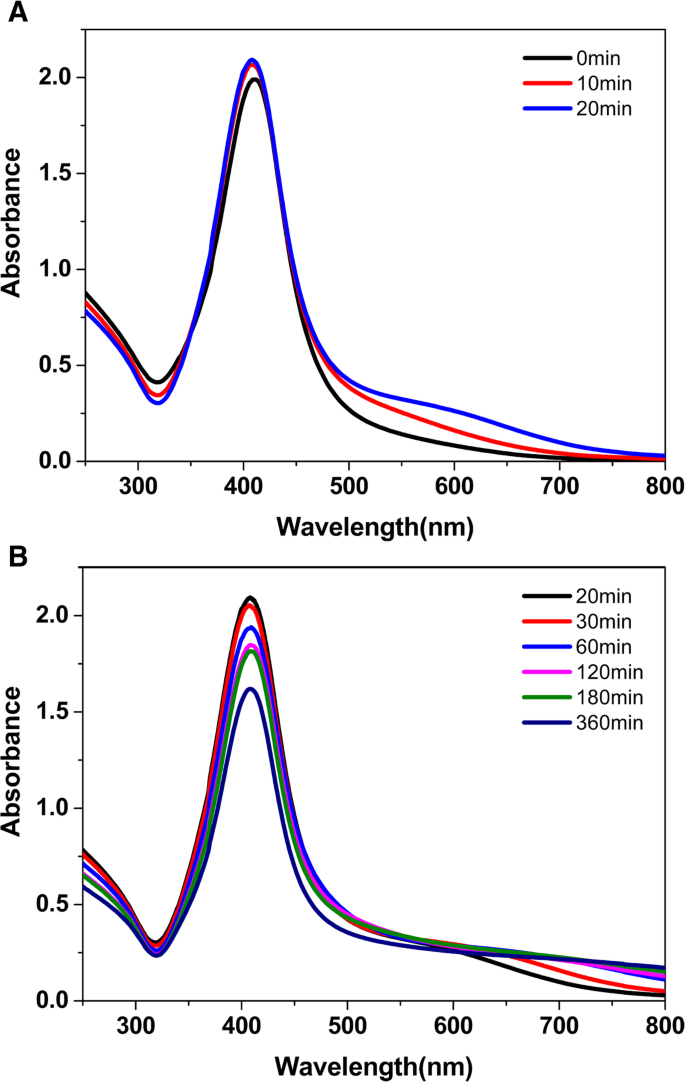
УФ-видимые спектры затравочных кристаллов, выдержанных от 0 до 6 ч, a 0–20 мин. б 20–360 мин.
Как показано на фиг. 5, поглощение затравочного раствора в продольном поверхностном плазмонном резонансе (более 600 нм) увеличивается со временем старения. Когда время старения семян составляет от 0 до 60 мин, поглощение на длине волны 600 нм постепенно увеличивается. Поскольку затравочный коллозол, полученный цитратом без ЦТАБ, почти не имеет поглощения более 600 нм [33], мы предполагаем, что появление при поглощении более 600 нм отражает изменение плотности заряда поверхностного состояния затравок. В нашей системе и TSC, и CTAB способны адсорбироваться на кристаллической поверхности затравок серебра. Из-за противоположных электрических свойств мы предположили, что плотность заряда в поверхностном состоянии изменяется со временем старения серебряных затравок за счет конкурентной селективной адсорбции ЦТАБ и цитрата на поверхности затравок. В результате наночастицы серебра с разной морфологией могут быть получены из семян, выдержанных в разное время. При 0 мин адсорбция отсутствует, и, следовательно, рост наночастиц серебра, приготовленных свежими затравками, не показывает анизотропии. В результате полученные наночастицы представляют собой наносферы и показывают типичное поглощение при ~ 410 нм. При коротком времени старения семян (например, 15 мин) конкурентная адсорбция цитрата семенами является доминирующей (поглощение более 600 нм является слабым). В этом случае анизотропный рост зародышей серебра происходил под управлением стержневидных мицеллярных темплатов, сформированных CTAB с образованием наностержней серебра. При длительном старении семян (например, более 30 мин) конкурентная адсорбция ЦТАБ является доминирующей (поглощение более 600 нм очевидно). Когда семена выдерживались более 60 минут, конкурентная адсорбция между цитратом и CTAB достигает баланса, а поглощение на длине более 600 нм имеет максимум и остается неизменным.
Хотя использовались свежие семена или семена, выдержанные в течение короткого времени, непрореагировавший BH 4 - в затравочном растворе может иметь некоторое влияние на образование AgNP. Как показано в Дополнительном файле 1:Рисунок S3, ясно, что изменение количества KBH 4 имеет небольшое влияние на образование семян серебра и AgNPs, приготовленных семенами. То есть непрореагировавший BH 4 - не является ключевым фактором для определения морфологии образующихся наночастиц. Подробные экспериментальные результаты и объяснение можно увидеть в разделе 2 Дополнительного файла.
На рис. 6 показано распределение гидродинамических диаметров затравок серебра при разном времени старения. Гидродинамический диаметр охарактеризован методом DLS. Как показано на рис. 6a, c и e, средние гидродинамические диаметры затравок серебра в процедуре старения через 5 мин, 30 мин и 120 мин составляют 3,77 ± 0,2 нм, 15,09 ± 0,2 нм и 17,54 ± 0,2 нм. Гидродинамический диаметр семян с течением времени становится все больше и больше. Соответствующие им изображения ПЭМ представлены на рис. 6. Очевидно, что затравочные кристаллы представляют собой все сферические наночастицы, и размер их частиц увеличивается со временем старения затравки. Как показано на рис. 6b, образовавшиеся затравочные кристаллы, которые состарились в течение 5 мин, очень малы и их средн. размер частиц составляет около 4,9 ± 1,6 нм, что примерно совпадает с гидродинамическим диаметром, полученным методом DLS. Рисунок 6d показал, что образовавшиеся затравочные кристаллы, которые состарились в течение 30 мин, представляли собой несколько более крупных сферических наночастиц с av. размер частиц 16,0 ± 3,0 нм. Хотя затравочный коллозол серебра выдерживался в течение более длительного времени, например 120 мин, между затравочными кристаллами наблюдалась степень агрегации, как показано на фиг. 6f. Размер небольшой части затравочных кристаллов увеличивается до более 20 нм, а их средн. размер частиц составляет около 16,9 ± 7,3 нм. Эти прямые данные показали тенденцию к увеличению размера частиц семян по мере их старения, что соответствовало результатам, полученным на основе гидродинамического диаметра и вывода из спектральных изменений в УФ-видимой области.
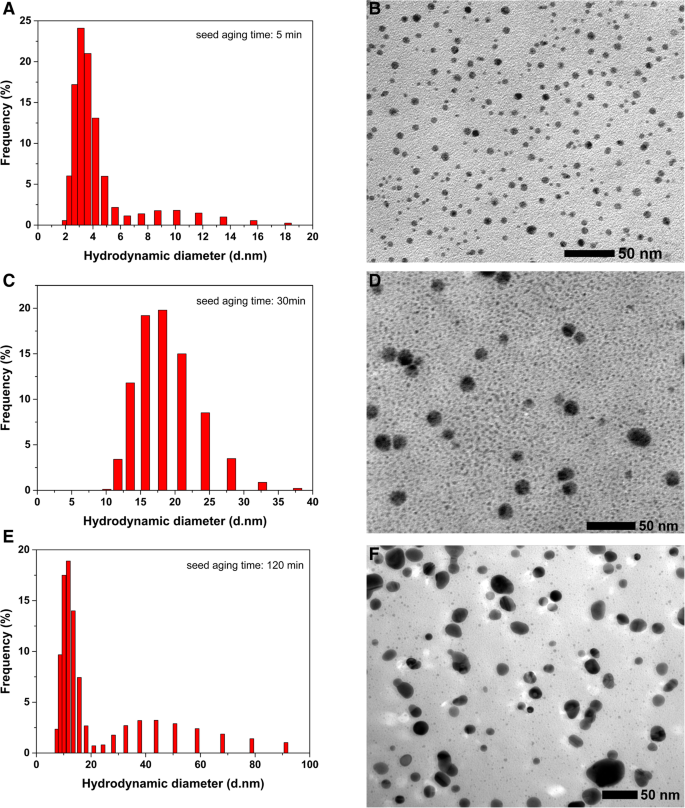
Распределение гидродинамических диаметров затравок серебра, охарактеризованных с помощью DLS и соответствующих изображений ПЭМ при разном времени старения: a , b 5 минут. c , d 30 минут. е , f 120 мин.
Сообщалось, что рост вершины треугольных наночастиц контролируется фасеткой (111), а латеральный рост контролируется фасеткой (100) [36]. Цитрат имеет предпочтительную адгезию к грани Ag (111) [37,38,39,40] и подавляет рост этой грани [41]. В нашем случае Br - полученный из CTAB был добавлен в затравочный раствор для образования AgBr с Ag + , что влияет на относительный рост фасетки (111, 100) затравок серебра. In addition, the competitive adsorption between citrate and CTAB achieves a balance on the seed surface to further adjust the relative growth ratio of the (111, 100) facet. As a result, the seeds can controllably grow to form truncated triangular nanoparticles. That is to say, we can obtain nanoparticles with different morphologies in the same reaction system by controlling the aging times of silver seeds.
Выводы
By using an improved seed-mediated method, we successfully obtained silver nanoparticles with different morphologies in the same reaction system. With the addition of CTAB in seed solution, we can achieve shape-controllable goal for silver nanoparticles by only simply changing the seed aging time. The seed collosol prepared by this method is very stable and can be used from 0 to 6 h and more. The seeds can be used immediately to form silver nanospheres. Silver nanorods and truncated triangular nanoplates can be prepared respectively by using the seeds aged for different times. The aging time of silver seeds is a key factor to form AgNPs with different morphologies.
Contrast to the polydisperse nanorods formed without the existence of CTAB in the seed solution, triangular nanoplates were easily prepared by the seeds added CTAB in moderation and aged for an appropriate time. The size of silver seeds nanocrystals increases with the aging time. We suggest that different aging times generate different effects on the competitive adsorption between CTAB and citrate. Thus, the nanospheres will be formed by the fresh seeds and the nanorods will be formed by the seeds aged for a shorter time (that is, the selective adsorption of citrate to the seeds is dominant). Similarly, triangular nanoplates can form by the seeds aged for a longer time (that is, the selective adsorption of citrate to the seeds is obviously adjusted by CTAB). These results imply that the adsorption balance of CTAB and citrate can affect the growth rate on different crystal faces to induce the orientation growth of silver seeds to form AgNPs with different morphologies, although the detailed mechanism is not that clear now.
Сокращения
- AgNPs:
-
Наночастицы серебра
- CMC:
-
Критическая концентрация мицелл
- CTAB:
-
Бромид цетилтриметиламмония
- DLS:
-
Динамическое рассеяние света
- FWHM:
-
Полная ширина на половине максимальной
- PVP:
-
Polyvinyl pyrrolidone
- ТЕМ:
-
Просвечивающий электронный микроскоп
- TSC:
-
Trisodium citrate
- Vc :
-
Ascorbic acid
- λmax :
-
Maximum absorption wavelength
Наноматериалы
- Разница между вольфрамовым серебряным сплавом и вольфрамово-медным сплавом
- The What, Why and How of Wrench Time
- В чем разница между AU и OEE?
- Получение наночастиц mPEG-ICA, нагруженных ICA, и их применение в лечении LPS-индуцированного повреждения клеток H9c2…
- Изучение in vitro влияния наночастиц Au на клеточные линии HT29 и SPEV
- Влияние воды на структуру и диэлектрические свойства микрокристаллической и наноцеллюлозы
- Настройка морфологии поверхности и свойств пленок ZnO путем создания межфазного слоя
- Влияние упругой жесткости и поверхностной адгезии на отскок наночастиц
- Последние достижения в синтетических методах и применении серебряных наноструктур
- Сапонины Platycodon из Platycodi Radix (Platycodon grandiflorum) для зеленого синтеза наночастиц золота и серебра



