Легкий синтез и повышенная фотокаталитическая активность в видимом свете новых композитов с гетеропереходом p-Ag3PO4 / n-BiFeO3 для деградации красителя
Аннотация
В этой работе Ag 3 ЗП 4 микрочастицы были декорированы на поверхности BiFeO 3 микрокубоидов методом осаждения с получением p-Ag 3 ЗП 4 / n-BiFeO 3 композиты с гетеропереходом. Композиты использовались для разложения кислого оранжевого 7 (АО7) под воздействием видимого света. Установлено, что композиты демонстрируют гораздо более высокую фотокаталитическую эффективность, чем чистый BiFeO 3 . Между тем, внутренняя фотокаталитическая активность Ag 3 , управляемая видимым светом, ЗП 4 / BiFeO 3 композиты были дополнительно подтверждены разложением фенола. Кроме того, была оценена каталитическая способность композита, подобная фотофентону. Анализ фототока показывает, что комбинация BiFeO 3 с Ag 3 ЗП 4 приводит к подавлению рекомбинации фотоиндуцированных электронов и дырок. Очевидное повышение фотокаталитической активности композита в основном приписывается эффективному фотогенерированному разделению зарядов и межфазной миграции заряда, вызванной образованием Ag 3 ЗП 4 / BiFeO 3 p-n гетеропереходы.
FormalPara PACS81.05.Hd82.65. + R82.50. – м
Фон
В последнее время фотокатализ полупроводников привлек большое внимание как многообещающая технология преобразования энергии и очистки от загрязнений [1,2,3]. Как известно, широко исследуемый фотокатализатор TiO 2 просто активен под воздействием ультрафиолетового (УФ) излучения, которое составляет только около 5% солнечного света и, таким образом, сильно ограничивает его фотокаталитическое применение под солнечным светом. Следовательно, необходимо разработать фотокатализаторы, работающие в видимом свете [4,5,6,7,8].
Полупроводниковые оксиды на основе висмута или железа обычно обладают умеренной шириной запрещенной зоны (~ 2,0 эВ) и считаются важным классом фотокатализаторов, чувствительных к видимому свету [9,10,11,12,13,14,15,16, 17,18,19]. Среди них BiFeO 3 со структурой типа перовскита проявляет интересные фотокаталитические характеристики для разложения красителя и расщепления воды при облучении видимым светом [20,21,22,23,24,25]. Однако его фотокаталитическая активность не впечатляет из-за высокой скорости рекомбинации фотогенерированных электронов (e - ) и дырки (h + ). К счастью, показано, что соединение BiFeO 3 с узкозонным полупроводником с согласованными краевыми потенциалами для формирования гетероперехода является одной из наиболее многообещающих стратегий, способствующих разделению фотогенерированных зарядов, что приводит к улучшенной фотокаталитической активности BiFeO 3 [26,27,28,29,30,31]. Например, Чайвичян и др. сообщил, что BiFeO 3 -Bi 2 WO 6 нанокомпозиты проявляют повышенную активность в деградации красителей [29]. Wang et al. заметил, что AgCl / Ag / BiFeO 3 показал гораздо более высокую фотокаталитическую активность в видимом свете, чем чистый BiFeO 3 [30]. Поклонник и его сотрудники обнаружили, что комбинация g-C 3 N 4 с BiFeO 3 очевидно может улучшить каталитическую активность по сравнению с чистым BiFeO 3 [31].
Ортофосфат серебра (Ag 3 ЗП 4 ), как превосходный фотокатализатор, работающий в видимом свете, привлек значительное внимание в области фотокаталитики [32,33,34,35,36,37]. Было показано, что Ag 3 ЗП 4 может достичь чрезвычайно высокого квантового выхода (~ 90%) для генерации кислорода при расщеплении воды [32, 33]. Кроме того, он обладает превосходной способностью к фотоокислению для разложения органических загрязнений благодаря своему положительному положению валентной зоны [34]. В большинстве случаев из-за подходящего положения энергетической зоны и узкой запрещенной зоны Ag 3 ЗП 4 широко используется в качестве сокатализатора для объединения с другими фотокатализаторами с образованием композитов, что приводит к очевидному улучшению фотокаталитических свойств, таких как Ag 3 ЗП 4 / Би 2 WO 6 , Ag 3 ЗП 4 / БиПО 4 , Ag 3 ЗП 4 / Би 2 О 2 CO 3 , Ag 3 ЗП 4 / g-C 3 N 4 , Ag 3 ЗП 4 / BiVO 4 , Bi 4 Ti 3 О 12 / Ag 3 ЗП 4 , Ag 3 ЗП 4 / ZnFe 2 О 4 , Ag 3 ЗП 4 / WO 3 , Ag 3 ЗП 4 / ZnO и Bi 2 МоО 6 / Ag 3 ЗП 4 [38,39,40,41,42,43,44,45,46,47]. Сообщается, что BiFeO 3 является полупроводником n-типа и Ag 3 ЗП 4 известен как полупроводник p-типа [43, 48]. Построение Ag 3 ЗП 4 / BiFeO 3 Композиты с p-n-гетеропереходом могут быть подходящим методом для получения эффективного фотокатализатора. Однако, насколько нам известно, исследованию фотокаталитических характеристик Ag 3 было посвящено мало работы. ЗП 4 / BiFeO 3 композиты.
В этой работе Ag 3 ЗП 4 / BiFeO 3 Композиты с p-n-гетеропереходом легко получали осаждением Ag 3 ЗП 4 микрочастицы на BiFeO 3 микрокубоиды. Кислотный оранжевый 7 (AO7) и фенол были выбраны в качестве модельного загрязнителя для оценки фотокаталитической активности композитов при облучении видимым светом. Кроме того, была исследована каталитическая активность композита по типу фотофентона. Обсужден основной механизм разложения органических загрязнителей, лежащий в основе композитов.
Методы
Подготовка Ag 3 ЗП 4 / BiFeO 3 Композиты
BiFeO 3 микрокубоиды были синтезированы гидротермальным путем. 0,005 моль Bi (NO 3 ) 3 • 5H 2 O и 0,005 моль Fe (NO 3 ) 3 • 9H 2 O растворяли в 20 мл разбавленного раствора азотной кислоты (5 мл HNO 3 + 15 мл деионизированной воды). Шестьдесят миллилитров раствора КОН с концентрацией 4,5 моль / л добавляли к вышеуказанному раствору по каплям при перемешивании магнитной мешалкой. После 8 минут ультразвуковой обработки и еще 30 минут интенсивного перемешивания магнитной мешалкой раствор смеси герметично закрывали в автоклаве из нержавеющей стали с тефлоновым покрытием емкостью 100 мл и подвергали гидротермальной реакции при 200 ° C в течение 6 часов. После естественного охлаждения автоклава до комнатной температуры осадок собирали центрифугированием, промывали деионизированной водой (два раза) и абсолютным этанолом (три раза), а затем сушили при 80 ° C в течение 12 часов с получением конечного BiFeO 3 продукт. Ag 3 ЗП 4 микрочастицы получали методом осаждения. Три миллимоля AgNO 3 растворяли в 30 мл деионизированной воды и 1 ммоль Na 3 ЗП 4 · 12ч 2 О добавляли в 30 мл деионизированной воды с помощью магнитной мешалки. После того как раствор стал гомогенным, последний раствор по каплям добавляли в первый при интенсивном перемешивании магнитной мешалкой в течение 7 часов. В ходе реакции цвет раствора изменился на желтый. Наконец, смесь центрифугировали для сбора осадка. Полученный осадок несколько раз промывали деионизированной водой, а затем сушили в вакуумном сушильном шкафу при 60 ° C в течение 8 ч.
Ag 3 ЗП 4 / BiFeO 3 композиты были синтезированы следующим образом:0,1 г BiFeO 3 микрокубоиды диспергировали в 30 мл деионизированной воды и затем обрабатывали ультразвуком в течение 2 часов. После этого определенное количество AgNO 3 растворяли в указанной выше суспензии. К этой смеси по каплям добавляли Na 3 определенной концентрации. ЗП 4 раствора (30 мл) при интенсивном перемешивании на магнитной мешалке в течение 7 часов. Полученные композиты разделяли центрифугированием, многократно промывали деионизированной водой и сушили в вакуумной печи при 60 ° C в течение 8 часов. Чтобы исследовать действие Ag 3 ЗП 4 На фотокаталитические свойства полученных композитов была изготовлена серия образцов с различным содержанием Ag 3 ЗП 4 массовые соотношения 5%, 10%, 20% и 40% и соответствующие образцы были обозначены как 5% масс. Ag 3 ЗП 4 / BiFeO 3 , 10 мас.% Ag 3 ЗП 4 / BiFeO 3 , 20 мас.% Ag 3 ЗП 4 / BiFeO 3 и 40 мас.% Ag 3 ЗП 4 / BiFeO 3 , соответственно. Для сравнения, композит, обозначенный как 20 мас.% Ag 3 ЗП 4 / BiFeO 3 -M был также получен прямым механическим смешиванием BiFeO 3 микрокубоиды и Ag 3 ЗП 4 микрочастицы, где Ag 3 ЗП 4 занимает в композите массовую долю 20%.
Фотоэлектрохимические измерения
Тест фототока проводился на электрохимической рабочей станции (CST 350) с трехэлектродной ячейкой, как описано в литературе [49]. В этой трехэлектродной системе платиновая фольга и стандартный каломельный электрод использовались в качестве противоэлектрода и электрода сравнения соответственно. Рабочий электрод был изготовлен следующим образом:15 мг фотокатализаторов, 0,75 мг сажи и 0,75 мг поливинилиденфторида (PVDF) были добавлены в 1-метил-2-пирролидион (NMP) для получения суспензии, которая затем была равномерно покрыта слоем 1,0 × 1,0 см 2 Стеклянный электрод из оксида олова, легированного фторидом. После этого электрод сушили при 60 ° C в течение 5 ч. В качестве источника видимого света использовалась лампа Xe мощностью 300 Вт с отсекающим фильтром на 420 нм. Фотоэлектрохимические измерения проводили в 0,1-М Na 2 SO 4 раствор электролита, и его значение pH составило ~ 5,3. Кривые фототока-времени (It) были измерены при фиксированном потенциале смещения 0,2 В. Испытание спектроскопии электрохимического импеданса (EIS) проводилось с использованием синусоидального импульса напряжения с амплитудой 5 мВ и в диапазоне частот от 10 −2 до 10 5 Гц.
Тест фотокаталитической активности
Фотокаталитическую активность образцов оценивали в отношении разложения AO7 и фенола при облучении видимым светом. Обычно начальная концентрация AO7 или фенола составляла 5 мг / л при загрузке катализатора 0,5 г / л. Измеренные значения pH раствора AO7 и фенола составили ~ 6,8 и ~ 6,2 соответственно. Перед освещением смесь перемешивали в темноте в течение 0.5 ч для достижения адсорбционно-десорбционного равновесия органической молекулы на поверхности катализаторов. Затем этот реакционный раствор подвергали воздействию ксеноновой лампы мощностью 300 Вт с фильтром, отсекающим 420 нм, и соответствующая интенсивность света составила ~ 50 мВт / см -2 . . Во время фотокаталитического эксперимента небольшое количество реакционного раствора собирали через заданные интервалы времени и затем центрифугировали для отделения катализаторов. Концентрацию АО7 или фенола определяли путем определения оптической плотности супернатанта при заданной длине волны (λ AO7 =484 нм и λ фенол =270 нм) с использованием спектрофотометра УФ-видимого диапазона. Чтобы оценить фотокаталитическую возможность повторного использования фотокатализаторов, был проведен эксперимент по переработке для разложения AO7. После завершения первого фотокаталитического испытания фотокатализаторы собирали центрифугированием, промывали дистиллированной водой и сушили. Собранные фотокатализаторы добавляли в свежий раствор красителя для следующего цикла фотокаталитического эксперимента. Чтобы исследовать способность фотокатализаторов к фото-фентоноподобному катализу, H 2 О 2 (5 ммоль / л) добавляли в реакционный раствор. Процедура фотофентоноподобного эксперимента была аналогична описанному выше фотокаталитическому процессу.
Характеристика
Фазовую чистоту образцов исследовали на рентгеновском дифрактометре (XRD, Bruker D8 Advanced) с использованием излучения Cu Kα. Морфологию образцов наблюдали с помощью автоэмиссионного сканирующего электронного микроскопа (SEM, JEOL JSM-6701F) и автоэмиссионного просвечивающего электронного микроскопа (TEM, JEOL JEM-2010). Состав образцов измерялся методом энергодисперсионной рентгеновской спектроскопии. Химическое состояние элемента было проверено с помощью рентгеновской фотоэлектронной спектроскопии (XPS, PHI-5702), где шкала энергии связи данных XPS была откалибрована по второстепенному пику C 1s при энергии связи 284,8 эВ. Спектры диффузного отражения продуктов в ультрафиолетовой и видимой (УФ-видимой) области были получены с использованием спектрофотометра УФ-видимой области (PERSEE TU-1901) с BaSO 4 в качестве справки. Спектры ФЛ образцов регистрировали на флуоресцентном спектрофотометре (SHIMADZU RF-6000) с длиной волны возбуждения ~ 350 нм.
Результаты и обсуждение
XRD-анализ
На рисунке 1 представлены дифрактограммы BiFeO 3 . , Ag 3 ЗП 4 , и Ag 3 ЗП 4 / BiFeO 3 композиты с разным содержанием Ag 3 ЗП 4 содержание. Для чистого BiFeO 3 образец, все дифракционные пики хорошо совпадают с ромбоэдрической структурой BiFeO 3 (Карточка PDF № 74-2016), а также для чистого Ag 3 ЗП 4 образец, дифракционные пики могут быть идеально проиндексированы до кубического Ag 3 ЗП 4 фаза (карточка PDF № 06-0505); это указывает на то, что BiFeO 3 высокой чистоты и Ag 3 ЗП 4 были успешно подготовлены. В случае композитов дифрактограммы могут быть отнесены к характерным дифракционным пикам BiFeO 3 и Ag 3 ЗП 4 , а дифракционные пики примеси на картинах не появляются. Более того, видно, что при увеличении содержания Ag 3 ЗП 4 , интенсивность характеристических пиков Ag 3 ЗП 4 постепенно увеличивается. Результаты показывают, что композиты состоят из ромбоэдрического BiFeO 3 и кубический Ag 3 ЗП 4 , и никакая другая фаза не создается во время подготовки композитов.
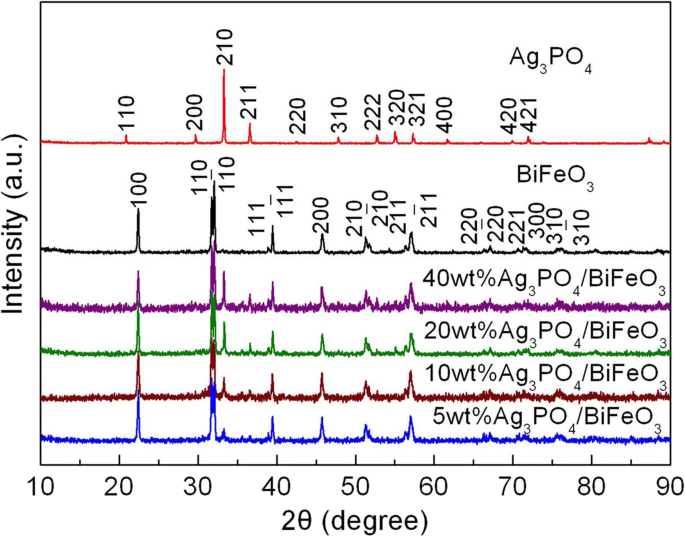
Рентгенограммы BiFeO 3 , Ag 3 ЗП 4 , и Ag 3 ЗП 4 / BiFeO 3 композиты
Наблюдение за морфологией
Морфологию образцов наблюдали с помощью SEM и TEM. На рис. 2а, б показаны СЭМ-изображение и ПЭМ-изображение чистого BiFeO 3 . , обнаружив, что подготовленный BiFeO 3 частицы имеют кубовидную форму размером 200–500 нм и гладкую поверхность. На вставке к рис. 2а показано распределение отношения длины к ширине BiFeO 3 . частиц, что показывает, что отношение длины к ширине колеблется от 1,1 / 1 до 2,5 / 1. Как видно из ПЭМ-изображения на рис. 2в, чистый Ag 3 ЗП 4 состоит из неправильных сферических частиц. Распределение по размерам Ag 3 ЗП 4 Размер частиц показан на вставке к рис. 2с, что указывает на широкое распределение частиц по размеру от 110 до 180 нм. Из изображения ПЭМ 20 мас.% Ag 3 ЗП 4 / BiFeO 3 Из композита (рис. 2г) видно, что микросферы неправильной формы прикреплены к частице кубовидной формы. Изображения ПЭМ высокого разрешения (ПЭМВР), полученные от различных частиц, показывают два различных набора полос решетки (вставки на рис. 2d). Межплоскостное расстояние ~ 0,288 нм соответствует BiFeO 3 (110), а межплоскостное расстояние ~ 0,267 нм соответствует Ag 3 ЗП 4 (210) самолеты. Кроме того, EDX-анализ показывает, что композит включает в себя все элементы Ag 3 ЗП 4 и BiFeO 3 фазы (рис. 2д). Наблюдаемые сигналы C и Cu в спектре EDX на рис. 2e могут возникать из микросети, используемой для поддержки образца [50]. Эти результаты показывают, что Ag 3 ЗП 4 частицы декорируются на поверхности BiFeO 3 микрокубоидов, в результате чего образуется Ag 3 ЗП 4 / BiFeO 3 p-n гетероструктуры.

а SEM (на вставке показано распределение отношения длины к ширине BiFeO 3 микрокубоиды) и b ПЭМ изображение BiFeO 3 микрокубоиды. ТЕМ-изображение c Ag 3 ЗП 4 микрочастицы (на вставке распределение Ag 3 по размерам ЗП 4 микрочастицы) и d 20 мас.% Ag 3 ЗП 4 / BiFeO 3 образец; на вставке - его изображение ВРЭМ. е EDX-спектр 20 мас.% Ag 3 ЗП 4 / BiFeO 3 образец
Анализ XPS
XPS-анализ был проведен для выявления химического состояния BiFeO 3 и 20 мас.% Ag 3 ЗП 4 / BiFeO 3 , как показано на рис. 3. На рис. 3а показан XPS-спектр Ag 3d в композите с высоким разрешением. Два очевидных пика при 373,8 и 367,7 эВ относятся к Ag 3d 3/2 и Ag 3d 5/2 энергии связи Ag + . На рис. 3б представлен XPS-спектр P 2p композита высокого разрешения. Пик около 133,2 эВ соответствует характерной энергии связи P 5+ степень окисления в Ag 3 ЗП 4 [51]. На рис. 3c, d показаны XPS-спектры высокого разрешения Bi 4f и Fe 2p соответственно. Для чистого BiFeO 3 , спектр Bi 4f показывает два сильных пика при энергиях связи 164,1 и 158,8 эВ, принадлежащих Bi 4f 5/2 и Би 4ф 7/2 соответственно, что указывает на то, что ион Bi имеет степень окисления +3. Для спектра Fe 2p пик, расположенный при 723,7 эВ, соответствует Fe 2p 1/2 Fe 3+ . Другой сильный сигнал XPS при ~ 711,6 эВ может быть уложен в два пика при 711,7 и 709,9 эВ. Пик при 709,9 эВ соответствует энергии связи Fe 2p 3/2 Fe 2+ . Энергия связи при 711,7 эВ принадлежит Fe 2p 3/2 Fe 3+ . Кроме того, сателлитный пик находится около 718,2 эВ, что связано со смешанными степенями окисления Fe. Из анализа XPS элемента Fe можно видеть, что Fe существует в форме Fe 3+ и Fe 2+ в голом BiFeO 3 . Стоит отметить, что энергии связи Bi 4f и Fe 2p в 20 мас.% Ag 3 ЗП 4 / BiFeO 3 демонстрируют небольшой сдвиг по сравнению с чистым BiFeO 3 , что в основном связано с взаимодействием BiFeO 3 и Ag 3 ЗП 4 . На рис. 3e показаны XPS-спектры высокого разрешения O 1s BiFeO 3 . и 20 мас.% Ag 3 ЗП 4 / BiFeO 3 . Для чистого BiFeO 3 сигнал O 1s можно разделить на два пика при 529,8 и 531,0 эВ. Энергия связи 529,8 эВ соответствует решеточному кислороду, в то время как небольшой пик при более высокой энергии связи 531,0 эВ вызван поверхностными дефектами и хемосорбированными формами кислорода. По сравнению с голым BiFeO 3 пик O 1s в композите претерпевает сдвиг, что также связано с взаимодействием между Ag 3 ЗП 4 и BiFeO 3 .
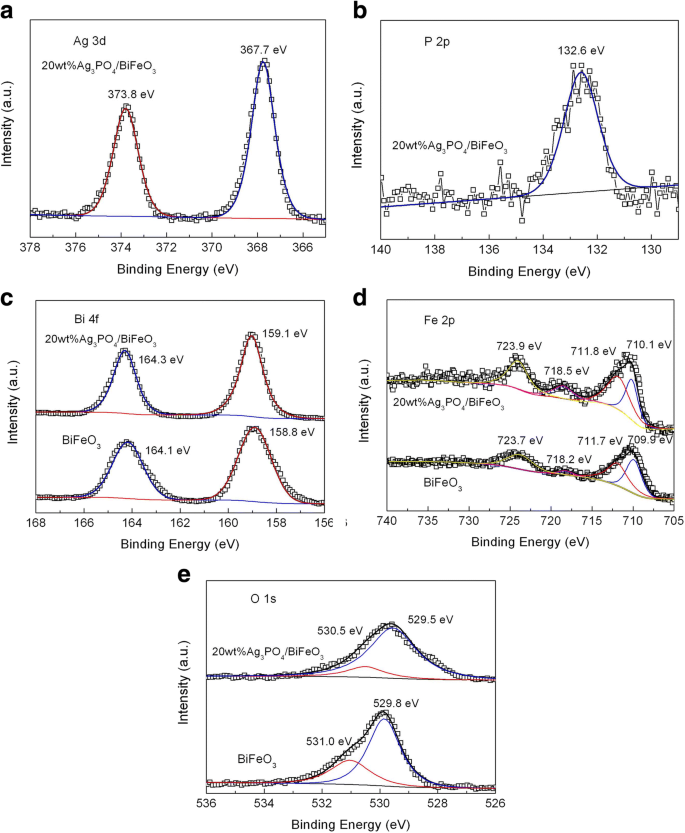
XPS-спектры высокого разрешения BiFeO 3 и 20 мас.% Ag 3 ЗП 4 / BiFeO 3 образец. а Ag 3d и b P 2p 20 мас.% Ag 3 ЗП 4 / BiFeO 3 образец. c Bi 4f, d Fe 2p и e O1s BiFeO 3 и 20 мас.% Ag 3 ЗП 4 / BiFeO 3 образец
Свойство оптического поглощения
Поведение образцов при оптическом поглощении исследовали путем измерения их спектров диффузного отражения в УФ-видимой области, как показано на рис. 4а. Соответствующие спектры поглощения, преобразованные из спектров диффузного отражения в соответствии с теорией Кубелки-Мунка (К-М), показаны на рис. 4b [52]. Видно, что все образцы демонстрируют значительное поглощение света при λ <600 нм. Чтобы получить край поглощения образцов, была проведена первая производная коэффициента отражения (R) по длине волны λ (т.е. dR / dλ), как показано на фиг. 4c. Край поглощения можно определить по длине волны пика в производных спектрах [53]. Видно, что край поглощения света оголенного Ag 3 ЗП 4 расположен на ~ 527 нм, что соответствует запрещенной энергии ( E g ) ~ 2.35 эВ. Голый BiFeO 3 имеет край поглощения около 567 нм, что соответствует E g ~ 2,18 эВ. Помимо края поглощения наблюдается слабый пик при ~ 700 нм, который, вероятно, объясняется существованием поверхностных состояний в середине запрещенной зоны BiFeO 3 . В сочетании с Ag 3 ЗП 4 край поглощения BiFeO 3 не претерпевает очевидных изменений, что указывает на то, что введение Ag 3 ЗП 4 не оказывает видимого влияния на структуру запрещенной зоны BiFeO 3 .
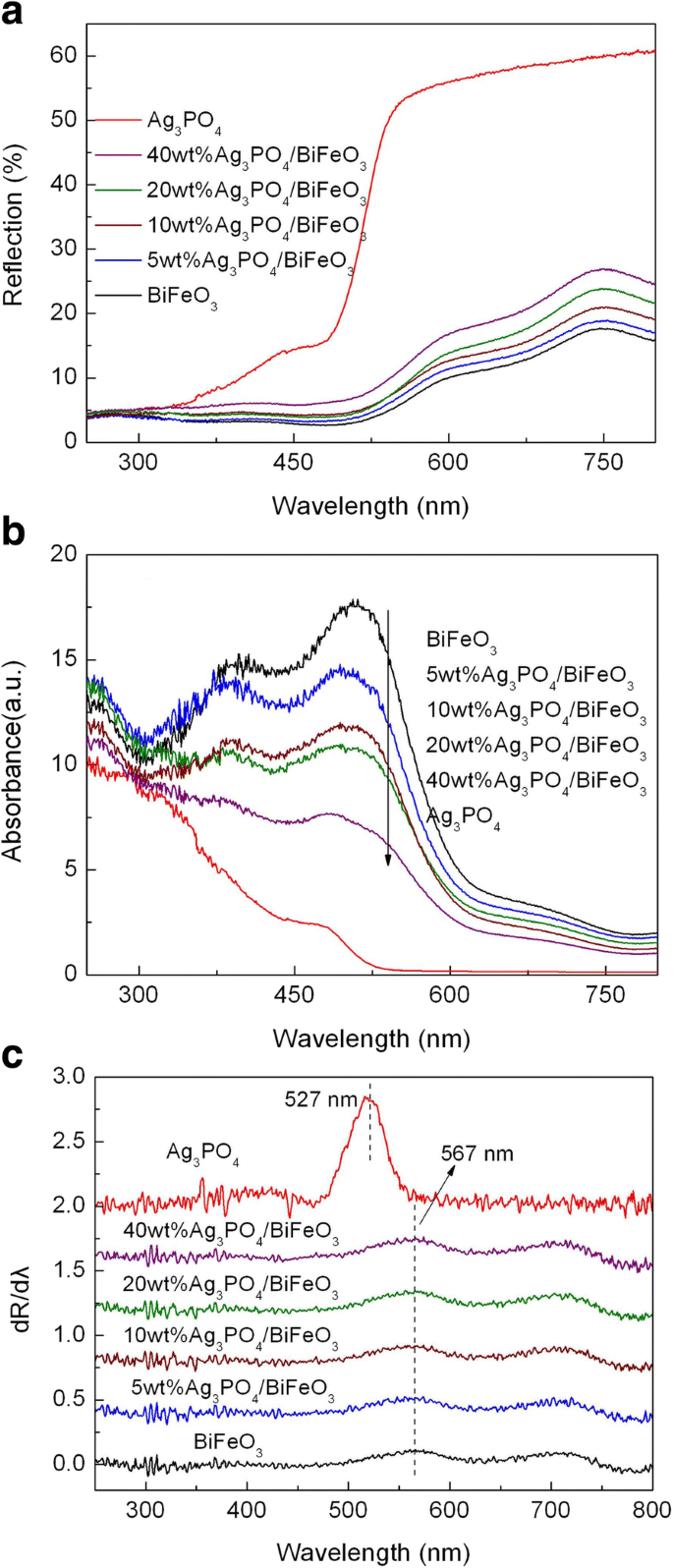
а УФ-видимые спектры диффузного отражения BiFeO 3 , Ag 3 ЗП 4 , и Ag 3 ЗП 4 / BiFeO 3 композиты. б Соответствующие спектры поглощения и c соответствующая первая производная спектров диффузного отражения
Измерение фотокаталитической активности
AO7 был выбран в качестве целевого загрязнителя для оценки фотокаталитических характеристик образцов. Фотокаталитическое разложение AO7 исследовали при облучении видимым светом, и результат показан на рис. 5. Перед фотокаталитической реакцией были проведены холостой эксперименты и эксперименты по поглощению. Видно, что не обнаруживается явной деградации красителя при облучении без катализаторов или в присутствии катализаторов без облучения, что позволяет предположить, что саморазложение и абсорбция AO7 во время фотокаталитического процесса незначительны. Голый BiFeO 3 имеет слабую фотокаталитическую активность, и только ~ 27% АО7 разлагается за 120 мин облучения. Когда BiFeO 3 микрокубоиды сочетаются с Ag 3 ЗП 4 микрочастицы, образующиеся Ag 3 ЗП 4 / BiFeO 3 композиты демонстрируют лучшую фотокаталитическую активность, чем чистый BiFeO 3 . После 120 минут воздействия процент разложения АО7 в образцах составляет порядка 40 мас.% Ag 3 ЗП 4 / BiFeO 3 (~ 91%)> 20 мас.% Ag 3 ЗП 4 / BiFeO 3 (~ 87%)> 10 мас.% Ag 3 ЗП 4 / BiFeO 3 (~ 69%)> 5 мас.% Ag 3 ЗП 4 / BiFeO 3 (~ 46%)> BiFeO 3 (~ 27%). Обнаружено, что фотокаталитические характеристики композитов имеют тенденцию к увеличению с увеличением содержания Ag 3 ЗП 4 содержание. Среди этих композитов фотокаталитическая эффективность 40 мас.% Ag 3 ЗП 4 / BiFeO 3 очень близок к 20 мас.% Ag 3 ЗП 4 / BiFeO 3 . Таким образом, в настоящем исследовании наиболее подходящее массовое соотношение Ag 3 ЗП 4 можно рассматривать как 20% в композитах. Кроме того, стоит отметить, что образец механической смеси 20 мас.% Ag 3 ЗП 4 / BiFeO 3 -M проявляет гораздо более низкую фотокаталитическую активность, чем 20 мас.% Ag 3 ЗП 4 / BiFeO 3 . Это показывает, что построение гетероперехода между BiFeO 3 и Ag 3 ЗП 4 необходим для повышения фотокаталитической активности. Более того, по сравнению с BiFeO 3 / a-Fe 2 О 3 и BiFeO 3 -Bi 2 WO 6 композиты [26, 29], Ag 3 ЗП 4 / BiFeO 3 композиты с гетеропереходом, полученные в настоящем исследовании, проявляют более высокую фотокаталитическую активность в отношении разложения красителя.
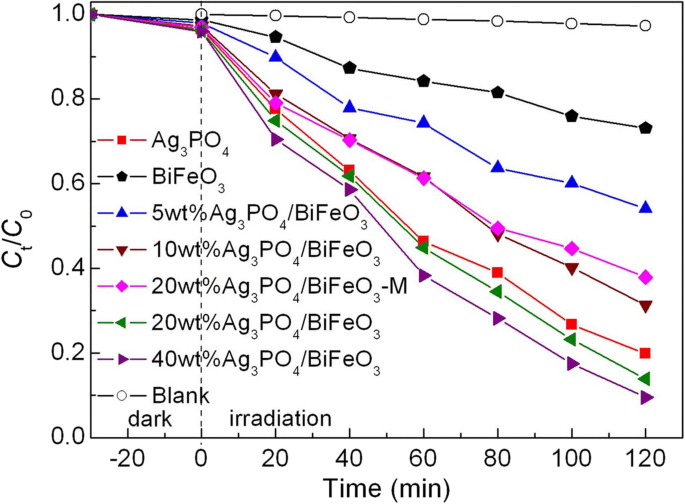
Фотокаталитическая активность BiFeO 3 и Ag 3 ЗП 4 / BiFeO 3 композитов в сторону разложения AO7 под воздействием видимого света, а также результаты холостого опыта и экспериментов по поглощению
Чтобы дополнительно подтвердить фотокаталитические свойства композитов, фотокаталитическое разложение бесцветного фенола более 20 мас.% Ag 3 ЗП 4 / BiFeO 3 и BiFeO 3 при облучении видимым светом. Как показано на фиг. 6, саморазложением и абсорбцией фенола можно пренебречь на основании результатов холостых экспериментов и экспериментов по абсорбции. Видно, что только ~ 9% фенола разлагается при катализе BiFeO 3 после 120 мин воздействия. В то время как при 20 мас.% Ag 3 ЗП 4 / BiFeO 3 используется в качестве фотокатализатора, очевидно, что при тех же условиях процент разложения фенола может быть увеличен. Результат предполагает, что разложение красителя на облученном видимым светом Ag 3 ЗП 4 / BiFeO 3 композиты объясняются их внутренней фотокаталитической активностью, а не сенсибилизацией красителем.
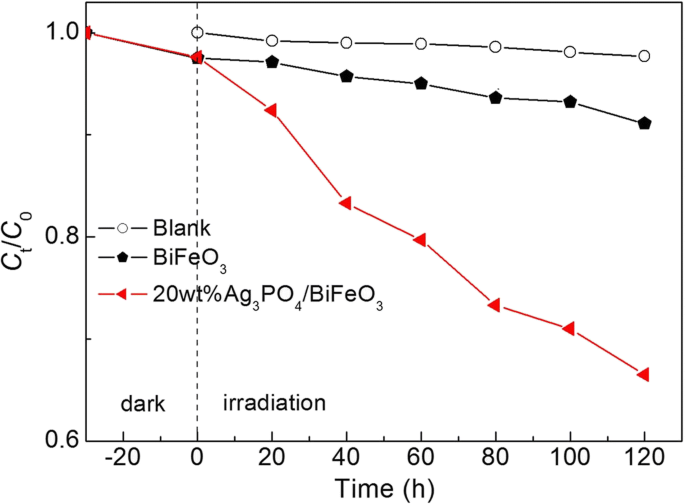
Фотокаталитическая деструкция фенола над BiFeO 3 и 20 мас.% Ag 3 ЗП 4 / BiFeO 3 образец под облучением видимым светом, а также результат холостого опыта и результатов эксперимента по поглощению
Чтобы оценить возможность повторного использования фотокатализаторов, эксперименты по переработке фотокаталитического разложения AO7 более 20% масс. Ag 3 ЗП 4 / BiFeO 3 и Ag 3 ЗП 4 проводились в тех же фотокаталитических условиях. Как показано на рис. 7, после трех последовательных циклов рециркуляции композит все еще проявляет относительно высокую фотокаталитическую активность, в то время как эффективность разложения по сравнению с Ag 3 ЗП 4 претерпевает явное снижение. На рис. 8a, b показаны ПЭМ-изображение и рентгенограмма композита после циклического эксперимента, соответственно. Понятно, что Ag 3 ЗП 4 микрочастицы все еще собираются на поверхности BiFeO 3 микрокубоидов без разрушения гетероструктур и явного изменения кристаллической структуры не наблюдается. Это говорит о том, что Ag 3 ЗП 4 / BiFeO 3 Композиты с p-n-гетеропереходом обладают хорошей фотокаталитической возможностью многократного использования.
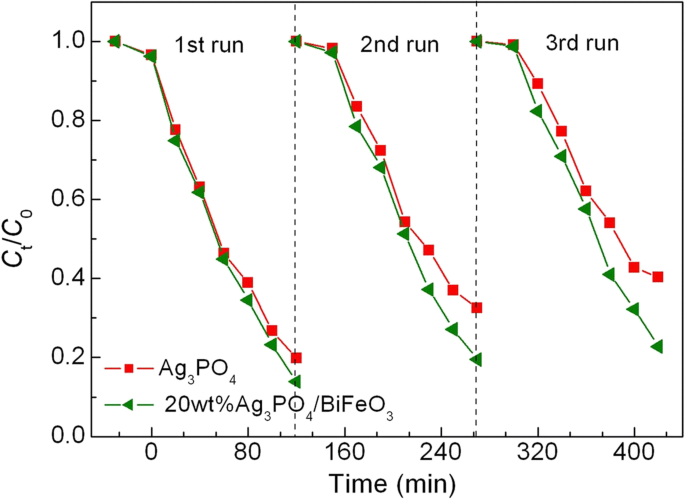
Фотокаталитическое разложение AO7 над Ag 3 ЗП 4 и 20 мас.% Ag 3 ЗП 4 / BiFeO 3 образец за три цикла
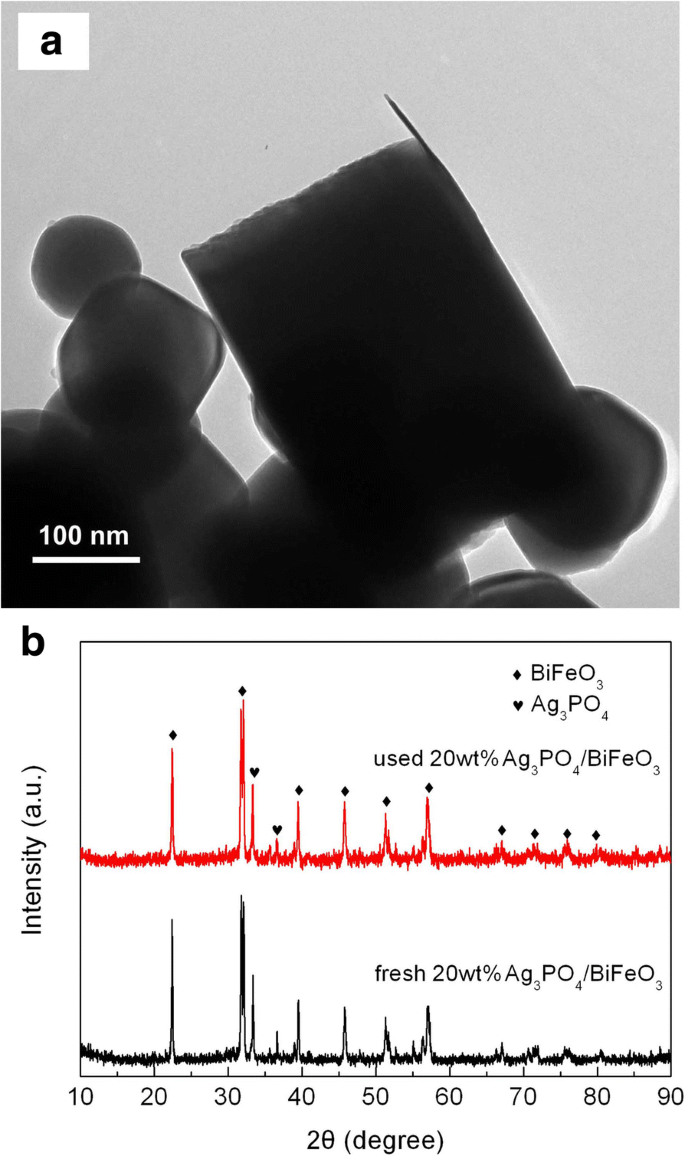
а Изображение TEM и b Диаграмма XRD 20 мас.% Ag 3 ЗП 4 / BiFeO 3 образец после циклических фотокаталитических экспериментов
Каталитическая активность, подобная фотофентону
Помимо своих фотокаталитических свойств, BiFeO 3 также проявляет заметную способность к фото-фентоноподобному катализу [54,55,56]. На рисунке 9 показано фото-фентоновское разложение AO7 при содержании Ag 3 на 20 мас.%. ЗП 4 / BiFeO 3 и BiFeO 3 в присутствии H 2 О 2 . По сравнению с реакционными системами без H 2 О 2 , введение H 2 О 2 заметно увеличивает процент деградации красителя. Этот результат в основном связан с механизмом фотофентоноподобной реакции. В присутствии излучения видимого света и H 2 О 2 , Fe 3+ на поверхности BiFeO 3 можно преобразовать в Fe 2+ с образованием гидроксильных (• OH) радикалов (уравнение 1). Следовательно, Fe 2+ может реагировать с H 2 О 2 для производства Fe 3+ и • OH (уравнение 2). Во время указанной выше циклической реакции образуется больше • ОН, который обычно считается первичным активным веществом для разложения красителя (о чем свидетельствует эксперимент по улавливанию активных частиц, приведенный на рис. 11). В случае голого BiFeO 3 , высокая скорость рекомбинации фотогенерированных зарядов ограничивает выход фотогенерированных электронов, что имеет тенденцию подавлять восстановление Fe 3+ в Fe 2+ (Уравнение 3). Это приводит к ограниченному увеличению процента деградации. Для Ag 3 ЗП 4 / BiFeO 3 композиты, фотогенерированные электроны и дырки могут быть эффективно разделены, и, таким образом, больше фотогенерированных электронов доступно для содействия быстрому преобразованию из Fe 3+ в Fe 2+ (Уравнение 3) [57]. Благодаря этому электронному восстановлению фото-фентоновский процесс для композитов более эффективен, чем для чистого BiFeO 3 . В результате Ag 3 ЗП 4 / BiFeO 3 Композиты с p-n-гетеропереходом демонстрируют значительно улучшенные характеристики фото-Фентона.
$$ {\ mathrm {Fe}} ^ {3 +} + {\ mathrm {H}} _ 2 \ mathrm {O} + \ mathrm {h} \ upnu \ to {\ mathrm {Fe}} ^ {2+} + \ bullet \ mathrm {OH} + {\ mathrm {H}} ^ {+} $$ (1) $$ {\ mathrm {Fe}} ^ {2 +} + {\ mathrm {H}} _ 2 {\ mathrm {O}} _ 2 \ to {\ mathrm {Fe}} ^ {3 +} + \ bullet \ mathrm {OH} + {\ mathrm {O} \ mathrm {H}} ^ {-} $$ (2) $$ {\ mathrm {Fe}} ^ {3 +} + {\ mathrm {e}} ^ {-} \ to {\ mathrm {Fe}} ^ {2+} $$ (3)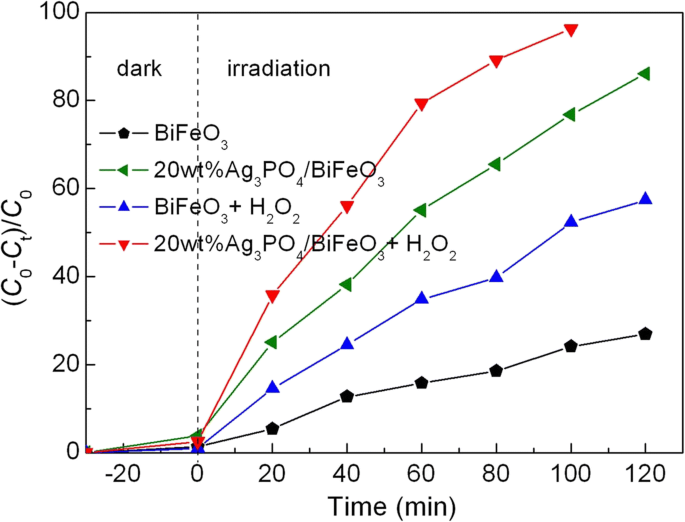
Фотокаталитическая активность BiFeO 3 и 20 мас.% Ag 3 ЗП 4 / BiFeO 3 образец в сторону разложения AO7 при облучении видимым светом в присутствии H 2 О 2
Эффективность фотогенерации заряда
Для оценки поведения разделения фотогенерированных зарядов образцов, переходных откликов фототока, спектров ESI и спектров ФЛ BiFeO 3 и 20 мас.% Ag 3 ЗП 4 / BiFeO 3 были измерены. На рисунке 10а показаны кривые фототока-времени (I-t) фотокатализаторов при прерывистом облучении видимым светом с несколькими циклами включения-выключения. Видно, что величина фототока композита намного выше, чем у чистого BiFeO 3 , что указывает на то, что конструкция Ag 3 ЗП 4 / BiFeO 3 p-n-гетеропереходы полезны для подавления рекомбинации фотогенерированных электронов и дырок. На рис. 10б представлены спектры ESI образцов. Видно, что композит имеет меньшие радиусы импеданса дуги по сравнению с BiFeO 3 , что свидетельствует о более низком сопротивлении переноса заряда композита. Эти результаты показывают, что разделение и миграция фотогенерируемых зарядов в композите можно улучшить, обеспечивая тем самым больше фотоиндуцированных дырок и электронов для фотокатализа. На рисунке 10c показан график Мотта-Шоттки на частоте 3000 Гц для Ag 3 ЗП 4 . Отрицательный наклон графика указывает на то, что Ag 3 ЗП 4 является полупроводником p-типа, что согласуется с отчетом [43]. Спектры ФЛ BiFeO 3 и 20 мас.% Ag 3 ЗП 4 / BiFeO 3 показаны на рис. 10d. The two samples exhibit obvious emission peaks at ~ 522 nm, which are mainly attributed to the recombination of the photogenerated electron/hole pairs. It is worth noting that the PL intensity of the composite is much smaller than that of bare BiFeO3 . This further confirms that the construction of Ag3 ЗП 4 /BiFeO3 heterojunction promotes the separation of photoinduced charges.
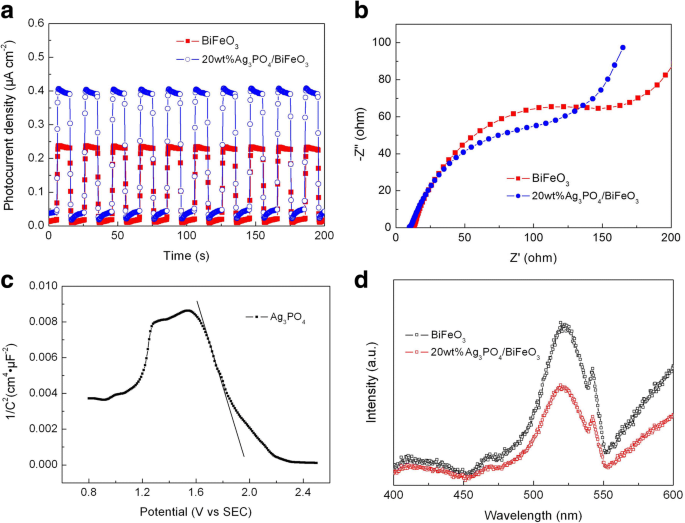
а Transient photocurrent response and b EIS spectra of BiFeO3 and 20wt%Ag3 ЗП 4 /BiFeO3 образец. c Mott-Schottky plot of Ag3 ЗП 4 . г PL spectra of BiFeO3 and 20wt%Ag3 ЗП 4 /BiFeO3 образцы
Active Species Trapping
It is well known that photogenerated hole (h + ), hydroxyl (•OH), and superoxide (•O 2− ) are considered to the main active species responsible for the photocatalytic degradation of dye. In order to clarify the role of the active species in the present photocatalytic system, the active species trapping experiments were carried out, as shown in Fig. 11. It can be seen that the degradation percentage of AO7 undergoes an obvious decrease after the introduction of ethanol (scavenger of •OH, 10% by volume) or ethylene diamine tetraacetic acid (EDTA, scavenger of h + , 2 mM). This indicates that •OH and h + are the major active species involved in the photocatalytic reaction. After the addition of benzoquinone (BQ, scavenger of •O 2− , 1 mM), a slight decrease of degradation percentage is detected, suggesting that •O 2− plays a relatively minor role in the dye degradation.
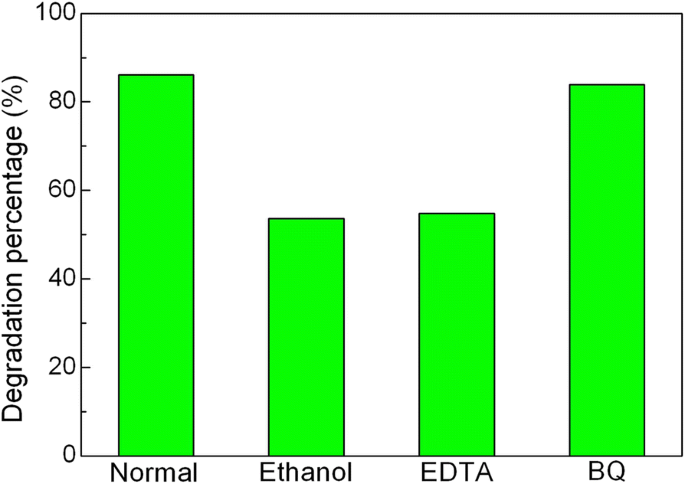
Effects of ethanol, EDTA, and BQ on the degradation percentage of AO7 over 20wt%Ag3 ЗП 4 /BiFeO3 составной
Proposed Photocatalytic Mechanism
It is well known that the redox ability and migration of photogenerated charges are highly related to the energy-band potentials of photocatalysts. The valence band (VB) and conduction band (CB) of BiFeO3 и Ag 3 ЗП 4 can be obtained using the following equation [58, 59]:
$$ {E}_{\mathrm{VB}}=X-{E}^{\mathrm{e}}+0.5{E}_{\mathrm{g}} $$ (4) $$ {E}_{\mathrm{CB}}=X-{E}^{\mathrm{e}}-0.5{E}_{\mathrm{g}} $$ (5)X is the absolute electronegativity of semiconductor (calculated as the arithmetic mean of the electron affinity and the first ionization of the constituent atoms). E e is the energy of free electrons on the hydrogen scale (~ 4.5 eV). The X values of BiFeO3 и Ag 3 ЗП 4 are estimated to be 5.93 and 5.98 eV, respectively [43, 60]. Based on Eqs. (4) and (5), the CB/VB potentials of BiFeO3 и Ag 3 ЗП 4 are calculated to be 0.34/2.52 V and 0.31/2.66 V vs. NHE, respectively. The energy-band potential diagram of the two photocatalysts is shown in Fig. 12a. It is reported that BiFeO3 is an n-type semiconductor and its Fermi level lies close to the CB [48]. Ag 3 ЗП 4 is demonstrated to be a p-type semiconductor (see Fig. 10c), whose Fermi energy level is close to the VB [43].When BiFeO3 is combined with Ag3 ЗП 4 to form p-n heterojunction (see Fig. 12b), the diffusion of electrons and holes between the two photocatalysts will build an internal electric field at the interface region of the p-n heterojunction with direction from BiFeO3 to Ag3 ЗП 4 . Simultaneously, the energy-band potential of BiFeO3 tends to move down along with its Fermi level whereas that of Ag3 ЗП 4 tends to raise up accompanied by its Fermi level until an equilibrium state of Fermi level of the two photocatalysts is achieved. Upon visible-light irradiation, both BiFeO3 и Ag 3 ЗП 4 can be excited to generate photoinduced electron and hole pairs. Under the promotion of the internal electric field, the photogenerated electrons in the CB of Ag3 ЗП 4 will migrate to the CB of BiFeO3 , while the photogenerated holes will transfer from the VB of BiFeO3 to that of Ag3 ЗП 4 . As a result, the recombination of photogenerated charges can be effectively inhibited, as evidenced by the photocurrent and PL analysis (see Fig. 10a, d). Thus, more photogenerated electrons and holes can participate in the photocatalytic redox reaction, leading to the enhancement of the photocatalytic activity for the Ag3 ЗП 4 /BiFeO3 p-n heterojunction composites.
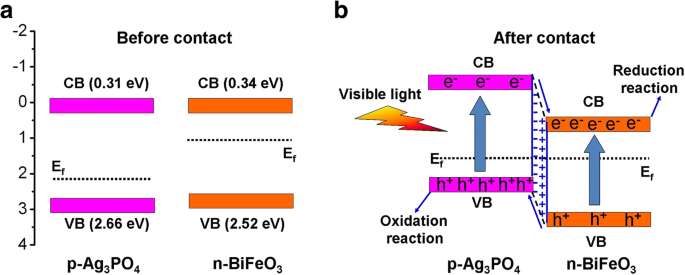
Schematic illustration of proposed photocatalytic mechanism for Ag3 ЗП 4 /BiFeO3 композитный. а Before contact. б After contact
Выводы
Ag 3 ЗП 4 /BiFeO3 p-n heterojunction composites were synthesized through the decoration of Ag3 ЗП 4 spherical-like microparticles on the surface of BiFeO3 microcuboids. Compared with bare BiFeO3 , the as-obtained composites exhibit enhanced visible-light photocatalytic activity for the degradation of AO7 and phenol. Moreover, the composites are demonstrated to be excellent photo-Fenton-like catalysts. The improved photocatalytic activity of the composites is mainly attributed to the efficient separation of photogenerated electrons and holes owing to the formation of the p-n heterojunction between BiFeO3 и Ag 3 PO4.
Сокращения
- AO7:
-
Acid orange 7
- CB:
-
Полоса проводимости
- DRS:
-
UV-vis diffuse reflectance spectra
- EDX:
-
Energy dispersive X-ray
- E g :
-
Bandgap energy
- I-t:
-
Photocurrent-time
- NMP:
-
1-Methyl-2-pyrrolidione
- PVDF:
-
Поливинилиденфторид
- R:
-
Reflectance
- SEM:
-
Сканирующий электронный микроскоп
- ТЕМ:
-
Просвечивающий электронный микроскоп
- VB:
-
Группа валентности
- XPS:
-
Рентгеновская фотоэлектронная спектроскопия
- XRD:
-
Рентгеновский дифрактометр
Наноматериалы
- Нановолокна и нити для улучшенной доставки лекарств
- Достижения и проблемы флуоресцентных наноматериалов для синтеза и биомедицинских приложений
- Гидротермальный синтез наночастиц In2O3, гибридные двойники, гексагональные дисковые гетероструктуры ZnO для по…
- Новый фотокатализатор на гетеропереходе Bi4Ti3O12 / Ag3PO4 с улучшенными фотокаталитическими характеристиками
- Легкий синтез червоточиноподобного мезопористого оксида олова за счет самосборки, вызванной испарением, и у…
- Синтез нанопластин Cu2ZnSnSe4 в одном резервуаре и их фотокаталитическая активность, управляемая видимым светом
- Простой одностадийный сонохимический синтез и фотокаталитические свойства композитов на квантовых точках г…
- Фотокаталитическая активность тройного нанокомпозита аттапульгит – TiO2 – Ag3PO4 для разложения родамина B при мод…
- Изготовление и фотокаталитические свойства новых нанокомпозитов SrTiO3 / Bi5O7I
- Простой метод получения гетероперехода Cu2O-TiO2 NTA с видимой фотокаталитической активностью



