Синтез углеродистых наночастиц, легированных церием, на основе биоминерализации для активности по улавливанию сильных гидроксильных радикалов
Аннотация
Наночастицы оксида церия в последнее время привлекли к себе пристальное внимание в биомедицинских приложениях из-за их превосходных антиокислительных свойств. В этом исследовании был разработан простой, мягкий и экологически чистый подход к синтезу углеродистых наночастиц, легированных церием (CNP, легированных церием), с использованием биоминерализации бычьего сывороточного альбумина (BSA) в качестве прекурсора. Полученные CNP, легированные Ce, имели однородную и ультрамалую морфологию со средним размером 14,7 нм. Результаты XPS и FTIR показали присутствие гидрофильной группы на поверхности CNP, легированных Ce, что привело к превосходной дисперсии в воде. Анализ CCK-8 продемонстрировал, что CNP, допированные Ce, обладают благоприятной биосовместимостью и незначительной цитотоксичностью. Использование H 2 О 2 -индуцированные химически активные формы кислорода (ROS) в качестве модели, CNP, легированные Ce, показали высокую способность улавливать гидроксильные радикалы. Кроме того, результаты проточной цитометрии и окрашивания живых мертвецов показали, что CNP, допированные Ce, защищают клетки от H 2 О 2 -индуцированное повреждение с дозозависимым эффектом, что является прямым доказательством антиоксидантной активности. Эти данные позволяют предположить, что CNP, допированные Ce, как новые поглотители ROS, могут обеспечить потенциальную терапевтическую перспективу при лечении заболеваний, связанных с окислительным стрессом.
Фон
Продолжительное и нерегулируемое воспаление считается частым этапом многих патологических процессов [1]. Окислительный стресс был обнаружен при многих клинических заболеваниях, при которых АФК имеют гораздо более высокую экспрессию, чем устранение антиоксидантных ферментов [2, 3, 4], что в конечном итоге определяется как дисбаланс между окислительной и антиоксидантной активностью. Высокоактивные АФК имеют тенденцию к образованию свободных радикалов (включая супероксид (O 2 - ), HO 2ˋ и гидроксил ( ˋ OH)), которые вызывают повреждение макромолекул в организме, таких как белки и нуклеиновые кислоты, тогда как избыточное производство ROS имеет решающее значение для устойчивого окислительного повреждения, приводя к значительным разрушениям клеточных структур и функций, таких как воспалительные инфильтраты [5,6 , 7], повреждение клеточных мембран и ДНК [8, 9] и даже увеличение гибели клеток. Таким образом, окислительный стресс играет ключевую роль в патогенезе макрососудистых заболеваний [10,11,12], рака и некоторых других заболеваний нервной системы [13]. Следовательно, это важная и неотложная проблема - контролировать концентрацию активных свободных радикалов кислорода в живых организмах и поддерживать их в подходящем диапазоне, что также является важным для уменьшения ряда окислительных аномалий.
В последнее время наночастицы оксида церия (CeO 2 НЧ) привлекли большое внимание благодаря своим уникальным окислительно-восстановительным свойствам, которые широко применялись в энергетике, катализе и биомедицине [14,15,16]. В частности, главный исполнительный директор 2 наночастицы продемонстрировали огромный потенциал в качестве идеального антиоксиданта для лечения заболеваний, связанных с АФК, в биомедицинских приложениях [17, 18]. Антиоксидантная активность наночастиц церия обусловлена их способностью улавливать свободные радикалы, такие как супероксид (• O 2- ) и гидроксильных радикалов (• ОН), и поддерживает антиоксидантный эффект как фермент в течение длительного периода [19]. Появляется все больше свидетельств того, что CeO 2 наночастицы обычно имеют кристаллическую структуру типа флюорита, а ионы церия обладают способностью обратимого преобразования между трехвалентностью (3+) и четырехвалентностью (4+) [20]. Переключатель Ce 3+ кому:Ce 4+ степени окисления могут устранить O 2 - через миметики супероксиддисмутазы (SOD) и • OH через окислительно-восстановительные реакции, тогда как Ce 4+ кому:Ce 3+ переключатель удалить H 2 О 2 через миметики каталазы (CAT) [21]. Однако физико-химические свойства CeO 2 НЧ могут влиять на биологическое поведение, включая его биораспределение, фармакокинетику, токсичность, растворение и выведение [22]. Учитывая гипотезу о том, что она хорошо обоснована на основе поверхностной химии CNP, легированных Ce, биологическое использование CNP, легированных Ce, в качестве терапевтического подхода все еще требует широкого изучения [23, 24].
Это исследование сосредоточено на разработке новых наночастиц на основе церия (называемых CNP, легированных церием) с превосходной биосовместимостью с использованием простого и экологически чистого пути синтеза, а также дальнейшее изучение их применимости в качестве антиоксидантного агента для биомедицинских приложений. Был использован ряд методов для характеристики физических и химических свойств CNP, легированных Ce. Воодушевленные хорошими характеристиками, мы дополнительно проверили биосовместимость приготовленных CNP, легированных Ce, и использовали их в качестве антиоксидантных реагентов для устранения свободных радикалов кислорода с помощью H 2 О 2 индуцированная модель. Наконец, антиоксидантный механизм CNP, допированных Ce, был выявлен на основе пути апоптоза клеток с использованием флуоресцентного окрашивания «живые-мертвые» и проточной цитометрии. Это исследование предоставит новый и эффективный поглотитель ROS для облегчения повреждения, вызванного окислительным стрессом при патологических условиях.
Экспериментальный раздел
Материалы и реагенты
Бычий сывороточный альбумин (BSA), диацетат флуоресцеина (FDA) и йодид пропидия (PI) были приобретены у Sigma (Нью-Йорк, Нью-Йорк, США). Фетальная бычья сыворотка (FBS) и минимальная основная среда Дульбекко (DMEM) были закуплены у Invitrogen China Limited (Шанхай, Китайская Народная Республика). Ce (NO 3 ) 3 · 6H 2 О, метиловый фиолетовый (MV) и гептагидрат сульфата железа (FeSO 4 . 7H 2 O) были приобретены у Aladdin Reagent Corporation (Шанхай, Китайская Народная Республика), а перекись водорода (30%) были получены от Sinopharm Chemical Reagent Co., Ltd. (Пекин, Китайская Народная Республика). Все химические вещества были аналитическими реагентами и использовались без дополнительной очистки. В экспериментах использовалась деионизированная вода.
Синтез наночастиц оксида церия
CNP, легированные Ce, были приготовлены с применением небольшой модификации метода биоминерализации на основе альбомов, как описано в документе [24]. Процесс синтеза проиллюстрирован следующим образом:1,25 г BSA растворяли в 50,0 мл деионизированной воды и постоянно перемешивали с образованием прозрачного раствора. Затем раствор предшественника металла 300 мМ Ce (NO 3 ) 3 · 6H 2 О, соответственно, медленно добавляли при интенсивном перемешивании. Одновременно 2,0 М NaOH растворяли в 50 мл деионизированной воды, которую использовали для регулирования значения pH смеси. Раствор, включающий NaOH, следует добавлять медленно, чтобы на него обратили внимание. CNP, легированные Ce, могут быть сформированы после энергичного перемешивания при PH 12 при 55 ° C. Достаточное время реакции для образования CNP, легированных Ce, составляло около 8 часов; система представляет собой смесь коричневого цвета, естественным образом охлаждающуюся до комнатной температуры. Дополнительную суспензию фильтровали через мембрану 0,22 мкм (полиэфирсульфон), чтобы уменьшить эти крупномасштабные агломерации. Первый раствор, наконец, подвергали диализу против воды в течение 3 дней в диализном мешке с отсечкой по молекулярной массе 14 кДа. Собранный диализный раствор лиофилизировали с использованием вакуумной сублимационной сушилки. В конечном итоге были получены порошки CNP, легированные Ce, и сохранены для дальнейшего изучения.
Приборы и характеристика наночастиц оксида церия
Морфологию CNP, легированных Ce, исследовали с помощью просвечивающей электронной микроскопии (TEM) на микроскопе JEM-2100 (JEOL, Токио, Япония) при ускоряющем напряжении 200 кВ. Распределение по размерам изучали с помощью программного обеспечения ImagingJ (Национальные институты здравоохранения, Бетесда, Мэриленд, США). Химические структуры CNP, легированных Ce, анализировали с помощью инфракрасного спектрометра с преобразованием Фурье (FT-IR) (Nicolet Nexus 470, GMI и Ramsey, MN, США). Элементный состав был определен с помощью элементного анализа, выполненного с помощью рентгеновской фотоэлектронной спектроскопии (XPS). Рентгеноструктурный анализ (XRD) выполняли на дифрактометре Rigaku D / MAX-2000 (Япония), работающем при 40 кВ и 100 мА, со щелью 0,5 ° и скоростью сканирования 7 ° мин -1 , снабженный источником излучения Cu Kα (λ =0,15418 нм). Спектры поглощения UV-Vis регистрировали с использованием спектрофотометра UV-2550 UV-Vis (Shimadzu, Киото, Япония).
Фотометрические эксперименты в УФ-видимом диапазоне
Антиоксидантные свойства CNP, легированного Ce, и активность по улавливанию свободных радикалов оценивали с помощью фотометрических экспериментов в УФ-видимом диапазоне. Растворы МВ готовили в деионизированной воде с концентрацией 3,0 × 10 −4 М. и 0,15 мМ FeSO 4 . 7H 2 O был растворен в качестве альтернативы. Суспендированный раствор CNP, легированных Ce, оставляли для использования в концентрациях 10 мкМ путем диспергирования в 0,1 М трис-HCl буфере при pH 5,0. Соответственно, ультразвуковая обработка может повысить растворимость CNP, легированных Ce. Реакционные растворы для фотометрии составляли 3,0 × 10 −5 M MV, 0,15 мМ FeSO 4 . 7H 2 O, 1,0 млн H 2 О 2 , 0,1 М трис-HCl буфер (pH 5,0) и 0,17 мМ CNP, легированные Ce для достижения необходимого объема 10 мл (смешайте раствор MV / FeSO 4 . 7H 2 O / H 2 О 2 / Главный исполнительный директор 2 ) в финале. Поглощение реакционного раствора можно было измерить после инкубации в течение 5 минут при комнатной температуре.
Цитотоксичность наночастиц оксида церия
Жизнеспособность CNP, допированных Ce, оценивали на клетках VSMC и 7721 с помощью анализа CCK-8 (Dojindo, Kumamoto, Japan) на основе расщепленного тетразолиевого кольца и снижения количества формазанового красителя в водорастворимой соли тетразолия дегидрогеназами. в живых клетках. Вкратце, VSMC и 7721 ячейки (1,5 × 10 4 клеток на лунку) высевали в 96-луночные планшеты с пятью повторами для каждой группы. После вылупления в течение 24 часов при 37 ° C и 5% CO 2 и плотность клеток достигла 80% конфлюэнтности, среду для роста заменили свежей DMEM, содержащей различные концентрации (0, 12,5, 25, 50, 100, 200, 400 мкг / мл) раствора CNP, допированных Ce, и инкубировали в течение 24 часов. Затем клетки промывали PBS и в каждую лунку добавляли 10 мкл раствора CCK-8. Затем 96-луночные планшеты инкубировали еще 4 часа при 37 ° C и 5% CO 2 . чтобы позволить экспоненциальный рост клеток. Наконец, оптическую плотность каждой лунки детектировали при длине волны излучения 490 нм с использованием Multi-Mode Microplate Reader Synergy HT (Bio-Tek, Winooski, VT, USA). Клетки (в DMEM) без обработки использовали в качестве контроля, и относительную жизнеспособность клеток (среднее значение ± стандартная ошибка среднего) рассчитывали, используя образец Abs / контроль Abs × 100%.
Модель анализа жизнеспособности клеток пероксида водорода in vitro
Как своего рода мощный окислительно-активный кислород, перекись водорода (H 2 О 2 ) легко проходит через клеточную мембрану и вступает в реакцию с внутриклеточными ионами железа с образованием высокореактивных свободных радикалов по теории Фентона, что приводит к цепочке изменений. В то же время разновидности окислительного стресса клеток, вызванного H 2 О 2 принимают непосредственное участие в процессе апоптоза. Следовательно, 30% H 2 О 2 был выбран для моделирования апоптоза клеток в этом исследовании, который также может быть использован в качестве IC 50 модель для дальнейшего исследования защитного действия CNP, допированных Ce, на окислительное повреждение. Основываясь на приведенном выше обсуждении, клетки VSMC и 7721 изначально были засеяны с плотностью 1,5 × 10 4 . клеток / лунку в 96-луночные планшеты. После того, как клетки прикрепились, их продолжали культивировать еще 24 часа. А в свежем препарате 30% H 2 О 2 в каждую лунку добавляли различные концентрации (50, 100, 200, 400, 800 мкмоль / мл) для стимуляции роста клеток. После 4-часового вылупления и последующей промывки PBS в каждую лунку добавляли 10 мкл раствора CCK-8 на 4 часа при 37 ° C в 5% CO 2 инкубатор . Многорежимный микропланшетный ридер Synergy HT (Bio-Tek, Winooski, VT, USA) использовали для определения значения абсорбции каждой лунки при 490 нм. Процент активности клеток рассматривался как показатель влияния на жизнеспособность клеток, который зависел от измерения выживаемости клеток по сравнению с контролем.
Анализ индукции апоптоза и жизнеспособности клеток in vitro
Таким же образом клетки VSMC и 7721 высевали в 96-луночные планшеты и культивировали. На следующий день клетки предварительно обрабатывали различными концентрациями CNP, легированными Ce (0, 12,5, 25, 50, 100, 200 и 400 мкг / мл) около 24 часов и подвергали воздействию свежего препарата 30% H 2. О 2 с подходящей концентрацией в каждой лунке. С другой стороны, следует установить пустую группу без 30% H 2 О 2 и CNP, легированные Ce, и контрольная группа была только с H 2 О 2 решения. Каждой группе было проведено шесть параллелей. После обработки в течение 4 часов и последующей промывки PBS анализ CCK-8 использовали для измерения условий апоптоза клеток в каждой лунке при оптической плотности 490 нм, как описано выше.
Анализ окрашивания живых мертвецов и проточная цитометрия
Чтобы оценить потенциал антиоксидантного действия CNP, допированных Ce, клетки 7721 выращивали на шестилуночных планшетах с 4,0 × 10 4 клеток в 100 мкл среды на лунку и дали развиваться в течение 24 часов. Затем шесть групп были настроены для одновременного контраста; он включает элемент управления H 2 О 2 группа, 50 мкг / мл CNP, легированные Ce + H 2 О 2 , 100 мкг / мл CNP, легированные Ce + H 2 О 2 , 200 мкг / мл CNP, легированные Ce + H 2 О 2 , и 400 мкг / мл CNP, легированных Ce + H 2 О 2 . В то время как клетки в каждой группе выросли до 80%, первая группа находилась в нормальных условиях роста без H 2 О 2 и CNP, легированные Ce; вторая группа только что инкубировалась с выбранным H 2 О 2 без CNP, легированных Ce в течение 4 ч, а именно без обработки; от третьей группы до шестой группы содержали разные концентрации CNP, легированных Ce (50, 100, 200 и 400 мкг / мл), и указывали H 2 О 2 инкубация в течение 4 ч соответственно. После этого для окрашивания клеток использовали рабочий буфер FDA и PI (Calcein AM / Ethidium Homodimer, Invitrogen). Флуоресценцию окрашенных клеток наблюдали под флуоресцентным микроскопом; живые клетки имели зеленый цвет, а мертвые - красный цвет.
Кроме того, набор для апоптоза аннексина V-FITC / пропидия иодида (PI) использовали для количественной оценки скорости апоптоза клеток путем окрашивания двойной флуоресценцией. Вкратце, клетки 7721 предварительно культивировали в шестилуночных культуральных планшетах в соответствии с описанными выше этапами в течение 24 часов до прилипшего роста клеток 7721. После этого клетки с разными дозами обработки собирали и трижды промывали PBS при 4 ° C в каждой группе. Было замечено, что клетки следует осторожно переваривать, собирать и центрифугировать с последующим 2000 об / мин в течение 5 мин. После этого клетки ресуспендировали в 500 мкл связывающего буфера и доводили до концентрации 1 × 10 6 . клеток / мл. Затем суспензию клеток переносили в проточную трубку, окрашивая 5 мкл аннексина V-FITC и 5 мкл 20 мкг / мл раствора PI, соответственно. Перед инкубацией смеси при комнатной температуре в течение 15 мин в реакционную пробирку необходимо добавить 500 мкл PBS. Наконец, экспериментальные результаты были обнаружены с использованием метода Аннексина-V на системе проточного цитометра Beckman Coulter Epics XL MCL (BD Accuri C6), а процент апоптотических клеток был уточнен с помощью программного анализа (Flowjo 7.6.2).
Статистический анализ
Все экспериментальные данные были выражены как среднее значение ± стандартная ошибка среднего. Для сравнения различных групп применялся статистический метод ANOVA с апостериорным критерием наименьшей значимой разницы (LSD) для анализа полученных данных. А P значение менее 0,05 ( P <0,05) считалось статистически значимым.
Результаты и обсуждение
Получение и характеристика наночастиц оксида церия
В данном исследовании водные дисперсии CNP, легированных Ce, были получены с использованием Ce (NO 3 ) 3 . 6H 2 O и BSA в качестве предшественников синтетическим методом, основанным на биоминерализации. Во время приготовления BSA, используемый в качестве основного источника углерода, может объединять ионы металлов с металлическими наночастицами благодаря своей уникальной пространственной структуре и гибкости молекулярных цепей. Другими словами, полученные наночастицы, легированные металлом, в основном состоят из углеродного каркаса и нагруженного металлического элемента, который может отличаться от обычных неорганических наночастиц церия [25]. Морфологическое исследование было охарактеризовано с помощью просвечивающей электронной микроскопии (ПЭМ), и полученные размеры частиц были проанализированы с помощью программного обеспечения ImagingJ. На рис. 1а показаны характерные ПЭМ-изображения полученных наночастиц, легированных Ce. Эти представления отражают, что CNP, легированные Ce, обладают многоугольной структурой, однородной дисперсией и дискретной формой без видимой агрегации. Статистический анализ показал, что CNP, легированные Ce, имеют узкое распределение по размерам со средним диаметром 14,7 ± 0,8 нм (рис. 1b), что согласуется с изображениями ПЭМ. Когда CNP, легированные Ce, находились в воде в течение нескольких дней, было обнаружено, что не было осаждения и все еще сохранялось утверждение об гомогенных растворах, что указывает на их долгосрочную стабильность в водном растворе, что может быть полезно для следующих биомедицинских применений. .
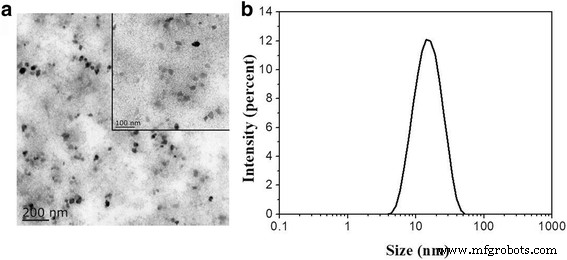
а ПЭМ-изображения CNP, легированных Ce. На вставке - ПЭМ-изображение высокого разрешения. б Распределение диаметров CNP, легированных Ce
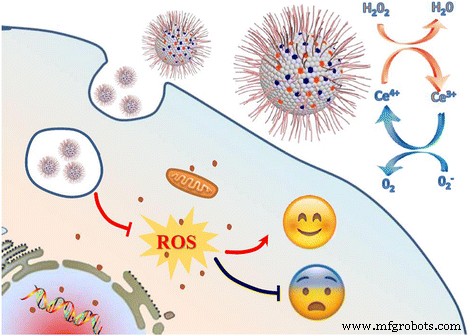
Схематическое изображение конструкции CNP, легированных Ce
Химическая структура и состав поверхности CNP, легированных Ce
Поверхностные функциональные группы и состав CNP, легированных Ce, были исследованы с использованием рентгеновской фотоэлектронной спектроскопии (XPS) и инфракрасного спектра с преобразованием Фурье (FT-IR). XPS использовался для характеристики степени окисления ионов церия на поверхности образцов. Обзорный XPS-спектр (рис. 2а) показал три преобладающих пика при 902,0, 285,0 и 531,8 эВ, что указывало на существование цериевых, углеродных и кислородных элементов в CNP, легированных Ce. Сигналы серы (S 2p) при 164,0 эВ позволяют предположить, что BSA успешно конъюгирован с CNP, легированными Ce. О сосуществовании Ce (III) и Ce (IV) в катализаторе CNP, легированных Ce, может свидетельствовать спектр на рис. 2b. Спектр высокого разрешения Ce3d (рис. 2b) может расщепляться на Ce3d 3 и Ce3d 5 (в результате спин-орбитального расщепления 32 эВ), показали наличие индексированных и сильных пиков, расположенных при 882,0, 884,0 и 902,0 эВ, соответственно. Сигналы Ce3d в основном были разделены на O 2 , 3д 5/2 , и 3d 3/2 пики между 875 и 895 эВ принадлежали Ce3d 3/2 уровень, который практически совпадал со спектром ранее опубликованного [26]. Более того, в спектре РФЭС также содержится 15,99% Ce3d. Эти наблюдения согласуются с литературными результатами для CeO 2 наночастицы [25]. Спектр C1s, показанный на рис. 2c, описывался тремя основными пиками при 285,0, 287,8 и 288,9 эВ, что соответственно означало, что CeO 2 наночастицы функционализировали с помощью энергетических уровней 1s, C =O, C − F и COOR C. Присутствие спектра O1s, как показано на рис. 2d, было связано с двумя основными пиками при 530,5 и 531,8 эВ, которые соответствовали связь между O 2 - и Ce 3+ .
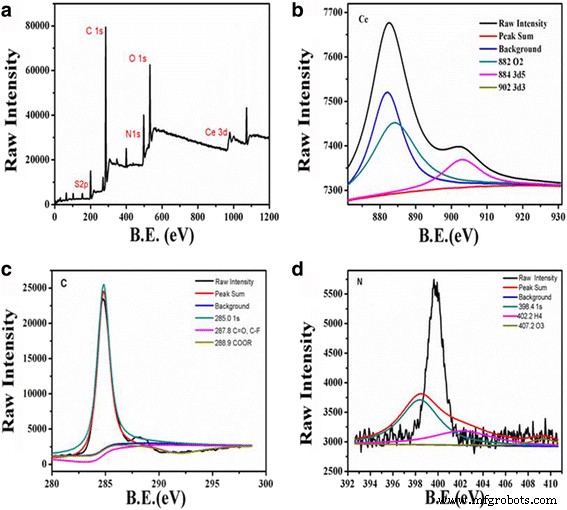
а XPS-спектры CNP, легированных Ce. Спектр обзора. б Спектр Ce3d. c Спектр C1s. г Спектр O1s
Далее был проведен FTIR-анализ для проверки образования CNP, легированных Ce, в процессе реакции. Как показано на рис. 3A, для CNP, легированных Ce, появился интенсивный и широкий пик при 3400 см -1 . , который был вызван растягивающим колебанием O – H и мог быть отнесен к изгибному колебанию поглощенной воды. Характерный пик при 1510 см −1 можно описать как антисимметричный участок –O – C – O, а пик при 1450 см −1 могут быть отнесены к симметричному валентному колебанию –O – C – O, оба из которых демонстрируют присутствие нитратных групп. Кроме того, полоса поглощения в 451 см −1 был отнесен к асимметричному участку Ce – O, что указывает на образование CNP, легированных Ce. Эти результаты показали, что функциональные группы CNP, легированных Ce, в основном содержат определенные -OH и -COO - группы.
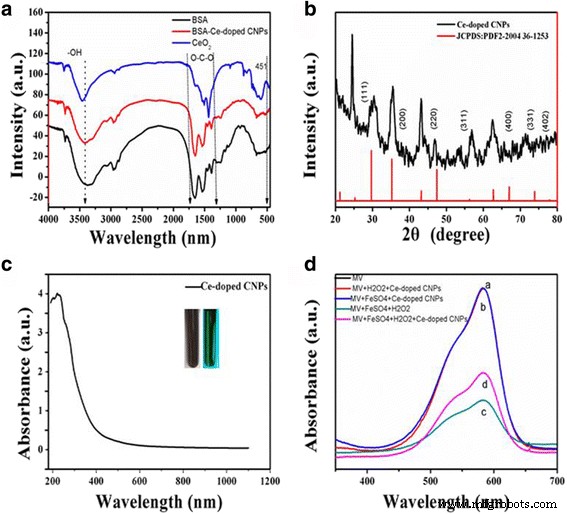
Спектры FTIR BSA и CNP, легированных Ce. B Рентгенограмма CNP, легированных Ce. C UV – Vis спектры поглощения CNP, легированных Ce. D УФ – видимые спектры поглощения метилового фиолетового (МВ) после различных обработок. а МВ, б МВ лечили H 2 О 2 и CNP, легированные Ce, c МВ, обработанный FeSO 4 и H 2 О 2 , и d МВ, обработанный FeSO 4 , H 2 О 2 и растворы CNP, легированные Ce, время инкубации 5 мин
По данным рентгеноструктурного анализа (XRD) была исследована кристаллическая структура CNP, легированных Ce. Как показано на фиг. 3B, имеется четыре основных дифракционных пика при 24,4 °, 30,3 °, 35,23 ° и 43,2 °. Один из этих пиков при 24,4 ° может быть приписан образовавшейся неорганической углеродистой структуре, которая аналогична зарегистрированным квантовым точкам углерода и характеристическим пикам графита [27,28,29]. По сравнению с упорядоченной кристаллической структурой графита (плоскости 002, 2 θ =26,5 °) дифракционный пик CNP, легированных Ce, около 24,4 ° с меньшим сдвигом становится слабым, что может быть связано с сильным разупорядочением углерода и увеличением sp 2 (C – C) расстояние между слоями в процессе карбонизации [30]. Пики дифракции под углами 30,3 °, 35,23 ° и 47,42 ° в основном совпадают с плоскостями (111), (200) и (220), соответственно, обычных наночастиц церия. Кроме того, другие пики под углами 56,30 °, 69,00 °, 75,57 ° и 78,99 ° соответствовали (311), (400), (331) и (402) упомянутого оксида церия (JCPDS 2004 36-1253). Соответствующий интервал \ (\ left (\ mathrm {Fm} 3 \ overline {\ mathrm {m}} \ right) \) был рассчитан согласно закону Брэгга (длина волны закона Cu-Kα составляет 0,154 нм). Эти результаты могут предварительно подтвердить, что CNP, легированные Ce, имеют гибридную кристаллическую структуру.
Было хорошо известно, что Fe 2+ может поочередно катализировать дисмутацию перекиси водорода (H 2 О 2 ) в другой реакционноспособный гидроксильный радикал по реакции Фентона [31]. Как хромогенный реагент раствор метилового фиолетового в основном имеет пурпурный цвет. Нацеленный на –C =C–, гидроксильный радикал может реагировать с метиловым фиолетовым, в результате чего MV приобретает неглубокий цвет, даже бесцветный, а его максимальное поглощение в УФ-видимой области при 582 нм уменьшается [32]. Согласно нашей конструкции, CNP, легированные Ce, безусловно, могут устранить гидроксильный радикал и, наконец, увеличить поглощение MV при 582 нм.
Чтобы подтвердить лежащую в основе способность CNP, легированных Ce, улавливать свободные радикалы, были использованы спектры поглощения MV в УФ-видимой области. В водном растворе CNP, легированных Ce, на рис. 3C значительного поглощения от 500 до 700 нм не наблюдалось. Однако мы могли наблюдать максимальное поглощение метилового фиолетового примерно при 582 нм, и поглощение ингибировалось под действием H 2 О 2 лечение (рис. 3D). При добавлении CNP, легированных Ce, в раствор смеси, поглощение, очевидно, восстанавливается, что доказывает, что CNP, легированные Ce, обладают способностью очищать гидроксильный радикал и защищать MV от атаки в этих экспериментальных условиях. Эти результаты будут иметь дальнейшее биомедицинское применение при лечении заболеваний, вызванных свободными радикалами.
Анализ цитотоксичности наночастиц оксида церия in vitro
Перед применением синтезированных CNP, допированных цеем, для лечения заболеваний, связанных с окислительным стрессом, важно оценить их биосовместимость. В этом исследовании влияние CNP, допированных Ce, на жизнеспособность клеток оценивали посредством инкубации клеток VSMC и 7721 с CNP, допированных Ce, с использованием тестов на жизнеспособность клеток в анализе CCK-8. Можно видеть, что жизнеспособность клеток не показала значительных изменений после обработки различными концентрациями CNP, легированных Ce, в течение 24 часов воздействия (рис. 4a). Даже при наивысшей дозе 400 мкг / мл жизнеспособность клеток во всех группах лечения составляла приблизительно 90%, демонстрируя, что CNP, допированные Ce, обладают очень незначительной цитотоксичностью по отношению к клеткам. Эти результаты подчеркнули благоприятную цито-совместимость CNP, допированных Ce, и сделали их пригодными для биомедицинских приложений.
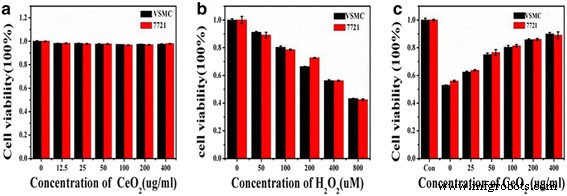
а Влияние различных концентраций CNP, допированных Ce, на жизнеспособность клеток VSMC и 7721 посредством CCK-8. Клетки предварительно обрабатывали CNP, легированными Ce, при различных концентрациях в течение 24 часов, а затем вводили H 2 О 2 в разных дозировках. б Жизнеспособность клеток VSMC и c Клетки 7721, культивированные с различными концентрациями CNP, допированных Ce, при 560 мкМ H 2 О 2 -индуцированный окислительный стресс a по анализу CCK-8
Антиоксидантные свойства и активность по улавливанию свободных радикалов CNP, допированных Ce, In Vitro
Свойство миметического фермента наноматериалов оксида церия способствует их потенциальному терапевтическому применению. Было исследовано, будут ли CNP, допированные Ce в растворе, в достаточной степени защищать клетки VSMC и 7721 от свободных радикалов. Для этих исследований H 2 О 2 был использован для индукции генерации активных форм кислорода (АФК), которые приводят к повреждению или гибели клеток. Во-первых, ИС 50 Ценность жизнеспособности клеток была определена для изучения защитного эффекта CNP, допированных цеем. Жизнеспособность клеток VSMC и 7721 показала низкое значение после добавления H 2 О 2 . Наблюдалась тенденция к увеличению апоптотической активности для клеток VSMC и 7721 с увеличением H 2 О 2 концентрация в растворе (рис. 4б). Другими словами, повышение ROS было дозозависимым, что также показало среднюю летальную дозу (LD 50 ) клеток VSMC и 7721 составляла приблизительно 549 и 556 мкмоль / мл соответственно. В результате LD 50 H 2 О 2 через окислительный стресс составлял 560 мкМ, что близко к литературным данным [33].
Далее, антиоксидантный эффект CNP, допированных Ce при LD 50 из H 2 О 2 был протестирован с использованием набора для подсчета клеток-6 (CCK-8). Благодаря своим уникальным электронным свойствам, CNP, легированные Ce, имеют внутреннюю тенденцию существовать в двойных степенях окисления (Ce 3+ и Ce 4+ ) и обладают антиоксидантной активностью за счет окислительно-восстановительного поведения. Когда существует ROS, Ce 4+ можно постоянно переключать на Ce 3+ наряду с постоянной активностью улавливания свободных радикалов [34, 35]. Как показано на фиг. 4c, эти результаты предполагают, что жизнеспособность клеток VSMC и 7721 постепенно улучшалась с увеличением концентрации CNP, допированных Ce, при том же окислительном стрессе. В частности, жизнеспособность клеток восстанавливалась примерно на 88,0% при концентрации CNP, легированной Ce, равной 400 мкг / мл. Следовательно, CNP, легированные Ce, проявляют выдающийся антиоксидантный эффект в зависимости от дозы за счет эффективного улавливания свободных радикалов.
Для дальнейшего раскрытия цитоантиоксидантного эффекта CNP, допированных Ce. Как показано на рис. 5, интенсивная зеленая флуоресценция без красного наблюдалась в клетках 7721, обработанных одиночными CNP, легированными Ce, но много красной флуоресценции можно было увидеть в H 2 О 2 обработка 556 мкМ, которая продемонстрировала H 2 О 2 может резко вызвать апоптоз клеток. Но H 2 О 2 -индуцированный апоптоз постепенно уменьшался с увеличением концентрации CNP, допированного Це. В частности, только небольшое количество красной флуоресценции можно было увидеть после обработки CNP, легированного Ce, в концентрации 400 мкг / мл в атмосфере H 2 О 2 -индуцированный окислительный стресс, который указывает на более высокую жизнеспособность клеток. Далее был проведен анализ проточной цитометрии для исследования антиоксидантного действия CNP, допированных Ce. На диаграмме рассеяния двойной переменной проточной цитометрии сигнал эмиссии Annexin-V-FITC был нанесен на x по оси, в то время как сигнал излучения PI был нанесен на y -ось. Несколько областей клеток были определены следующим образом:Аннексин V- / PI –– считается живыми клетками, Аннексин V + / PI –– обозначает клетки раннего апоптоза, а Аннексин V + / PI + –– обозначает клетки позднего апоптоза / некроза. Как показано на рис. 6, в контрольной группе наблюдалась небольшая и нормальная доля позднего апоптоза клеток 1,45%, но H 2 О 2 лечение показало чрезвычайно высокий уровень позднего апоптоза клеток - 46,4%. Как мы и ожидали, доля апоптотических клеток, обработанных различными концентрациями CNP, допированных цеем, имеет тенденцию к постепенному снижению. По сравнению с 46,4% позднего апоптоза клеток при H 2 О 2 После обработки CNP, допированного Ce, в концентрации 50, 100, 200 и 400 мкг / мл процент апоптоза заметно снизился до 24,2, 20,0, 15,1 и 11,2%. Основываясь на результатах окрашивания живых мертвецов и проточной цитометрии, было обнаружено, что CNP, допированные Ce, обладают благоприятным антиоксидантным действием против апоптоза, вызванного окислительным стрессом, в зависимости от дозы.
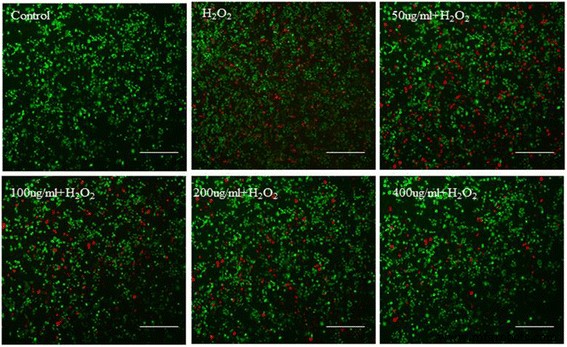
Fluorescent images of 7721 cells incubated with different concentrations of Ce-doped CNPs under H2 О 2 -induced oxidative stress for 24 h by live-dead staining (scale bars = 50 μm)
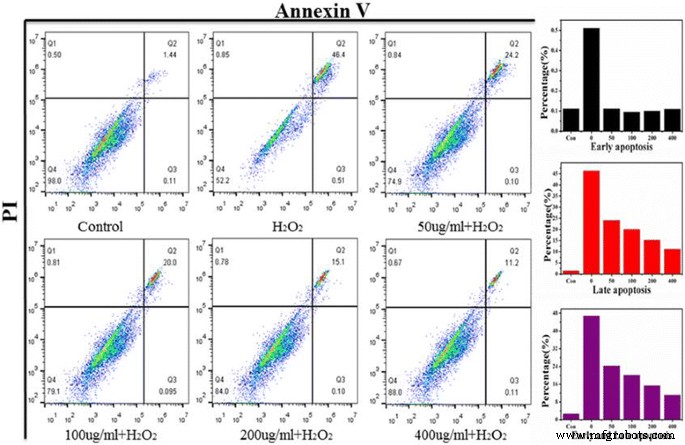
Flow cytometry profiles of 7721 cells were examined to determine the percentages of early apoptosis and late apoptosis cells with different treatments
Выводы
In summary, we reported a novel Ce-doped CNPs with the capability of scavenging free radicals. The preparation method is simple by using one-step synthesis in the bio-mineralization manner. Different from the former surface modification (such as PVP), the as-prepared Ce-doped CNPs exhibited the improvement in biocompatibility and dispersibility in aqueous solution. Furthermore, in vitro studies showed albumin-based bio-mineralization Ce-doped CNPs not only own superoxide dismutase feature but also alleviate the oxidative damage caused by H2 О 2 , which have a protective effect on cells in this periods of study. Furthermore, the concentration of Ce-doped CNPs plays important roles in the recovery of apoptotic cells. Herein, the novel Ce-doped CNPs have promising biomedical applications in diseases prevention and treatment of oxidative stress-mediated.
Наноматериалы
- Наночастицы золота для химиотерапевтических датчиков
- Наночастицы для терапии рака:текущий прогресс и проблемы
- Оптимизация высокоотражающей тонкой пленки для полноугольных микро-светодиодов
- Простой синтез наночастиц SiO2 @ C, закрепленных на MWNT, в качестве высокоэффективных анодных материалов для лити…
- Наночастицы альбумина, содержащие ресвератрол, с длительным кровообращением и улучшенной биосовместимостью…
- Гидротермальный синтез наночастиц In2O3, гибридные двойники, гексагональные дисковые гетероструктуры ZnO для по…
- Наночастицы кремнезема для доставки внутриклеточного белка:новый подход к синтезу с использованием зеленог…
- Метод последующей обработки для синтеза монодисперсных бинарных наночастиц FePt-Fe3O4
- Синтез и эффективность in vitro покрытых полипирролом железо-платиновых наночастиц для фототермической терапии…
- Сапонины Platycodon из Platycodi Radix (Platycodon grandiflorum) для зеленого синтеза наночастиц золота и серебра



