Излучающие в ближнем инфракрасном диапазоне Cr3 + / Eu3 + со-легированные галлогерманатом цинка стойкие люминесцентные наночастицы для визуализации клеток
Аннотация
Стойкие люминесцентные наночастицы, излучающие в ближней инфракрасной области (NIR), были разработаны в качестве потенциальных агентов для биоимиджинга. Однако синтез однородных наночастиц с длительным послесвечением для долгосрочной визуализации отсутствует. Здесь мы продемонстрировали синтез структурированного шпинели Zn 3 Ga 2 Ge 2 О 10 :Cr 3+ (ZGGO:Cr 3+ ) и Zn 3 Ga 2 Ge 2 О 10 :Cr 3+ , Eu 3+ (ZGGO:Cr 3+ , Eu 3+ ) наночастиц золь-гель методом в сочетании с последующим прокаливанием без восстановительной атмосферы. Образцы были исследованы с помощью подробных характеристик с помощью комбинированных методов XRD, TEM, STEM, дифракции электронов в выбранной области, спектроскопии возбуждения фотолюминесценции (PLE) / фотолюминесценции (PL) и анализа зависимой от температуры PL. Монокристаллические наночастицы представляют собой однородный твердый раствор, имеющий однородную кубическую форму и поперечный размер ~ 80–100 нм. При УФ-возбуждении при 273 нм ZGGO:Cr 3+ , Eu 3+ демонстрирует полосу излучения в ближнем ИК-диапазоне при 697 нм ( 2 E → 4 A 2 переход искаженного Cr 3+ ионы в галлогерманате), в отсутствие Eu 3+ эмиссия. Непрерывное свечение образца в ближнем ИК-диапазоне может длиться более 7200 с и при этом сохранять высокую интенсивность. Eu 3+ включение увеличило интенсивность стойкой люминесценции и время послесвечения ZGGO:Cr 3+ , но на термостабильность это существенно не повлияло. Полученный ZGGO:Cr 3+ , Eu 3+ -NH 2 наночастицы обладают отличной способностью визуализировать клетки in vitro.
Фон
Стойкие люминесцентные материалы могут излучать длительное время до часов после прекращения возбуждения [1]. В основном из-за большого исследовательского интереса люминофоры были коммерциализированы в качестве материалов для ночного или темного видения окружающей среды для широкого спектра применений, таких как знаки безопасности, указатели аварийных маршрутов, опознавательные знаки или медицинская диагностика [2]. Типичные долговечные люминофоры - это коммерчески выпускаемые излучатели основных цветов, такие как красный Y 2 О 2 S:Eu 3+ , Mg 2+ , Ti 4+ или CaS:Eu 2+ , Тм 3+ , Ce 3+ [3, 4], зеленый SrAl 2 О 4 :Eu 2+ , Ду 3+ или MgAl 2 О 4 :Mn 2+ [5, 6] и синий CaAl 2 О 4 :Eu 2+ , Nd 3+ или SrMgSi 2 О 6 :Eu 2+ , Ду 3+ [7, 8] люминофоры. Хотя многие успехи были достигнуты в видимых стойких люминофорах, исследования и разработки стойких люминофоров в ближней инфракрасной (БИК) области (~ 700–2500 нм) недостаточны. В последние годы возможности применения стойких люминофоров, демонстрирующих красное или ближнее ИК-свечение, расширились от знаков безопасности ночного видения до систем визуализации in vivo [1, 9, 10].
Стойкие люминесцентные материалы с прикрепленными фотосенсибилизаторами в качестве агента in vivo впервые были опробованы Ченом и Чжаном для фотодинамической терапии [11]. Затем Scherman et al. сообщил о важной работе по созданию биовизуализации in vivo с использованием люминофора Са 0,2 , излучающего в ближнем инфракрасном диапазоне. Zn 0,9 Мг 0,9 Si 2 О 6 :Eu 2+ , Mn 2+ , Ду 3+ [12]. Вскоре после этого были выпущены два новых люминофора CaMgSi 2 , излучающих в ближнем ИК-диапазоне. О 6 :Eu 2+ , Mn 2+ , Pr 3+ и Ca 2 Si 5 N 8 :Eu 2+ , Тм 3+ с улучшенными характеристиками были разработаны той же группой [13, 14]. Недавно Cr 3+ -допированные галлатные стойкие люминофоры с БИК-излучением и длительным послесвечением, включая шпинель ZnGa 2 О 4 :Cr 3+ и их варианты, такие как Zn 3 Ga 2 Ge 2 О 10 :Cr 3+ , Zn 3 Ga 2 Гео 8 :Cr 3+ , Yb 3+ , Er 3+ , и ZnGa 2 - x (Ge / Sn) x О 4 :Cr 3+ , были получены твердотельным методом [1, 9, 10, 15,16,17,18,19,20,21]. Образцы с керамическими дисками показали время послесвечения до 360 часов в ближней ИК-области, но громоздкие материалы не подходят для биоимиджинга in vivo. Долго стойкие люминесцентные наночастицы ZnGa 2 , излучающие в ближнем ИК-диапазоне. О 4 :Cr 3+ [22, 23], ZnGa 2 О 4 :Cr 3+ , Sn 4+ [19,20,21], и Zn 2,94 Ga 1,96 Ge 2 О 10 :Cr 3+ , Pr 3+ [9] были синтезированы золь-гель методом в сочетании с последующим прокаливанием без восстановительной атмосферы. Постоянная люминесценция порошка наночастиц демонстрирует яркую люминесценцию в ближнем ИК-диапазоне в окне биологической прозрачности со сверхдлительным временем послесвечения. ПЭГилирование значительно улучшает биосовместимость и растворимость в воде наночастиц, которые обладают большим потенциалом для долгосрочного применения в области биовизуализации in vivo с высоким SNR без необходимости возбуждения in situ. Считается, что ионы, выбранные из группы, состоящей из ионов щелочноземельных металлов, ионов лантаноидов и Li + совместное допирование Cr 3+ в галлате цинка и галлогерманате цинка дает замечательную стойкую люминесценцию в ближнем ИК-диапазоне [1]. Eu 3+ в оксидных хозяевах всегда проявляет красную эмиссию на ~ 700 нм, возникающую из-за 5 D 0 - 7 F 4 интра-4 f электронный переход при коротком УФ-возбуждении в полосу переноса заряда (СТ) при 250 нм [24]. С другой стороны, Cr 3+ является благоприятным люминесцентным центром в твердых телах из-за его узкополосного излучения (обычно при 700 нм) из-за запрещенного по спину 2 E- 4 A 2 переход или широкополосное излучение (650–1600 нм) из-за разрешенного спина 4 Т 2 - 4 A 2 переход [1, 20]. Ввиду этого Cr 3+ / Eu 3+ совместно легированный галлат цинка и галлогерманат цинка будут давать интенсивную стойкую люминесценцию в ближнем ИК-диапазоне из-за того, что полоса переноса заряда (CTB) O 2- -Eu 3+ перекрывается с CTB O 2− -Ga 3+ , а излучение на ~ 700 нм от 5 D 0 - 7 F 4 переход Eu 3+ перекрывается с этим из 2 E- 4 A 2 переход Cr 3+ . Кроме того, Eu 3+ ионы, замещающие Ga 3+ ионы в искаженных октаэдрических узлах могут дать подходящую напряженность кристаллического поля хозяина около Cr 3+ ионы, тем самым влияя на БИК-излучение. В этой работе Zn 3 Ga 2 Ge 2 О 10 :Cr 3+ , Eu 3+ (обозначается как ZGGO:Cr 3+ , Eu 3+ ) наночастицы были синтезированы золь-гель методом в сочетании с последующим кальцинированием без восстановительной атмосферы, которые будут использоваться в качестве многообещающих нанозондов для будущего биоимиджинга. Образцы были исследованы с помощью детальных характеристик с помощью комбинированных методов рентгеновской дифрактометрии (XRD), просвечивающей электронной микроскопии (TEM), STEM, электронной дифракции на выбранной площади (SAED), фотолюминесцентной спектроскопии возбуждения (PLE) / фотолюминесценции (PL) и температуры. -зависимый анализ PL. В следующих разделах мы сообщаем о синтезе, описании и применении ZGGO:Cr 3+ , Eu 3+ наночастицы.
Экспериментальный
Синтез
Исходными источниками металлов являются Zn (NO 3 ) 2 · 6H 2 O, Cr (NO 3 ) 3 · 9H 2 О, Га 2 О 3 , Eu 2 О 3 , и GeO 2 все продукты чистотой 99,99% были закуплены у Sinopharm (Шанхай, Китай). Остальные реагенты имеют аналитическую чистоту и были приобретены на заводе химических реагентов Шэньяна (Шэньян, Китай). Zn (NO 3 ) 2 · 6H 2 O и Cr (NO 3 ) 3 · 9H 2 О растворяли в деионизированной воде. Ga 2 О 3 и Eu 2 О 3 растворяли в растворе азотной кислоты. Гео 2 и этилендиаминтетрауксусную кислоту (EDTA) растворяли в разбавленном гидроксиде аммония. К смешанному раствору медленно добавляли раствор EDTA без какого-либо осаждения, и молярное отношение общего количества ионов металла к EDTA поддерживали на уровне 1:2. Молярное соотношение атомов Zn:Ga:Ge:Cr:Eu было установлено равным 3:1,984:2:0,01:0,006. Конечный раствор интенсивно перемешивали при комнатной температуре в течение 1 ч, затем нагревали в печи при 85 ° C для медленного испарения воды до тех пор, пока раствор не превратился в золь, который, наконец, превратился в гель. Полученный гель нагревали при 200 ° C в течение 3 ч с образованием пористых материалов черного цвета. Наконец, пористые материалы были измельчены и отожжены в потоке O 2 . газ (200 мл / мин) при выбранных температурах в течение 2 ч.
Функционализация поверхности
ZGGO:Cr 3+ , Eu 3+ порошок измельчали в течение 30 мин, затем 150 мг полученного образца добавляли в 50 мл 0,1 моль / л раствора NaOH. После обработки ультразвуком в течение 1 часа суспензию интенсивно перемешивали в течение 24 часов при комнатной температуре. Полученный коллоидный раствор центрифугировали при 1000 об / мин в течение 10 минут для удаления частиц большого размера, а супернатант центрифугировали при 10000 об / мин в течение 10 минут для сбора осадка. Полученный ZGGO:Cr 3+ , Eu 3+ Наночастицы -ОН трижды промывали деионизированной водой.
Десять миллиграммов ZGGO:Cr 3+ , Eu 3+ Наночастицы -ОН диспергировали в 4 мл диметилформамида (ДМФ) с помощью обработки ультразвуком в течение 10 мин. Затем при интенсивном перемешивании в течение 24 часов при комнатной температуре добавляли 40 мкл 3-аминопропилтриэтоксисилана (APTES). Полученный ZGGO:Cr 3+ , Eu 3+ -NH 2 Наночастицы собирали центрифугированием при 10 000 об / мин в течение 10 мин и трижды промывали ДМФА для удаления непрореагировавших APTES.
Получение изображений клеток
Клетки Hek293T культивировали в среде DMEM с 10% FBS и высевали в 35-миллиметровые чашки для культивирования на 2 часа в CO 2 инкубатор. Полученный ZGGO:Cr 3+ , Eu 3+ -NH 2 Наночастицы диспергировали в клеточной среде (50 мг / мл), которую возбуждали в течение 10 мин УФ-лампой с длиной волны 254 нм, а затем перемещали в чашки для культивирования, обработанные в течение 1 ч. После удаления клеточной среды добавляли 0,1 мл 1% формальдегид-PBS и клетки окрашивали 0,5 мл красителя DAPI в темноте в течение 10 мин. Наконец, клетки несколько раз промывали PBS для дальнейшей характеристики.
Все исследования с участием животных были одобрены университетским комитетом по уходу за животными и их использованию.
Методы характеризации
Идентификацию фаз выполняли с помощью XRD (модель SmartLab; Rigaku, Tokyo, Japan), работающего при 40 кВ / 40 мА, с использованием никелевого фильтра Cu Kα-излучения и скорости сканирования 6,0 ° 2 θ / мин. Морфологию продуктов наблюдали с помощью ТЕМ (модель JEM-2000FX; JEOL, Токио). Фотолюминесценцию люминофоров анализировали на флуороспектрофотометре FP-8600 (JASCO, Токио). Постоянные сигналы люминесценции получали с помощью прибора Horiba JY FL3-21. Изображения затухания послесвечения были записаны в темной комнате с использованием системы визуализации Kodak In-Vivo FX Pro. Визуализацию клеток проводили с помощью лазерного сканирующего конфокального микроскопа (LEICA TCS SP2, Германия).
Все исследования с участием животных были одобрены университетским комитетом по уходу за животными и их использованию.
Результаты и обсуждение
Фазовую чистоту образцов сначала исследовали методом XRD. На рис. 1 (вверху) показаны дифрактограммы свежеприготовленного ZGGO:Cr 3+ . и ZGGO:Cr 3+ , Eu 3+ прокаленные при 1000 ° C, которые были идентифицированы вместе со структурой шпинели Zn 3 Ga 2 Ge 2 О 10 [1, 9]. Кристаллическая структура Zn 3 Ga 2 Ge 2 О 10 то же самое, что и ZnGa 2 О 4 (JCPDS No. 38-1240), который представляет собой твердый раствор ZnGa 2 О 4 и Zn 2 Гео 4 . В составе Zn 3 Ga 2 Ge 2 О 10 , Ge играет роль замещения Ga, способствующего образованию ловушек, а ZnGa 2 О 4 является доминирующей кристаллической структурой [1]. В одноэлементной ячейке есть два вида катионов; Zn 2+ и Ga 3+ окружены четырьмя и шестью анионами кислорода, образующими тетраэдр и октаэдр соответственно (рис. 1 ниже). Расчеты по дифракционным данным дают постоянные ячейки для ZGGO:Cr 3+ являются a = b =~ 0,8335 нм, что близко к шпинели ZnGa 2 О 4 ( а = b =~ 0,8335 нм, JCPDS № 38-1240). Из-за больших ионных радиусов Eu 3+ (для шестикратной координации \ ({r} _ {\ mathrm {Eu}} ^ {3+}} \) =0,0947 нм и \ ({r} _ {{\ mathrm {Ga}} ^ {3+} } \) =0,062 нм) [25], большее значение a = b =~ 0,8336 нм наблюдалось для ZGGO:Cr 3+ , Eu 3+ . Анализ уширения профиля брэгговского отражения (311) был проведен с применением уравнения Шеррера для средних размеров кристаллитов 83 ± 6 нм для ZGGO:Cr 3+ и ZGGO:Cr 3+ , Eu 3+ образцы. На рис. 1 (вверху) мы также видим, что полученные продукты, прокаленные при 900 ° C, представляют собой смесь шпинельной фазы (JCPDS № 38-1240) и ромбоэдрической фазы (JCPDS № 11-0687), что указывает на температуру прокаливания. ≥ 1000 ° C необходимо для получения шпинели Zn 3 Ga 2 Ge 2 О 10 в фазовом чистом виде.
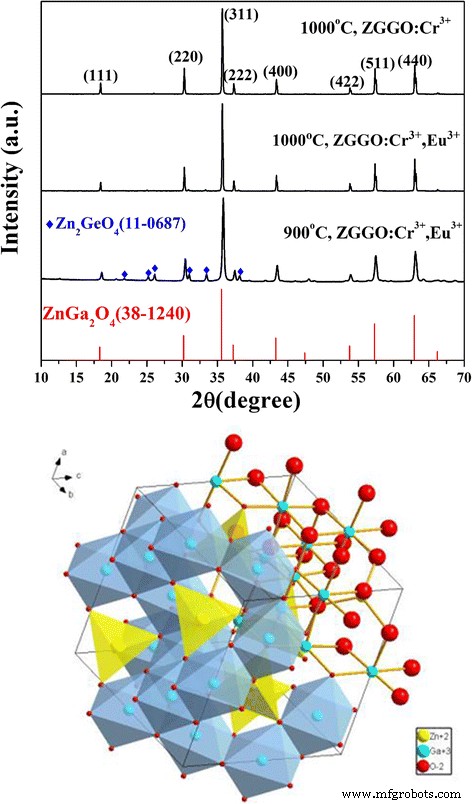
Рентгенограммы свежеприготовленного ZGGO:Cr 3+ и ZGGO:Cr 3+ , Eu 3+ и кристаллическая структура шпинели ZnGa 2 О 4
На рисунке 2 (слева) показана морфология ПЭМ для ZGGO:Cr 3+ . , Eu 3+ частиц, что ясно указывает на то, что они полностью состоят из кубических частиц с латеральными размерами ~ 80–100 нм. Острые углы и хорошо разрешенные полосы решетки указывают на их превосходную кристалличность, а расстояние ~ 0,29 нм хорошо соответствует плоскости (220) шпинели со структурой ZnGa 2 О 4 ( г (220) =~ 0.29 нм, JCPDS No. 38-1240) (вставка на рис.2). Поскольку размеры частиц близки к среднему размеру кристаллитов, рассчитанному по данным XRD, полученные образцы могут быть монокристаллическими. Анализ SAED (рис. 2 (справа)) дополнительно подтвердил, что анализируемые наночастицы являются монокристаллическими. Исследуемые наночастицы представляют собой прямые твердые растворы, а не механическую смесь. Картирование элементов Zn, Ga, Ge, Cr и Eu свидетельствует о наличии этого твердого раствора, как показано на рис. 3 для ZGGO:Cr 3+ , Eu 3+ . Каждая частица не только содержит Zn, Ga, Ge, Cr и Eu, но и все элементы равномерно распределены между частицами.

TEM, HR-TEM (слева) и шаблон SAED (справа) ZGGO:Cr 3+ , Eu 3+ наночастицы

Морфология частиц STEM (изображение в светлом поле, первое изображение) и элементарное отображение ZGGO:Cr 3+ , Eu 3+ наночастицы
На рисунке 4 показаны спектры возбуждения ZGGO:Cr 3+ . и ZGGO:Cr 3+ , Eu 3+ порошок комнатной температуры. Спектр возбуждения, контролируемый при 697 нм, охватывает очень широкую спектральную область (от 200 до 650 нм) и состоит из четырех основных полос возбуждения с максимумами на 273, 328, 410 и 569 нм соответственно. Полоса возбуждения при 273 нм приписывается полосе переноса заряда O 2- -Ga 3+ в ZnGa 2 О 4 хост, в то время как более поздние полосы происходят из внутренних переходов Cr 3+ , включая полосу 328 нм, происходящую от 4 A 2 → 4 Т 1 ( te 2 ), полоса 410 нм, происходящая от 4 A 2 → 4 Т 1 ( т 2 е ), а полоса 569 нм, происходящая от 4 A 2 → 4 Т 2 ( т 2 е ) [19, 20]. Учреждение Eu 3+ не изменил заметно положение полос PLE, но значительно увеличил интенсивности внутренних переходов Cr 3+ , с I 410 / Я 273 увеличивается с 0,18 до 0,56. Приведенные выше результаты показывают, что Eu 3+ включение способствует возбуждению видимого света. Однако самая сильная полоса возбуждения при 273 нм также показала, что полоса переноса заряда O 2− -Ga 3+ - наиболее эффективная длина волны возбуждения. Возбуждение порошка при 273 нм давало полосу излучения в ближнем ИК-диапазоне при 697 нм (рис. 5) из-за 2 E → 4 A 2 переход в искаженном Cr 3+ ионы в галлогерманате, в отсутствие Eu 3+ эмиссия.
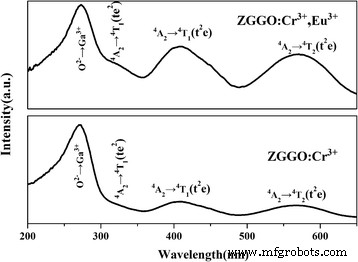
Спектры возбуждения фотолюминесценции (ВФЭ) ZGGO:Cr 3+ и ZGGO:Cr 3+ , Eu 3+ порошки
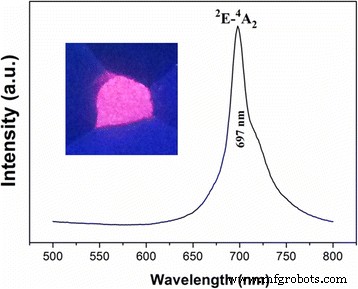
Спектры фотолюминесценции (ФЛ) ZGGO:Cr 3+ , Eu 3+ порошки
Кривые затухания стойкой люминесценции в ближнем ИК-диапазоне ZGGO:Cr 3+ и ZGGO:Cr 3+ , Eu 3+ Наночастицы контролировали на длине волны 697 нм после облучения УФ-светом 254 нм (ксеноновая лампа в качестве источника света) в течение 5 минут при комнатной температуре, как показано на рис. 6. Результат демонстрирует, что стойкая люминесценция в ближнем ИК-диапазоне ZGGO:Cr 3 + образец может длиться более 7200 с и при этом сохранять заметную интенсивность. Постоянная интенсивность люминесценции ZGGO:Cr 3+ , Eu 3+ увеличивается с включением Eu 3+ ион. Считается, что совместное легирование ионов лантаноидов с Cr 3+ в галлогерманате цинка будет давать замечательную стойкую люминесценцию в ближнем ИК-диапазоне из-за его важной роли в увеличении количества антиузельных дефектов, которые ответственны за стойкое свечение Cr 3+ в хозяине галлогерманата цинка [1]. С другой стороны, стойкое свечение ZGGO:Cr 3+ в ближнем ИК-диапазоне , Eu 3+ образец может длиться дольше, чем у ZGGO:Cr 3+ , что указывает на то, что Eu 3+ включение может увеличить время послесвечения. На рисунке 7 показаны изображения затухания послесвечения в ближнем ИК-диапазоне ZGGO:Cr 3+ . , Eu 3+ порошки, полученные с помощью системы визуализации Kodak In-Vivo FX Pro в разное время после прекращения УФ-облучения, что еще раз подтверждает, что послесвечение может длиться более 120 минут и сохранять интенсивность ближнего ИК-излучения.
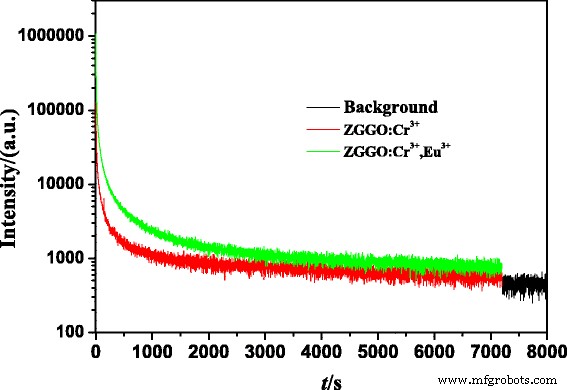
Кривые затухания стойкой люминесценции в ближнем ИК-диапазоне ZGGO:Cr 3+ и ZGGO:Cr 3+ , Eu 3+ порошки, контролируемые на длине волны 697 нм после облучения УФ-светом 254 нм в течение 5 минут

Изображения распада послесвечения в ближнем ИК-диапазоне ZGGO:Cr 3+ , Eu 3+ порошки, полученные с помощью системы визуализации Kodak In-Vivo FX Pro в разное время после прекращения УФ-облучения
Для оценки эффективности применения люминофора, особенно для приложений с большой мощностью, термическая стабильность является ключевым параметром. Для оценки термического тушения люминофоров в данной работе спектры ФЛ были проанализированы в диапазоне температур от 298 до 573 К (рис. 8). Для всех образцов повышение температуры приводило к уменьшению интенсивности излучения на 697 нм. Чтобы получить более полную картину поведения термического тушения и оценить значение его энергии активации ( E а ) уравнение Аррениуса (уравнение (1)) использовалось следующим образом [26,27,28]:
$$ {I} _ {\ mathrm {T}} =\ frac {I_0} {1 + c \ exp \ left (- \ frac {E _ {\ mathrm {a}}} {kT} \ right)} $$ (1)где I 0 и я T - интенсивности начальной и конечной температур соответственно; c - константа скорости; E а - энергия активации; и k - постоянная Больцмана (8.629 × 10 −5 эВ K −1 ). На рисунке 8 показан вход In ( I 0 / Я T - 1) против 10 000 / T линии соотношения для полосы излучения с центром при 697 нм для ZGGO:Cr 3+ и ZGGO:Cr 3+ , Eu 3+ . Были рассчитаны аналогичные энергии активации: E а =0,23 эВ для ZGGO:Cr 3+ и E а =0,25 эВ для ZGGO:Cr 3+ , Eu 3+ . Вероятность того, что безызлучательный переход произойдет в единицу времени ( α ) можно определить в соответствии с формулой. (2) следующим образом [29]:
$$ \ alpha =s \ \ exp \ left (- \ frac {E _ {\ mathrm {a}}} {kT} \ right) $$ (2)где s коэффициент частоты (s −1 ), k - постоянная Больцмана, а T это температура. Видно, что более низкая энергия активации ( E а ) приводит к большей вероятности ( α ) безызлучательного перехода. Из-за схожей энергии активации ZGGO:Cr 3+ и ZGGO:Cr 3+ , Eu 3+ демонстрирует закрытую термостабильность, что указывает на Eu 3+ включение существенно не повлияло на термическую стабильность. Однако ассоциированные боковые фононные полосы (PSB) с центром на 670 нм стали доминировать при более высокой температуре, что привело к усилению пиков излучения.
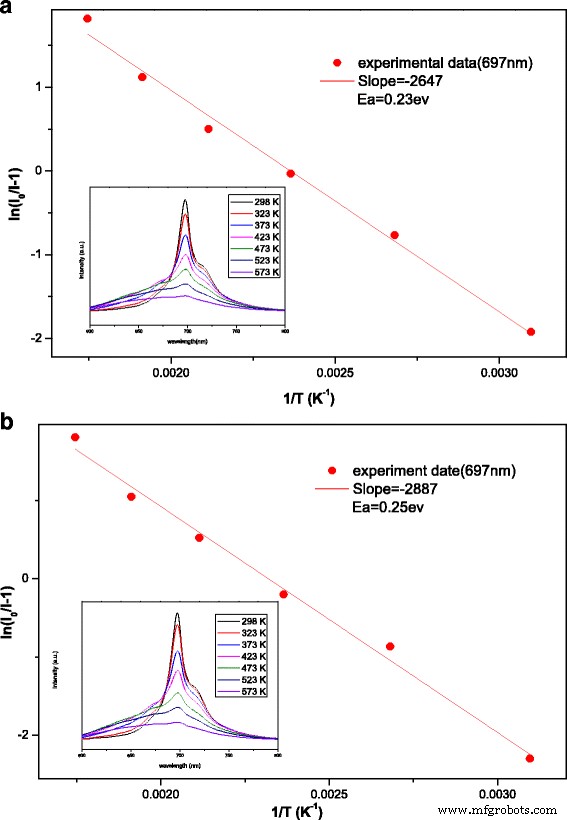
Энергия активации термического тушения для полос излучения в а ZGGO:Cr 3+ и b ZGGO:Cr 3+ , Eu 3+ порошки. На вставках показаны соответствующие температурные зависимости спектров ФЛ от 298 до 573 К
Мы также исследовали спектры возбуждения и излучения ФЛ водной дисперсии ZGGO:Cr 3+ , Eu 3+ (Рис.9). По сравнению с ZGGO:Cr 3+ , Eu 3+ порошка водная дисперсия показала почти такой же профиль кривых возбуждения и испускания ФЛ, за исключением относительно слабой интенсивности возбуждения при 300 и 600 нм. Снижение интенсивности, вероятно, связано с гасящим эффектом колебания O – H воды.
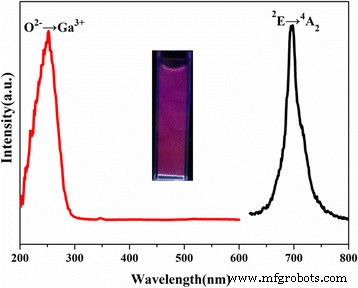
Спектры возбуждения и излучения ZGGO:Cr 3+ , Eu 3+ водный раствор при комнатной температуре. На вставке представлены цифровые фото ZGGO:Cr 3+ , Eu 3+ водный раствор при облучении УФ-светом 254 нм
Клетки Hek293T были использованы здесь для тестирования изображений in vitro. Полученный ZGGO:Cr 3+ , Eu 3+ -NH 2 Наночастицы диспергировали в клеточной среде (50 мг / мл), которую возбуждали в течение 10 мин УФ-лампой с длиной волны 254 нм, а затем перемещали в чашки для культивирования, обработанные в течение 1 ч. На рисунке 10 (слева, красный цвет) показаны изображения люминесценции клеток, полученные на лазерном сканирующем конфокальном микроскопе в отсутствие возбуждения. Сигнал люминесценции послесвечения клеток Hek293T был все еще достаточно сильным, чтобы его можно было точно измерить через 1 час, хотя сигналы люминесценции послесвечения постепенно уменьшались с течением времени. Для сравнения, изображение люминесценции клеток было получено на лазерном сканирующем конфокальном микроскопе в другом режиме от тех же клеток, окрашенных 0,5 мл красителя DAPI (справа на фиг. 10, одновременное возбуждение). Подобные сигналы изображения предполагают, что ZGGO:Cr 3+ , Eu 3+ -NH 2 наночастицы обладают отличной способностью визуализировать клетки in vitro.
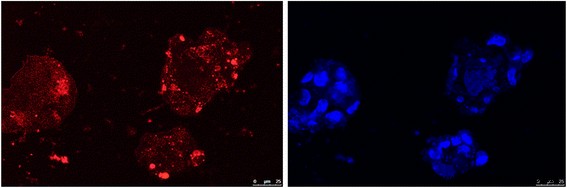
Изображение LSCM (слева, красный цвет) клеток Hek293T, инкубированных с ZGGO:Cr 3+ , Eu 3+ -NH 2 наночастиц в течение 1 ч. Правое изображение (синий цвет) представляет собой внешний вид тех же клеток, окрашенных 0,5 мл красителя DAPI. Масштабная линейка =25 мкм
Выводы
В данной работе шпинель структурирована ZGGO:Cr 3+ и ZGGO:Cr 3+ , Eu 3+ Наночастицы были синтезированы золь-гель методом в сочетании с последующим прокаливанием без восстановительной атмосферы. Образцы были исследованы с помощью детальных характеристик с помощью комбинированных методов XRD, TEM, STEM, SAED, PLE / PL спектроскопии и анализа зависимой от температуры PL. Наночастицы однородной кубической формы и поперечным размером ~ 80–100 нм представляют собой монокристаллический и однородный твердый раствор. Возбуждение порошка при 273 нм давало полосу излучения в ближнем ИК-диапазоне при 697 нм из-за 2 E → 4 A 2 переход в искаженном Cr 3+ ионы в галлогерманате, в отсутствие Eu 3+ эмиссия. Постоянное свечение ZGGO:Cr 3+ в ближнем ИК-диапазоне , Eu 3+ может длиться более 7200 с и при этом сохранять высокую интенсивность. Постоянная интенсивность люминесценции ZGGO:Cr 3+ и время послесвечения увеличивается с введением Eu 3+ ион. Однако Eu 3+ включение существенно не повлияло на термическую стабильность. Наконец, полученный ZGGO:Cr 3+ , Eu 3+ -NH 2 наночастицы обладают отличной способностью визуализировать клетки in vitro.
Наноматериалы
- Ученые IBM впервые продемонстрировали раскачку броуновских двигателей для наночастиц
- Наночастицы золота для химиотерапевтических датчиков
- Наночастицы для терапии рака:текущий прогресс и проблемы
- Эмульгированный полисорбат 80-донепезил, нацеленный на мозг, наночастицы, содержащие лекарственное средство,…
- Нанотехнологии:от системы визуализации in vivo к контролируемой доставке лекарств
- Изучение in vitro влияния наночастиц Au на клеточные линии HT29 и SPEV
- Новые биосовместимые наночастицы Au Nanostars @ PEG для КТ-визуализации in vivo и свойства очищения почек
- Синтез и эффективность in vitro покрытых полипирролом железо-платиновых наночастиц для фототермической терапии…
- Сравнение функционализации магнитных наночастиц Fe3O4 на основе фолиевой кислоты и пептида gH625 для усиления ин…
- Метод мечения клеток с помощью микроскопии, адаптированный для использования в визуализации всего тела



