Нанотехнологии:от системы визуализации in vivo к контролируемой доставке лекарств
Аннотация
Наука и технологии всегда были жизненно важными элементами борьбы человечества, использовавшимися исключительно для разработки новых инструментов и продуктов, от микро- до наноразмеров. Нанотехнология привлекла к себе большое внимание благодаря ее широкому применению в биомедицине, особенно в области био-визуализации и доставки лекарств. Для диагностики и лечения различных заболеваний разработаны различные наноустройства и наноматериалы. Здесь мы описали два основных аспекта наномедицины, то есть визуализацию in vivo и доставку лекарств, подчеркнув недавние достижения и будущие исследования. Недавно были отмечены огромные достижения в области нанотехнологий для получения изображений, особенно раковых клеток. Наночастицы предлагают подходящую среду для проведения модификаций на молекулярном уровне, включая сайт-специфическую визуализацию и нацеливание. Изобретение радионуклидов, квантовых точек, магнитных наночастиц и углеродных нанотрубок, а также использование наночастиц золота в биосенсорах произвело революцию в области визуализации, что привело к легкому пониманию патофизиологии заболевания, улучшенной диагностике и улучшенному терапевтическому лечению. Такая высокая специфичность и избирательность наномедицины важны, и, следовательно, необходимо понимать последние достижения в этой области, чтобы добиться лучшего сегодня и более благополучного будущего.
Обзор
Введение
Фактически, нанотехнология продвигается вперед во всех важнейших областях инженерии и науки, и ученые революционизируют все отрасли и человеческую жизнь, создавая вещи, способные работать в мельчайших масштабах, атом за атомом [1]. Нанотехнология предполагает изучение в высшей степени небольших структур. Нанотехнологию можно всесторонне определить как исследование, создание, проектирование, синтез и внедрение функциональных материалов, систем и устройств посредством управления материей в диапазоне размеров 1–100 нм в нанометровом масштабе. Более того, манипулирование инновационными явлениями и улучшенными свойствами материи в этом нанометровом масштабе, также известное как молекулярная нанотехнология, является волшебной точкой на масштабе, где мельчайшие искусственные устройства сталкиваются с молекулами и атомами Вселенной [2,3,4 ].
Концепция нанотехнологии и наномедицины зародилась на основе проницательной идеи Фейнмана о том, что крошечные нанороботы и связанные с ними устройства могут быть разработаны, изготовлены и внедрены в человеческий организм для восстановления клеток на молекулярном уровне. Хотя позднее, в 1980-х и 1990-х годах, эта новаторская концепция пропагандировалась в знаменитых трудах Дрекслера [5, 6], а в 1990-х и 2000-х годах - в популярных трудах Фрейтаса [7, 8]. Фейнман предложил первое известное предложение наномедицинской процедуры для лечения сердечных заболеваний. В целом миниатюризация медицинских инструментов обеспечит более точные, контролируемые, надежные, универсальные, экономичные и быстрые подходы к повышению качества жизни человека [9]. В 2000 году впервые была запущена Национальная нанотехнологическая инициатива; затем с этого момента моделирование электроники и молекулярных структур новых материалов, создание наноразмерных фотонных и электронных устройств [10, 11], развитие трехмерных сетей, наноробототехника [12] и появление многочастотной силовой микроскопии [13] проложили путь путь появления молекулярных нанотехнологий.
Наночастицы считаются важнейшими строительными блоками нанотехнологий. Наличие сильных химических связей, обширная делокализация валентных электронов, меняющихся в зависимости от размера, и структурные модификации наночастиц приводят к различным физическим и химическим свойствам, включая точки плавления, оптические свойства, магнитные свойства, удельную теплоемкость и поверхностную реактивность. Эти сверхмелкозернистые наночастицы демонстрируют совершенно новые и улучшенные свойства по сравнению с их объемными аналогами из-за различий в конкретных характеристиках, таких как размер, распределение и частицы, которые приводят к увеличению отношения площади поверхности к объему [14,15,16]. По мере развития области наноструктурированных материалов используется множество различных обозначений и терминологии, включая трехмерные наночастицы, нанокристаллы, нанопленки, нанотрубки, нанопроволоки и квантовые точки с многообещающим потенциалом бесконечного числа свойств [17]. Из-за разнообразия потенциальных применений (включая промышленное и военное) правительства вложили миллиарды долларов в исследования в области нанотехнологий. США инвестировали 3,7 миллиарда долларов в рамках своей Национальной инициативы в области нанотехнологий, Европейский союз также субсидировал 1,2 миллиарда долларов, а 750 миллионов долларов были инвестированы Японией [18].
Сегодня нанотехнология - одна из самых инновационных и авангардных областей научных исследований, и она продолжает развиваться ошеломляющими темпами [19]. Благодаря развитию нанотехнологий для доставки лекарств стали доступны многие современные технологии. Исследователи всесторонне исследовали потенциал наноустройств для целевой и контролируемой доставки различных микро- и макромолекул, включая лекарства, белки, моноклональные антитела и ДНК (дезоксирибонуклеиновая кислота), в различных биомедицинских приложениях, таких как рак [20, 21], вакцинация [22]. , стоматологические [23], воспалительные [24] и другие нарушения здоровья. Поэтому сегодня необходимо продемонстрировать эффективное использование приложений нанотехнологий, начиная от системы визуализации in vivo и заканчивая контролируемой доставкой лекарств, чтобы отметить текущий прогресс и получить указания для предстоящих исследований в медицинских областях.
Фармацевтические наносистемы
Фармацевтические нанотехнологии можно разделить на две основные категории нанотехнологий, то есть наноматериалы и наноустройства. Наноматериалы можно разделить на три основных параметра, включая структуру, размер и фазовый состав. Наноструктуры далее подразделяются на полимерные и неполимерные структуры, включая наночастицы, мицеллы, дендримеры, конъюгаты лекарств, металлические наночастицы и квантовые точки [25]. В зависимости от размеров наноматериалы делятся на четыре группы:материалы с нулевым, одним, двумя и тремя наноразмерными размерами. По фазовому составу эти наноматериалы можно разделить на три группы. Наноустройства подразделяются на три группы, включая микроэлектромеханические системы / наноэлектромеханические системы (MEMS / NEMS), микроматрицы и респироциты. Эти структуры и устройства могут быть изготовлены с высокой степенью функциональных свойств для использования в медицине для взаимодействия с клетками на молекулярном уровне, что позволяет достичь такой степени интеграции между биологическими системами и новейшими технологиями, которая ранее была недостижима [26]. Подробная классификация фармацевтических наноинструментов с примерами описана в Таблице 1.
Подходы к производству
Технологии наноразмеров приобрели большое значение для создания лекарств, плохо растворимых в воде. При уменьшении размера частиц до наномасштаба скорость растворения и биодоступность увеличиваются из-за увеличения площади поверхности в соответствии с уравнением Нойса-Уитни [27]. Подходы, используемые для изготовления материалов, подразделяются на методы снизу вверх, методы сверху вниз и комбинации методов снизу вверх и сверху вниз. Методы «снизу вверх» включают построение молекул. Некоторые из методов, которые следуют восходящему подходу для производства наноразмерных материалов, включают жидкофазные методы, основанные на обращенных мицеллах, химическом осаждении из паровой фазы (CVD), золь-гель обработке и молекулярной самосборке. Компоненты, полученные снизу вверх, значительно сильнее, чем компоненты макромасштаба, из-за ковалентных сил, удерживающих их вместе. В методах «сверху вниз» материалы тонко измельчаются путем резки, вырезания и формования для производства наноматериалов. Примеры включают измельчение, физическое осаждение из паровой фазы, гальваническое покрытие с использованием гидродермальных технологий и нанолитографию [28]. Различные подходы к производству с соответствующими типами описаны в таблице 2.
Биомедицинские приложения передовых нанотехнологий
Изображение
Сообщалось об огромных достижениях за последнее десятилетие в использовании инструментов нанотехнологии для визуализации и терапии в исследованиях, особенно нацеленных на раковые клетки. Наночастицы размером 10–100 нм представляют собой очень подходящую среду для проведения модификаций на молекулярном уровне, таких как сайт-специфическая визуализация и нацеливание на раковые клетки [29]. В следующем разделе кратко описаны некоторые недавние достижения в области методов визуализации.
Радионуклидное изображение
Из-за невозможности наблюдения за небольшими молекулами с помощью неинвазивной техники, сайт-нацеленные контрастные агенты используются для идентификации выбранного биомаркера, который невозможно отделить от нормальных окружающих тканей [30]. Радионуклидная визуализация была разработана с концепцией, согласно которой экспрессируемый белок исследуется с помощью радиофармацевтического или изотопно-меченного агента или клетки и далее отслеживается in vivo [31]. Позитронно-эмиссионная томография (ПЭТ) успешно используется у онкологических больных для визуализации множественной лекарственной устойчивости через транспорт P-гликопротеина с использованием 99 m тетрофосмина и сестамиби в качестве радиоактивно меченых субстратов для P-гликопротеина [32, 33]. Механизм визуализации определяется типом модальности, используемой для визуализации, такой как наноносители, включая липосомы [34], дендримеры [35], шары Баки [36] и многочисленные полимеры и сополимеры [37]. Они могут быть заполнены большим количеством частиц для визуализации, таких как оптически активные соединения и радионуклиды, для обнаружения с помощью оборудования для визуализации. Меченые BODIPY (дипиррометан бора) аналоги джасплакинолида были использованы для визуализации долгоживущих актиновых филаментов внутри живых клеток [38, 39].
Огромный рост нанотехнологий ведет к исследованиям в области молекулярной визуализации с использованием многих контрастных веществ. Чтобы получить соответствующее изображение, выбранный контрастный агент должен иметь более длительный период полужизни, низкий фоновый сигнал, специфическое связывание эпитопа и усиление контрастности к шуму. Наличие большого числа носителей позволяет определить больше достижений в области визуализации с особым вниманием к молекулярным и клеточным механизмам заболевания; это создаст больше возможностей для рационального развития систем визуализации и доставки лекарств [30].
Квантовые точки
Полупроводниковые квантовые точки теперь используются как новый класс флуоресцентных меток. Эти полупроводниковые нанокристаллы являются многообещающим инструментом для визуализации биологических клеток из-за их легкого химического состава поверхности, обеспечивающего биосовместимость и, следовательно, конъюгацию с увеличением времени флуоресценции [29, 40]. Визуализирующие свойства квантовых точек (длина волны флуоресценции) сильно зависят от размера. Оптические свойства квантовых точек зависят от их структуры, поскольку они состоят из внешней оболочки и металлического ядра. Например, графемные квантовые точки (GQD), разновидность углеродных наноматериалов с зеленой флуоресценцией, изготавливаются путем сольвотермической резки оксида графема и, как выяснилось, доминируют в визуализирующих свойствах [41].
Ядро квантовой точки обычно состоит из селенида кадмия, сульфида кадмия или теллурида кадмия. Внешняя оболочка изготовлена на сердечнике с большой шириной запрещенной зоны, чтобы обеспечить электрическую изоляцию с сохранением флуоресцентных свойств квантовых точек. Точно настроенное ядро и оболочки различного размера и состава с визуализирующими свойствами определенной длины волны обеспечивают большое количество биомаркеров [40]. Квантовые точки конъюгированы с разными лигандами для получения специфического связывания с биологическими рецепторами. Лиганды, нацеленные на опухоль, связаны с квантовыми точками амфифильных полимеров и используются для проведения визуализационных исследований рака простаты у мышей [42]. Точно так же квантовые точки обладают значительными преимуществами по сравнению с обычными красителями, такими как узкая ширина полосы излучения, более высокая фотостабильность и расширенный спектр поглощения для единственного источника возбуждения. Более того, проблема гидрофобности квантовых точек была решена за счет того, что они стали водорастворимыми. Примером водных квантовых точек с длительным временем удерживания в биологических жидкостях является разработка квантовых точек с высокой флуоресценцией сульфидов металлов (МС), изготовленных с тиолсодержащими заряженными группами [43]. Кроме того, уникальные флуоресцентные свойства квантовых точек сделали их подходящими инструментами для визуализации раковых клеток [42]. Квантовые точки, связанные с аптамером РНК A10, конъюгированным с доксорубицином (QD-Apt-Dox), являются примером нацеленной визуализации раковых клеток [44]. Однако наблюдалась повышенная токсичность квантовых точек из-за включения тяжелых металлов, что привело к их ограниченному использованию для визуализации in vivo. Тем не менее, недавние подходы сосредоточены на снижении токсичности и повышении биосовместимости квантовых точек с клетками организма. Также стоит упомянуть, что квантовые точки диаметром менее 5,5 нм быстро и эффективно выводятся из мочи, что снижает токсичность. Это явление было продемонстрировано синтезом без кадмия, CulnS 2 / ZnS (сульфид меди, индия / сульфид цинка) в качестве ядра и оболочки квантовых точек, что привело к повышению стабильности живых клеток при визуализации лимфатических узлов с четким снижением острой местной токсичности [45, 46].
Биосенсоры
Одним из величайших достижений в области наноматериалов за последние несколько лет является разработка биосенсоров. Биосенсоры - это устройства, которые содержат биологический чувствительный элемент, подключенный или интегрированный в датчик. Биосенсор проявляет свое действие путем распознавания определенных молекул в организме на основе их структуры, включая антиген антитела, ферментный субстрат и рецепторный гормон. Два основных свойства биосенсора, включая их специфичность и избирательность, зависят от этой системы распознавания. Эти основные свойства биосенсоров наиболее важны для определения концентрации, которая пропорциональна сигналам [47,48,49].
Для производства биосенсора с высокой эффективностью предварительным условием является выбор субстрата для диспергирования чувствительного материала. На биосенсоры наносятся различные типы наноматериалов, включая квантовые точки [50], магнитные наночастицы [51], углеродные нанотрубки (УНТ) [52] и наночастицы золота (ЗНЧ) [53]. Отличительные химические, физические, магнитные, оптические и механические свойства наноматериалов приводят к их повышенной специфичности и чувствительности для обнаружения. Биосенсоры, содержащие ЗНЧ, предложили совместимую среду для биомолекул, которая увеличила концентрацию иммобилизованных биомолекул на поверхности электрода. Это привело к повышению чувствительности биосенсоров [54, 55]. Наиболее широко используемые электродные поверхности в биосенсорах - это стеклоуглеродные электроды (GCE), модифицированные на основе ЗНЧ. Кроме того, они показали лучшую чувствительность, а также электрохимическую стабильность. В этом отношении метиленовый синий (МБ) и ЗНЧ легко собираются и модифицируются методом слой за слоем (LBL) в виде пленок на GCE, чтобы определять концентрацию хорионического гонадотропина человека (ХГЧ) [56]. Благодаря большой площади поверхности, содержащейся в наночастицах для загрузки анти-ХГЧ, эти иммуносенсоры могут использоваться для определения концентраций ХГЧ в образцах крови или мочи человека. Точно так же УНТ нашли широкое применение в биомедицинской инженерии, биоанализе, био-зондировании и наноэлектронике [57,58,59]. Более того, многослойные углеродные нанотрубки (MWNT) в виде бионанокомпозитных слоев полимеров могут быть использованы для обнаружения ДНК [60]. Кроме того, магнитные наночастицы также нашли широкое применение благодаря своим магнитным свойствам, включая контрастный агент для магнитно-резонансной томографии (МРТ) [61], гипертермию [62], иммуноанализ [63], восстановление тканей [64], разделение клеток [65], GMR-сенсор [66] и доставка лекарств или генов [67].
Аналогичным образом, новый тип магнитных микросфер хитозана (MCMS) был произведен простым использованием хитозана и магнитных наночастиц, покрытых углеродом [68]. В этом исследовании гемоглобин также был успешно иммобилизован на поверхности GCE, модифицированной MCMS, с использованием глутаральдегида в качестве сшивающего агента. Другое важное применение биосенсоров - это оптическая технология, которая включает обнаружение различных видов ДНК-олигонуклеотидов с использованием зондов SsDNA-CNT в качестве биосенсоров [69]. Точно так же биосенсоры на основе липосом также привлекли значительное внимание, поскольку они использовались для мониторинга фосфорорганических пестицидов, включая параоксон и дихлофос на минимальных уровнях [70].
Магнитные наночастицы
Магнитные наночастицы (МНЧ) обладают исключительными магнитными свойствами, поскольку они обладают способностью работать на молекулярном или клеточном уровне биологических взаимодействий, что делает их лучшими соединениями в качестве контрастных агентов при МРТ и в качестве носителей при доставке лекарств. Недавние достижения в области нанотехнологий привлекли внимание, поскольку они помогли изменить свойства и особенности MNP для биомедицинских приложений. В этом отношении было показано, что визуализация опухоли печени и метастазов с помощью RES-опосредованного поглощения суперпарамагнитных оксидов железа (SPIO) способна дифференцировать поражения размером всего 2–3 мм [70, 71]. Более того, эти сверхмалые сверхмагнитные оксиды железа (USPIO) также очень эффективны при визуализации метастазов лимфатических узлов диаметром всего от 5 до 10 мм [72]. Кроме того, важность этого неинвазивного подхода также была продемонстрирована при обнаружении лимфатической диссеминации, поскольку она считается важной частью при определении стадии, а также при определении подходов к лечению рака молочной железы, толстой кишки и предстательной железы [73].>
Доставка лекарств
Нанотехнологии - привлекательный инструмент для различных дисциплин, от материаловедения до биомедицины, из-за их различных физических, оптических и электронных характеристик. Наиболее эффективными областями исследований в области нанотехнологий являются наномедицина, в которой применяются принципы нанотехнологий для лечения, профилактики и диагностики заболеваний. Более того, многие продукты наномедицины были проданы в связи с резким ростом исследований наномедицины в течение последних нескольких десятилетий по всему миру. В настоящее время на наномедицину влияют системы доставки лекарств, на долю которых приходится более 75% общих продаж [74]. В этом отношении платформы доставки лекарств на основе наночастиц завоевали доверие ученых как наиболее подходящие средства для устранения фармакокинетических недостатков, связанных с традиционными лекарственными формами [75]. Таким образом, различные наноформы были опробованы в качестве систем доставки лекарств, таких как липосомы, твердые липидные наночастицы, дендримеры и твердые металлсодержащие НЧ, для повышения терапевтической эффективности лекарств [76, 77]. Некоторые из основных областей интересов обсуждаются ниже.
Офтальмология
Доставка лекарств офтальмологическим путем является очень привлекательной, но сложной задачей для ученых-фармацевтов. Глаз - это крошечный замысловатый орган с множеством отделений. Его биохимия, физиология и анатомия сделали его наиболее непроницаемым для ксенобиотиков. Общие состояния, требующие окулярного введения, включают глазные инфекции, такие как конъюнктивит, наряду с заболеваниями роговицы, такими как глаукома. Наиболее распространенные классы лекарств, используемых для доставки в глаза, включают мидриатические или циклоплегические миотики, противоинфекционные, противовоспалительные, диагностические и хирургические адъюванты. При небольшом нарушении зрения также требуется генная терапия, и в этой области проводится большой объем работы. Подходы, поддерживаемые наноносителями, привлекли внимание ученых своей пригодностью и специфичностью. Сообщалось, что система доставки частиц, такая как микросферы и наночастицы, и везикулярные носители, такие как липосомы, ниосомы, фармакосомы и дискомы, улучшают фармакокинетические и фармакодинамические свойства различных типов молекул лекарств [76]. Появилось много новых систем контролируемой доставки лекарств, включая гидрогели, мукоадгезивные полимеры, микроэмульсии, дендримеры, ионтофоретическую доставку лекарств, подходы на основе миРНК, технологию стволовых клеток, невирусную генную терапию и лазерную терапию с помощью заглушек склеры [78] . Для доставки лекарственного средства глазным путем используются различные системы доставки лекарств. Основная цель всех систем доставки лекарств - улучшить период пребывания, повысить проницаемость роговицы и высвободить лекарство в задней камере глаза, что приведет к увеличению биодоступности и улучшению соблюдения пациентом режима [79].
Abrego et al. подготовили наночастицы пранопрофена PLGA (сополимер молочной кислоты) для офтальмологической доставки в форме гидрогеля. Этот состав гидрогеля имеет подходящие реологические и физико-химические свойства для доставки пранопрофена в глаза с улучшенными биофармацевтическими характеристиками лекарственного средства. Кроме того, он усилил местные противовоспалительные и обезболивающие эффекты препарата, что привело к улучшению соблюдения пациентом режима лечения [80]. В другом исследовании наночастицы хитозана, нагруженные цефуроксимом, были разработаны с использованием двойного сшивания в технике двойной эмульсии. Вывод указывает на то, что частицы хитозан-желатина являются потенциально практическими кандидатами на ДД на внутриглазном уровне [81]. Более того, нагруженные диклофенаком наночастицы N-триметил хитозана (DC-TMCNs) были разработаны для офтальмологического применения с целью улучшения биодоступности препарата в глазах [82]. Кроме того, были разработаны наноразмерные супрамолекулярные сборки дексаметазон фосфата на основе хитозана для улучшения времени пребывания лекарственного средства на роговице благодаря его мукоадгезивным характеристикам. Эти наночастицы сильно взаимодействуют как с поверхностью глаза, так и с лекарством и защищают лекарство от метаболической деградации, что приводит к длительному пребыванию на роговице [83]. Глаукому, офтальмологическое заболевание, лечили нагруженными твердыми липидными наночастицами с замедленным высвобождением на основе бримонидина с использованием моностеарата глицерина в качестве твердого липида [84, 85]. Аналогичным образом были разработаны нагруженные даптомицином наночастицы альгината, покрытого хитозаном (CS-ALG), с подходящим размером для глазных применений и высокой эффективностью инкапсуляции (до 92%). Это исследование показало, что система наноносителя даптомицина может быть использована в будущем для доставки этого антибиотика непосредственно в глаз, чтобы действовать в качестве перспективной терапии против бактериального эндофтальмита и в качестве эффективной альтернативы наночастицам хитозана [86].
Одной из основных причин краткосрочной и долгосрочной несостоятельности трансплантатов при трансплантации роговицы является иммунологическое отторжение трансплантата. Для этой цели была приготовлена система биоразлагаемых наночастиц дексаметазона-фосфата натрия (DSP) на основе PLGA, в результате чего кортикостероиды замедлялись, чтобы предотвратить отторжение трансплантата роговицы [87]. Более того, сообщалось о наночастицах куркумина MePEG-PCL (полиэтиленгликоль-поликапролактон), которые показали повышенную эффективность, улучшенное удержание куркумина в роговице и значительное улучшение предотвращения неоваскуляризации роговицы по сравнению со свободным куркумином [88]. Точно так же был разработан тканевый клей, наполненный наночастицами серебра (2-октилцианоакрилат), с повышенной механической прочностью и антибактериальной эффективностью. Эти легированные адгезивы (наночастицы серебра) способствовали использованию тканевых адгезивов в качестве жизнеспособного дополнения или альтернативы шовным материалам [89].
Пульмонология
Заболевания легких, вероятно, астма, хроническая обструктивная болезнь легких (ХОБЛ) и рак легких, встречаются часто и часто опасны для жизни. Например, описано, что ХОБЛ является четвертой основной причиной смерти, а рак легких - наиболее распространенной причиной смерти от рака во всем мире. Наночастицы исследуются как средство выбора для улучшения терапии этих тяжелых заболеваний [90]. Различные наночастицы, содержащие лекарственные препараты, были использованы из-за их местного и системного воздействия при лечении заболеваний легких. Доставка лечебных агентов к месту действия при заболеваниях легких может позволить эффективное лечение хронических инфекций легких, рака легких, туберкулеза и других респираторных патологий [91]. К наноносителям, используемым для этой цели, относятся липосомы, мицеллы на основе липидов или полимеров, дендримеры и полимерные НЧ [92]. Полимерные наночастицы представляют собой предварительный интерес, поскольку полимеры могут быть сополимеризованы, поверхностно модифицированы или биоконъюгированы для улучшения направленной способности и распределения инкапсулированных агентов. Обычно используемые наноносители для доставки лекарств в легкие содержат природные полимеры, такие как желатин, хитозан и альгинат, и синтетические полимеры, такие как полоксамер, PLGA и PEG [93].
Было замечено, что НЧ PLGA демонстрируют наиболее удобный набор характеристик в качестве носителей для доставки легочного белка / ДНК, в то время как НЧ желатина являются приемлемым обоюдным выбором [94]. Точно так же анизотропные или янусовые частицы доксорубицина и куркумина были приготовлены для доставки противоопухолевых препаратов для лечения рака легких путем ингаляции. Частицы были составлены с использованием бинарных смесей биосовместимых и биоразлагаемых материалов. Эти частицы не проявляли гено- и цитотоксических последствий. Раковые клетки усваивают эти частицы Януса и собирают их в ядре и цитоплазме, что приводит к их длительному удержанию. Более того, дендримеры полиамидоамина (PAMAM) были оценены как наноносители для легочной доставки модельного слаборастворимого противоастматического фармацевтического препарата беклометазона дипропионата (BDP) с использованием дендримеров G3, G4 и G4 [12]. Это исследование показало, что BDP-дендримеры обладают потенциалом для легочной ингаляции с использованием небулайзеров с воздушной струей и вибрирующей сеткой. Кроме того, было замечено, что на характеристики аэрозоля влияет конструкция распылителя, а не образование дендримеров [95]. Кроме того, инженерные наночастицы (ENP), состоящие из неорганических металлов, оксидов металлов, металлоидов, органических биоразлагаемых и неорганических биосовместимых полимеров, эффективно использовались в качестве носителей для доставки вакцины и лекарств, а также для лечения различных заболеваний легких. Свойства и эффективное воздействие ENP на легкие представлены на рис. 1. Неорганические ENP (серебро, золото и углерод), оксиды металлов (оксиды железа, оксиды цинка и диоксид титана) и органические ENP (на основе липидов, на основе полисахаридов, на основе полимерной матрицы) были разработаны и оценены для легочного иммунного гемостаза. Современные исследования показали, что они не только являются относительно безопасными носителями, но и обеспечивают благоприятные исходы с противовоспалительными свойствами (например, серебро и полистирол) и легкие, которые обеспечивают поддержание иммунного гомеостаза (например, полистирол). Дальнейшее знание механизмов может помочь лучше понять полезные эффекты ENP на легочный иммунный гомеостаз и / или управление воспалительным заболеванием легких [96].
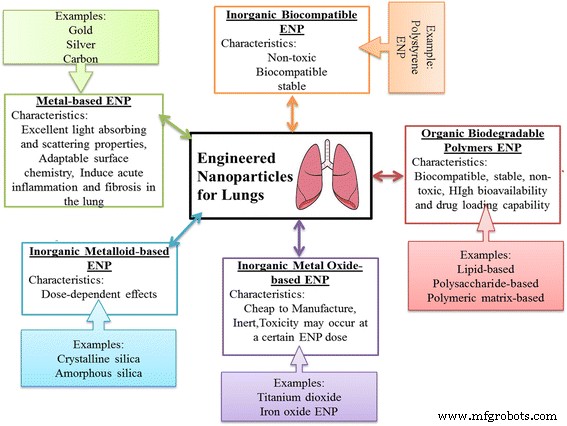
Свойства и эффективное действие ENP на легкие
Важно отметить, что функционализированный катионный липо-полиамин (Star:Star-mPEG-550) был недавно разработан для доставки siRNA (короткая интерференционная РНК) in vivo к легочным сосудистым клеткам. Этот сбалансированный липидный состав усиливает удержание миРНК в легких мыши и обеспечивает значительную разборку целевого гена. Результаты оказались полезными и со сниженной токсичностью доставки ингибитора miRNA-145 в легкие за счет использования функционализированных катионных наночастиц липополиамина для активизации легочной артериопатии и исправления функции сердца у крыс с интенсивной легочной артериальной гипертензией (ЛАГ) [97]. / P>
Сердечно-сосудистая система
Сердечно-сосудистые заболевания - это заболевание, поражающее сердечно-сосудистую систему, сосудистые заболевания головного мозга и почек, а также заболевание периферических артерий. Несмотря на все достижения в фармакологическом и клиническом лечении, сердечная недостаточность является основной причиной заболеваемости во всем мире. Многие новые терапевтические стратегии, включающие трансплантацию клеток, доставку генов или терапию, а также цитокины или другие небольшие молекулы, были изучены для лечения сердечной недостаточности [98]. В развивающихся странах страдает недостаточное количество людей; более 80% смертей от сердечно-сосудистых заболеваний происходит в слаборазвитых странах и почти равномерно среди мужчин и женщин [99]. Mathers et al. по оценкам 2008 г., ежегодно умирает 9,4 миллиона человек [100]. Это означает, что 45% смертей вызваны ишемической болезнью сердца, а 51% - сердечными приступами [101]. Существует множество различных типов носителей для доставки лекарств, таких как полимерные мицеллы, липосомы, дендримеры, фармацевтические носители на липопротеинах и носители лекарств в виде наночастиц.
Липосомы сиролимуса на основе хитозана с эффективностью захвата ≥83% были разработаны для лечения рестеноза и оказались новой платформой для эффективной адресной доставки [102]. Точно так же ниосомы карведилола, обогащенные желчными солями, с эффективностью захвата 85% привели к повышенной биодоступности лекарственного средства и, таким образом, к лучшему терапевтическому эффекту [103]. Ингибирование рестеноза в сонной артерии, поврежденной баллоном, достигается у крыс путем разработки наночастиц на основе PLGA, инкапсулирующих AGL 2043 и AG1295, селективных блокаторов рецепторов факторов роста тромбоцитов (PDGF) [104]. Angiogenic therapy of myocardial ischemia with vascular endothelial growth factor (VEGF) is a favorable approach to overcome hypoxia and its sequel effects. Polymeric particles loaded with VEGF have been proved a promising system for delivery of cytokines to rat myocardial ischemic model. This approach could be further explored for clinical studies [105]. Coenzyme Q10 (CoQ10) owing to its role in mitochondrial electron transport chain appears to be a reliable candidate to treat myocardial ischemia (MI) but its poor biopharmaceutical characteristics needed to be addressed by developing promising delivery approaches. Polymeric nanoparticles were developed to encapsulate CoQ10 to overcome its poor pharmaceutical properties and administered to MI-induced rats. Cardiac function was analyzed by determining ejection fraction before and after 3 months of therapy. Results showed significant betterment in the ejection fraction after 3 months [106].
Oncology
Cancer is a prime cause of mortality around the globe. The World Health Organization determines that 84 million people die of cancer between 2005 and 2015. The eventual target of cancer therapeutics is to increase the life span and the quality of life of the patient by minimizing the systemic toxicity of chemotherapy [107]. Chemotherapeutic agents have widely been studied in oncology for the past 25 years, but their tumor specificity is unsatisfactory and therefore exhibit dose-dependent toxicity. To overcome this limitation, recent interest has been centered on developing nanoscale delivery carriers that can be targeted directly to the cancer cell, deliver the drug at a controlled rate, and optimize the therapeutic efficacy [108, 109]. Passive and active targeting is used to deliver the drug at its tumor site. The passive phenomenon called the “enhanced permeability and retention (EPR) effect,” discovered by Matsumura and Maeda, is the dominated pathway used for chemotherapeutics [110, 111]. Active targeting is achieved by grafting ligand at the surface of nanocarriers that bind to receptors or stimuli-based carriers, e.g., dual reverse thermosensitive [112], photo-responsive [113], magnetic nanoparticles [114], and enzymatically activated pro-drugs [115]. Nanoparticles (NPs) can be conjugated with various smart therapeutic carriers like polymeric nanoparticles [116], micelles [117], liposomes [118], solid lipid nanoparticles (SLNs) [119], protein nanoparticles [120], viral nanoparticles [121], metallic nanoparticles [122], aptamers [123], dendrimers [124], and monoclonal antibody [125] to improve their efficacy and decrease the systemic toxicity. Table 3 summarizes the different approaches for drug deliveries which are widely studied to target the tumor with maximize therapeutic response and minimum toxicity.
Biodegradable poly (o-caprolactone) nanocarriers loaded with tamoxifen were developed for the management of estrogen receptor-specific breast cancer [126]. This study suggested that the nanoparticle preparations of selective estrogen receptor modulators deliver the drug in the specific estrogen receptor zone resulting in enhanced therapeutic efficacy. Similarly, a nanoconjugation of doxorubicin and cisplatin was developed by Chohen et al. [127], which have exhibited enhanced efficiency and reduced side effects of the loaded drugs in the treatment of localized progressive breast cancer. Likewise, chemotherapeutic drug oxaliplatin-loaded nanoparticulate micelles were prepared by Cabral et al. [128], with sustained release of loaded drug in the tumor microenvironment, resulted in enhanced antitumor effect [128]. Furthermore, SLN loaded-5-FU resulted in enhanced bioavailability and sustained release of the encapsulated anticancer drug, leading to enhanced antitumor effect [129].
Conclusions
Nanotechnology is subjected to inordinate progress in various fronts especially to make innovations in healthcare. Target-selective drug delivery and approaches for molecular imaging are the areas of prime importance for research where nanotechnology is playing a progressive role. This review provides readers with a wide vision on novel ongoing potentialities of various nanotechnology-based approaches for imaging and delivery of therapeutics. In order to obtain effective drug delivery, nanotechnology-based imaging has enabled us to apprehend the interactions of nanomaterials with biological environment, targeting receptors, molecular mechanisms involved in pathophysiology of diseases, and has made the real time monitoring of therapeutic response possible. Development of analytical technologies to measure the size of particles in nanometer ranges, and advent of latest manufacturing approaches for nanomaterials, has resulted in establishment of more effective methods for delivery of therapeutics for the treatment of ophthalmological, pulmonary, cardiovascular diseases, and more importantly cancer therapy. These new drug therapies have already been shown to cause fewer side effects and be more effective than traditional therapies. Furthermore, the imaging techniques have enhanced the determination of tumor location in human bodies and their selective targeting. Altogether, this comparatively new and thriving data suggest that additional clinical and toxicity studies are required further on the “proof-of-concept” phase. Nanomedicine cost and manufacturing at larger scale is also a matter of concern that needs to be addressed. Notwithstanding, future of nanomedicines is propitious.
Сокращения
- AIE:
-
Aggregation-induced emission
- BDP:
-
Beclometasone dipropionate
- BODIPY:
-
Boron dipyrromethane
- CNTs:
-
Carbon nanotubes
- COPD:
-
Chronic obstructive pulmonary disease
- CulnS2 /ZnS:
-
Copper indium sulfide/zinc sulfide quantum dots
- CVD:
-
Химическое осаждение из паровой фазы
- DNA:
-
Deoxyribonucleic acid
- ENPs:
-
Engineered nanoparticles
- EPR:
-
Enhanced permeability and retention
- GCE:
-
Стеклоуглеродный электрод
- ВНП:
-
Наночастицы золота
- GQD:
-
Grapheme quantum dots
- HCG:
-
Human chorionic gonadotrophin
- MEMS:
-
Microelectromechanical systems
- MI:
-
Myocardial ischemia
- MNPs:
-
Magnetic nanoparticles
- MSNs:
-
Mesoporous silica nanoparticles
- MWNT:
-
Multi-walled carbon nanotubes
- NEMS:
-
Nanoelectromechanical system
- PAH:
-
Pulmonary arterial hypertension
- PCL:
-
Poly caprolactone
- PDGF:
-
Platelet-derived growth factors
- PEG:
-
Poly ethylene glycol
- PET:
-
Positron emission tomography
- PLGA:
-
Poly lactic-co-glycolic acid
- ROS:
-
Reactive oxygen species
- SiRNA:
-
Short interference RNA
- SLNS:
-
Solid lipid nanoparticles
- SPIOs:
-
Superparamagnetic iron oxides
- VEGF:
-
Vascular endothelial growth factor
Наноматериалы
- Аквапоника под управлением Raspberry Pi
- Нановолокна и нити для улучшенной доставки лекарств
- Биосовместимые наночастицы FePO4:доставка лекарств, стабилизация РНК и функциональная активность
- Металлоорганические каркасы, реагирующие на окружающую среду, как система доставки лекарств для терапии опу…
- Доставка лекарств на основе клеток для онкологических приложений
- Рыба-данио:многообещающая модельная система в реальном времени для доставки нейроспецифических лекарств, оп…
- PLGA-липидные наночастицы с отслеживанием 131I как носители доставки лекарств для целевого химиотерапевтическо…
- Новые биосовместимые наночастицы Au Nanostars @ PEG для КТ-визуализации in vivo и свойства очищения почек
- Исследование физико-химических характеристик системы на основе нанолипосом для двойной доставки лекарств
- Компактная система визуализации 3D LiDAR



