Разработка мультиконцентрированных биметаллических наночастиц Cu:Ag как перспективного бактерицидного средства для устойчивых к антибиотикам бактерий, согласно оценке с помощью молекулярного докинга
Аннотация
Настоящее исследование посвящено оценке влияния различных концентраций Ag в биметаллических наночастицах Cu:Ag, разработанных для использования в качестве многообещающего антибактериального агента против устойчивых к антибиотикам бактерий. Здесь были синтезированы биметаллические наночастицы Cu:Ag с различным соотношением концентраций (2,5, 5,0, 7,5 и 10 мас.%) Ag в фиксированном количестве Cu, обозначенные как 1:0,025, 1:0,050, 1:0,075 и 1:0,1. с использованием метода соосаждения с гидроксидом аммония и деионизированной водой в качестве растворителя, поливинилпирролидоном в качестве блокирующего агента и боргидридом натрия и аскорбиновой кислотой в качестве восстановителей. Эти сформулированные продукты были охарактеризованы с помощью различных методов. XRD подтвердил чистоту фазы и обнаружил присутствие отчетливых ГЦК-структур, принадлежащих фазам Cu и Ag. ИК-Фурье спектроскопия подтвердила наличие колебательных мод, соответствующих различным функциональным группам, и зарегистрировала характерный пик, исходящий от биметаллического соединения. УФ-видимая спектроскопия показала уменьшение ширины запрещенной зоны с увеличением содержания Ag. Микрофотографии СЭМ и ВР-ПЭМ выявили сферическую морфологию биметаллической меди, легированной серебром, с мелкими и крупномасштабными агломерациями. Образцы имели разные размеры и расстояние между слоями. Бактерицидное действие синтезированных биметаллических НЧ Cu:Ag показано статистически значимым ( P <0,05) зоны ингибирования, зарегистрированные для различных концентраций допанта Ag против Staphylococcus aureus ( S. aureus ) , кишечная палочка ( E. coli ) , и Acinetobacter baumannii ( А. бауманний ) в пределах (0,85–2,8 мм), (0,55–1,95 мм) и (0,65–1,85 мм) соответственно. В целом, биметаллические НЧ Cu:Ag оказались более эффективными против грамположительных по сравнению с грамотрицательными. Исследование молекулярного докинга биметаллических НЧ Ag – Cu было выполнено против β -лактамаза, которая является ключевым ферментом пути биосинтеза клеточной стенки из S. золотистый (Оценка связывания:- 4,981 ккал / моль) и A. bauminnii (Оценка связывания:- 4,013 ккал / моль). Аналогичным образом, анализ связывающего взаимодействия с FabI, принадлежащим к пути биосинтеза жирных кислот из A. bauminnii (Оценка связывания:- 3,385 ккал / моль) и S. золотистый (Оценка связывания:-3,012 ккал / моль) вместе с FabH от E. coli (Оценка связывания:- 4,372 ккал / моль). Эти теоретические расчеты указывают на биметаллические НЧ Cu-Ag как на возможный ингибитор выбранных ферментов. Предполагается, что изучение ингибирующего потенциала этих материалов in vitro может открыть новые возможности для открытия антибиотиков.
Введение
На Земле и в окружающей среде обитают разнообразные микроорганизмы, состоящие из бактерий, грибов, вирусов и паразитов. Эти виды вызывают сложности при производстве и использовании медицинского оборудования, товаров для здравоохранения, обработанных пищевых продуктов, систем очистки воды и средств бытовой санитарии [1, 2]. Врачи обычно используют антибиотики для уничтожения бактерий, вызывающих болезни у людей и животных. Недостатком частого использования антибиотиков является то, что они со временем делают бактерии устойчивыми к лекарствам. Антибиотики также служат для уменьшения количества «хороших» бактерий, присутствующих в организме, которые борются с инфекциями. Заболевания, вызванные инфекциями, вызванными устойчивыми к антибиотикам бактериями, сегодня стали серьезной причиной для беспокойства в области медицины. В этом отношении многие микробы оказались устойчивыми к лекарствам [3,4,5,6,7]. В настоящее время предпринимаются новые усилия по решению проблемы бактерий, устойчивых к лекарственным средствам, и по замене существующих противомикробных средств более эффективными и дополнительными методами лечения. В этом отношении нанотехнологии внесли существенный вклад в производство наноматериалов, таких как наночастицы металлов и оксидов металлов (например, Ag, Cu, CuO, TiO 2 , SiO 2 , MgO и ZnO) для борьбы с постоянно растущим числом устойчивых к противомикробным препаратам микроорганизмов. Среди них НЧ Cu и Ag показали обнадеживающие антимикробные свойства [8,9,10,11,12].
В последние годы биметаллические наночастицы были разработаны и используются в различных областях химии, материаловедения, биотехнологии и защиты окружающей среды. Биметаллические НЧ, содержащие медь (Cu) и серебро (Ag), с высокой долей поверхностных атомов и большой удельной поверхностью, широко изучаются [13]. Эти биметаллические НЧ представляют большой интерес из-за их улучшенных химических, оптических, каталитических, биологических, плазмонных и особенно антимикробных свойств [14,15,16,17,18,19,20]. Ионы Ag могут быть восстановлены этанолом в атмосферных условиях при температуре от 800 до 1000 ° C с получением НЧ серебра [21, 22]. НЧ серебра обладают хорошей антимикробной эффективностью, поэтому его используют при производстве солнцезащитных кремов и водоподготовке [23]. НЧ Cu получают восстановлением сульфата меди гидразином в этиленгликоле под воздействием микроволнового излучения, а также могут использоваться в качестве антибактериального агента [24,25,26].
Металлы, такие как Cu и Ag, по отдельности не обладают многообещающими оптическими, каталитическими и структурными свойствами и не могут быть превращены в биметаллические соединения. С другой стороны, объединение обоих металлов (Cu:Ag) открывает новые возможности для настройки структуры и морфологии получаемого продукта для желаемых областей применения. Основываясь на своей окончательной структуре, например, ядро-оболочка, структура гантели, структура с двумя интерфейсами, случайно перемешанная структура или структура в форме цветка, биметаллические наночастицы могут проявлять диапазон антимикробной активности [27,28,29,30 , 31]. Доступны различные методы синтеза биметаллических НЧ, включая соосаждение, золь-гель, гидротермальный, восстановительный, микроэмульсионный и полиольный метод [32,33,34,35,36,37].
В этом исследовании биметаллические наночастицы Cu:Ag были синтезированы методом соосаждения с использованием гидроксида аммония и деионизированной воды в качестве растворителя, поливинилпирролидона в качестве блокирующего агента и боргидрида натрия и аскорбиновой кислоты в качестве восстановителей. Были приготовлены четыре образца с различными концентрациями. При увеличении концентрации Ag в приготовленных биметаллических НЧ образцы показали повышенную активность против бактерий acinetobacter baumannii что вызывает жар и тошноту. Синтезированный материал приобрел красный цвет во время быстрого роста, что свидетельствует о том, что антимикробная активность усиливалась с увеличением концентрации Ag в биметаллических НЧ. Кроме того, были выполнены прогнозы In silico с использованием молекулярного докинга для определения характера взаимодействия биметаллических НЧ Cu:Ag с β -лактамаза пути биосинтеза клеточной стенки наряду с ферментами FabI и FabH пути биосинтеза жирных кислот.
Методы
Настоящее исследование было направлено на синтез различных концентраций Ag в биметаллических наночастицах Cu:Ag гидротермальным путем для изучения эффективности антибактериального агента против устойчивых к антибиотикам бактерий.
Материалы
Хлорид меди (II) (CuCl 2 0,2 H 2 O 98,9%) и нитрат серебра (AgNO 3 ) в качестве прекурсоров, поливинилпирролидон (ПВП, средняя молекулярная масса 40 000) в качестве кэпирующего агента, боргидрид натрия (NaBH 4 , 99,9%) и L-аскорбиновая кислота (C 6 H 8 О 6 , 99,0%) в качестве восстановителей и гидроксида аммония (NH 4 OH) были использованы в настоящем исследовании после приобретения их у Sigma Aldrich, США.
Синтез биметаллических НЧ Cu:Ag
Биметаллические НЧ Cu:Ag получали с использованием метода соосаждения, как показано на фиг. 1. В деионизированную воду добавляли 1,25 г PVP и 0,5 г аскорбиновой кислоты и интенсивно перемешивали при 100 ° C. По отдельности готовили два раствора гидроксида аммония по 40 мл; в один раствор добавляли 1,7 г хлорида меди, а в другой раствор - 1,7 г нитрата серебра. Затем эти два раствора один за другим вливают в изначально приготовленный раствор с добавлением 0,5 г NaBH 4 . После этого конечный раствор перемешивали при 100 ° C в течение 4 часов, чтобы сделать его гомогенным, а затем центрифугировали при 6000 об / мин для полной экстракции НЧ. Полученные биметаллические НЧ сушили при 100 ° C для полного удаления влаги и примесей, чтобы убедиться в чистоте полученных биметаллических продуктов [12]. Аналогичным образом были приготовлены четыре образца с различными концентрациями Ag (моль 2,5%, 5%, 7,5% и 10%) с фиксированными отношениями Cu.
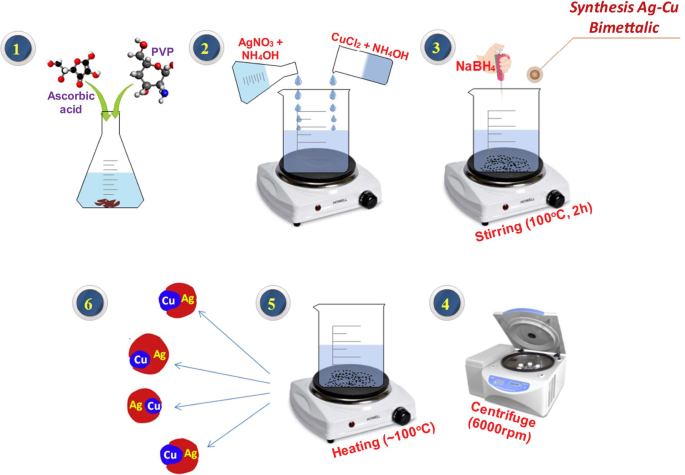
Иллюстрация, демонстрирующая синтез биметаллических НЧ Cu:Ag
Противомикробное действие
Бактерицидный потенциал биметаллических НЧ Cu:Ag in vitro был оценен против патогенных бактерий S. aureus, E. coli и А. baumannii изоляты, полученные из маститного молока крупного рогатого скота с использованием метода скважинной диффузии. Маннитоловый солевой агар, агар МакКонки и агар Lauria Bertani протирали изолированными бактериями, активировавшими рост 1,5 × 10 8 КОЕ / мл. После затвердевания среды готовили пять лунок, используя желтую пипетку диаметром 15 мм и десять микролитров (5 мкг / мл). Свежеприготовленные биметаллические НЧ Cu:Ag загружали в лунки с различными соотношениями по сравнению с десятью микролитрами амоксициллина (5 мкг / мл) в качестве положительного контроля и 50 мкл DIW в качестве отрицательного контроля. Бактерицидную активность синтезированных биметаллических НЧ Cu:Ag определяли путем измерения зон ингибирования (в мм), образовавшихся после инкубации в течение 15 ч при 37 ° C.
Статистический анализ
Бактерицидная активность синтезированных НЧ с измерениями зоны ингибирования (мм) считалась статистически значимой с использованием SPSS 20.0, одностороннего дисперсионного анализа (ANOVA) [57].
Исследование молекулярного докинга
Антибиотики уменьшают рост бактерий и вызывают гибель бактерий из-за повреждения клеточной стенки, нарушения биохимических процессов, повреждения клеточной мембраны и проникновения через биопленку [38]. В последние десятилетия сообщалось о большом количестве наночастиц с потенциальной бактерицидной активностью, которые убивают бактерии либо за счет разрушения клеточной стенки, либо путем блокирования источника пищи по механизму, аналогичному известным антибиотикам [39,40,41]. Следовательно, ферменты, принадлежащие к этим биохимическим путям, считаются важной и привлекательной мишенью для открытия антибиотиков [12]. Здесь ключевые ферменты пути биосинтеза клеточной стенки (т. Е. β -лактамаза) и путь биосинтеза жирных кислот (т.е. FabH и FabI) были выбраны в качестве возможных мишеней для оценки механизма взаимодействия биметаллических НЧ Cu:Ag с их активным карманом в качестве ингибиторов (см. рис. 2).
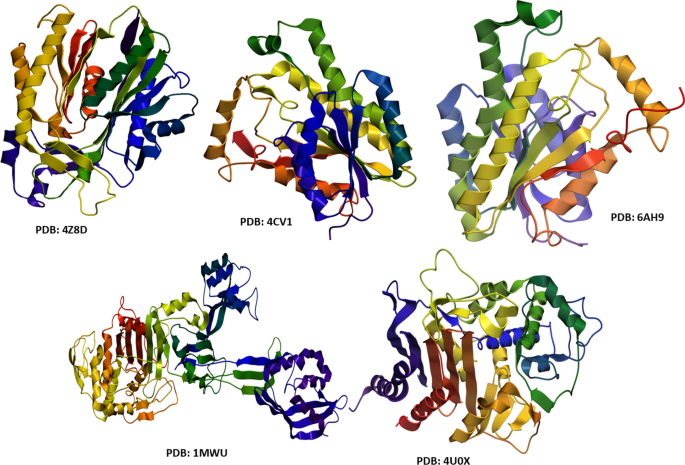
3D-структура белков-мишеней β -лактамаза, FabI (из A. bauminnii & С. золотистый ) и FabH из E. coli
Трехмерные структурные параметры выбранных ферментов были получены из банка данных белков с кодом PDB:4U0X (разрешение 2,03 Å) для β -лактамаза [42] и 6AH9; Разрешение 1,74 Å [43] для эноил- [ацил-белок-носитель] редуктазы (FabI) из A. bauminnii . β -лактамаза (трехмерная структура) с PDB ID:1MWU; Разрешение 2,6 Å [44] и FabI с кодом PDB:4CV1; Резолюция 1.95 [45] от С. золотистый а для FabH от E. coli имеет код PDB:4Z8D; Разрешение 2,0 Å [46].
Исследование молекулярного докинга биметаллических НЧ Cu:Ag проводили с использованием программного обеспечения ICM Molsoft v3.8–4a или выше (Molsoft L.L.C., La Jolla, CA) для выявления связывающих взаимодействий с ключевыми остатками активного сайта [47]. Инструмент ICM для подготовки белков / рецепторов использовался для оптимизации и подготовки структуры выбранных ферментов-мишеней. Включенные шаги включали добавление полярных H-атомов, удаление молекул воды и минимизацию энергии с использованием параметров по умолчанию. Молекула сокристаллизованного лиганда была удалена, чтобы обеспечить место для стыковки наночастиц. Связывающий карман определяли с использованием ячейки сетки, определяющей положение кристаллизованного лиганда. Конформация с наименьшей энергией связи из 10 верхних пристыкованных конформаций была выбрана в каждом случае для анализа характера взаимодействия и тенденции связывания биметаллических наночастиц Ag – Cu внутри активного кармана. Программное обеспечение визуализатора Pymol и Discovery studio использовалось для анализа и трехмерного изображения связывающих взаимодействий [48]. Структура биметаллических НЧ Cu:Ag была получена из PubChem в формате .sdf.
Характеристика
Структурный анализ и фазовую чистоту наблюдали с помощью XRD (PAN Analytics X’pert pro XRD) с излучением Cu-Kα ( λ =0,154 нм, от 20 ° до 80 °). Наличие колебательных мод, соответствующих различным функциональным группам, оценивали с помощью инфракрасной спектроскопии с преобразованием Фурье-FTIR на спектрометре Perkin Elmer. Спектры поглощения регистрировали с использованием спектрофотометра Genesys 10S в УФ-видимом диапазоне. FESEM в сочетании со спектрометром EDS (JSM-6610LV) и HR-TEM (JEOL JEM 2100F) использовались для визуализации морфологии поверхности. Программное обеспечение ICM v3.8-4a или выше (Molsoft L.L.C., La Jolla, CA) использовалось для молекулярного док-анализа.
Результаты и обсуждение
Рентгеноструктурный анализ был проведен для оценки фазового состава и кристаллической структуры приготовленных продуктов. На рис. 3а показана диаграмма дифракции рентгеновских лучей, построенная между 20 ° и 80 °. В биметаллическом Cu:Ag наблюдаемые рефлексы около ~ 38,2 °, 46 °, 64,4 ° и 77,1 ° приписываются граням (111), (200), (220) и (311) ГЦК фазы Ag согласно JCPDS № 04-0783 [32, 49,50,51,52]. Тогда как в случае Cu дифракции, возникающие при 32,6 °, 44,2 ° и 51 °, обозначили плоскости решетки (110), (111) и (200), что подтвердило присутствие CuO с ГЦК-структурой и металлической Cu соответственно, и хорошо сочетается с JCPDS № 04-0836 [32, 53,54,55,56]. На извлеченном образце наблюдались пики как Ag, так и Cu, что означает присутствие НЧ, составляющих фазы Ag и Cu. Более того, наличие CuO в образцах с более низким содержанием Ag (например, 1:0,025, 1:0,050 и 1:0,075) показывает, что НЧ Cu окислялись и проявляли незащищающее поведение при высокой температуре из-за более низких концентраций Ag [ 52]. Напротив, в образце с наибольшим содержанием Ag (1:0,1) пик CuO имеет низкую интенсивность, что свидетельствует об образовании частично безоксидного продукта [57]. Это говорит о том, что улучшенная стойкость биметаллических НЧ к окислению будет происходить за счет добавления Ag [52]. Никакого дополнительного пика примеси не было обнаружено в пределах обнаружения прибора, в то время как каждая кристаллографическая плоскость содержит энергетически различные участки, основанные на плотности атомов. И Cu, и Ag НЧ имеют грани с высокой атомной плотностью в точке (111), которые служат для выявления максимальной ориентации плоскостей [51, 58]. Используя закон Брэгга, d-расстояние Ag и Cu оказалось равным 0,24 и 0,21 нм, соответственно, что соответствует отдельной плоскости (111) обоих элементов и согласуется с данными HR-TEM (рис. 6) [51, 59 , 60,61,62]. Соответствующие кольца SAED (рис. 3b – d), полученные из приготовленных биметаллических продуктов, демонстрируют отчетливые структуры колец, которые демонстрируют хорошо кристаллизованные продукты и хорошо согласуются с картинами XRD.
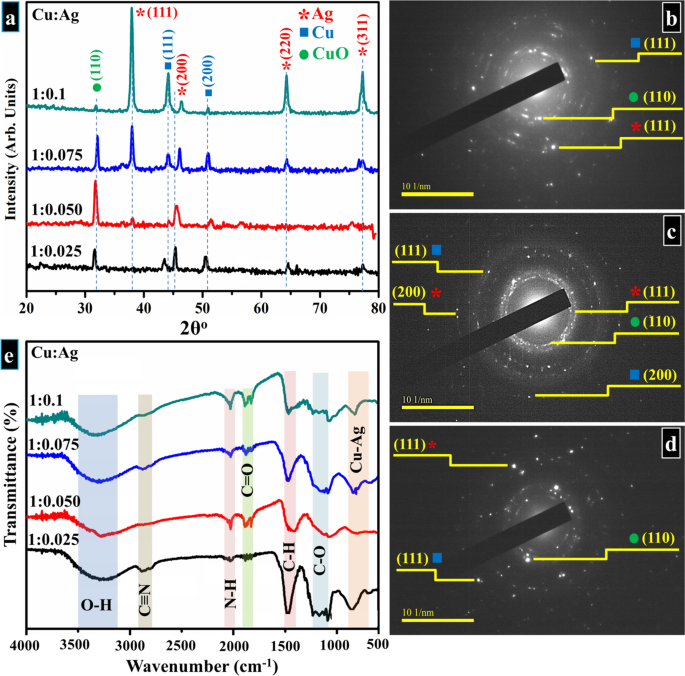
а Профили XRD, полученные для биметаллических НЧ Cu:Ag, b - г Кольца SAED, полученные с помощью HR-TEM для образцов b 1:0,025, c 1:0,050 и d 1:0,10, e ИК-Фурье спектры приготовленных образцов
Спектры FTIR были записаны в диапазоне от 500 до 4000 см -1 . как показано на фиг. 3e; полоса пропускания находится между 600 и 900 см −1 вызвано образованием связи Cu:Ag [63]. Наблюдаемая полоса около ~ 1200 и 1400 см −1 относится к C – O и C – H соответственно; пики на ~ 1800 и 2100 см −1 соответствует связыванию C =O и N – H за счет PVP и NH 4 ОН [64]. Коэффициент пропускания наблюдается около ~ 2800 см −1 и 3400 см −1 объясняются наличием C≡N и гидроксильной группы (O – H) [64].
На рис. 4а показаны спектры поглощения биметаллических НЧ Ag – Cu с четкими полосами поглощения при 340, 410 и 500 нм, которые приписываются поверхностному плазмонно-резонансному поглощению металлических Ag и Cu [52]. Полоса, появляющаяся при 410 нм, обычно возникает из-за присутствия НЧ Ag, а последний пик, расположенный при 510 нм, объясняется существованием НЧ Cu [52, 57,58,59, 65,66,67]. Можно предположить, что биметаллические наночастицы развиваются с отдельными фазами Ag и Cu, а не с биметаллическими формами, что также было подтверждено результатами XRD, как обсуждалось ранее [52]. Наблюдалось небольшое красное смещение полосы поглощения при 410 нм и увеличение максимального поглощения с увеличением содержания Ag [58]. Используя уравнение Таука,
$$ [\ alpha h \ nu =K \ left ({h \ nu - Eg} \ right) ^ {n}] $$ (1)где α считается коэффициентом поглощения [2.303 log ( T / d ), Т проходит свет и d показывает толщину ячейки образца], h символизирует постоянную Планка (6,62607015 × 10 −34 Js), \ (\ nu \) - частота света, K показывает индекс абсорбции, а E g равна ширине запрещенной зоны в эВ. Значение « n »Связано с электронным переходным типом запрещенной зоны [13, 26, 68, 69]. Ширина запрещенной зоны полученных биметаллических продуктов была рассчитана и составила 3,2, 2,9, 2,7 и 2,6 эВ, как показано на рис. 4b – e.
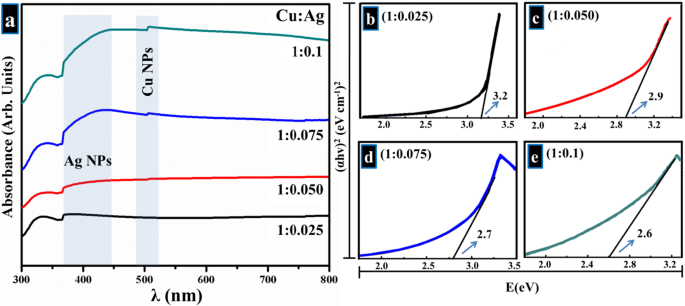
УФ – видимые спектры, полученные из биметаллических b - е Анализ сюжета Таука
Из изображений SEM (рис. 5a – d) биметаллических нанокомпозитов Cu:Ag в исходном состоянии было обнаружено, что частицы небольшого размера осаждаются на поверхности крупных частиц. Увеличение содержания Ag с 2,5 до 7,5% привело к образованию различных частиц с разной морфологией, которые в конечном итоге привели к образованию массивных НЧ Cu:Ag. Кроме того, накопление неровных и крошечных частиц Ag увеличивалось с увеличением концентрации легирующей примеси, что свидетельствовало о появлении более рассеянных блоков на его поверхности. Это означает большое влияние, которое легирование Ag на Cu оказывает на морфологию, что было дополнительно подтверждено микрофотографиями HR-TEM (см. Рис. 5e-h).

а – д СЭМ-изображения, полученные из готовых продуктов, e – h Микрофотографии HR-TEM
Для дальнейшей проработки морфологии и d-расстояния приготовленного биметаллического материала была задействована ПЭМ-ВР с разрешением 10 нм. На рис. 6a расстояние d (0,21 нм) наночастиц Cu соответствует грани (111) Cu, что также очевидно из результатов XRD (рис. 3a). На рисунке 6b показано небольшое увеличение расстояния между слоями (от 0,21 до 0,22 нм) и показаны НЧ Ag с межплоскостным расстоянием 0,24 нм, совпадающие с плоскостью (111). Точно так же на рис. 6c, d показаны расчетные расстояния между слоями и отдельные фазы биметалла, а на рис. 6e показана форма частиц наночастиц Ag и Cu. Видно, что на изображениях ВР-ПЭМ частицы обладают структурой ядро-оболочка. На рис. 6г в пределах одной частицы были зарегистрированы полосы решетки, исходящие от Cu и Ag. Это убедительно свидетельствует об образовании биметаллических наночастиц ядро-оболочка с различным соотношением Cu:Ag с образованием наночастиц неправильной квазисферической формы. Кроме того, изображение ПЭМ показало, что частицы выглядят как темные и светлые области. Такое изменение контраста в пределах одной частицы может указывать на присутствие двух различных составляющих материалов, предполагающих создание биметаллических частиц Cu:Ag [70, 71].

а – д Изображения HR-TEM (10 нм) для измерения d-расстояния для всех подготовленных образцов, e изображение с низким увеличением, показывающее биметаллические частицы
Наличие отчетливого пика в спектре EDS и элементного состава, происходящего от биметалла, подтвердили успешное образование НЧ Cu:Ag. На рис. 7а представлен спектр EDS, полученный для образца 1:0,050, который показывает четкие пики Cu и Ag. Рисунок 7b взят из образца 1:010, где пики C и O были обнаружены в легированных образцах. Они появляются, поскольку угольные вкладки используются для удержания образцов во время исследования SEM и / или из-за фонового подсчета в датчике SEM – EDS.
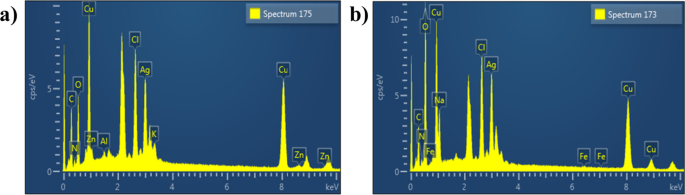
Профили ЭДС, полученные из биметаллических НЧ
Бактерицидная эффективность биметаллических НЧ Cu:Ag in vitro с использованием анализа диффузии в лунках агара представлена в Таблице 1. Результаты демонстрируют прямую пропорциональную зависимость между концентрацией синтезированных НЧ и зонами ингибирования (мм). Статистически значимый ( P <0,05) зоны ингибирования, зарегистрированные для (2,5, 5, 7,5 и 10 мас.%) Добавки Ag против S. aureus, E. coli и А. baumannii варьировались от 0,85–2,8 мм, 0,55–1,95 мм и 0,65–1,85 мм соответственно, см. Таблицу 1. Все результаты сравнивали с DIW (0 мм) и амоксициллином (4 мм) в качестве отрицательного и положительного контроля, соответственно. Аналогичным образом возрастная эффективность допированных НЧ увеличилась (21,2–70%), (13,7–48,7%) и (16,2–46,2%) против S. aureus, E. coli и А. baumannii , соответственно. В целом биметаллические НЧ Cu:Ag оказались более эффективными против S. золотистый (т.е. грамм + ive) по сравнению с E. coli и А. baumannii (т.е. грамм −ive).
Размер, концентрация и форма наночастиц напрямую влияют на окислительный стресс, создаваемый наноструктурами. Бактерицидная эффективность в виде зон ингибирования (мм) улучшилась благодаря большему весу% легирования биметаллических НЧ Cu, легированных серебром, за счет увеличения доступности катионов (++). Бактерицидное действие в отношении размера и концентрации показывает обратную зависимость от размера [58, 59]. Наноразмерные структуры эффективно производят активные формы кислорода (АФК), которые находятся в мембранах бактериальных клеток, что приводит к экструзии клеточных органелл и, в конечном итоге, к гибели бактерий [60]. Помимо производства АФК, катионное взаимодействие Ag + и Cu ++ с отрицательно заряженными частями клеточной мембраны бактерий приводит к повышению бактерицидной эффективности при возрастающих концентрациях за счет лизиса клеток и разрушения бактерий [58, 61].
Биологические применения различных классов наночастиц широко изучаются за последние несколько десятилетий. Благодаря уникальным характеристикам наночастиц, они широко используются в качестве бактерицидных агентов, способных заменять традиционные антибиотики. НЧ взаимодействуют с бактериальными клетками, нарушают проницаемость клеточной мембраны и разрушают ключевые метаболические пути [72]. Необходимо изучить конкретный механизм токсичности наночастиц по отношению к бактериям. Считается, что НЧ взаимодействуют с бактериальной клеткой, используя электростатические силы, силы Ван-дер-Ваальса или гидрофобные взаимодействия, которые в конечном итоге приводят к гибели бактерий. Сообщается, что ферменты являются основным фактором вирулентности, вовлеченным в бактериальную инфекцию и нацеленным на них, чтобы ингибировать их активность, помогая бороться с вызванной инфекцией [73]. В данном случае исследование молекулярного стыковки НЧ Cu:Ag с ферментными мишенями клеточной стенки наряду с путем биосинтеза жирных кислот выявило паттерн связывающего взаимодействия этих НЧ внутри активного кармана. Принимая во внимание антибактериальный потенциал этих НЧ in vitro против A. bauminnii , С. золотистый и Э. coli , ферменты-мишени были выбраны из этих микроорганизмов, чтобы понять возможный механизм их бактерицидной активности.
Наилучшая стыкованная конформация наблюдается в случае биметаллических НЧ Cu:Ag с β -лактамаза из A. bauminnii выявили водородное связывание с Glu272 (2,8 Å) и Ser286 (3,2 Å) наряду с контактным взаимодействием металла с Val292, в то время как оценка стыковки составила -4,013 ккал / моль (рис. 8a). Точно так же оценка связывания биметаллических НЧ Ag – Cu наблюдалась с β -лактамаза из S. золотистый составляла - 4,981 ккал / моль, обладая Н-связывающим взаимодействием с Ser403 (3,2 Å), Tyr519 (3,6 Å), Gln521 (3,0 Å) и Asn464 (3,1 Å), как показано на рис. 8b.
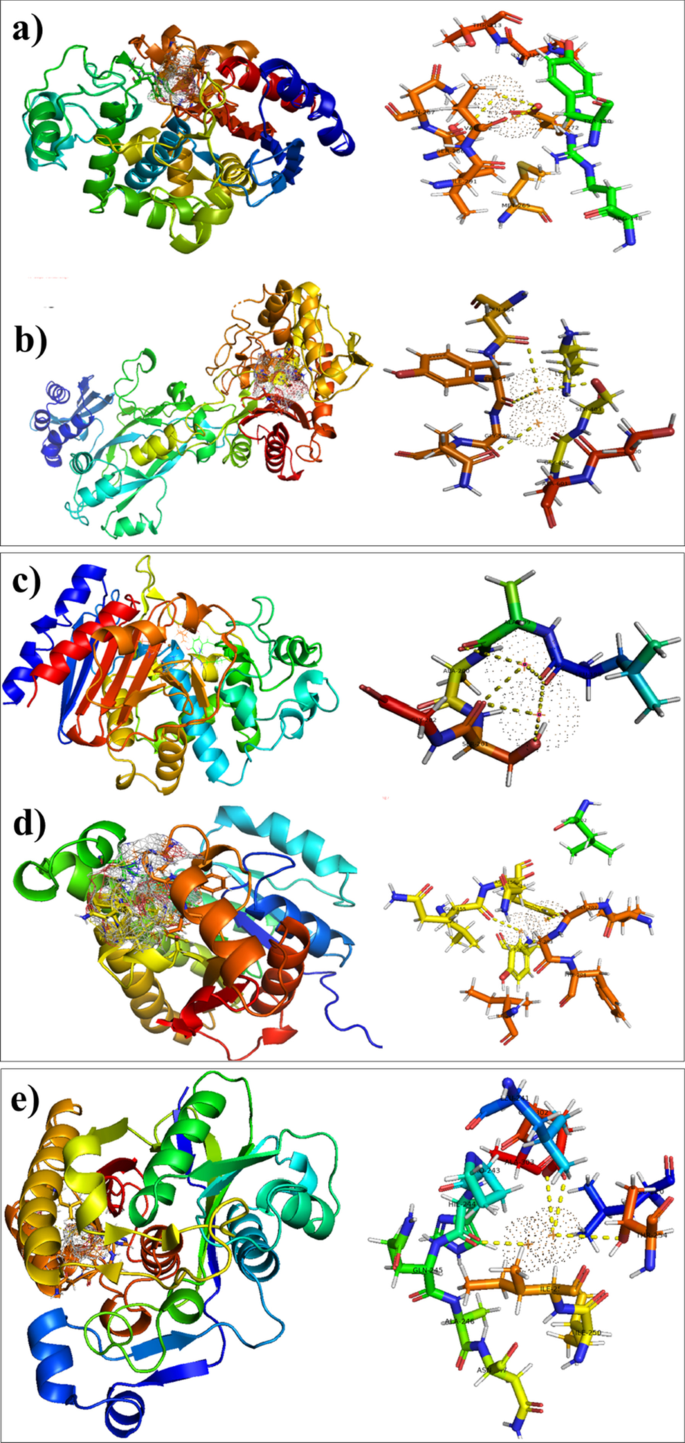
Характер связывающего взаимодействия биметаллических НЧ Ag – Cu внутри активного кармана. а β -лактамаза из A. bauminnii , b β -лактамаза из S. золотистый . c , d Схема связывающего взаимодействия биметаллических НЧ Ag – Cu внутри активного кармана c еноил- [ацил-белок-носитель] редуктаза (FabI) из A. bauminnii , d еноил- [ацил-белок-носитель] редуктаза (FabI) из S. золотистый , e паттерн связывания биметаллических НЧ Ag – Cu внутри активного кармана FabH из E. coli
Вторая ферментная мишень, выбранная в текущем исследовании, FabI относится к пути биосинтеза жирных кислот, и предсказания молекулярного стыковки предполагают, что биметаллические НЧ Cu:Ag в качестве потенциального ингибитора против этой мишени. Биметаллические НЧ Cu:Ag показали хорошую оценку связывания (-3,385 ккал / моль) с FabI из A. bauminnii имеющий водородную связь с Ser201 (2,7 Å), Ala199 (3,5 Å) и Leu198 (3,3 Å), как показано на фиг. 8c. Точно так же наилучшая стыкованная конформация НЧ Ag – Cu с активным центром FabI из S. золотистый показал Н-связывание с Gly202 (2,5 Å) и Gln155 (2,5 Å), имеющее показатель связывания - 3,012 ккал / моль (рис. 8d).
Кроме того, связывающая способность биметаллических НЧ Cu:Ag против FabH из E.coli также оценивали, и наблюдаемая оценка связывания составила -4,372 ккал / моль, имея H-связывающее взаимодействие с Thr254 (3,5 Å), HIE244 (2,6 Å) и Glu302 (3,0 Å), как показано на рис. 8e.
Заключение
Биметаллические наночастицы Cu:Ag были приготовлены методом соосаждения для использования в приложениях для борьбы с болезнями, связанными с бактериями. Профили XRD подтвердили присутствие CuO с ГЦК-структурой и металлических частиц Cu и Ag. Наблюдались пики как Ag, так и Cu, что означает биметаллические наночастицы, содержащие фазы Ag и Cu. Плоскости, наблюдаемые при рентгеноструктурном анализе, хорошо соответствуют кольцам SAED. Присоединенные химические группы с сформулированными продуктами и характеристической полосой пропускания от 600 до 900 см -1 был вызван образованием связи Cu:Ag. Построенные спектры УФ – видимой области показали поглощение при 410 нм, которое обычно возникает из-за присутствия НЧ Ag, а последний пик, расположенный при 510 нм, был отнесен к существованию НЧ Cu. На изображениях ВР-ПЭМ было видно, что частицы имеют структуру ядро-оболочка. НЧ Cu:Ag четко продемонстрировали образование биметаллических НЧ с различным соотношением Cu:Ag с образованием нерегулярных квазисферических НЧ. Кроме того, d-расстояние наночастиц Cu, то есть 0,21 нм, соответствует грани (111) Cu, обнаруженной в результатах XRD. Небольшое увеличение расстояния между слоями (с 0,21 до 0,22 нм) также показывает, что НЧ Ag с расстоянием между слоями 0,24 нм совпадают с плоскостью (111). Исследование молекулярного докинга показало хорошее согласие с бактерицидной активностью in vitro. Тенденция связывания биметаллических НЧ Cu:Ag с β Фермент -лактамаза пути биосинтеза клеточной стенки наряду с ферментами FabI и FabH пути биосинтеза жирных кислот продемонстрировал свой ингибирующий потенциал, который необходимо дополнительно изучить с помощью исследований ингибирования ферментов.
Доступность данных и материалов
Все данные полностью доступны по запросу.
Сокращения
- EDS:
-
Энергодисперсионная рентгеновская спектроскопия
- FTIR:
-
Инфракрасная спектроскопия с преобразованием Фурье
- G + ve:
-
Грамположительные
- G −ve:
-
Грамотрицательный
- HR-TEM:
-
Просвечивающая электронная микроскопия высокого разрешения
- JCPDS:
-
Объединенный комитет по стандартам порошковой дифракции
- Ag:
-
Серебро
- UV – Vis:
-
Ультрафиолетовая видимая спектроскопия
- XRD:
-
Рентгеновская дифракция
Наноматериалы
- Наночастицы золота для химиотерапевтических датчиков
- Электроспряденные полимерные нановолокна, украшенные наночастицами благородных металлов для определения х…
- Наночастицы альбумина, содержащие ресвератрол, с длительным кровообращением и улучшенной биосовместимостью…
- Повышенная стабильность магнитных наночастиц золота с помощью сополимера поли (4-стиролсульфоновой кислоты …
- Исследование влияния направления удара на абразивный нанометрический процесс резания с помощью молекулярно…
- Нанокомпозиты на основе оксида графена, украшенные наночастицами серебра в качестве антибактериального аге…
- Оболочки диатомовых водорослей из кремнезема, адаптированные с использованием наночастиц Au, позволяют прово…
- Простой подход к получению наноразмерного оксида цинка в воде / глицерине с чрезвычайно концентрированными и…
- Антипролиферативный и запускающий апоптоз потенциал целевых липидных наночастиц на основе паклитаксела с у…
- Хорошо выровненные массивы нанотрубок TiO2 с наночастицами Ag для высокоэффективного обнаружения ионов Fe3 +



