Флуоресцентные точки нанобиомассы:экстракция с помощью ультразвука и их применение в качестве нанозонда для обнаружения Fe3 +
Аннотация
Биомасса как устойчивый и возобновляемый ресурс была одним из важных источников энергии для жизни человека. Здесь люминесцентные точки нанобиомассы (NBD) были извлечены из сои с помощью ультразвукового метода, который наделяет биомассу свойством флуоресценции. Свежеприготовленные NBD имеют аморфную структуру со средним диаметром 2,4 нм и демонстрируют ярко-синюю флуоресценцию с квантовым выходом 16,7%. Благодаря использованию съедобного сырья и процесса синтеза без нагрева, тест на цитотоксичность показывает, что жизнеспособность клеток все еще сохраняется на 100%, даже если концентрация NBD достигает 800 мкг / мл, что свидетельствует о хорошей биосовместимости NBD. Кроме того, флуоресценция NBD очень чувствительна к Fe 3+ , который можно использовать для Fe 3+ обнаружение с точки зрения их превосходства в отношении здоровья. Предел обнаружения (LOD) предложенного сенсора был определен как 2,9 мкМ, что ниже максимально допустимого уровня Fe 3+ . (5,37 мкМ) в питьевой воде.
Фон
Люминесцентные наноматериалы нашли широкое применение благодаря своим уникальным оптическим свойствам, особенно в светодиодах, детекторах, биовизуализации и обнаружении ионов металлов [1,2,3,4,5,6]. До сих пор сообщалось о различных люминесцентных наноматериалах, таких как полупроводниковые квантовые точки (КТ), углеродные наноточки и КТ серы, которые привели к большим успехам во многих областях [7,8,9,10,11,12] . КТ как превосходный представитель люминесцентных наноматериалов использовались во многих областях из-за их превосходных оптических и электрических свойств. Несмотря на все это, токсичность квантовых точек по-прежнему сильно ограничивает их применение [13, 14]. Всегда очень важно найти более экологичные и устойчивые наноматериалы с люминесценцией. Биомасса - это оригинальное органическое вещество, которое можно производить посредством фотосинтеза, и оно выделяется своими устойчивыми и возобновляемыми свойствами. В частности, биомасса определяется как биоразлагаемая фракция продуктов, отходов и остатков организма [15, 16]. В контексте нанотехнологий биомасса обычно используется в качестве прекурсора, и после специальной обработки ее можно превратить в наноточки с некоторыми оптическими свойствами. По сравнению с химическими предшественниками основными компонентами биомассы, особенно пищевой биомассы, являются сахара и белки, которые безвредны при последующих обработках. Следовательно, точки нанобиомассы (NBD) должны обладать высокой биосовместимостью, что гарантирует их применение в биологических и экологических областях без образования вредных веществ.
До сих пор сообщалось только о флуоресцентных углеродных наноточек, полученных из биомассы. По сути, некоторая естественная биомасса, такая как листья, яичный белок и лимонный сок, была обработана гидротермальным методом для синтеза флуоресцентных углеродных наночастиц [17,18,19]. Существует также еще один вид углеродных наноточек, существующих в пищевых продуктах, которые образуются при дальнейшей переработке природной биомассы [20, 21]. Все без исключения были связаны с типичными процессами высокотемпературной карбонизации. Этот процесс может занимать длительное время и при высокой температуре, и его трудно достичь в крупномасштабном серийном производстве [22]. По сравнению с высокими температурами, условия комнатной или низкой температуры легче поддерживаются и сохраняют исходные свойства самой биомассы.
Нанозонд - одно из важных приложений люминесцентных наноматериалов [23]. Ввиду яркой флуоресценции и высокой биосовместимости NBD могут использоваться как своего рода нанозонды в области биологии и экологии. Fe 3+ является важным ионом металла в организме человека, для которого они играют значительную роль в синтезе гемоглобина и миоглобина [24]. Но чрезмерное Fe 3+ накопление в организме может привести к повреждению тканей и отказу органа. Разработка эффективных и экологически чистых сенсорных систем для качественного и количественного определения Fe 3+ имеет большое значение для клинических, медицинских и экологических проблем. Это позволяет нам решить, можно ли превратить биомассу в наноточки с желаемыми свойствами непосредственно из натуральной съедобной биомассы без какой-либо обработки. Однако насколько нам известно, ни о каком из таких люминесцентных NBD не сообщалось. Следовательно, поиск более естественных предшественников биомассы для получения NBD с желаемыми свойствами и высокой биосовместимостью может сделать шаг в сторону более экологичных люминесцентных наноматериалов и Fe 3+ обнаружение.
Здесь впервые были продемонстрированы люминесцентные точки нанобиомассы (NBD) с помощью стратегии ультразвуковой экстракции (UES) из соевых бобов. Квантовый выход (QY) фотолюминесценции (ФЛ) готовых NBD может достигать 16,7%, и NBD демонстрируют яркое излучение в твердом состоянии. Тест на цитотоксичность показывает, что NBD обладают высокой биосовместимостью. Кроме того, NBD использовались для Fe 3+ обнаружение линейной зависимости интенсивности его флуоресценции от Fe 3+ концентрация, а предел обнаружения (LOD) может достигать 2,9 мкМ.
Методы
Материалы
Сорта северо-восточной сои в соответствии с Национальным стандартом Китайской Народной Республики ( GB1352-2009 ) были куплены в местном супермаркете и несколько раз промыты дистиллированной водой перед использованием. Хлорид кальция (CaCl 2 ), хлорид марганца (MnCl 2 ), хлорид меди (CuCl 2 ), хлорид кобальта (CoCl 2 ), нитрат свинца (Pb (NO 3 ) 2 ) и нитрат хрома (Cr (NO 3 ) 3 ) были приобретены у Aladdin Ltd. (Шанхай, Китай). Хлорид железа (FeCl 3 ), хлорид железа (FeCl 2 ), хлорид кадмия (CdCl 2 ), дихлорид ртути (HgCl 2 ), хлорид натрия (NaCl) и хлорид цинка (ZnCl 2 ) были получены от Sinopharm Chemical Reagent Co., Ltd. (Шанхай, Китай). Все химические вещества являются аналитическими реагентами (чистота> 99,0%) и используются в том виде, в котором они были получены, без дополнительной очистки.
Синтез NBD
Сначала 100 кусочков сои промывали смесью спирта и дистиллированной воды 3 раза для удаления примесей. Затем соевые бобы помещали в стакан с 50 мл дистиллированной воды с последующей обработкой ультразвуком в течение 2 часов. Во время этого процесса цвет раствора изменился с прозрачного на темно-желтый, что указывает на то, что кожура сои была адаптирована к наноразмерным размерам для образования NBD. Затем темно-желтый раствор переносили в центрифужные пробирки и дважды центрифугировали при 7000 об / мин в течение 3 минут для удаления крупных частиц, после чего супернатант фильтровали через мембрану 0,22 мкм для дальнейшего удаления крупных или агломерированных частиц. После этого раствор помещали в холодильник с последующей обработкой замораживанием при -5 ° . C в течение 6 ч. Затем его перенесли в лиофилизатор при -50 ° . C в течение 12 ч для получения порошков. Замороженные порошки диспергировали в воде с образованием NBD для дальнейшего применения.
Характеристика
Картину дифракции рентгеновских лучей (XRD) NBD регистрировали с использованием дифрактометра X 'Pert Pro, в котором рентгеновские лучи генерировались источником Cu-Kα. Просвечивающий электронный микроскоп (ПЭМ) JEM-2010 был использован для определения размера и кристалличности NBD. Спектры флуоресценции NBD получали на флуоресцентном спектрофотометре F-7000. Спектры поглощения NBD в УФ-видимой области были получены с использованием спектрофотометра UH4150. Инфракрасные спектры с преобразованием Фурье (FTIR) образцов регистрировали с помощью спектрометра Thermo Scientific Nicolet iS10 FTIR. Спектры рентгеновской фотоэлектронной спектроскопии (XPS) образцов были получены с использованием спектрометра Thermo Fisher Scientific ESCALAB 250Xi, оборудованного источником рентгеновского излучения Al-Kα.
Квантовое измерение выхода фотолюминесценции
Тестирование PL QY проводилось на спектрофлуориметре F-9000 с интегрирующей сферой. Прежде всего, водный раствор NBD разбавляли до интенсивности поглощения менее 0,1. Затем этот водный раствор добавляли в кювету для флуоресценции, помещали в интегрирующую сферу и возбуждали монохроматическим светом с длиной волны 370 нм. Спектры флуоресценции регистрировались в диапазоне 430–450 нм. Между тем, такие же спектры флуоресценции чистой воды также были записаны в идентичных условиях. Наконец, PL QY был рассчитан с использованием программного обеспечения для флуоресценции на основе спектров PL как образца, так и воды.
Тест на клеточную токсичность
Цитотоксичность NBD оценивают методами МТТ (3- (4,5) -диметилтиахиазо (-z-y1) -3,5-ди-фенитетра-золиумромид). Клетки культивировали в нормальном RPMI-1640 с 10% фетальной бычьей сывороткой в 5% CO 2 и 95% воздуха при 37 ° C в увлажненном инкубаторе. Для измерения жизнеспособности клеток клетки HeLa помещали в 96-луночные планшеты и затем инкубировали в течение 72 часов. После инкубации клеток Hela с различными концентрациями NBD и CD в течение 72 часов регистрировали жизнеспособность клеток.
Обнаружение Fe 3+
1 мл раствора с разной концентрацией Fe 3+ добавляли в 1 мл NBD с раствором 3 г / л перед измерениями ФЛ. Растворы тщательно перемешивали и оставляли реагировать в течение 1 мин при комнатной температуре, а затем регистрировали соответствующие спектры флуоресценции. Измерения ФЛ проводились при возбуждении 370 нм.
Результаты и обсуждение
Морфология и химический состав
НБД были подготовлены методами РАО ЕЭС; все процессы показаны на схеме 1. Размеры и морфология NBD были охарактеризованы с помощью просвечивающей электронной микроскопии (ПЭМ), как показано на рис. 1a и b. Изображения ПЭМ показывают, что NBD были почти сферическими по форме. Диаметры NBD находятся в диапазоне от 1 до 3 нм со средним диаметром 2,4 нм, и соответствующее распределение по размерам показано на рис. 1c. Полосы решетки NBD не могут быть обнаружены на изображении ПЭМ высокого разрешения (вставка на рис. 1b), что указывает на аморфную природу NBD. Изображения многоугольной кольцевой сканирующей электронной микроскопии в темном поле (HAADF-STEM) и соответствующие элементные карты (углерод, азот и кислород) NBD показаны на рис. 1d – g. Видно, что преобладающими элементами NBD являются углерод, азот и кислород. Кроме того, твердотельный 13 Измерения ядерным магнитным резонансом (ЯМР) C для NBD показаны на рис. 1h. Сигналы находятся в диапазоне 160–180 м.д., а пики при 164 и 170 м.д. соответствуют связям C =O, что указывает на sp 2 атомы углерода [25, 26].
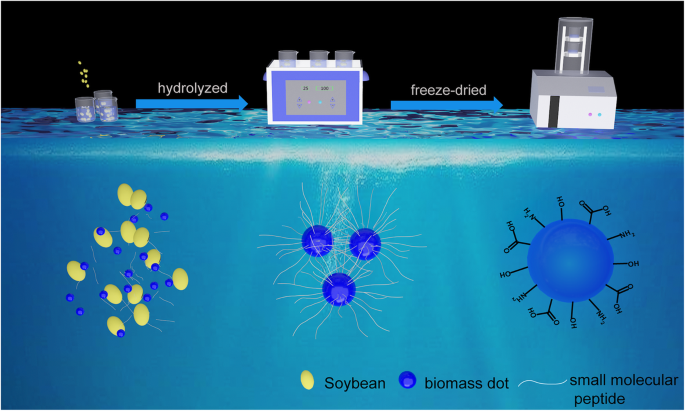
Схематическое изображение процесса приготовления NBD из соевых бобов
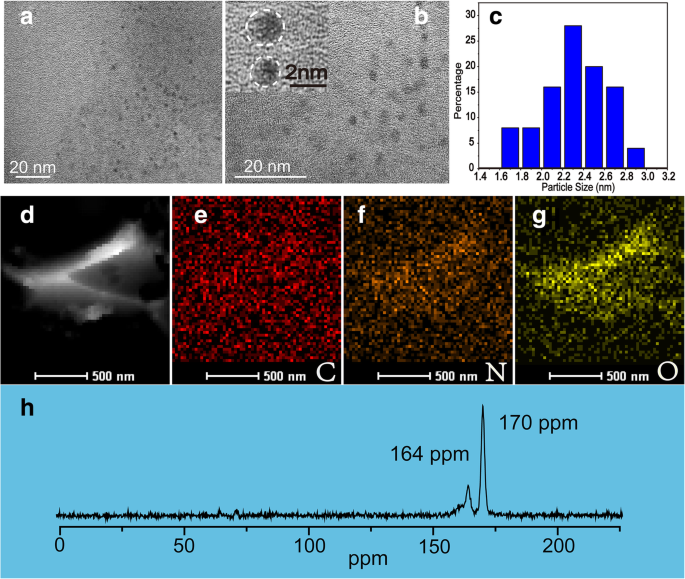
ПЭМ-изображения NBD ( a ) и ( b ). c Гранулометрический состав NBD. Изображение HAADF ( d ) и соответствующее отображение элементарного распределения углерода ( e ), азот ( f ) и кислород ( г )
Для дальнейшего изучения структурных характеристик NBD была записана картина дифракции рентгеновских лучей (XRD). Как показано на рис. 2а, на типичной рентгенограмме отображается широкий пик, расположенный примерно при 21,5 o и пик плеча на отметке 41,0 o , который можно отнести к аморфной углеродной фазе [27]. Кроме того, характерные пики поглощения соевых бобов и NBD были исследованы с помощью инфракрасной спектроскопии с преобразованием Фурье (FTIR), как показано на рис. 2 (b). Полосы поглощения около 3380 см −1 можно отнести к валентным колебаниям O – H / –N – H, полоса около 2906 см −1 валентным колебаниям C – H, а полоса около 1650 см −1 валентным колебаниям C =O. Пики на 1400 см −1 и 1071 см −1 соответствуют деформационным колебаниям C – H и C – O соответственно [28]. Существует очевидная разница между спектром соевых бобов и NBD на отметке 1750 см −1 . , который принадлежит валентным колебаниям связей C =O липидов сои [29, 30]. Нерастворимые липиды в водном растворе были отделены от образца при вымачивании в воде, что привело к исчезновению связей в FTIR-спектре NBD. Восстановленные связи C =O в образце происходят от карбоксильной группы в белке. Пик с центром около 1543 см −1 также исчез, что может быть связано с протеолизом в процессе замачивания соевых бобов. При сравнении всех пиков до и после ультразвукового процесса можно увидеть образование групп –OH, –C =O (амид I) и –NH на поверхности NBD [31]. Приведенные выше результаты демонстрируют наличие гидроксильных, амидогенных и карбоксильных групп на поверхности NBD, и эти функциональные группы играют важную роль в гидрофильности и стабильности NBD в водном растворе. Спектры рентгеновской фотоэлектронной спектроскопии (XPS) были выполнены для дальнейшего выяснения компонентов NBD, как показано на рис. 2c. Спектр XPS показывает три сильных пика при 532,0, 401,1 и 286,1 эВ, которые можно отнести к O 1s, N 1s (рис. 2d) и C 1s (рис. 2e) соответственно [32]. Эти результаты показывают, что NBD в основном содержат C (64,33%), O (32,34%) и N (2,72%), а также ограниченное количество P, а элемент P может происходить из фосфолипидов соевых бобов [33] . В спектре XPS высокого разрешения спектр C 1s показывает три пика при 287,6, 285,8 и 284,6 эВ, которые могут быть отнесены к C =O, C – O / C – N и C – C / C =C. группы, как показано на рис. 2c. Связь C =O происходит от растворимых карбоксильных групп [24]. C – O / C =N и C – C / C =C происходят от азотистого углерода и sp 2 / sp 3 углерода соответственно [34]. Спектр N 1s, показанный на рис. 2d, подтверждает две основные полосы при 399,5 эВ и 401,6 эВ, показывая наличие пиридинового азота и пирролинового азота, что согласуется с анализом FTIR. Спектр O 1s, представленный на рис. 2е, имеет два пика при 531,4 эВ и 533,0 эВ, которые можно отнести к группам C – OH / C – O – C и C =O соответственно [9].
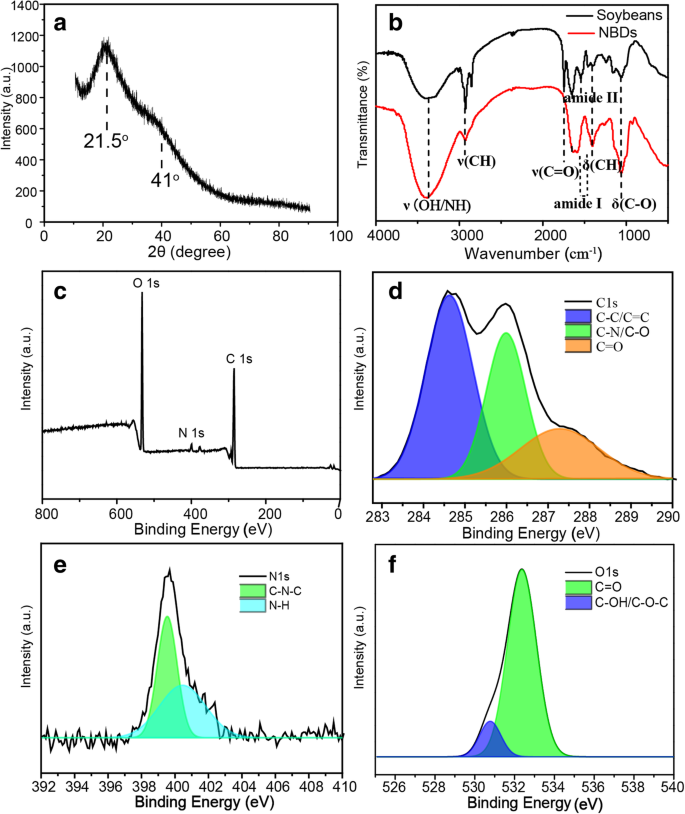
а Рентгенограмма NBD. б FTIR-спектры сои и NBD. c Спектр обзора XPS NBD. Спектры XPS высокого разрешения C 1s ( d ), N 1 с ( e ) и O 1s ( f )
Возможный механизм образования NBD из сои был предложен на основе приведенного выше анализа. Во-первых, некоторые крупные частицы биомассы, взвешенные в растворе, дробятся до нанометрового размера под действием ультразвукового сотрясения. Изменения в растворе до и после ультразвуковой экстракции показаны в дополнительном файле 1:Рисунок S1. Затем белок в соевых бобах был гидролизован до низкомолекулярного пептида и аминокислоты в вышеупомянутом процессе, и множество низкомолекулярных пептидных цепей присоединяется к наноразмерной биомассе с образованием точек биомассы с высокой степенью функциональности поверхности. Функциональные группы на поверхности точек биомассы вносят основной вклад в флуоресценцию. Согласно механизму, маш также использовался в качестве предшественников, и были также получены синие флуоресцентные NBD, как показано в Дополнительном файле 1:Рисунок S2.
Оптические свойства
NBD демонстрируют зависящие от возбуждения флуоресцентные свойства, и когда длина волны возбуждения изменяется от 320 до 520 нм, пик излучения постепенно смещается в красную область, указывая на то, что излучение NBD можно настраивать путем изменения длины волны возбуждения, как показано на рис. 3a. Водный раствор NBD прозрачен при внутреннем освещении и показывает синюю флуоресценцию при УФ-освещении, как показано на вставке к рис. 3b. Спектр возбуждения фотолюминесценции (PLE) NBD показан в дополнительном файле 1:Рисунок S3, а длина волны оптического возбуждения находится в диапазоне от 360 до 420 нм. Чтобы изучить происхождение ФЛ NBD, спектры поглощения NBD в УФ и видимой областях были записаны при комнатной температуре (концентрация NBD снизу вверх составляет 0,03, 0,06, 0,13, 0,25, 0,25, 0,50, 0,50. , 0,75, 1,00 и 1,50 г / л), как показано на рис. 3b. Спектры поглощения NBD в УФ-видимой области демонстрируют два четких пика поглощения при 270 нм и 330 нм соответственно. Первый можно отнести к π-π * переход связей C – C / C =C, а последний - к n-π * переход связей C =O / N [35, 36]. Эти функциональные группы являются основными хромогенными группами, которые вносят вклад в флуоресценцию NBDs [37, 38]. Спектры ФЛ соевых бобов во время ультразвуковой экстракции показаны в Дополнительном файле 1:Рисунок S4, и интенсивность ФЛ увеличивается со временем, а затем достигает максимума. На рисунке 3c показаны спектры ФЛ NBD, измеренные от 80 до 300 K. NBD демонстрируют типичное поведение термического гашения, при котором все пики монотонно уменьшаются по интенсивности с увеличением температуры. Такое поведение ФЛ можно объяснить увеличением безызлучательной рекомбинации и уменьшением радиационной рекомбинации с повышением температуры [39, 40]. Чтобы оценить стабильность NBD, фотостабильность и термостабильность NBD были охарактеризованы, как показано на рис. 3d. Для фотостабильности изображение настройки измерения показано в Дополнительном файле 1:Рисунок S5. Значения интенсивности флуоресценции показаны в Дополнительном файле 1:Рисунок S6 и S7. Интенсивность излучения NBD остается выше 90% при освещении УФ лампой в течение 6 часов, что свидетельствует об их хорошей фотостабильности. Для термостабильности интенсивности флуоресценции NBD немного уменьшаются при изменении температуры от 20 до 80 ° . C, что свидетельствует об их высокой термостойкости.
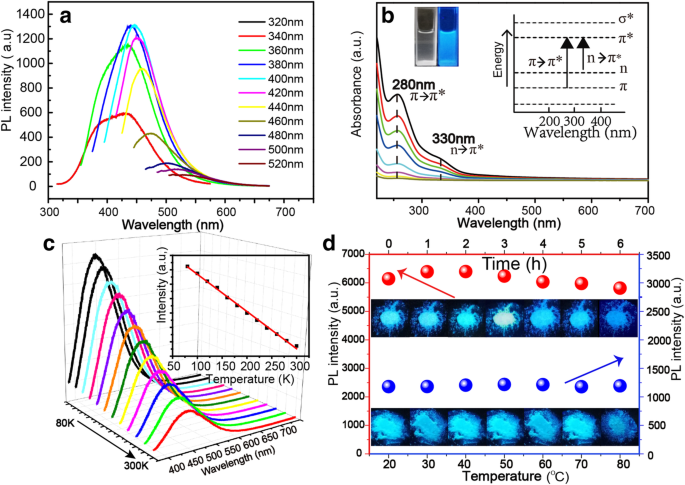
а Спектры флуоресценции NBD с длиной волны возбуждения изменяются от 320 до 520 нм. б Спектры поглощения NBD в УФ-видимой области. c Спектры флуоресценции NBD при разной температуре, на вставке - график зависимости интенсивности флуоресценции NBD от температуры. г Интенсивность флуоресценции и изображения порошков NBD при освещении лампой с длиной волны 365 нм для разной продолжительности и флуоресценции порошков NBD при разной температуре измерения
Оценка цитотоксичности
Анализы MTT использовали для оценки цитотоксичности NBD. Жизнеспособность клеток HeLa, инкубированных с NBD, и двумя другими типами CD, синтезированных гидротермальным методом, как показано на рис. 4. Как показано на рисунке, жизнеспособность клеток мало снижается при введении раствора NBD, даже когда концентрация NBD достигает 800 мкг / мл. Выживаемость клеток составляла 70% и 67%, когда клетки HeLa инкубировали с двумя другими видами CD в концентрации 800 мкг / мл. Очевидно, что NBD демонстрируют лучшую биосовместимость, чем компакт-диски, полученные из химических реагентов.
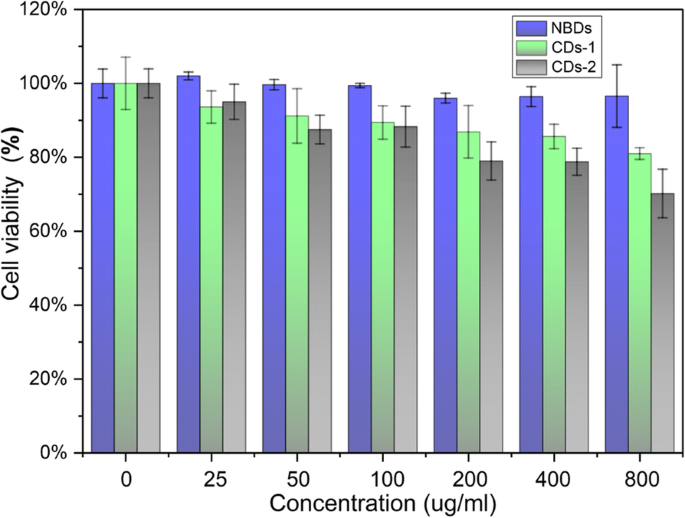
Жизнеспособность клеток HeLa после 72 ч инкубации с различными концентрациями NBD и CD
Свойства чувствительности NBD к Fe 3+
Интересно, что флуоресценцию NBD можно эффективно погасить с помощью Fe 3+ , как показано на рис. 5а, и интенсивность ФЛ NBD значительно уменьшается с увеличением Fe 3+ концентрация. Более того, между F 0 можно построить хорошую линейную зависимость. / F и Fe 3+ концентрация от 0 до 30 мкМ ( R 2 =0,99), где F 0 и F - интенсивность ФЛ NBD при ex / em 370/445 нм в отсутствие и в присутствии Fe 3+ , как показано на рис. 5b. Эффективность гашения рассчитывалась по формуле Штерна-Фольмера:
$$ \ frac {{\ mathrm {F}} _ 0} {\ mathrm {F}} =1+ {K} _ {\ mathrm {SV}} \ left [Q \ right] $$ (1) <изображение>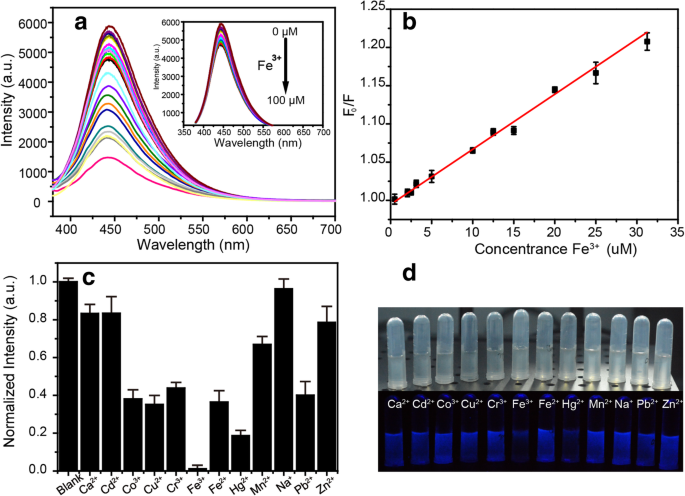
а Спектры ФЛ NBD в присутствии различных концентраций Fe 3 + . б Градуировочная кривая датчика как функция Fe 3 + концентрация. c Интенсивность флуоресценции NBD в присутствии различных ионов. г Фотографические изображения раствора НБД с различными ионами металлов при внутреннем и УФ-освещении
где K sv - константа тушения Штерна-Фольмера, а [ Q ] - это Fe 3+ концентрация. Уравнение линейной регрессии: Y =0,0072 X + 0,99479, R 2 =0,99. Предел обнаружения (LOD) предложенного сенсора был определен как 2,9 мкМ, что ниже максимально допустимого уровня Fe 3+ . (5,37 мкМ) в питьевой воде, установленным Агентством по охране окружающей среды США (USEPA) [24]. Селективность - еще один важный параметр для химических сенсоров. Следовательно, флуоресцентный отклик датчика на несколько мешающих ионов металлов был исследован, включая Ca 2+ , CD 2+ , Co 2+ , Cu 2+ , Cr 3+ , Fe 3+ , Fe 2+ , Hg 2+ , Mn 2+ , Na + , Pb 2+ , и Zn 2+ . Ионы металлов каждый в концентрации 10 −2 M добавляли в 1 мл раствора NBDs с концентрацией 3 г / л. На рис. 5c можно увидеть, что интенсивность флуоресценции NBD более чувствительно реагирует на Fe 3+ чем другие ионы металлов. Фотографии на рис. 5d представляют собой изображения NBD с различными ионами при внутреннем и УФ-освещении, а концентрация ионов металлов составляла 100 мкМ. Очевидно, что NBD тушатся в присутствии Fe 3+ , указывая на то, что их можно использовать для визуального обнаружения.
Механизм гашения
Механизм тушения NBD в присутствии Fe 3+ обсуждалось на основе спектров поглощения в УФ-видимой области и времени жизни флуоресценции NBD. Из спектров поглощения UV-Vis, показанных в дополнительном файле 1:Рисунок S8, нет изменений пиков поглощения при 270 нм и 340 нм с введением Fe 3+ . , что указывает на то, что Fe 3+ не влияет на структуру NBD [41]. Помимо спектра поглощения UV-Vis, эффект Fe 3+ на срок службы NBD также был изучен. На рис. 6а время жизни флуоресценции становится короче после добавления Fe 3+ . , который может включать частичный перенос электронов NBD на d орбиталь Fe 3+ , тем самым уменьшая излучательную рекомбинацию NBD [42]. Механизм тушения флуоресценции NBD, вызванный Fe 3+ показан на рис. 6б. Чувствительный эффект гашения флуоресценции NBD в присутствии Fe 3+ может происходить из-за сильного взаимодействия между Fe 3+ и поверхностные группы NBD. Fe 3+ имеет более сильное сродство связывания и более быструю кинетику хелатирования с амино и карбоксильными группами на поверхности NBD. Особая координация между Fe 3+ ионы и фенольные гидроксильные / аминогруппы NBD широко используются для обнаружения Fe 3+ ионы или окрашенные реакции в традиционной органической химии [43, 44]. Кроме того, окислительно-восстановительные потенциалы Fe 3+ / Fe 2+ ( Ф =0,77) расположены между самой низкой незанятой молекулярной орбиталью (НСМО) и самой высокой занятой молекулярной орбиталью (ВЗМО) NBD, вызывая фотоиндуцированный перенос электронов от НСМО к сложным состояниям Fe 3+ [45]. Эти результаты демонстрируют, что NBD очень чувствительны к Fe 3+ над ионами других металлов.
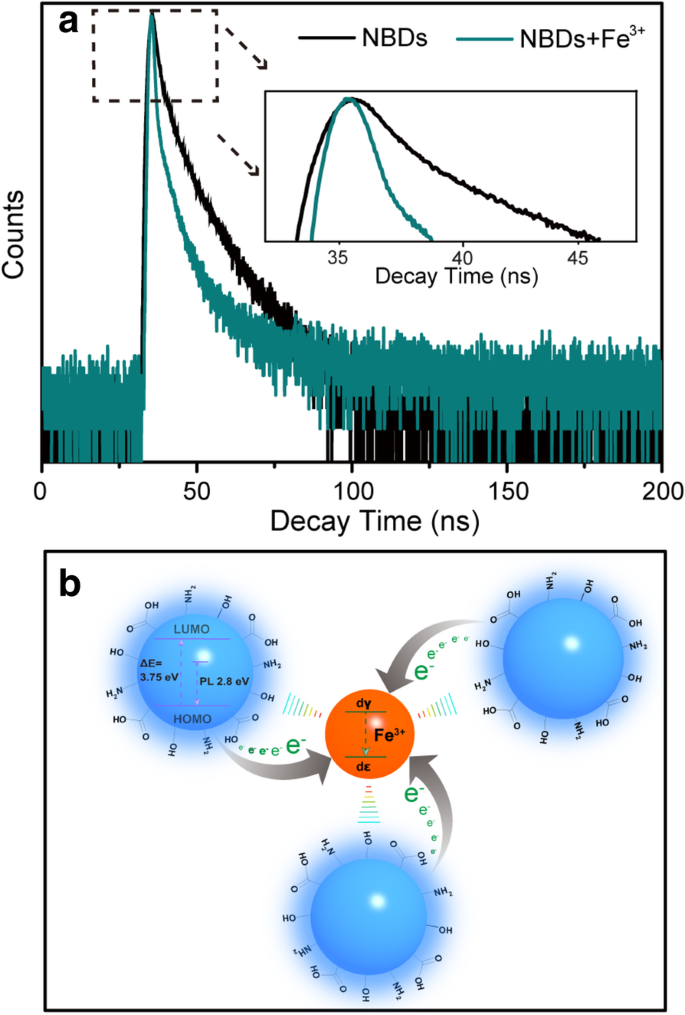
а Следы затухания флуоресценции НИЗ в отсутствие и в присутствии Fe 3 + при возбуждении на 370 нм и испускании на 445 нм. б Схематическая иллюстрация возможного механизма тушения флуоресценции NBD в присутствии Fe 3 + ионы
Заключение
Таким образом, люминесцентные NBD были получены из сои с использованием метода UES без нагревания. NBD демонстрируют ярко-синюю флуоресценцию с PL QY, равным 16,7%, и благодаря использованию съедобной биомассы и процесса синтеза без нагрева жизнеспособность клеток по-прежнему сохраняется на 100%, даже если концентрация NBD достигает 800 мкг / мл. Кроме того, флуоресценция NBD проявляет специфическую чувствительность к Fe 3+ , а LOD может достигать 2,9 мкМ. Низкая токсичность и высокий предел обнаружения указывают на то, что NBD, как ожидается, найдут потенциальное применение в биологических и экологических системах.
Сокращения
- FTIR:
-
Инфракрасное преобразование Фурье
- HAADF-STEM:
-
Сканирующая просвечивающая электронная микроскопия с кольцевым кольцом и большим углом в темном поле
- LOD:
-
Предел обнаружения
- NBD:
-
Точки нанобиомассы
- ЯМР:
-
Ядерный магнитный резонанс
- PL:
-
Фотолюминесценция
- QD:
-
Квантовые точки
- КГ:
-
Квантовый выход
- ТЕМ:
-
Просвечивающая электронная микроскопия
- UES:
-
Стратегия ультразвуковой экстракции
- USEPA:
-
Агентство по охране окружающей среды США
- XPS:
-
Рентгеновская фотоэлектронная спектроскопия
- XRD:
-
Рентгеновская дифракция
Наноматериалы
- Демонстрация гибкого биосенсора на основе графена для чувствительного и быстрого обнаружения клеток рака яи…
- Многофункциональные наночастицы золота для улучшенных диагностических и терапевтических применений:обзор
- Достижения и проблемы флуоресцентных наноматериалов для синтеза и биомедицинских приложений
- N, N-диметилформамид, регулирующий флуоресценцию квантовых точек MXene для чувствительного определения Fe3 +
- Синтез квантовых точек ZnSe / CdS / ZnS Core / Shell с подавленной реабсорбцией и их применение для иммуносорбентного ана…
- Простой подход к синтезу флуоресцентных квантовых точек углерода из сточных вод тофу
- Синтез водорастворимых квантовых точек сульфида сурьмы и их фотоэлектрические свойства
- Возобновляемый флуоресцентный зонд BHN-Fe3O4 @ SiO2 Гибридная наноструктура для Fe3 + и ее применение в биоимиджинге
- Экологичный и простой синтез нанопроволок Co3O4 и их перспективное применение с графеном в литий-ионных батаре…
- Причины коробления печатных плат и меры по их устранению



