Фосфид кобальта (Co2P) с заметной электрокаталитической активностью, разработанный для чувствительного и селективного бесферментного биоанализа перекиси водорода
Аннотация
В данной работе наночастицы фосфида кобальта (Co 2 P НЧ) были получены простым и мягким гидротермальным методом без использования вредного источника фосфора. Морфологическая структура и поверхностный компонент Co 2 P характеризовали методами просвечивающей электронной микроскопии, рентгеновской дифракции и рентгеновской фотоэлектронной спектроскопии. Учитывая превосходную активность электрокаталитического восстановления и хорошую электропроводность фосфида переходного металла, мы получили Co 2 НЧ P на подложке из оксида индия и олова (ITO) (Co 2 P / ITO) для H 2 О 2 обнаружение. Ко 2 Датчик P / ITO показал быстрый амперометрический отклик менее 5 с, более широкий диапазон отклика от 0,001 до 10,0 мМ и низкий предел обнаружения 0,65 мкМ. Кроме того, неферментативный Co 2 Датчик P / ITO показал выдающуюся селективность, воспроизводимость, повторяемость и стабильность, что соответствует требованиям Co 2 Электрод P / ITO для достаточно надежного и перспективного биосенсора на H 2 О 2 зондирование.
Введение
Перекись водорода (H 2 О 2 ) является типичным представителем активных форм кислорода в живых организмах и играет решающую роль в нормальном физиологическом функционировании [1]. Концентрация H 2 О 2 в живых клетках тесно связана с физиологическим балансом клетки [2]. Также сообщалось о многочисленных исследованиях, что рак, болезнь Альцгеймера, болезнь Паркинсона и некоторые тяжелые заболевания могут быть вызваны аномальной концентрацией H 2 О 2 [3,4,5]. Разработка точных, чувствительных, быстрых и селективных методов определения концентрации H 2 О 2 , нормальный биомаркер окислительного стресса, несомненно, будет полезен для ранней диагностики. До сих пор в H 2 применялось множество аналитических методов, таких как спектроскопия [6], колориметрия [7], флуоресценция [8, 9] и электрохимические методы [10,11,12]. О 2 определение. Электрохимический метод, особенно амперометрический тест, постепенно становится одним из самых простых и эффективных методов определения H 2 О 2 биологический анализ среди различных методов зондирования благодаря его преимуществам, таким как высокая чувствительность, исключительная селективность и низкая стоимость.
Доказано, что ферментативные электрохимические сенсоры являются эффективными инструментами для обнаружения H 2 О 2 . Однако широкое практическое применение сенсоров на основе ферментов ограничено сложной иммобилизацией, нестабильностью окружающей среды и низкой воспроизводимостью. Следовательно, разработка неферментативного электрохимического H 2 О 2 датчики совершенно незаменимы.
В последние годы все большее количество сенсоров на основе благородных металлов [13,14,15], неблагородных металлов и их соответствующих соединений [16,17,18,19] или углеродных материалов [20, 21] используется для электрохимический H 2 О 2 обнаружение. В качестве электрохимических активных материалов для изготовления неферментативных биосенсоров соединения переходных металлов привлекают все больший интерес. Фосфиды переходных металлов (TMP) - это класс недавно разработанных материалов с превосходной электрокаталитической активностью, хорошей электропроводностью и множеством выдающихся свойств. Таким образом, они были широко изучены для применения в разделении воды [22, 23], гидрообессеривании [24] и электродах суперконденсаторов [25]. Недавние исследования показывают, что CoP, Ni 2 P и Cu 3 P [26,27,28] также можно использовать в качестве эффективного электрокатализатора для неферментативного H 2 О 2 обнаружение. Однако количество исследований по применению ТМП в биоанализе в настоящее время все еще ограничено. Кроме того, использование трифенилфосфина [29, 30], белого фосфора [31, 32] или другого источника фосфора, опасного для окружающей среды [33], может увеличить операционный риск при приготовлении ТМФ. Поэтому в этой области стоит дополнить некоторые исследовательские работы по разработке зеленого метода подготовки ТМП.
В данной работе наночастицы фосфида кобальта (Co 2 P NP) были получены одностадийным гидротермальным методом с использованием ацетата кобальта и красного фосфора в качестве сырья. Здесь мы изготовили Co 2 НЧ P на подложке из оксида индия и олова (ITO) методом капельного литья H 2 О 2 обнаружение. Со 2 P продемонстрировал отличную электрокаталитическую активность по отношению к H 2 О 2 снижение. Более того, он показал благоприятную селективность, отличную воспроизводимость и хорошую стабильность, что, таким образом, продемонстрировало его потенциальное применение в качестве чувствительной платформы для H 2 О 2 обнаружение.
Экспериментальный раздел
Реагенты и материалы
Все реагенты были аналитической чистоты и использовались без дополнительной очистки. Тетрагидрат ацетата кобальта (II) (Co (Ac) 2 · 4H 2 O), гексагидрат хлорида кобальта (CoCl 2 · 6H 2 O), D - (+) - глюкоза, L-глицин (L-Gly), аскорбиновая кислота (AA), мочевая кислота (UA), мочевина, NaCl, KCl, NaH 2 ЗП 4 , Na 2 HPO 4 , перекись водорода (30% H 2 О 2 ), этанол и ацетон были приобретены у Sinopharm Chemical Reagent Co., Ltd. China. D - (-) - фруктоза, L-аргинин (L-Arg), L-лизин (L-Lys), дофамин (DA), ацетаминофен (APAP), аминотриметиленфосфоновая кислота (ATMP, 50 мас.%) Были приобретены в Aladdin Ltd. Коммерческий красный фосфор (98,5%, 100 меш) был приобретен у Energy Chemical Technology (Shanghai) Co., Ltd. Полимерная дисперсия Nafion PFSA (5%) была приобретена у Beijing Honghaitian Technology Co., Ltd. Использовалась деионизированная вода. во всех экспериментах. Стекло из оксида индия и олова (ITO) (10 × 20 × 1,1 мм с пленкой ITO 185 ± 2 нм и поверхностным сопротивлением 6,6 ± 0,1 Ом) было поставлено компанией Shenzhen South Xiangcheng Technology Co., Ltd.
Синтез Co 2 P Наночастицы
Технический красный фосфор (2 г) диспергировали в 15 мл H 2 . O под обработкой ультразвуком и гидротермической обработкой при 200 ° C в течение 12 часов в 50-миллилитровом автоклаве из нержавеющей стали с тефлоновым покрытием для очистки оксидных слоев [34]. Затем обработанный гидротермальным способом красный фосфор сушили в вакуумной печи. После завершения предварительной обработки красным фосфором 1 ммоль Co (Ac) 2 · 4H 2 О растворяли в 30 мл дистиллированной воды с получением водного раствора. Затем гидротермально обработанный красный фосфор добавляли в раствор при ультразвуковой обработке в течение 15 мин с молярным соотношением Co / P 1/10. Приготовленную суспензию быстро вылили в автоклав на 50 мл с тефлоновым покрытием. Затем автоклав помещали в электронную печь и подвергали гидротермической обработке при 160, 200, 240 ° C в течение 12 часов соответственно. Затем продукт собирали центрифугированием и трижды промывали дистиллированной водой и этанолом соответственно. Наконец, Co 2 НЧ P сушили при 60 ° C в течение 3 ч на воздухе.
Синтез Co (PO 3 ) 2
Способ приготовления Co (ПО 3 ) 2 была сделана ссылка на предыдущий отчет [35]. 0,1 М CoCl 2 · 6H 2 Первоначально готовили О-метанольный раствор. Затем 2 мл ATMP (50 w t%) по каплям добавляли к 20 мл вышеуказанного пурпурного раствора и перемешивали в течение 30 мин. Впоследствии в растворе образовался нерастворимый координационный полимер кобальт-метафосфат. Полученный розовый порошок дополнительно нагревали до 900 ° C в потоке Ar со скоростью нагрева 5 ° C · мин -1 . а затем выдержали 2 ч. После охлаждения до комнатной температуры черный продукт собирали и повторно нагревали при 650 ° C в течение 4 часов на воздухе для удаления карбонизированного органического лиганда. Наконец, светло-фиолетовый порошок Co (PO 3 ) 2 был получен.
Изготовление Co 2 Электрод P / ITO
Сначала стекло ITO (1 см × 2 см) очищали в ацетоне, этаноле и деионизированной воде в течение 10 мин, соответственно, обработкой ультразвуком. После этого обработанный ITO сушили в атмосфере азота. Для модификации электрода 5 мг Co 2 НЧ P диспергировали в 1 мл деионизированной воды с образованием 5 мг / мл -1 Со 2 Подвеска P. Затем к суспензии добавляли 5 мкл 5% раствора нафиона и смесь обрабатывали ультразвуком в течение 15 мин для получения однородной суспензии, напоминающей чернила. Ко 2 Электрод P / ITO был приготовлен путем заливки 100 мкл Co 2 P суспендировали на поверхности ITO и сушили на воздухе в качестве рабочего электрода. Схема процесса подготовки Co 2 Электрод P / ITO показан на схеме 1.
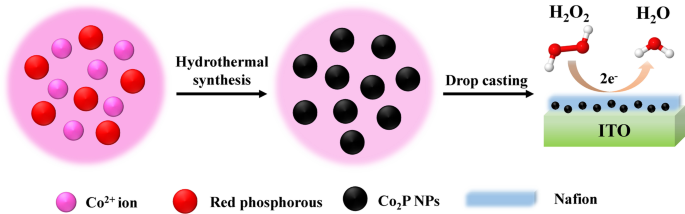
Схема приготовления Co 2 Электрод P / ITO и H 2 О 2 зондирование
Характеристики
Данные рентгеновской дифракции (XRD) анализировали на дифрактометре D8 ADVANCE с Cu Kα-излучением. Измерения с помощью просвечивающей электронной микроскопии (ПЭМ) проводили с использованием Tecnai G2 F20 с детектором энергодисперсного спектра. Спектры рентгеновской фотоэлектронной спектроскопии (XPS) были измерены на спектрометре Thermo ESCALAB 250XI.
Электрохимические измерения
Измерения вольтамперометрии проводились на электрохимической станции CHI 660E в трехэлектродной системе с использованием Co 2 Электрод P / ITO в качестве рабочего электрода, платиновая фольга (1 см × 1 см) в качестве противоэлектрода и Ag / AgCl с 3 M раствором KCl в качестве электрода сравнения для исследования электрохимической активности синтезированных образцов для H 2 О 2 обнаружение. Фосфатный буферный раствор (PBS; 0,1 М, pH 7,4) использовали в качестве электролита для моделирования физиологической среды в организме человека. Сенсорные характеристики Co 2 Электрод P / ITO в направлении H 2 О 2 Детектирование исследовали методами циклической вольтамперометрии (CV) и амперометрии (I-t). Все эксперименты по обнаружению проводили при перемешивании со 100 об / мин и комнатной температуре. Испытания электрохимического импеданса проводились на электрохимической рабочей станции VersaSTAT 3F, а раствор феррицианида использовался в качестве электролита для измерения импеданса.
Результаты и обсуждение
Характеристика Co 2 P НП
Кристаллическая структура Co 2 Количество P NP подтверждено рентгеноструктурным анализом. На рисунке 1а показаны дифрактограммы Co 2 . Образцы P готовили при 160, 200 и 240 ° C в течение 12 ч. Ко 2 Образец P, приготовленный при 200 ° C, показывает дифракционные пики около 40,7 °, 40,9 °, 52,0 ° и 56,2 °, которые соответствуют характерным плоскостям дифракции в точках (121), (201), (002) и (320) для орторомбической фазы. из Co 2 P (JCPDS № 32-0306). При изменении температуры от 160 до 200 ° C интенсивности дифракционных пиков увеличивались, а пики становились более узкими и резкими, что указывает на то, что продукты имеют более высокую кристалличность при 200 ° C. Однако, когда температура достигла 240 ° C, образовались некоторые примеси, и дифракционные пики при 29,7 ° были отнесены к плоскости дифракции при (-222) Co (PO 3 ) 2 (JCPDS № 27-1120). Влияние синтетического времени на получение Co 2 P ниже 200 ° C показано в Дополнительном файле 1:Рис. S1. Когда продолжительность контролировалась в пределах 12 часов, полученный Co 2 P NP показали наименьшее значение полной ширины на половине максимума пика (121), что свидетельствует о лучшей кристалличности. Кроме того, при изменении времени реакции от 6 до 24 ч в образце не было примесей. Согласно формуле Шеррера, рассчитанный размер зерна Co 2 НЧ P, полученные при 200 ° C в течение 12 ч, имели размер 14,2 нм.
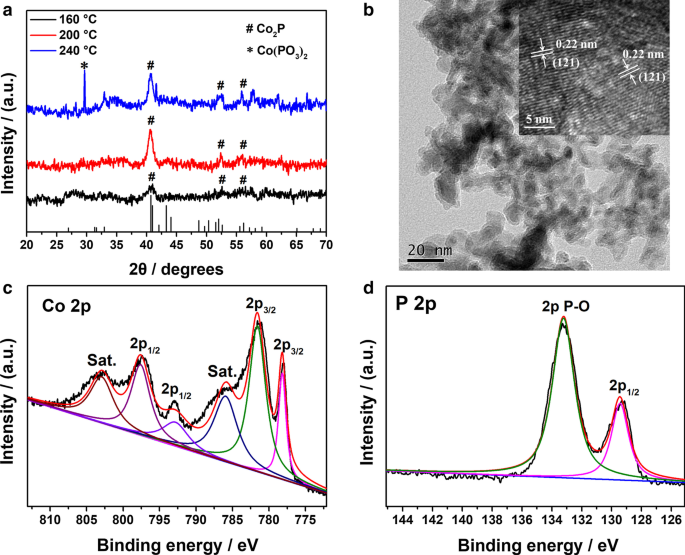
а Рентгенограммы Co 2 НЧ П готовили при разных температурах в течение 12 ч. б Изображение на просвечивающем электронном микроскопе и изображение на просвечивающем электронном микроскопе высокого разрешения (вставка) Co 2 P НП. XPS-спектры Co 2 P в c Co 2 p регион и d P 2 p регион
Морфология Co 2 P НЧ оценивали с помощью ПЭМ-измерений. Как показано на рис. 1b, продукт, полученный при 200 ° C, состоит из наночастиц неправильной формы с диаметром около 10–20 нм, и две полосы решетки могут быть четко видны на изображении ПЭМ высокого разрешения (HRTEM) (вставка на рис. 1б). Расстояние между соседними плоскостями составляет 0,22 нм, что соответствует грани (121) Co 2 P, что дополнительно подтверждает, что образование TMP представляет собой Co 2 П.
Метод XPS был использован для анализа химического состава на поверхности Co 2 P. Дополнительный файл 1:Рис. S2 показывает спектр обзора XPS Co 2 В образце обнаруживаются элементы P. Co, P и O, что подтверждает наличие Co 2 P и некоторые окисленные продукты. Спектры энергодисперсионной рентгеновской спектроскопии (EDX) Co 2 P (дополнительный файл 1:рис. S3) дополнительно подтверждает сосуществование трех элементов (Co, P, O) в образце. Спектры РФЭС высокого разрешения Co 2p и P 2p показаны на рис. 1c, d соответственно. В спектре Co 2p пики при 781,1 и 797,6 эВ могут быть отнесены к энергиям связи (BE) Co 2+ 2 п 3/2 и Co 2+ 2 п 1/2 соответственно [26, 36]. Пики при 786,0 и 803,1 эВ - это два очевидных сателлитных пика встряски. БЭ Co 2p, равное 778,2 эВ, сдвигается в положительную сторону по сравнению с металлическим Co (777,9 эВ), что позволяет предположить, что Co в Co 2 P имеет частичный положительный заряд ( δ + ) с малым значением (0 < δ <2) [37]. Напротив, P 2 p BE 129,4 эВ отрицательно смещается от элементарного P (130,2 эВ), так что P имеет частичный отрицательный заряд ( δ - ) в Co 2 P. Изменения BE в Co и P элементе по сравнению с их элементарным веществом, соответственно, показывают, что направление переноса электронной плотности в Co 2 P от Co до P [38]. Поверхностное окисление Co 2 P генерирует несколько окисленных P в образце. Следовательно, пики при 133,2 эВ в диапазоне высоких значений BE относятся к оксидам [39].
Электрохимическое обнаружение H 2 О 2 в Co 2 Электрод P / ITO
Для исследования электрокаталитической активности Co 2 P НП в H 2 О 2 восстановления, мы разработали неферментативный H 2 О 2 электрод методом капельного литья Co 2 Подвешивание НЧ П на голой поверхности ITO. На рис. 2а показаны ВАХ чистого ITO и Co 2 . P / ITO в 0,1 M PBS при pH 7,4 с 5,0 мМ H 2 и без него О 2 , соответственно. Пунктирные линии показывают, что ответ голого ITO на H 2 О 2 снижение незначительно. Однако Co 2 Электрод P / ITO показывает замечательный пик восстановления при -0,5 В в присутствии H 2 О 2 , который демонстрирует заметную электрокаталитическую активность Co 2 P НП в сторону H 2 О 2 снижение. На рисунке 2b представлены ВАХ Co 2 . P / ITO при разных скоростях развертки (от 30 до 100 мВ с −1 ) с 2,5 мМ H 2 О 2 . При увеличении скорости сканирования пиковый ток уменьшения увеличивался, а максимальный потенциал сдвигался в сторону с более отрицательным потенциалом, указывая на уменьшение H 2 О 2 на Co 2 P / ITO была необратимой реакцией. Соответствующая калибровочная кривая (вставка, рис. 2b) показывает, что пиковые плотности тока восстановления увеличиваются линейно пропорционально скорости сканирования, предполагая, что электрохимическое восстановление H 2 О 2 на поверхности Co 2 Электрод P / ITO - это процесс с контролируемой поверхностью [40].
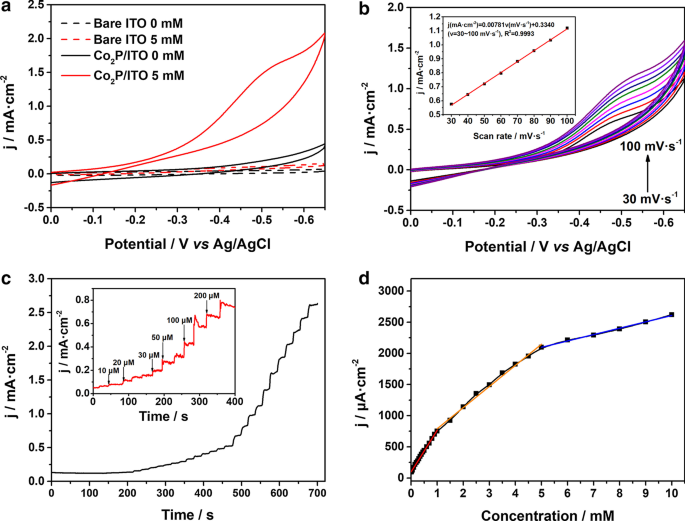
а Кривые CV чистого ITO и Co 2 Электрод P / ITO в 0,1 M PBS с 5,0 мМ H 2 и без него О 2 при скорости сканирования 100 мВ с −1 . б Кривые CV Co 2 Электрод P / ITO в 2,5 мМ H 2 О 2 при скоростях развертки от 30 до 100 мВ с −1 . Вставка:соответствующий график зависимости тока от скорости сканирования. c Амперометрические характеристики Co 2 Электрод P / ITO с последовательным добавлением H 2 О 2 в 0,1 М PBS. г Градуировочная кривая постоянного тока в зависимости от концентрации H 2 О 2
На рис. 2c, d показан амперометрический отклик и калибровочная кривая Co 2 . Электрод P / ITO при последовательном добавлении H 2 О 2 в 0,1 М PBS при -0,5 В при перемешивании. Ко 2 Электрод P / ITO показал быструю реакцию на добавление H 2 О 2 и достиг установившегося тока в течение 5 с. Калибровочная кривая на рис. 2d показывает, что датчик отображает полилинейный диапазон H 2 О 2 концентрация от 0,001 до 1,0 мМ, 1,0–5,0 мМ и 5,0–10,0 мМ. Чувствительность датчика изменяется с увеличением концентрации H 2 . О 2 , за счет изменения кинетики электрокаталитического восстановления H 2 О 2 на поверхности электрода. Согласно предыдущим отчетам, шаг определения скорости H 2 О 2 В редукции преобладает H 2 О 2 адсорбция при низкой концентрации, тогда как активация H 2 О 2 является основным определяющим фактором при высокой концентрации. В средней области кинетика восстановления H 2 О 2 контролируется адсорбцией и активацией одновременно [10]. Множество аналитиков будут адсорбировать на поверхности Co 2 P и покрывают активные центры в высокой концентрации, что приводит к снижению чувствительности [41].
Сравнение на H 2 О 2 зондирование характеристик подготовленного Co 2 Образец P при различных температуре и времени реакции показан в дополнительном файле 1:рис. S4, S5 и в таблице S1, что указывает на то, что Co 2 Образец P, приготовленный при 200 ° C в течение 12 часов, показывает лучший H 2 О 2 зондирование спектаклей. При повышении температуры реакции до 240 ° C образовавшийся Co (PO 3 ) 2 в Co 2 P можно рассматривать как примесь. Чтобы дополнительно прояснить влияние Co (PO 3 ) 2 на H 2 О 2 обнаружение, электрохимические свойства Co (PO 3 ) 2 были исследованы. Как показано в Дополнительном файле 1:Рис. S6, Co (PO 3 ) 2 демонстрирует незначительный электрохимический отклик по отношению к H 2 О 2 и его проводимость уступает Co 2 P, который снижает текущий сигнал Co 2 P / ITO в амперометрическом тесте. Следовательно, более высокая чистота и лучшая кристалличность Co 2 Образец P может способствовать улучшению характеристик зондирования. Таким образом, мы выбираем Co 2 Образец P приготовлен при 200 ° C и 12 ч как лучший H 2 О 2 чувствительный материал. Калибровка I - т кривая также представляет хорошую линейную зависимость в концентрации 1,0–50 мкМ, физиологический диапазон H 2 О 2 концентрации в биосистеме (рис. S7) [28], что может быть полезно для улучшения возможности практического применения этого датчика. Кроме того, предел обнаружения (LOD) H 2 О 2 Датчик может быть рассчитан как 0,65 мкМ при отношении сигнал / шум 3. По сравнению с ранее сообщенным H 2 О 2 сенсор, комплексные электрохимические характеристики нашего Co 2 Преобразователи P / ITO превосходят датчики с подходящей чувствительностью, линейным диапазоном и уровнем детализации, как показано в таблице 1.
После обнаружения 1,0 мМ H 2 О 2 многократно 35 раз (рис. 3а, б) РФЭС-спектры в Co 2 p и P 2 p область Co 2 P анализируются для дальнейшего изучения механизма восприятия. Нет значительного изменения положения пиков в P 2 p область до и после H 2 О 2 обнаружение. Однако пики при 778,2 и 793,0 эВ в Co 2 p спектр исчез после многократных измерений. Поскольку пик при 778,2 эВ указывает на существование восстановленных частиц Co в Co 2 В образце P [37] исчезновение этих двух пиков демонстрирует, что восстановленные частицы Co с низкой валентностью в Co 2 P может быть окислен H 2 О 2 во время процесса обнаружения, особенно с высокой концентрацией H 2 О 2 . Остаточные пики в Co 2 p области (782,1 и 798,3 эВ) относятся к Co 2+ 2 п 3/2 и Co 2+ 2 п 1/2 , соответственно, предполагая исключительное существование разновидностей Co (II) в Co 2 P после нескольких измерений. Согласно предыдущим отчетам об использовании электрокатализатора на основе кобальта в H 2 О 2 обнаружение, Co 2+ разновидности показаны как каталитические активные центры для H 2 О 2 сокращение [46,47,48]. Обычно электрохимическое восстановление H 2 О 2 проходит два этапа в PBS [49, 50], как показано ниже.
$$ {\ text {H}} _ {{2}} {\ text {O}} _ {{2}} + {\ text {e}} ^ {-} \ to {\ text {OH}} _ {{{\ text {ad}}}} + {\ text {OH}} ^ {-} $$ (1) $$ {\ text {OH}} _ {{{\ text {ad}}}} + {\ text {e}} ^ {-} \ to {\ text {OH}} ^ {-} $$ (2) $$ {\ text {2OH}} ^ {-} + {\ text {2H}} ^ {+} \ to {\ text {2H}} _ {{2}} {\ text {O}} $$ (3)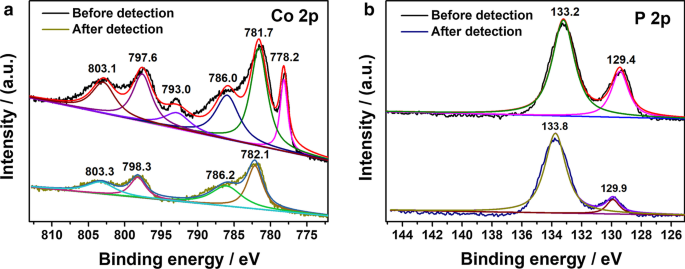
Сравнение спектров XPS в a Co 2 p регион и b P 2 p область Co 2 P до и после обнаружения
На первом этапе H 2 О 2 получает электрон для образования адсорбированного OH - (ОН реклама ). Когда промежуточный OH ad получает дополнительный электрон, конечный продукт восстановления H 2 О 2 , H 2 O, генерируется. Поскольку окислительно-восстановительный потенциал H 2 О 2 / H 2 O выше Co 3+ / Co 2+ , формы Co (II) в Co 2 P может быть окислен до Co (III) в процессе переноса электрона, а H 2 О 2 уменьшается до H 2 О безвозвратно. Во время амперометрического теста приложенное смещение составляет -0,5 В по сравнению с Ag / AgCl (равно 0,14 В по сравнению с . NHE), что ниже стандартного окислительно-восстановительного потенциала Co 3+ / Co 2+ . В результате окисленный Co (III) может быть восстановлен до Co (II), и эти каталитические активные центры Co (II) снова регенерируются. Таким образом, можно сделать вывод, что каталитический цикл разновидностей Co (II) имеет место во время электрохимического обнаружения H 2 О 2 а восстановленные частицы Co с низкой валентностью окисляются H 2 О 2 после повторных измерений.
Избирательность, стабильность, воспроизводимость и повторяемость Co 2 Электрод P / ITO
Эффективность защиты от помех - еще одно важное свойство биосенсора. Азот высокой чистоты использовался, чтобы избежать влияния растворенного кислорода в растворе, поскольку кислород можно было восстановить при аналогичном потенциале, который применялся в амперометрическом тесте [51]. Сравнение кривых CV Co 2 P / ITO в 0,1 M PBS с продувкой азотом или без нее, потенциал восстановления и отклик по току 2,5 мМ H 2 О 2 аналогичны, как показано на рис. S8, что позволяет предположить, что вмешательством растворенного кислорода можно пренебречь. Селективность Co 2 P / ITO был также протестирован с обычными веществами и другими небольшими молекулами в жидкости организма, такими как некоторые неорганические соли, сахариды, аминокислоты и восстановительные биомолекулы. Как показано на рис. 4a, текущим откликом после добавления вышеупомянутых помех можно пренебречь по сравнению с откликом 1,0 мМ H 2 О 2 . Поскольку оба двух атома кислорода H 2 О 2 может быть связан с одним или двумя атомами Co [52], H 2 О 2 молекула будет химически адсорбироваться на частицах Co (II) в Co 2 P конкретно. Кроме того, помехи от неизбирательного окисления некоторых восстанавливающих соединений в реальных биологических образцах при высоком потенциале также могут быть значительно уменьшены при более низком потенциале смещения [53]. Следовательно, благоприятная селективность Co 2 P в сторону H 2 О 2 в основном извлекает выгоду из разновидностей Co (II) как специфических участков адсорбции и прикладываемого отрицательного потенциала смещения во время процесса зондирования.
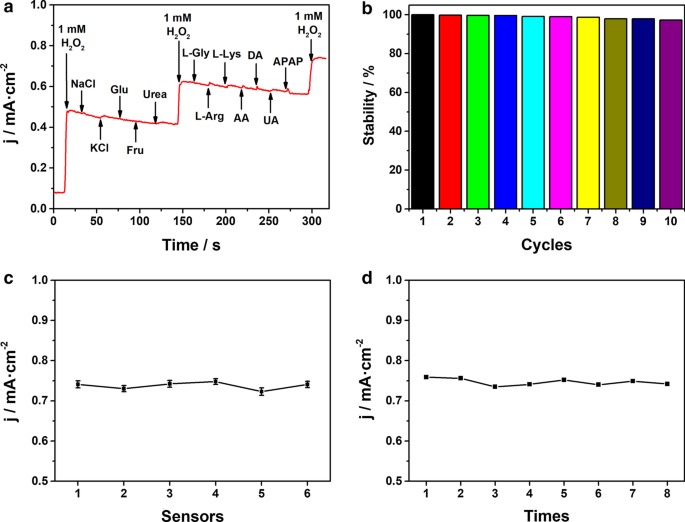
а Амперометрические характеристики Co 2 Электрод P / ITO с добавкой 1 мМ H 2 О 2 и другие мешающие частицы (10 мМ NaCl, KCl, Glu, Fru, мочевина, L-Gly, L-Arg, L-Lys, AA; 1 мМ DA, UA; 0,5 мМ APAP) в 0,1 М PBS. б Катодные пиковые токи десяти последовательных сканирующих CV-кривых в 50 мкМ H 2 О 2 . c Воспроизводимость шести Co 2 Электроды P / ITO для обнаружения 1,0 мМ H 2 О 2 . г Повторяемость Co 2 Электрод P / ITO для обнаружения 1,0 мМ H 2 О 2 восемь раз
Кроме того, стабильность, воспроизводимость и повторяемость Co 2 Также были оценены преобразователи P / ITO. Пиковые токи восстановления десяти последовательных кривых CV при сканировании в 50 мкМ H 2 О 2 показан на рис. 4б. После десяти циклов пиковый ток электрода снизился только на 2,7%. Кроме того, после хранения на воздухе в течение одного месяца датчик оставался примерно 98,2% от своего первоначального отклика по току (рис. S9), демонстрируя идеальную стабильность обнаружения и выдающуюся долговечность. Воспроизводимость между электродами исследуется путем вычисления относительного стандартного отклонения (RSD) H 2 О 2 текущие ответы. Чтобы исключить потенциальную ошибку при изготовлении электродов, насколько это возможно, установившаяся плотность тока в присутствии H 2 О 2 вычитается из исходного фонового сигнала отдельного электрода, и полученное значение разности рассматривается как электрохимический отклик каждого электрода. Шесть Co 2 Электроды P / ITO были изготовлены в тех же условиях для контролируемых экспериментов, и RSD откликов по току составляло 1,24%, как показано на рис. 4c, что указывает на относительно превосходную воспроизводимость Co 2 П / ИТО. Между тем, повторяемость была измерена на одном электроде путем обнаружения 1,0 мМ H 2 О 2 восемь раз, и было достигнуто RSD 1,14% (рис. 4d). Приведенные выше результаты иллюстрируют удовлетворительную стабильность, воспроизводимость и повторяемость электрода для неферментативного электрохимического обнаружения H 2 . О 2 .
Заключение
Таким образом, Co 2 НЧ П были успешно синтезированы гидротермальным методом. Кроме того, Co 2 НЧ P, приготовленные при 200 ° C в течение 12 часов, зарекомендовали себя как эффективный катализатор электрохимического восстановления H 2 . О 2 в pH 7,4 PBS. В качестве неферментативного H 2 О 2 датчик, Co 2 Электрод P / ITO показал быстрый амперометрический отклик менее 5 с, более широкий диапазон отклика от 0,001 до 10,0 мМ и низкий предел обнаружения 0,65 мкМ, а также удовлетворительную селективность, воспроизводимость и стабильность. Эта работа направлена на расширение исследований по применению фосфида переходного металла в электрохимическом обнаружении малых биомолекул и нашего Co 2 Датчик P / ITO может быть разработан как новая неферментативная платформа для H 2 О 2 обнаружение.
Доступность данных и материалов
Все данные и материалы доступны в полном объеме без ограничений.
Сокращения
- НП:
-
Наночастицы
- ITO:
-
Оксид индия и олова
- ТЕМ:
-
Просвечивающая электронная микроскопия
- HRTEM:
-
Просвечивающая электронная микроскопия высокого разрешения
- XRD:
-
Рентгеновская дифракция
- XPS:
-
Рентгеновская фотоэлектронная спектроскопия
- EDX:
-
Энергодисперсионная рентгеновская спектроскопия
- Резюме:
-
Циклическая вольтамперометрия
- Я-т:
-
Амперометрия
- Gly:
-
Глицин
- AA:
-
Аскорбиновая кислота
- UA:
-
Мочевая кислота
- Arg:
-
Аргинин
- Lys:
-
Лизин
- DA:
-
Дофамин
- APAP:
-
Ацетаминофен
- ATMP:
-
Триметиленфосфоновая кислота
- PBS:
-
Фосфатный буфер
- LOD:
-
Предел обнаружения
- RSD:
-
Относительное стандартное отклонение
Наноматериалы
- Демонстрация гибкого биосенсора на основе графена для чувствительного и быстрого обнаружения клеток рака яи…
- MoS2 с контролируемой толщиной для электрокаталитического выделения водорода
- Углеродные наноточки как двухрежимные нанодатчики для селективного обнаружения перекиси водорода
- Изготовление, характеристика и биологическая активность систем нано-доставки авермектина с различными разм…
- Оболочки диатомовых водорослей из кремнезема, адаптированные с использованием наночастиц Au, позволяют прово…
- Простой метод получения гетероперехода Cu2O-TiO2 NTA с видимой фотокаталитической активностью
- Новая кластерная микроструктура наноконусов с антиотражающими и супергидрофобными свойствами для фотоэлек…
- Плазмонный ИФА для чувствительного обнаружения биомаркеров заболеваний с помощью считывателя на смартфоне
- Влияние материалов, гетероструктуры и ориентации наногибридов на фотокаталитическую активность
- Токарный станок, созданный для точности и скорости



