Окисление и нано-диспергирование натуральных шелковых волокон
Аннотация
Натуральный Bombyx mori шелк (BS) и Antheraea pernyi шелк (AS) окисляли в растворах гипохлорита натрия (NaClO). После этого индивидуальные нановолокна шелка (SN) были получены после обработки суспензий окисленного шелка ультразвуком, при этом диаметры полученных SN составляли ~ 100 нм и составляли несколько микрометров в длину. Тонкие мембраны были сформированы путем отливки SN, которые обладали оптически прозрачными (пропускание более 75%), механически прочными (~ 4,5 ГПа модуля Юнга) и улучшенными смачивающими свойствами. Интересный процесс агрегации-диспергирования (повторного диспергирования) с использованием этих SN строго регулировался путем регулирования значений pH. Следовательно, отрицательно заряженные сверхновые могут быть сконцентрированы до ~ 20 мас.% (В 100 раз больше, чем исходная дисперсия) и предлагают исключительные преимущества для хранения, транспортировки и инженерных приложений.
Введение
Материалы с иерархической структурой вездесущи в естественных биологических системах [1, 2]. Они обеспечивают разнообразие функций благодаря первичным свойствам полимеров и функциональной адаптации структур в каждой иерархии [3,4,5]. Для создания искусственных материалов с расширенными функциями, которые воспроизводят такие особые свойства, необходимы процессы экстракции, которые сохраняют исходные наноструктуры полимеров [6,7,8,9,10]. Разнообразные исследования были посвящены выделению полисахаридных нановолокон (например, целлюлозы и хитина) из их волокнистых композитных структур с использованием химических, физических и биологических подходов [11,12,13]. В частности, полностью индивидуализированные и высококристаллические нановолокна были получены с помощью окисления природной целлюлозы / хитина, опосредованного 2,2,6,6-тетраметилпиперидин-1-оксильным радикалом (TEMPO), с последующей мягкой механической обработкой [14, 15 ]. Однако экономические и экологические проблемы все еще остаются; Эти существующие методы выделения нанофибрилл требуют дорогих и / или токсичных реагентов, таких как ТЕМПО и гексафторизопропанол (HFIP). Что еще более важно, низкая концентрация дисперсии полученных нановолокон ограничивает их хранение, транспортировку и применение.
Шелк животных, изготовленный широким кругом насекомых и пауков, также обладает иерархической волокнистой структурой [16, 17]. Эти белковые молекулы находятся в форме собранных фибрилл от наноразмеров до макромасштабов, что приводит к выдающимся механическим и биохимическим свойствам шелковых материалов [18,19,20,21]. Однако для получения наноструктур шелка процессы экстракции остаются проблемами из-за (i) сложной иерархической структуры, (ii) высокой кристалличности и (iii) адгезии между микро- / нано-фибриллами шелковых волокон. Расщепленные шелковые волокна подвергались ультразвуковой обработке [22]; однако полученные нановолокна были переплетены и не обрабатывались. При частичном растворении шелковых волокон с помощью системы соль-муравьиная кислота были получены неустойчивые древовидные пучки нановолокон [23]. Комплексный подход с использованием частичного растворения и обработки ультразвуком позволил получить шелковые волокна, размер которых был уменьшен до диаметра одной нанофибриллы [24], в то время как соотношение сторон и выход таких нановолокон еще предстоит улучшить.
Для решения этих проблем мы разработали простую и масштабируемую стратегию извлечения полноразмерных мезошелков [25]. Подобно выделению полисахаридов [26], карбоксильные группы были введены в Bombyx mori шелк (BS) и Antheraea pernyi шелковые (AS) волокна для диспергирования нановолокон за счет электростатического отталкивания; однако избыточные химические вещества, такие как TEMPO и бромид натрия (NaBr), были исключены, поскольку в селективном окислении не было необходимости. Здесь мы раскрыли эффективность этого процесса для получения отдельных нановолокон с высоким соотношением сторон. В результате были получены мембраны из шелковых нановолокон (SN), оптически прозрачные, механически прочные и улучшенные смачивающие свойства. По сравнению с нановолокнами на основе полисахаридов (т.е. нановолокнами целлюлозы и хитина) интересные агрегационно-редиспергирующие свойства SN регулировались значениями pH.
Материалы и методы
Окисление разобранных шелковых волокон
Разобранные шелковые волокна были приготовлены из сырого Bombyx mori . (или Antheraea pernyi ) волокна тутового шелкопряда (Xiehe Silk Co., Китай). Вкратце, 5 г шелковых волокон кипятили в течение 30 минут в водном растворе 0,02 М карбоната натрия с массовым соотношением 1:400 с последующей тщательной промывкой в дистиллированной воде и затем сушкой на воздухе. Затем очищенные шелковые волокна были погружены в раствор муравьиной кислоты (88 мас.%) С массовым соотношением 1:20. Смесь инкубировали при комнатной температуре не менее 1 ч, а затем гомогенизировали при 10000 об / мин в течение 3 мин для получения суспензии. Разобранные шелковые волокна были получены в твердом состоянии после центрифугирования суспензии при 8000 об / мин.
Для окисления разобранные шелковые волокна промывали до pH 7 и разрезали на короткие кусочки длиной несколько сантиметров, и желаемое количество раствора гипохлорита натрия (NaClO) добавляли в 100 мл воды с 1 г разобранных шелковых волокон. Гидроксид натрия (NaOH) непрерывно добавляли в смесь для поддержания pH на уровне 10. Когда потребление NaOH больше не наблюдалось, реакцию гасили добавлением капель 0,5 М соляной кислоты (HCl), чтобы довести pH до 7. Затем, Нерастворимую в воде фракцию центрифугировали при 10000 об / мин и несколько раз промывали. Наконец, шелковые нановолокна были получены после обработки нерастворимой в воде фракции ультразвуковым гомогенизатором при 19,5 кГц с выходной мощностью 300 Вт в течение 20 мин. Во избежание перегрева в течение длительного времени обработки ультразвуком использовалась баня с ледяной водой.
Рентгеноструктурный анализ окисленных шелковых волокон
Эксперименты по дифракции рентгеновских лучей (XRD) проводили с использованием многоцелевой системы дифракции рентгеновских лучей Ultima IV (Ultima IV, Ригаку, Япония) с источником Cu-Kα ( λ =0,1542 нм). Напряжение и ток источника рентгеновского излучения составляли 40 кВ и 30 мА соответственно. Результаты деконволюции окисленных шелковых волокон анализировали с использованием программного обеспечения PeakFit (4.0). Номера и положения пиков определялись по результатам вторых производных из спектров и фиксировались в процессе деконволюции. Пропускная способность была автоматически скорректирована программным обеспечением.
Наблюдения за морфологией нановолокон
Для наблюдения за образованием различных нановолокон дисперсию разбавляли до 0,01 мас.%. Для сканирующей электронной микроскопии аликвоту разбавленной дисперсии объемом 10 мкл помещали на кремниевую пластину и затем сушили на воздухе. Образцы были покрыты золотом и палладием и визуализированы с помощью СЭМ JEOL-JSM 7600F (JEOL, Япония) при напряжении 5 кВ. Для просвечивающей электронной микроскопии (ПЭМ) аликвоту разбавленной дисперсии объемом 10 мкл помещали на покрытую углеродом сетку для электронной микроскопии из Cu. Избыток жидкости абсорбировали фильтровальной бумагой, а затем сушили на воздухе. Сетку образцов наблюдали при 80 кВ с помощью просвечивающего электронного микроскопа Titan 80-300 (FEI, США). Размеры нанофибрилл анализировали с помощью программного обеспечения ImageJ (1.48), разработанного Национальным институтом здравоохранения США.
Механическое тестирование
Мембраны BS, AS, CN (нановолокно целлюлозы) и ChN (нановолокно хитина) толщиной примерно 50 мкм были отлиты методом испарения растворителя. Каждую мембрану из нановолокна делали на несколько полос длиной 60–80 мм и диаметром 5 мм, которые растягивали на универсальной электронной испытательной машине (AG-Xplus, SHIMADZU, Япония) для определения их механических свойств. В этом тесте начальный интервал крепления составлял 20 мм, а скорость растяжения - 1 мм / мин.
Оптические и смачивающие свойства
Коэффициент пропускания света различных мембран толщиной 25 мкм был определен от 350 до 800 нм с использованием спектрометра Ultrospec 2100 pro от Amersham Biosciences.
Для измерения угла смачивания использовали измеритель капель (Kyowa Interface Science Co., Ltd.). Анализ изображений проводился автоматически по форме капель 4 мкл дистиллированной воды, упавших на мембраны в течение ~ 0,5 с.
Результаты и обсуждение
Окисление и изоляция шелковых нановолокон
На рис. 1а представлена стратегия выделения нановолокон из материалов шелкового волокна. Сначала мы применили процесс предварительной обработки, чтобы разобрать эти шелковые волокна путем обработки муравьиной кислотой (не было химической реакции между аминокислотными или гидроксильными группами с муравьиной кислотой, как показано в спектрах комбинационного рассеяния в Дополнительном файле 1:Рис. S1 и соответствующем обсуждении Дополнительных файл). В ходе этой предварительной обработки шелковые волокна были разбиты на структуры из микроволокон шириной 5–20 мкм (рис. 1а). Затем гипохлорит натрия (NaClO) был использован для окисления / частичного растворения (разложения) разобранных шелковых волокон. Гидроксид натрия (NaOH) непрерывно добавляли в смесь для поддержания pH на уровне 10 в соответствии с условиями для TEMPO (2, 2, 6, 6-тетраметилпиперидин-1-оксирадикала) опосредованного окисления полисахаридов с использованием TEMPO. / NaClO / NaBr, тогда как в этом случае TEMPO и NaBr больше не нужны для окисления шелковых волокон из-за ограниченного количества реакционноспособных аминокислот в последовательностях фиброина шелка. Исходные шелковые волокна имели концентрацию карбоксильных групп ~ 0,3 мМ / г белка, что относилось к аспарагиновой и глутаминовой кислотам в молекулярной последовательности [27]. После этого содержание карбоксильных групп в окисленном шелке увеличивалось приблизительно линейно после добавления NaClO из-за окисления гидроксиметильных групп на остатках серина. Когда добавление NaClO достигло 20 мМ / г белка, конечная концентрация карбоксильных групп окисленного шелка составила 0,889 и 1,013 мМ / г белка для BS и AS, соответственно (рис. 1b, c). Однако избыточное количество NaClO могло разрушить шелковые волокна [28]. Например, нерастворимая в воде фракция BS и AS составляла 58,52 и 69,30 мас.% Соответственно при добавлении 20 мМ / г белка NaClO. Потеря веса нерастворимой в воде фракции после окисления свидетельствует о том, что добавление NaClO ≤ 10 мМ / г белка было приемлемым (осталось более 75% белка) в отношении ограниченного разложения во время окисления. Поэтому мы использовали 10 мМ NaClO на грамм белка для окисления волокон BS и AS, где содержание карбоксилатов составляет 0,724 и 0,837 мг / г белка для BS и AS соответственно.
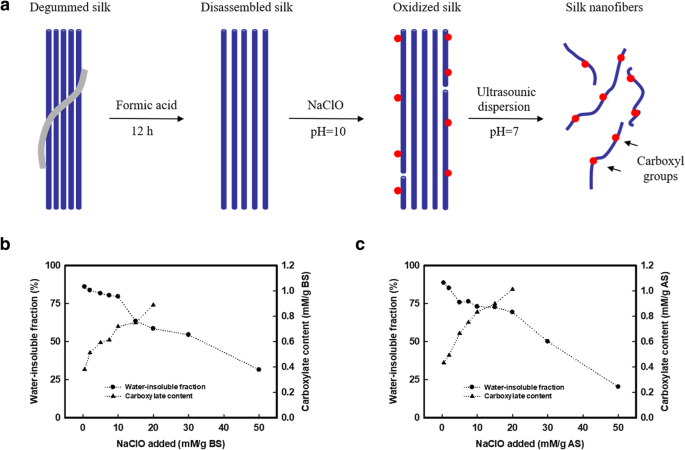
Схема процесса содержания СН и карбоксильных групп в BS и AS. а Схема окисления и диспергирования шелкового волокна до шелковых нановолокон (SN). б Содержание карбоксильных групп и масса, остающаяся нерастворимой в воде фракции после окисления Bombyx mori (BS) соответствует добавлению гипохлорита натрия (NaClO). Содержание карбоксила увеличивалось с 0,293 до 0,889 мМ / г BS (добавление NaClO составляло 20 мМ / г белка), при этом оставалось 58,52 мас.% Белка. c Для Antheraea pernyi шелк (AS). Содержание карбоксила увеличилось с 0,347 до 1,013 мМ / г AS (добавление NaClO составило 20 мМ / г белка), при этом осталось 69,30 мас.% Белка
Наконец, нановолокна были получены после обработки нерастворимой в воде фракции ультразвуковым гомогенизатором (рис. 2). Наблюдения с помощью сканирующей электронной микроскопии показали, что окисление разрыхляет шелк на микроуровне, образуя волокна диаметром несколько микрон, а обработка ультразвуком дополнительно диспергирует их в нановолокна диаметром 105 ± 27 нм (рис. 2c). По сравнению с другими процессами [24], которые в основном расслаивают поверхностный слой шелковых волокон, конечный выход ~ 50% в пересчете на оксидированные шелки был получен для нановолокон из-за электростатических сил отталкивания в окисленных шелках. Аналогичная стратегия была применена и к волокнам AS. Диаметр полученных нановолокон AS составил 112 ± 33 нм, а контурная длина - более 1 мкм (рис. 2е).
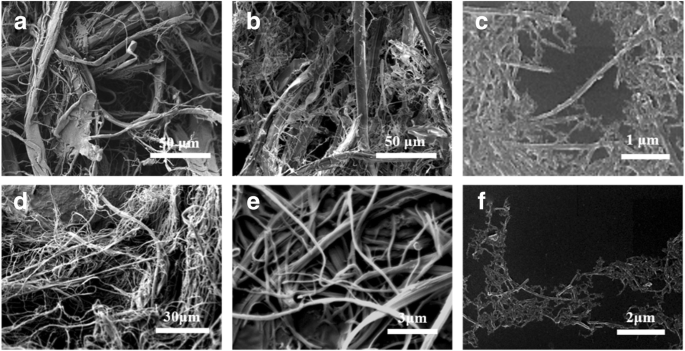
Репрезентативное СЭМ-наблюдение полученных шелковых волокон в каждом процессе. а Разобранные волокна BS после предварительной обработки муравьиной кислотой, b окисленные волокна BS и c нановолокна БС диаметром 105 ± 27 нм. г Разобранные волокна AS после предварительной обработки муравьиной кислотой, e окисленные волокна AS и f нановолокна АС диаметром 112-33 нм. Контурная длина нановолокон БС и АС более 1 мкм
Кристалличность шелковых волокон
Молекулы протеина шелка действовали как гидрофильные-гидрофобно-гидрофильные полимеры, которые складывались в мицеллы неправильного размера во время образования гидрофильных шариков (аморфных областей), выходящих из гидрофобных ядер (кристаллических областей) [17]. Сборка SN происходила за счет слипания внешних областей между мицеллами. Однако предполагается, что окисление шелковых волокон NaClO предполагает слабую адгезию между их наноструктурами [25]. Как показано на фиг. 3a и b, после окисления дифрактограммы рентгеновских лучей (XRD) окисленных волокон BS были подобны их исходной картине, а также картины XRD окисленных волокон AS. Таким образом, оксидированные шелковые волокна оставались их естественным нано-строительным блоком, то есть β-листовыми структурами в шелковых волокнах. С другой стороны, деконволюция этих рентгенограмм (рис. 3c, d) свидетельствует о значительном изменении кристалличности как в BS, так и в AS-волокнах после окисления, детали которого перечислены в таблице 1. Хотя окисление в основном происходило на остатках серина. белка шелка было несколько аминогрупп в аморфных областях, которые могли быть атакованы NaClO [29]. Следовательно, понятно, что кристалличность окисленных волокон BS в таблице 1 увеличилась с 24,8% (разобранный BS) до 41,3% (с добавлением 10 мМ / г белка NaClO), за которым последовало увеличение содержания карбоксильных групп. Аналогичная тенденция наблюдалась и в случае окисленных волокон AS, где кристалличность этих волокон AS была увеличена с 22,9 до 39,2%. Результаты предполагают, что, помимо сил электростатического отталкивания, разрушение аморфных областей в белках шелка также было важным фактором в диспергировании SN. Кристалличность окисленных шелковых волокон (как BS, так и AS) сопровождалась увеличением содержания карбоксильных групп, когда добавление NaClO составляло <10 мМ / г белка. Разложение аморфных областей предшествует кристаллизованным ядрам протеина шелка. Однако избыточное количество NaClO (20 мМ / г белка) может испортить шелк. Это явление хорошо согласуется с результатами, показанными на рис. 1b и c.
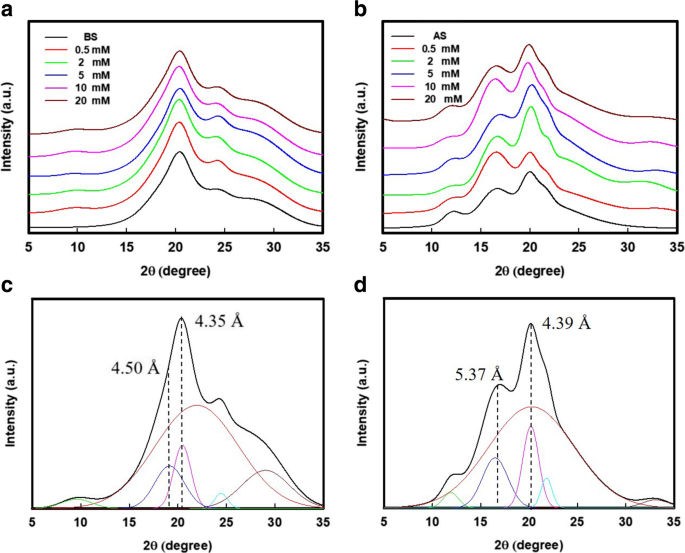
Рентгеноструктурный анализ окисленных волокон шелка. Картина дифракции рентгеновских лучей (XRD) a BS и b AS, который окислился при различных добавках NaClO. Репрезентативная деконволюция и результаты c BS и d Материалы AS
Характеристики шелковых нановолокон
Морфология окисленных нановолокон BS и AS, которые были получены ультразвуковой обработкой 10 мМ NaClO оксидированных шелковых волокон, показаны на рис. 4a и b. Нановолокна BS и AS имеют аналогичное соотношение сторон (рассчитанное программой ImageJ), где в среднем 16,92 для нановолокон BS и 19,12 для нановолокон AS, соответственно. Для сравнения, нановолокна целлюлозы (CN) и хитиновые нановолокна (ChN), полученные с использованием TEMPO-опосредованного окисления, показаны на фиг. 4c и d. Чтобы дополнительно охарактеризовать эти SN, были отлиты мембраны толщиной примерно 50 мкм с использованием метода испарения растворителя. Оптически прозрачные (пропускание более 75%) шелковые мембраны оценивали с помощью спектрофотометра UV-Vis (от 350 до 800 нм) (рис. 4e).
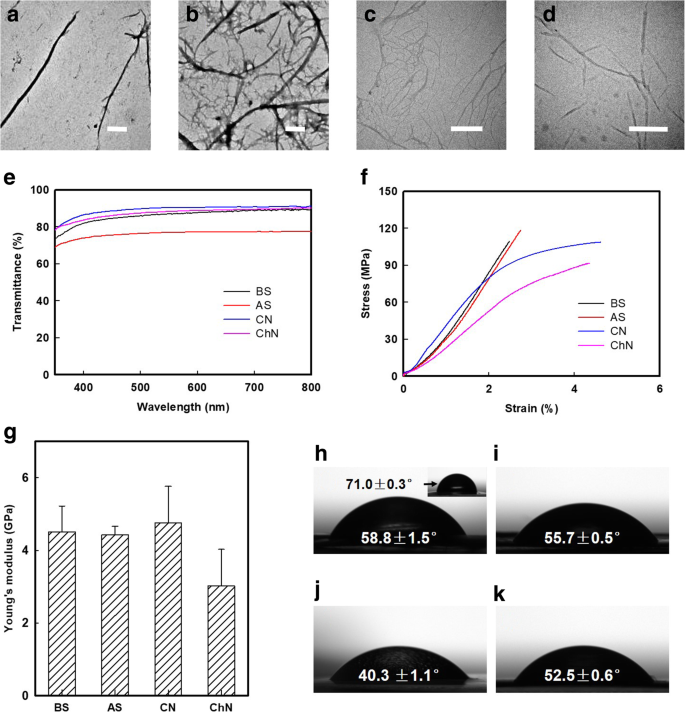
Исследование морфологии и свойств СН, ХН и ХН. Наблюдение с помощью просвечивающей электронной микроскопии (ПЭМ) полученного a BS и b Нановолокна AS, окисленные добавлением 10 мМ / г белка NaClO, c нановолокна целлюлозы (CN) и d хитиновые нановолокна (ХН), полученные за счет ТЕМПО-опосредованного окисления. Масштабная линейка составляет 500 нм. е Пропускание в УФ-видимой области для мембран толщиной примерно 50 мкм, отлитых из нановолокон BS, AS, целлюлозы (CN) и хитина (ChN). е Типичные кривые напряжение-деформация для мембран толщиной примерно 50 мкм, отлитых из нановолокон BS, AS, CN и ChN. г Модуль Юнга мембран, отлитых из нановолокон BS, AS, CN и ChN. Данные представляют собой среднее стандартное отклонение ( n =5). ч - к Краевой угол смачивания водой мембраны, отлитой f Нановолокна BS составляли 58,8 ± 1,5 °, что значительно меньше, чем у регенерированной мембраны BS (71,0 ± 0,3 °, изображение на вставке). Угол смачивания воды 55,7 ± 0,5, 40,3 ± 1,1 и 52,5 ± 0,6 ° был представлен в мембранах АС, ЦН и ЧН соответственно
Нановолокна, полученные с помощью этого метода уменьшения размера, сохранили высококристаллическую структуру и высокое соотношение сторон. В результате эти мембраны продемонстрировали надежные механические свойства (рис. 4g) с модулями Юнга 4,51 ± 0,71 и 4,43 ± 0,23 ГПа для BS и AS, соответственно, которые были сопоставимы с таковыми для мембран CN и ChN (типичная деформация и кривые напряжения приведены на рис. 4е). Кроме того, смачивающие свойства BS-мембраны были значительно улучшены в регенерированной мембране из-за введения карбоксильных групп. Как показано на фиг. 4h, краевой угол смачивания водой литейной мембраны из нановолокон BS составляет 58,8 ± 1,5 °, в то время как регенерированная мембрана из BS (изображение на вставке на фиг. 4h) составляет 71,0 ± 0,3 °. Кроме того, угол смачивания воды 55,7 ± 0,5, 40,3 ± 1,1 и 52,5 ± 0,6 ° был представлен в мембранах AS (рис. 4i), CN (рис. 4j) и ChN (рис. 4k) соответственно.
И CN, и ChN, и шелковые устройства широко применялись в материаловедении на протяжении десятилетий [13, 30, 31] из-за их одинаковой механической прочности, технологической пластичности, биохимических свойств и т. Д. Конечно, в этих полисахаридных и белковые материалы. Поэтому мы задались вопросом, как их различия регулируют формирование нановолокон. Правильно диспергированные дисперсии BS и AS имели дзета-потенциал -39,5 ± 0,66 и -37,4 ± 2,4 мВ, соответственно, в нейтральных условиях. Электростатическое отталкивание между карбоксильными группами препятствует адгезии между интерфейсами микро- / нано-фибрилл шелка; таким образом, эти нановолокна однородно диспергированы в водной фазе. Интересно, что при снижении pH H + экранировал отрицательно заряженные поверхности, ведущие к агрегации нановолокон, как показано на рис. 5a и b. Агрегаты SN можно повторно диспергировать в воде, регулируя pH> 7, или их можно легко собрать после центрифугирования и затем повторно диспергировать при легком перемешивании. На нижних диаграммах фиг. 5 показан оставшийся вес агрегатов SN, собранных при различных условиях pH. Для ДО 80,1 ± 1,7 и 90,9 ± 2,2 мас.% (85,7 ± 2,2 и 93,6 ± 1,5 мас.% Для СА) агрегатов было извлечено при pH 5 и 3 соответственно. Между тем, этот процесс концентрировал СН примерно в 100 раз (~ 20 мас.%) По сравнению с исходной дисперсией с концентрацией ~ 0,2 мас.%. Это удивительное свойство SN было приписано (i) собственному pH-отклику материалов на основе белка и (ii) гибкости SN мягкого вещества во время процессов агрегации и повторного диспергирования. Феномен агрегации-редисперсии предполагает многообещающее применение этих SN в качестве носителей для загрузки и высвобождения лекарств. Кроме того, не оспаривалось, что полученные SN хорошо подходят для хранения и транспортировки.
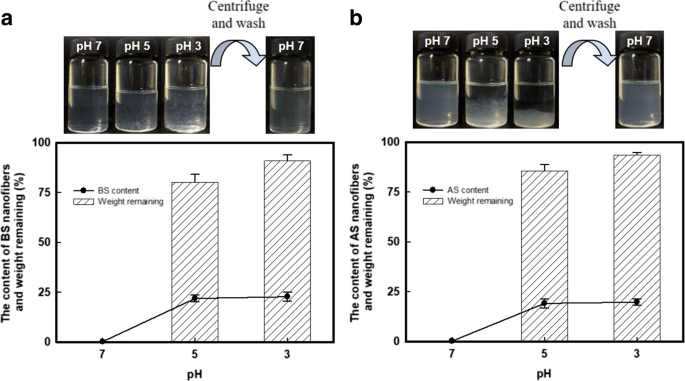
Процесс повторного диспергирования СН. Фотография явления реакции pH для a BS и b Нановолокна AS. После центрифугирования осталось более 80 мас.% Белков (как BS, так и AS) с содержанием белка ~ 20 мас.%
Выводы
Таким образом, индивидуальные диспергированные нановолокна BS и AS были получены после окисления NaClO. Подход был подобен ТЕМПО-опосредованному окислению полисахаридов для получения нановолокон; однако катализаторы TEMPO / NaBr не требовались. Свежеприготовленные СН имели диаметр ~ 110 нм и длину несколько микрон с отрицательно заряженными поверхностями. Оптически прозрачные, механически прочные и улучшенные смачивающие свойства были получены в мембранах SN. В частности, SN можно было сконцентрировать до ~ 20 мас.% За счет снижения pH, и эти подобные пульпе SN можно повторно диспергировать в нейтральных водных растворах. Основываясь на этих результатах, SN являются отличным кандидатом для материаловедения и биомедицины.
Доступность данных и материалов
Все данные, полученные или проанализированные в ходе этого исследования, включены в эту опубликованную статью.
Сокращения
- AS:
-
Antheraea pernyi шелк
- BS:
-
Bombyx mori шелк
- ChN:
-
Хитиновые нановолокна
- CN:
-
Нановолокно целлюлозы
- SEM:
-
Сканирующая электронная микроскопия
- SN:
-
Шелковое нановолокно
- ТЕМ:
-
Просвечивающая электронная микроскопия
- XRD:
-
Рентгеновская дифракция
Наноматериалы
- Industrie 4.0 и IIC Bury the Hatchet
- Плюсы и минусы литья под давлением
- Цепочка поставок и машинное обучение
- Буря - и цифровая сеть
- Оценка IoT и влияния 5G
- Неудобная, непредсказуемая и случайная сторона обслуживания
- Плюсы и минусы контракта на техническое обслуживание
- Возвращение Китая и кочевые источники:тенденции пандемии, которые сохранятся
- Изучение взаимосвязи EDM и аэрокосмической промышленности
- Разница между двигателями постоянного и переменного тока



