Обзор электрохимически самоорганизованных массивов нанотрубок титана:синтез, модификации и биомедицинские приложения
Аннотация
Нанотрубки из диоксида титана, выращенные путем анодного окисления, заинтриговали материаловедческое сообщество своими многочисленными уникальными и потенциальными свойствами, и синтез технологий приближается к своей зрелой стадии. Настоящий обзор посвящен TiO 2 . нанотрубки, выращенные путем самоорганизованного электрохимического анодирования из металлической подложки Ti, что критически подчеркивает синтез этого типа самоорганизованных слоев нанотрубок из диоксида титана и средства влияния на размер, форму, степень порядка и кристаллизованные фазы путем регулировки анодирования параметры и последующий термический отжиг. Взаимосвязь между размерами и свойствами анодного TiO 2 будут представлены массивы нанотрубок. Последние достижения и значимость исследований механизма образования анодного TiO 2 кратко обсуждаются нанотрубки. Кроме того, мы покажем наиболее многообещающие применения, о которых сообщалось в последнее время в биомедицинских направлениях, и модификации, осуществленные путем легирования, модификации поверхности и термического отжига для улучшения свойств анодно сформированного TiO 2 нанотрубки. Наконец, обозначены некоторые нерешенные вопросы и возможные будущие направления в этой области.
Введение
С начала ХХ века диоксид титана (TiO 2 ) был использован в качестве коммерческого производства в солнцезащитных средствах, красках, сенсорах, фотокатализе, солнечных элементах, электрохромных устройствах, доставке лекарств и т. д. [1,2,3,4,5,6,7]. Явление, что TiO 2 может производить фотогенерированные электронно-дырочные пары при освещении, может помочь расщепить воду на кислород и водород, что поможет решить энергетический кризис в будущем как наиболее потенциальное топливо. Фудзисима и его сотрудники впервые сообщили о фотокаталитическом расщеплении воды на TiO 2 электрод под воздействием ультрафиолетового (УФ) света [8,9,10], и с тех пор диоксид титана стал одним из наиболее изученных соединений в материаловедении. Среди всех оксидов переходных металлов он обладает широким спектром функциональных свойств, таких как химическая инертность, коррозионная стойкость и стабильность, особенно улучшение биосовместимости [11], а также электрических и оптических свойств [1]. С тех пор, как Иидзима обнаружил углеродные нанотрубки в 1991 году [12], продемонстрировав уникальное сочетание формы и функциональности, где на свойства может напрямую влиять геометрия, в области нанотехнологий были предприняты огромные усилия, в основном в химической, физической и биомедицинской областях. материаловедение.
Хотя наиболее изученным наноматериалом до сих пор остается углерод, другой класс нанотрубчатых материалов, которые обычно основаны на оксидах переходных металлов, привлекает значительный интерес за последние 20 лет. Первая попытка сформировать нанотрубки из анодированного диоксида титана была предпринята Ассефпур-Дезфули [13], который применил щелочную обработку перекисью водорода с последующим электрохимическим анодированием в электролите, содержащем хромовую кислоту. А поскольку Zwilling et al. сообщили, что они создали первые слои самоорганизующихся нанотрубок на подложке из Ti путем электрохимического анодирования в электролитах хромовой кислоты, содержащих ионы фтора, в 1999 г., область чрезвычайно быстро расширилась [14]. За последнее десятилетие было опубликовано более 33 800 статей с ключевым словом «нанотрубки диоксида титана». На Рисунке 1 показано общее количество публикаций с разбивкой по годам в области TiO 2 . нанотрубок и проводит сравнение различных методов синтеза в период 2002–2017 гг., которое не только демонстрирует тенденцию экспоненциального роста, но и очевидно указывает на то, что самоорганизованный анодный TiO 2 массивы нанотрубок привлекают большое внимание с большим потенциалом и преимуществами. В последнее время Ли и др. предоставил всесторонний и современный взгляд на область анодных нанотрубок диоксида титана, который охватил почти все аспекты, включая рост, модификации, свойства и приложения, с кратким описанием различных подходов к синтезу [15]. По сравнению с другими методами приготовления, такими как гидро / сольвотермические [16,17,18] и методы с использованием темплатов [19, 20], прямое окисление оказывается простым методом с высокой функциональностью, позволяющим получить желаемую контролируемую наноструктуру за счет регулирования размера, форма и степень порядка могут быть увеличены путем оптимизации параметров окисления, таких как приложенный потенциал, время, температура, pH и состав электролита [15]. Благодаря особой геометрии, слои самовыравнивающихся оксидных нанотрубок, которые имеют высокоорганизованную структуру и отношение поверхности к объему, обладают уникальными свойствами, такими как очень высокая механическая прочность и большая удельная площадь поверхности, даже обеспечивая электронные свойства, такие как высокий уровень электронов. скорость подвижности или эффекты квантового ограничения [15, 21]. Кроме того, электрохимическое анодирование является недорогим процессом и не ограничивается титаном, но также может подходить для других переходных металлов Hf [22], Zr [23], Nb [24], Ta [25], V [26] или сплавов. TiAl [27] и TiZr [28]. Настоящий обзор по-прежнему будет посвящен TiO 2 . нанотрубки, выращенные методом самоорганизованного электрохимического анодирования из металлической подложки Ti. Кроме того, мы сделаем упор на синтез этого типа самоорганизованных слоев нанотрубок диоксида титана и средствах влияния на размер, форму, степень упорядоченности и кристаллизованные фазы путем настройки параметров анодирования и последующего термического отжига, включая четыре различных поколения. отличающиеся от электролитов разновидностями и определенным двухэтапным анодированием и т. д. Соотношение между размерами и свойствами анодного TiO 2 будут представлены массивы нанотрубок. Последние достижения и значимость исследований механизма образования анодного TiO 2 кратко обсуждаются нанотрубки. Мы покажем наиболее многообещающие применения, о которых сообщалось в последнее время в биомедицинских направлениях, и модификации, осуществленные путем легирования, модификации поверхности и термического отжига для улучшения свойств анодно сформированного TiO 2 нанотрубки. Мы также рассматриваем нерешенные вопросы и возможные будущие направления в этой сфере. Текст основного абзаца следует прямо здесь.
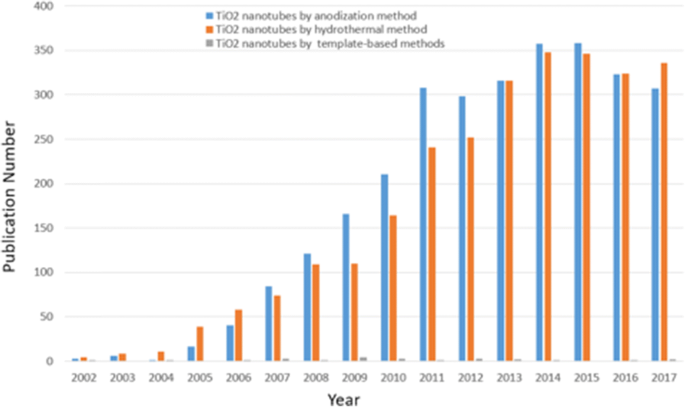
Направление исследований. Количество статей с разбивкой по годам, относящихся к TiO 2 нанотрубки, дифференцированные различными методами синтеза с 2002 по 2017 гг. (данные были собраны из индекса научного цитирования, расширенного с использованием нанотрубок из диоксида титана, анодирования, гидротермальных методов или методов на основе шаблонов в качестве ключевых слов)
Синтез TiO 2 Матрицы нанотрубок методом электрохимического анодирования
В последние годы, хотя многие различные формы наноструктурированного диоксида титана, включая наностержни, наночастицы, нанопроволоки и нанотрубки, были успешно разработаны [29,30,31], нанотрубки привлекают все больший интерес для технологических приложений из-за уникальной самоорганизующейся структуры с большая межфазная поверхность и удобное управление размером и формой, которые могут быть применены к приложениям, зависящим от площади поверхности, как лучший кандидат. Имеется ряд отличных обзоров [1, 2, 15, 32,33,34], посвященных характеристикам TiO 2 . наноматериалы, классифицированные с помощью различных синтетических методов. Доказано, что электрохимическое анодирование является одним из наиболее эффективных методов получения нанотрубок диоксида титана как относительно простой технологии, которую можно легко автоматизировать. Мы укажем основные методы изготовления анодного TiO 2 . нанотрубки внизу.
Самоорганизующийся анодный TiO 2 Массивы нанотрубок
Как было тщательно изучено, слои нанотрубок диоксида титана могут быть сформированы при определенных заданных условиях окружающей среды. Устройство окисления состоит из трех частей:(I) трехэлектродная система с подготовленной Ti-фольгой в качестве рабочего электрода, которая обезжиривается путем последовательной обработки ультразвуком в ацетоне, этаноле и деионизированной воде, платина в качестве противоэлектрода и обычно Ag / AgCl. в качестве электрода сравнения (рис. 2a), а pH-электрод иногда добавляют для получения предельной концентрации F - и HF [35] или другая простая двухэлектродная система, состоящая из фольги Ti в качестве анода и инертного металлического электрода в качестве катода (рис. 2b) [36]; (II) обычно фторид-ион, хлорид-ион, хром-ион, бромид-ион или перхлорат, содержащие электролиты; и (III) источник питания постоянного тока. Существуют две основные особенности, на которые влияют условия образования анодирования, влияющие на перспективные применения нанотрубок диоксида титана:(I) геометрия:размер, форма, степень упорядоченности, кристаллизованные фазы и т. Д. И (II) свойства в химических, физических и химических свойствах. биомедицинский. Другими словами, посредством управления параметрами электрохимического анодирования (приложенный потенциал, продолжительность анодирования, система электролита, включая концентрацию ионов фтора и воды в электролите, температуру электролита, pH электролита и т. Д., Которые будут обсуждаться более подробно. в разделе «Синтез массивов нанотрубок TiO2 методом электрохимического анодирования») можно изготавливать различные наноструктуры диоксида титана, такие как плоский компактный оксид [1], пористый слой [1, 36], неупорядоченный TiO 2 слои нанотрубок, растущие в пучки [37], или, наконец, высокоорганизованный регулярный TiO 2 нанотрубки или усовершенствованный нанотрубчатый слой:разветвленная трубка [38], подобная бамбуку [38, 39], двустенная [40], нанолучная [38] или двухслойная [39] структуры, в которых свойства могут быть обнаружены по-разному. На рисунках 3 и 4 показаны изображения типичных примеров такого TiO 2 , полученные с помощью автоэмиссионной сканирующей электронной микроскопии (FE-SEM). морфологии нанотрубок.
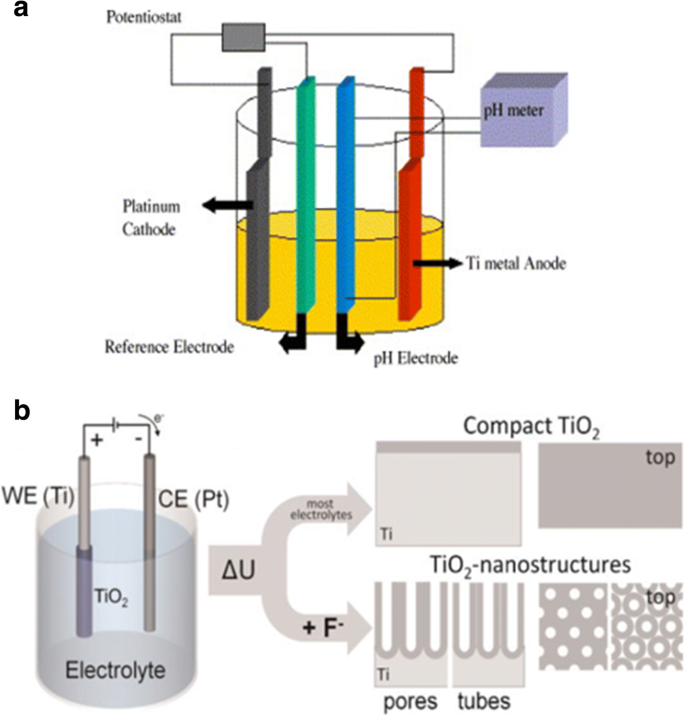
Схема настройки. а Иллюстративный чертеж трехэлектродной системы с подготовленной Ti-фольгой в качестве рабочих электродов, платиной в качестве противоэлектрода и, как правило, Ag / AgCl в качестве электрода сравнения, а рН-электрод в качестве рН-метра. Воспроизведено из исх. [35]. б Иллюстративный чертеж простой двухэлектродной системы, состоящей из Ti-фольги в качестве анода и инертного металлического электрода в качестве катода. Анодирование приводит к получению разного анодированного оксидного слоя в разных условиях. В большинстве нейтральных и кислых электролитов может образовываться плотный диоксид титана. Но если используются разбавленные фторидные электролиты, нанотрубчатые / нанопористые оксидные слои будут непосредственно прикрепляться к поверхности металла. Воспроизведено из исх. [36]

СЭМ изображения анодированного TiO 2 слои нанотрубок различными процессами анодирования Ti. а Высокоупорядоченный TiO 2 нанотрубки (на виде сверху и сбоку) получаются в системах с органическими электролитами с самоупорядоченными поверхностными ямками (справа), которые фактически являются металлическими поверхностями при удалении слоев трубки. Воспроизведено из исх. [1]. б Неупорядоченный TiO 2 нанотрубки выращиваются участками на поверхности и сплавлены вместе в пучки в хлоридсодержащем электролите с помощью метода сверхбыстрого анодирования, известного как анодирование с быстрым пробоем (RBA). Воспроизведено из исх. [1] и [37]

СЭМ-изображения усовершенствованного TiO 2 морфологии нанотрубок. а Армированный бамбуком TiO 2 нанотрубки производятся в определенных условиях переменного напряжения (AV) в этиленгликоле, состоящем из 0,2 моль / л HF, с последовательностью 1 мин при 120 В и 5 мин при 40 В. Воспроизведено из исх. [38]. б Переход от гладкого к бамбуковому TiO 2 нанотрубки могут быть индуцированы анодированием с контролируемым добавлением воды (содержание воды:от 1 до 8%) в 0,135 M NH 4 Электролит F / этиленгликоль
воспроизведено из исх. [39]. c Структуры 2D-нанолазов получаются при циклическом изменении напряжения, проводимом в течение продолжительного периода времени во фторидсодержащем электролите, с последовательностью 50 с при 120 В и 600 с при 0 В. Воспроизведено из исх. [38]. г Двустенный TiO 2 нанотрубки выращиваются путем анодирования Ti во фторидсодержащем этиленгликолевом электролите при 120 В после отжига при 500 ° C со скоростью нагрева 1 ° C с -1 . Воспроизведено из исх. [40]. е Разветвленные нанотрубки можно наблюдать путем ступенчатого изменения напряжения, сначала при 120 В (6 ч), а затем при 40 В (2 ч). Воспроизведено из исх. [38]. е Видны двухслойные нанотрубки с одинаковым или двумя разными диаметрами трубок. Воспроизведено из исх. [38]
(В настоящее время TiO 2 Могут быть получены массивы нанотрубок с диаметром трубок от 10 до 500 нм, толщиной слоев от нескольких сотен нанометров до 1000 мкм и толщиной стенок от 2 до 80 нм [15, 41].)
Это было два десятилетия назад, когда Масуда и Фукуда впервые сообщили о высокоупорядоченном пористом оксиде алюминия, установив оптимальные условия анодирования [42]. Позже исследователи потратили свои усилия на создание аналогичных структур и для TiO 2 . слои нанотрубок. И есть три решающих фактора, влияющих на степень порядка в анодном TiO 2 массивы нанотрубок (в соответствии с полигонами в слоях и стандартным отклонением диаметра трубки):Ti-подложка, приложенное напряжение и повторяющееся анодирование [33, 43]. Очевидно, что меньше дефектов в устройстве может быть получено для материала высокой чистоты при максимально возможном напряжении ниже диэлектрического пробоя [33] и идеально гексагональном самоупорядоченном TiO 2 нанотрубки, как показано на рис. 5, могут быть значительно улучшены путем роста вторичных трубок [43]. Sopha et al. показали, что примеси сильно влияют на результирующие различные размеры и порядок нанотрубок после второго анодирования [44]. Более того, кристаллографическая ориентация зерен подложки Ti оказалась решающим фактором в характеристиках роста TiO 2 . массивы нанотрубок методом дифракции обратного рассеяния электронов (EBSD). Леонарди и др. обнаружили, что нанотрубки можно наблюдать только с ориентацией, которая позволяет оксиду вентильного металла образовываться на зернах, обеспечивая проникновение ионов фтора через окислительную пленку, где 1 M (NH 4 ) H 2 ЗП 3 +0,5 мас.% NH 4 F использовались в качестве электролита [45]. Точно так же Макак и соавторы сообщили, что рост нанотрубок на зернах не замедляется в широко используемом электролите на основе этиленгликоля по сравнению со случаем использования водного электролита, как известно из последней литературы [46]. На полированном листе Ti зерна с ориентацией [0 0 0 1] или близкой к ней оказались идеальными зернами, и использование монокристаллического Ti с идеальной ориентацией было бы большим шагом вперед для получения наиболее однородных массивов нанотрубок [46] .

СЭМ изображения TiO 2 нанотрубки. Нанотрубки образуются в этиленгликолевых электролитах, содержащих 0,27 М NH 4 . F путем многократного анодирования Ti. Поперечные сечения берутся вверху слоя, в середине и внизу слоя. Воспроизведено из исх. [43]
Тем не менее, некоторые недочеты, влияющие на порядок, все же есть. В последнее время он был расширен за счет равномерного наноимпринтинга Ti. Кондо и др. разобрался в производственном производстве идеально упорядоченного анодного TiO 2 путем наноимпринтинга поверхности Ti или двухслойного образца со слоем Al наверху и слоем Ti внизу с использованием никелевой формы с упорядоченными выпуклостями. И TiO 2 слои могут быть сгенерированы более упорядоченным образом, если неглубокие впадины предварительно текстурированного рисунка действовали как места инициирования путем последующего анодирования в NH 4 Раствор этиленгликоля F [47, 48]. Следуя внимательно, Sopha et al. сначала покрыл TiN-защитный слой на Ti-подложке, подготовленный осаждением атомных слоев (ALD), перед предварительным текстурированием, выполняемым сфокусированным ионным пучком (FIB), и последующим анодированием с использованием этиленгликоль-электролита для получения идеально расположенных гексагонально слоев нанотрубок с толщиной 2 мкм, что может ограничить рост нанотрубок только на заданных участках инициирования и продлить время анодирования без каких-либо дефектов [49].
Механизм образования анодного TiO 2 Нанотрубки
Технология анодного окисления и исследования механизма образования анодного TiO 2 нанотрубки уже давно привлекают к себе внимание самых разных дисциплин. Исследование механизма, о котором Диггл сообщил в 1969 году о пленках из компактного анодного оксида и пористого анодного оксида [50], теперь все еще играет чрезвычайно важную направляющую роль. Значительное количество последних работ показывает, что переход от пор к трубкам носит постепенный характер [1, 27, 36]; однако полностью теоретическая модель и рассуждения не приводились.
Традиционное растворение с помощью поля (FAD) является наиболее приемлемой теорией [1, 33, 51]. То есть в процессе электрохимического анодирования TiO 2 Массивы нанотрубок образуются в результате самоорганизации диоксида титана в результате трех относительно независимых процедур:электрохимического окисления Ti до TiO 2 , индуцированное электрическим полем растворение TiO 2 , и индуцированное ионами фтора химическое растворение TiO 2 , достигая хрупкого баланса. В качестве характеристической кривой зависимости тока от времени, показанной на рис. 6 для электролитов, содержащих фторид, которые приводят к образованию нанотрубок [51], и типичного изображения, которое может помочь схематично проиллюстрировать процесс образования [33], показанного на рис. 7, переходный процесс можно разделить на три отдельных этапа:(I) В первой части происходит спад тока, вызванный вновь образованным барьерным оксидом, когда два основных процесса, миграция внутрь O 2- ионы к границе раздела металл / оксид и миграция Ti 4+ наружу по направлению к поверхности раздела оксид / электролит, достигается баланс. (II) Во второй части ток снова начинает расти с запаздыванием по времени, вызванным увеличением площади поверхности анода. Чем короче задержка, тем выше будет концентрация фторида из-за индуцированного фторидом растворения образовавшегося TiO 2 , и поры начинают формироваться беспорядочно, что впоследствии оказывается первоначальным образованием TiO 2 нанотрубки. (III) Затем ток достигает установившегося состояния, когда скорость роста пор на границе раздела оксидов металла и индуцированная скорость растворения образовавшегося TiO 2 на внешней границе раздела достигают состояния равновесия. Таким образом, конечные трубы приобретают все более v-образную форму, то есть верхние части трубок имеют значительно более тонкие стенки, чем их днища, где трубы закрыты. Градиент толщины стенки трубки на рис. 5 может быть объяснен разным временем воздействия и концентрацией электролитов вдоль трубок [43].
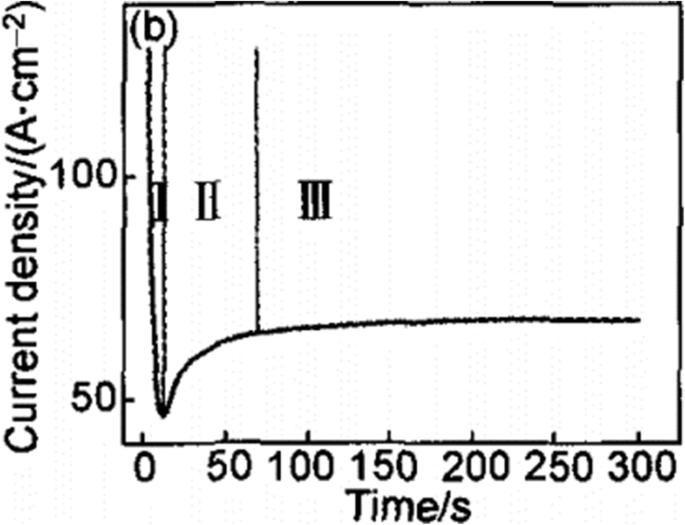
Типичная кривая зависимости тока от времени при постоянном напряжении в электролитах, содержащих фторид. Переходный процесс можно разделить на три отдельные области ( I - III ). ( Я ) В первой части наблюдается резкое спадание тока. ( II ) Во второй части ток снова начинает расти с запаздыванием. ( III ) В третьей части ток достигает установившегося состояния, воспроизведенного из исх. [51]
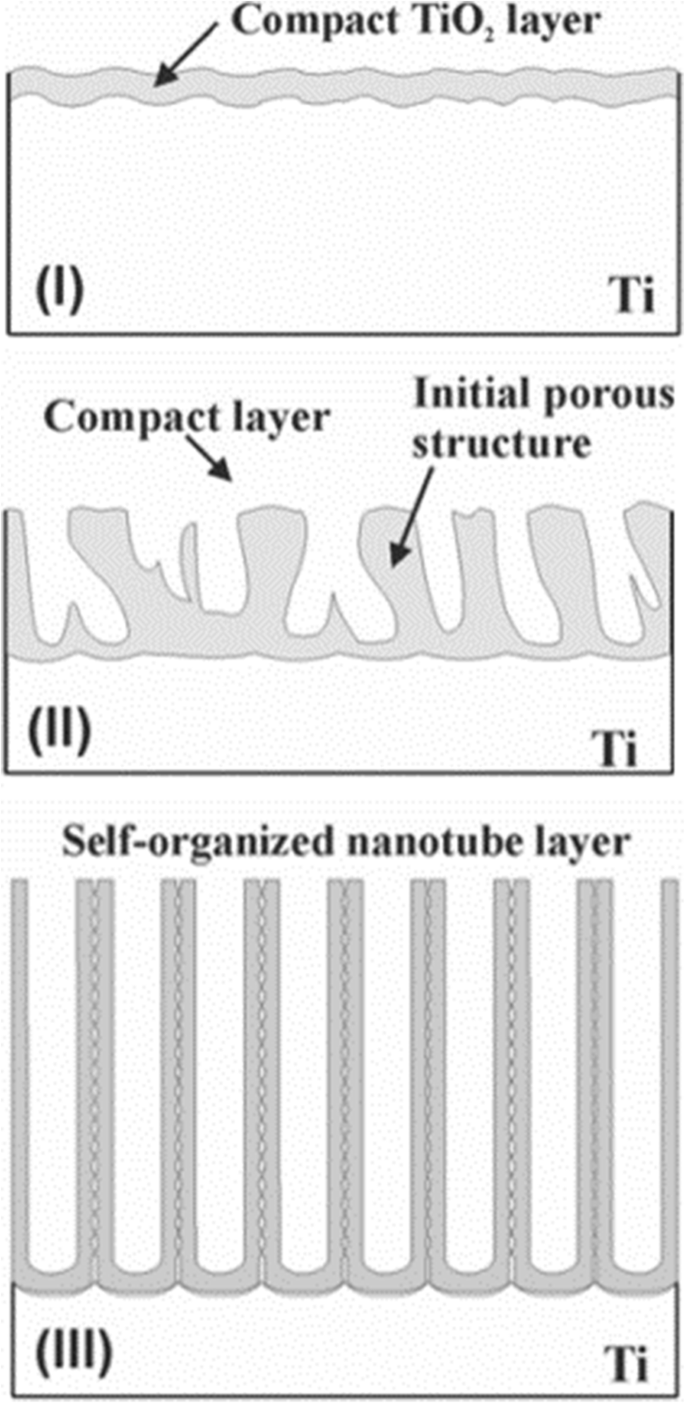
Процесс формирования TiO 2 массивы нанотрубок. Образование TiO 2 Массивы нанотрубок можно разделить на три различных морфологических этапа ( I - III ). ( Я ) Образуется барьерный оксид. ( II ) Поверхность активируется локально, и поры начинают беспорядочно расти. ( III ) Формируется самоорганизованный слой нанотрубок, воспроизведенный из исх. [33]
Однако эта теория не может объяснить явление разделения на трубки в отличие от нанопористой структуры, и Fahim et al. наблюдали, что при соответствующих напряжениях можно получить нанотрубки диоксида титана в растворе серной кислоты без ионов фтора, и в этом случае кривая I-t напоминала ту, которую мы только что обсуждали выше [52]. Как указали Хаузер и Хеберт, механизм роста еще не разработан, чтобы объяснить количественные отношения между процессом образования пористой мембраны из диоксида титана и кривой I-t [53]. Поскольку интерпретация недостаточно убедительна, в последнее время появились новые сведения о механизме, такие как модель вязкого течения и модель роста двух течений. Что касается этих механизмов, обзор [51] показывает множество ограничений для традиционной теории растворения с помощью поля и дает некоторые объяснения последних достижений и значимости исследований модели вязкого течения и модели роста двух течений.
Влияние условий анодирования, влияющих на геометрию и свойства
Состав и концентрация электролитов имеют существенное влияние на формирование массивов нанотрубок. В соответствии с различием используемых электролитов, разработка в основном делится на три этапа:в таблице 1 приведены условия анодирования и размеры полученного TiO 2 Массивы нанотрубок трех поколений исследованы различными исследовательскими группами на сегодняшний день.
Первое поколение:водные электролиты на основе плавиковой кислоты (HF)
Важной вехой является то, что Gong et al. впервые представлены однородные массивы нанотрубок диоксида титана путем анодного окисления Ti в водных электролитах на основе HF [54]. В электролитах водного раствора HF, где pH относительно низкий, что означает высокую концентрацию ионов водорода, химическое растворение TiO 2 индуцированная ионами фтора играет доминирующую роль в процессе анодирования [55]. Динамическое равновесие было достигнуто за короткий период времени в процессе формирования нанотрубок диоксида титана, и поэтому максимально достижимая длина нанотрубок была ограничена примерно 0,5 мкм [54,55,56].
Второе поколение:буферные электролиты
В последующей работе, чтобы уменьшить химическое растворение, удлинение трубок Cai et al. продемонстрировали, что путем добавления более слабых кислот, таких как KF или NaF, в буферный раствор и доведения pH до слабокислого (pH =4,5) с помощью серной кислоты или гидроксида натрия, были получены нанотрубки длиной примерно 4,4 мкм [57]. Значение pH влияет на гидролиз ионов титана, которые, как оказывается, препятствуют электрохимическому травлению и химическому растворению. Cai et al. также указал, что более низкие значения pH приводят к более коротким, но чистым нанотрубкам, а более высокие значения pH приводят к более длинным нанотрубкам, но нежелательным осколкам [57]. По мере увеличения значения pH скорость гидролиза будет увеличиваться, что, в свою очередь, замедлит химическое растворение, что приведет к получению более длинных нанотрубок, в то время как щелочной раствор не подходит для роста нанотрубок [57, 58]. Макак и др. Продемонстрировали, что в нейтральном электролите NaF при соответствующем напряжении могут быть получены нанотрубки гораздо большей длины, чем в кислых растворах. [58]. При определенном напряжении во фторидсодержащем электролите, регулируя градиент pH, можно достичь требуемых пропорций и толщины слоев [59].
Третье поколение:полярные органические электролиты
Электролиты, такие как глицерин [59], диметилсульфоксид [60], формамид или диэтиленгликоль [61, 62], этиленгликоль [41, 63], содержащие фторидные соединения, такие как NH 4 Постепенно появляются F, NaF и KF. Макак и соавторы взяли на себя ведущую роль в использовании вязкого глицеринового электролита для изготовления массивов нанотрубок из диоксида титана толщиной примерно 7 мкм и средним диаметром трубок 40 нм [59]. Показано, что более высокое соотношение сторон TiO 2 нанотрубки можно выращивать в таком полярном органическом электролите благодаря надлежащему контролю pH электролита, уменьшающему химическое растворение диоксида титана [64]. Paulose et al. сформированные нанотрубки длиной приблизительно 134 мкм, полученные с использованием этиленгликоля, содержащего 0,25 мас.% NH 4 F при потенциале анодирования 60 В в течение 17 ч [60]. Вскоре после этого TiO 2 толщиной более 250 мкм О массивах нанотрубок сообщил Альбу [65]. Кроме того, содержание воды в этом процессе играет двоякую роль:оно необходимо для образования диоксида титана, но также ускоряет химическое растворение [63]. Следовательно, как уменьшить влияние содержания воды до минимального значения требуется для увеличения толщины и степени упорядоченности TiO 2 массивы нанотрубок. В общем, ограничение содержания воды менее 5% является ключом к успешному получению очень длинных нанотрубок [60], а для образования хорошо организованных нанотрубок диоксида титана требуется минимальное количество воды (0,18 мас.%) [66]. Сообщалось, что с добавлением воды зарегистрированная плотность тока уменьшалась, что было самым высоким в безводном растворе этиленгликоля [66]. Paulose et al. первое сообщение о формировании самоорганизующихся массивов гексагональных нанотрубок из диоксида титана длиной примерно 1000 мкм при 60 В в течение 216 часов в этиленгликоле, содержащем 0,6 мас.% NH 4 F и 3,5% воды [41]. Другим заметным явлением является то, что гладкие стенки трубок растут при низком содержании воды, в то время как рябь на боковых стенках формируется при более высоком содержании, как показано на рис. 4b [59, 67]. Являясь наиболее часто используемым типом электролитов, этиленгликоль, содержащий воду и фторид-ионы, всегда приводит к структурам нанотрубок с двойными стенками (рис. 4d) [40, 68,69,70], в то время как внутренний слой может быть удален с помощью подходящая обработка отжигом с последующим простым процессом химического травления. После удаления внутренней оболочки расширенные трубки позволяют послойно декорировать наночастицами с использованием повторяющегося подхода на основе TiCl 4 -гидролиз [71]. В то время как одностенные трубки показали значительно увеличенную проводимость и время переноса электронов в сенсибилизированных красителями солнечных элементах (DSSC) [71, 72], где толщина всей трубки в основном такая же, а внутренняя оболочка больше не появляется, Mirabolghasemi et al. провели сравнение двух- и одностенных трубок и представили желаемые одностенные трубки с добавлением диметилсульфоксида (ДМСО) в электролиты с 1,5 М H 2 O и 0,1 М NH 4 F [72].
Недавно сообщалось, что электролиты на нефторидной основе увеличивают содержание TiO 2 . массивы нанотрубок, которые можно рассматривать как четвертое поколение синтеза, включая соляную кислоту, перекись водорода, растворы хлорной кислоты и их смеси [73, 74]. Аллама и Граймс описали хорошо разработанные массивы нанотрубок длиной 300 нм, внутренним диаметром 15 нм и внешним диаметром 25 нм, которые были получены в 3 М водном электролите соляной кислоты (HCl) при напряжении окисления от 10 до 13 В. Но добавление H 3 в низкой концентрации ЗП 4 привело к переходу от нанотрубок к стержням. Они также предположили, что им не удалось получить массивы самоорганизованных нанотрубок в HCl-содержащих электролитах при концентрации ниже или выше 3 M [73]. Аллама обнаружил, что добавление перекиси водорода к водному раствору, содержащему соляную кислоту, может быть одним из возможных методов удлинения нанотрубок диоксида титана, которые обладают сильным окислительным свойством после более толстого оксидного слоя, демонстрируя, что фторид-ионы могут успешно заменяться хлорид-ионами в процессе роста. массивов нанотрубок [74]. Кроме того, в последние годы ионные жидкости без добавления свободных фторидных частиц рассматриваются как еще один тип системы растворителей для нанотрубок из диоксида титана [75, 76].
Помимо стандартных параметров, геометрия полученных нанотрубок зависит от многократного использования электролита («эффект использованного раствора»). По сравнению с трубками, полученными из свежих растворов, с использованием однажды использованных растворов, наблюдается увеличение длины нанотрубок и лучшее качество, при этом достигаемая скорость роста нанотрубок постоянно выше для однократно используемых растворов при 60 В и выше [77] и можно отметить несколько иное, но различимое переходное поведение тока [66]. Более того, в дважды используемом растворе не была получена нанотрубчатая структура, а образовалась оксидная пленка из-за обеднения F - виды [78]. Однако Sopha et al. исследовали различный возраст электролитов на основе этиленгликоля по морфологии TiO 2 нанотрубки, показывающие, что в старых электролитах массивы имеют более низкое соотношение сторон [79].
Прикладной потенциал
Напряжение анодирования является критическим фактором, определяющим диаметр трубок [80, 81]. Размер массивов нанотрубок можно предсказать, просто приложив подходящий диапазон напряжения, называемый потенциальным окном, поперек электрода [67]. При низком напряжении происходит меньшее растворение электрического поля, образуя TiO 2 . нанотрубки меньшего диаметра. Если напряжение слишком низкое, TiO 2 слой становится компактным, но нанотрубчатой структуры не наблюдается. Напротив, при слишком высоком напряжении будет видна губчатая пористая структура. При контролируемом напряжении диаметр нанотрубок пропорционален напряжению [81]. Furthermore, studies show that the range of voltage forming nanotubes is also related to the electrolyte system. In aqueous electrolytes, the potential window should be controlled from 10 to 25 V, which in organic electrolytes is much wider between several volts and some hundred volts. Wang and Lin found out the fact that in aqueous electrolytes, the anodization potential exhibits significant influence on the growth of TiO2 nanotube arrays, which exhibited slight influence in non-aqueous electrolytes in this regard [82]. The voltage dependence has a significant reduction in non-aqueous electrolytes which is attributed to a large extent to the low conductivity of organic electrolytes [83, 84].
The Duration on Anodization
The duration of anodization affects the nanotubes mainly in two aspects:(I) the formation of the tubes or not and (II) the length of the tubes. That is, in the early stage of the anodization, a compact TiO2 film is formed. If the duration is too short to reach an equilibrium in reaction, the regular nanotube array cannot be achieved instead of a disordered porous layer [67]. With increasing the anodization time, porous structure gradually grows deeper and converts into the TiO2 nanotubular array [1, 33, 51]. If other electrochemical parameters are kept unchanged, increase in the nanotube length is observed over time while no significant effect on diameter and tube wall thickness until a steady-state situation occurs [67, 85, 86]. However, due to the decrease of the F − concentration in the electrolyte, where the ion transport rate decreased, the growth rate of nanotubes is reduced. After reaching a stable condition between tube growth at the bottom and chemical/electrochemical dissolution at the top, we will find no further increase in length of the nanotubes [87]. As time continues to go, pipe orifice becomes an irregular polygon resulting in TiO2 spikes and coverings which can be seen on the surface of the TiO2 nanotube arrays [36]. It is worth mentioning that enlightened by the success of aluminum-repeated anodization for self-organized porous alumina [88], the two-step anodization of titanium for such a highly ordered hexagonally packed nanostructure of titania has appeared [43, 77, 89,90,91]. After the first-step anodization, the first nanotube layer from the Ti foil should be removed ultrasonically or by using an adhesion tape which leads to a surface where the remaining Ti is covered by comparably ordered dimples. Researches have shown that the former treatment helps to avoid potential mechanical damage to the Ti surface and also improve the structural uniformity of the TiO2 nanotubes to a great extent [77, 90, 91]. In the second anodization step, the pretreated Ti foil would be used as anode again with or without changes in parameters of oxidation conditions. It is subsequently found that the highly ordered and vertically oriented titania nanotubes, have greater potential in such fields as photocatalysis [77], photoelectriochemical activity [92, 93], and biological interaction with cells [94] than the disordered nanotubular titania.
Electrolyte Temperature
Temperature restricts the growth and quality of titania nanotube arrays, directly affecting the rate of oxide growth, length, and wall thickness of the structure [64, 95]. Wang and Lin first reported the effect of electrolyte temperature in both aqueous and non-aqueous electrolyte on anodic oxidation of titanium [82]. In aqueous electrolyte, with the temperature increasing, a slight diminish in the internal diameters was observed while the external diameters remained the same [68]. The reason may be the dissolution induced by electrical field and fluoride ions are similar while the oxide formation rate is higher than that at lower temperature. In non-aqueous electrolyte containing fluoride ions, the outer nanotube diameter was found to be largely increased by the increasing electrolyte temperature [82]. This may be because at lower temperature, the ion mobility of fluorine in some viscous electrolyte is further inhibited, leading to much slower dissolution of newly formed titania, which subsequently lead to a smaller nanotube diameter. As chemical dissolution rate increases, surface of TiO2 nanotubes arrays can easily produce excessive corrosion, resulting in lodging nanotubes and agglomeration. Therefore, the appropriate bath temperature for stable TiO2 nanotube arrays is at room temperature [82, 95, 96].
Modification of Nanotubes Properties
Increasing applications of TiO2 nanotubes as a novel semiconductor are closely related to its photoelectriochemical (PEC) performance; however, they are sometimes prevented by two fundamental drawbacks:(I) the wide band gap (3.0 eV for the rutile phase and 3.2 eV for the anatase phase) can only absorb ultraviolet light, which accounts for less than 10% of the sunlight [97], resulting in low average utilization ratio of solar energy and (II) the low electrical conductivity cannot efficiently transfer photogenerated carries. At the same time, the photoelectrons and vacancies can be easily recombined, thus making low electron mobility rate or quantum confinement effects [98]. Hence, post-treatment of TiO2 nanotubes is the key to improve the performance of its materials and related devices successfully. Considerable researches have been reported on modified methods to reduce the recombination of photogenerated electron-hole pair rate, speed up the electron transfer rate, and enhance the photoelectriochemical activity of TiO2 nanotubes. The research of the methods for the improvement of the photoelectriochemical properties of TiO2 nanotubes will be reviewed, including thermal annealing, doping, and surface modification. As for promising modification in biomedical fields, we will present in the application section.
Thermal Annealing
The crystallinity of the nanotube arrays and their conductivity, lifetime of charge carrier, and photoresponse depend mainly on the thermal annealing temperature and atmosphere [99, 100]. The as-prepared TiO2 nanotubes above are amorphous in nature but can be annealed to anatase or rutile phase, or mixtures of both phases relying on the specific temperature [1, 3, 40, 92, 100]. It is demonstrated that amorphous nanotube layers grown in a glycerol-based electrolyte containing fluoride ions have low photocurrents and an incident photon-to-electron conversion efficiency (IPCE) below 5% due to lots of structural defects while anatase phase nanotubes exhibit an IPCE value up to 60% thus attracting more interest to applications such as dye-sensitized or perovskite solar cells [93]. As well in mixed water-glycerol electrolyte with F − , Das et al. stated their points that if the self-organized TiO2 nanotube arrays with thickness about 1 μm were annealed around 300–500 °C, the anatase phase of TiO2 as the most preferred crystalline structure could be observed. The single anatase structure of nanotubes with the best photoelectriochemical properties and the lowest resistivity could be fabricated when annealed at 400 °C. At temperature higher than 600 °C, a track of typical rutile appeared and with a further increase in annealing temperature the percentage and quality of the rutile phase increased [92]. It should be noted that in Jaroenworaluc’s work, rutile phase was detected in anodic nanotube layers grown in aqueous NaF/Na2 SO 4 with thickness of approximately 1.5 μm at 500 °C heat treatment and became the dominant phase at 600 °C. Whereas at 550 °C, partial nanotubes began to break down [101]. It begins to cause the collapse of the entire nanostructure formed in aqueous NaF/Na2 SO 4 with the continuous increase of temperature (800–900 °C) or the extended annealing time [3]. While for extended temperature, the crystalline structure of the nanotubes completely converts to rutile phase at above 900 °C [3]. Some researchers demonstrated a loss of the typical single-walled nanotube layers morphology when the annealed temperature rose above 580 °C [102]. Besides the whole annealing process especially the heating rate controls, the morphological structures of the entire nanotube arrays [40]. The double-walled nanotube layers prepared from ethylene glycol (containing less than 0.2 wt% H2 O), with the addition of HF and H2 О 2 , have such a high stability that can keep their structure intact until temperature is higher than 900 °C with a heating rate of 1 °C s −1 . However, the double-walled nanotubes begin to collapse as soon as the temperature reaches 500 °C when the heating rate is 25 °C s −1 . Most extraordinarily, with the high speed of 50 °C s −1 the entire separated nanotubes fuse into a highly ordered porous membrane [40]. Xiao et al. obtained crystallized titania nanotubes arrays with calcination in different gases like dry nitrogen, air, and argon indicating nanotubes in dry nitrogen appeared to have enhanced electrochemical and photoelectrical properties who also found out that with the increasing temperature internal diameter decreased while wall thickness increased at the expense of nanotubes length [103].
As shown in Fig. 8, the conductivity along the TiO2 nanotubes with three different thickness is strongly affected by annealing temperature. Smallest resistance is observed at about 350–450 °C when the amorphous nanotube arrays are totally converted into anatase layers [99]. And it is evident to see that specific resistivity increases with thicker nanotube arrays which can be shown more clearly in the inset in Fig. 8. Furthermore, calcination temperature is responsible for the decrease in the length of the anatase TiO2 nanotubes. As shown in Fig. 9a, increment of temperature between 300 and 500 °C causes the as-prepared nanotube arrays slightly changing in thickness from 13.6 to 12.6 μm. When annealing temperature continuously increases to 600 °C, the average length of the nanotubes decrease dramatically to 6.6 μm. Figure 9b shows conversion from anatase TiO2 to rutile phase TiO2 occuring at 500 °C when the rutile barrier layer is formed on the bottom of the TiO2 nanotube arrays along the anatase nanotubes by consuming the bottom layer if the annealed temperature is further increased. This leads to a length decrease and corresponding photocatalytic activity decline [104].
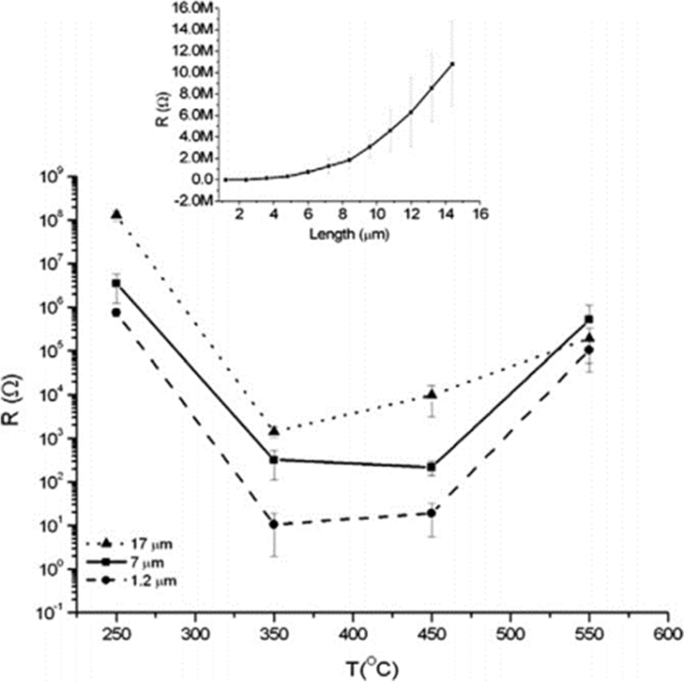
Electrical resistance as a function of the annealing temperature for the different nanotube layer thicknesses. The curve shows electrical resistance measurement for different titania nanotube arrays grown in ethylene glycol based electrolyte containing HF and water at different temperature and the influence of thickness on resistance. The inset shows more details about the relationship between the thickness of the nanotube arrays annealed at 250 °C and their specific resistivity. Reproduced from ref. [99]
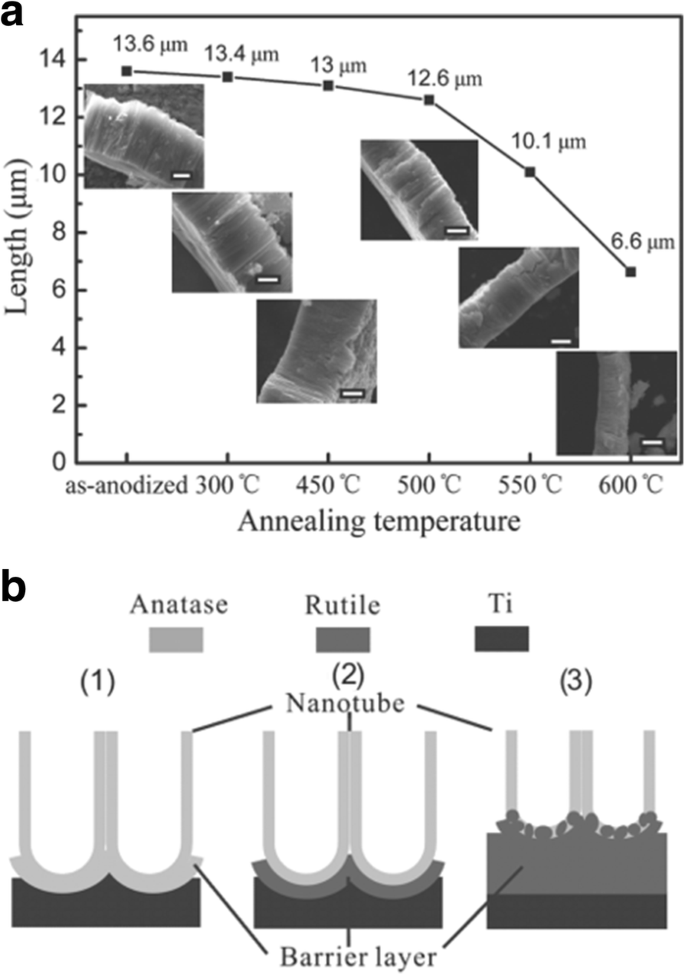
Evolution of titania nanotube arrays at different calcination temperatures. The electrolyte was ethylene glycol containing 0.3 wt% ammonium fluoride and 5 vol% distilled water. а The decrease in the thickness of titania nanotube arrays at different annealing temperature from 300 to 600 °C. The insets are corresponding SEM images and the scale bar is 5 μm. б The schematic of crystallization process of anodic titania nanotubes annealed at (1) 450 °C, (2) 500 °C, and (3) 600 °C in air. Reproduced from ref. [104]
Doping
Doping ions or atoms into titania lattice, a substitution within the lattice either at Ti 4+ or O 2− sites, on the one hand, changes the lattice constants and bond energy. On the other hand, it is beneficial to the separation between photogenerated electron and hole pair, which in turn adjusts the band gap and improves the photoelectrochemical performance of nanotubes [15]. The impurity doping has been commonly applied to extend the light absorption onset of TiO2 nanotubes by either introducing subbandgap states or adjusting its bandgap width [105]. Lately, co-doping approach has been proposed as a more efficient way to reduce the band gap and adjust energy band level in favor of photoelectriochemical reactions [106, 107]. There are various kinds of doped-elements and preparation methods, and Table 2 summarizes some methods and the doping effects of doped titania nanotubes.
The most typical doped TiO2 nanotubes are as follows:
- i.
Metal-doped TiO2 nanotubes such as Nb [107], Fe [108], Cu [109], Cr [110], Zr [111], Zn [112], and V [113]
- ii.
Non-metal-doped TiO2 nanotubes such as N [105], F [114], B [115], C [116], S [117], and I [118]
- iii.
Co-doped TiO2 nanotubes such as N–Ta [105], N–Nb [107], and C–N–Ni [119]
Choiet systematically studied the photoreactivities of 21 metal ion-doped quantum-sized TiO2 doping with Fe, Mo, Ru, Os, Re, V, and Rh significantly increases quantum efficiency, while Co and Al doping decreases the photoreactivity [120]. Momeni et al. recently obtained Fe-TiO2 nanotube (Fe-TNT) composites using different amounts of irons to decorate anodically formed TiO2 nanotubes with potassium ferricyanide as the iron source, indicating that Fe doping efficiently accelerates the photocatalytic performance for water splitting [108]. Not limited to transition metals, other elements including N [105], F [114], B [115], C [116], S [117], and I [118] are successfully explored. Nitrogen-doped TiO2 nanotubes turns out to be a promising path to narrow the band gap energy with enhanced photocurrent response in the visible light and the tube length influences the magnitude of conversion efficiency [121, 122]. Kim and co-workers proved that TaOxNy layer-decorated N-TNT (N-doped TiO2 nanotubes) as dual modified TNTs have significantly improved both visible (3.6 times) and UV (1.8 times) activities for water splitting [105]. At present, more researches are aimed at co-doping which exhibits remarkable synergistic effect causing a significant improvement on photoelectriochemical properties. Chai et al. grew Gd–La co-doped TiO2 nanotubes by an ultrasonic hydrothermal method, enhancing visible light photocatalysts [123]. Cottineau et al. modified titania nanotubes with nitrogen and niobium to achieve co-doped nanotubes with noticeably enhanced photoelectriochemical conversion efficiency in the visible light range [107]. Nevertheless, the mechanism for increasing photoconductivity and synergistic effect of various elements on co-doping remains a further study.
Surface Modification
Surface modification means decoration on surface of TiO2 nanotube arrays with nanoparticles (metal, semiconductors, and organic dyes). Nanowire arrays can also be fabricated by electrodeposition into titanium oxide nanotubes [124]. TiO 2 nanotube is a semiconductor with a wide band gap, which can only absorb ultraviolet light [97, 125]. Any other nanomaterials which possess a narrow band gap or can absorb the visible light can be used as a sensitizer for titania nanotubes. Silver nanoparticles can be decorated on the tube wall by soaking the titania nanotube arrays in AgNO3 solutions and photocatalytically reducing Ag + on a TiO2 surface by UV illumination [126]. Ag/TiO2 nanotubes show a significantly higher photocatalytic activity and good biological performance compared with neat TiO2 nanotubes [126, 127]. Some compositions such as graphene oxide GO [128], CdS [129], CdSe [130], and ZnFe2 О 4 [131]. can be modified on TiO2 nanotube arrays. Lately, GO have attracted much scientific interest in nanoscale devices and sensors which is easy to combine with nanostructure materials to compose some compounds. Titania nanotubes fabricated by anodization in water-ethylene glycol electrolyte consisting of 0.5 wt% ammonium fluoride (NH4 F) can be incorporated with GO by cyclic voltammetric method, which achieve higher photocatalytic activity and more effective conversion efficiency (GO-modified vs pure nanotubes =26.55%:7.3%) of solar cell than unmodified TiO2 nanotubes [128]. Semiconductor composite is a method improving the performance of titania nanotubes via, in some specific way, combining two kinds of semiconductors with different band gap [132]. Ян и др. decorated CdSe nanoparticles on the surface of TiO2 nanotubes by applying an external electric field to accelerate CdSe nanoparticles in nanochannels resulting in a material with more stable and higher photoresponse to visible light. Furthermore, the degeneration rate of anthracene-9-carbonxylic acid when exposed to the green light irradiation indicating that CdSe dominates the photocatalytic process under visible light [130].
Besides, other oxide nanoparticle deposition such as WO3 [133] or TiO2 [134] onto TiO2 nanotubes by the hydrolysis of a chloride precursor also turns out to augment the surface area and improve the solar cell efficiency. Another very effective approach is to consider organic dyes as sensitizers for TiO2 nanotubes to improve its optical properties [135]. Lately, atomic layer deposition (ALD) becomes an established procedure to modify TiO2 nanotube layers. ALD appears to be a very uniform and precisely controllable deposition process to functionalize nanotubes in conformably coating the surface of the nanotube layers with one atomic layer after another of a secondary material, such as Pd [136], ZnO [137], Al2 О 3 [138], CdS [139], or TiO2 [140].
Biomedical Applications
Historically, the mentioned milestones were reported on the fabrication of titania nanotube arrays contributing to widen the promising applications over the past 20 years in the areas ranging from anticorrosion, self-cleaning coatings, and paints to sensors [141,142,143], dye-sensitized and solid-state bulk heterojunction solar cells [144,145,146], photocatalysis [147, 148], eletrocatalysis, and water photoelectrolysis [149, 150]. They also outperform in biomedical directions as biocompatible materials, toward biomedical coatings with enhanced osseointegration, drug delivery systems, and advanced tissue engineering [15, 135, 141, 142, 151]. In the following section, we will give an overview of current efforts toward TiO2 nanotubes biomedical applications. Titania nanotubes possess good biocompatibility as they show some antibacterial property, low cytotoxicity, good stability, and cytocompatibility including promoting adhesion, proliferation, and differentiation of osteoblast and mesenchymal stem cells (MSCs) with a high surface area-to-volume ratio and controllable dimensions [152,153,154,155].
However, Ti products have inadequate antibacterial ability and efforts have been made to improve their antibacterial properties such as modifications on titania nanotubes for biomedical applications like bioimplant [126, 156].
Biological Coatings And Interactions with Cells
A number of in vitro and in vivo studies have demonstrated that MSCs, osteoblasts and osteoclasts show size-selective response which means the effect of size holds an important position in cell interaction where the optimized size for cell adhesion, proliferation, growth, and differentiation is ranging from 15 to 100 nm [153, 157, 158]. Particularly, it was demonstrated that the TiO2 nanotubes with a diameter of 70 nm was the optimal nanoscale geometry for the osteogenic differentiation of human adipose-derived stem cells (hASCs) [159]. Smith et al. reported increased dermal fibroblasts and decreased epidermal keratinocyte adhesion, proliferation, and differentiation on TiO2 nanotube arrays (diameter 70–90 nm, length 1–1.5 μm) [160]. As shown in Fig. 10, Peng et al. found that nanotubular surface preferentially promoted proliferation and function in endothelial cells (EC) while decreased in vascular smooth muscle cell (VSMC) by measuring EdU, a thymidine analog which is incorporated by proliferating cells [161]. Furthermore, it is pointed out that surface wettability of the TiO2 nanotube layers is recognized as a critical factor for cell behavior which can be adjusted by changing the diameter of the nanotubes. That is to say, water contact angles can be altered without changing the surface chemistry [158]. To get further understanding of the effect of TiO2 nanotube layers to bone-forming cells as well as stem cells response, Park et al. seeded green fluorescent protein-labeled rat MSCs on TiO2 nanotube layers with six different diameters (15, 20, 30, 50, 70, and 100 nm), resulting in cell activity that is sensitive to nanoscale surface topography with a maximum in cell activity obtained for tube diameters of approximately 15–30 nm. Such lateral spacing exactly corresponds to the predicted lateral spacing of integrin receptors in focal contacts on the extracellular matrix, forcing clustering of integrins into the closest packing, resulting in optimal integrin activation. While tube diameters larger than 50 nm, severely impaired cell spreading, adhesion, and spacing of 100 nm may lead to the cell apoptosis [94]. Besides adjusting the size of the nanotubes, surface modification loaded with bioactive factors should be highlighted, in which case biomedical properties can be further optimized. In the case of bone implants, hydroxyapatite (HA) formation is important for osseointegration. Recent works have shown hydroxyapatite nanocrystalline coating onto the nanotubular TiO2 results in further enhanced osseointegration with strong adhesion and bond strength, and a drastic enhancement of deposition rate is observed [162, 163]. Nanotubular TiO2 surface can greatly enhance the natural apatite growth rate in simulated body fluid (SBF) compared with flat surfaces [10, 164]. The alkaline-treated TiO2 nanotubes with NaOH solutions are more bioactive in SBF, where sodium titanate can significantly accelerate nucleation and the growth of HA formation presenting a well-adhered bioactive surface layer on Ti due to its larger surface area and promoted mechanical interlocking between HA and TiO2 nanotubes [165, 166]. Electrodeposited with hydroxyapatite, higher adhesion of TiO2 nanotubes has been described in the literature by means of adhesive tape test and the live/dead cell staining study which is essential for early bone formation [166]. The results also showed that at the length of 560 nm the highest adhesion of HA surface on the nanotubes is observed. Also the nanotube surface can indeed strengthen Collagen type I expression in vivo experiment which is considered to be a basic initial bone matrix protein in bone formation [167]. Moreover, annealing of the amorphous nanotubes to anatase or a mixture of anatase and rutile was found to be an important factor in the apatite formation process [164].
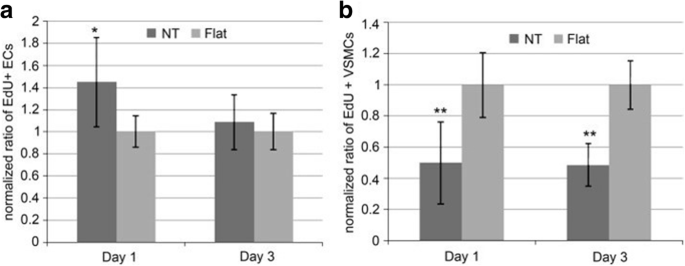
Ratio of EdU positive a ECs and b VSMCs on flat or nanotube substrate. It is normalized by the average proportion of positive cells on flat surfaces on day 1 and 3. Data is presented as average ± standard deviation. * p < 0.05, **p < 0.01 versus same day flat control, n = 6 reproduced from ref. [161]
Drug Delivery and Antibacterial Ability
Furthermore, the tubular nature of TiO2 in biomedical devices may be exploited as gene and drug delivery carriers with living matter due to its high surface area, controllable pore, and self-ordered structure [1, 15]. When the orthopedic bioimplant is placed into the bone defect, persistent and chronic infection is one of the most common and serious complications associated with biomedical implantation [16, 168]. Certain dimension and crystallinity may be useful to prevent bacteria adhesion and promote bone formation. The thermal annealing has decreased the number of bacteria adhering to the Ti surface. It could be in part because heat treatment removes the fluorine content which has a tendency to attract bacteria. The research also indicates that nanotubes with 60 or 80 nm in diameter decrease the number of live bacteria as compared to lower diameter (20 or 40 nm) nanotubes [169, 170].
Bauer et al. loaded epidermal growth factor (EGF) and bone morphogenetic protein-2(BMP-2) onto the TiO2 nanotubes surface by covalent attachment. They observed positive influence on the behavior of MSCs on 100-nm nanotube arrays where cell count was at much higher levels compared to the untreated one [171]. Lately, titania nanotubes loaded with antibiotics contribute to suppressing bacterial infections. As gentamicin sulphate (GS) is mostly widely used with highly water solubility, Feng et al. loaded titania nanotubes with GS through physical adsorption and cyclic loading which can treat many types of bacterial infections [172]. Zhang et al. fabricated titania nanotubes loaded with vancomycin to investigate the increasing biocompatibility and obvious antibacterial effect on Staphylococcus aureus [173]. However, systemic antibiotics in clinical will bring many side effects. The release of antibiotics from the nanotubes is too fast to maintain the long-term antibacterial ability, and the use of antibiotics may develop resistant strains [126, 168, 174]. Ensuring a constant release rate becomes a crucial but difficult part in the field of drug delivery. In strategies like surface modification, controlling the dimension of nanotube arrays, biodegradable polymer coating have been employed to solve the issue [21]. Drug release of several drugs such as antibiotics or growth factors from titania nanotube arrays can be adjusted by varying their diameters and lengths [152, 175, 176]. Feng et al. covered a thin film comprising a mixture of GS and chitosan on GS-loaded titania nanotubes and showed a controlled release of the drug providing sustained release effects to a certain extent [172]. Titania nanotube arrays as drug nanoreservoirs on Ti surface for loading of BMP-2 were fabricated by Hu et al. and then further covered with gelatin/chitosan multilayers to control the release of the functional molecule meanwhile maintain the bioactivity for over 120 h via a spin-assisted layer-by-layer assembly technique which is mainly based on electrostatic interactions between polyanions and polycations as well as promote osteoblastic differentiation of MSCs [177]. Lai et al. successfully fabricated Chi/Gel multilayer on melatonin-loaded TiO2 nanotube arrays to control the sustained release of melatonin and promote the osteogenic differentiation of mesenchymal stem cells [178]. Karan et al. synthesized titania nanotubes loaded with the water-insoluble anti-inflammatory drug indomethacin and modified lactic-co-glycolic acid on surface as a polymer film in order to extend the drug release time of titania nanotubes and produce favorable bone cell adhesion properties, with reduced burst release (from 77 to> 20%) and extended overall release from 4 days to more than 30 days [152]. As previous study reported that surface treatment of implants with N -acetyl cysteine (NAC) may reduce implant-induced inflammation and promote faster bone regeneration [179], Lee et al. examined the feasibility of N -acetyl cysteine-loaded titania nanotubes as a potential drug delivery system onto an implant surface, and the data indicates the enhanced osseointegration and the value of the small animal model in assessing diverse biological responses to dental implants. Besides, TiO2 nanotube arrays are suitable for loading inorganic agents like Ag, Sr, and Zn to obtain long-term antibacterial ability and osseointegration [126, 180,181,182]. Ag nanoparticles have been incorporated into TiO2 nanotube arrays previously with satisfactory small possibility to develop resistant strains, a broad-spectrum antibacterial property, low cytotoxicity, and good stability by immersion in a silver nitrate solution followed by ultraviolet light radiation [126]. Zhang et al. demonstrated that a series of porous TiO2 coatings with different concentrations of silver had significant inhibition effect on Escherichia coli и золотистый стафилококк . Besides, only with the optimum amount of silver can the coatings retain the antibacterial effect but without any measurable cytotoxicity to cells [183]. Due to cytotoxicity observed by the excessive release of Ag + subsequently, titania nanotube arrays with Ag2 O nanoparticles embedded in the wall are prepared on Ti by TiAg magnetron sputtering and anodization in order to get slower and more controllable silver ion release [184]. That is because the TiO2 barrier is surrounded thereby minimizing the cytotoxicity induced by burst or large Ag + release.
Similar to Ag, Zn possesses antibacterial and anti-inflammation properties, and osteogenesis induction [185,186,187]. Huo et al. produced anodic TiO2 nanotube arrays at 10 V and 40 V (NT10 and NT40) incorporated with Zn by hydrothermal treatment at 200 °C for 1 and 3 h (NT10-Zn1, NT10-Zn3, NT40-Zn1, and NT40-Zn3) in Zn containing solutions, followed by annealing at 450 °C for 3 h in air. NT40-Zn3 has the largest Zn loading capacity and releases more Zn compared with other samples. The amounts of Zn released diminish gradually with time and nearly no Zn can be detected 1 month later except sample NT40-Zn3 (Fig. 11). The NT-Zn samples present different antibacterial ability. It is evident that NT40-Zn3 and NT10-Zn3 effectively kill more adherent bacteria as well as surrounding planktonic bacteria in the early stage. Figure 12a describes a synergistic effect of both released and surface incorporated Zn while Fig. 12b explains the effect of the released Zn [181].
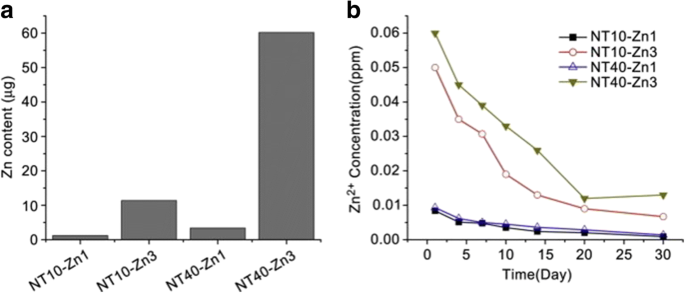
а Total amounts of Zn incorporated into the NT-Zn samples for the 1 cm 2 coatings and b non-cumulative Zn release profiles from NT-Zn into PBS. Reproduced from ref. [181]
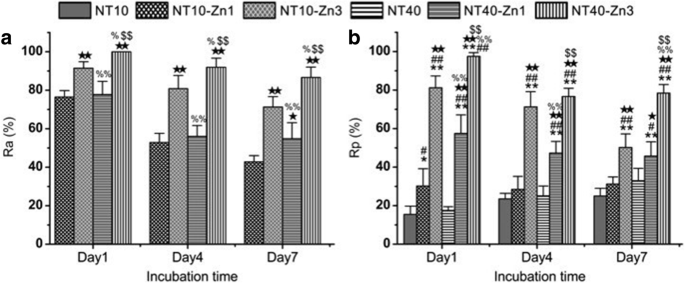
а Antibacterial rates versus adherent bacteria on the specimen (Ra) and b antibacterial rates against planktonic bacteria in the medium (Rp) *, **p < 0.05 and 0.01 vs NT10; # , ## p < 0.05 and 0.01 vs NT40; ★ , ★★ p < 0.05 and 0.01 vs NT10-Zn1; % , %% p < 0.05 and 0.01 vs NT10-Zn3; $ , $$ p < 0.05 and 0.01 vs NT40-Zn1. Reproduced from ref. [181]
Выводы
This review presents the historical developments and traditional formation mechanism of titania nanotube arrays grown by electrochemical anodization as well as the approaches to influence and modify morphology in order to improve their performances. We also focus on current efforts toward TiO2 nanotubes applications in biomedical directions. Those steady progresses have demonstrated that TiO2 nanotubes are playing and will continue to play an important role in material science, but there are still some aspects needed to be further improved.
- 1.
The synthesis of TiO2 nanotube arrays is already comparatively mature so far in fact, but how to simplify the technology for the purpose of large-scale production in industry with extending practical operability and how to precisely control nanotube geometry efficiently by varying the anodic parameters so as to obtain optimized properties have yet to be further investigated.
- 2.
The formation mechanisms of anodic TiO2 nanotubes have gradually become a hotspot of research due to their unique structure and excellent performances but the exact mechanism remains controversial. Conventional FAD explains the growth process and the porous structure of TiO2 nanotubes, but the combination of viscous flow model and growth model of two currents can give a comprehensive explanation to the growth process. Notably, the validity of oxygen evolution resulting from electronic current has much room for investigation.
- 3.
Modification is key for improving performances of titania nanotube arrays. Thus, we need to explore more methods for modification and take full advantage of the self-organized nanostructure. Through self-assembling inorganic, organic, metallic, and magnetic nanoparticles into or onto the tubes as nanocomposites with broad spectral response to visible light, high quantum efficiency, and stabilizing properties, applications could be widened. Currently, ALD appears to be an option to coat the titania nanotube layers homogenously and precisely from the bottom to the tube mouth, resulting in many advanced functionalities of the newly prepared nanotube layers. Nevertheless, further optimization of the ALD process toward coatings and inner fillings is demanded.
- 4.
TiO 2 nanotube researches in biomedical directions are still in their infancy and have a long distance to go in clinical use. The biological reaction between cells and titania nanotubes has to develop from cellular level to molecular level and from morphological changes to molecular alterations. It has been shown that adhesion, spreading, and growth of osteoblast and mesenchymal stem cells strongly depends on nanotube diameter, so the regularity and principle of this phenomenon as well as other factors affecting cells’ behaviors need to be further explored.
Сокращения
- ALD:
-
Осаждение атомного слоя
- BMP-2:
-
Bone morphogenetic protein-2
- DMSO:
-
Диметилсульфоксид
- DSSCs:
-
Dye-sensitized solar cells
- EBSD:
-
Electron Backscatter Diffraction
- EC:
-
Endothelial cells
- EdU:
-
A thymidine analog
- EGF:
-
Epidermal growth factor
- FAD:
-
Conventional field-assisted dissolution
- FE-SEM:
-
Field-emission scanning electron microscopy
- Fe-TNTs:
-
Fe-doped TiO2 nanotubes
- FIB:
-
Focused ion beam
- GO:
-
Оксид графена
- GS:
-
Gentamicin sulphate
- HA:
-
Hydroxyapatite
- hASCs:
-
Adipose-derived stem cells
- IPCE:
-
Incident photon-to-electron conversion efficiency
- MSCs:
-
Mesenchymal stem cells
- NAC:
-
N -Acetyl cysteine
- N-TNT:
-
N-doped TiO2 nanotubes
- PEC:
-
Photoelectriochemical
- SBF:
-
Simulated body fluid
- UV:
-
Ультрафиолет
- VSMC:
-
Vascular smooth muscle cell
Наноматериалы
- 4 использования гафния | Применение гафния и сплавов гафния.
- Многофункциональные наночастицы золота для улучшенных диагностических и терапевтических применений:обзор
- Достижения и проблемы флуоресцентных наноматериалов для синтеза и биомедицинских приложений
- Графен и полимерные композиты для суперконденсаторов:обзор
- На пути к наножидкости TiO2 - Часть 2:Приложения и проблемы
- Влияние контактной неравновесной плазмы на структурные и магнитные свойства шпинелей Mn Х Fe3 - X О4
- Массивы нанотрубок TiO2:изготовлены с помощью мягко-твердого шаблона и зависимости характеристик эмиссии поля…
- Сравнительное исследование электрохимических, биомедицинских и тепловых свойств природных и синтетических…
- Фрезерный шпиндель и замечательные приложения
- 9 типов инструментов для работы с потоками и приложения



