Изготовление и фотокаталитические свойства новых нанокомпозитов SrTiO3 / Bi5O7I
Аннотация
Роман SrTiO 3 / Би 5 О 7 Нанокомпозиты I были успешно изготовлены методом термического разложения. Свежеприготовленные образцы характеризовали с помощью спектров XRD, XPS, SEM, EDS, FTIR, DRS и PL. Результаты показывают, что SrTiO 3 / Би 5 О 7 Нанокомпозиты I состоят из перовскита SrTiO 3 наночастицы и тетрагональный Bi 5 О 7 Я наностержни. SrTiO 3 / Би 5 О 7 Нанокомпозиты I демонстрируют отличные фотокаталитические характеристики разложения раствора RhB под воздействием искусственного солнечного света, что превосходит таковые у чистого Bi 5 О 7 Я и SrTiO 3 . В частности, 30 мас.% SrTiO 3 / Би 5 О 7 Нанокомпозит I считается оптимальным композитом, над которым деградация красителя достигает 89,6% за 150 мин фотокатализа. Скорость фотокаталитического разложения 30 мас.% SrTiO 3 / Би 5 О 7 Нанокомпозит I в 3,97 раза и в 12,5 раз выше, чем у чистого Bi 5 О 7 Я и SrTiO 3 , соответственно. Эксперименты по отлову реактивных частиц показывают, что \ (\ bullet {\ mathrm {O}} _ 2 ^ {-} \) и дыры являются основными активными частицами, ответственными за деградацию RhB. Кроме того, спектры ФЛ показывают эффективное разделение фотоиндуцированных электронно-дырочных пар. Кроме того, возможный фотокаталитический механизм SrTiO 3 / Би 5 О 7 Нанокомпозиты I также выяснены на основе экспериментальных данных.
Фон
Красители текстильной промышленности или производства красителей вызывают серьезную озабоченность из-за воздействия на качество водных ресурсов и токсичных и канцерогенных продуктов разложения [1]. Поэтому необходимы более грамотные методы очистки, чтобы полностью исключить красители из сточных вод. Несколько традиционных методов, включающих физические, химические и биологические методы, применялись для очистки сточных вод от красителей [2]. Эти методы позволяют удалять красители из сточных вод, но они часто дороги, неэффективны и приводят к образованию вторичных отходов [3, 4]. Среди различных технологий очистки сточных вод от красителей фотокатализ на основе полупроводников вызвал большой интерес и привлек внимание всего мира [5,6,7]. Это связано с тем, что он использует солнечную энергию для разложения красителей, загрязняющих окружающую среду, чей источник энергии является обильным, неисчерпаемым, экологически чистым и бесплатным [8, 9]. В настоящее время TiO 2 является наиболее широко используемым полупроводниковым фотокатализатором из-за его высокой фотоактивности, низкой стоимости, химической и фотохимической стабильности, нетоксичности и экологичности. Однако он показал очень низкую фотокаталитическую активность при облучении видимым светом из-за его широкой запрещенной зоны 3,2 эВ и быстрой рекомбинации фотогенерированных носителей [10]. Для эффективного решения вышеупомянутых проблем много работ было посвящено модификации поверхности или комбинации полупроводниковых фотокатализаторов [11]. Тем не менее, разработка новых и высокоэффективных фотокатализаторов по-прежнему остается серьезной проблемой [12].
Би 5 О 7 I - это недавно обнаруженный полупроводник p-типа, который показывает относительно более высокий уровень положительной валентной зоны (VB), чем другие оксиодиды висмута, благодаря большему количеству фотовозбужденных дырок и, следовательно, облегчает разделение фотогенерированных носителей [13]. Следовательно, Bi 5 О 7 Фотокатализатор I проявляет высокую активность в отношении фотодеградации родамина B (RhB) в воде и ацетальдегиде при облучении видимым светом [14]. К сожалению, практическое применение Bi 5 О 7 Фотокатализатор I для дезактивации окружающей среды все еще ограничен, что объясняется его низкой эффективностью переноса, вызванной рекомбинацией фотогенерированных электронов и дырок [15]. С целью дальнейшего улучшения фотоактивности Bi 5 О 7 I было выполнено много попыток, таких как легирование металлами или неметаллами [16] или соединение с другими полупроводниками. Например, Хуанг и др. синтезированный g-C 3 N 4 / Би 5 О 7 I гетеропереходом методом сокристаллизации, и композит показал скорость разложения в 2,9 раза выше, чем у чистого Bi 5 О 7 I [17]; Cheng et al. сфабрикованный Bi 5 О 7 I / Bi 2 О 3 композит методом химического травления, показавший высокую фотокаталитическую активность при разложении малахитовой зелени [18]; Hu et al. сообщил, что композит, содержащий Sr 2 n-типа TiO 4 и р-типа Bi 5 О 7 Я показал повышенную фотоактивность из-за ингибирования электронно-дырочной рекомбинации [19]; Cui et al. изготовленные AgI / Bi 5 О 7 Я гибридизирую посредством простой одностадийной ионной реакции, и AgI / Bi 5 О 7 Композит I усиливал фотокаталитическую активность [20] и так далее. Эти результаты показали, что Bi 5 О 7 Композиты на основе I показали улучшенные фотокаталитические характеристики при облучении видимым светом. Следовательно, мы можем изготовить Bi 5 О 7 Композиты на основе I через соединение с другим полупроводником с подходящей зоной проводимости (CB) и позициями VB в качестве многообещающего фотокатализатора, управляемого видимым светом. Среди различных кандидатов титанат стронция (SrTiO 3 ) представляет собой полупроводниковый материал n-типа, который был тщательно изучен из-за его многих превосходных свойств, например, термической стабильности, хорошей термостойкости, коррозии и сопротивления [21,22,23]. Чистый SrTiO 3 поглощает только УФ-свет из-за своей широкой запрещенной зоны 3,1 ~ 3,4 эВ [24]. К счастью, VB SrTiO 3 расположен между CB и VB Bi 5 О 7 I, а его CB расположен над CB Bi 5 О 7 I. Принимая во внимание конструктивные достоинства Bi 5 О 7 I, комбинация SrTiO 3 с Bi 5 О 7 I, чтобы сформировать SrTiO 3 / Би 5 О 7 Композит I может быть жизнеспособным и целесообразным способом реализации высокой фотокаталитической активности.
В этой работе серия SrTiO 3 / Би 5 О 7 Впервые синтезированы нанокомпозитные фотокатализаторы I. Их кристаллическая фаза, микроструктура и оптические свойства были исследованы с помощью ряда методов. SrTiO 3 / Би 5 О 7 Нанокомпозиты I показали улучшенные фотокаталитические характеристики при разложении раствора родамина B (RhB) под воздействием искусственного солнечного излучения. Кроме того, возможный фотокаталитический механизм SrTiO 3 / Би 5 О 7 Нанокомпозиты I также были выяснены на основе экспериментальных данных.
Методы
Подготовка SrTiO 3 / Би 5 О 7 I Композиты
SrTiO 3 наночастицы и SrTiO 3 / Композиты BiOI были впервые синтезированы золь-гель методом, как описано в литературе [25, 26]. SrTiO 3 / Би 5 О 7 Затем композиты I были синтезированы методом термического разложения. Все химические реагенты использовали непосредственно для экспериментов без дополнительной очистки. Во время термического разложения свежеприготовленный SrTiO 3 / Композиты BiOI были помещены в трубчатую печь, и программа нагрева была установлена следующим образом:линейное изменение температуры 5 ° C мин - 1 до 500 ° C непрерывно и выдерживают при 500 ° C в течение 3 часов. Затем печь естественным образом охлаждали до комнатной температуры с получением 10 мас.% SrTiO 3 / Би 5 О 7 Я нанокомпозит. Другой SrTiO 3 / Би 5 О 7 Нанокомпозитные материалы I с различными SrTiO 3 контент был изготовлен аналогичным способом.
Образец характеристики
Кристаллические структуры синтезированных образцов охарактеризованы методом рентгеновской дифракции (XRD) с Cu K α радиация (Д / макс-2500, Ригаку). Морфологию образцов исследовали с помощью автоэмиссионного сканирующего электронного микроскопа сверхвысокого разрешения (FE-SEM; SUAPR55, Германия Zeiss) с использованием энергодисперсной рентгеновской спектроскопии (EDS). Элементный компонент поверхности и химическое состояние образцов анализировали с помощью рентгеновской фотоэлектронной спектроскопии (XPS; Axis Ultra DLD, Kratos Analytical, Великобритания) с монохроматизированным Al K α Источник рентгеновского излучения (hν =1486,6 эВ). Спектры диффузного отражения (DRS) в ультрафиолетовой-видимой (УФ-видимой области) области получали с использованием спектрофотометра УФ-видимой области (UV-2450, Shimadzu). Функциональные группы на поверхности образцов исследовали с помощью инфракрасной спектроскопии с преобразованием Фурье Nicolet iS50 (FTIR; Thermo Fisher Scientific, США). Спектры излучения фотолюминесценции (ФЛ) измеряли на стационарном флуоресцентном спектрометре LH110911.
Фотокаталитические оценочные исследования
Фотокаталитическую активность материалов оценивали по разложению RhB при моделировании облучения солнечным светом (УФ-светом) в аппарате для фотореакции. После 30-минутной адсорбции в темноте адсорбция-десорбция находится в равновесии между фотокатализатором и молекулами RhB. В качестве источника искусственного солнечного света (УФ-лампа) использовалась ксеноновая лампа мощностью 500 Вт. Сто миллиграммов фотокатализатора полностью диспергировали в 100 мл раствора RhB (20 мг / л). Во время каждого фотокаталитического эксперимента 3 мл суспензии отбирали пипеткой каждые 30 мин и центрифугировали для удаления частиц катализатора. Концентрацию RhB измеряли с помощью УФ-видимого спектрофотометра.
Результаты и обсуждение
XRD-анализ
Картины рентгеновской дифракции порошка предоставляют информацию о кристаллической структуре и фазе синтезированных образцов, как показано на рис. 1. SrTiO 3 Образец сильно кристаллизован со структурой перовскита (JCPDS № 35-0734). Пики дифракции при 2 θ значения 22,75 °, 32,39 °, 39,95 °, 46,47 °, 52,34 °, 57,78 °, 67,82 ° и 77,18 ° могут быть индексированы как (100), (110), (111), (200), (210), Плоскости кристалла (211), (220) и (310) соответственно [27]. Никаких других специфических дифракционных пиков не обнаружено. Из рентгенограммы чистого Bi 5 О 7 I видно, что основные дифракционные пики при 7,71 °, 13,31 °, 15,38 °, 23,19 °, 28,08 °, 31,09 °, 33,43 °, 46,28 °, 47,69 °, 53,45 °, 56,51 ° и 58,02 ° соответствуют на номера (001), (201), (002), (401), (312), (004), (020), (024), (224), (714), (332) и (624) самолеты Би 5 О 7 I (JCPDS № 10-0548) соответственно [28]. Самый сильный пик соответствует плоскости кристалла (312) Bi 5 О 7 I. Из рентгенограммы 30 мас.% SrTiO 3 / Би 5 О 7 I, можно обнаружить, что все заметные дифракционные пики возникают из тетрагонального Bi 5 О 7 I и перовскит SrTiO 3 . Других очевидных пиков примесей не наблюдается, что указывает на то, что Bi 5 О 7 Я и SrTiO 3 Фазы сосуществуют в композите.
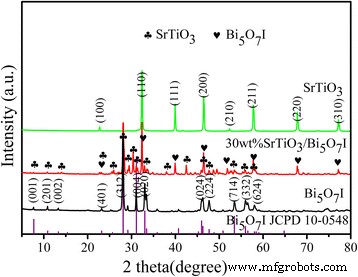
Рентгенограммы чистого Bi 5 О 7 Я, SrTiO 3 и 30 мас.% SrTiO 3 / Би 5 О 7 I нанокомпозит
Анализ XPS
Измерения XPS предоставляют дополнительную информацию для оценки элементного состава поверхности и чистоты 30 мас.% SrTiO 3 / Би 5 О 7 Я нанокомпозит. Энергия связи, полученная при анализе XPS, была скорректирована с учетом заряда образца путем привязки C 1 с к 284,65 эВ, и результаты показаны на рис. 2. Спектр обзора XPS-сканирования композита показан на рис. 2a, который показывает наличие в композите элементов Ti, Sr, Bi, I и O. Два сильных пика при 159,02 и 164,25 эВ соответственно относятся к Bi 4f 5/2 и Би 4ф 7/2 пики Bi 3+ в SrTiO 3 / Би 5 О 7 I нанокомпозитов, как показано на рис. 2b [29]. В XPS-спектрах I 3d, показанных на рис. 2c, два сильных пика при 617,88 и 630,22 эВ, соответствующих I 3d 5/2 а я 3d 3/2 соответственно, предполагают степень окисления йода -1 [30]. Как показано на рис. 2d, энергии связи Ti 2p 3/2 и Ti 2p 1/2 соответствуют пикам при 457,90 и 463,80 эВ в спектре Ti 2p соответственно. Разделение пиков между Ti 2p 3/2 и Ti 2p 1/2 составляет 5,90 эВ, что указывает на степень окисления +4 Ti в SrTiO3 / Bi 5 О 7 I композиты [31]. На рис. 2д пики при 132,50 и 134,25 эВ соответствуют энергиям связи Sr 3d 5/2 и Sr 3d 3/2 соответственно, что указывает на его существование в Sr 2+ состояние [32]. На рис. 2е пики при 529,65 и 531,25 эВ относятся к O 1 с. Пик при 529,65 эВ приписывается решеточному кислороду SrTiO 3 . / Би 5 О 7 I, а пик при 531,25 эВ обычно связывают с хемосорбированным кислородом, вызванным кислородными вакансиями [33]. Результат XPS дополнительно подтверждает образование SrTiO 3 / Би 5 О 7 I, и была достигнута тесная интеграция, что хорошо согласуется с результатами XRD.
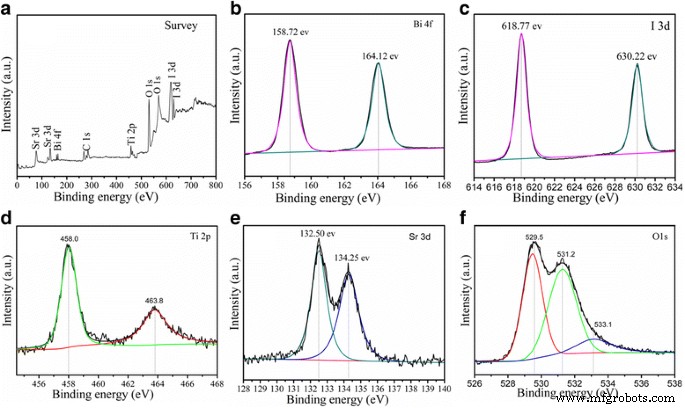
Образцы РФЭС 30% SrTiO 3 / Би 5 О 7 I нанокомпозиты: a опрос, b Bi 4f, c Я 3d, d Ti 2p, e Sr 3d и f O1s
Анализ SEM и EDS
Состав и морфология поверхности чистого SrTiO 3 в исходном состоянии. , Би 5 О 7 I и 30 мас.% SrTiO 3 / Би 5 О 7 Нанокомпозит I наблюдали с помощью FE-SEM. Как видно на рис. 3а, чистый SrTiO 3 состоит из сфероидальных или сферических частиц диаметром от 50 до 300 нм. SrTiO 3 меньшего размера частицы, очевидно, до некоторой степени агрегированы вместе. На рис. 3б для Bi 5 О 7 I нанолистов, они имеют средний размер около 1 мкм и толщину в диапазоне 80 ~ 100 нм, что аналогично тому, о котором сообщалось ранее [13]. Напротив, после комбинации Bi 5 О 7 I - это не нанолисты, а морфология наностержней, которая состоит из множества наностержней, как показано на рис. 3c. Для Би 5 О 7 I, длина находится в диапазоне 100 ~ 300 нм, а средний диаметр составляет около 80 нм. Хорошо видно, что SrTiO 3 частицы плотно прилипают к поверхности Bi 5 О 7 I, и считается, что это благоприятно для фотокаталитических характеристик. Кроме того, EDS был дополнительно использован для анализа химического состава 30 мас.% SrTiO 3 / Би 5 О 7 Я нанокомпозит. Как показано на рис. 3d, наблюдаемый сигнал C может быть получен из проводящего клея, который используется для фиксации образца. Отмечено, что EDS удобно использовать для количественного определения содержания тяжелых элементов (например, Bi, Ti, I и Sr), но не легких элементов (например, P и O) [34]. Атомное отношение Bi к I получается как 11/63 из спектра EDS, что хорошо согласуется с атомным отношением Bi / I Bi 5 О 7 I этап. Атомное соотношение Sr / Bi очень близко к 1 / 12,5, что означает, что SrTiO 3 Фаза составляет около 30% от общего молярного содержания композита.
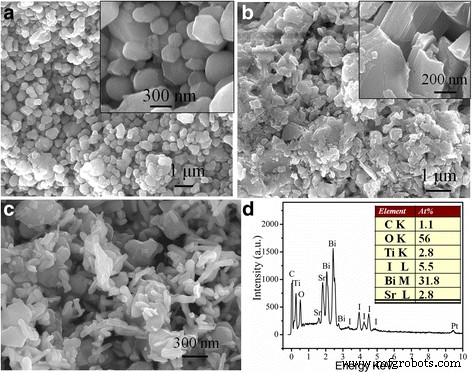
SEM-изображения a чистый SrTiO 3 , b чистый Bi 5 О 7 Я, c 30 мас.% SrTiO 3 / Би 5 О 7 I нанокомпозит, и d Спектр EDS 30 мас.% SrTiO 3 / Би 5 О 7 I нанокомпозит
Анализ оптических свойств
Спектры DRS в УФ и видимой областях для различных катализаторов показаны на рис. 4a. Чистый SrTiO 3 имеет край полосы поглощения при 380 нм в УФ-области, что может быть связано с большой шириной запрещенной зоны [35, 36]. Би 5 О 7 I показывает гораздо более длинный край поглощения 520 нм, который может реагировать на видимый свет. Край поглощения SrTiO 3 / Би 5 О 7 Нанокомпозиты I имеют размер 480 ~ 520 нм. По сравнению с чистым SrTiO 3 , после связывания с Bi 5 О 7 I, интенсивность пика поглощения SrTiO 3 / Би 5 О 7 Нанокомпозиты I значительно улучшились.
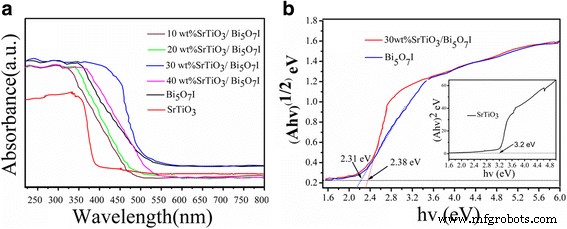
а Спектры DRS SrTiO 3 / Би 5 О 7 I нанокомпозиты и b график Таука (Ahν) 1/2 по сравнению с hν чистый Bi 5 О 7 I и 30 мас.% SrTiO 3 / Би 5 О 7 Нанокомпозит I, график Таука (Ahν) 2 по сравнению с hν чистый SrTiO 3 изображение-вставка b
Судя по спектрам поглощения, E g полупроводника можно рассчитать по формуле Aһν =A ( һν - E g ) n / 2 уравнение [37]. Значения n для SrTiO 3 и Би 5 О 7 Мне 4 и 1 соответственно. Энергия запрещенной зоны SrTiO 3 можно оценить по графику (Aһν) 2 в зависимости от энергии плотона (һν) и ширины запрещенной зоны Bi 5 О 7 Меня можно оценить по сюжету (Aһν) 1/2 против һν. Пересечение касательной к X ось дает приближение энергии запрещенной зоны образцов, как показано на рис. 4b. Значения ширины запрещенной зоны чистого Bi 5 О 7 I, 30 мас.% SrTiO 3 / Би 5 О 7 Нанокомпозит I и чистый SrTiO 3 составляют около 2,31, 2,38 и 3,2 эВ соответственно, что согласуется с данными, приведенными в соответствующей литературе [38, 39].
Анализ FTIR-спектроскопии
Би 5 О 7 Я и SrTiO 3 / Би 5 О 7 Нанокомпозиты I были дополнительно охарактеризованы с помощью ИК-Фурье спектроскопии для анализа их химической связи. Как показано на рис. 5. Видно, что почти во всех образцах полосы адсорбции 3445,5 и 1621,9 см −1 были обусловлены валентным колебанием O – H и деформационным колебанием хемосорбированных молекул воды [40]. Ремешок на 2906,5 см −1 приписывается валентному колебанию Ti – O [41]. Остальные пики в диапазоне 1471,6–500 см −1 соответствуют режимам растяжения и деформации с участием связей Bi – O [42].
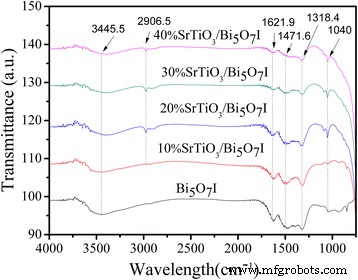
ИК-Фурье спектры чистого Bi 5 О 7 Я и SrTiO 3 / Би 5 О 7 I нанокомпозиты
Фотокаталитическая активность
Как Би 5 О 7 Я и SrTiO 3 имеют очень четкое фотопоглощение и SrTiO 3 в основном реагирует на ультрафиолетовый свет, имитируемый солнечный свет и ультрафиолетовый свет в тех же условиях используются отдельно в качестве источника света для исследования фотокаталитических характеристик Bi 5 О 7 Я, SrTiO 3 , и SrTiO 3 / Би 5 О 7 Нанокомпозиты I. На рис. 6а показаны кривые деградации RhB при моделировании солнечного излучения. Обнаружено, что RhB стабилен и практически не разлагается без катализатора при моделировании солнечного облучения в течение 150 мин. Чистый SrTiO 3 проявляет умеренную каталитическую активность, и только 18% восстановления RhB было достигнуто после 150 мин облучения. Это связано с низким поглощением света SrTiO 3 . в области видимого света или его большой ширине запрещенной зоны. Чистый Би 5 О 7 Я демонстрирую очень отчетливую активность, которая разрушает более 52% RhB за 150 минут. По сравнению с чистым SrTiO 3 и Би 5 О 7 Я, SrTiO 3 / Би 5 О 7 Нанокомпозиты I демонстрируют значительно повышенную фотокаталитическую активность в тех же условиях. С увеличением SrTiO 3 При содержании от 10 до 40% фотокаталитическая активность композитов сначала увеличивается, а затем снижается, причем наибольшая фотокаталитическая активность наблюдается у 30 мас.% SrTiO 3 / Би 5 О 7 Я нанокомпозит. Для этого оптимального композита деградация красителя достигает приблизительно 89,6% при моделированном облучении солнечным светом в течение 150 мин. Такая высокая активность может быть приписана фотогенерированным электронам, имеющим более быструю подвижность и разделение.
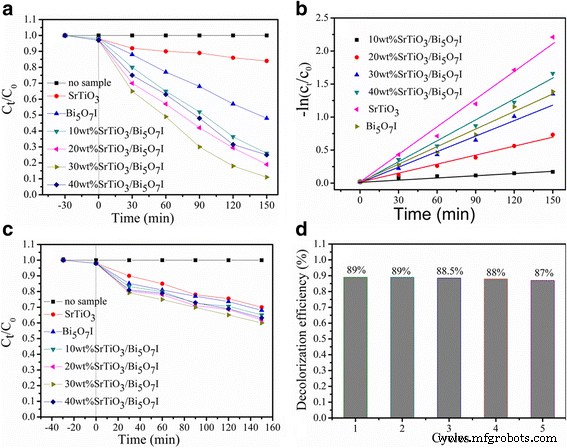
а Фотокаталитическая деградация раствора RhB для всех образцов при моделировании облучения солнечным светом. б Графики -ln (C t / C 0 ) от времени для всех образцов. c Фотокаталитическая деградация раствора RhB для всех образцов при УФ-освещении. г Циклическая эффективность разложения RhB по сравнению с SrTiO 3 / Би 5 О 7 I нанокомпозиты
Чтобы лучше понять кинетику реакции фотокаталитического разложения RhB для различных фотокатализаторов, эффективность фотокаталитического разложения была рассчитана с использованием следующего уравнения:ln ( C 0 / C т ) = K приложение т , где C 0 , C t , и K приложение представляют начальную концентрацию, концентрацию в момент времени t и кажущуюся константу скорости псевдопервого порядка соответственно [43]. -Ln (C t / C 0 ) демонстрирует линейную зависимость от времени облучения, а фотокаталитическая реакция относится к реакции псевдопервого порядка, как показано на рис. 6b. k приложение значения, полученные для Bi 5 О 7 Я, SrTiO 3 , 10 мас.% SrTiO 3 / Би 5 О 7 I, 20 мас.% SrTiO 3 / Би 5 О 7 I, 30 мас.% SrTiO 3 / Би 5 О 7 I и 40 мас.% SrTiO 3 / Би 5 О 7 Нанокомпозиты I имеют размер 1,16 × 10 −3 , 4,88 × 10 −3 , 9 × 10 −3 , 1,06 × 10 −2 , 1,45 × 10 −2 , и 9,24 × 10 −3 мин −1 , соответственно. Примечательно, что 30 мас.% SrTiO 3 / Би 5 О 7 Нанокомпозит I демонстрирует максимальную константу скорости фотокаталитической реакции, которая примерно в 2,97 раза выше, чем у чистого Bi 5 О 7 I, и в 12,5 раз больше, чем у чистого SrTiO 3 .
Кривые деградации RhB для всех образцов при облучении УФ-светом показаны на рис. 6c. Хорошо видно, что явление аналогично изображенному на рис. 6а. Однако все образцы демонстрируют очень низкую фотокаталитическую эффективность из-за небольшого поглощения УФ-света, а сенсибилизация красителем влияет на фотокаталитическую активность. Как показано на рис. 6а, 30 мас.% SrTiO 3 / Би 5 О 7 Нанокомпозит I по-прежнему проявляет лучшую активность; однако фотодеградация RhB составляет всего 40% в течение 150 мин. Эти результаты демонстрируют, что SrTiO 3 / Би 5 О 7 Нанокомпозиты I обладают более эффективной фотокаталитической активностью при моделировании солнечного излучения.
Стабильность и возможность повторного использования 30 мас.% SrTiO 3 / Би 5 О 7 Нанокомпозит I был исследован путем повторения тестов на деградацию RhB. После каждого цикла SrTiO 3 / Би 5 О 7 Нанокомпозиты I повторно использовали в следующем цикле перед сбором центрифугированием, несколько раз промывали деионизированной водой и этиловым спиртом и, наконец, сушили при 80 ° C в течение 3 часов. Как показано на рис. 6d, фотокаталитическая активность композита явно не снижается даже после пятого рецикла при моделированном солнечном облучении, что свидетельствует о хорошей стабильности для рециркуляции 30 мас.% SrTiO 3 / Би 5 О 7 Я нанокомпозит.
Обсуждение фотокаталитического механизма
Чтобы получить некоторое представление об активных частицах, участвующих в фотодеградации SrTiO 3 / Би 5 О 7 I, мы провели эксперименты по улавливанию реактивных частиц над 30 мас.% SrTiO 3 / Би 5 О 7 I нанокомпозит для определения основных активных частиц в фотокаталитической реакции. Как показано на рис. 7, добавление изопропанола (IPA) почти не влияет на разложение RhB по сравнению с SrTiO 3 / Би 5 О 7 I, что указывает на отсутствие образования радикалов • OH. Напротив, значительное уменьшение разложения красителя наблюдается после добавления бензохинона (BQ) или динатриевой соли этилендиаминтетрауксусной кислоты (EDTA-2Na), что означает \ (\ bullet {\ mathrm {O}} _ 2 ^ {- } \) и дырки являются основными реактивными веществами для фотодеградации RhB.
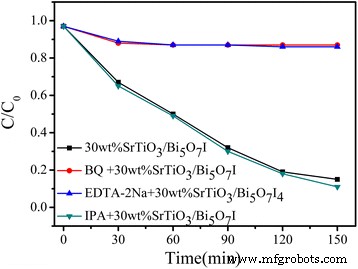
Константа эффективности разложения RhB для 30 мас.% SrTiO 3 / Би 5 О 7 Нанокомпозит I в присутствии различных поглотителей
Для исследования разделения зарядов готовых фотокатализаторов была использована спектроскопия фотолюминесценции. На рисунке 8 показано сравнение спектров ФЛ Bi 5 О 7 I и 30 мас.% SrTiO 3 / Би 5 О 7 I нанокомпозит при возбуждении 320 нм. Спектры фотолюминесценции обоих образцов характеризуются пиком при 497 нм, который приписывается излучению энергии перехода в запрещенной зоне Bi 5 О 7 I. Однако наблюдается резкое снижение интенсивности 30 мас.% SrTiO 3 / Би 5 О 7 Я нанокомпозит. Это явление демонстрирует эффективное разделение фотогенерированных носителей в композите между SrTiO 3 и Би 5 О 7 I.
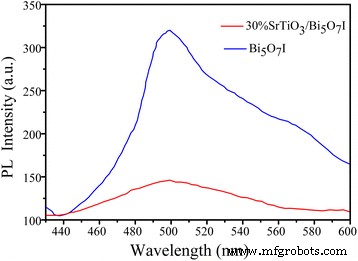
Спектры ФЛ чистого Bi 5 О 7 Нанолисты I и 30 мас.% SrTiO 3 / Би 5 О 7 I нанокомпозит
Чтобы лучше понять механизм повышенной фотокаталитической активности SrTiO 3 / Би 5 О 7 Нанокомпозиты I при моделировании солнечного излучения, соответствующие положения CB и VB для SrTiO 3 и Би 5 О 7 Теоретически I вычисляется согласно \ ({E} _ {VB} =\ chi - {E} _0 + \ frac {1} {2} {E} _g \) и E CB = E VB - E г , где E VB потенциал VB, E CB потенциал CB, E 0 - энергия свободных электронов в водородном масштабе (около 4,5 эВ), E g - ширина запрещенной зоны, а χ рассчитывается как среднее геометрическое значение электроотрицательностей по Малликену компонентов в полупроводнике [44]. Следовательно, E VB и E CB из Би 5 О 7 Я был рассчитан на 2,92 и 0,56 эВ, тогда как энергии SrTiO 3 составили около 2,03 и - 1,15 эВ соответственно. Эти два полупроводника имеют подходящие зонные потенциалы и, таким образом, могут образовывать композитную структуру.
Согласно приведенным выше результатам, схематическая иллюстрация соответствия энергетических зон между SrTiO 3 и Би 5 О 7 I и возможные способы переноса зарядов изображены на рис. 9. Оба SrTiO 3 и Би 5 О 7 Я возбужден моделированным солнечным светом (УФ-светом), и электроны в VB обоих SrTiO 3 и Би 5 О 7 Был бы в восторге от CB, дырки остались в его VB. Поскольку потенциал CB SrTiO 3 (- 1,15 эВ) более отрицательный, чем у Bi 5 О 7 I (+0,56 эВ), электроны SrTiO 3 легко вводятся в CB Bi 5 О 7 I. Фотогенерированные электроны могут реагировать с O 2 для образования супероксидного радикала активных форм кислорода (\ (\ bullet {\ mathrm {O}} _ 2 ^ {-} \)), который затем вызывает деградацию RhB [45]. С другой стороны, дыры в VB Bi 5 О 7 Я перехожу на VB SrTiO 3 , что приводит к эффективному разделению фотоиндуцированных электронов и дырок. Таким образом, фотогенерированные электроны и дырки эффективно разделяются в SrTiO 3 / Би 5 О 7 Нанокомпозиты I. VB SrTiO 3 составляет 2,23 эВ, что ниже окислительно-восстановительного потенциала • OH / H 2 O (+2,27 эВ). Согласно соответствующим сообщениям [46, 47], ВК SrTiO 3 недостаточно для окисления H 2 О в • ОН. Это указывает на то, что \ (\ bullet {\ mathrm {O}} _ 2 ^ {-} \) и дырки являются основными кислородными активными частицами для SrTiO 3 / Би 5 О 7 Нанокомпозиты I в процессе обесцвечивания RhB под воздействием искусственного солнечного света. Следовательно, синтезированный SrTiO 3 / Би 5 О 7 Нанокомпозитный фотокатализатор I демонстрирует гораздо более высокие фотокаталитические характеристики, чем у SrTiO 3 и Би 5 О 7 I.
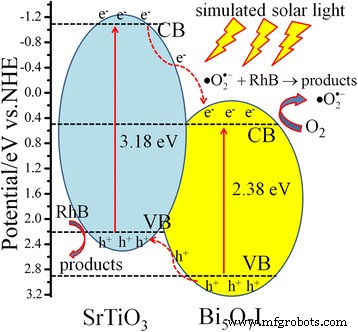
Схематическая диаграмма энергетических зон и возможный фотокаталитический процесс SrTiO 3 / Би 5 О 7 I нанокомпозиты
Выводы
Таким образом, роман SrTiO 3 / Би 5 О 7 Фотокатализаторы нанокомпозитов I были разработаны и изготовлены с использованием сольвотермического подхода в сочетании с термическим разложением. Измерения XRD, XPS и EDS показывают, что продукты действительно состоят из SrTiO 3 / Би 5 О 7 Нанокомпозиты I. Анализ UV-vis DRS показывает, что SrTiO 3 / Би 5 О 7 Нанокомпозиты I обладают хорошими характеристиками поглощения света. Результаты спектров ФЛ показывают, что рекомбинация фотоиндуцированных электронно-дырочных пар явно ингибируется в SrTiO 3 / Би 5 О 7 Нанокомпозиты I. Полученные нанокомпозиты демонстрируют хорошую стабильность и способность к переработке в фотокаталитическом процессе. Синтезированный SrTiO 3 / Би 5 О 7 Фотокатализаторы I демонстрируют высокоэффективное фотокаталитическое свойство деградации RhB под воздействием искусственного солнечного света, которое превосходит таковое у SrTiO 3 и Би 5 О 7 I. The outstanding photocatalytic activity of the photocatalysts is ascribed to the efficient separation and migration of photogenerated charge carriers. The \( \bullet {\mathrm{O}}_2^{-} \) and holes are the main oxygen-active species causing the dye degradation. This work could provide insights into the design and development of other excellent photocatalytic materials for environmental and energy applications.
Сокращения
- BQ:
-
Бензохинон
- CB:
-
Полоса проводимости
- DRS:
-
Diffuse reflectance spectra
- EDS:
-
Energy-disperse X-ray spectroscopy
- EDTA-2Na:
-
Ethylenediaminetetraacetic acid disodium salt
- FE-SEM:
-
Field-emission scanning electron microscope
- FTIR:
-
Fourier-transform infrared spectroscopy
- IPA:
-
Изопропанол
- PL:
-
Фотолюминесценция
- RhB:
-
Родамин Б
- UV-vis:
-
Ultraviolet-visible
- VB:
-
Группа валентности
- XPS:
-
Рентгеновская фотоэлектронная спектроскопия
- XRD:
-
Рентгеновская дифракция
Наноматериалы
- Видимые световые фотокаталитические характеристики нанокомпозитов ZnO / g-C3N4, легированных азотом
- Подготовка и фотокаталитические характеристики фотокатализаторов LiNb3O8 с полой структурой
- Новый фотокатализатор на гетеропереходе Bi4Ti3O12 / Ag3PO4 с улучшенными фотокаталитическими характеристиками
- Изготовление тонких пленок SrGe2 на подложках Ge (100), (110) и (111)
- Синтез нанопластин Cu2ZnSnSe4 в одном резервуаре и их фотокаталитическая активность, управляемая видимым светом
- Изготовление и характеристики высокоэффективного поглощения электромагнитных волн структурированных нано…
- Изготовление и характеристика ZnO Nano-Clips с помощью процесса, опосредованного полиолом
- Производство спиральных нановолокон из CA / TPU и анализ их механизма
- Модуляция морфологии и оптических свойств мультиметаллических наноструктур из PdAuAg и сплавов PdAg
- Изготовление иерархических гетероструктур ZnO @ NiO Core – оболочка для улучшения фотокаталитических характерист…



